Ks. artikkelin pdf-versio «http://www.fimnet.fi/cl/laakarilehti/pdf/2017/SLL412017-2297.pdf»1 Lääkärilehden sivuilla (vaatii FiMnet-tunnuksen).
Polymyalgia rheumatica (PMR) on tavallinen tulehduksellinen reumasairaus ja kliininen haaste niin yleislääkärin kuin reumatologinkin vastaanotolla. Vaikka sairaus on yleinen, sen etiologia tunnetaan huonosti. Potilas aistii oireet lihaskipuna ja jäykkyytenä olka-hartiaseudussa sekä lantion ja reisien alueen lihaksissa, mutta objektiivisilla mittareilla, kuten laboratoriokokeilla, lihassähkökäyrällä tai kuvantamalla, ei kuitenkaan ole todettavissa varsinaista lihasvauriota. Potilaan tulehdusarvot voivat olla korkeat, mutta emme tiedä, missä kudoksessa tulehdus täsmällisesti sijaitsee (1,2).
Epidemiologinen yhteys polymyalgia rheumatican ja jättisoluarteriitin (temporaaliarteriitin) välillä on tunnettu pitkään. Jättisoluarteriittipotilaista 40-60 %:lla on myös polymyalgia ja ja polymyalgiapotilaista 20 %:lla todetaan myös jättisoluarteriitti (3). Uudet kuvantamismenetelmät sekä sairauksien patofysiologian tutkimukset ovat tukeneet käsitystä, jonka mukaan polymyalgia rheumatica ja jättisoluarteriitti muodostavat jatkumon (3). Näiden sairauksien hoidot kuitenkin poikkeavat toisistaan; jättisoluarteriitista on julkaistu katsaus Lääkärilehdessä aiemmin (4).
Polymyalgia rheumaticalle on vuosikymmenten saatossa esitetty useita erilaisia diagnostisia kriteerejä, mikä on vaikeuttanut eri tutkimusten vertailua ja tulosten yleistämistä käytännön työhön (5). Tämän vuoksi Euroopan ja Yhdysvaltain reumatologian alan yhdistykset EULAR ja ACR julkaisivat 2012 kirjallisuuskatsaukseen, konsensukseen ja prospektiiviseen tutkimukseen perustuvan ehdotuksen taudin uusiksi luokittelukriteereiksi (6,7). Hoitoa koskevan kirjallisuuskatsauksen ja suosituksen yhdistykset julkaisivat vuonna 2015 (8,9).
Tässä katsauksessa pohditaan, tuliko uusien luokittelukriteerien ja hoitosuositusten myötä vanhasta jälleen nuori ja miten uudet suositukset palvelevat potilastyötä tekevää lääkäriä.
Polymyalgia rheumatican ilmaantuvuus on vahvasti iästä riippuvainen. Sairaus on harvinainen alle 60 vuoden ikäisillä, mutta ilmaantuvuus alkaa suurentua 60-70 vuoden iässä ja se on tuolloin 50-100 tapausta 100 000:ta potilasta kohti vuodessa. 70-80-vuotiaiden ikäluokassa vuotuinen ilmaantuvuus kasvaa jo 100-230 tapaukseen 100 000:ta potilasta kohti. Sairaus on yleisempi naisilla erityisesti nuoremmissa ikäluokissa, mutta miehet näyttävät kirivän eron kiinni 80 ikävuoteen tultaessa (10,11).
Polymyalgian ei ole todettu vaikuttavan elinaikaan (10), mutta elämänlaatututkimuksissa potilaiden tulos on selvästi huonompi kuin verrokkien (12). Hoito parantaa elämänlaatua, mutta altistaa potilaat tavanomaisille glukokortikoidihoidon haitoille, kuten murtumille, turvotuksille, heikentyneelle sokeritasapainolle ja ihon ohenemiselle. Myös sydän- ja verisuonisairauksien riskin on havaittu suurentuneen (13).
Taudilla on siis iso merkitys potilaalle, ja hoidossa joudutaan tasapainoilemaan elämänlaadun ja glukokortikoidihoidon haittojen välillä.
Polymyalgia rheumaticalle ei ole ainuttakaan spesifistä löydöstä tai tutkimusta. Niinpä aiemmin diagnostiset kriteerit kokosivat kliinisiä oireita ja löydöksiä sekä laboratoriotuloksia erilaisiin yhdistelmiin ja siten tunnistivat erilaisia potilaita. Useimmin kriteereiksi esitettiin yli 50 vuoden ikää, molemminpuolista olka-hartiaseudun sekä lantion alueen kipua, yli tunnin mittaista aamujäykkyyttä, laskoarvoa yli 40 mm/t, nopeaa vastetta glukokortikoidihoitoon ja muiden diagnoosien poissulkemista (14-17).
EULAR:n ja ACR:n työ uusien kriteerien luomiseksi alkoi kirjallisuuskatsauksella, jonka perusteella tunnistettiin 68 mahdollista oiretta ja löydöstä. Tämän jälkeen työ eteni kolmessa kokouksessa, joissa syntyi konsensus seitsemästä ydinoireesta tai -löydöksestä (7). Näiden toimivuus testattiin prospektiivisessa monikeskustutkimuksessa (6), johon rekrytoitiin 125 polymyalgia rheumaticaa sairastavaa potilasta ja 169 potilasta, joilla oli jokin sitä muistuttava sairaus. Uusi ehdotus luokittelukriteereiksi syntyi, kun tutkimuksen tulokset käsiteltiin tilastollisesti monimuuttujamallissa (6) (taulukko «»1).
Ehdotuksessa pakollisiksi kriteereiksi on valittu vähintään 50 vuoden ikä, molemminpuolinen olka-hartiakipu ja viitearvosta poikkeava CRP tai lasko. Tämän jälkeen potilaan muista oireista ja löydöksistä lasketaan pisteitä. Yli 45 minuutin aamujäykkyydestä saa kaksi pistettä, samoin reumatekijä- sekä sitrulliinipeptidivasta-ainetulosten negatiivisuudesta. Yhden pisteen voi saada lonkkien kivusta tai liikerajoitteisuudesta ja yhden pisteen siitä, ettei muissa nivelissä (paitsi olkapäissä ja lonkissa) ole oireita tai löydöksiä. Näin laskettuna korkein mahdollinen pistearvo on kuusi ja polymyalgia rheumatican diagnoosiin vaaditaan pakollisten kriteerien lisäksi neljä pistettä.
Mikäli diagnostiikassa on käytössä ultraäänilaite, potilas saa yhden lisäpisteen, jos toisessa olkapäässä ja toisessa lonkassa on tulehduksellinen löydös, ja yhden lisäpisteen, jos molemmissa olkapäissä on tulehduksellinen löydös. Tällöin korkeimmat pisteet ovat kahdeksan ja polymyalgia rheumatican diagnoosiin vaaditaan viisi pistettä pakollisten kriteerien lisäksi.
Ehdotettujen luokittelukriteerien ansioiksi voidaan katsoa, että niiden lähtökohta oli systemaattinen kirjallisuuskatsaus ja monessa vaiheessa pyrittiin eri näkökulmien konsensukseen, joka arvioitiin prospektiivisessa tutkimuksessa. Kriteeristöä kohtaan on kuitenkin esitetty myös kritiikkiä.
Uusien ja vanhojen kriteerien herkkyyttä ja tarkkuutta arvioitiin turkkilaisessa prospektiivisessa monikeskustutkimuksessa (18). Tutkimukseen osallistui 133 potilasta, joilla arvioitiin olevan polymyalgia rheumatica, ja 142 verrokkia, joilla oli jokin sitä muistuttava sairaus. Kultaisena standardina tutkimus käytti vuoden seurannan jälkeen kokeneen kliinikon arviota siitä, onko sairaus polymyalgia vai ei. EULAR/ACR:n kriteerien osalta tulos oli hienoinen pettymys: herkkyys oli hyvä 90 %, mutta tarkkuus jäi heikoksi 58 %. Tutkijat arvioivat tarkkuutta heikentäneen merkittävästi sen, että tulehdusarvojen raja-arvot on asetettu aiempaa alemmas (viitearvosta poikkeava CRP tai lasko), jolloin kriteerit tunnistivat polymyalgia rheumaticaksi muitakin tuki- ja liikuntaelinvaivoja. Tarkkuus voisi olla korjattavissa raja-arvoa nostamalla.
Ehdotetut luokittelukriteerit eivät ole diagnostiset kriteerit, eli ne sisältävät ajatuksen, ettei niissä pystytä huomioimaan kaikkia yksittäisen potilaan diagnostiikassa tarpeellisia yksityiskohtia. Ne on tarkoitettu yhdenmukaistamaan tieteellisen tutkimuksen aineistoja ja siten helpottamaan niin epidemiologista kuin lääketutkimustakin.
Käytännön kliinikko voi kuitenkin hyödyntää luokittelukriteerejä potilaan diagnostiikassa muistilistana. Päätös diagnoosista tulee perustaa kliiniseen harkintaan. Liian yksioikoisesti sovellettuina EULAR/ACR:n ehdottamat kriteerit saattavat johtaa polymyalgia rheumatican ylidiagnostiikkaan. Aiemmin esitetyt kriteerit ovat tuttuja ja edelleen käyttökelpoisia, kunhan muistaa, ettei mikään kriteeristö ole täydellinen.
Luokittelukriteerit osoittavat, miten vaikeaa on täsmällisesti määritellä sairaus, jonka patofysiologia tunnetaan vaillinaisesti ja jonka diagnostiikkaan ei ole kultaista standardia eikä yhtään objektiivista tautispesifistä mittaria. Kriteeristöä voidaan jatkossa täsmentää, mutta perusongelmaa tuskin ratkaistaan, ennen kuin jokin objektiivinen mittari pystytään sisällyttämään diagnostiikkaan.
Myös EULAR/ACR:n vuonna 2015 julkaisemassa polymyalgia rheumatican hoitosuosituksessa oli pohjana systemaattinen kirjallisuuskatsaus (9). Siinä arvioitiin sekä hoitointerventioita että ennustetekijöitä. Työn pohjalta yhdistykset laativat näyttöön perustuvan hoitosuosituksen asioista, joista näyttöä oli saatavilla, ja täydensivät sitä kokemusperäisillä asiantuntijamielipiteillä (8).
Kirjallisuuskatsauksen ja hoitosuosituksen yllättävin löydös oli näyttöön perustuvan tiedon vajavaisuus. Työryhmä ei löytänyt korkeatasoiseen tutkimukseen perustuvaa vastausta esimerkiksi sellaisiin peruskysymyksiin kuin millaisella annoksella glukokortikoidihoito tulisi aloittaa, millaista glukokortikoidin purkuohjelmaa tulisi noudattaa tai miten pitkään hoidon tulisi jatkua. Sen sijaan metotreksaatin käytön perusteeksi löytyi tutkimusnäyttöä. Näyttö ennustetekijöiden merkityksestä oli vaatimatonta, joskin naissukupuoleen, perifeerisiin niveltulehduksiin ja hypersedimentaatioon liittyi joissain tutkimuksissa suurempi relapsiriski.
Niinpä suosituksen laatijat muistuttavat, että suositus on kliininen neuvo (clinical advice), joka ei sanele yksittäisen potilaan hoitoa. Lopulliset ratkaisut tekee hoitava lääkäri potilaskohtaisesti.
Hoitosuosituksessa esitetään konsensuspohjaiset perusperiaatteet (overarching principles) sekä kirjallisuuskatsaukseen ja asiantuntijamielipiteisiin perustuvat täsmällisemmät hoitosuositukset (specific recommendations).
Hoidon perusperiaatteisiin kuuluu huolellinen diagnostiikka. Kliinisen tutkimuksen lisäksi tutkitaan verenkuva, maksa- ja munuaisarvot, plasman kalsium, verensokeri, tulehdusarvot, virtsanäyte, reumatekijä ja sitrulliinipeptidivasta-aineet. Tapauskohtaisesti lääkärin tulee harkita proteiinien elektroforeesin, kilpirauhaskokeiden, kreatiniinikinaasin, D-25-vitamiinin, tumavasta-aineiden ja neutrofiilien sytoplasma antigeenien vasta-aineiden (ANCA) tutkimista. Myös keuhkoröntgenkuvan ja tuberkuloosidiagnostiikan tarpeellisuus arvioidaan tapauskohtaisesti.
Varhaisvaiheessa tulee huomioida potilaan muut sairaudet, joihin glukokortikoidihoito vaikuttaa. Tärkeimpiä ovat verenpainetauti, sokeriaineenvaihdunnan häiriöt, sydän- ja verisuonisairaudet, dyslipidemia, mahahaava, osteoporoosi ja murtumat, harmaakaihi, glaukooma, toistuvat infektiot sekä muu lääkitys.
Erikoislääkärin konsultaatiota on syytä harkita, jos oireet ovat epätyypilliset, potilaalla on perifeeristen nivelten tulehduksia tai matalat tulehdusmerkkiainetasot, ikä on alle 60 vuotta, hoitoon liittyy huomattavia riskejä, ilmenee relapseja tai glukokortikoidihoito on pitkittynyt. Potilaille tulee järjestää hoidon ohjaus ja seuranta sekä suunnitella yksilöllinen glukokortikoidihoidon kevennys.
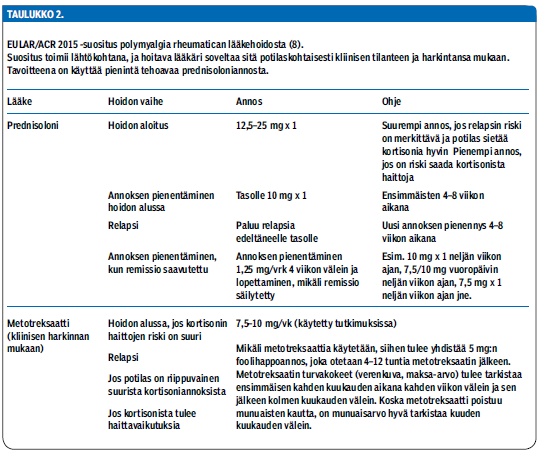
Täsmällisemmissä hoitosuosituksissa neuvotaan käyttämään pienintä tehokasta glukokortikoidiannosta (taulukko «»2). Hoidon aloitukseen suositellaan prednisolonia 12,5-25 mg/vrk. Annoksen yläpäätä voidaan käyttää tilanteessa, jossa uusiutumisriskin katsotaan olevan suurempi ja potilaan arvioidaan sietävän paremmin glukokortikoidihoitoa. Pienemmät annokset sopivat paremmin potilaille, joilla on liitännäissairauksia ja glukokortikoidihoidon riskit ovat suuremmat. Yli 30 mg:n vuorokausiannoksia tulee välttää.
Glukokortikoidiannos tulee räätälöidä yksilöllisesti vastetta, tulehdusmerkkiaineita ja hoidon haittoja seuraten, mutta hyväksi lähtökohdaksi yhdistykset suosittelevat, että ensimmäisten 4-8 viikon aikana prednisoloniannos tulisi pienentää 10 mg:aan/vrk. Mikäli potilaan oireet uusiutuvat, annosta lisätään takaisin tasolle, jolla oireita ei ollut, ja yritetään pienentää uudelleen seuraavien 4-8 viikon aikana. Kun potilas on remissiossa, pidemmänaikavälin annosta pienennetään neljän viikon välein 2,5 mg joka toiselta päivältä (esim. 10 mg × 1 neljän viikon ajan; 10/7,5 mg vuoropäivin neljän viikon ajan; 7,5 mg × 1 neljän viikon ajan jne.). Mikäli vaste glukokortikoidihoitoon on heikko, diagnoosia tulee pohtia uudelleen ja arvioida erityisesti, onko potilaalla samanaikainen jättisoluarteriitti, jolloin tarvitaan suurempia glukokortikoidiannoksia.
Metotreksaattihoidon aloittamiseen glukokortikoidien rinnalle jo varhaisvaiheessa yhdistykset ottivat varovaisen positiivisen kannan neljän satunnaistetun tutkimuksen perusteella (taulukko «»2). Metotreksaatti näytti vähentävän glukokortikoidien tarvetta, ja sitä voi harkita potilaille, joilla on suurentunut riski saada glukokortikoideista haittoja, jotka saavat relapsin tai jäävät riippuvaisiksi suuresta glukokortikoidiannoksesta. Tutkimuksissa polymyalgia rheumaticaan on käytetty metotreksaattia 7,5-10 mg:n viikkoannoksin eli vähemmän kuin nivelreuman hoidossa. Metotreksaattia koskeva suositus on kuitenkin ehdollinen, sillä tutkimuksissa potilasmäärä oli pieni (n = 194) eivätkä tulokset olleet täysin yhdenmukaiset. Metotreksaatin käyttö edellyttää enemmän turvakokeita ja terveydenhuollon kontakteja ja saattaa lisätä erikoislääkärikonsultaatioita aiheuttaen lyhyellä aikavälillä resurssien lisätarvetta.
On myös muistettava, että metotreksaatti poistuu munuaisten kautta ja munuaistoiminta voi olla heikentynyt iäkkäillä potilailla. Niinpä polymyalgia rheumatican hoito glukokortikoideilla ilman metotreksaattia on edelleen käypää hoitoa.
Biologisista lääkkeistä TNFα:n salpaajia ei suositella polymyalgia rheumatican hoitoon.Muihin biologisiin tai perinteisiin reumalääkkeisiin suositus ei ota kantaa.
Potilaille suositellaan yksilöllistä lihasharjoittelua.
Systemaattisten kirjallisuuskatsausten ja uusien suositusten ehkäpä suurin yllätys oli, miten heikosti tutkimukseen perustuvaa tietoa on olemassa toiseksi yleisimmästä tulehduksellisesta reumasairaudesta. Uudet luokittelukriteerit palvelevat tutkimustyötä, mutta diagnoosi perustuu jatkossakin potilaan yksilöllisiin oireisiin ja löydöksiin sekä kliiniseen arvioon.
Polymyalgia rheumatican etiologia on laajalti tuntematon ja hoito nojaa paljolti kokemusperäiseen tietoon. Uusi hoitosuositus on silti hyvin kliiniseen käytäntöön sopiva, ja sen voidaan olettaa johtavan hyvään potilaiden hoitoon. Luulo ei ole kuitenkaan tiedon väärti tässäkään sairaudessa.
Käytännön kliinikko jää toistaiseksi kipeimmin kaipaamaan tautispesifisiä diagnostisia työkaluja sekä täsmällisempää tietoa glukokortikoidihoidon ohjaamiseksi. Niitä odotellessa nykyinen suositus antaa reunaehdot, joiden sisällä kliinikon hoitoratkaisuissa korostuvat huolellinen perehtyminen potilaan sairaushistoriaan, yksilölliset hoitoratkaisut, jatkuva hoitosuhde sekä potilaan toiveiden huomioiminen.
Polymyalgia rheumatica (PMR) is a common inflammatory disease and a challenge for general practitioners and rheumatologists. PMR is a rare condition in patients under the age of 60 years but its incidence increases with age. Even though the prognosis of PMR is relatively good, it impairs quality of life, and patients with PMR may suffer adverse effects of glucocorticoid treatment. Many different diagnostic criteria have been presented but these sets of criteria are different from each other and recognize different patients. Therefore, the European League Against Rheumatism (EULAR) and the American College of Rheumatology (ACR) presented new classification criteria for PMR in the year 2012. The purpose of these criteria is to unify PMR classification and to advance epidemiological research and clinical trials. However, the diagnosis of individual patients needs to be evaluated from a clinical basis. In the year 2015 EULAR/ACR published treatment guidelines for PMR. The guidelines are based on systematic review, but the clinical evidence for the treatment of PMR is incomplete and many recommendations are based on expert opinion and clinical experience. Still, these guidelines offer a good basis for treating clinicians to plan individual treatment for each patient. More research is needed on the aetiology of PMR and clinical research about treatment of PMR.