Ks. artikkelin pdf-versio «http://www.fimnet.fi/cl/laakarilehti/pdf/2018/SLL392018-2190.pdf»1 Lääkärilehden sivuilla (vaatii FiMnet-tunnuksen).
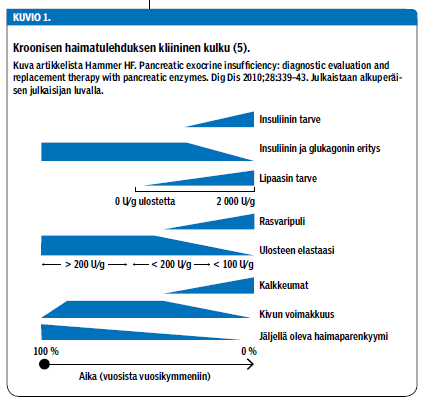
Krooninen haimatulehdus on seurausta toistuvista akuuteista haimatulehduksista, jotka johtavat haimakudoksen korvautumiseen sidekudoksella (1). Sidekudoksen lisääntyminen johtaa etenevään haiman ekso- ja endokriiniseen vajaatoimintaan. Sairauteen liittyy elämänlaadun huonontumista ja erilaisia pitkäaikaisvaikutuksia, kuten kroonista kipua (kuvio 1 «»3). Se voi myös johtaa aliravitsemukseen. Muita pitkäaikaiskomplikaatioita ovat diabetes ja haimasyöpä.
Taudin ilmaantuvuus Euroopassa on 5-10/100 000 asukasta kohden, Suomessa 5-7/100 000 asukasta. Kroonista pankreatiittia sairastavien elinajan mediaani diagnoosin jälkeen on 20 vuotta, ja näin ollen sairauden esiintyvyydeksi arvioidaan noin 120/100 000. Sairastumisikä on etiologiasta riippuvainen; esimerkiksi miehet sairastuvat alkoholin aiheuttamaan krooniseen haimatulehdukseen 30-49 vuoden iässä ja autoimmuunipankreatiittiin 50-59 vuoden iässä. Sairauden diagnosoiminen on tärkeää, jotta oireisille potilaille voidaan aloittaa hoito ja potilaat voidaan ohjata terveydenhuollon seurantaan mm. pitkäaikaiskomplikaatioiden löytämiseksi.
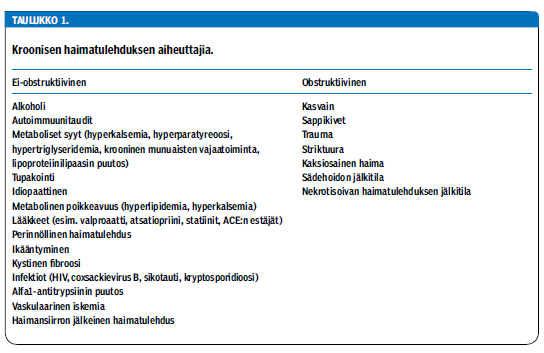
Alkoholi on tärkein sairauden taustalla oleva syy, jopa 90 %:ssa tapauksista (taulukko 1 «»1). Potilas on lähes poikkeuksetta suurkuluttaja, joka on käyttänyt alkoholia puhtaana alkoholina laskien 80-150 grammaa päivittäin 10-15 vuoden ajan ennen sairauden kliinistä puhkeamista (2). Lähes yhtä tärkeä kroonisen haimatulehduksen etiologinen tekijä on tupakointi (3). Muita syitä ovat sappikivitauti, metaboliset sairaudet (hypertriglyseridemia tai hyperparatyreoosi) ja perinnöllinen tautimuoto (perinnöllinen haimakalsinoosi). Syynä voi olla myös autoimmuunisairaus, esimerkiksi autoimmuunihaimatulehduksen jälkitila, tai sairaus liittyy primaariseen sklerosoivaan kolangiittiin, primaariseen biliaariseen kolangiittiin tai Sjögrenin oireyhtymään. Ikäihmisillä idiopaattisen ja autoimmuunitulehduksen osuus on suurempi kuin nuoremmilla (4).
Kroonisen haimatulehduksen diagnoosi perustuu oireisiin, haiman toimintakokeisiin ja kuvantamistutkimuksiin. Tärkeimmät oireet ovat selkään säteilevä ylävatsakipu, johon voi liittyä pahoinvointia ja oksentelua. 10-20 %:lla potilaista krooninen haimatulehdus on kivuton, mutta silti saattaa ilmentyä diabetes, keltaisuus tai imeytymishäiriö. Rasvaripuli ja painonlasku ilmaantuvat sairauden edenneessä vaiheessa. Ikäihmisillä krooniseen pankreatiittiin liittyy kipua, haiman kalkkeutumista ja rasvaripulia harvemmin kuin nuoremmilla (4).
Oireanamneesin lisäksi tulee selvittää potilaan sukutausta, alkoholinkäyttö, tupakanpoltto ja lääkkeiden käytön historia. Lisäksi on huomioitava infektioiden mahdollisuus, mukaan lukien HIV. Diagnoosin tulee perustua oireisella potilaalla todettuihin kuvantamislöydöksiin.
Tietokonetomografiassa (TT) todetut haimakalkit ovat patognomoninen löydös kroonisessa haimatulehduksessa. Krooninen kalsifioiva haimatulehdus viittaa vahvasti alkoholiin etiologisena tekijänä. Muita kuvantamismenetelmiä ovat kaikuendoskopia, magneettikuvaus ja tavallinen kaikukuvaus. Magneettikuvaus voidaan tehdä tavanomaisena tai sekretiinitehosteisena magneettikolangiografiana (MRCP). Tyypillisiä kuvantamislöydöksiä ovat lisääntynyt haimaparenkyymin tiheys, haima-atrofia, kalkit parenkyymissä, pseudokysta, päätiehyen epäsäännöllisyys ja siihen liittyvät sivuhaarat. Kaikuendoskopia on herkkä menetelmä kroonisen haimatulehduksen alkuvaiheen muutoksien havainnoinnissa.
Invasiivisia toimenpiteitä suunniteltaessa tietokonetomografia on suositeltavin kuvantamismenetelmä. Se on syytä uusia, mikäli potilaan kivut lisääntyvät, ja toisaalta tarkisteltaessa esimerkiksi endoskooppisen hoidon tulosta. Endoskooppista haimatiehytkuvausta käytetään erityisesti krooniseen haimatulehdukseen liittyvien tiehytmuutosten tarkempaan diagnostiikkaan ja komplikaatioiden endoskooppiseen hoitoon.
Jos kuvantamistutkimuksissa on viitteitä autoimmuunihaimatulehduksesta tai potilaalla epäillään IgG4-assosioituvaa kolangiopatiaa, voidaan papillasta tai haimaparenkyymistä ottaa koepala kaikuendoskopiaohjauksessa IgG4-kertymien diagnosoimiseksi. Kaikuendoskopiaa pidetään herkimpänä kuvantamismenetelmänä kroonisen haimatulehduksen varhaisvaiheessa.
Kroonisen haimatulehduksen varhaisdiagnostiikkaan katsotaan kuuluvan etiologiaa ja haiman toimintaa kuvaavia laboratoriokokeita (taulukko 2 «»2). Seerumin amylaasi- ja lipaasitasot ovat yleensä normaalit tai lievästi suurentuneet. Haimasta suolistoon erittyvä elastaasi 1 poistuu muuttumattomana ulosteeseen, ja sen määrittämistä voidaan käyttää kroonisen haimatulehduksen diagnostiikassa. Pitoisuus yli 200 µg/g ulosteessa on normaali, 100-200 µg/g viittaa lievään haiman vajaatoimintaan ja alle 100 µg/g vaikeaan haiman vajaatoimintaan. Entsyymikorvaushoito ei häiritse tutkimusta, mutta voimakkaassa vesiripulissa tulos voi olla väärä positiivinen. Tutkimus voidaan hyvin tehdä myös avoterveydenhuollossa kroonista haimatulehdusta epäiltäessä.
Kroonisen haimatulehduksen aiheuttamassa haiman vajaatoiminnassa imeytymishäiriön oireet ilmaantuvat vasta taudin myöhäisessä vaiheessa (kuvio 1 «»3) (5). Endokriininen haiman vajaatoiminta ilmaantuu myös suhteellisen myöhään. Noin 10 %:lle potilaista, joilla on alkoholin aiheuttama krooninen haimatulehdus, kehittyy diabetes. Haiman ekso- ja endokriinisestä kapasiteetista 80-90 % on tuhoutunut, ennen kuin diabetes tai imeytymishäiriö ilmaantuu. Krooniseen haimatulehdukseen liittyy myös osteopenian ja osteoporoosin riski.
Kroonisen haimatulehduksen hoidossa on tärkeää kivun sekä eksokriinisen ja endokriinisen vajaatoiminnan hoito (taulukko 3 «»5). Alkoholinkäytön ja tupakoinnin lopettamista pidetään hyvin tärkeänä. Potilaille suositellaan vähärasvaista ruokavaliota. Toisaalta aliravitsemuksen tiedetään olevan tärkeä ennustetekijä, koska sen vaikeusaste korreloi suoraan komplikaatioiden esiintymiseen. Ravitsemusterapeutin konsultaatiota tulee tarjota kaikille kroonista haimatulehdusta sairastaville. Antioksidanttien (esim. seleeni, C-vitamiini, beetakaroteeni, E-vitamiini ja metioniini) on todettu tutkimuksissa lieventävän kipua, mutta niiden kliininen merkitys on edelleen epävarma (6).
Haimakivun hoidossa kannattaa olla aktiivinen, jotta kipu ei pääse kroonistumaan ja muuttumaan vaikeasti hallittavaksi esimerkiksi opiaattiriippuvuuden vuoksi (7). Ellei kipu ole hallittavissa tulehduskipulääkkein (NSAID tai parasetamoli) ja elintapamuutoksin, potilas lähetetään erikoissairaanhoidon selvityksiin. Tällöin harkitaan myös kroonisen haimatulehduksen endoskooppisia, radiologisia ja kirurgisia hoitoja.
Lääkehoitona käytetään trisyklisiä masennuslääkkeitä, gabapentiiniä ja pregabaliinia. Serotoniinin takaisinoton estäjiä voidaan käyttää kipukynnystä nostavina lääkkeinä. Tramadolilla on saatu yhtä tehokas kivunlievitys vähemmin sivuvaikutuksin kuin morfiinilla, mutta opioidien pitkäaikaiskäyttöä on syytä välttää toleranssi- ja riippuvuusriskin vuoksi.
Mikäli kipulääkitykseen liittyy merkittäviä haittoja tai kipua ei saada hallintaan konservatiivisella hoidolla, voidaan käyttää kaikuendoskopiateitse tehtävää sisusvaltimohermosolmun (ganglium coeliacum) nekrolyysiä (alkoholi) tai salpausta (puudutusaine).
Potilaan pitää syödä säännöllisesti, mieluummin useita pieniä aterioita, jotka sisältävät riittävästi energiaa. Hoitomyöntyvyyden turvaamiseksi ateriakertoja on hyvä olla 5-6 vuorokaudessa. Proteiinia tulisi saada 1,0-1,5 grammaa painokiloa kohti. Rasvaa tulisi olla 30-40 % energiamäärästä. Kasvisrasvat ovat eläinrasvoja paremmin siedettyjä. Keskipitkäketjuiset triglyseridit imeytyvät sellaisenaan ilman hydrolyysiä, joten niitä voi tarvittaessa käyttää, jos entsyymikorvaus ei riitä. Rasvaliukoisten vitamiinien (A, D, E, K) riittävästä saannista tulee myös huolehtia.
Entsyymikorvaushoito on tarpeen, mikäli krooniseen haimatulehdukseen liittyy haiman eksokriininen vajaatoiminta. Se saattaa myös vähentää kipuja. Sitä suositellaan erityisesti potilaille, joilla esiintyy rasvaripulin lisäksi munuaiskiviä. Ruoansulatushäiriön estämiseksi suositeltu lipaasiannos pääaterioilla on 25 000-50 000 KY, välipaloilla riittää 10 000 KY. Amylaasin ja proteaasin korvaaminen ei ole yhtä tärkeää, mutta yleisimmin käytetyissä entsyymikorvauskapseleissa niitä on mukana lipaasin lisäksi. Entsyymikapselit suositellaan ottamaan aterian aikana tai heti sen jälkeen, ja kapselit on nieltävä kokonaisina, pureskelematta, riittävän nesteen kera.
Mikäli hoitovaste ei ole riittävä, lipaasiannos voidaan suurentaa 2-3-kertaiseksi, mutta sivuvaikutusten riskin takia annos ei saa olla yli 75 000 KY. Ennen kuin annosta suurennetaan, on tärkeää tarkistaa hoitomyöntyvyys ja selvittää mahdolliset muut samankaltaisia oireita aiheuttavat sairaudet (hypertyreoosi, keliakia, lyhytsuolioireyhtymä, suoliston bakteeriylikasvu, tulehduksellinen suolistosairaus tai sappihapporipuli).
Endokriininen vajaatoiminta ilmaantuu vasta myöhäisessä vaiheessa (kuvio 1 «»3). Diabetes johtuu insuliinin puutteesta ja sen hoidoksi tarvitaan insuliinia. Myös glukagonin erittyminen voi huonontua, mikä entisestään vaikeuttaa diabeteksen hoitoa. Tälle sekundaariselle diabetekselle onkin tyypillistä hypoglykemiaherkkyys.
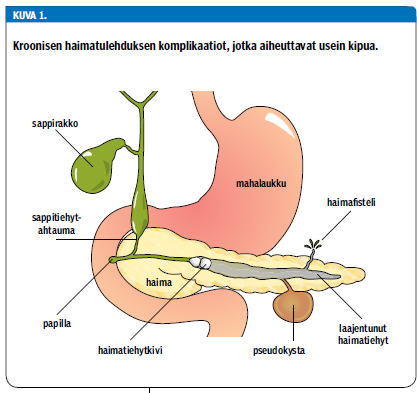
Kroonisen haimatulehduksen invasiivinen hoito on aiheellista, jos konservatiivinen hoito ei tuota riittävää tulosta esimerkiksi vaikean kivun tai komplikaatioiden, kuten haimatiehyttukoksen, sappitiehyttukoksen, pohjukaissuolitukoksen, pseudokystan tai haimafistelin, vuoksi (kuva 1 «»5). Ennen invasiivisen hoidon harkitsemista tulee kuitenkin varmistaa, että kroonisen haimatulehduksen akutisoitumista aiheuttavat tekijät on karsittu. Lähinnä tämä tarkoittaa alkoholinkäytön ja tupakoinnin lopettamista ja sappikivitaudissa sappirakon poistoa.
Endoskooppinen hoito duodenoskoopilla on yleensä ensisijainen invasiivisen hoidon muoto, mutta avoleikkauskin on edelleen joissakin tapauksissa perusteltu. Esimerkiksi silloin, kun kroonista haimatulehdusta sairastavalla todetaan sappirakkokivet, laparoskooppinen sappirakon poisto on aiheellinen. Avokirurgiaan turvaudutaan lähinnä silloin, kun epäillään kasvainta. Kroonisen haimatulehduksen invasiivinen hoito on kaikessa monimuotoisuudessaan haastavaa ja tulisi keskittää erikoistuneisiin yksikköihin, joissa on käytettävissä kaikki endoskooppisen ja kirurgisen hoidon eri mahdollisuudet.
Haimatiehyttukoksen invasiivista hoitoa harkitaan, jos tukoksen aiheuttama ylävatsakipu ei helpotu lääkkein. Kipu on tyypillisimmillään jomottavaa, jaksoittaista tai jatkuvaa ja säteilee selkään. Tukoksen aiheuttaa yleensä striktuura, haimatiehytkivi tai pseudokysta. Kun haimaneste ei pääse suoleen, sen ajatellaan aiheuttavan painetta haiman sisälle ja samalla kipua. Tätä teoriaa puoltaa se, että tukoksen invasiivinen hoito useimmiten vähentää tai poistaa kivun.
Ahtaumat ja niiden syyt näkyvät parhaiten tietokonetomografiassa. Siinä haimatiehyt on tukoksen proksimaalipuolella laajentunut. Myös magneettikuvausta voidaan käyttää, mutta haimatiehytkiviä on siinä vaikeampi arvioida. Cochrane-katsauksen (8) mukaan pitkäaikaisseurannassa avokirurgialla saadaan parempi haimatiehyttukokseen liittyvän kivun lievittyminen kuin endoskooppisella toimenpiteellä, mutta kyseessä on iso leikkaus, johon liittyy sairastavuutta ja joskus kuolleisuuttakin. Näin ollen endoskooppinen hoito on useimmissa keskuksissa ensilinjan hoitomuoto kivuliaaseen haimatiehyttukokseen. Kroonisen haimatulehduksen komplikaationa, usein haimatiehyttukokseen liittyen, voi kehittyä pseudokysta tai haimafisteli, joka aiheuttaa kivun lisäksi usein myös infektio-oireita. Nekin ovat tavallisimmin hoidettavissa endoskooppisesti (9,10).
Endoskooppisessa hoidossa haimatiehyen ahtauman hoito on ensisijaista. Se hoidetaan yleensä muovistentein papillan kautta. Tukoksen aiheuttava haimatiehytkivi voidaan ensin yrittää murskata kehonulkoisella paineaallolla endoskooppisen hoidon helpottamiseksi. Joskus pelkkä kivenmurskaus helpottaa potilaan kipuoiretta riittävästi (11). Yleensä kuitenkin kivenkappaleet pyritään poistamaan haimatiehyestä endoskooppisesti pallolla tai korilla. Samalla tarkistetaan haimatiehyen tila ja tarvittaessa hoidetaan ahtauma stenteillä. Tämä yhdistelmähoito on osoittautunut tehokkaaksi (12). Jos haimatiehyttä tukkivaa kiveä ei muuten saada hoidettua, voidaan edetä haimatiehyttähystykseen ja murskata kivi näkökontrollissa joko elektrohydraulisella kivenmurskaimella tai laserilla.
Haiman pään fibrotisoituminen kroonisessa haimatulehduksessa voi aiheuttaa sappitietukoksen. Jos potilas on ikteerinen ja varsinkin jos hänellä on sappitietulehduksen oireet, tukos tulee hoitaa kiireellisesti endoskopiassa. Jos hälyttäviä oireita ei ole, maksa-arvoja voidaan jäädä seuraamaan. Mikäli maksa-arvot pysyvät suurentuneina yli kuukauden, invasiivinen hoito on aiheellinen, jotta tila ei johda sekundaariseen biliaariseen kirroosiin. Joskus sappitieahtauman syynä on sappiteitä painava pseudokysta, jolloin ongelman hoidoksi riittää yleensä pseudokystan hoito.
Sappitieahtauma voidaan hoitaa useampaa vierekkäistä muovistenttiä käyttäen (13) tai yhdellä muovipäällysteisellä metalliverkkoproteesilla (14). Aina tulee myös harkita, onko samalla syytä tehdä myös haimatiehyen toimenpiteitä. Perkutaanista reittiä käytetään harvoin krooniseen haimatulehdukseen liittyvän sappitietukoksen hoidossa.
Kroonisessa haimatulehduksessa pseudokysta on yleinen komplikaatio. Oireetonta pseudokystaa ei tarvitse hoitaa, mutta mikäli potilaalla on oireita eikä pseudokysta häviä seurannassa, hoito on usein aiheellista. Pseudokysta voi myös infektoitua, jolloin tila voi vaatia päivystystoimenpiteen.
Mikäli pseudokystasta on yhteys haimatiehyisiin, endoskooppinen pseudokystadrenaasi voidaan tehdä transpapillaarisesti asettamalla stentti haimatiehyisiin tai pseudokystaan. Jos pseudokysta on läheisessä kontaktissa mahalaukun tai pohjukaissuolen seinämään, siihen voidaan asettaa kaksoissaparostentit mahalaukun tai pohjukaissuolen seinämän läpi. Mikäli pseudokysta ei aiheuta selvää pullotusta endoskooppiseen näkymään, on turvallisinta tehdä toimenpide kaikuendoskopiaohjauksessa. Isompikaliiberinen muovipäällysteinen metalliverkkoproteesi on hyvä vaihtoehto, jos pseudokysta on infektoitunut ja sisältää paksua märkää, sillä silloin sen tyhjeneminen on tehokkaampaa. Mikäli infektoitunut pseudokysta ei ole kontaktissa mahalaukkuun, se on syytä kanavoida perkutaanisesti kaikuohjauksessa.
Haimafisteli on melko harvinainen kroonisen haimatulehduksen komplikaatio. Se voi aiheuttaa haima-askitesta tai fisteli voi tunkeutua pleuraan tai jopa mediastinumiin. Se saadaan yleensä hoidettua endoskooppisesti asetetulla haimatiehytstentillä.
Mikäli endoskooppinen hoito ei onnistu tai onnistuneen endoskooppisen hoidon jälkeen tila uusii toistuvasti, tulee harkita leikkaushoitoa (15). Haimatiehyttukos voidaan hoitaa yhdistämällä haimatiehyt suoleen tekemällä ns. lateraalinen pankreatikojejunostomia toisen linjan hoitona. Vastaavasti sappitietukos voidaan hoitaa yhdistämällä sappitiehyt suoleen tekemällä hepatikojejunostomia tai joissakin tapauksissa kolekystojejunostomia. Nämä kolme operatiivista interventiota ovat kuitenkin nykyään harvoin tarpeellisia, sillä instrumentit ja osaaminen ovat kehittyneet niin, että nämä tiehyttukospotilaat saadaan pääsääntöisesti hoidetuksi endoskooppisesti. Joskus harvoin joudutaan myös pseudokystien tai haimatiefistelien leikkaushoitoon. Yleisin kirurginen toimenpide pseudokystien hoidossa on laparoskooppinen pseudokystogastrostomia.
Joskus leikkaus on kroonisessa haimatulehduksessa ensisijainen invasiivisen hoidon vaihtoehto. Esimerkiksi krooniseen haimatulehdukseen liittyvässä pohjukaissuolitukoksessa useimmiten laparoskopiateitse tehtävä gastrojejunostomia on yleensä perusteltu. Kirurginen hoito on paras hoitovaihtoehto myös sellaisille potilaille, joilla kipu ei reagoi hoitoon ja joilla sairauden aiheuttamat muutokset rajoittuvat haiman häntään. Näissä tilanteissa haiman hännän poisto on perusteltu hoito. Jos taas kipupotilaan kroonisen haimatulehduksen muutokset paikantuvat haiman päähän ja varsinkin jos on epäilyä kasvaimen mahdollisuudesta, voidaan harkita jopa pankreatikoduodenektomiaa.
Potilaiden säännöllinen seuranta on tarpeen, ja se voidaan toteuttaa ensisijaisesti avoterveydenhuollossa. Seurannassa on tärkeää tarkistaa potilaan pysyminen raittiina ja ravitsemustila (mm. painon säännöllinen mittaus). On myös varmistettava, ettei potilaalle kehity diabetesta tai rasvaliukoisten vitamiinien puutosta. Jos potilaalle ilmaantuu ikterus, hän laihtuu nopeasti tai kivunhoito on ongelmallista, on syytä konsultoida erikoissairaanhoitoa. Rutiininomaista kuvantamiskontrollia ei tarvita, mutta jos ilmaantuu hälyttäviä oireita (mm. nopea laihtuminen tai ikterus), tehdään esimerkiksi tietokonetomografia.
Krooninen haimatulehdus on alidiagnosoitu kroonisen ylävatsakivun ja ravitsemushäiriön syynä. Näiden potilaiden laadukas ja tuloksellinen hoito edellyttää gastroenterologin ja gastrokirurgin tiivistä yhteistyötä. Hoito onnistuukin parhaiten yksiköissä, joissa on tarjottavana kaikki konservatiivisen ja invasiivisen tutkimuksen ja hoidon mahdollisuudet.
Chronic pancreatitis is a progressive inflammation of the pancreas with destruction of pancreatic secretory cells leading to chronic or recurrent acute episodes of abdominal pain, steatorrhoea, diabetes, or jaundice.
Chronic pancreatitis is uncommon (prevalence ranging from 5 to 10 per 100,000 people in Europe). Excessive alcohol consumption is the most common cause. Other aetiologies include autoimmune pancreatitis, metabolic and genetic causes, medications, or pancreatic duct obstruction.
Common complications are diabetes, malabsorption, pancreatic cancer, pseudocysts, osteoporosis or osteopenia, steatorrhoea, and bile duct, duodenal, or gastric obstruction.
Abstinence from alcohol and tobacco is important to limit disease progression. Low fat diet and analgesics are initial medical treatment for pain. Pancreatic enzymes are useful in exocrine insufficiency. Endoscopic treatment can be considered in patients with localized strictures or stones in the main pancreatic duct.
Follow-up should include early and regular screening for diabetes, malnutrition and lack of fat-soluble vitamins.