Ks. artikkelin pdf-versio «http://www.fimnet.fi/cl/laakarilehti/pdf/2018/SLL422018-2409.pdf»1 Lääkärilehden sivuilla (vaatii FiMnet-tunnuksen).
Kawasakin tauti (KD) on saanut nimensä japanilaiselta lastenlääkäriltä Tomisaku Kawasakilta (1). Hän kuvasi vuonna 1967 potilassarjan, johon kuului 50 lapsipotilasta, ja antoi näiden yhteneväiselle taudinkuvalle nimen akuutti kuumeinen mukokutaaninen imusolmukeoireyhtymä (2). Tauti rauhoittui itsekseen, ja ennustetta pidettiin hyvänä. Esiintyvyyden seuraamiseksi luotiin diagnostiset kriteerit, jotka ovat nykyluokituksenkin pohjalla. Pian Japanissa kuitenkin raportoitiin Kawasakin taudin sairastaneiden potilaiden äkkikuolemia. Ruumiinavauksissa potilailla havaittiin sepelvaltimolaajentumia. Niiden ymmärrettiin olevan yhteydessä tautiin, ja se luokiteltiin vaskuliitteihin (3).
Perhe hakeutui terveyskeskuspäivystykseen aiemmin terveen 5 kuukauden ikäisen poikansa kanssa kaksi päivää jatkuneen kuumeen vuoksi. Pojalla oli ollut viikon ajan harvakseltaan pientä yskää, mutta ei muita oireita. Laboratoriokokeissa todettiin CRP-pitoisuuden olevan 29 mg/l ja leukosyyttien määrän 14,2 E9/l. Virtsanäytteessä leukosyyttien määrä oli 33 E6/l. Oireiden tulkittiin johtuvan virtsatieinfektiosta, ja poika kotiutettiin hyväkuntoisena. Kefaleksiiniantibiootti aloitettiin suun kautta annettuna.
Kuume jatkui kuitenkin korkeana, ja perhe hakeutui uudelleen hoitoon seuraavana päivänä. Uutena oireena oli ilmaantunut vesiripulia. Tulehdusarvot olivat samalla tasolla kuin edellisenä päivänä. Viljelyvastauksen mukaan virtsassa kasvoi sekaflooraa. Antibioottihoito lopetettiin, ja lapsi kotiutui diagnoosina gastroenteriitti.
Seitsemän päivän kuumeilun jälkeen potilas sai lähetteen lastentautien päivystykseen. Vointi oli selvästi huonompi, ja löydöksinä todettiin silmien sidekalvojen verestys, nielun punoitus sekä vartalon laaja-alainen eksanteema. Kaulalla ei todettu poikkeavia imusolmukesuurentumia eikä raajoissa löydöksiä. Tulehdusarvot olivat suurentunet: CRP-pitoisuus oli jo 110 mg/l ja leukosyyttien määrä 18,4 E9/l. Syke oli 190/min. Lapsi otettiin infektio-osastolle, ja suoneen annettava kefuroksiimihoito aloitettiin. Kawasakin taudin kriteereistä täyttyivät kuume ja kolme viidestä pääoireesta (taulukko 1 «»1). Sydämen kaikukuvauksessa todettiin tautiin sopien sepelvaltimoiden tyvien laajentumat, kaliiberin vaihtelua ja perikardiumnesteilyä.
Hoidoksi aloitettiin immunoglobuliini 2 g/kg/10 h infuusiona suoneen sekä asetyylisalisyylihappo 50 mg/kg/vrk jaettuna kolmeen annokseen. Silmälääkärin tutkimuksessa löydöksenä oli lievä iriitti, jonka hoidoksi aloitettiin deksametasonitipat. Laboratoriokokeissa todettiin natriureettisen propeptidin (ProBNP) pitoisuudeksi 880 ng/l (viitearvo alle 84 ng/l) ja troponiini T:n (TnT) pitoisuudeksi 18 ng/l (viitearvo alle 15 ng/l).
Lapsi virkistyi nopeasti immunoglobuliini-infuusion aikana, ja kuume laski. Ihottuma ja silmien verestys rauhoittuivat. Tulehdusarvot alkoivat pienentyä, ja potilas kotiutui hyväkuntoisena kolmen päivän osastohoidon jälkeen.
Potilas oli kardiologin seurannassa, ja sepelvaltimomuutokset normaalistuivat kolmessa viikossa. Asetyylisalisyylihappolääkitystä jatkettiin annoksella 5 mg/kg yhteensä kahden kuukauden ajan. Seurantakäynti lastentautien poliklinikalla ohjelmoitiin vuoden päähän sairastumisesta.
Kawasakin tauti on pääasiassa pienten lasten akuutti korkeakuumeinen keskisuurten verisuonten vaskuliitti. Se on lasten toiseksi yleisin vaskuliitti Henoch-Schönleinin purppuran jälkeen. Sairastuneista 80 % on alle 5-vuotiaita, ja tauti on noin 1,5 kertaa yleisempi pojilla kuin tytöillä. Tautia tavataan kaikilla mantereilla, mutta selvästi yleisin se on Itä-Aasiassa (4). Japanissa vuosittainen ilmaantuvuus alle 5-vuotiailla lapsilla on 265/100 000 (5). Länsimaisessa väestössä vastaava luku on noin 10/100 000 ja Suomessa 11,4/100 000 (6).
Kawasakin taudin etiologia on edelleen arvoitus, vaikka sitä on tutkittu lähes 50 vuotta. Jonkin tai joidenkin ulkoisten tekijöiden ajatellaan laukaisevan immunologisen reaktion geneettisesti alttiilla potilaalla. Laukaisevaa tekijää ei tunneta, mutta sitä ajatellaan esiintyvän laajalti ympäristössä, ja potilaan arvellaan altistuvan sille ylähengitysteiden kautta. Taudin epidemiologiset piirteet ja kliininen kuva viittaavat infektioalkuperään (7), mutta patogeeniä ei ole löydetty eikä tarttumista potilaasta toiseen ole osoitettu. Tautia kuitenkin esiintyy joskus ryppäinä samalla paikkakunnalla. Lisäksi ilmaantuvuudessa on todettu vuodenaikavaihtelua: pohjoisella pallonpuoliskolla tautia esiintyy eniten tammi-maaliskuussa (8). Vanhemman tai sisaruksen sairastaman Kawasakin taudin on todettu suurentavan sairastumisriskiä (9,10). Varmuuden puuttuessa taudin aiheuttajaksi on tarjottu ympäristötekijää, tavallista tai superantigeeniä sekä vasta-ainevälitteistä mekanismia (11,12).
Kawasakin taudissa aktivoituvat sekä luontainen että hankittu immuunijärjestelmä. Akuutissa vaiheessa voidaan todeta proinflammatoristen sytokiinien sekä neutrofiilien lisääntyminen ja hankinnaiseen immuniteettiin liittyen T- ja B-lymfosyyttien aktivoituminen (13).
Geneettiseen taustaan viittaa sairastumisriskin säilyminen suurempana maastaan muuttaneiden japanilaisten jälkeläisillä, vaikka muutto olisi tapahtunut sukupolvia aiemmin. Taudin geneettinen tausta on kuitenkin monitekijäinen ja selittää vain osan sairastumisalttiudesta. Mahdollisia altistavia geenejä tunnetaan tällä hetkellä yli 60, ja niistä suurin osa liittyy elimistön immuuni- ja inflammaatioreaktioiden säätelyyn (14). Suurin osa geenitutkimuksista on tehty aasialaisilla väestöillä.
Taudin kulku on kolmivaiheinen. Se alkaa korkeakuumeisella akuutilla vaiheella, joka kestää hoitamattomana jopa 10-14 vrk. Alku on äkillinen, ja kuume reagoi huonosti kuumelääkitykseen. Akuutin vaiheen aikana ilmaantuvat taudin kliiniset oireet. Lapset ovat selvästi kivuliaita ja ärtyisiä. Laboratoriolöydökset sopivat akuuttiin bakteeritautiin. Akuutissa vaiheessa neutrofiilivaltainen nekrotisoiva tulehdusreaktio tuhoaa etenevästi verisuonen seinämän rakenteita adventitiaan saakka. Arteriitti heikentää valtimoiden seinämiä altistaen aneurysmille.
Akuuttia vaihetta seuraa 2-4 viikon kestoinen subakuutti vaihe. Lapset toipuvat kliinisesti, yleisvointi normaalistuu ja näkyvät oireet katoavat.Kawasakin taudin merkittävin komplikaatio, sepelvaltimoaneurysmat, ilmaantuvat juuri subakuutissa vaiheessa, kun potilas on usein jo kotiutunut. Verihiutaleiden määrä voi reaktiivisesti ylittää jopa arvon 1 000 E9/l. Verisuonten seinämissä alkaa lymfosyyttivaltainen subakuutti inflammaatio. Se saattaa jatkua kuukausista vuosiin limittyen taudin kolmanteen vaiheeseen, luminaaliseen myofibroblastiseen proliferaatioon (LMP). Tässä vaiheessa suonen sisällä tapahtuu kudoksen myofibroplastista uudiskasvua mediaalisen sileälihassolukon aktivoimana (15).
Toipumisvaiheen katsotaan alkavan, kun lasko ja verihiutaleiden määrä ovat normaalistuneet. Se voi kestää kuukausista vuosiin, ja sen aikana verisuonissa tapahtuu paranemista ja joskus arpeutumista. Aneurysman seinämän myötäinen tromboosi tai luminaalinen myofibroblastinen proliferaatio voivat edetä suonen stenoosiksi ja edelleen sydäninfarktiksi.
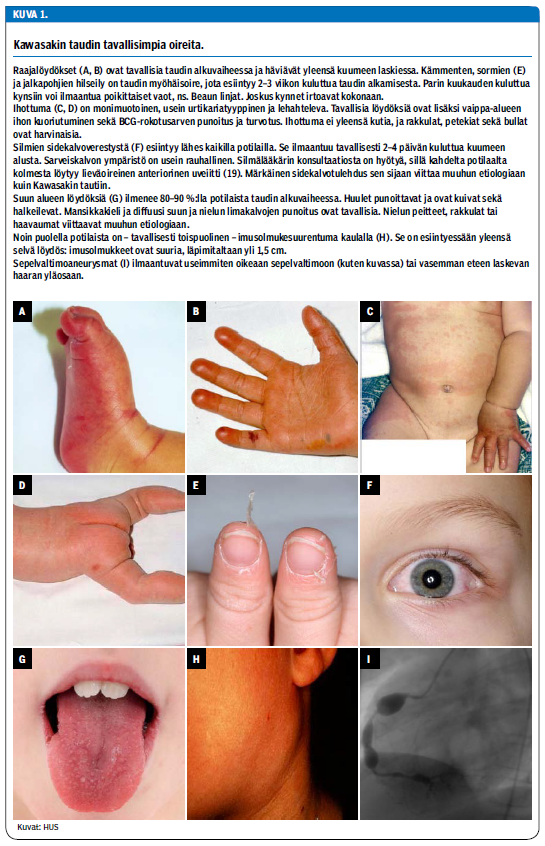
Diagnoosi on kliininen ja perustuu taudinkuvaan (taulukko 1 «»1). Spesifistä diagnostista testiä ei ole. Diagnoosin asettamiseksi vaaditaan vähintään 5 päivää kestänyt kuume (> 38 °C) ja neljä viidestä pääoireesta. Vähemmät oireet riittävät, jos todetaan sepelvaltimomuutoksia (taulukko 1 «»1). Nykysuositusten mukaan diagnoosin voi asettaa jo ennen 5 kuumepäivän rajaa, jos oireita on vähintään neljä ja mukana on raajaoire (16). Viidestä pääoireesta (kuva 1 «»2) tavallisimmat ovat silmien sidekalvoverestys, suun tai huulien alueen muutokset ja monimuotoinen ihottuma. Lisäksi pääoireisiin kuuluvat raajalöydökset sekä noin puolella potilaista tavattava kaulan imusolmukesuurentuma. Diagnoosia tukevat lukuisat tautiin yhdistetyt liitännäisoireet (taulukko 1 «»1).
Edellä esitellyn potilastapauksen lapsella kaikki kriteerit eivät täyttyneet. Tämä viivästytti diagnosointia, ja sepelvaltimomuutoksia ehti kehittyä. Potilastapaus osoittaa Kawasakin taudin tunnistamisen vaikeuden: oireet sopivat moniin tavallisiin infektioihin. Lapsen äidin mukaan lasta käytettiin yhteensä 8 kertaa terveydenhuollon vastaanotoilla ennen taudin diagnosointia. Työdiagnoosi ehti vaihtua useamman kerran ennen kuin diagnoosin varmistaneet sepelvaltimomuutokset todettiin. Potilas olisi kuitenkin todennäköisesti hoidettu immunoglobuliinilla myös ilman näitä muutoksia. Iriittilöydös nimittäin tuki diagnoosia, ja oletettavasti inflammaation merkit olisivat jatkuneet antibioottihoidosta huolimatta.
Kawasakin taudissa haasteena on diagnosoida ja hoitaa lapsi - jonka oireista suurin osa sopii tavallisiin infektioihin - ennen sepelvaltimomuutosten kehittymistä. Taudin tunnistaminen voi olla vaikeaa siksikin, että oireet saattavat fluktuoida ja osa niistä voi olla jo väistynyt hoitoon hakeutuessa. Näin ollen huolellisen anamneesin merkitys korostuu. Lisäksi on havaittu, että kolmasosalla potilaista on samanaikaisesti bakteeri- tai virustautiin sopiva löydös, kuten keuhkokuvamuutos tai nieluviljelyssä kasvava streptokokki, mikä voi vaikeuttaa diagnoosiin pääsyä (17).
Korkeakuumeisen ihottuman voivat aiheuttaa monet bakteeri- ja virustaudit, esim. stafylokokki-infektiot (toksinen sokkioireyhtymä, scalded skin -oireyhtymä), tulirokko, enterorokko, tuhkarokko sekä adeno- tai Epstein-Barrin virus. Taudinkuva voi muistuttaa Kawasakin tautia myös muissa vaskuliiteissä, Stillin taudissa ja tietyissä lääkeainereaktioissa, kuten Stevens-Johnsonin oireyhtymässä.
Epätyypilliseksi tai epätäydelliseksi Kawasakin taudiksi kutsutaan tilannetta, jossa kliiniset kriteerit eivät täyty (taulukko 2 «»3). Tilanne on tavallisin ikäjakauman ääripäissä eli alle 1-vuotiailla ja yli 9-vuotiailla. Näissä ikäryhmissä sepelvaltimomuutokset ovat tavallisia ja kuolleisuus tautiin yleisintä. Imeväisikäisillä tavallisimmat löydökset ovat kuume ja ihottuma, ja puuttumaan jäävät useimmiten lymfadenopatia ja raajamuutokset. Laboratoriolöydöksissä ei ole eroa ikäryhmien välillä (18).
Epätyypillinen Kawasakin tauti on syytä ottaa huomioon myös imeväisen aseptisen meningiitin tai pyelonefriitin yhteydessä. Edellä kuvatussa potilastapauksessakin todettu pyuria tarjoaa helpon selityksen imeväisen kuumeelle, jolloin muut löydökset voivat jäädä huomioimatta. Lisäksi ihottumaa sekä silmien ja suun punoitusta saatetaan pitää lääkeainereaktiona aloitetulle antibioottikuurille, ja tauti voi jäädä diagnosoimatta.
Kun kaulan imusolmuketurvotus on huomattava oire, lapsi saattaa päätyä korvatautien osastolle kaulan lymfadeniitin hoitoon. Kawasakin tauti voi ilmentyä viljelynegatiivisena sokkina, ja tauti onkin pidettävä mielessä, jos epäillyn sepsiksen mikrobilääkehoidolla ei saada vastetta. Mikäli taas vatsa-suolikanavaoireet hallitsevat, lapsi voi päätyä jopa kirurgiseen hoitoon.
Koska Kawasakin taudin inflammaatio rauhoittuu itsekseen, lapsi saatetaan kuumeen ja oireiden helpotettua kotiuttaa ilman diagnoosia, vaikka pahimmillaan hänelle on jo kehittynyt sepelvaltimoaneurysmat. Viikon kuumeilleelle alle 6 kk:n ikäiselle lapselle tulisikin aina tehdä sydämen kaikututkimus, jos kuumeen etiologiasta ei ole varmuutta.
Tavoitteena on pysäyttää inflammaatioreaktio nopeasti ja ehkäistä näin sepelvaltimomuutosten kehittyminen. Diagnoosin viivästyminen liittyy suurempaan riskiin muutosten synnylle, ja kokonaan ilman hoitoa sepelvaltimoaneurysmia kehittyy neljäsosalle potilaista.
Hoidon kulmakivi on suoneen annettu immunoglobuliini (taulukko 3 «»4). Kriteerien täyttyessä tai selvässä tautiepäilyssä hoito tulisi aloittaa viipymättä. Taudin komplikaatiot ovat pahimmillaan fataaleja, ja ajoissa aloitettu immunoglobuliinihoito on tehokasta ja vaaratonta (23). Jotta sepelvaltimomuutosten kehittyminen saataisiin ehkäistyä, hoito tulisi aloittaa 7-10 vrk:n kuluessa kuumeen alkamisesta. Hoito on indisoitu myöhemminkin, jos kuume jatkuu eivätkä tulehdusarvot pienene (mikä kertoo inflammaation jatkumisesta) (16). Rajut oireet kertovat voimakkaasta inflammaatiosta ja ovat huonomman ennusteen merkkejä. Tällöin tehokas hoidon aloitus on erityisen tärkeää (taulukko 3 «»4) (8,24).
Suoneen annetun immunoglobuliinin teho Kawasakin taudin hoidossa havaittiin vuonna 1984 (23). Sepelvaltimomuutosten ilmaantuminen vähenee 25 %:sta 5 %:iin, ja myös muut kliiniset löydökset väistyvät nopeasti. Hoidon vaikutustapaa ei kuitenkaan tunneta.
Hoidolla ei ole vakavia haittavaikutuksia (25), mutta tavallista on 1-2 vrk:n kuluttua ilmaantuva lyhytkestoinen päänsärky, jonka hoidoksi riittää särkylääke. Infuusioreaktioina voi ilmaantua kuumetta, ihottumaa, pahoinvointia ja verenpaineen laskua (24), mutta ne useimmiten helpottavat infuusionopeutta pienentämällä. Eläviä taudinaiheuttajia sisältäviä rokotteita suositellaan annettavan vasta 6 kk:n kuluttua immunoglobuliinihoidosta.
Vaskuliittien hoidon kulmakivi ovat perinteisesti olleet kortikosteroidit. Kawasakin taudissakin niiden hyöty ja turvallisuus on osoitettu useissa tutkimuksissa. Kortikosteroideista hyötyvät erityisesti potilaat, joilla on suuri riski komplikaatioihin (27). Niiden hyödystä jo ensilinjan lääkkeenä on saatu näyttöä japanilaisesta väestöstä (28). Myös länsimaiselle potilaalle tulee harkita metyyliprednisolonin aloittamista primaarisesti immunoglobuliinin rinnalla, jos diagnoosi viivästyy tai taudinkuva on vaikea (29).
Asetyylisalisyylihapon (ASA) käytöllä on pitkä perinne sepelvaltimosairauksien hoidossa, mutta näyttö lääkkeen tehosta Kawasakin taudin sepelvaltimomuutosten ehkäisyssä on vähäistä.
Asetyylisalisyylihappolääkitys aloitetaan suurella anti-inflammatorisella annoksella. Kuumeen laskettua siirrytään pienempään antitromboottiseen annokseen (taulukko 3 «»4). Jos sepelvaltimomuutoksia on todettu, lääkettä käytetään, kunnes sepelvaltimot normaalistuvat. Tarvittaessa käytetään muuta antikoagulaatiohoitoa kuten varfariinia.
Moderneja biologisia lääkkeitä on tutkittu pääasiassa immunoglobuliinihoidolle reagoimattomien potilaiden sekundaarisessa hoidossa. Infliksimabista on näyttöä inflammaation rauhoittamisessa, mutta sepelvaltimomuutosten ilmaantumista sillä ei ole pystytty vähentämään. Muita tutkittuja lääkkeitä ovat esimerkiksi etanersepti, anakinra, siklosporiini ja atorvastatiini (30).
Noin 10-20 % Kawasakin tautia sairastavista ei saa apua primaarisesta hoidosta, ja kuume jatkuu tai uusii immunoglobuliinin annon jälkeen. Nämä refraktaarisesta tautimuodosta kärsivät potilaat ovat kliinisesti merkittävä ryhmä, sillä riski sepelvaltimomuutosten kehittymiselle on heillä yhdeksänkertainen muihin verrattuna. Potilailla, joille muutoksia on kehittynyt, on myös suurempi riski myöhempään sydän- ja verisuonisairastavuuteen (31).
Tämän potilasryhmän tunnistamiseksi ja optimaalisen hoidon löytämiseksi on tehty intensiivistä tutkimusta. Japanissa immunoglobuliinihoidolle reagoimattomien potilaiden seulontaan on käytössä riskilaskureita, mutta näistä ei ole todettu olevan hyötyä länsimaisessa väestössä (32). Nykyisin hoitosuosituksena refraktaarisessa Kawasakin taudissa on immunoglobuliini-infuusion uusiminen ja metyyliprednisolonin tai joskus infliksimabin aloittaminen samanaikaisesti.
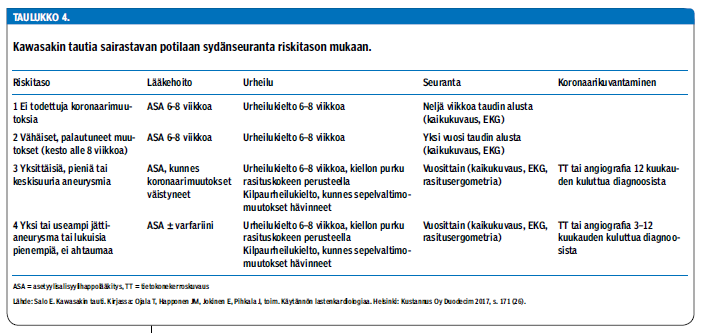
Yleensä immunoglobuliinihoito lievittää nopeasti potilaiden oireita, ja he voivat kotiutua muutaman päivän kuluessa. Koska vakavat sepelvaltimokomplikaatiot saattavat kehittyä vasta kotiutumisen jälkeen, sydämen kaikukuvausta suositellaan diagnoosivaiheessa sekä 2 ja 6 viikon kuluttua taudin alkamisesta (taulukko 4 «»5). Myös sydämen vajaatoiminta, rytmihäiriöt ja sydänlihastulehdus voivat oireilla vasta kotiutumisen jälkeen. Kliinistä tutkimusta suositellaan kontrollikäyntien yhteydessä sekä vuoden kuluttua taudista.
Kawasakin tauti on kehittyneissä maissa yleisin lasten hankinnaisten sydänvikojen aiheuttaja. Taudin on todettu altistavan äkkikuolemalle, sydäninfarktille, vakaville kammioperäisille rytmihäiriöille ja vasemman kammion toiminnanvajaukselle aikuisiällä. Nuoren aikuisen yllättäen ilmaantuvan infarktin tai äkkikuoleman taustalta voikin löytyä lapsuudessa diagnosoimatta jäänyt Kawasakin tauti (33). Suurimmillaan sydäninfarktin riski on vuoden ajan sairastumisesta (34).
Kawasakin tauti todetaan Suomessa noin 30-50 lapsella vuosittain. Vuodesta 1979 alkaen tautiin tiedetään kuolleen yhteensä 9 lasta, ja kahdelle on tehty sepelvaltimoiden ohitusleikkaus. Immunoglobuliinihoito on kuitenkin parantanut ennustetta selvästi. Kuolleisuus on nykyisin noin 0,1 %.
Suurin kuoleman riski on aneurysmapotilailla. Aneurysmien luokittelussa suositellaan käytettäväksi potilaan mittoihin perustuvaa Z-score -luokitusta (31). Merkittävimmät riskitekijät myöhemmille sepelvaltimotapahtumille ovat miessukupuoli, resistenssi immunoglobuliinihoidolle ja suuret (Z-score > 10 tai suonen läpimitta ≥ 8 mm) aneurysmat (31). Pienet, lievästi laajentuneet aneurysmat palautuvat useimmiten normaaleiksi, vaikka joissain tutkimuksissa onkin havaittu, että seinämien rakenne jää pysyvästi paksummaksi ja jäykemmäksi niiden kohdalla (35,36). Tämä saattaa lisätä riskiä ateroskleroosin varhaiselle kehittymiselle. Suurimmat aneurysmat ovat menettäneet verisuoniseinämärakenteensa sisimmät kerrokset, eivätkä voi normaalistua. Yli 8 mm:n läpimittaisiin jättianeurysmiin liittyy merkittävä repeytymisriski taudin ensimmäisten viikkojen aikana ja myöhemmin infarktiriski. Huonoin ennuste on potilailla, joille on kehittynyt useita aneurysmia tai jättianeurysmia (37,38).
Potilaat, joille on kehittynyt sepelvaltimomuutoksia, kuuluvat lastenkardiologin seurantaan. Tromboosien ehkäisyyn käytetään varfariinia ja pienimolekylaarista hepariinia. Jos sepelvaltimoihin kehittyy trombooseja, voidaan tarvita liuotushoitoa tai invasiivisia toimenpiteitä kuten pallolaajennusta ja stenttausta tai jopa ohitusleikkausta. Jos taas potilaalle ei kehity sepelvaltimomuutoksia, seurannan voi nykytiedon mukaan lopettaa vuoden kuluttua sairastumisesta.
Kawasakin taudin diagnosointi voi olla vaikeaa, erityisesti epätyypillisessä taudinkuvassa. Diagnostiikka ei ole täsmällistä, mutta diagnoosin varmistumista eli sepelvaltimomuutosten ilmaantumista ei voi jäädä odottamaan. Näin ollen on hyväksyttävä, että osa potilaista voi saada tarpeettoman hoidon.
Tutkimushaasteena on taudin etiologia. Patogeneesiä ymmärtämällä voitaisiin sekä diagnostiikkaa että hoitokeinoja kehittää spesifisemmiksi. Tärkeää olisi myös tunnistaa ja hoitaa oikein refraktaarisesta tautimuodosta kärsivät potilaat. Lisää tutkimustietoa tarvittaisiin myös taudin pitkäaikaisvaikutuksista ja potilaiden myöhemmästä sairastavuudesta, jotta seuranta voitaisiin järjestää optimaalisesti.
Kiitos Pediatric Research Centerille kirjoitustyön rahoittamisesta.
Kawasaki disease (KD) is a systemic vasculitis occurring in small children and affecting predominantly medium size vessels such as the coronary arteries. It is nowadays the most common cause of acquired heart disease in children. KD has been known now for 50 years. The incidence is highest in Japan, at over 250 per 100 000 children <5 years of age per year; in Caucasian children it is much lower, at about 10 per 100 000 children <5 years of age. Despite intensive research the cause of the disease is unknown, and the long-term cardiovascular risk remains to be ascertained. Coronary artery aneurysms (CAA) are the most serious complication.
Diagnosis is clinical and based on the diagnostic criteria. There is no confirmatory laboratory test. Intravenous immunoglobulin (IVIG) is an effective treatment which lowers the incidence of CAAs from 25% to 5%. Some children do not respond to IVIG and need repeated treatment combined with corticosteroids. Those patients are at a higher risk of developing coronary artery changes.
According to current knowledge, the prognosis of the disease is good. Mortality is about 0.1%. Most patients do not develop coronary changes. Small changes tend to improve by themselves. Long-term morbidity correlates with the size of the CAAs. Large aneurysms may lead to stenosis and obstruction and need bypass surgery or percutaneous interventions.
More research is needed of many issues around KD. The long term cardiovascular risk of patients without coronary artery changes is unknown. Optimal treatment, accurate diagnosis and identification of high-risk patients are essential questions still waiting to be answered.