
Ks. artikkelin pdf-versio «http://www.fimnet.fi/cl/laakarilehti/pdf/2019/SLL192019-1193.pdf»1 Lääkärilehden sivuilla (vaatii FiMnet-tunnuksen).
Ympäristömykobakteerien (eng. nontuberculous mycobacteria eli nontuberkuloottiset mykobakteerit, NTM) ryhmään kuuluu yli 170 lajia, joista parikymmentä aiheuttaa valtaosan ihmisten tulehduksista (1). Ryhmän bakteereita esiintyy hyvin laajasti maaperässä ja vesistöissä myös Suomessa, ja altistumme ympäristömykobakteereille käytännössä koko elämämme ajan jo hyvin nuoresta iästä lähtien (2,3,4). Suomessa noin 70 % kaikista lasten tulehduksista aiheuttaa Mycobacterium avium (5).
Lapsilla ympäristömykobakteerit aiheuttavat pääosin alle kouluikäisten imusolmuketulehduksia (6,7,8). Viljelyvarmistettuja tapauksia todetaan Suomessa alle 5-vuotiailla noin 10 vuosittain (ilmaantuvuus noin 4/100 000 henkilövuotta) (5). Viljelynegatiiviset tapaukset mukaan arvioiden taudin todellinen ilmaantuvuus lienee moninkertainen.
Ulkomailla tapausten esiintyvyydessä on havaittu vuodenajasta riippuvaa vaihtelua, ja esimerkiksi Ruotsissa selkeä tautihuippu sijoittuu syksylle (9,10). Suomessa tautihuippu ei ole yhtä selkeä, vaan tapauksia todetaan yhtä paljon myös keväisin. Lasten yleisin sairastumisikä on 1-5 vuotta, ja tapauksia todetaan Suomessa tytöillä kaksinkertainen määrä poikiin verrattuna (2,5,11,12).
Tulehduksen tarkkaa tartunta- tai syntymekanismia ei tiedetä (2). Imusolmuketulehduksessa tartunta saadaan todennäköisesti suun tai hengitysteiden limakalvojen kautta ympäristöstä; lapsilla hampaiden puhkeaminen tarjoaa infektioportin ja epäkypsä immuunipuolustus lisää tulehdusriskiä (2,12,13).
Valtaosa imusolmuketulehdukseen sairastuvista lapsista on perusterveitä (2,12). Joitain suojaavia tekijöitä ja riskitekijöitä on tunnistettu, mutta on epäselvää, miksi vain pieni osa lapsista sairastuu imusolmuketulehdukseen (2,13). Veden äärellä asumisen ja eläinkontaktien on todettu lisäävän sairastumisriskiä hieman - nämä todennäköisesti lisäävät ympäristömykobakteereille altistumista (9,14).
Harvinaisia iho- tai pehmytkudostulehduksia edeltää usein haava tai vesikontakti, ja lapsilla hyvin harvinaisten keuhkotulehduksen ja eri puolille elimistöön levinneen eli disseminoituneen tulehduksen taustalla on lähes aina jokin altistava tekijä kuten krooninen keuhkosairaus tai immuunipuutos (2,15,16).
Bacillus Calmette-Guérin (BCG)- eli tuberkuloosirokote antaa suojaa ympäristömykobakteerien aiheuttamia imusolmuketulehduksia vastaan. Myös Suomessa tautitapaukset lisääntyivät selvästi yleisen BCG-rokotusohjelman loputtua (1,5). Rokottamattoman lapsen sairastumisriski arvioidaan noin 20-kertaiseksi BCG-rokotettuun verrattuna (1,5).
BCG-rokotteen käyttäminen taudin ehkäisyyn ei kuitenkaan kannata, koska noin 4 835 lasta tulisi rokottaa, jotta ehkäistäisiin yksi tautitapaus. Lisäksi BCG-rokote itsessään aiheuttaa märkivän imusolmuketulehduksen noin 1-2 rokotetulle 1 000:ta rokotettua kohden (1,17).
Taudin ehkäisy ei nykytiedon valossa ole mahdollista, ja yksittäisen perusterveen lapsen sairastumisriski on pieni. Sairastunut lapsi ei myöskään aiheuta muille tartuntavaaraa ja saa käydä normaalisti päiväkodissa.
Ympäristömykobakteeritulehdus voi ilmetä eri puolilla elimistöä, mutta lapsilla tulehduspesäke sijaitsee tavallisesti yhdessä tai useammassa imusolmukkeessa toispuolisena korvan edessä, leukakulmassa tai kaulalla (11,18,19). Havaittu patti ei arista tai kuumota, lapsi on kuumeeton ja hyvävointinen, ja tulehdusarvot ovat normaalit tai vain hieman suurentuneet (12,15,16,19).
Imusolmuketulehdus voi parantua itsestään nopeasti, mutta yleensä tulehdus etenee hiljalleen viikkojen tai kuukausien aikana; imusolmuke nekrotisoituu, kudos hajoaa ja kehittyy märkäkertymä (2). Iho imusolmukkeen päältä ohenee ja muuttuu sinipunaiseksi (2,18,19). Lopulta märkä purkautuu iholle ja muodostuneen fistelin märkäeritys voi kestää muutamasta päivästä jopa useisiin viikkoihin (18,19).
Yleisvointi pysyy hyvänä koko taudinkuvan ajan, ja imusolmuketulehdus paranee itsekseen hyvin. Iho on ehjä yleensä viimeistään vuoden kuluttua (11,18,19). Paikalle jää punoittava arpi, joka vaalenee vuosien saatossa (15,19,20).
Varhaisessa vaiheessa ympäristömykobakteeritulehduksen erottaminen muista tavallisemmista imusolmuketulehduksen aiheuttajista voi olla haastavaa. Hoitokokeilu esimerkiksi kefalosporiinilla on aiheellinen, jos avohoidossa herää epäily muiden bakteerien (esim. streptokokki tai stafylokokki) aiheuttamasta imusolmuketulehduksesta. Vanhempien ohjeistaminen ja vasteen seurannan järjestäminen on kuitenkin tärkeää, koska tilanteen pitkittyessä potilas tulee ohjata erikoissairaanhoitoon.
Pitkittyneesti suurentuneen imusolmukkeen erotusdiagnostiikassa on huomioitava syövän mahdollisuus. Tulehtuneen imusolmukkeen taustalla voi myös olla muu taudinaiheuttaja kuten streptokokki, Bartonella henselae (kissanraapimatauti), Francisella tularensis (jänisrutto) tai Toxoplasma gondii (2). Virusten aiheuttamat imusolmuketulehdukset ovat yleensä molemminpuolisia.
Lapsen hyvä yleisvointi, yleisoireiden puuttuminen, sekä tyypillisen taudinkuvan mukaisesti etenevät kliiniset löydökset ohjaavat työdiagnoosin yleensä ympäristömykobakteeritulehdukseen (16). Taudinkuva on kuitenkin tyypillinen myös tuberkuloosille, jonka mahdollisuus on huomioitava tuberkuloosiriskiryhmään (esim. kotoisin korkean ilmaantuvuuden maasta) kuuluvalla lapsella (2,16,21,22). Tuberkuloottiseen imusolmuketulehdukseen sairastuva lapsi on kuitenkin harvoin alle 5-vuotias (2,22).
Pitkittyneen kaulapatin perustutkimuksiin kuuluvat täydellinen verenkuva, C-reaktiivinen proteiini ja kaikututkimus. Kaikututkimuksen tulkinta vaatii röntgenlääkäriltä kokemusta, ja löydös riippuu imusolmuketulehduksen vaiheesta. Valtaosalla todetaan imusolmukkeen keskustassa kaiuton nesteontelo, joka sopii märkäkertymäksi (23).
Diagnostiikassa on apuna immunologinen verikoe, joka on tällä hetkellä saatavilla ainakin HUSLABissa (B-LyTbIFN) ja TYKSLABissa (B-LyPPDIFN) (24,25). Verikokeessa todetaan valkosolujen reaktio tuberkuliinille (purified protein derivate eli PPD), mutta ei reaktiota tuberkuloosibakteerille spesifisille antigeeneille (26). BCG-rokotus voi aiheuttaa vastaavan tuloksen, joten BCG-rokotetuilla testiä ei voi käyttää diagnostiikassa.
Yleensä tämän laajempia tutkimuksia ei tarvita. Märkäeritteestä voidaan ottaa mykobakteeriviljely kuivaan näyteputkeen tai epäselvissä tilanteissa imusolmukkeesta neulanäyte jatkotutkimuksia varten. Mykobakteerivärjäyksessä tai -viljelyssä bakteeri havaitaan kuitenkin vain noin puolella potilaista (2,26,27). Ympäristömykobakteerin aiheuttaman imusolmuketulehduksen tyypillinen histologinen löydös on nekrotisoiva granulomatoottinen tulehdus (16).
Lasten ympäristömykobakteeritulehdusten hoidosta on vähän laadukasta tutkimustietoa, ja hoitokäytännöt vaihtelevat maailmalla (10,15). Jos tauti tunnistetaan varhain, mahdollisuudet kirurgiseen hoitoon ovat yleensä paremmat. Seurantatutkimusten ja kliinisen kokemuksen perusteella imusolmuketulehdus paranee kuitenkin itsekseen viimeistään vuoden kuluessa, joten kirurginen hoito ei ole välttämätöntä (11,18).
Kokenut korva-, nenä- ja kurkkutautien lääkäri voi harkita imusolmukkeen kokonaispoistoa, mikä voi nopeuttaa paranemista (15,28,29). Kirurgiseen hoitoon liittyy merkittävänä komplikaationa kasvohermohalvauksen riski (10,15). Laajassa katsausartikkelissa kirurgisesti hoidetuista noin 10 % sai väliaikaisen ja 2 % pysyvän kasvohermohalvauksen (11).
Hoitopäätös perustuu yksilölliseen arvioon ja siihen vaikuttavat imusolmukkeen sijainti ja koko sekä vanhempien toiveet (15). Käytännössä imusolmukkeen kirurgista kokonaispoistoa voidaan harkita, kun tulehtunut imusolmuke on alkuvaiheessa vielä pieni ja kiinteä, iho on ehjä ja poiston komplikaatioriski on pieni: imusolmuke sijaitsee muualla kuin korvanedussylkirauhasessa tai kasvohermon alahaaran kulkureitillä alaleukaluun päällä tai alla.
Muilla kirurgisilla toimenpiteillä, kuten kaavinnalla, ei yleensä saavuteta nopeampaa paranemista, mutta käytännössä näillä voidaan helpottaa kookkaan patin aiheuttamaa epämukavuutta (11,29). Vuosien 2007-2017 aikana Helsingin ja Uudenmaan sairaanhoitopiirin korva-, nenä- ja kurkkutautien klinikassa on ollut seurannassa 52 ympäristömykobakteerin aiheuttamaan imusolmuketulehdukseen sairastunutta lasta. Heistä kirurgisesti on hoidettu 19, eikä yhdellekään ilmaantunut kasvohermokomplikaatiota.
Muualla kuin imusolmukkeissa ilmeneviä ympäristömykobakteeri-infektioita hoidetaan yleensä tuberkuloosilääkkeillä, ja useassa maassa myös imusolmuketulehduksen hoitona käytetään edelleen mikrobilääkkeitä (2,10).
Nykynäytön perusteella vaikuttaa kuitenkin siltä, että mikrobilääkkeet eivät nopeuta paranemista (11,30). Hyödystä ei ole näyttöä, mikrobilääkkeillä on haittoja ja imusolmuketulehdus paranee itsekseen hyvin, joten mikrobilääkkeitä ei ole syytä käyttää ympäristömykobakteerin aiheuttaman imusolmuketulehduksen hoidossa.
Ympäristömykobakteerin aiheuttama imusolmuketulehdus paranee itsekseen hyvin, mutta vuotaneesta imusolmukkeesta jää jäljelle yleensä arpi, joka vaalenee vuosien saatossa (20). Valtaosa perheistä on tyytyväisiä pelkkään seurantahoitoon, mutta arpi voi aiheuttaa myös huolta ja kosmeettisen haitan (20). Tarvittaessa lapsi voidaan ohjata plastiikkakirurgin arvioon, mutta luonnollista paranemista kannattaa odottaa ainakin vuoden ajan infektion paranemisesta. Luonnollisesti leikkaushoidosta jää myös aina jäljelle arpi.
Perusterve 3-vuotias tyttö saapui loppukesästä lastentautien poliklinikkaan vasemmassa leukaperässä sijainneen pitkittyneen patin johdosta. Lähettävässä yksikössä täydellinen verenkuva oli ollut normaali ja C-reaktiivinen proteiini alle 3 mg/l. Hoitokokeiluksi oli jo aloitettu amoksisilliini-klavulaanihappo.
Kuumetta tai muita yleisoireita ei ollut, ja vastaanotolla yleisvointi oli hyvä. Iho patin päällä punoitti, ja patti oli tunnustellen kiinteä, liikkuva ja aristamaton. Kaikututkimuksessa nähtiin 20 × 17 × 11 mm:n imusolmukepaketti ilman pahanlaatuiseen tautiin viittaavaa. Amoksisilliini-klavulaanihappokuuria jatkettiin ja hoitoon lisättiin klindamysiini.
Muutaman päivän kuluttua kontrollissa tilanne oli ennallaan, uusittu täydellinen verenkuva normaali ja lasko 7 mm/h. Seuraavassa kontrollissa antibioottikuurien jälkeen patti oli pehmentynyt ja lisätutkimuksena pyydetty keuhkojen röntgenkuva normaali.
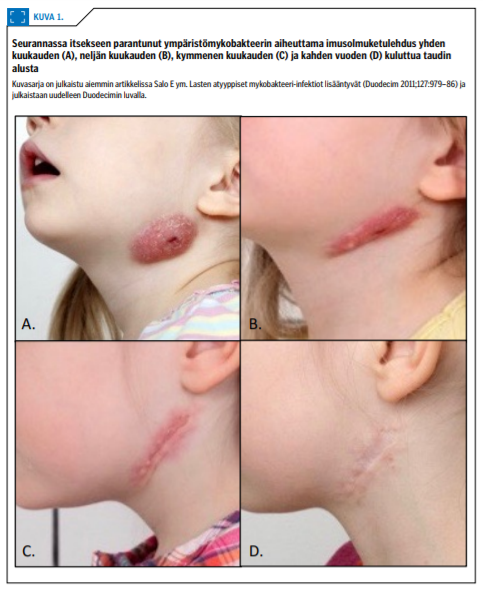
Tytöstä tehtiin lähete yliopistosairaalaan, missä ensimmäisellä käynnillä todettiin, että patti oli hieman kasvanut ja iho patin päällä alkanut hilseillä (kuva 1A «»1). Yleisvointi oli edelleen erinomainen ja tunnustellen patti oli nestetäyteinen.
Uusituissa verikokeissa täydellinen verenkuva oli normaali ja lasko 5 mm/h. B-LyTbIFN-verikokeessa todettiin valkosolujen reaktio PPD:lle, mutta ei reaktiota tuberkuloosibakteerille spesifisille antigeeneille. Tyttö ei ollut saanut BCG-rokotusta, joten tulos vahvisti epäilyä ympäristömykobakteerin aiheuttamasta imusolmuketulehduksesta.
Korva-, nenä- ja kurkkutautien erikoislääkärin arviossa kirurgisesta hoidosta pidättäydyttiin imusolmukkeen sijainnin ja märkäkertymään saakka edenneen tulehduksen johdosta - koko infektoitunut ihoalue olisi jouduttu poistamaan. Perhe ohjeistettiin keräämään mykobakteeriviljelynäyte, kun märkäkertymä aikanaan puhkeaisi. Patti puhkesi kotona ja vanhempien ottamassa viljelynäytteessä kasvoi Mycobacterium malmoense.
Kontrollissa neljä kuukautta taudin alusta puhkeamishaava oli jo kuivunut ja arpeutumassa (kuva 1B). Kymmenen kuukauden ja kahden vuoden kuluttua kontrolleissa todettiin noin 4 cm:n pituinen arpi, joka hiljalleen vaalentui (kuvat 1C ja D «»1).
Ympäristömykobakteerin aiheuttama imusolmuketulehdus on kiusallinen, mutta vaaraton. Pitkälle jatkuneen yleisen BCG-rokotusohjelman johdosta tauti on suomalaiselle tautikirjolle käytännössä uusi - tauti voi säikäyttää niin lapsen vanhemman kuin hoitavan lääkärinkin. Aikainen tunnistaminen on tärkeää, jotta vältytään turhilta lasta ja perhettä rasittavilta tutkimuksilta ja hoidoilta.
Diagnoosin apuna on mahdollista käyttää immunologista verikoetta, jolloin yleensä ei tarvita kajoavia lisätutkimuksia. Taudin luonnollinen kulku on hyvä selventää perheelle heti diagnoosivaiheessa, jotta hidas paraneminen ei yllätä ja aiheuta ylimääräistä huolta.
Kirurgisesta hoidosta päättäminen kuuluu kokeneelle korva-, nenä- ja kurkkutautien erikoislääkärille yhteisymmärryksessä vanhempien kanssa. Valtaosalle hoidoksi riittää perheen kanssa keskusteleminen.
Nontuberculous mycobacteria (NTM) are a large group of ubiquitous environmental bacteria. In children NTM infections present predominantly as cervicofacial lymphadenitis between 1 and 5 years of age. Other clinical manifestations, such as skin, soft tissue, lung or disseminated infection, are rare. Bacillus Calmette-Guérin (BCG) immunisation offers protection against childhood NTM disease. Since discontinuation of universal BCG immunisations in Finland childhood NTM infections have increased. In Finland, the incidence of culture confirmed NTM infection in children under five years of age is approximately 4/100 000/year. The usual clinical presentation is prolonged unilateral cervicofacial lymphadenitis that slowly develops into an abscess with discharge. The child is otherwise healthy. The differential diagnosis of prolonged lymphadenopathy includes other bacterial causes and malignancies and, therefore, the patient must be referred to a paediatrician for consultation. The clinical presentation and progression of NTM lymphadenitis is usually distinctive, however tuberculosis (TB) must be considered in those with a high TB risk. Complete blood count and C-reactive protein are usually normal. Ultrasound imaging and a novel blood based immunodiagnostic test can provide additional diagnostic clues to support the clinical diagnosis rendering further invasive investigations unnecessary. There is no good evidence concerning the optimal treatment of NTM lymphadenitis. However, observational studies and clinical experience show that without any treatment the lymphadenitis heals well within a year. In some cases, surgery can expedite the healing. Early surgical intervention and removal of the infected lymph node is possible if the risks of surgery, e.g. facial nerve palsy, are small. NTM lymphadenitis should not be treated with antibiotics. In Finland, NTM lymphadenitis is an emerging disease that is still new to many clinicians. Early recognition is essential so that unnecessary concern, investigations and treatments can be avoided.