
Ks. artikkelin pdf-versio «http://www.fimnet.fi/cl/laakarilehti/pdf/2020/SLL12020-39.pdf»1 Lääkärilehden sivuilla (vaatii FiMnet-tunnuksen).
Vulvovaginaalisten ongelmien aiheuttama tautitaakka on suuri. Esimerkiksi emätintulehdus on yksi 25 yleisimmästä syystä, joiden takia potilas hakeutuu lääkärin vastaanotolle (1,2). Muista ongelmista tässä käsitellään ulkosynnytinalueen dermatooseja, vulvodyniaa ja emättimen pohjan kiputilaa.
Hyvin varustettuun gynekologiseen potilasvastaanottoon kuuluvat kolposkooppi, vagina-anturilla varustettu ultraäänilaite ja valomikroskooppi vaginaeritteen mikroskopointia eli fluornatiivitutkimusta varten. Fluornatiivitutkimuksen hallitseminen on tärkeää vulvovaginaalisten ongelmien diagnostiikassa.
Koska satunnaistettuja kontrolloituja tutkimuksia ei ole tehty edes monien yleistenkään vulvovaginaalisten ongelmien hoidosta, kliinisen osaamisen ja kokemuksen merkitys korostuu. Hoito-ohjeistusta ei useinkaan ole. Tämä katsaus perustuu 40 vuoden kokemukseeni.
Bakteerivaginoosi on emättimen bakteeritasapainon kvalitatiivinen ja kvantitatiivinen muutos. Terveen emättimen laktobasillifloora puuttuu ja on korvautunut anaerobibakteereilla. Mikrobimäärä on ainakin 1 000-kertainen terveeseen mikrobistoon verrattuna. Anaerobibakteerit tuottavat orgaanisia kaasuja, josta aiheutuu tärkein oire, kalan haju ("fishy smell").
Spesifinen mikrobiologinen syy on epäselvä, vaikka tutkimusta on tehty pitkään. Emättimen mikrobiomi on epänormaali, jolloin suojaava biofilmi puuttuu tai ei toimi. Mikrobiologisia markkereita ovat esimerkiksi Gardnerella vaginalis, Clostridium ja Atopobium vaginalis, mutta bakteerivaginoosia ei voida nimetä yhden spesifisen mikrobin aiheuttamaksi. Geneettisillä tekijöilläkin on merkitystä, koska tila on mustaihoisilla yleisempi kuin valkoihoisilla tai aasialaisilla. Muita riskitekijöitä tunnetaan huonosti.
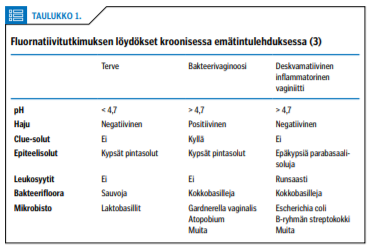
Tyypilliset oireet ovat runsas maitomainen valkovuoto ja haju. Diagnoosi perustuu fluornatiivitutkimukseen (taulukko 1 «»1) ja ns. clue-solujen toteamiseen. Valkosolujen määrä ei ole lisääntynyt.
Bakteerivaginoosi hoidetaan klindamysiiniä sisältävällä paikallisvoiteella tai paikallisella tai peroraalisella metronidatsolilla (taulukko 2 «»2) (3). Lyhyiden mikrobilääkehoitojen jälkeen bakteerivaginoosi uusii helposti. Seksipartnerin hoito ei paranna hoitovastetta.
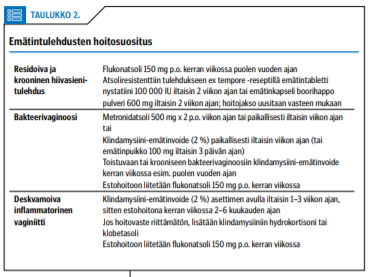
Uusiutuminen on ongelma, johon auttaa parhaiten estohoito mikrobilääkkeellä (klindamysiinivoide) kerran viikossa jopa puolen vuoden ajan. Probioottien tehosta estohoidossa ei ole näyttöä (3).
Bakteerivaginoosi altistaa raskaushäiriöille, sisäsynnytintulehdukselle ja leikkauksenjälkeisille infektioille. Tupakointi kaksinkertaistaa bakteerivaginoosin riskin (4), joten siihen on syytä puuttua.
Deskvamatiivinen inflammatorinen vaginiitti on huonosti tunnettu ja alidiagnosoitu krooninen emätintulehdus (3). Toisin kuin bakteerivaginoosissa, siinä ilmenee voimakas inflammaatio, fluornatiivitutkimuksessa leukosytoosina ja ns. parabasaalisolujen esiintymisenä. Virulentit aerobiset bakteerit aiheuttavat emättimen mikrobiomin häiriö, tavallisesti E. colin, B-ryhmän streptokokin ja enterokokin liikakasvun (tästä nimitys aerobinen vaginiitti).
Tyypillinen oire on runsas, kellertävä (purulentti) valkovuoto. Emättimen limakalvolla voi näkyä punoittavia läiskiä tai petekioita inflammaation merkkinä.
Erotusdiagnostiikka bakteerivaginoosiin ja erottaminen normaalista ei ole mahdollista ilman fluornatiivitutkimusta (taulukko 1 «»1). Mikrobidiagnostiikkaa ei tarvita, koska fluornatiivilöydös on diagnostinen.
Hoidon kulmakivi on paikallinen klindamysiinivoide. Sillä on antimikrobisen vaikutuksen lisäksi anti-inflammatorinen vaikutus, joka parantaa hoitovastetta. Uusimistaipumukseen auttaa estohoito (taulukko 2 «»2). Paikalliseen klindamysiiniin on tärkeätä liittää antimykoottilääkitys, esimerkiksi flukonatsoli 150 mg kerran viikossa. Vaikeissa tapauksissa klindamysiiniin lisätään hydrokortisoni tai klobetasoli anti-inflammatorisen tehon parantamiseksi.
Hiivasienen aiheuttama tautitaakka on ongelma kaikkialla (2). Sukupuolielinten hiivasienitulehduksista valtaosan aiheuttaa Candida albicans.
Hiivasienitulehdus uusii helposti, ja silloin on syytä turvautua estohoitoon, esimerkiksi flukonatsolilla 150 mg kerran viikossa puolen vuoden ajan (taulukko 2 «»2). Estohoidon tehosta on vahva näyttö (5). Seksipartnerin hoidon tehosta uusintaepisodien ehkäisemisessä ei ole näyttöä.
Pieni osa hiivasienitulehduksista on Candida glabratan aiheuttamia. Se on resistentti atsoleille, joten hoidossa pitää turvautua paikalliseen nystatiiniin tai boorihappokapseleihin intervallihoitona kahden viikon jaksoissa. Nystatiini ja boorihappo vaativat ex tempore -reseptin. Sokerin ja ylipäätään makean välttäminen vähentää uusimisia, koska potilailla, joilla on uusiva hiivasienitulehdus, glukoosinsieto on heikentynyt (6).
Lichen sclerosus eli valkojäkälä on ulkosynnytinalueen ihon krooninen dermatoosi, joka on autoimmuunitauti. Diagnoosi on kliininen. Tavallisin oire on hoitoresistentti kutina, joka pakottaa raapimaan. Se taas johtaa ihon jäkälöitymiseen ja aiheuttaa fissuuroita ja häpyhuulten yhteenliimautumista. Valkojäkälää tavataan myös lapsilla, ja heilläkin oireena on kutina (7). Lapsipotilaan tutkiminen on usein ongelmallista.
Histopatologinen diagnoosi tarvitaan hoitoresistenteissä tapauksissa tai jos taudinkuva on epätyypillinen ja diagnoosi epävarma. Histopatologiset löydökset ovat tyypilliset (8).
Valkojäkälän hoito aloitetaan intensiivisellä hoidolla ja sen jälkeen jatketaan estohoitoa. Paras hoitovaste saavutetaan potentilla glukokortikoidilla, klobetasolilla, kahden viikon intervallihoitona 2 kuukauden ajan, niin että hoitojaksojen välillä on kahden viikon tauko. Jos hoitovaste on riittämätön, tutkitaan kolposkopiabiopsia.
Intensiivisen intervallihoidon jälkeen jatketaan estohoitoa 1-2 kertaa viikossa, oli oireita tai ei. Estohoito voidaan tauottaa puolivuosittain. Jos oireet palaavat, hoitoa on syytä jatkaa.
Eurooppalainen hoitosuositus ohjeistaa käyttämään klobetasolia ensimmäisen kuukauden ajan päivittäin, toisen kuukauden ajan joka toinen päivä ja kolmannen kuukauden ajan kahdesti viikossa (9). Ongelma on usein se, että potilas ei uskalla käyttää potenttia kortikosteroidia, koska pelkää sen "ohentavan ihoa". Tämä johtaa usein oireiden uusimiseen ja ihomuutosten pahenemiseen.
Valkojäkälän hoitoon kuuluu myös antimykoottinen estohoito, esimerkiksi flukonatsoli 150 mg kerran viikossa tai painon mukaan. Autoimmuunitautiin liittyvä relatiivisesti heikentynyt soluvälitteinen immuunivaste ja heikentynyt immunologinen valvonta altistavat hiivasienen kantajuudelle.
Valkojäkälä altistaa ulkosynnytinalueen karsinoomalle, useimmiten vanhalla iällä (10). Riski on suurilla potilasaineistoilla tehtyjen syöpärekisteritutkimusten mukaan pieni mutta kiistaton. Jatkuva estohoito pienentää syöpävaaraa.
Seksuaalineuvonta on hyvä muistaa harvinaisissa vaikeissa tapauksissa, joissa tauti on muuttanut ulkosynnyttimien anatomian. Emättimen aukon ahtautuessa ns. vaginasauvadilataatiosta on apua.
Lichen planus eli punajäkälä on toinen ulkosynnytinalueen dermatoosi, joka on myös autoimmuunitauti. Diagnoosi on myös kliininen ja perustuu kutinaan, kirvelyyn ja punoittaviin alueisiin emättimen eteisen limakalvolla. Punoittavat leesiot ovat tarkkarajaisia, epäsymmetrisiä ja kosketusarkoja. Iho-limakalvorajalla voi näkyä tyypillisiä vaaleita arpia, Wickhamin strioja. Näitä voi näkyä myös suussa poskien limakalvoilla ja ikenissä. Diagnoosin varmistamiseksi voidaan tarvita biopsia. Punajäkälän histopatologinen löydös on diagnostinen (11).
Hoidon kulmakiviä ovat potentit kortikosteroidit, kuten klobetasoli, sekä liitännäishoito antimykootilla. Punajäkälään liittyy myös emättimen limakalvon inflammaatio, ns. lichenoidi reaktio. Se näkyy fluornatiivitutkimuksessa mononukleaaristen leukosyyttien lisääntymisenä. Emättimen limakalvon inflammaatioon suositellaan klindamysiiniä paikallisesti estohoitona kerran viikossa, koska sillä on anti-inflammatorinen vaikutus.
Haavaiseen punajäkälään liittyy emättimen limakalvon haavaumia, arpeutumista ja striktuuraa, jotka heikentävät seksuaaliterveyttä. Klobetasolivoiteen applikointi emättimeen sauvan avulla auttaa.
Punajäkälän taudinkuvaan kuuluu usein pitkiäkin remissioita, jolloin hoito voidaan tauottaa. Infektiot altistavat relapseille. Myös punajäkälä lisää syöpävaaraa, erityisesti ulkosynnytinalueen, emättimen ja suunielun syöpien (12).
Zoonin vulviitti eli plasmasoluvulviitti on punajäkälää harvinaisempi ulkosynnytinalueen autoimmuunitauti. Se voi olla yksi punajäkälän ilmenemismuoto.
Oireet ovat samat kuin punajäkälässä eli hoitoresistentti kipu ja kirvely. Tyypillinen löydös on tarkkarajaisten multippelien ruosteenruskeiden tai voimakkaasti punoittavien leesioiden esiintyminen emättimen eteisen limakalvolla.
Oireet ovat invalidisoivia ja hoito ongelmallista. Paras hoitovaste saavutetaan injisoimalla kortiskosteroidia suoraan leesioihin limakalvonalaiskudokseen. Tässäkin taudissa auttaa liitännäishoito antimykootilla.
Lichen simplex eli neurodermatiitti kehittyy kutinan aiheuttaman raapimisen seurauksena. Iho paksuntuu ja jäkälöityy, mikä taas pahentaa kutinaa ja lisää raapimista.
Kutinakierre katkaistaan potentilla kortiskosteroidilla, jota käytetään parin kuukauden intervallihoitona. Hoidon kesto ja räätälöinti vaihtelevat vaikeusasteen mukaan. Hoitoon kannattaa liittää antimykoottinen estohoito.
Neuropaattinen vulvodynia johtuu nervus pudenduksen eli häpyhermon aiheuttamasta kroonisesta kiputilasta. Kipu paikallistuu hermon haarautumisen mukaan joko klitorikseen, häpyhuuliin, perianaalialueelle tai koko ulkosynnytinalueelle.
Gynekologisen sisätutkimuksen tai rektovaginaalitutkimuksen yhteydessä tehty istuinkyhmyn palpaatio provosoi kiputilan. Häpyhermo kulkee kyhmyn mediaalipuolella. Positiivinen palpaatiotesti tukee kliinistä diagnoosia.
Kiputilan syy on tuntematon. Kipu voi alkaa tulehdukseen (esim. vaikea hiivasienitulehdus) tai traumaan liittyvänä (esim. gynekologinen leikkaus tai synnytystrauma). Istuminen pahentaa kiputilaa. Kipu on lievää tai kokonaan poissa aamuisin ja pahenee iltaa kohti.
Potilaista tulee helposti terveyspalvelujen suurkuluttajia. Heille tehdään turhaan laboratorio-, kuvantamis- ja tähystystutkimuksia sekä leikkaustoimenpiteitä. On vaikeaa hyväksyä invalidisoivaa kiputilaa, joka heikentää elämänlaatua. Ohjaus, neuvonta ja valistus ovat avainasemassa, koska potilaat ovat usein muuten suhteellisen terveitä vaikkakin iäkkäitä.
Oman kokemukseni mukaan amitriptyliini on ensisijainen lääke. Sillä saavutetaan lähes aina hyvä tai tyydyttävä hoitovaste, jos potilas sietää lääkkeen. Hoito on syytä aloittaa pienellä annoksella, 10 mg iltaisin pari tuntia ennen nukkumaanmenoa, ja annosta suurennetaan parin viikon välein. Hoitovaste tulee muutaman viikon viiveellä, ja kun se saavutetaan, annosta ei enää suurenneta; useimmiten 10-40 mg riittää.
Amitriptyliinin sivuvaikutukset ovat suhteellisen harvinaisia, jos hoitomyöntyvyys on hyvä. Polyfarmasia ja yhteisvaikutukset muiden lääkkeiden kanssa on syytä pitää mielessä, varsinkin iäkkäämmillä potilailla. Yhteisvaikutusten esiintyvyys on pieni; esimerkiksi amitriptyliinin ja flukonatsolin yhteisvaikutus ei juuri koskaan ole ongelma pieniä annoksia käytettäessä.
Gabapentinoidit ovat amitriptyliinin hoitovaihtoehto, joskaan teho ei ole parempi.
Hyvä ohje on, että lääkitys ajetaan alas pienentämällä annosta kahden viikon välein esimerkiksi puolivuosittain. Jos kipu palaa, potilas on motivoitunut jatkamaan lääkitystä. Lääkityksen tarpeen keston ennakoiminen on vaikeaa.
Vestibuliitti aiheuttaa emättimen eteisen kosketusarkuutta ja yhdyntäkipua. Kirjallisuudessa siitä käytetään eniten termiä vulvar vestibulitis syndrome (VVS) (13,14), muita termejä ovat vulvar pain syndrome, vestibulodynia tai localized provoked vulvodynia.
Vestibuliittioireyhtymä voi olla primaarinen, jolloin kosketusarkuus on ilmaantunut jo esimerkiksi tamponin käytön yhteydessä. Sekundaarinen oireyhtymä ilmaantuu myöhemmin kosketusarkuutena ja yhdyntäkipuna. Potilas kokee kosketuksen kipuna (allodynia). Anamneesi on tyypillinen.
Diagnoosi on helppo tehdä vanutikkutestin avulla (kuva 1 «»3). Kliininen tutkimuslöydös on useimmiten normaali lukuun ottamatta vaginismusta eli emätinkouristusta. Tämä pikkulantion ja emätintä ympäröivien lihasten spasmi liittyy vestibuliittiin sekundaarisena. Kosketusarkuuden ja vaginismuksen takia gynekologista tutkimustakin on usein vaikeaa tai mahdotonta tehdä.
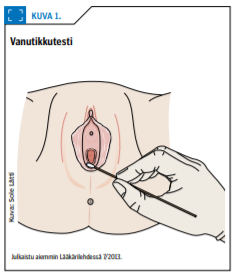
Vestibuliittioireyhtymä johtuu emättimen eteisen limakalvon kroonisesta inflammaatiosta (15). Se johtaa hermosäikeiden proliferaatioon (16), joka taas selittää allodynian. Riskitekijöitä ovat pitkään jatkunut ja nuorella iällä aloitettu yhdistelmäehkäisytablettien käyttö sekä krooninen hiivasienitulehdus tai hiivasienen oireeton tai lähes oireeton kantajuus.
Kliinisessä työssä auttaa hoitopolku (kuvio 1 «»4). Ensivaiheen hoito perustuu yhdistelmäehkäisytablettien käytön tauottamiseen, fysioterapiaan ja pitkään antimykoottihoitoon (esim. flukonatsoli 150 mg kerran viikossa puolen vuoden ajan).
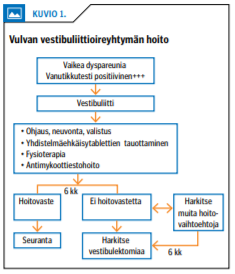
Hoitoresistentit tapaukset ohjataan päiväkirurgiseen vestibulektomiaan, jossa emättimen eteisen kipeä limakalvo poistetaan ja korvataan emättimen limakalvolla (jossa ei esiinny hermosäikeiden proliferaatiota). Vestibulektomia on tehokas hoito vaikeassa vestibuliitissa, ja potilaiden elämänlaadun ja seksuaaliterveyden paranemisesta on hyvä näyttö (17). Ennen toimenpidettä ohjaus, neuvonta ja valistus ovat tärkeitä, koska kirurgiseen hoitoon liittyy myös komplikaatioita kuten verenvuotoa tai haavatulehdus.
Emättimen huipun eli apexin kiputila tunnetaan huonosti ja kirjallisuutta siitä löytyy niukasti (18). Siinä alavatsan ja pikkulantion invalidisoivaan kipuun liittyy emättimen apexin kosketusarkuus. Potilailta on kohtu poistettu vuosia aikaisemmin eri syistä. HYKS:n Naistenklinikan aineistossa potilaiden ikäjakauma oli 44-70 vuotta ja kohdunpoisto oli tehty keskimäärin 11 vuotta aikaisemmin. Tutkimustietoa oireyhtymän ilmaantuvuudesta kohdunpoiston läpikäyneillä potilailla ei ole.
Kiputilaa on vaikea paikallistaa. Jatkuvaa kipua tuntuu pikkulantiossa navan alapuolella keskellä tai molemmin puolin, ja se säteilee ulkosynnyttimiin, ristiselkään, pakaroihin tai reisiin. Kipu pahenee iltaa kohti. Se vaikeuttaa pitkään paikallaan istumista ja estää harrastuksia.
Diagnostinen testi on helppo. Gynekologisen spekulatutkimuksen yhteydessä (ns. ankannokkaspekula) etsitään emättimen apex ja varmistetaan, että limakalvo on normaali. Kun vanutikulla tai papaharjalla koskettaa kevyesti apexin molempia nurkkia ja keskiviivaa, seurauksena on suhteettoman voimakas kipu (allodynia) ja väistöreaktio.
Kiputilan takia potilaille on tehty runsaasti laboratorio-, tähystys- ja kuvantamistutkimuksia, mutta löydökset ovat normaaleja. Potilaat käyttävät suuria määriä kipulääkkeitä ja hermokipulääkkeitä saamatta apua. Paikallinen tai systeeminen estrogeenihoito ei myöskään auta.
Oireyhtymän on ensimmäisenä kuvannut LL Eero Saarela, ja siksi sitä on kutsuttu myös Saarelan taudiksi. Kiputilan tunnistaminen on tärkeää, koska potilaista tulee helposti terveyspalvelujen suurkuluttajia. Tunnistaminen on suuri helpotus potilaille.
Kiputilaa hoidetaan emättimen apexin neuromodulaatiolla, kortisoni-bupivakaiinipistoksilla kipupisteisiin, häpyhermon puudutuksella ja pieniannoksisella hermokipulääkityksellä (amitriptyliini) tai näiden yhdistelmällä. Niiden avulla potilaiden elämänlaatu paranee.
Vulvovaginaaliset ongelmat aiheuttavat ahdistusta ja masennusta. Elämänlaatu heikkenee ja seksuaaliterveys kärsii. Ongelmilla on myös taipumus uusia. Tämä johtaa helposti tutkimus- ja hoitokierteeseen, ja potilaista tulee helposti terveyspalvelujen suurkuluttajia. Hyvä ja pysyvä hoitosuhde lääkärin kanssa on erityisen tärkeä näitä potilaita hoidettaessa, koska näyttöön perustuvaa hoito-ohjeistusta ei ole.
Vulvovaginal problems cause a large disease burden. The most common clinical problems are bacterial vaginosis, desquamative inflammatory vaginitis, recurrent yeast infection, vulvar dermatoses, and vulvar pain syndromes. Expert opinions are often needed since evidence based guidelines on the diagnosis and treatment of these syndromes are few or non-existent. This review is based on the author´s clinical experience in the management of these problematic conditions, and is intended to assist clinicians in the management of such problem cases. These patients suffer from low quality of life, are often depressed and anxious, frequently undergo unnecessary more or less invasive tests, and often are heavy health care users.