
Ks. artikkelin pdf-versio «https://www.laakarilehti.fi/pdf/2020/SLL102020-607.pdf»1 Lääkärilehden sivuilla (vaatii FiMnet-tunnuksen).
Yhdeksän kymmenestä SLE-tautiin sairastuneesta on naisia. Heillä tauti puhkeaa useimmiten hedelmällisten vuosien tai menopaussin tienoilla. Lapsilla tauti alkaa keskimäärin 13 vuoden iässä (1,2).
Mikä tahansa elin voi sairastua. Tyypillisiä löydöksiä ovat perhosihottuma kasvoilla, limakalvohaavaumat, nivelkivut, nestekertymä keuhko- tai sydänpussissa, muutokset verenkuvassa ja proteinuria (1,3).
Taudinkuva vaihtelee yksilöllisesti. Rauhalliset ja aktiiviset tautivaiheet aaltoilevat. Pitkään aktiivisena jatkuva tulehduksellisuus johtaa kudostuhoon (4). Vaikeahoitoiseen tautiin viittaavat keskushermosto-oireet, vakavat verenkuvamuutokset, munuaislöydökset, fosfolipidivasta-aineet sekä sydän- ja keuhkolöydökset (3-5).
Taudin synty tunnetaan huonosti, mutta poikkeavan immunologisen prosessin uskotaan alkavan jo vuosia ennen taudin kliinisiä merkkejä. Taudille altistavia immunologisia poikkeavuuksia ilmenee monella eri tasolla. Immunologinen häiriö on erilainen eri yksilöillä, ja tausta on yleensä monigeeninen (6).
Keskeistä on immunologisen toleranssin murtuminen, jolloin elimistö tunnistaa omia solurakenteita vieraiksi ja aloittaa patologisen puolustusreaktion (7). Tulehdusreaktiossa tärkeitä soluvälittäjäaineita tuotetaan tavallista runsaammin (mm. IFN-α, IL-17, IL-6 ja IL-21), ja ne kiihdyttävät edelleen tautiprosessia.
Taudille ovat tyypillisiä moninaiset autovasta-aineet sekä immunokompleksien runsas muodostuminen ja kertyminen kudoksiin. Kudoksissa, esimerkiksi munuaisten tyvikalvoilla, immunokompleksit häiritsevät kohde-elimen toimintaa.
Lisäksi ilmenee suoraa kudostuhoa autovasta-aineiden ja aktivoituneen immuunijärjestelmän myötä, normaalia runsaampaa neutrofiileillä esiintyvää erityistä solukuolemaa (NEToosia) ja komplementin toimintahäiriöitä (7,8). Immunologisessa prosessissa syntyviä kudosjätteitä poistuu normaalia tehottomammin, mikä johtaa apoptoottisen materiaalin kertymiseen kudokseen sekä edelleen lisääntyneeseen antigeenin esittelyyn (7).
Viime vuosina on opittu tuntemaan epigeneettisiä säätelymekanismeja taudin taustalla (8). Tupakoinnilla ja tietyillä virusinfektioilla (esim. Epstein-Barrin virus) on todennäköisesti osuus taudin synnyssä (1,9). Naishormonien, kuten estrogeenin, merkittävään rooliin tautiprosessissa viittaa se, että tauti ilmaantuu enimmäkseen naisille ja ilmaantuminen ajoittuu hormonitasojen heilahteluvaiheisiin (1,8). Auringonvalo voi laukaista ihomuutoksia, kuten tyypillistä kasvojen perhosihottumaa, ja aktivoida perustautia (1,10).
Taudin ilmaantuvuus ja taudinkuva vaihtelevat huomattavasti etnisen ryhmän, sukupuolen ja taudin puhkeamisiän mukaan. Tauti on selvästi harvinaisempi ja taudinkuvaltaan usein lievempi eurooppalaisilla kuin esimerkiksi afroamerikkalaisilla tai aasialaisilla (1,4,8). Lapsilla SLE on harvinaisempi mutta taudinkuvaltaan usein rajumpi kuin aikuisilla (1,2). Suomessa taudin ilmaantuvuus on aikuisilla 1,7-3,8/100 000 henkilöä/vuosi (2,11) ja lapsilla 0,4/100 000/v (2,12). Taudin esiintyvyys on 28/100 000 (13).
Lievän tai alkavan taudin tunnistaminen on haasteellista. Yleisoireina on usein lämpöilyä, voimakasta väsymystä ja laihtumista. Käytännössä löydöksiä voi olla missä tahansa kudoksessa tai kohde-elimessä. Niveloireet ovat yleisiä. Laajakirjoiset, useaan kohde-elimeen liittyvät samanaikaiset oireet ja löydökset voivat herättää epäilyn taustalla olevasta systeemisestä taudinkuvasta.
Taudissa esiintyy usein verenkuvamuutoksia. Tyypilliset oireet, kuten limakalvohaavaumat, auringon laukaisemat iho-oireet, sydän- ja keuhkopussitulehdus sekä Raynaud’n oire voivat ohjata ajatukset SLE:hen. Toisinaan SLE voi alkaa vaikealla taudinkuvalla, kuten psykoosilla, epileptisellä kohtauksella tai munuaistulehduksella (1,3,6,14). Tällöin tarvitaan laaja-alaisia selvittelyjä ennen diagnoosia.
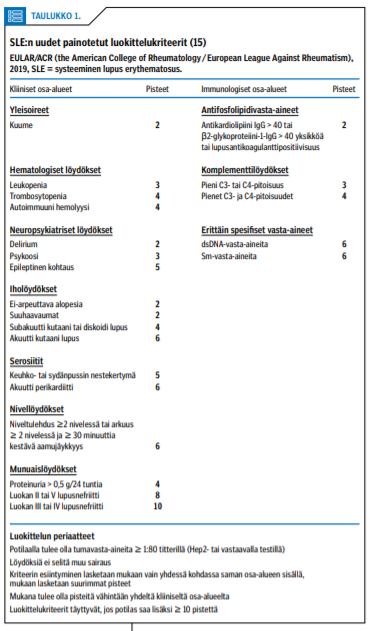
Tyypillinen taudinkuva, kliiniset tutkimuslöydökset ja laboratoriotutkimukset varmistavat diagnoosin, joka tehdään yleensä erikoissairaanhoidossa. Oirekirjoa kuvaavat hyvin luokittelukriteerit, joita voi käyttää apuna taudin erottelemiseksi muista autoimmuunisidekudossairauksista. Uudet painotetut luokittelukriteerit on julkaistu äskettäin (15) (taulukko 1 «»1). Laajan oirekuvan vuoksi vaihtoehtoisia diagnooseja on runsaasti (16,17) (taulukko 2) «»2.

Potilailla on usein hypersedimentaatiota. CRP-arvo voi olla normaali mutta suurenee toisinaan aktiivisessa taudissa. Se voi viitata myös infek-tioon. Verenkuvassa havaitaan leuko-, neutro- ja lymfopeniaa, lievää anemiaa ja trombosyto-peniaa. Usein erityisesti leuko- ja lymfopenia heijastelevat aktiivista tautia.
PLV-näyte on hyvä seulontakoe epäiltäessä SLE:tä. Virtsassa voi olla valkuaista, valkosoluja ja punasolulieriöitä. Seerumin kreatiniiniarvo on hyvä tarkistaa. Proteinurian yhteydessä tutkitaan joko vuorokausivirtsan proteiini tai albumiinin ja kreatiniinin suhde virtsasta (15,18).
SLE:tä epäiltäessä kannattaa tutkia tumavasta-aineet. Jos niitä löytyy, jatkotutkimuksina pyydetään DNA-vasta-aineet ja tuman liukoiset vasta-aineet eli ENA-vasta-aineet. Jos epäillään lääkeainelupusta, tutkitaan lisäksi histonivasta-aineet.
Laboratorioiden tutkimuspaketeissa on jonkin verran eroja, mutta ENA-vasta-aineet sisältävät yleensä SLE:n alkudiagnostiikassa tarvittavat tumavasta-aineiden alaluokkajaottelut (Smithin, SSA-, SSB- ja RNP-vasta-aineet) (19,20). Osassa laboratorioista jatketaan suoraan ENA-vasta-ainetutkimukseen, kun tumavasta-ainetutkimuksen tulokset ovat positiiviset.
Potilaiden vasta-aineprofiilit vaihtelevat. Positiiviset DNA- ja Smithin vasta-aineet tukevat SLE-diagnoosia (15,19). SSA- ja SSB- tyypin vasta-aineita esiintyy SLE:n lisäksi Sjögrenin oireyhtymässä ja U1-RNP-vasta-aineita sekamuotoisessa sidekudossairaudessa (MCTD) (19,20). Taudin merkkejä voivat olla komplementtien C3 ja C4 kulutus sekä komplementin toimintaa kuvastavan kokonaishemolyyttisen aktiivisuuden (CH50) pieni arvo. C3- ja C4-komplementtien pienet pitoisuudet ja suuret DNA-vasta-ainepitoisuudet voivat kertoa aktiivisesta taudista. Hoidon ratkaisee kuitenkin taudin kliininen kuva (18). Aktiivisen SLE:n lisäksi komplementtipitoisuudet voivat olla pienet myös perinnöllisissä puutoksissa.
Erikoissairaanhoidossa tutkitaan harkinnanvaraisesti fosfolipidivasta-aineet toistuvia tukoksia tai keskenmenoja saavilta potilailta, ribosomaaliset P-proteiini-vasta-aineet neuropsykiatrisesti oireilevilta ja C1q-vasta-aineet munuaispotilailta (19).
Iho- ja limakalvomuutokset ovat tavallisia, ja iholta otettu koepala voi olla tarpeen diagnostiikassa. Iho-oireet jaetaan kutaanisiin (sisältäen akuutit ja subakuutit ihomuutokset) ja kroonisiin kutaanisiin lupus-muutoksiin.
Ensimmäiseen luokkaan kuuluvat mm. auringon laukaisemat ihomuutokset, esimerkiksi kasvojen perhosihottuma sekä subakuutti ja makulopapulaarinen lupus. Jälkimmäiseen luokkaan sisältyy mm. keskeltä arpeutuva diskoidi lupus (1). Taudissa esiintyy myös ei-arpeuttavaa pälvikaljuisuutta (15). Oirekirjoon liittyy vaskuliitti tavallisesti pienten suonten alueella, ja nämä löydökset havaitaan usein iholla. Vaskuliitti voi esiintyä muuallakin, kuten suolistossa, ääreis- ja keskushermoston alueella tai munuaisissa (14,21).
Munuaismuutokset ovat yleisiä ja lisääntyvät taudin edetessä. Ne ovat alkuun vähäoireisia, ja vasta myöhemmässä vaiheessa ilmaantuu turvotuksia, polyuriaa ja munuaisten vajaatoiminnan muita merkkejä. Virtsan seulonta kannattaa kaikissa taudin vaiheissa.
Munuaistaudin ns. hiljaisia löydöksiä ovat valkuaisvirtsaisuus, mikroskoopissa nähtävät virtsan punasolulieriöt, verenpaineen nousu, suuret DNA- ja C1q-vasta-ainepitoisuudet ja pieni C3-komplementtipitoisuus. Seerumin kreatiniinipitoisuuden suureneminen viittaa munuaisten toiminnan häiriöön (18,21). Munuaistaudin vaikeusastetta arvioidaan munuaisista otetun koepalan histologian perusteella. SLE:hen liittyvän munuaistaudin vaikeusasteen histologinen jaottelu ohjaa hoidon valintaa (22).
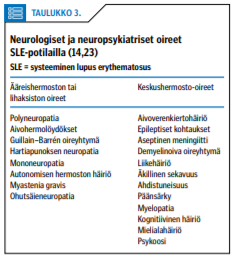
Neuropsykiatriset oireet ovat moninaiset (taulukko 3 «»3). Niiden yhdistäminen SLE:hen on haastavaa ja etenee yleensä poissulkumenetelmällä (14,23).
Nivelten ja lihasten kipuilu on tavallista. Niveltulehduksia esiintyy, mutta ne eivät yleensä syövytä niveliä. Käsien nivelmuutoksia aiheuttavaa Jaccoudin artropatiaa tavataan. Lihastulehdukset ovat harvinaisia. Potilailla esiintyy myös avaskulaarista luunekroosia ja luukatoa, joka voi johtua osin glukokortikoidihoidosta (3,18,21).
Keuhko- ja sydänpussitulehdus sekä ateroskleroottinen sydänsairaus ovat sydän- ja keuhko-oireista tavallisimpia. SLE-potilailla on suuri sydän- ja verisuonisairauksien riski. Perinteiset sydän- ja verisuonisairauksien riskitekijät eivät selitä potilaiden tavallista runsaampaa ateroskleroosia, jonka on todettu kiihtyneen jo taudin alkuvaiheessa. Myös sydämen johtumis- ja rytmihäiriöitä, sydänlihastulehdusta, endokardiittia ja sydämen läppien toimintahäiriöitä esiintyy (21,24). Keuhkolöydöksiä ovat mm. keuhkoverenvuoto, pneumoniitti, keuhkoverenpaineen nousu ja keuhkoembolia (21).
Noin puolella sairastuneista on ruuansulatuskanavan oireilua. Oireet ovat tavallisesti lieviä, esimerkiksi pahoinvointia tai vähäistä vatsakipua. Oirekirjo on laaja, esimerkiksi vatsakalvon tulehdus, ruokatorven oireet, vatsahaava, tulehduksellinen suolistosairaus, haima- ja maksatulehdus sekä maksan suureneminen. Vaikeampia ja harvinaisia ilmentymiä ovat suoliliepeen vaskuliitti ja tromboosi. Tämän kaltainen vaskuliitti on todennäköisin, kun perustauti on aktiivinen ja potilaalla on kovaa vatsakipua (21,25).
Verenkuvassa leuko- ja lymfopenia ovat tavallisesti lieviä eivätkä tällöin edellytä jatkotoimia. Neutropenia voi viitata infektioon tai lääkesivuoireeseen mutta liittyy toisinaan myös perustautiin.
Anemia johtuu usein tulehduksesta ja korjaantuu tautiaktiivisuuden sammuessa. Anemia voi olla taustaltaan monisyinen ja liittyä esimerkiksi vuotoon, munuaisten vajaatoimintaan tai lääkehoitoon. Joskus harvoin potilailla esiintyy autoimmuunihemolyyttistä anemiaa, jolloin iho voi kellertää ja virtsa värjäytyä punertavaksi. Retikulosytoosi on tuolloin lisääntynyt ja Coombsin kokeen tulos on positiivinen.
Trombosytopenia johtuu usein autovasta-aineista, kuten trombosyytti- tai fosfolipidivasta-aineista. Trombosytopenia on yleensä lievä (50-150 x 10<sup>9</sup>/l). Tromboottista trombosytopeniaa tavataan hyvin harvoin (26,27). Fosfolipidivasta-aineita on noin kolmanneksella potilaista. Niihin liittyy laskimoiden ja valtimoiden tukosten, alkuraskauden toistuvien keskenmenojen, raskaustoksemian sekä ennenaikaisen synnytyksen suurentunut riski (14,21,28).
Aktiivinen tauti, erityisesti munuaismuutokset, voi hankaloittaa raskauden kulkua merkittävästi. Keskenmenot, ennenaikaisuus, raskausmyrkytys ja lapsen pienipainoisuus ovat SLE-potilailla yleisempiä kuin muilla.
Fosfolipidivasta-aineiden lisäksi myös SSA- ja SSB-vasta-aineilla voi olla vaikutusta raskauden kulkuun. Ne voivat altistaa sikiön neonataalilupukselle tai sydämen eteiskammiokatkokselle. Neonataalilupuksessa vastasyntyneellä saattaa olla iho-oireita, maksa-arvojen suurenemista ja verenkuvamuutoksia, jotka väistyvät yleensä puolen vuoden kuluessa synnytyksestä. Tämän kaltaiset ongelmat ovat hyvin harvinaisia SLE-potilailla (3,28).
Laajan ja vaihtelevan oirekirjon vuoksi jokaisen potilaan hoito on suunniteltava yksilöllisesti. Lääkevalintoja ohjaavat elinkohtaiset oireet (1,29). Jo syntyneet elinvauriot on eroteltava edelleen jatkuvasta tulehduksesta (30).
Kun taudinkuva on lievä, hoidoksi riittää ihon suojaaminen auringolta, hydroksiklorokiini ja tulehduskipulääkkeet (1,29). Hydroksiklorokiini parantaa kokonaisennustetta ja rasvaprofiilia sekä estää tukoksia ja taudin lieviä pahenemisvaiheita. Sitä suositellaankin kaikille SLE-potilaille, joilla ei ole vasta-aiheita. Vaikeammissa taudinkuvissa hydroksiklorokiinin teho jää vajaaksi (31).
Glukokortikoidit ovat hoidon peruspilari erityisesti vaikeampien tautimuotojen, kuten lupusnefriitin, hoidossa. Haitallisten sivuvaikutusten vuoksi pyritään lyhytkestoiseen hoitoon ja pienentämään annosta nopeasti tilanteen salliessa (32). Usein rinnalle lisätään muuta immunosuppressiivista hoitoa, joka valitaan yksilöllisesti taudinkuvan mukaan (29).
Lupusnefriitin hoito aloitetaan usein syklofosfamidilla tai mykofenolaatilla. Ylläpitohoitoon soveltuvat mykofenolaatti ja atsatiopriini sekä vaihtoehtoisena siklosporiini. Niveltulehdusoireiset potilaat voivat hyötyä metotreksaatista (1,27,29). Raskaana olevia potilaita voidaan tarvittaessa lääkitä hydroksiklorokiinilla, atsatiopriinilla tai siklosporiinilla (28).
Ihon suojaaminen auringonvalolta on tärkeää. Iho-oireissa riittää usein paikallinen glukokortikoidivoide tai takrolimuusi. Tarvittaessa käytetään myös hydroksiklorokiinia ja glukokortikoidia suun kautta sekä toissijaisena immunosuppressiivista hoitoa, kuten metotreksaattia.
Kun tauti vastaa perinteiseen hoitoon huonosti, voidaan potilasta tietyissä tilanteissa hoitaa erityisesti immunologisesti aktiivisen SLE:n hoitoon kehitetyllä ja suoneen annettavalla belimumabilla. Perinteiseen hoitoon reagoimattomassa taudissa, esimerkiksi vaikeissa verenkuvamuutoksissa tai lupusnefriitissä, voidaan kokeilla rituksimabia (1,27). European League Against Rheumatism (EULAR) on antanut yleisohjeistusta potilaiden lääkehoitoon ja seurantaan (18,29).
Jos potilaalta löydetään fosfolipidivasta-aineita kahdesti kolmen kuukauden välein mitattuna, tukosten primaariseksi ehkäisyksi suositellaan pieniannoksista asetyylisalisyylihappoa. Immobilisaation yhteydessä suositellaan lisäksi pienimolekyylistä hepariinia. Pysyvä antikoagulaatiohoito on paikallaan, jos potilas on aiemmin saanut useita tukoksia (29,33).
Osin tautiin liittyvien immunologisten häiriöiden, osin lääkityksen vuoksi potilaat saavat herkästi infektioita. Rokotuksilla on keskeinen rooli infektioiden ehkäisyssä. Immunosuppressiivista lääkitystä saaville potilaille ei kuitenkaan suositella eläviä taudinaiheuttajia sisältäviä rokotteita (9).
Potilaiden merkittävästi suurentunut sydän- ja verisuonisairauksien riski tulisi huomioida seurannassa aiempaa paremmin. Kohonnutta verenpainetta, verensokeri- ja rasva-arvoja sekä lihavuutta hoidetaan samojen Käypä hoito -suositusten määrittelemien raja-arvojen ja hoitomenetelmien mukaan kuin hoidettaessa muitakin potilaita, joilla sydän- ja verisuonisairauksien riski on suuri (29, 34). Taudin aktiivisten vaiheiden tehokas hoito ehkäisee myös ateroskleroosin muodostusta (1). Lääkityksessä suositaan hydroksiklorokiinia (1,31), ja glukokortikoidihoidon kestoa pyritään rajaamaan (32).
Osa SLE:n hoitoon käytetyistä lääkkeistä, kuten metotreksaatti, mykofenolaatti ja syklofosfamidi, ei sovellu käytettäväksi raskauden aikana. Siksi tarvitaan luotettavaa raskauden ehkäisyä (28,29). Ehkäisymenetelmä valitaan potilaskohtaisesti.
Huomioon on otettava mm. taudin aktiivisuus, munuaissairaus, vasta-aineprofiili, aiempi tukostausta ja verenpaine. Yhdistelmäehkäisypillerit eivät sovellu potilaille, joilla on fosfolipidivasta-aineita tai vaikea, aktiivinen perussairaus. Jos potilaalla ei ole fosfolipidivasta-aineita, voidaan harkita progestiinia sisältäviä pillereitä sekä kohdunsisäistä kierukkaa (hormoni tai kupari). Jos tukosriski on suurempi, potilaalle suositellaan kuparikierukkaa tai estemenetelmiä, kuten kondomia (28).
Potilaan suunnitellessa raskautta pyritään siihen, että tauti olisi ollut rauhallinen vähintään puoli vuotta ennen kuin raskautta yritetään. Raskausaikana äidin ja sikiön hyvinvointia (mm. kasvu ja syke) seurataan tiiviisti neuvolassa ja äitiyspoliklinikalla. Hydroksiklorokiini voi suojata sikiötä eteis-kammiokatkokselta, ja sen käyttöä suositellaankin jatkettavaksi raskausajan yli etenkin, jos äidillä on SSA- ja SSB-tyypin vasta-aineita (28,29).
Jos potilaalla on suurentunut riski saada raskausmyrkytys esimerkiksi fosfolipidivasta-aineiden tai munuaistaudin vuoksi, suositellaan pieniannoksista aspiriinihoitoa. Jos tautiin liittyy fosfolipidivasta-aineoireyhtymä, suositellaan lisäksi hepariinia (29,35).
Taudin diagnoosi varmistetaan erikoissairaanhoidossa. Lieviä taudinkuvia voidaan seurata ja hoitaa perusterveydenhuollossa. Jos tauti on rauhallisessa vaiheessa, suositellaan vastaanottoa noin kerran vuodessa. SLE:n seurannassa on huomioitava monia tekijöitä, kuten laaja oirekirjo, infektioherkkyys ja liitännäissairaudet (taulukko 4). Tilanteen aktivoituessa suositellaan konsultoimaan erikoissairaanhoitoa.
Varhainen, tehokas ja liitännäissairaudet huomioiva hoito parantaa ennustetta. SLE-potilailla on jo taudin varhaisessa vaiheessa noin viisinkertainen työkyvyttömyysriski muuhun väestöön nähden. Ennenaikaisen eläköitymisen taustalla ovat useimmiten itse perussairaus, tuki- ja liikuntaelinongelmat sekä psyyken sairaudet (36).
Potilaiden eliniänodote kasvoi vuosituhannen vaihteeseen saakka ainakin lyhyellä aikavälillä tarkasteltuna, mutta hyvä kehitys on tasaantunut viime vuosikymmeninä (37). Kuolleisuuden riski varhaisessa taudissa on Suomessa noin 1,5-kertainen muuhun väestöön nähden. Kuolinsyistä tärkeimmät ovat sydän- ja verisuonisairaudet, maligniteetit, SLE itse ja infektiot (38).
Uudet painotetut kriteerit tuovat taudin diagnostiikkaan uuden työkalun. Taudinkuvan moninaisuus haastaa hoitavan lääkärin, ja yhteistyötä tarvitaan perusterveydenhuollon sekä erikoissairaanhoidon eri erikoisalojen välillä. Keskeistä on tunnistaa tavallista aktiivisempaa hoitoa tarvitseva potilas ja sitouttaa hänet hoitoon jo varhain.
Systemic lupus erythematosus is a rare and multi-dimensional disease which can potentially be life-threatening. Most of the patients are females. Drug therapy is always individually designed according to the disease course and affected organs. Hydroxychloroquine is highly recommended for every patient who can tolerate it. Most patients need a combination of glucocorticoids and immunosuppressive agents for therapy. The risk for cardiovascular disease or infection is increased among these patients. Early diagnosis using the new EULAR/ACR classification criteria, active drug therapy and treatment of comorbidities ensure the best possible result.