
Ks. artikkelin pdf-versio «http://www.fimnet.fi/cl/laakarilehti/pdf/2023/SLL39-40-2023-1503.pdf»1 Lääkärilehden sivuilla (vaatii FiMnet-tunnuksen).
Virtsatieinfektiot aiheuttavat noin 5-10 % lasten päivystyskäynneistä (1). Niiden ilmaantuvuus on suurin imeväisillä ja pienillä lapsilla (2). Noin 2 % lapsista sukupuolesta riippumatta sairastaa virtsatieinfektion kahden vuoden ikään mennessä (3). Imeväisiän jälkeen ilmaantuvuus laskee erityisesti pojilla. Leikki-iässä infektioita esiintyy edelleen tytöillä kohtuullisen usein, pojilla ne ovat hyvin harvinaisia (4). Infektio uusiutuu noin 12-15 %:lla lapsista (5).
Virtsatieinfektiossa suoliston mikrobistoon kuuluvat bakteerit pääsevät nousemaan virtsateihin. Tapauksista 80-90 % aiheuttaa Escherichia coli (6,7). Seuraavaksi yleisimmät patogeenit ovat klebsiellat ja Pseudomonas aeruginosa. Grampositiivisia enterokokkeja löytyy muutamassa prosentissa tapauksista (6,7).
Vaippahygienialla eli vaippojen vaihtotiheydellä, tyypillä tai vaippa-alueen pesujen tiheydellä ei ole osoitettu olevan vaikutusta virtsatieinfektion riskiin (8). Imetys suojaa tehokkaasti infektiolta ensimmäisten elinkuukausien aikana (9). Suojaava teho säilyy sitä pidempään, mitä pidempään imetystä on jatkettu (10).
Suojavaikutuksen mekanismeista on useita teorioita. Imetys todennäköisesti muovaa lapsen mikrobiomia suotuisaan suuntaan. Lisäksi imetettyjen lasten virtsaan erittyy verrokkeja enemmän laktoferriiniä sekä IgA-luokan vasta-aineita, jotka molemmat tarjoavat suojaa patogeenejä vastaan (9).
Lapsilla vähäisen juomisen ja harvoin tapahtuvan virtsaamisen on osoitettu lisäävän toistuvien virtsatieinfektioiden riskiä. Myös ummetusta on perinteisesti pidetty riskitekijänä, mutta tämän suhteen tieteellinen näyttö on epäselvää (9). Imeväisillä virtsaamisen yhteydessä tapahtuva virtsan takaisinvirtaus virtsarakosta munuaisia kohti (vesikoureteraalisen takaisinvirtaus) on tavallinen ilmiö, mikä selittänee pyelonefriitin eli munuaisaltaan ja munuaisen tulehduksen yleisyyttä ja uusiutumista imeväisillä (5,9).
Poikien ympärileikkausta ei Suomessa käytetä virtsatieinfektioiden ehkäisyyn. Muista syistä tehdyn ympärileikkauksen on osoitettu vähentävän hieman poikien virtsatieinfektioita imeväisiässä (11), mutta hyöty on vähäinen eikä ympärileikkausta tule käyttää virtsatieinfektion ehkäisykeinona.
Pienillä lapsilla on harvoin suoraan virtsateihin viittavia infektio-oireita, kuten kipua virtsatessa, vaikeutunutta virtsaamista tai kylkikipua. Virtsanäyte tulee ottaa kuumeiselta imeväiseltä tai pieneltä lapselta, jolla ei ole osoitettavissa muuta infektiofokusta. Näyte otetaan ennen antibioottihoidon aloitusta (12). Positiivisen näytteen antaneiden potilaiden uusintanäytteistä kaksi kolmesta on negatiivisia yhden antibioottiannoksen jälkeen. Kolmen annoksen jälkeen vain noin 7 % uusintanäytteistä on positiivisia (13).
Isommat lapset voivat antaa keskisuihkunäytteen samaan tapaan kuin aikuiset. Jos lapsi käy potalla, sen etuosaan voidaan asettaa näytteenottokuppi, jolloin saadaan keskisuihkunäytettä vastaava näyte. Keskisuihkunäytteestä saatua positiivista seulontatulosta ei ole välttämätöntä varmistaa toisella näytteellä.
Imeväisillä ja pienillä lapsilla useimmat kansainväliset hoitosuositukset pitävät lentovirtsanäytteen ottoa ensisijaisena vaihtoehtona (12). Virtsanäyte pyritään saamaan siten, että lapsi riisumisen yhteydessä usein virtsaa spontaanisti ja näyte voidaan tästä kerätä suoraan keräysastiaan. Näytteen saamista voidaan nopeuttaa Quick-Wee-menetelmällä, jossa lapsen alavatsan ihoa sivellään kylmään (3-5°C) veteen kostutetuilla nestelapuilla. Näin näyte saadaan 20-30 %:lla imeväisistä muutamassa minuutissa (14).
Jos lentovirtsanäytteen saaminen ei onnistu, voidaan imeväisen virtsanäyte ottaa näytetyynyllä tai -pussilla. Nämä on vaihdettava puolen tunnin välein kontaminaatioiden vähentämiseksi. Tyynyn vaihtaminen on lapselle miellyttävämpää kuin pussin teippien irrottaminen iholta. Pienin kontaminaatioriski on lentovirtsanäytteillä (10-25 %) ja suurin näytetyynyllä tai -pussilla kerätyillä näytteillä (50-60 %) (12,15). Mikäli ensimmäinen seulontanäyte on negatiivinen, ei uutta näytettä tarvitse ottaa.
Jos seulontanäyte on positiivinen, kuumeisen imeväisen virtsatieinfektiodiagnoosin varmistamiseksi suositellaan rakkopistonäytettä (kuvio 1 «»1), jonka kontaminaatioriski on alle 1 % (taulukko 1) (15). Rakkopisto vaatii onnistuakseen kokemusta, joskin kaikuohjaus voi lisätä onnistumisen todennäköisyyttä (16).
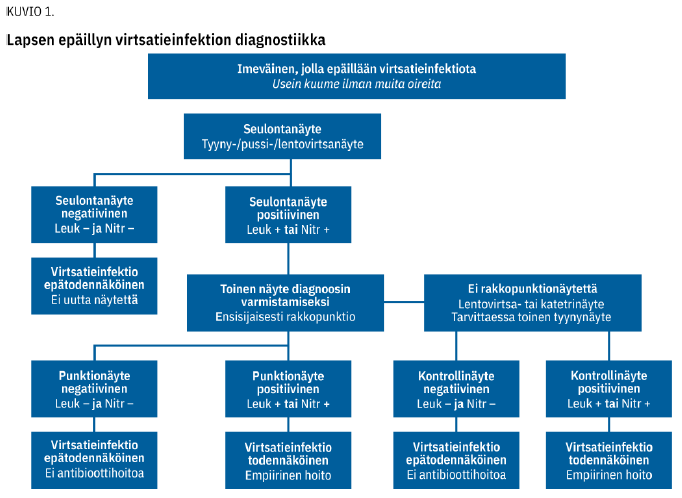
Katetrointi onnistuu yleensä hyvin (12), ja näytteistä noin 10 % kontaminoituu (13). Katetroinnin hyötyä ja haittoja kannattanee kuitenkin pohtia potilaskohtaisesti, koska toimenpide on invasiivinen ja kivulias. Jos rakkopistolla ei saada näytettä ja katetroinnista halutaan pidättäytyä, on suositeltavaa ottaa toinen lentovirtsanäyte tai tyyny- tai pussivirtsanäyte ennen antibioottihoidon aloitusta.
Avoterveydenhuollossa riittää hyväkuntoisilla imeväisillä ja pienillä lapsilla varmistavaksi toiseksi näytteeksi lentovirtsanäyte, tyynynäyte tai keräyspussinäyte. Hyvävointista lasta ei siis yleensä tarvitse lähettää erikoissairaanhoitoon pelkästään rakkopunktiota tai katetrointia varten.
Lapsen virtsanäytteestä pyydetään sekä virtsan seulontatutkimus että viljely. Seulontanäytteen leukosyytit ovat herkkä työkalu virtsatieinfektion todentamiseksi, joten niiden puuttuminen virtsanäytteestä sulkee pois infektion 90-95 %:n todennäköisyydellä (7,17). Nitriittien löytyminen virtsasta on spesifi löydös, mutta lyhyen rakkoajan vuoksi sen herkkyys on huono pienillä lapsilla: alle kaksivuotiaiden virtsatieinfektiopotilaiden näytteistä ainoastaan 23 % on nitriittipositiivisia (19). Mikäli seulontanäytteen leukosyytti- ja nitriittitulokset ovat negatiiviset, virtsatieinfektio on epätodennäköinen, eikä empiirinen hoito ole perusteltua.
Leukosyyttien seulontatesti voi olla virheellisesti negatiivinen, jos aiheuttaja on jokin muu kuin E. coli. Esimerkiksi P. aeruginosa -kantojen suhteen seulontanäytteen leukosyyttien herkkyys on noin 60 % ja enterokokkien 55 % (18). Virtsan kemiallisessa seulassa positiiviset veri, proteiinit ja ketoaineet eivät yleensä johdu virtsatieinfektiosta, eikä niiden perusteella tule tehdä virtsatieinfektiodiagnoosia tai aloittaa antibioottihoitoa.
Diagnoosi varmistuu lopullisesti bakteeriviljelyn perusteella (taulukko 1 «»2). Viljelyn tulkinta riippuu virtsanäytteiden laadusta, lukumäärästä sekä todetusta bakteerikasvusta.
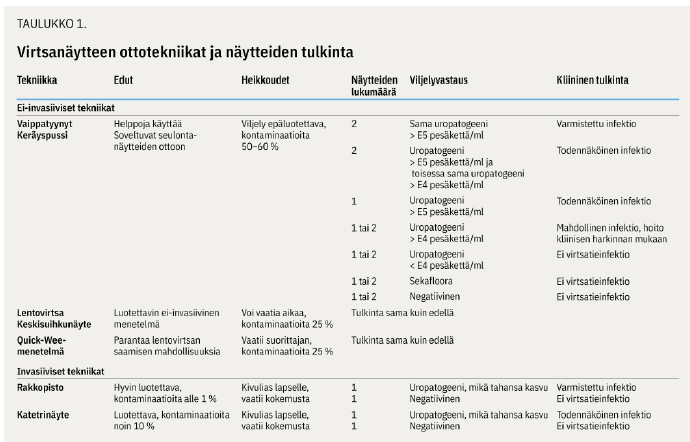
Hoitopäätös tehdään virtsatieinfektioon sopivien oireiden ja positiivisen seulontatutkimuksen perusteella. Kuumeisen virtsatieinfektion hoito kannattaa aloittaa nopeasti. Kahden vuorokauden viive antibioottihoidon aloituksessa lisää kuvantamisella havaittavan munuaiskudosvaurion riskiä noin 50 % (20). Alle kolmen kuukauden ikäinen lapsi lähetetään erikoissairaanhoitoon, mikäli hänellä epäillään kuumeista virtsatieinfektiota, ja hoito aloitetaan suonensisäisellä antibiootilla (taulukko 2).
Vanhempien lasten virtsatieinfektiot voidaan hoitaa avoterveydenhuollossa suun kautta annettavalla antibiootilla, jos yleistila on hyvä ja muut vakavat infektiot on suljettu pois (21). Jos yleistila on heikentynyt, kaikenikäisten lasten ja nuorten hoito aloitetaan suonensisäisellä antibiootilla sairaalassa. Aloitusantibiootin tulee kattaa todennäköisin taudinaiheuttaja E. coli.
Suomen resistenssitilanne huomioiden kefuroksiimi on yleensä hyvä valinta kuumeisen virtsatieinfektion suonensisäiseen hoitoon. Suun kautta annosteltavista lääkkeistä ensisijaisia vaihtoehtoja ovat kefaleksiini ja sulfa-trimetopriimi (22). Nitrofurantoiinilla ei saavuteta merkittäviä kudospitoisuuksia munuaisissa, minkä vuoksi se ei sovellu pyelonefriitin hoidoksi. Asianmukaisella hoidolla kaksi kolmesta lapsesta on kuumeettomia jo yhden vuorokauden hoidon jälkeen ja 90 % kahden vuorokauden hoidon jälkeen (23). Lasten virtsatieinfektiot paranevat yleensä hyvin. Oireettomilta lapsilta ei oteta kontrollinäytteitä hoidon päättymisen jälkeen.
Lapsen kuumeisen virtsatieinfektion hoidon optimaalisesti kestosta ei ole olemassa laadukkaita satunnaistettuja tutkimuksia. Sekä suomalainen Käypä hoito -suositus (22) että Yhdysvaltain lastenlääkäriyhdistys (24) suosittavat kestoksi 7-14 vuorokautta. Havainnoivien tutkimusten perusteella vaikuttaa kuitenkin siltä, että noin viikon kestoinen hoito on yhtä tehokas kuin 10-14 vuorokauden hoito (25-26). Todennäköisesti noin viikon kestoinen hoito onkin riittävä kuumeisessa virtsatieinfektiossa.
Rakkotason infektioiden hoidon kestosta on huomattavasti enemmän tutkimuksia (27). Niiden perusteella kolmen vuorokauden hoito lapsilla on pidemmän hoidon veroinen (28-29). Käypä hoito -suosituksen viiden vuorokauden hoito on siis todennäköisesti mahdollista lyhentää turvallisesti kolmeen vuorokauteen.
Lapsen ensimmäinen virtsatieinfektio voi viitata virtsaelinten rakennepoikkeavuuteen. Suomalaisessa aineistossa virtsatieinfektion sairastaneista lapsista 1,4 % tarvitsi kirurgista hoitoa kaikututkimuksella todetun rakennepoikkeavuuden vuoksi (30).
Tämän hetken tutkimusnäyttö ei tarjoa yksiselitteistä vastausta siihen, missä tilanteissa virtsatieinfektion sairastaneen lapsen virtsaelimet tulisi kuvantaa. Suomessa kaikututkimus tehdään yleensä alle kaksivuotiaan ensimmäisen virtsatieinfektion jälkeen, ensimmäisen pyelonefriitin jälkeen ja poikien virtsatieinfektion jälkeen (22).
Britanniassa suositellaan kaikututkimusta kaikille alle puolivuotiaille lapsille ja yli puolen vuoden iässä ainoastaan toistuvien tai epätyypillisten infektioiden yhteydessä (31). Yhdysvalloissa kaikututkimusta suositellaan alle kaksivuotiaille lapsille ensimmäisen infektion jälkeen ja vanhemmille lapsille toistuvien infektioiden yhteydessä (24).
Miktiokystografiasta osana vesikoureteraalisen takaisinvirtauksen diagnostiikkaa on pitkälti luovuttu, koska siitä ei ole osoitettu olevan merkittävää lisähyötyä pelkkään kaikututkimukseen verrattuna (32). Tutkimus on lisäksi lapselle epämiellyttävä ja aiheuttaa säderasitusta. Vesikoureteraalinen takaisinvirtaus häviää yleensä itsestään lapsen kasvaessa (33).
Virtsatieninfektion uusiutumisen riskiä voi pienentää lääkkeettömillä keinoilla. Harvoin tapahtuvaa virtsaamista voidaan pyrkiä korjaamaan lisäämällä lapsen juomista. Karpalomehun säännöllinen nauttiminen saattaa estää infektioiden uusiutumista (22). Ehkäisyssä tulee huomioida myös virtsarakon ja suolen toiminnalliset tekijät, kuten virtsan päiväaikaisen panttaamisen ja ummetuksen hoito, mutta tutkimusnäyttö näiden hoidon ehkäisevästä vaikutuksesta on toistaiseksi vähäistä (22).
Antibioottiestohoito vähentää infektion uusiutumista noin 30 % (34,35). Estohoitoon liittyy kohonnut antibioottiresistenssin riski (5), joten sen aloitusta tulee harkita huolellisesti. Ensimmäisen infektion jälkeen estolääkitystä ei yleensä kannata aloittaa, mikäli virtsaelinten kuvantamislöydös on normaali.
Estohoidosta kannattaa konsultoida lastentautien erikoissairaanhoitoa, jos aloitusta suunnitellaan pienelle lapselle. Toistuvista kystiiteistä eli virtsarakkotulehduksista kärsivien isompien lasten estohoidon voi aloittaa avoterveydenhuollossa kuuden kuukauden ajaksi, mikäli rakkotasoiset infektiot ovat olleet oireisia ja varmennettuja, niitä on ollut vähintään kolme puolen vuoden aikana ja lapsella on ollut normaali löydös kaikututkimuksessa (22). Estohoitona voidaan käyttää nitrofurantoiinia (annoksella 1 mg/kg/vrk) tai sulfa-trimetopriimia (annoksella 2 mg trimetopriimia/kg/vrk) kerran vuorokaudessa.
Lapsuusiän virtsatieinfektiot on yhdistetty kuvantamistutkimuksissa munuaisten arpeutumismuutoksiin (19). Merkittävät pitkäaikaishaitat ovat kuitenkin hyvin harvinaisia, mikäli ensimmäisen infektion yhteydessä tehdyssä kaikututkimuksessa ei todeta rakenteellista poikkeavuutta (36).
Suomalaisen seurantatutkimuksen perusteella 15 %:lla lapsuudessa virtsatieinfektion sairastaneista potilaista on kaikututkimuksella todettavia munuaisparenkyymin muutoksia, mutta munuaisten toiminnassa tai verenpaineessa ei havaittu poikkeavuuksia (32). Raskaus voisi tuoda esille munuaisten toimintahäiriöitä, jotka eivät ilmenisi ilman raskautta. Lapsuusiässä sairastetulla virtsatieinfektiolla ei kuitenkaan ole yhteyttä myöhempiin raskaudenaikaisiin komplikaatioihin, kuten raskaushypertensioon tai pre-eklampsiaan (37).