
Ks. artikkelin pdf-versio «http://www.fimnet.fi/cl/laakarilehti/pdf/2023/SLL42-2023-1679.pdf»1 Lääkärilehden sivuilla (vaatii FiMnet-tunnuksen).
Suonipoikkeavuuksilla tarkoitetaan veri- tai imusuonten poikkeavaa kasvua tai kehitystä. Kansainvälinen suonipoikkeavuuksien tutkimusyhdistys (ISSVA) luokittelee ne kahteen pääryhmään: proliferatiivisiin suonikasvaimiin ja suonten paikallisista kehityshäiriöistä johtuviin suoniepämuodostumiin. Pääryhmät jaetaan edelleen alaryhmiin kliinisten löydösten, kuvantamisen ja tarvittaessa histologisten ja geneettisten löydösten perusteella (taulukko 1 «»1).

Suonipoikkeavuudet on tärkeä erottaa toisistaan erilaisten hoitolinjojen takia. Sekä suonikasvaimiin että suoniepämuodostumiin liittyy harvinaisia oireyhtymiä. (1).
Diagnosointi voi olla haastavaa, koska löydökset voivat olla osittain samankaltaisia ja niiden nimeäminen on ollut pitkään epäjohdonmukaista. Useita erilaisia suonipoikkeavuuksia nimetään edelleen usein virheellisesti hemangioomiksi (2,3).
Suonipoikkeavuuksien diagnostiikka ja hoito on moniammatillista. Jokaisessa yliopistosairaalassa on työryhmä, johon kuuluu tavallisesti lastenhematologi, lastenkirurgi, plastiikkakirurgi, radiologi, suonianomalioihin perehtynyt patologi, ihotautilääkäri sekä tarpeen mukaan muitakin erikoisaloja.
Tämän katsauksen tavoitteena on tarjota yleislääkärille ja lastenlääkärille tietoa lasten suonipoikkeavuuksista.
Infantiili hemangiooma (IH) eli mansikkaluomi on lasten tavallisin hyvänlaatuinen kasvain. Niitä esiintyy noin 5 %:lla lapsista, pienipainoisista keskosista jopa 25 %:lla.
Suurin osa infantiileista hemangioomista ei vaadi hoitoa, ja niitä voidaan seurata neuvolakäyntien yhteydessä. On kuitenkin tärkeä tunnistaa ne, jotka vaativat lisätutkimuksia ja hoitoa (kuva 1 «»2). Paras hoitovaste saadaan, kun hoito aloitetaan varhain (4-8).
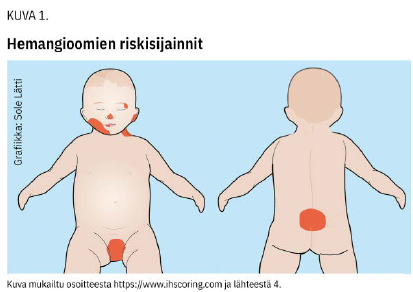
Infantiili hemangiooma voi näkyä jo vastasyntyneellä, mutta yleensä se ilmaantuu 1-4 viikon iässä (kuva 2 «»3). Nopein kasvun vaihe kestää 3-4 kuukautta, ja sen jälkeen hidasta kasvua voi tapahtua vuoden ikään asti, pään ja kasvojen alueella jopa 2-3 vuotta. Sen jälkeen hemangiooma useimmiten surkastuu 5 vuoden ikään mennessä. Paikalle voi jäädä rasva- ja sidekudoksesta koostuva arpi (4-8).
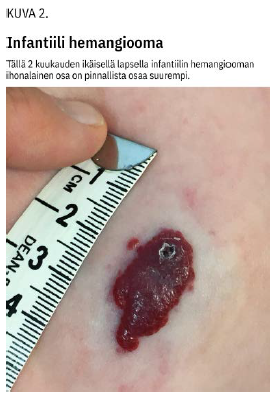
Lähete lasten hemangioomien hoidosta alueella vastaavaan erikoissairaanhoidon yksikköön tulisi tehdä jo lapsen ollessa kuukauden ikäinen, jotta hoito voidaan aloittaa infantiilin hemangiooman nopeimman kasvun aikana. Lähetteen aiheet on esitetty taulukossa (taulukko 2 «»4). Lähetteeseen on hyvä liittää valokuva (4-8).

Laajat segmentaaliset hemangioomat voivat esiintyä osana harvinaisia oireyhtymiä. Yli 5 cm halkaisijaltaan oleva segmentaalinen infantiili hemangiooma pään, ylävartalon, tai olkavarren alueella herättää epäilyn PHACE-oireyhtymästä (posterior fossa malformations, haemangioma, arterial anomalies, coarctation of the aorta, cardiac defects and eye anomalies), johon liittyy aivojen, aivo- ja kaulavaltimoiden, aortankaaren, sydämen ja silmien rakennepoikkeavuuksia. Yli 2,5 cm halkaisijaltaan oleva keskiviivan ylittävä lumbosakraalinen tai perineaalinen IH herättää puolestaan epäilyn LUMBAR-oireyhtymästä, johon liittyy luuston, selkäytimen, valtimoiden urogenitaali- ja anorektaalielinten rakennepoikkeavuuksia sekä hemangiooman haavautumista (9,10).
Hemangiooman diagnoosi voidaan yleensä tehdä kliinisin perustein. Kaikukuvausta suositellaan vain, jos diagnoosi on epäselvä. Mikäli hemangioomia on 5 tai useampia, tehdään kaikututkimus maksan hemangioomien poissulkemiseksi (4). PHACE-oireyhtymää epäiltäessä suositellaan aivojen, aivo- ja kaulaverisuonten, kaulan ja mediastinumin magneettikuvausta (4). Lumbosakraalisten ja perineaalisten segmentaalisten hemangioomien yhteydessä suositellaan vatsan ja lantion alueen magneettikuvausta (4).
Parta-alueen hemangioomissa suositellaan nasofiberoskopiaa hengitysteiden hemangioomien poissulkemiseksi. Periorbitaalisissa hemangioomissa silmälääkäri arvioi mahdollista vaikutusta näön kehitykseen.
Koepala on diagnostiikassa harvoin tarpeen, mutta erotusdiagnostiikassa tulee huomioida muut hyvänlaatuiset suonikasvaimet, suoniepämuodostumat sekä muut kasvaimet.
Infantiilista hemangioomasta poiketen synnynnäiset hemangioomat ovat täydessä koossaan jo vastasyntyneellä (kuva 3 «»5). Ne luokitellaan kolmeen alatyyppiin surkastumistaipumuksen mukaan (taulukko 1 «»1).
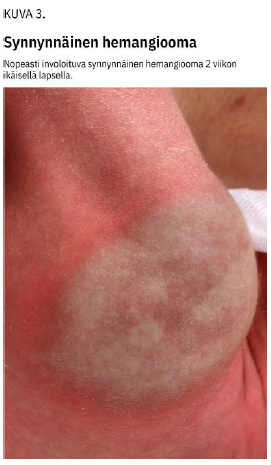
Pyogeeninen granulooma sekoitetaan usein infantiiliin hemangioomaan. Se on lasten tavallisin hankinnainen suonikasvain ja ilmaantuu iholle tyypillisesti pienen trauman, kuten hyönteisenpiston jälkeen. Pyogeeninen granulooma on tavallisesti kooltaan 1-10 mm ja vuotaa herkästi. Se hoidetaan kirurgisesti tai hiilidioksidilaserilla.
Tufted angiooma ja kaposiforminen hemangioendoteliooma ovat harvinaisia imeväisillä ilmeneviä suonikasvaimia, joiden diagnoosiin päästään yleensä vasta koepalan avulla (5,6). Niihin voi liittyä Kasabach-Merritin ilmiöksi kutsuttu vakava hyytymisjärjestelmän häiriö (11).
Propranololi on vakiinnuttanut paikkansa infantiilin hemangiooman ensilinjan hoitona silloin, kun hoitoa tarvitaan (4,6,12-14). Hoitoarviosta sekä lääkehoidosta vastaa hemangioomien hoitoon perehtynyt lääkäri paikallisesti sovitun hoitoketjun mukaisesti (4). Propranololihoitoa käsitellään tarkemmin Aikakauskirja Duodecimissa vuonna 2012 julkaistussa kirjoituksessa, eivätkä siinä esitetyt periaatteet ole muuttuneet (12).
Haavautuneeseen hemangioomaan ja PHACE-oireyhtymään suositellaan tavallista pienempää, esimerkiksi puolta annosta. Pienille imeväisille hoito aloitetaan sairaalassa, samoin jos taustalla on jokin sydän- tai verenkiertoelimistön sairaus, hengityselimistön sairaus tai suurentunut hypoglykemian riski.
Hoitovaste nähdään yleensä nopeasti. Hoidon kesto on vähintään 6 kuukautta, kasvojen alueen ja syvien hemangioomien hoitoa jatketaan pidempään (4,6). Haittavaikutukset ovat melko vähäisiä, mutta verenpaineen lasku, hypoglykemia, bradykardia, vatsaoireet ja hengitystieoireet ovat mahdollisia ja unihäiriöitä sekä raajojen kylmyyttä voi esiintyä.
Propranololi suositellaan ottamaan aterian yhteydessä. Hypoglykemiariskin takia lääke suositellaan tauottamaan gastroenteriitin tai muun syömistä heikentävän infektion sekä obstruktiivisen hengitystieinfektion yhteydessä. Unihäiriöistä kärsiville suositellaan lääkkeen ottamista kahtena annoksena niin, että ilta-annos on jo klo 17 (4,6).
Muista beetasalpaajista mm. atenololia on tutkittu infantiilin hemangiooman hoidossa. Propranolin käyttöä puoltavat kuitenkin laaja käyttökokemus ja tutkimusnäyttö turvallisuudesta (4,6,7,15-19). Paikallisesti käytettävät beetasalpaajavoiteet eivät ole saavuttaneet vakiintunutta käyttöä. Synnynnäiseen hemangioomaan beetasalpaajahoito ei tehoa (5).
Mikäli beetasalpaajalla ei saada aikaan riittävää vastetta, harkitaan muita hoitovaihtoehtoja. Haavautuneisiin hemangioomiin (kuva 4 «»6) käytetään pulssivärilaserhoitoa. Kirurgiaa harkitaan tapauskohtaisesti. Suun kautta tai paikallisina pistoksina annettujen kortikosteroidien teho on vaatimattomampi kuin propranololin ja haittavaikutukset hankalampia (4,6,14).
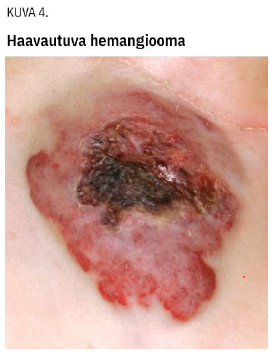
Infantiilin hemangiooman jälkitilan hoidon tarvetta arvioidaan lapsen ollessa noin 5 vuoden iässä. Hoitovaihtoehtoja ovat pulssivärilaser ja kirurgia.
Suoniepämuodostumat ovat veri- tai imusuonten paikallisia kehityshäiriöitä, joista valtaosa aiheutuu sikiöaikaisesta somaattisesta mutaatiosta. Ne ovat synnynnäisiä mutta tulevat usein esille vasta myöhemmin lapsuudessa tai nuoruudessa.
Suoniepämuodostumat voivat olla pinnallisia päälle päin näkyviä tai sijaita syvemmissä kudoksissa, kuten lihaksissa, luustossa tai sisäelimissä. Ne luokitellaan virtausolosuhteiden ja pääasiallisen suonityypin mukaan (taulukko 1 «»1). Hoidon aiheita ovat oireet sekä toisinaan toiminnallinen tai kosmeettinen haitta.
Hiussuoniepämuodostuma (tuliluomi, portviiniläiskä) on tarkkarajainen tai verkkomainen ihomuutos, jonka väri vaihtelee vaaleanpunaisesta violettiin ja koko pienistä yksittäisistä läiskistä laajoja ihoalueita kattaviin karttamaisiin muutosalueisiin. Nevus simplex (haikaranpurema) luokitellaan hiussuoniepämuodostumaksi, mutta on kiistanalaista, onko tämä usein iän myötä pois haalistuva muutos todellinen epämuodostuma (8,20-22).
Imutie-epämuodostumat muodostuvat rakkulamaisesti laajentuneista imusuonista. Ne sijaitsevat tavallisimmin pään, kaulan tai kainaloiden alueella. Palpaatiolöydöksenä on pehmeä, kasaan painumaton massa, ja iholla voi olla sinerrystä tai rakkuloita. Epämuodostuma voi muuttua kivuliaaksi esimerkiksi spontaanin vuodon tai infektoitumisen seurauksena.
Laskimoepämuodostuma on pinnallisena sinertävä pullistuma, joka on palpoiden pehmeä ja kasaan painuva. Tyypillisiä sille ovat asentoon ja rasitukseen liittyvät koon ja oireiden muutokset. Multippelit muutokset viittaavat periytyvään muotoon. Laskimoepämuodostumiin voi liittyä hyytymisjärjestelmän poikkeavuuksia.
Nopeavirtauksisissa valtimo-laskimoepämuodostumissa hiussuoniverkosto on korvautunut poikkeavilla yhteyksillä valtimoista laskimoihin. Niihin liittyy merkittävää sairastuvuutta, joten varhaisen diagnoosin ja keskitetyn hoidon merkitys on suuri (8,20).
Sekä hidas- että nopeavirtauksiset suoniepämuodostumat voivat liittyä erilaisiin oireyhtymiin. Oireyhtymää on aihetta epäillä, mikäli suonipoikkeavuuksia on useita, sukuhistoria viittaa perinnöllisyyden mahdollisuuteen tai lapsella todetaan suonipoikkeavuuden lisäksi raajojen eriparisuus, poikkeava kasvu, poikkeavat kasvonpiirteet tai muita anomalioita (22-24).
Suoniepämuodostumien haastavaan diagnostiikkaan tarvitaan moniammatillinen työryhmä. Husin suonianomaliatyöryhmän arvioon tulleiden lasten infantiili hemangiooma oli diagnosoitu oikein 89 %:ssa tapauksista, mutta suoniepämuodostuma vain 38 %:ssa. Suonipoikkeavuusepäilyn vuoksi arvioon tulleista lapsista 9 %:lla diagnoosi oli muu kuin suonipoikkeavuus (2).
Myös suoniepämuodostumien oikeaan diagnoosiin päästään usein hyvän kliinisen tutkimuksen ja kaikukuvauksen avulla (2,7,8,20). Periorbitaalisissa hiussuoniepämuodostumissa tarvitaan silmälääkärin arvio. Kasvojen alueen segmentaalisia hiussuoniepämuodostumia lukuun ottamatta leikekuvantamista tarvitaan usein vasta hoidon suunnittelussa.
Magneettikuvauksella pystytään kartoittamaan muutoksen tarkka anatominen sijainti, koko ja suhde ympärillä oleviin muihin rakenteisiin (25). Se tehdään yliopistosairaalassa tai erikseen sovitusti keskussairaalassa, jolloin yhdellä hyvin suunnitellulla kuvauskerralla vältetään toistuva anestesian ja varjoaineen käyttö.
Diagnostiset haasteet ja epämuodostuman taustalla olevan mahdollisen geenimuutoksen selvittäminen ovat aiheita biopsiaan. Geenilöydöksellä voi myös olla vaikutusta hoidon valintaan.
Suoniepämuodostumien hoito vaihtelee harvakseltaan tapahtuvasta seurannasta moniammatillisen työryhmän arviota vaativaan yhdistelmähoitoon ja tiiviiseen seurantaan (20-24,27). Hoitona voidaan käyttää skleroterapiaa, kirurgista hoitoa, lääkehoitoja, embolisaatiota tai näiden yhdistelmiä. Lisäksi monet hyötyvät painetekstiileistä ja fysio-, lymfa- tai toimintaterapiasta. Myös kivun hoito on tärkeää.
Suoniepämuodostumien taustalla on usein epätarkoituksenmukainen aktivaatio keskeisessä solunsisäisessä signalointijärjestelmässä, PIK3/AKT/mTOR-järjestelmässä. Ensisijaisena lääkehoitona hankalia oireita aiheuttavissa suoniepämuodostumissa käytetäänkin mTOR:n estäjä sirolimuusia (23,26). PIK3CA-geenin estäjä alpelisibi on tutkimuskäytössä PIK3CA-mutaatioon liittyvissä liikakasvuoireyhtymissä ja suoniepämuodostumassa (27).
Suonipoikkeavuuden oikea diagnoosi on keskeinen, jotta hoito voidaan suunnata oikein. Komplisoituneiden tai oireyhtymiin liittyvien suonipoikkeavuuksien diagnostiikka ja seurannan koordinointi on suositeltavaa keskittää yliopistosairaaloihin.
Hus-alueella toimii säännöllisesti kokoontuva moniammatillinen työryhmä (Vam-ryhmä), jota voidaan konsultoida potilaiden diagnostiikan, eri hoitomuotojen (kirurginen hoito, toimenpideradiologian tarve, lääkehoidot) ja seurannan kysymyksissä myös muiden yliopistosairaaloiden alueelta ja tarvittaessa lähettää potilas työryhmän arvioon. Työryhmä tekee tiivistä yhteistyötä kansainvälisesti (Vascern-keskus vuodesta 2017 alkaen).