
Ks. artikkelin pdf-versio «http://www.fimnet.fi/cl/laakarilehti/pdf/2025/SLL6-2025-445.pdf»1 Lääkärilehden sivuilla (vaatii FiMnet-tunnuksen).
Rakenteelliset sydänviat ovat vastasyntyneiden yleisimpiä rakennepoikkeamia. Sydämen rakenteiden kehitys on monivaiheinen tapahtumasarja, joka alkaa varhain alkiovaiheessa ja jatkuu ensimmäisen raskauskolmanneksen ajan.
Synnynnäinen sydämen rakennepoikkeavuus todetaan noin 1 %:lla vastasyntyneistä (1,2). Näin ollen Suomessa syntyy vuosittain noin 400-450 lasta, joilla poikkeavuus diagnosoidaan.
Rakenteellisten sydänvikojen etiologia on monitekijäinen. Noin 20 % synnynnäisistä sydänvioista liittyy kromosomipoikkeavuuksiin tai perinnöllisiin oireyhtymiin (3). Noin 80 %:ssa tapauksista taustalta ei voida osoittaa yhtä selvää altistavaa tekijää.
Ympäristötekijöistä sydämen rakenne-poikkeavuuden riskiä lisäävät esimerkiksi äidin poikkeava sokeritasapaino tai lihavuus, tietyt varhaisraskaudessa sairastetut infektiot sekä altistuminen eräille lääkeaineille (4-8). Perintötekijöistä vanhempien, etenkin äidin, synnynnäinen sydänvika lisää riskiä vian tyypin mukaan (5,9).
Synnynnäisen sydänvian merkitys vastasyntyneelle riippuu vian tyypistä. Kriittisessä rakenteellisessa viassa keuhko- tai systeemiverenkierto on riippuvainen sikiöaikaisesta avoimesta valtimotiehyestä (duktus arteriosus). Tiehyen sulkeutuessa vastasyntyneen verenkierto romahtaa. Suomessa noin 50 lapsella diagnosoidaan vuosittain kriittinen vika, joka tarvitsee toimenpiteen pian syntymän jälkeen.
Muut merkittävät sydänviat aiheuttavat oireita tyypillisesti myöhemmin vastasyntyneisyyskaudella tai sen jälkeen kun lapsen verenkierto on sopeutunut kohdunulkoiseen elämään (kuvio 1 «»1).
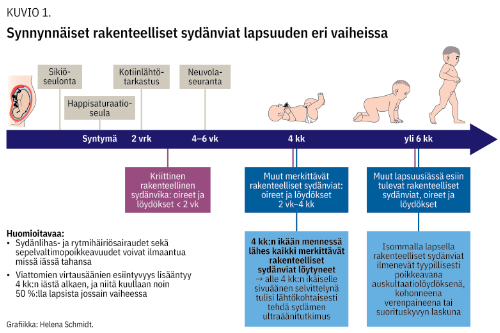
Tämä katsaus käsittelee rakenteellisia synnynnäisiä sydänsairauksia ja niiden seulontaa. Muut sydänsairaudet, kuten sydänlihaksen sairaudet ja rytmihäiriöt, on rajattu ulkopuolelle.
Oireet ja kliiniset löydökset voivat olla hyvin vähäiset tai puuttua kokonaan välittömästi syntymän jälkeen, vaikka sydämen rakennepoikkeavuus olisi merkittävä.
Synnynnäisten sydänvikojen seulonnan tarkoitus on löytää merkittävät viat mahdollisimman varhain ennen synnytyssairaalasta kotiutumista, ennen kuin lapsen vointi romahtaa. Sydämen rakennevikoja seulotaan osana sikiöaikaista rakenneseulaa, syntymän jälkeen synnytyssairaalassa happisaturaatiomittauksella ja kliinisellä kotiinlähtötarkastuksella sekä 4-6 viikon iässä neuvolalääkärin tarkastuksella.
Rakenneultraäänitutkimus tehdään raskausviikolla 18-21 tai perheen toiveesta viikon 24 jälkeen. Tavoitteena on löytää ne rakenteelliset sydänviat, jotka ovat riippuvaisia valtimotiehyen aukiolosta tai tarvitsevat hoidon heti syntymän jälkeen, kuten valtasuonten transpositio.
Sikiödiagnostiikka mahdollistaa vastasyntyneen hoitopolun optimoinnin ja perheen sopeutumisen lapsen sydänsairauteen. Perhe voi myös harkita raskauden keskeytystä, jos sydänvika on vaikea. Sikiödiagnostiikkaan perehtyneen gynekologin tai sikiökardiologin arviota tarvitaan, jos seulonnassa epäillään merkittävää rakennepoikkeavuutta tai sellaiselle altistavaa muuta poikkeavuutta.
Happisaturaatioseulan tekee kätilö sikiön ollessa kahden tunnin ikäinen. Saturaatio mitataan pulssioksimetrillä samanaikaisesti oikeasta yläraajasta ja jommastakummasta alaraajasta.
Tarkoituksena on löytää avoimesta valtimotiehyestä riippuvaiset kriittiset synnynnäiset sydänviat arvioimalla happeutumista kokonaisuudessaan sekä vertaamalla preduktaalista (oikea yläraaja) ja postduktaalista (alaraaja) happeutumista. Seulontatulos tulkitaan normaaliksi, jos saturaatio on molemmissa raajoissa yli 95 % ja raajojen välillä on enintään kolmen prosenttiyksikön ero (10).
Happisaturaation mittaaminen on yksinkertainen, toimiva ja kustannustehokas keino seuloa synnynnäisiä sydänvikoja (11-15). Se on hyvin spesifinen ja kohtalaisen sensitiivinen menetelmä vikojen havaitsemiseen ja nopeuttaa niiden diagnostiikkaa (12,13,15). Saturaatioseulonnassa löytyy myös muita vastasyntyneen voinnin kannalta merkittäviä tiloja, kuten vastasyntyneen sepsis ja pulmonaalihypertensio (12-15).
Poikkeava saturaatiolöydös ilman ilmeistä selittävää syytä on aihe sydämen ultraääniutkimukselle.
Kotiinlähtötarkastus tehdään kaikille vastasyntyneille ennen sairaalasta kotiutumista, tyypillisesti 1-2 vuorokauden iässä. Kliininen tutkimus toistetaan 4-6 viikon iässä ensimmäisessä lääkärineuvolassa. Oleellisinta on sydämen huolellinen auskultaatio sekä rintakehästä että selästä ja reisivaltimopulssien palpaatio.
Yli 2 vuorokauden iässä kotiinlähtötarkastuksessa tai ensimmäisessä lääkärineuvolassa kuultu sivuääni on lähtökohtaisesti aihe sydämen ultraäänitutkimukselle. Tutkimuksen kiireellisyys arvioidaan lapsen yleisvoinnin perusteella. Vastasyntyneistä, joilla kuullaan sivuääni kotiinlähtötarkastuksessa, noin 7 %:lla todetaan ultraäänitutkimuksessa seurantaa vaativa rakennepoikkeavuus ja noin 2 %:lla kriittinen sydänvika (16).
Reisivaltimopulssit voivat olla heikentyneet tai puuttua aortan koarktaatiossa. Mikäli pulssit palpoituvat poikkeavina, on syytä tarkastaa neliraajaverenpaineet erikoissairaanhoidossa. Jos luotettavissa verenpainemittauksissa todetaan yli 10 mmHg korkeampi systolinen verenpaine ylä- kuin alaraajassa, on se aihe sydämen ultraäänitutkimukselle.
Joihinkin oireyhtymiin, kuten Downin oireyhtymään, voi liittyä rakenteellisia sydänvikoja tai muita merkittäviä rakennepoikkeavuuksia. Jos sellaista epäillään vastasyntyneellä, on sydämen rakenteet syytä tarkastaa ultraäänitutkimuksella.
Seulonnan ansiosta noin 90 % merkittävistä rakenteellisista sydänvioista diagnosoidaan ennen vastasyntyneen kotiutumista synnytyssairaalasta (17,18).
Sydänvikojen sikiöaikainen diagnostiikka on kohentunut vuosien saatossa (19). Tällä hetkellä Suomessa kriittisistä ja muista merkittävistä poikkeavuuksista yli 60 % diagnosoidaan sikiöseulonnassa. Käytännössä raskauden aikana diagnosoidaan kaikki rakenteelliset sydänviat, jotka johtavat jommankumman kammion vajaakehittymiseen, ja noin 80 % valtasuonten transpositioista (suullinen tiedonanto dosentti Olli Pitkänen-Argillanderilta).
Vastasyntyneen happisaturaatioseulonta ja kliininen tutkimus kotiinlähtötarkastuksessa täydentävät toisiaan. Yhdessä ne löytävät suurimman osan sikiöaikana diagnosoimattomista merkittävistä poikkeavuuksista (14,17,18).
Saturaatioseulonnan merkitys diagnostiikassa riippuu muun muassa sikiöaikaisen seulonnan tarkkuudesta (17,18,20). Viimeaikaisissa tutkimuksissa maista, joissa on samankaltainen seulontajärjestelmä kuin Suomessa, sen suhteellinen osuus diagnostiikassa on vaihdellut alle 10 %:sta yli 20 %:iin (17,18). Herkimmin seulan avulla löydetään keuhkoverenkiertoa rajoittavat ja siten pienen happisaturaation aiheuttavat syanoottiset synnynnäiset sydänviat, kuten kriittinen keuhkovaltimoläpän ahtauma.
Noin 15 % merkittävistä synnynnäisistä sydänvioista diagnosoidaan kotiinlähtötarkastuksessa. Lisäksi osa diagnosoidaan lapsen oireyhtymän tai muun rakennepoikkeavuuden selvittelyn yhteydessä tai muiden poikkeavien löydösten vuoksi (17,18).
Seulonnasta huolimatta noin 10 % vastasyntyneistä, joilla on merkittävä rakenteellinen sydänvika, kotiutuu synnytyssairaalasta ilman diagnoosia (17,18). Suomessa tämä tarkoittaa noin 10-15:tä lasta vuosittain. Osa vioista aiheuttaa kliinisiä löydöksiä ja oireita vasta kotiutumisen jälkeen.
Neuvolajärjestelmä toimii hyvin seulonnan viimeisenä tarkastajana. Synnynnäiseen sydänvikaan viittaavissa oireissa ja löydöksissä onkin syytä olla tarkkana, kun arvioidaan alle 4 kuukauden ikäisiä lapsia (taulukko 1 «»2). Viimeisten vuosien aikana sydänvikaisia lapsia ei ole menehtynyt seulontajärjestelmän pettämisen vuoksi.

Erityinen haaste seulontajärjestelmälle ovat vasemman kammion ulosvirtausta ja siten systeemiverenkiertoa rajoittavat viat, kuten aorttaläpän ahtauma ja aortan koarktaatio. Nämä viat eivät rajoita keuhkoverenkiertoa ja aiheuta merkittävää syanoosia, mutta systeemiverenkierto voi olla täysin riippuvainen valtimotiehyen aukiolosta.
Yleisin seulonnassa diagnosoimatta jäävä kriittinen vika on aortan koarktaatio. Näistä lapsista noin kolmasosa kotiutuu synnytyssairaalasta ilman diagnoosia (17,18).
Keuhkoverenkierron vastus pienenee ensimmäisen 1-2 elinkuukauden aikana. Kun keuhkoverenpaine laskee, keuhko- ja systeemiverenkierron ja siten kammioiden välille muodostuu paine-ero. Merkittävässä oikovirtausviassa (esim. kammioväliseinäaukko, avoimeksi jäänyt valtimotiehyt) sydämen sivuääni ja oikovirtauksen koosta riippuvat sydämen vajaatoiminnan oireet ilmenevät vasta paine-eron muodostuessa eli kun lapsi on yli kuukauden ikäinen.
Kaikkia rakenteellisia sydänvikoja ei ole mahdollista löytää vastasyntyneiltä. Esimerkiksi toiseksi yleisin synnynnäinen rakenteellinen sydänvika, eteisväliseinäaukko, aiheuttaa auskultaatiolöydöksen (pysyvästi jakautunut toinen sydänääni ja pulmonaalialueen virtausääni) ja oireet vasta myöhemmin lapsuudessa tai aikuisiällä. Lisäksi ei-kriittinen aortan koarktaatio, joka ei ole riippuvainen valtimotiehyen aukiolosta, voi löytyä vastasyntyneisyyskauden jälkeen esimerkiksi kohonneen verenpaineen selvittelyssä.
On hyvä muistaa, että lapsilla voi esiintyä myös sydänlihas- ja rytmihäiriösairauksia, sydänlihastulehduksia ja hyvin harvoin sepelvaltimoiden rakennepoikkeavuuksia. Näihin liittyvät oireet ja löydökset voivat ilmetä missä iässä tahansa.
Vastasyntyneen rakenteellisten sydänvikojen seulonta alkaa jo sikiöaikana ja toimii Suomessa kokonaisuutena varsin hyvin. Seulonta parantaa vikojen hoitoa ja ennustetta.
Seulonnasta huolimatta noin 10 % sydänvikaisista lapsista kotiutuu synnytyssairaalasta ilman diagnoosia. Neuvolajärjestelmällä on keskeinen rooli viimeisenä tarkastajana.
Etenkin aortan koarktaation mahdollisuus on syytä pitää mielessä, kun arvioidaan kriittisesti sairasta imeväistä. Alle 4 kuukauden ikäisen sivuääni on peruste konsultoida sydänsairauksiin perehtynyttä lastenlääkäriä tai lastenkardiologia.
Toisaalta 4 kuukauden ikään mennessä suurin osa lasten merkittävistä sydämen rakennepoikkeavuuksista on diagnosoitu. Tämä on tärkeää huomioida arvioitaessa yli 4 kuukauden ikäisen sivuääntä, sillä yli 50 %:lla lapsista kuuluu jossain vaiheessa hyvänlaatuinen virtausääni. Tällöin lapsella ei ole sydänvikaan viittaavia löydöksiä eikä sydämen rakenteita tarvitse tarkastaa. Kiitämme yleislääkäri, LT Anniina Jääskeläistä arvokkaista kommenteista käsikirjoitukseen liittyen.