Mikrobilääkkeet hammasperäisten infektioiden hoidossa ja komplikaatioiden ehkäisyssä
Miten viitata Käypä hoito -suositukseen? «K1»1
Keskeinen sanoma
- Hammashoidossa mikrobilääkkeitä voidaan käyttää profylaktisesti estämään toimenpiteestä tai toimenpidealueen infektiosta mahdollisesti seuraavia paikallisia tai systeemisiä infektiokomplikaatioita sekä äkillisissä infektioissa hammaslääketieteellisen hoidon tukena.
- Valtaosa äkillisistä suun ja leukojen alueen infektioista on hammasperäisiä suun normaalimikrobistoon kuuluvien aerobisten ja anaerobisten bakteerien aiheuttamia sekainfektioita.
- Huolellinen päivittäinen omahoito ja säännöllinen hammashoito ovat tärkeimmät tekijät hammasperäisten infektioiden ehkäisyssä.
- Useimmat potilaat eivät tarvitse mikrobilääkeprofylaksia hammashoidon yhteydessä. Mikrobilääkeprofylaksia ei tarvita toimenpiteissä, joissa komplikaatioiden ilmaantuvuus on pieni, kuten limakalvobiopsiassa tai terveen potilaan infektoitumattoman hampaan poistossa.
- Mikrobilääkeprofylaksi on aiheellinen pääasiassa ennen infektoituneen alueen kirurgisia toimenpiteitä. Se annetaan kerta-annoksena 30–90 minuuttia ennen toimenpidettä.
- Profylaksissa käytetään ensisijaisesti amoksisilliinia. Penisilliinille allergisten potilaiden (ei anafylaksia) profylaksissa käytetään ensisijaisesti kefaleksiinia ja anafylaktisen reaktion saaneiden profylaksissa klindamysiiniä.
- Hammasperäisten infektioiden hoidossa infektiopesäkkeen hoito on ensisijaista. Mikrobilääkitystä ei pidä käyttää infektiopesäkkeen hoidon vaihtoehtona. Infektion syyn hoidon viivästyminen tai puutteellinen hoito voi johtaa infektion leviämiseen ja kehittymiseen henkeä uhkaavaksi.
- Epäiltäessä hammasperäistä infektiota, tulee potilas ohjata viipymättä hammashoitoon.
- Mikrobilääkehoitoa hammaslääketieteellisen hoidon lisänä käytettäessä potilaan seurannan tulee olla yhtä tiivistä ja huolellista kuin ilman mikrobilääkkeitä annettavan hoidon yhteydessä. Jos infektiofokus on saatu eliminoiduksi, infektion hoidossa riittää yleensä 3–5 vuorokauden mikrobilääkehoito. Jos oireet eivät selvästi lievity 3 vuorokauden kuluessa tai pahenevat, on uusi arvio pikaisesti tarpeen.
- Hammasperäisten infektioiden hoidossa ensisijaisesti käytettäviä lääkkeitä ovat penisilliini tai amoksisilliini tarvittaessa yhdessä metronidatsolin kanssa. Penisilliinille allergisten (ei anafylaksia) hoidossa käytetään kefaleksiinia penisilliinin sijasta. Anafylaktisen reaktion penisilliinistä saaneiden hoidossa voidaan käyttää klindamysiiniä.
- Mikrobilääkevalinnassa huomioidaan infektion vakavuus, potilaan infektioalttius ja mikrobilääkkeiden viimeaikainen käyttö.
Tiivistelmä ja potilasversio
- Suosituksen tiivistelmä «Mikrobilääkkeet hammasperäisten infektioiden hoidossa ja komplikaatioiden ehkäisyssä»1
- Suosituksen yleiskielinen potilasversio suomeksi «Mikrobilääkkeet hammasperäisten infektioiden hoidossa ja komplikaatioiden ehkäisyssä»2 ja ruotsiksi (päivitettävänä)
Aiheen rajaus
- Suositus käsittelee mikrobilääkeprofylaksin käyttöä hammashoidossa ja mikrobilääkehoitoa äkillisten hammasperäisten infektioiden hoidon yhteydessä perusterveydenhuollossa.
- Suositus ei kata hammasperäisen infektion hoidossa tehtäviä hammaslääketieteellisiä toimenpiteitä, jotka ovat lähes aina hoitona ensisijaisia.
- Suosituksessa käsitellään paikallisantisepteista ainoastaan klooriheksidiinin käyttöä.
- Suosituksessa ei käsitellä mikrobilääkkeiden paikallista käyttöä suun infektioiden hoidossa.
- Suositus ei kata suun limakalvoinfektoiden ehkäisyä tai hoitoa, sylkirauhasinfektioita eikä suun ja leukojen alueen kroonisten infektioiden tai leukamurtumien tutkimus- ja hoitolinjoja.
- Bakteeriendokardiitin mikrobilääkeprofylaksia koskevat suositukset noudattavat European Society of Cardiologyn (ESC) vuonna 2023 julkaisemaa suositusta «2023 ESC Guidelines for the management of endocard...»1.
- Suositus ei kata hammasperäisten etäinfektioiden hoitoa.
Tavoitteet
- Suosituksen tavoitteina on
- päivittää tiedot mikrobilääkeprofylaksin käytöstä hammashoidossa ja suun äkillisten infektioiden mikrobilääkehoidosta
- ohjeistaa mikrobilääkkeen valinnassa niin, että otetaan huomioon potilaan muut sairaudet ja niiden hoito
- edistää mikrobilääkkeiden tarkoituksenmukaista käyttöä hammashoidossa.
Kohderyhmä
- Suosituksen kohderyhminä ovat
- perusterveydenhuollon hammaslääkärit ja lääkärit
- muut terveydenhuollon ammattihenkilöt.
Määritelmät
- Mikrobilääkeprofylaksilla tarkoitetaan systeemistä mikrobilääkitystä, joka annetaan ennen toimenpidettä ja jolla pyritään estämään joko toimenpidealueen infektio, sen vaikeutuminen tai yleistyneen infektion, kuten sepsiksen tai etäinfektion, kehittyminen.
- Mikrobilääkehoidon kohteena on jo todettu infektio.
- Empiirisellä mikrobilääkehoidolla tarkoitetaan hoitoa, joka annetaan ilman mikrobiologista diagnoosia kokemusperäisen tiedon ja alueellisen herkkyystilanteen perusteella.
- Kohdennettu mikrobilääkehoito perustuu mikrobiologiseen diagnoosiin.
- Äkillisellä suun alueen infektiolla tarkoitetaan tässä suosituksessa äkillisesti alkanutta infektiota, jonka keskeisiä oireita ovat kipu ja turvotus ja johon voi liittyä infektion yleisoireita, kuten kuumetta.
- Paikallisantisepti on pinnallisesti käytettävä kemiallinen aine tai aineseos, joka vähentää mikrobimäärää.
Hammasperäisten infektioiden ilmaantuvuus
- Lievät hammasperäiset infektiot ovat perusterveydenhuollossa huomattavan yleisiä, mutta niiden tarkkaa ilmaantuvuutta ei tiedetä.
- Vakavien sairaalahoitoa vaativien hammasperäisten infektioiden (taulukko «Vakavan infektion tunnusmerkit....»1, sairaalaan lähettämisen aiheet) ilmaantuvuus on eri tutkimusten perusteella 5,4–11,1/100000/v ja ilmaantuvuus on lisääntynyt viimeisten 20 vuoden aikana «Meisgeier A, Pienkohs S, Dürrschnabel F, ym. Risin...»2, «Robertson DD, Smith AJ. Significant increase in ho...»3.
- Sairaalahoitoa vaativaan hammasperäiseen infektioon sairastuneet ovat yleisimmin muuten terveitä aikuisia «Furuholm J, Rautaporras N, Uittamo J, ym. Health s...»4, «Velhonoja J, Lääveri M, Soukka T, ym. Deep neck sp...»5.
- Hammasperäiset sairaalahoitoa vaativat infektiot ovat lapsilla harvinaisia.
| Potilaan tutkiminen | Perusterveydenhuollossa hoidettava | Sairaalaan lähettämisen aiheet |
|---|---|---|
| Esitiedot | Ei pitkäaikaissairauksia | Infektiokomplikaatioille altistava sairaus tai lääkitys: huomattavasti suurentuneen
infektioriskin potilaat (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) |
| Yleistila | Normaali | Kuume Suuri syketaajuus Matala verenpaine Sairauden tunne Poikkeava huimaus tai väsymys Tajunnantason häiriö |
| Inspektio ja palpaatio | Paikallinen turvotus, lievä punoitus tai kuumotus | Lisääntyvä turvotus Nielemis-, puhe- tai hengitysvaikeudet Leviävä punoitus/ihoreaktio Äkillinen infektio, joka etenee asianmukaisesta hoidosta huolimatta |
| Suun avaus | Normaali tai vähän rajoittunut | Selkeästi rajoittunut |
Komplikaatiot ja kuolleisuus hammasperäisiin infektioihin
- Valtaosa leukojen alueen levinneistä infektioista sekä syvistä kaulainfektioista on hammasperäisiä «Chow A. Infections of the oral cavity, neck and h...»6, «Velhonoja J, Lääveri M, Soukka T, ym. Deep neck sp...»5, «Jäsberg, H, Kellokoski, J. 2021. Poski turvoksissa...»7.
- Suomalaisessa aineistossa todettiin komplikaatioita 22 %:ssa syvistä kaulainfektioista ja kuolleisuus syvään kaulainfektioon oli 1,4 % «Velhonoja J, Lääveri M, Soukka T, ym. Deep neck sp...»5. Toisessa, vain hammasperäisiä sairaalahoitoisia infektioita käsittäneessä suomalaisessa aineistossa 8 %:lle potilaista kehittyi etäinfektio tai muu vakava infektiokomplikaatio ja kuolleisuus oli 1 % «Furuholm J, Uittamo J, Rautaporras N, ym. Streptoc...»8. Esimerkiksi endokardiitissa kuolleisuutta huomattavasti yleisempiä ovat erilaiset neurologiset komplikaatiot, kuten aivoinfarktit, jotka aiheuttavat usein pysyvän toimintakyvyn heikkenemisen «García-Cabrera E, Fernández-Hidalgo N, Almirante B...»9.
- Vaikeat pitkäaikaissairaudet ja immuunivastetta heikentävät sairaudet ja hoidot lisäävät kuolleisuutta hammasperäiseen infektioon «Furuholm J, Rautaporras N, Uittamo J, ym. Health s...»4, «Lee JJ, Hahn LJ, Kao TP, ym. Post-tooth extraction...»10, «Seppänen L, Lauhio A, Lindqvist C, ym. Analysis of...»11.
Äkillisten hammasperäisten infektioiden etiologia
- Äkillisen hammasperäisen infektion lähtökohtana voi toimia
- hampaan juuren kärkeä ympäröivä apikaalinen parodontiitti «Hampaan ytimen tulehduksen keskeiset käsitteet»1, «Ylijoki S, Suuronen R, Jousimies-Somer H, ym. Diff...»12, «Søndenbroe R, Markvart M, Cort ID, ym. Patients wi...»13
- Apikaalinen parodontiitti on tavallisin äkillisen hammasperäisen infektion syy «Furuholm J, Uittamo J, Rautaporras N, ym. Are ther...»14, «Mahmoodi B, Weusmann J, Azaripour A, ym. Odontogen...»15.
- Tavallisimmin infektio saa alkunsa pulpanekroosista ja mikrobien leviämisestä juurikanavista periapikaalialueelle, mikä voi johtaa laajempaan infektioon.
- Sairaalahoitoa vaativat hammasperäiset infektiot ovat yleisimmin lähtöisin sellaisen hampaan apikaalisesta parodontiitista, jonka juurihoitoa ei ole vielä aloitettu tai, jonka juurihoito on kesken «Furuholm J, Uittamo J, Rautaporras N, ym. Are ther...»14.
- hampaanpoiston jälkeinen poistoalueen infektio «Jäsberg, H, Kellokoski, J. 2021. Poski turvoksissa...»7, «Ylijoki S, Suuronen R, Jousimies-Somer H, ym. Diff...»12, «Søndenbroe R, Markvart M, Cort ID, ym. Patients wi...»13
- Tavallisimmin alueella on jo infektio, joka laajenee poiston jälkeen.
- puhkeavan hampaan ympäryskudosten infektio eli perikoroniitti «Jäsberg, H, Kellokoski, J. 2021. Poski turvoksissa...»7, «Ylijoki S, Suuronen R, Jousimies-Somer H, ym. Diff...»12, «Søndenbroe R, Markvart M, Cort ID, ym. Patients wi...»13
- hampaan kiinnityskudossairaus eli parodontiitti «Jäsberg, H, Kellokoski, J. 2021. Poski turvoksissa...»7
- Hampaan kiinnityskudosten äkillisiä infektioita ovat
- parodontaalipaise, jonka taustalla on yleensä hoitamaton krooninen parodontiitti, harvoin vierasesine «Melnick, P, Takei, H. Diagnosis and Management of ...»16, «Herrera D, Roldán S, González I, ym. The periodont...»17, «Herrera D, Retamal-Valdes B, Alonso B, ym. Acute p...»18 (ks. myös Käypä Hoito -suositus Parodontiitti «Parodontiitti»3 ja «Parodontaalisten absessien luokittelu»2)
- nekrotisoivat parodontaalisairaudet «Herrera D, Retamal-Valdes B, Alonso B, ym. Acute p...»18
- endo-paroleesio «Herrera D, Retamal-Valdes B, Alonso B, ym. Acute p...»18 (ks. myös Käypä hoito -suositus Parodontiitti «Parodontiitti»3 ja «Endo-paroleesioiden luokittelu»3).
- Hampaan kiinnityskudosten äkillisiä infektioita ovat
- hammasvamma «Flores MT, Andersson L, Andreasen JO, ym. Guidelin...»19, «Flores MT, Andersson L, Andreasen JO, ym. Guidelin...»20, «Flores MT, Malmgren B, Andersson L, ym. Guidelines...»21, «Hinckfuss SE, Messer LB. An evidence-based assessm...»22.
- Leukojen alueella myös leukamurtuma «Andreasen JO, Jensen SS, Schwartz O, ym. A systema...»23 tai kirurginen toimenpide, kuten hammasimplantin asettaminen, voivat olla infektion lähtökohtia «Esposito M, Grusovin MG, Worthington HV. Intervent...»24.
Mikrobiologia
- Suun märkäiset infektiot ovat tavanomaisesti suun normaalimikrobistoon kuuluvien bakteereiden aiheuttamia sekainfektioita «Furuholm J, Uittamo J, Rautaporras N, ym. Streptoc...»8, «Siqueira JF Jr, Rôças IN. Microbiology and treatme...»25.
- Yleisimpiä suun alueen märkäisten infektioiden patogeeneja ovat viridans-streptokokit, anaerobiset gramnegatiiviset sauvat, kuten Prevotella-, Fusobacterium- ja Porphyromonas-lajit, sekä anaerobisista kokeista Parvimonas- ja Veillonella-lajit «Furuholm J, Uittamo J, Rautaporras N, ym. Streptoc...»8, «Herrera D, Retamal-Valdes B, Alonso B, ym. Acute p...»18, «Siqueira JF Jr, Rôças IN. Microbiology and treatme...»25.
- Hammasperäiset paiseet ovat yleisimmin viridans-streptokokkien ja anaerobisten gram-negatiivisten sauvojen aiheuttamia sekainfektioita. Viridans-streptokokeista erityisesti Streptococcus anginosus -ryhmä yhdistetään vakaviin hammasperäisiin infektioihin «Furuholm J, Uittamo J, Rautaporras N, ym. Streptoc...»8.
- Harvinaisesti patogeenina voi olla Staphylococcus aureus, beetahemolyyttinen streptokokki tai aerobinen gramnegatiivinen sauva (esim. Klebsiella-laji). Tuoreessa kotimaisessa tutkimuksessa näistä kutakin todettiin vain 1 %:ssa sairaalahoitoisista hammasperäisistä infektioista «Furuholm J, Uittamo J, Rautaporras N, ym. Streptoc...»8. Harvinaisuutensa vuoksi niitä ei siksi tarvitsekaan rutiininomaisesti kattaa mikrobilääkkein empiirisessä hoidossa.
- Suuperäisissä etäinfektioissa on todettu lukuisia eri bakteerilajeja «Lou Y, Sun Z, Ma H, ym. Odontogenic infections in ...»26, «Lee JJ, Hahn LJ, Kao TP, ym. Post-tooth extraction...»27. Löydöksistä yleisimpiä ovat suun streptokokit, joita on raportoitu 40–65 %:ssa suuperäisiksi tulkituista etäinfektioista «Parahitiyawa NB, Jin LJ, Leung WK, ym. Microbiolog...»28. Fusobakteerit ovat löydöksistä toiseksi yleisin «Parahitiyawa NB, Jin LJ, Leung WK, ym. Microbiolog...»28. Endokardiiteissa viridans-streptokokit ovat yleisin suuperäinen löydös, ja siksi ne on aina katettava endokardiittiprofylaksissa «Delgado, V, Marsan, N, de Waha, S ym. ESC Scientif...»29. Muuten ei ole tietoa tietyn suun bakteerin assosioitumisesta eri etäinfektioihin.
- Nekrotisoivissa parodontaalisairauksissa spirokeetoilla ja muilla anaerobeilla katsotaan olevan keskeinen rooli «L...»30, «Loesche WJ, Syed SA, Laughon BE, ym. The bacteriol...»31, «Gmür R, Wyss C, Xue Y, ym. Gingival crevice microb...»32, «Herrera D, Retamal-Valdes B, Alonso B, ym. Acute p...»18.
Mikrobilääkeherkkyys
- Suun alueen märkäisten infektioiden keskeisten patogeenien herkkyys V-penisilliinin
ja metronidatsolin yhdistelmälle on Suomessa edelleen hyvä «Rihtniemi L, Tjäderhane L, Kotiranta A ym. Juurika...»33, «Hjelm K, Seppänen L, Richardson R. Hammasperäisten...»34. Katso Helsingin ja Uudenmaan alueen herkkyystilastot «https://diagnostiikka.hus.fi/mikrobiologian-herkkyystilastot»1.
- Klindamysiinin ja makrolidien (esim. atsitromysiini) herkkyystilannetta tulee seurata, ja niiden käyttö vaatii harkintaa, koska myös suun mikrobien, etenkin streptokokkien, resistenssin yleistymisestä ja huonosta hoitovasteesta on saatu viitteitä «Rihtniemi L, Tjäderhane L, Kotiranta A ym. Juurika...»33. Katso Helsingin ja Uudenmaan alueen herkkyystilastot «https://diagnostiikka.hus.fi/mikrobiologian-herkkyystilastot»1.
- Bakteerien herkkyys mikrobilääkkeille on maailmanlaajuisesti heikentynyt suuresti, ja Maailman terveysjärjestö WHO on tuoreessa raportissaan pitänyt sitä yhtenä merkittävimmistä kansanterveyden uhista «WHO; Antimicrobial resistance: A global report on ...»35, «WHO: Antimicrobial resistance, 2023. https://www.w...»36. Mikrobilääkkeiden käytön kohdistaminen vain sellaisiin tilanteisiin, joissa niistä todennäköisimmin on apua, on yksi tärkeistä keinoista torjua mikrobilääkeresistenssin yleistymistä «Tamma PD, Cosgrove SE. Addressing the Appropriaten...»37, «Maunuksela T, Huovinen P, Vuopio J. Suomessa käyte...»38.
Altistavat tekijät
- Hammasperäisen infektion paikalliselle leviämiselle ja infektion yleistymiselle saattavat
altistaa:
- hoitamaton hampaisto ja hampaiston huono kunto «Velhonoja J, Lääveri M, Soukka T, ym. Risk factors...»39, «Aksoy A, Demirkıran BB, Bora A, ym. Comprehensive ...»40, «Opitz D, Camerer C, Camerer DM, ym. Incidence and ...»41, «Seppänen L, Lemberg KK, Lauhio A, ym. Is dental tr...»42
- infektion sijainti alaleuan poskihampaassa «Furuholm J, Rautaporras N, Uittamo J, ym. Health s...»4
- tupakointi, runsas alkoholinkäyttö ja huumeidenkäyttö «Furuholm J, Rautaporras N, Uittamo J, ym. Health s...»4, «Aksoy A, Demirkıran BB, Bora A, ym. Comprehensive ...»40
- vaikeat pitkäaikaissairaudet, immuunivastetta heikentävät sairaudet ja hoidot, psykiatriset sairaudet, dementia, yli 60 vuoden ikä «Dou K, Shi Y, Yang B, ym. Risk factors for life-th...»43, «Grubeck-Loebenstein B, Wick G. The aging of the im...»44, «Velhonoja J, Lääveri M, Soukka T, ym. Deep neck sp...»5 sekä diabetes «Diabetes may increase the risk of severe infection complications of dental origin, and the length of hospital stay.»C. Katso myös taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2.
- Nekrotisoiville parodontaalisairauksille voivat altistaa stressi, heikentynyt elimistön puolustusvaste (esim. edennyt HIV, akuutti leukemia), huono suuhygienia, tupakointi ja vajaaravitsemus «Albandar JM. Aggressive and acute periodontal dise...»45, «Herrera D, Retamal-Valdes B, Alonso B, ym. Acute p...»18.
| Suurentunut infektioriski | Huomattavasti suurentunut infektioriski |
|---|---|
| Taulukossa esitettyjen tekijöiden vaikutuksesta infektioriskin suuruuteen ei ole suoraa
näyttöä, ja asiantuntijoiden käsitys riskistä vaihtelee. Riskiä tulee arvioida tapauskohtaisesti. Suurentuneen infektioriskin potilaat hoidetaan yleensä perusterveydenhuollossa ja mikrobilääkeprofylaksin käyttöä harkitaan toimenpidealueen infektion vakavuuden ja toimenpiteen invasiivisuuden perusteella. Huomattavasti suurentuneen infektioriskin potilaita ei tulisi yleensä hoitaa perusterveydenhuollossa ilman hoitavan erikoissairaanhoidon lääkärin konsultaatiota. * Näille potilaille European Society of Cardiology (ESC) suositelee mikobilääkeprofylaksia endokardiitin ehkäisemiseksi bakteremiaa aiheuttavissa toimenpiteissä (ks. «Delgado, V, Marsan, N, de Waha, S ym. ESC Scientif...»29). Sitä on harkittava myös potilaille, joille on tehty katetriteitse mitraaliläpän tai trikuspidaaliläpän korjaus (MitraClip tai TriClip). Näille potilaille ESC suosittelee endokardiitin ehkäisyssä jatkuvaa suun terveyden ylläpitoa päivittäisen omahoidon ja yksilöllisesti suunnitellun säännöllisen ammattimaisen hoidon keinoin (ks. myös kappale Ehkäisy «A1»2). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- Kun hammashoidon tarve ei ole kiireellinen, voidaan toisinaan infektiokomplikaatioriskiä pienentää toimenpiteen ajoittamista muuttamalla (esim. tekemällä toimenpiteet postoperatiivisen varoajan jälkeen tai huomioimalla harvoin annosteltavien infektioriskiä suurentavien lääkkeiden annosteluajankohta).
- Jos potilaan infektioriski on huomattavasti suurentunut
- toimenpiteistä tulisi pidättäytyä, ellei niiden tarve ole erityisen tärkeä tai kiireellinen. Näin on tyypillisesti esimerkiksi silloin, kun hampaan hoitamattomuudesta seuraa suurempi riski kuin sen hoidosta (esim. tiedossa oleva infektioherkkyyden lisääntyminen syöpähoitojen edetessä).
- hoito kohdistetaan pääasiassa vain selkeisiin fokushampaisiin.
Ehkäisy
- Huolellinen päivittäinen omahoito (hampaiden puhdistus kahdesti päivässä) ja säännöllinen hammashoito ovat tärkeimmät tekijät hammasperäisten infektioiden ehkäisyssä «Delgado, V, Marsan, N, de Waha, S ym. ESC Scientif...»29.
- Suuperäisten etä- ja yleisinfektioiden estämiseksi suun alueen infektiot suositellaan hoidettavan ennen sellaisia leikkauksia, joissa elimistöön asetetaan vierasesine (sydänläppä, nivel- tai verisuoniproteesi), avosydänleikkauksia, elinsiirtoja ja voimakkaan immunosuppressiivisen lääkehoidon aloittamista «Yamagata K, Onizawa K, Yanagawa T, ym. A prospecti...»46, «Bergmann OJ. Oral infections and septicemia in imm...»47, «Melkos AB, Massenkeil G, Arnold R, ym. Dental trea...»48, «Elad S, Raber-Durlacher JE, Brennan MT, ym. Basic ...»49, «Delgado, V, Marsan, N, de Waha, S ym. ESC Scientif...»29 sekä säännöllisesti niiden jälkeen.
- Suun infektioiden hoito on tärkeää myös ennen leukojen alueelle kohdistuvaa sädehoitoa ja ennen luunkorjaajalääkkeiden (esim. denosumabi, bisfosfonaatit) aloitusta, etenkin kun lääkkeitä käytetään syöpätaudeissa «Elad S, Raber-Durlacher JE, Brennan MT, ym. Basic ...»49, «Bamias A, Kastritis E, Bamia C, ym. Osteonecrosis ...»50, «Dodson TB. The Frequency of Medication-related Ost...»51, sekä säännöllisesti niiden aloittamisen jälkeen.
- Suun alueen infektioiden tehokas hoitaminen potilaan ollessa terve – ilman suuperäisille infektiolle altistavia pitkäaikaissairauksia tai lääkityksiä (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) – vähentäisi merkittävästi mikrobilääkkeiden käytön tarvetta hammashoidon yhteydessä.
Diagnostiikka
- Diagnostiikka perustuu huolelliseen anamneesiin, potilaan kokonaisvaltaiseen kliiniseen tutkimukseen ja radiologiseen kuvantamiseen «Jäsberg, H, Kellokoski, J. 2021. Poski turvoksissa...»7.
- Jos potilaalla on merkkejä infektion leviämisestä, yleisoireita tai jokin vakava pitkäaikaissairaus, tehdään lisäksi infektion ja pitkäaikaissairauden kannalta keskeiset laboratoriotutkimukset.
Anamneesi
- Anamneesista on tärkeää huomioida muun muassa:
- pitkäaikaissairaudet ja niiden lääkitykset (ks. taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2)
- raskaus ja imetys
- lääkeaineallergiat
- edeltävä mikrobilääkkeiden käyttö
- hammasinfektion oirehistoria
- tehdyt toimenpiteet.
Kliininen diagnoosi
- Hammasperäisen äkillisen infektion oireet vaihtelevat epämukavasta olosta voimakkaaseen kipuun ja vähäisestä turvotuksesta suun avauksen ja nielemisen vaikeutumiseen sekä ilmateiden ahtautumiseen. Suunsisäinen turvotus ei välttämättä näy ulospäin «Jäsberg, H, Kellokoski, J. 2021. Poski turvoksissa...»7, «Siqueira JF Jr, Rôças IN. Microbiology and treatme...»25 (ks. myös taulukko «Vakavan infektion tunnusmerkit....»1).
- Infektion lähtökohtana oleva hammas voi olla puru- ja koputusarka ja kohonnut. Sen liikkuvuus voi olla lisääntynyt, ien voi olla arka ja turvonnut ja ientaskuista voi tulla verta tai märkää.
- Suunsisäinen ja -ulkoinen turvotus ja laajuus tutkitaan palpoimalla ja mahdollinen puoliero havainnoidaan, suunpohjan alueella molempikätisesti palpoiden.
- Muita oireita ja löydöksiä voivat olla kuume, paikallisten imusolmukkeiden suurentuminen tai arkuus ja pahanhajuinen hengitys «Jäsberg, H, Kellokoski, J. 2021. Poski turvoksissa...»7, «Herrera D, Roldán S, González I, ym. The periodont...»17, «Siqueira JF Jr, Rôças IN. Microbiology and treatme...»25 (ks. myös taulukko «Vakavan infektion tunnusmerkit....»1).
- Nielemis-, puhe-, suunavaus-, päänkääntämis- ja hengitysvaikeudet, kaulan turvotus,
kova kuume sekä oireiden nopea kehittyminen ovat vakavan infektion merkkejä (taulukko
«Vakavan infektion tunnusmerkit....»1).
- Jos yksikin näistä esiintyy, on yleensä aiheellista lähettää potilas erikoissairaanhoidon päivystykseen arvioitavaksi.
- Mahdolliset infektion kliiniseen kuvaan vaikuttavat lääkeaineet on syytä huomioida vakavuusastetta arvioitaessa (esim. kipulääkkeiden kuumetta alentava vaikutus).
- Lievätkin yleisoireet voivat olla merkki levinneestä infektiosta. Lähettämistä suu- ja leukasairauksien erikoissairaanhoidon yksikköön tulee harkita etenkin silloin, jos potilaalla on sairauden tai lääkityksen vuoksi suurentunut infektioriski.
- Neutropeenisella potilaalla infektion paikallisoireet voivat olla lievät, vaikka kyse olisi jo levinneestä infektiosta. Siksi etenkin näiden potilaiden infektion vaikeusastearviossa tulee huomioida kuume ja muut yleisoireet mahdollisina ainoina vakavan infektion merkkeinä.
- Nekrotisoivissa parodontaalisairauksissa on kolme aina esiintyvää piirrettä: haavainen ja nekroottinen ienpapilla, herkästi verta vuotavat ikenet ja kipu. Haavaumia voi peittää kellertävän valkoinen tai harmahtava peite «Klokkevold, PR, Carranza, FA. Acute Gingival Infec...»52.
- Hammasperäisten infektioiden erotusdiagnostiikassa tulee huomioida laaja kirjo muita tulehduksellisia ja neoplastisia muutoksia ja sairauksia, kuten nieluinfektiot, sinuiitti, sylkirauhasinfektiot, lymfadeniitti ja mononukleoosi. Katso myös Käypä hoito -suositukset Suusyöpä «Suusyöpä»4, Viisaudenhammas «Viisaudenhammas»5, Hampaan juurihoito «Hampaan juurihoito»6, Parodontiitti «Parodontiitti»3 ja Purentaelimistön kipu ja toimintahäiriöt «Purentaelimistön kipu ja toimintahäiriöt (TMD)»7.
Radiologiset tutkimukset
- Perusterveydenhuollossa hampaiston panoraamatomografia (PTG) ja intraoraaliröntgenkuva ovat ensisijaiset tutkimukset «Jäsberg, H, Kellokoski, J. 2021. Poski turvoksissa...»7. Joissakin tapauksissa tarvitaan lisäkuvauksia.
- Nopeasti etenevissä infektioissa osteiitin röntgenlöydökset voivat jäädä vähäisiksi.
Laboratoriotutkimukset
- Vakavaa infektiota epäiltäessä anamneesin ja kliinisen tutkimuksen antamaa informaatiota
voidaan täydentää määrittämällä perusverenkuva (leukosyytit) ja seerumin C-reaktiivinen
proteiini (CRP).
- CRP:n pitoisuus yli 50 mg/l tai leukosyyttimäärä yli 10 x 109/l viittaavat vakavaan tautiin «Furuholm J, Rautaporras N, Uittamo J, ym. Health s...»4, «Póvoa P, Almeida E, Moreira P, ym. C-reactive prot...»53.
- Yleisoireisilta (yleistilaltaan heikentyneiltä, septisiltä tai kuumeilevilta) potilailta otetaan lisäksi veriviljelynäytteet kahdesti ennen mikrobilääkehoidon aloitusta «HUS. Mikrobilääke-hoito-opas. 2024. https://www.hu...»54.
- Vaikka mikrobilääkitys aloitetaan äkillisessä infektiossa empiirisesti, on mikrobinäytteen
otto suositeltavaa ennen mikrobilääkityksen aloittamista, jos
- potilaalla on vakavan infektion merkit (taulukko «Vakavan infektion tunnusmerkit....»1)
- potilaalla on huomattavasti infektioriskiä suurentava pitkäaikaissairaus tai lääkitys (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2)
- infektio persistoi tai vaikeutuu tavanomaisesti tehokkaana pidetystä hammaslääketieteellisestä hoidosta huolimatta.
- Mikrobinäytteestä tulisi tunnistaa suun infektioiden keskeiset patogeenit ja muut vakavat taudinaiheuttajat, ja niiden mikrobilääkeherkkyys tulisi määrittää «Siqueira JF Jr, Rôças IN. Microbiology and treatme...»25, «Furuholm J, Uittamo J, Rautaporras N, ym. Streptoc...»8, «Herrera D, Retamal-Valdes B, Alonso B, ym. Acute p...»18. Mikrobilääkitystä kohdennetaan tarvittaessa löydösten mukaisesti potilaan kliininen tilanne huomioiden.
Mikrobilääkkeet hammashoidossa
Yleistä
- Useimmat potilaat eivät tarvitse mikrobilääkkeitä hammashoidon yhteydessä.
- Mikrobilääkkeiden käyttöaiheet hammashoidossa ovat (taulukot «Profylaksin käyttöaiheet eri toimenpiteissä potilaan infektioriskin (ks. taulukko
) mukaan eriteltynä. Profylaksia käytetään lisäksi aina, jos on suunniteltu mikrobilääkehoidon
aloittamista toimenpiteen jälkeen....»3, «Mikrobilääkehoidon käyttöaiheet potilaan infektion vaikeusasteen ja yleisterveyden
mukaan eriteltynä....»5)
- kerta-annosprofylaksi infektiokomplikaatioiden ennaltaehkäisemiseksi
- verekkäät toimenpiteet, etenkin luuhun ulottuvat
- toimenpidealueen infektioasteen, potilaan yleistilan ja toimenpiteen luonteen perusteella
- äkillisen infektion hoito hammaslääketieteellisen hoidon lisänä
- kerta-annosprofylaksi infektiokomplikaatioiden ennaltaehkäisemiseksi
- Mikrobilääkkeiden käyttö tulee rajata toimenpiteen tai potilaan infektioriskin perusteella
sellaisiin tilanteisiin, joissa voidaan perustellusti olettaa mikrobilääkkeen käytöstä
olevan hyötyä.
- Mikrobilääkkeitä ei tule käyttää kipulääkkeinä ( «https://www.kaypahoito.fi/hoi50103»2 ja «https://www.duodecimlehti.fi/duo16798»3).
- Infektioriskiä arvioitaessa on otettava huomioon potilaan kaikkien sairauksien ja lääkitysten aiheuttama riski kokonaisuutena.
- Mikrobilääkkeen soveltuvuus potilaalle tulee varmistaa huomioiden muun muassa allergiat,
interaktiot, raskaus, imetys ja mahdollisesti muuttunut lääkeainemetabolia. Katso
muun muassa:
- Lääkkeiden käyttö kroonisessa munuaisten vajaatoiminnassa (Renbase) «https://www.terveysportti.fi/apps/renbase/»4
- Lääkkeiden käyttö maksan vajaatoiminnassa (Heparbase) «https://www.terveysportti.fi/apps/heparbase/»5
- Lääkeinteraktiot ja haitat (Riskbase, Inxbase) «https://www.terveysportti.fi/apps/interaktio/»6
- Lääkkeiden käyttö raskauden ja imetyksen aikana (Gravbase, Lactbase) «https://www.terveysportti.fi/apps/raim/»7
- Potilaan edeltävän kuukauden aikana saamat mikrobilääkkeet sekä moniresistenttien
mikrobien altistukset ja kantajuudet tulee selvittää ja resistenttien kantojen valikoitumisen
ja rikastumisen mahdollisuus tulee ottaa lääkevalinnassa huomioon.
- Potilaan edeltävän kuukauden aikana saama mikrobilääke ei välttämättä ole mikrobiston muuttumisen vuoksi tehokas. Siten näissä tilanteissa esimerkiksi V-penisilliini korvataan tarvittaessa amoksisilliinilla ja amoksisilliini kefaleksiinilla tai klindamysiinillä.
- Moniresistenttien mikrobien kantajia (esim. MRSA, ESBL) hoidettaessa korostuu tarve välttää tarpeetonta mikrobilääkkeiden käyttöä normaalimikrobiston suojelemiseksi «Anttila, V-J. Moniresistentit bakteerit. Helsinki...»55, «Anttila, V-J. MRSA (metisilliinille resistentti St...»56.
- Mikrobilääkeresistenssin kehitystä suosivaa ja dysbioosin syntyä edistävää tarpeettoman laajakirjoista mikrobilääkitystä tulee välttää.
- Mikrobilääkityksen tulee olla riittävä, mutta mahdollisimman kapeakirjoinen ja lyhytkestoinen.
- Mikrobilääkkeen käyttö aiheuttaa normaalimikrobiston häiriöitä (dysbioosi) kaikkialla elimistössä «Kirchner M, Mafura M, Hunt T, ym. Antimicrobial re...»57, «Zaura E, Brandt BW, Teixeira de Mattos MJ, ym. Sam...»58.
- Pidempi mikrobilääkehoito aiheuttaa lyhyttä hoitoa isompia muutoksia normaalimikrobistoon «Abeles SR, Jones MB, Santiago-Rodriguez TM, ym. Mi...»59.
- Jo yksi kerta-annos amoksisilliinia muuttaa mikrobistoa ja saa aikaan resistenttien streptokokkien valikoitumista suuhun «Khalil D, Hultin M, Rashid MU, ym. Oral microflora...»60.
- Kliinisesti näkyviin mikrobilääkkeiden haittoihin lukeutuvat muun muassa Clostridioides difficile -suolistotulehdus ja limakalvojen hiivasieni-infektiot.
- Klooriheksidiiniä sisältävän suuhuuhteen kuuriluontoisesta käytöstä voi olla hyötyä
systeemisen mikrobilääkkeen lisänä, mutta se ei korvaa mikrobilääkettä «Ugwumba CU, Adeyemo WL, Odeniyi OM, ym. Preoperati...»61, «Duvall NB, Fisher TD, Hensley D, ym. The comparati...»62, «Barbosa M, Prada-López I, Álvarez M, ym. Post-toot...»63, «Maharaj B, Coovadia Y, Vayej AC. A comparative stu...»64.
- Klooriheksidiinihuuhtelu ennen toimenpidettä vähentää bakteremian ilmaantuvuutta, mutta sen vaikutus yksinään on pienempi kuin systeemisen mikrobilääkkeen «Barbosa M, Prada-López I, Álvarez M, ym. Post-toot...»63, «Arteagoitia I, Rodriguez Andrés C, Ramos E. Does c...»65.
Vasta-aiheet
- Mikrobilääkeprofylaksin ja -hoidon vasta-aiheet ovat
- yleiset lääkehoidon ehdottomat ja suhteelliset vasta-aiheet (esim. allergia lääkeaineelle tai valmisteen muulle ainesosalle, yhteisvaikutukset muiden potilaan käyttämien lääkkeiden kanssa, pitkäaikaissairauksien tai niiden hoidon aiheuttama poikkeava lääkeainemetabolia tai muu yhteisvaikutus)
- aiempi raju antibioottiripuli (Clostridioides difficile -ripuli), etenkin jos se on ollut edeltävien kuukausien aikana. Jos mikrobilääkkeen käyttö kuitenkin arvioidaan aiheelliseksi, konsultoidaan infektiolääkäriä.
- raskauden ja imetyksen aikana tetrasykliinit ovat vasta-aiheisia, mutta penisilliinijohdoksia voi käyttää
- akuutti pulpiitti, jonka oireita mikrobilääkehoito ei vähennä «Mikrobilääkehoidoista ei ilmeisesti ole hyötyä eikä sitä suositella äkillisen pulpiitin hoidossa.»C.
Mikrobilääkeprofylaksin periaatteet
- Suurin osa potilaista ei tarvitse mikrobilääkeprofylaksia hammashoidon toimenpiteissä.
- Profylaksi voi olla tarpeen toimenpidealueen infektioasteen, toimenpiteen luonteen
tai potilaan yleisterveyden perusteella (ks. taulukot
«Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon
PDF-versio tästä linkistä )...»2 ja «Profylaksin käyttöaiheet eri toimenpiteissä potilaan infektioriskin (ks. taulukko
) mukaan eriteltynä. Profylaksia käytetään lisäksi aina, jos on suunniteltu mikrobilääkehoidon
aloittamista toimenpiteen jälkeen....»3
sekä kuva
«Hammasperäisen infektion hoidon periaatteet»1).
- Infektioriskipotilaat voidaan karkeasti jakaa kahteen eri ryhmään. Taulukossa «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2 on esimerkkejä molempien ryhmien potilaiden lääkehoidosta ja taustasairauksista.
- Ensisijaisesti käytetään kerta-annosprofylaksia, joka otetaan noin 60 (30–90) minuuttia ennen toimenpidettä.
- Profylaksin tulee kattaa riittävän laajasti toimenpidealueen mikrobeista keskeisimmät hammasperäisten infektioiden aiheuttajat ja kunkin potilasryhmän keskeisimmät etäinfektioiden aiheuttajat (ks. kappale Mikrobiologia «A2»3) «Furuholm J, Uittamo J, Rautaporras N, ym. Streptoc...»8, «Siqueira JF Jr, Rôças IN. Microbiology and treatme...»25. Näihin kuuluvat aina suun streptokokit.
- Suun mikrobit saattavat spontaanisti tai infektiolähteeseen kohdistuvan toimenpiteen yhteydessä aiheuttaa paikallisen infektiokomplikaation «Seppänen L, Lemberg KK, Lauhio A, ym. Is dental tr...»42 tai etäinfektion muualle elimistöön «Rajasuo A, Nyfors S, Kanervo A, ym. Bacteremia aft...»66, «Kinane DF, Riggio MP, Walker KF, ym. Bacteraemia f...»67, «Lou Y, Sun Z, Ma H, ym. Odontogenic infections in ...»68, «Thornhill MH, Gibson TB, Yoon F, ym. Antibiotic Pr...»69, «Delgado, V, Marsan, N, de Waha, S ym. ESC Scientif...»29.
- Infektioherkkyyden lisäksi toimenpidealueen infektioaste sekä toimenpiteen laajuus ja vaikeusaste vaikuttavat paikallisten infektiokomplikaatioiden syntyyn. Tästä on saatu näyttöä erityisesti viisaudenhammaskirurgian yhteydessä «Arteagoitia I, Diez A, Barbier L, ym. Efficacy of ...»70, «Lacasa JM, Jiménez JA, Ferrás V, ym. Prophylaxis v...»71, «Halpern LR, Dodson TB. Does prophylactic administr...»72, «Lee JY, Do HS, Lim JH, ym. Correlation of antibiot...»73, «Chuang SK, Perrott DH, Susarla SM, ym. Risk factor...»74, «Mikrobilääkeprofylaksi ilmeisesti vähentää terveiden potilaiden viisaudenhammaskirurgian infektiokomplikaatioita 66 % ja lisää lievien, ohimenevien haittavaikutusten esiintyvyyttä.»B.
- Mikrobilääkeprofylaksi ei ole tarpeen terveen potilaan infektoitumattoman hampaan poistossa, jossa ei tarvita osteotomiaa «Mikrobilääkeprofylaksi ei ole tarpeen terveen potilaan infektoitumattoman hampaan poistossa, jossa ei tarvita osteotomiaa.»A.
- Mikrobilääkeprofylaksi ei estä terveiden potilaiden implantin varhaista menettämistä «Toimenpidettä edeltävästi annettu mikrobilääkeprofylaksi ei estä terveiden henkilöiden implantin varhaista menettämistä.»A.
- Mikrobilääkeprofylaksi ilmeisesti vähentää bakteremian ilmaantuvuutta «Amoxicillin 2 g p.o.»B.
- Hampaisiin ja limakalvoon kohdistuvat toimenpiteet kuten myös päivittäinen omahoito aiheuttavat bakteremiaa «Sonbol H, Spratt D, Roberts GJ, ym. Prevalence, in...»75, «Mougeot FK, Saunders SE, Brennan MT, ym. Associati...»76, «Tomás I, Diz P, Tobías A, ym. Periodontal health s...»77, «Zhang W, Daly CG, Mitchell D, ym. Incidence and ma...»78.
- Infektoituneen alueen hammastoimenpiteet aiheuttavat kuitenkin runsaamman hetkellisen bakteremian kuin omahoito «Lucas VS, Gafan G, Dewhurst S, ym. Prevalence, int...»79, «Lockhart PB, Brennan MT, Sasser HC, ym. Bacteremia...»80. Ientulehdus ja parodontiitti lisäävät bakteremian määrää ja kestoa omahoidon ja biofilmien poistamisen yhteydessä verrattuna tilanteeseen, jossa ientulehdusta ei ole «Forner L, Larsen T, Kilian M, ym. Incidence of bac...»81. Toimenpiteistä yleisimmin bakteremiaa esiintyy hampaanpoistossa ja toiseksi yleisimmin parodontologisessa instrumentoinnissa «Martins CC, Lockhart PB, Firmino RT, ym. Bacteremi...»82. Myös muut limakalvoa rikkovat eli invasiiviset toimenpiteet aiheuttavat bakteremiaa «Martins CC, Lockhart PB, Firmino RT, ym. Bacteremi...»82.
- Etäinfektioriskin kannalta keskeisiä ovat bakteremian taso ja etenkin potilaan infektioherkkyys «Shelburne SA, Sahasrabhojane P, Saldana M, ym. Str...»83, «Whimbey E, Kiehn TE, Brannon P, ym. Clinical signi...»84.
- Mikrobilääkeprofylaksia suositellaan suuren endokardiittiriskin potilaille ja harkinnan mukaan muille potilaille, joilla on infektiokomplikaatioille altistava sairaus tai lääkitys (ks. taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2 ja kuva «Hammasperäisen infektion hoidon periaatteet»1. Suositus noudattaa ESC:n suositusta bakteeriendokardiitin profylaksista «Delgado, V, Marsan, N, de Waha, S ym. ESC Scientif...»29, «Laine, J, Ryödi, E. Bakteeriendokardiitin ehkäisy ...»85.
- Tutkimusnäyttö mikrobilääkeprofylaksin vaikutuksesta muihin kuin yllä mainittuihin infektiokomplikaatioihin tai etäinfektioihin on ristiriitaista «Cahill TJ, Harrison JL, Jewell P, ym. Antibiotic p...»86, «Sperotto F, France K, Gobbo M, ym. Antibiotic Prop...»87, «Thornhill MH, Gibson TB, Yoon F, ym. Endocarditis,...»88, «Rutherford SJ, Glenny AM, Roberts G, ym. Antibioti...»89, «Vähäsarja, N. 2023. Antibiotic prophylaxis in dent...»90, «Rademacher WMH, Walenkamp GHIM, Moojen DJF, ym. An...»91, «Thornhill MH, Crum A, Rex S, ym. Analysis of Prost...»92, «McGregor JC, Wilson GM, Gibson G, ym. The effect o...»93.
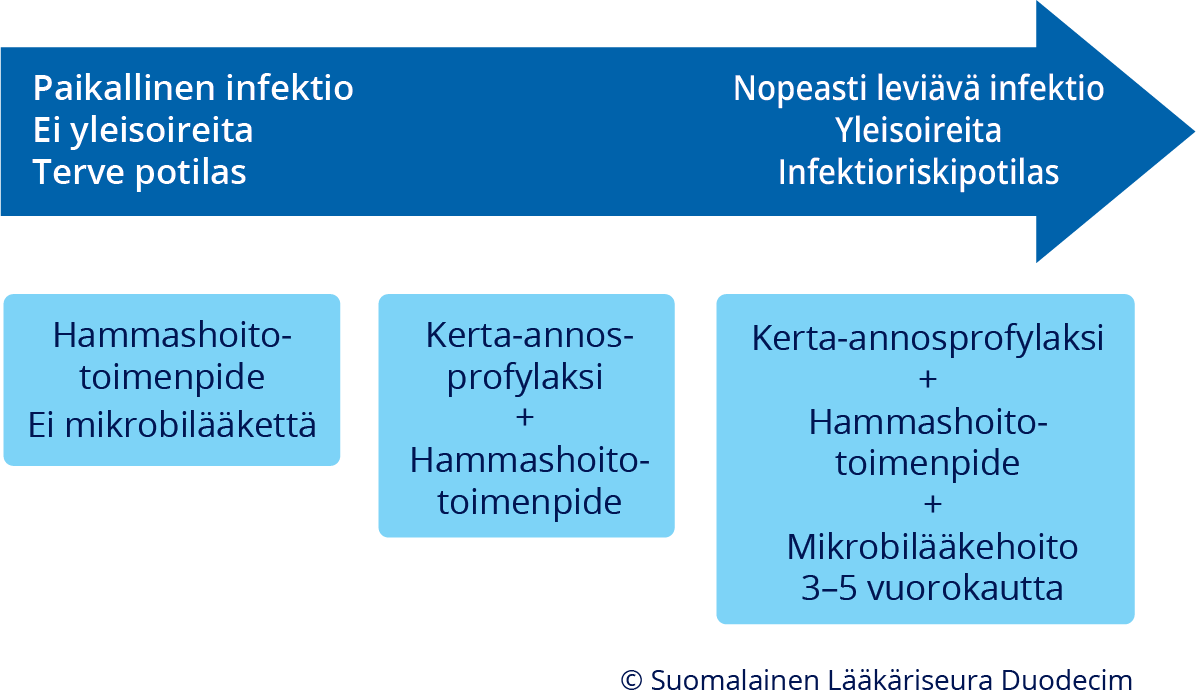
Hammasperäisen infektion hoidon periaatteet.
Hammasperäisten infektioiden hoidossa mikrobilääkehoito on toissijainen, eikä sen aloittamisella voi perustella hammaslääketieteellisen hoidon lykkäämistä. Useimmat potilaat eivät tarvitse mikrobilääkeprofylaksia tai -hoitoa hammasperäisen infektion hoidon yhteydessä. Jos mikrobilääkitystä tarvitaan, se aloitetaan ennen hammashoitotoimenpidettä kerta-annosprofylaksilla.
© Suomalainen Lääkäriseura Duodecim
Mikrobilääkeprofylaksin käyttöaiheet
- Profylaksi ei pääsääntöisesti ole tarpeen seuraavissa tutkimus- tai hoitotoimenpiteissä:
- suun ja hampaiden tutkimus
- ientaskumittaus
- hampaan paikkaushoito ja muu korjaava hoito
- supragingivaalinen biofilmin ja hammaskiven poisto
- juurihoito
- oikomishoito
- hammasproteesin sovitus
- tavanomainen terveen potilaan infektoitumattoman hampaan poisto
- terveen potilaan yksittäisen implantin tavanomainen asettaminen tai tavanomainen parodontaalikirurgia.
| Ei suurentunutta infektioriskiä (terve) |
|---|
| Hampaanpoisto, kun hampaaseen liittyy paise (pysyvät hampaat) Luuhun kajoava toimenpide, esimerkiksi leikkauksellinen hampaanpoisto, johon liittyy merkittäviä riskitekijöitä (alueella on paikallinen infektio, esimerkiksi perikoroniitti ja porataan luuta (osteotomia), hampaan sijainti syvällä luussa, mahdollisesti kudokseen syntyvä hematooma on laaja) |
| Suurentunut infektioriski |
Bakteremiaa aiheuttavat hoitotoimenpiteet seuraavissa potilasryhmissä:
|
Muilla suurentuneen infektioriskin potilailla profylaksia käytetään kuten terveillä.
Lisäksi käyttöä tulee harkita huomioiden potilaan infektiokomplikaatioriski, toimenpidealueen
infektioaste sekä toimenpiteen invasiivisuus, kesto, vaikeusaste ja laajuus. Profylaksia
voivat edellyttää
|
| Huomattavasti suurentunut infektioriski |
| Hammaslääketieteelliset invasiiviset tutkimus- ja hoitotoimenpiteet |
Mikrobilääkeprofylaksin toteutus
- Kerta-annosprofylaksi annetaan suun kautta noin 60 minuuttia (30–90 minuuttia) ennen toimenpidettä «Ren YF, Malmstrom HS. Effectiveness of antibiotic ...»94. Huomattavasti suurentuneen infektioriskin potilaille profylaksi annetaan tarvittaessa sairaalaolosuhteissa suonensisäisesti.
- Suun kautta otettavassa mikrobilääkeprofylaksissa tulee ensisijaisesti käyttää lääkkeitä,
jotka imeytyvät hyvin suun kautta otettuna, joilla saavutetaan hyvät pitoisuudet kohdekudoksessa
ja joiden herkkyystilanne on hyvä.
- Hammasperäisten infektiokomplikaatioiden ehkäisyyn käytetään ensisijaisesti amoksisilliinia ja penisilliinille allergisille (ei anafylaksia) ensimmäisen polven kefalosporiinia joko yksinään tai yhdessä metronidatsolin kanssa «Terveysportti. Lääkkeet ja hinnat 2025. https://ww...»95. Katso myös suositustekstin erikoisalakohtaiset ohjeet (mikrobilääkkeet suu- ja leukakirurgiassa «A3»4, endodontiassa «A4»5, parodontologiassa «A5»6, hammastraumojen hoidossa «A6»7 ja lapsilla «A7»8).
- Penisilliiniryhmän lääkkeestä anafylaktisen allergisen reaktion saaneille potilaille ensisijainen vaihtoehto on klindamysiini. Moksifloksasiinia voidaan harkita, jos klindamysiini ei sovellu (ks. myös kappale Mikrobilääkehoidon toteutus «A8»9). Mikrobilääkeprofylaksisuositukset esitetään taulukossa «Ensisijaiset mikrobilääkkeet kerta-annosprofylaksissa....»4.
| Riski | Ensisijaisesti | Penisilliinille allergiset (muu kuin anafylaktinen reaktio) | Penisilliinille allergiset (anafylaktinen reaktio) | |
|---|---|---|---|---|
| * Metronidatsolin 400 mg yhdistämistä kerta-annosprofylaksiin harkitaan tapauskohtaisesti.
Yleensä se on tarpeen suurentuneen ja huomattavasti suurentuneen infektioriskin potilaille
silloin, kun toimitaan märkäisellä alueella, on epäily infektion paikallisesta leviämisestä,
potilaalla on yleisoireita tai kun mikrobilääkehoitoa jatketaan yhdistelmälääkityksellä.
** Endokardiittiprofylaksissa aikuisten kefaleksiiniannos on 2 g European Society of Cardiologyn (ESC) suosituksen mukaisesti «2023 ESC Guidelines for the management of endocard...»1. *** Jos klindamysiini ei sovellu käytettäväksi, voidaan toissijaisena endokardiittiprofylaksissa ESC:n suosituksen mukaisesti käyttää atsitromysiiniä tai klaritromysiiniä: aikuisten annos on 500 mg ja lasten annos 15 mg/kg (lasten enimmäisannos on 500 mg) «2023 ESC Guidelines for the management of endocard...»1. Näistä vaihtoehdoista raskaana oleville suositellaan atsitromysiiniä. |
||||
| Toimenpiteeseen liittyvä (taulukko «Profylaksin käyttöaiheet eri toimenpiteissä potilaan infektioriskin (ks. taulukko
) mukaan eriteltynä. Profylaksia käytetään lisäksi aina, jos on suunniteltu mikrobilääkehoidon
aloittamista toimenpiteen jälkeen....»3) tai
suurentuneeseen infektioriskiin liittyvä (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) |
Aikuiset | Amoksisilliini* 2 g |
Kefaleksiini** 1,5 g |
Klindamysiini*** 600 mg |
| Lapset | Amoksisilliini 50 mg/kg (enimmäisannos 2 g) |
Kefaleksiini 50 mg/kg (enimmäisannos 1,5 g) |
Klindamysiini 20 mg/kg (enimmäisannos 600 mg) |
|
| Huomattavasti suurentuneen infektioriskin potilaat (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) | Aikuiset ja lapset | Lääkitys suun kautta tai laskimoon, erikoissairaanhoito Hoito perusterveydenhuollossa vain hoitavan lääkärin konsultaatioon perustuen. |
||
Mikrobilääkehoidon periaatteet
- Hammasperäisen infektion hoidossa ensisijaista on infektiopesäkkeen kirurginen hoito (hampaanpoisto, paiseen avaus ja tarvittaessa kanavointi), juurikanavan instrumentointi tai muu mekaaninen puhdistus. Pelkkä mikrobilääkitys ei riitä infektion hoidoksi «Seppänen L, Lemberg KK, Lauhio A, ym. Is dental tr...»42, «Brennan MT, Runyon MS, Batts JJ, ym. Odontogenic s...»96, «Rautaporras N, Uittamo J, Furuholm J, ym. Severe i...»97.
- Mikrobilääkehoito ei yleensä ole tarpeen, jos infektio saadaan paikallisesti hyvin hoidettua, merkkejä infektion paikallisesta leviämisestä tai yleistyneestä infektiosta ei ole eikä potilaan infektioriski ole suurentunut.
- Mikrobilääkehoidon tarve hammasperäisen infektion akuuttihoidon yhteydessä arvioidaan potilaan yleisoireiden, muiden sairauksien (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2), elimistössä olevien vierasesineiden, toimenpidealueen infektioasteen ja verenkierron sekä toimenpiteen luonteen ja laajuuden perusteella (taulukko «Mikrobilääkehoidon käyttöaiheet potilaan infektion vaikeusasteen ja yleisterveyden mukaan eriteltynä....»5).
- Valittavan mikrobilääkkeen tulee kattaa suun mikrobit, jotka todennäköisimmin ovat aiheuttaneet toimenpidealueen infektion, ja jotka voivat aiheuttaa etäinfektion syntymisen (ks. kappale Mikrobiologia «A2»3).
Mikrobilääkehoidon käyttöaiheet
- Mikrobilääkehoidon käyttöaiheet äkillisten hammasperäisten infektioiden yhteydessä on esitetty taulukossa «Mikrobilääkehoidon käyttöaiheet potilaan infektion vaikeusasteen ja yleisterveyden mukaan eriteltynä....»5.
| Aina, jos potilaalla on yleisoireita tai nopeasti leviävä infektio |
Hampaanpoisto tai muu äkillisen infektion hoitotoimenpide, kun hampaaseen liittyy
paise
|
| Harkittava suurentuneen ja huomattavasti suurentuneen infektioriskin potilaiden juurihoidon lisänä apikaalisessa parodontiitissa |
| Harkittava nekrotisoivien parodontaalisairauksien paikallishoidon lisänä |
Mikrobilääkehoidon toteutus
- Hammasperäisen infektion mikrobilääkehoito aloitetaan noin 60 minuuttia (30–90 minuuttia) «Ren YF, Malmstrom HS. Effectiveness of antibiotic ...»94 ennen infektiolähteeseen kohdistuvaa hammaslääketieteellistä hoitoa kerta-annosprofylaksilla (taulukko «Ensisijaiset mikrobilääkkeet kerta-annosprofylaksissa....»4).
- Hoidon kesto tulee arvioida yksilöllisesti infektion vaikeusasteen, toimenpiteen ja potilaan kudosten paranemisedellytysten perusteella. Jos infektiopesäkkeen eliminaatio onnistuu, infektiofokus saadaan tyydyttävästi hoidetuksi ja kudosten verenkierto on hyvä, 3–5 vuorokauden mittainen hoito on yleensä riittävä «Ribeiro ED, de Santana IHG, Viana MRM, ym. Optimal...»98. Jos oireet eivät selvästi lievity 3 vuorokauden kuluessa tai oireet pahenevat, on uusi arvio pikaisesti tarpeen.
- V-penisilliini ainoana mikrobilääkkeenä on terveen potilaan mikrobilääkehoidoksi yleensä riittävä «Cooper L, Stankiewicz N, Sneddon J, ym. Indication...»99, kun infektiofokus rajoittuu alveoliharjanteen alueelle ja on saatu hammaslääketieteellisellä hoidolla hyvin hoidetuksi. V-penisilliinin rinnalle hoitoon yhdistetään metronidatsoli, jos infektiopesäkettä ei saada heti hoidetuksi tyydyttävästi, on merkkejä infektion paikallisesta leviämisestä tai potilaalla on yleisoireita (taulukko «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6).
- Vakavat infektiokomplikaatiot kehittyvät yleisimmin alaposkihampaiden periapikaalisista infektioista «Furuholm J, Uittamo J, Rautaporras N, ym. Are ther...»14, mikä on lisäksi hyvä huomioida mikrobilääkityksestä päätettäessä.
- Vakavampien infektioiden hoidossa, suurentuneen ja huomattavasti suurentuneen infektioriskin potilaalle (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) tai hiljattain useita penisilliinikuureja saaneelle potilaalle ensisijaisena vaihtoehtona on amoksisilliini joko yksin tai yhdessä metronidatsolin tai klavulaanihapon kanssa (taulukko «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6). Jos potilas on yliherkkä penisilliinille (ei anafylaksia), V-penisilliini korvataan ensimmäisen polven kefalosporiinilla (taulukko «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6). Penisilliinistä anafylaktisen reaktion saaneen hoidossa käytetään ensisijaisesti klindamysiiniä. Penisilliinille allergisen potilaan vakavien infektioiden hoidossa voidaan erityistilanteessa käyttää moksifloksasiinia, jolla on raportoitu klindamysiiniä parempia hoitovasteita «Cachovan G, Böger RH, Giersdorf I, ym. Comparative...»100. Moksifloksasiinia tulee kuitenkin käyttää erityisen harkitusti mahdollisten haittavaikutusten vuoksi ja toisaalta, jotta teho säilyisi sen muissa ensisijaisissa käyttöaiheissa.
- Lasten ensisijaislääke on amoksisilliini tarvittaessa metronidatsoliin yhdistettynä. Penisillinille allergisten hoidossa amoksisilliini korvataan kefaleksiinilla (ei anafylaksia penisilliinistä). Anafylaktisen reaktion penisilliinistä saaneelle ensisijaisvaihtoehto on klindamysiini. Moksifloksasiini ei sovellu lapsille. Katso taulukko «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6.
- Parodontaali-infektioiden osalta katso suosituksen kohta Mikrobilääkkeet parodontologiassa «A5»6.
- Klooriheksidiiniä sisältävän suuhuuhteen käyttö lyhytaikaisesti on hammaslääketieteellisen hoidon yhteydessä usein aiheellista systeemisen mikrobilääkkeen lisänä.
| Ensisijaisesti | Penisilliinille allergiset (muu kuin anafylaktinen reaktio) |
Penisilliinille allergiset (anafylaktinen reaktio) |
||
|---|---|---|---|---|
| * Metronidatsolin yhdistämistä mikrobilääkehoitoon harkitaan tapauskohtaisesti. Yleensä
se on tarpeen silloin, kun infektiopesäkettä ei saada tyydyttävästi välittömästi hoidettua,
on epäily infektion paikallisesta leviämisestä alveoliharjanteen ulkopuolelle tai
kun potilaalla on yleisoireita. ** Jos V-penisilliinin ja metronidatsolin yhdistelmähoito ei ole mahdollinen, voidaan vaihtoehtoisena lääkityksenä käyttää amoksisilliini-klavulaanihappoa annoksella 500 (125) mg x 3. |
||||
| Terveet ja suurentuneen infektioriskin potilaat (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) |
Aikuiset | V-penisilliini 1 milj. IU x 3–4 +/- metronidatsoli* 400 mg x 3** | kefaleksiini 500 mg x 3 +/- metronidatsoli* 400 mg x 3 | klindamysiini 300 mg x 4 |
| Lapset | Terveet: amoksisilliini 50 mg/kg/vrk jaettuna 3 antokertaan (enimmäisannos 1500 mg/vrk) Suurentuneen infektioriskin potilaat: amoksisilliini 50 mg/kg/vrk +/- metronidatsoli* 22,5 mg/kg/vrk jaettuna 3 antokertaan (enimmäisannos 1200 mg/vrk) tai amoksisilliini-klavulaanihappo 50 (12,5) mg/kg/vrk jaettuna 3 antokertaan (enimmäisannos 2800 (400) mg/vrk) |
Terveet: kefaleksiini 50 mg/kg/vrk jaettuna 3 antokertaan (enimmäisannos 1500 mg/vrk) Suurentuneen infektioriskin potilaat: kefaleksiini 50 mg/kg/vrk +/- metronidatsoli* 22,5 mg/kg/vrk jaettuna 3 antokertaan (enimmäisannos 1200 mg/vrk) |
klindamysiini 20 mg/kg/vrk jaettuna 4 antokertaan (enimmäisannos 1200 mg/vrk) | |
| Huomattavasti suurentuneen infektioriskin potilaat (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) |
Aikuiset ja lapset | Lääkitys suun kautta tai laskimoon, erikoissairaanhoito Hoito perusterveydenhuollossa vain hoitavan lääkärin konsultaatioon perustuen |
||
Erikoisalakohtaiset suositukset
Mikrobilääkkeet suu- ja leukakirurgiassa
Profylaksi
- Mikrobilääkeprofylaksi ei ole tarpeen terveen potilaan infektoitumattoman alueen kirurgisissa toimenpiteissä, joissa komplikaatioiden ilmaantuvuus on pieni (esim. limakalvobiopsia ja tavanomainen hampaanpoisto) «Mikrobilääkeprofylaksi ei ole tarpeen terveen potilaan infektoitumattoman hampaan poistossa, jossa ei tarvita osteotomiaa.»A.
- Suu- ja leukakirurgisissa toimenpiteissä tulee suosia kerta-annosprofylaksia ja se
pitää kohdentaa niin, että huomioidaan potilaan infektioalttius, toimenpidealueen
infektioaste ja toimenpiteen vaikeus sekä mikrobilääkehistoria. Toimenpidealueen infektoitumisen
riskiä lisäävät myös alueelle kohdistunut, erityisesti suuriannoksinen, sädehoito
sekä antiresorptiiviset luustolääkkeet. Luustolääkkeiden aiheuttaman leukaluunekroosin
riski on annosriippuvainen.
- Juuri ennen toimenpidettä tai heti toimenpiteen jälkeen annettu mikrobilääkeprofylaksi ilmeisesti ehkäisee viisaudenhammaskirurgian paikallisia infektiokomplikaatioita ja ilmeisesti lisää lievien, ohimenevien haittavaikutusten (esim. gastrointestinaaliärsytys ja ihottuma) esiintyvyyttä «Mikrobilääkeprofylaksi ilmeisesti vähentää terveiden potilaiden viisaudenhammaskirurgian infektiokomplikaatioita 66 % ja lisää lievien, ohimenevien haittavaikutusten esiintyvyyttä.»B. Tämän ja kasvavan resistenssiongelman vuoksi profylaksin tarvetta tulee harkita potilaan immuunivasteen, toimenpidealueen infektioasteen ja toimenpiteen vaikeusasteen mukaan. Katsauksessa ei löydetty selvää näyttöä siitä, että mikrobilääkkeen antamisajankohdalla (juuri ennen toimenpidettä, heti toimenpiteen jälkeen tai molemmat) olisi merkitystä toimenpiteen jälkeisen paikallisen infektiokomplikaation kehittymisen kannalta.
- Mikrobilääkeprofylaksilla ei ole vaikutusta hammasimplantin asettamisen varhaisiin infektiokomplikaatioihin «Toimenpidettä edeltävästi annettu mikrobilääkeprofylaksi ei estä terveiden henkilöiden implantin varhaista menettämistä.»A.
- Muiden luuhun kajoavien suu- ja leukakirurgisten toimenpiteiden (esim. endodonttinen kirurgia ja paikalliset luusiirteet) yhteydessä annettavan mikrobilääkeprofylaksin tehosta ei ole riittävää tieteellistä näyttöä, mutta sen voidaan olettaa vähentävän infektiokomplikaatioita samalla tavalla kuin hampaanpoiston yhteydessä «Lindeboom JA, Frenken JW, Valkenburg P, ym. The ro...»101, «Lindeboom JA, Tuk JG, Kroon FH, ym. A randomized p...»102.
- Mikäli toimenpiteen luonteen tai leikkausalueen infektion vuoksi mikrobilääkitys katsotaan tarpeelliseksi toimenpiteen jälkeen, suositellaan käytettävän lyhyitä (1–3 päivän) kuureja.
- Suun kautta annosteltavat ensisijaiset mikrobilääkevaihtoehdot ovat tällöin:
- Aikuiset:
- V-penisilliini 1 milj. IU x 3–4
- kefaleksiini 500 mg x 3 (penisilliiniallergia, ei anafylaksia)
- doksisykliini aloitusannos 100 mg x 2, sen jälkeen 100 mg x 1 tai klindamysiini 300 mg x 4 (penisilliinistä anafylaksia)
- Lapset:
- amoksisilliini 50 mg/kg/vrk jaettuna 3 antokertaan
- kefaleksiini 50 mg/kg/vrk jaettuna 3 antokertaan (penisilliiniallergia, ei anafylaksia)
- klindamysiini 20 mg/kg/vrk jaettuna 4 antokertaan (penisilliinistä anafylaksia)
- Aikuiset:
Äkillisen infektion hoito
- Hammasperäisen infektion hoidossa keskeistä on infektiolähteen poistaminen. Hoito käsittää paiseen avauksen lisäksi hampaanpoiston tai juurikanavien avauksen. Pelkkä mikrobilääkitys ei riitä infektion hoidoksi «Seppänen L, Lemberg KK, Lauhio A, ym. Is dental tr...»42, «Brennan MT, Runyon MS, Batts JJ, ym. Odontogenic s...»96.
- Hammasperäisen infektion mikrobilääkehoito aloitetaan noin 60 minuuttia (30–90 minuuttia) ennen infektiolähteeseen kohdistuvaa hammaslääketieteellistä hoitoa kerta-annosprofylaksilla (taulukko «Ensisijaiset mikrobilääkkeet kerta-annosprofylaksissa....»4).
- Hoidon kesto tulee arvioida yksilöllisesti toimenpiteen ja potilaan kudosten paranemisedellytysten perusteella. Jos infektiopesäkkeen avaus onnistuu ja kudosten verenkierto on hyvä, yleensä 3–5 vuorokauden mittainen hoito riittää. Antiseptisen suuveden käyttö on aiheellista systeemisen mikrobilääkkeen lisänä.
- Äkillisen infektion hoidossa käytettävät lääkkeet on koottu taulukoon «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6.
Mikrobilääkkeet endodontiassa
Profylaksi
- Terveen potilaan juurihoidon yhteydessä ei käytetä mikrobilääkeprofylaksia. Siitä ei ole hyötyä äkillisen pulpiitin hoidossa «Mikrobilääkehoidoista ei ilmeisesti ole hyötyä eikä sitä suositella äkillisen pulpiitin hoidossa.»C, eikä se ehkäise oireettoman apikaalisen parodontiitin akutisoitumista juurikanavien avauksen ja laajennuksen yhteydessä «Penisilliini tai amoksisilliini ei ehkäise oireettoman apikaalisen parodontiitin akutisoitumista juurikanavien avauksen ja laajennuksen yhteydessä.»B.
- Juurihoitotoimenpiteissä tulee suosia kerta-annosprofylaksia ja sen valinnassa pitää huomioida potilaan infektioalttius, toimenpidealueen infektioaste sekä potilaan mikrobilääkehistoria.
- Kofferdamin käyttö juurihoidon yhteydessä on suositeltavaa «http://www.kaypahoito.fi/nak08716»8, koska se pienentää juurikanavan kontaminaatioriskiä. Tässä tulee kuitenkin huomioida, että kofferdamin asettaminen voi aiheuttaa merkittävän bakteremian, etenkin jos hammasta ympäröivä ien on tulehtunut «Sonbol H, Spratt D, Roberts GJ, ym. Prevalence, in...»75.
- Mikrobilääkehoidolla ei terveillä koehenkilöillä yleensä ole osoitettu olevan vaikutusta juurihoitotoimenpiteiden jälkeiseen kipuun tai infektion vaikeutumiseen «Penisilliini tai amoksisilliini ei ehkäise oireettoman apikaalisen parodontiitin akutisoitumista juurikanavien avauksen ja laajennuksen yhteydessä.»B.
Äkillisen infektion hoito
- Pulpiitti (ks. lisätietoaineisto «Hampaan ytimen tulehduksen keskeiset käsitteet»1):
- Hammaspulpa on ainakin osittain vitaali, mikä estää mikrobien lisääntymistä ja leviämistä elimistöön «Segura-Egea JJ, Gould K, Şen BH, ym. Antibiotics i...»103.
- Mikrobilääkehoidosta ei ilmeisesti ole hyötyä eikä sitä suositella äkillisen pulpiitin hoidossa «Mikrobilääkehoidoista ei ilmeisesti ole hyötyä eikä sitä suositella äkillisen pulpiitin hoidossa.»C. Katso Vältä viisaasti -suositus «Mikrobilääkkeet äkillisen pulpiitin hoidossa»5.
- Hoitona on ensisijaisesti hampaan korjaava hoito tai pulpan poisto ja sitä seuraava juurihoito.
- Primaarinen äkillinen apikaalinen parodontiitti:
- Mikrobilääkkeiden tehoa primaarisen äkillisen apikaalisen parodontiitin hoidossa ei ole tutkittu.
- Koska primaarisessa äkillisessä apikaalisessa parodontiitissa on juurikanavassa edelleen elävää kudosta jäljellä ainakin juuren kärkikolmanneksessa, se on infektioasteeltaan verrattavissa pulpiittiin. Mikrobilääkehoidolle ei siten ole käyttöaiheita «Segura-Egea JJ, Gould K, Şen BH, ym. Antibiotics i...»103.
- Sekundaarinen äkillinen apikaalinen parodontiitti (ks. lisätietoaineisto «Hampaan ytimen tulehduksen keskeiset käsitteet»1):
- Ensisijaisena hoitona on tulehduseritteen poistaminen hampaan juurikanavien kautta tai insisiolla. Myös hampaanpoisto voi tulla kyseeseen.
- Infektio on hampaan juurikanavassa, jossa ei tässä vaiheessa ole verenkiertoa jäljellä. Se on siten systeemisen mikrobilääkehoidon tavoittamattomissa, eikä sitä tule hoitaa yksinomaan mikrobilääkkeillä «Segura-Egea JJ, Gould K, Şen BH, ym. Antibiotics i...»103, «Matthews DC, Sutherland S, Basrani B. Emergency ma...»104.
- Mikrobilääkehoidolla ei yleensä saavuteta lisähyötyä dreneerauksen lisänä terveiden potilaiden infektion hallinnassa tai kivun lievityksessä «Juurikanavien avauksen ja laajennuksen jälkeen aloitetusta mikrobilääkehoidoista ei ilmeisesti ole hyötyä äkillisen apikaalisen parodontiitin hoidossa.»B. Katso Vältä viisaasti -suositus «Mikrobilääkkeet äkillisen apikaalisen parodontiitin hoidossa»6.
- Jos potilaalla on yleisoireita (esim. kuume, huonovointisuus, ks. taulukko «Vakavan infektion tunnusmerkit....»1), paise sijaitsee leukakulman alla tai nenä-silmäalueella tai potilaalla on selluliitti, etenevä diffuusi turvotus tai trismus, hänelle kuuluu antaa mikrobilääkitys (taulukot «Vakavan infektion tunnusmerkit....»1 ja «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6), vaikka tulehduserite saataisiinkin poistetuksi hampaan kautta tai insision avulla (tai mieluummin molempia reittejä) tai hampaanpoistolla «Segura-Egea JJ, Gould K, Şen BH, ym. Antibiotics i...»103, «Matthews DC, Sutherland S, Basrani B. Emergency ma...»104. Potilaat, joilla on vakavaan infektioon viittaavia oireita, on lähetettävä erikoissairaanhoidon päivystykseen. Mikrobilääkitys on usein aiheellinen myös sellaisen yleisoireettoman potilaan hoidossa, jolla on suurentunut tai huomattavasti suurentunut infektioriski (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2).
- Lyhyttä mikrobilääkehoitoa tulee harkita juurihoidon tukena, jos potilaalla on pitkäaikaissairauden tai sen hoidon vuoksi heikentynyt kudosvaste ja suurentunut tai huomattavasti suurentunut infektioalttius (taulukko «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6). Jos mahdollista, hoito tehdään infektioriskipotilaille vasta, kun potilaan infektioalttius on pienempi.
- Äkillisen sekundaarisen apikaalisen parodontiitin hoidosta on julkaistu useita eri mikrobilääkkeitä vertailevia tutkimuksia. Niille on yhteistä se, että yleensä mikrobilääkkeiden välillä ei vastemuuttujasta riippumatta ole kyetty osoittamaan tehoeroja ja että useimmat mikrobilääkkeiden vertailututkimukset ovat olleet menetelmällisesti tai raportoinniltaan sellaisia, ettei niistä voi luotettavasti todeta mahdollisia tehoeroja.
- V-penisilliini yhdessä metronidatsolin kanssa oli suomalaisessa tutkimuksessa «Rihtniemi L, Tjäderhane L, Kotiranta A ym. Juurika...»33 edelleen tehokas juurikanavaperäisten infektioiden empiirisessä mikrobilääkehoidossa. Myös systemaattisen katsauksen mukaan endodonttisten infektioiden mikrobit olivat herkkiä beetalaktaameille (penisilliini, amoksisilliini, kefaleksiini) «Lang PM, Jacinto RC, Dal Pizzol TS, ym. Resistance...»105. Etenkin suurentuneen infektioriskin potilaille amoksisilliinia voidaan pitää ensisijaisena vaihtoehtona V-penisilliiniin nähden, koska se imeytyy paremmin ja on tehokkaampi enterokokkeja vastaan «Rihtniemi L, Tjäderhane L, Kotiranta A ym. Juurika...»33, (taulukko «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6). Amoksisilliinin ja klavulaanihapon yhdistelmä tulee kyseeseen lähinnä vain, jos epäillään amoksisilliinille resistenttien anaerobien tai stafylokokkien osallisuutta. Penisilliiniryhmän lääkkeestä anafylaktisen allergisen reaktion saaneille potilaille ensisijainen vaihtoehto on klindamysiini «Rihtniemi L, Tjäderhane L, Kotiranta A ym. Juurika...»33, «Lang PM, Jacinto RC, Dal Pizzol TS, ym. Resistance...»105 (taulukko «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6).
- Suurentuneen tai huomattavasti suurentuneen infektioriskin potilaille (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) mikrobilääkehoitoa tulee harkita, vaikkei yleisoireita olisi. Huomattavasti suurentuneen infektioriskin potilaat on syytä hoitaa aina suu- ja leukasairauksien erikoissairaanhoidon yksikössä (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2).
Mikrobilääkkeet parodontologiassa
Profylaksi
- Mikrobilääkeprofylaksia käytetään parodontologisessa hoidossa taulukon «Profylaksin käyttöaiheet eri toimenpiteissä potilaan infektioriskin (ks. taulukko
) mukaan eriteltynä. Profylaksia käytetään lisäksi aina, jos on suunniteltu mikrobilääkehoidon
aloittamista toimenpiteen jälkeen....»3 mukaisesti.
- Toimenpidealueen laajuus ja parodontiitin vaikeusaste sekä tehtävä toimenpide vaikuttavat profylaksin tarpeeseen. Jos arvioidaan, että toimenpiteestä aiheutuva bakteremia on vähäistä ja samaa suuruusluokkaa omahoidon kanssa, profylaksia ei yleensä tarvita.
- Terveillä potilailla parodontaalikirurgiassa ei yleensä tarvita profylaksia. Mikäli toimenpiteeseen liittyy laaja osteotomia, profylaksin tarve arvioidaan tapauskohtaisesti.
- Subgingivaalinen instrumentointi voidaan toteuttaa profylaksia tarvitsevalle potilaalle kerta-annosprofylaksilla esimerkiksi noin viikon välein tehtävillä hoitokäynneillä.
Äkillisen infektion hoito
- Parodontaalipaise:
- Hoito kohdistetaan syyn mukaisesti. Parodontiittiin liittyvän paiseen ensivaiheen hoitona on märän poistaminen joko ientaskun kautta tai insisoimalla sekä kovien ja pehmeiden peitteiden poistaminen juuren pinnalta «Parodontiitti. Käypä hoito -suositus. Suomalaisen ...»106, «Herrera D, Alonso B, de Arriba L, ym. Acute period...»107. Katso myös Käypä hoito -suositus Parodontiitin kohta Parodontiittiin liittyvä paise «Parodontiitti»3 ja lisätietoaineisto «Parodontaalisten absessien luokittelu»2. Jos hampaan ennuste on toivoton, voi ensisijainen hoito olla myös hampaanpoisto «Klokkevold, P, Carranza, F. Acute Periodontal Infe...»108 (ks. Käypä hoito -suositus Parodontiitti «Parodontiitti»3).
- Mikrobilääkehoidon lisähyödystä ei ole olemassa lumekontrolloituja tutkimuksia «Leroy R, Bourgeois J, Verleye L, ym. Should system...»109. Terveen potilaan parodontiittiin liittyvän paiseen hoidossa ei yleensä tarvita mikrobilääkitystä.
- Kun kyseessä on nopeasti kasvojen alueella leviävä tulehdus tai potilaalla on diffuusia turvotusta, yleisoireita (≥ 38 °C:n kuume) tai suurentunut tai huomattavasti suurentunut infektioriski (taulukot «Vakavan infektion tunnusmerkit....»1 ja «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) tai märkää ei saada purkautumaan, käytetään parodontologisen hoidon lisäksi systeemistä mikrobilääkettä «Heitz-Mayfield LJ. Systemic antibiotics in periodo...»110, «Slots J, Research, Science and Therapy Committee. ...»111 ja potilas ohjataan erikoissairaanhoidon päivystykseen (taulukko «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6).
- Parodontiittiin liittyvän paiseen valtaosaltaan anaerobisen mikrobiston vuoksi metronidatsoli tai amoksisilliini-klavulaanihappo ovat ensisijaisia mikrobilääkevaihtoehtoja «Herrera D, Alonso B, de Arriba L, ym. Acute period...»107, «Herrera D, Roldán S, O'Connor A, ym. The periodont...»112. Penisilliinille allergisten hoidossa on käytetty klindamysiiniä tai atsitromysiiniä «Heitz-Mayfield LJ. Systemic antibiotics in periodo...»110. Jos valitaan amoksisilliini, se voidaan aloittaa suurennetulla (1 g) annoksella «Melnick, P, Takei, H. Diagnosis and Management of ...»113, «Slots J, Research, Science and Therapy Committee. ...»111.
- Akuutin vaiheen hoidon jälkeen tarkistetaan hoidon vaste.
- Nekrotisoivat parodontaalisairaudet:
- Primaarihoidon tarkoitus on saada potilas kivuttomaksi, eliminoida altistavia tekijöitä ja estää sairauden eteneminen. Akuuttihoito käsittää pseudomembraanin varovaisen poiston ja mekaanisen hoidon ikeniä ärsyttämättä. Hoitoa jatketaan 1–2 vuorokauden kuluttua «Preshaw PM. Antibiotics in the treatment of period...»114, «Holmstrup P WJ. Necrotizing periodontal disease. K...»115, «Dufty J, Gkranias N, Donos N. Necrotising Ulcerati...»116.
- Omahoitoon kuuluvat klooriheksidiiniä sisältävät suuhuuhteet «Klokkevold, P, Carranza, F. Acute Periodontal Infe...»108, «Holmstrup P WJ. Necrotizing periodontal disease. K...»115, «Hartnett AC, Shiloah J. The treatment of acute nec...»117 ja varovainen bakteeribiofilmin poisto sairaalta alueelta.
- Jos potilaalla on yleisoireita (kuume, imusolmukkeiden turvotus), mekaanisen hoidon tueksi aloitetaan mikrobilääkehoito «Holmstrup P WJ. Necrotizing periodontal disease. K...»115, «Marucha PT. Treatment of acute gingival disease. K...»118, «Ahl DR, Hilgeman JL, Snyder JD. Periodontal emerge...»119, «Johnson BD, Engel D. Acute necrotizing ulcerative ...»120.
- Laadukkaita nykykäytäntöjen mukaisia tutkimuksia mikrobilääkkeiden käytöstä nekrotisoivien parodontaalisairauksien hoidossa ei ole tehty. Mikrobilääkehoito perustuukin asiantuntijoiden kokemukseen ja suosituksiin. Hoitoon voidaan suositella metronidatsolia, amoksisilliinia, penisilliiniä tai doksisykliiniä «Herrera D, Alonso B, de Arriba L, ym. Acute period...»107, «Holmstrup P WJ. Necrotizing periodontal disease. K...»115, «Marucha PT. Treatment of acute gingival disease. K...»118, «American Academy on Pediatric Dentistry Council on...»121, «Dar-Odeh N, Atef A, Flaifl Y, ym. Evaluation of me...»122 (taulukko «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6).
- Kroonisen parodontiitin hoitoon mahdollisesti tarvittavasta mikrobilääkityksestä on ohjeet Käypä hoito -suosituksessa Parodontiitti «Parodontiitti»3, «Parodontiitti. Käypä hoito -suositus. Suomalaisen ...»106.
Mikrobilääkkeet hammasvammojen hoidossa
- Hammasvammoissa systeemisellä mikrobilääkkeellä pyritään ehkäisemään hampaan juuren tulehduksellista resorptiota tai suojaamaan suurentuneen infektioriskin potilasta trauma-alueen mikrobeilta «Hinckfuss SE, Messer LB. An evidence-based assessm...»22.
- Mikrobilääkehoidon tehosta juuren tulehduksellisen resorption ehkäisyssä tai avulsoituneen hampaan kokonaisennusteen paranemisessa ei ole vahvaa tutkimuksellista näyttöä «Hinckfuss SE, Messer LB. An evidence-based assessm...»22, «Bourgeois J, Carvalho JC, De Bruyne M, ym. Antibio...»123. Sen puuttuessa hammasvammojen yhteydessä tulee noudattaa yleisiä kansainvälisiä hoitokäytäntöjä, joiden mukaan mikrobilääkitystä tulee potilaskohtaisesti harkita lähinnä tilanteissa, joissa kuopastaan irronnut pysyvä hammas (avulsio) palautetaan paikoilleen (replantaatio). Tällöin kyseeseen tulevat V-penisilliini, amoksisilliini tai doksisykliini «Bourguignon C, Cohenca N, Lauridsen E, ym. Interna...»124, «Fouad AF, Abbott PV, Tsilingaridis G, ym. Internat...»125, «Day PF, Flores MT, O'Connell AC, ym. International...»126. Kehittyvän hampaan värjäytymisen riski doksisykliiniä käytettäessä näyttää olevan vähäinen, ja doksisykliinin käyttöä voi tapauskohtaisesti harkita yli 8-vuotiaiden lasten hoidossa «Cross R, Ling C, Day NP, ym. Revisiting doxycyclin...»127, «Pöyhönen H, Nurmi M, Peltola V, ym. Dental stainin...»128.
Mikrobilääkkeet lasten hammashoidossa
Profylaksi
- Mikrobilääkeprofylaksin käyttöaiheet ja yleisperiaatteet ovat lapsilla ja aikuisilla samat (taulukko «Ensisijaiset mikrobilääkkeet kerta-annosprofylaksissa....»4).
Äkillisen infektion hoito
- Maitohampaiden aiheuttamista infektioista suurin osa on paikallisia ja suuonteloon rajoittuvia «Leroy R, Bourgeois J, Verleye L, ym. Are systemic ...»129, «Joachim MV, Abdo M, Alkeesh K, ym. Factors associa...»130.
- Infektoituneen maitohampaan ensisijainen hoito on sen poistaminen.
- Mikrobilääkehoitoa on syytä käyttää muun hoidon tukena, jos
- terveellä lapsella on nopeasti etenevä hammasperäinen infektio, joka aiheuttaa kasvojen alueen turvotusta, kuumetta ja yleistä sairauden tunnetta
- lapsen immuunipuolustus poikkeaa normaalista joko sairauden tai sen hoidon vuoksi «American Academy of Pediatric Dentistry. Antibioti...»131, «American Academy of Pediatric Dentistry. Use of an...»132, «https://www.aapd.org/globalassets/media/policies_guidelines/bp_antibioticprophylaxis.pdf»9, «https://www.aapd.org/globalassets/media/policies_guidelines/bp_antibiotictherapy.pdf»10
- Jos lapsella on vaikeita yleisoireita (taulukko «Vakavan infektion tunnusmerkit....»1), hänet pitää lähettää erikoissairaanhoidon päivystykseen.
- Lasten hammasperäisen selluliitin hoidossa nopea kirurginen hoito lyhentää tarvittavaa sairaalahoitoa ja vähentää hoidon kustannuksia «Thikkurissy S, Rawlins JT, Kumar A, ym. Rapid trea...»133, «Kara A, Ozsurekci Y, Tekcicek M, ym. Length of hos...»134.
- Lasten aineenvaihdunta ja muun muassa elimistön vesipitoisuus poikkeavat selvästi aikuisten vastaavista, minkä vuoksi kaikkia mikrobilääkkeitä annosteltaessa tulee pitäytyä painonmukaisissa suosituksissa.
- Lasten hammasinfektioiden hoidossa käytetään pääosin samoja lääkkeitä kuin aikuistenkin. Metronidatsolin lisäämistä mikrobilääkehoitoon harkitaan tapauskohtaisesti. Metronidatsolia tarvitaan yleensä vain vaikeiden ja nopeasti etenevien infektioiden hoidossa, erityisesti silloin kun infektiopesäkettä ei saada tyydyttävästi välittömästi hoidettua, epäillään infektion leviämistä alveoliharjanteen ulkopuolelle tai potilaalla ilmenee yleisoireita, etenkin jos potilaan infektioriski on suurentunut «Ensilinjan mikrobilääkityksen (3–5 vrk) vaihtoehdot hammasperäisen infektion hoidossa....»6.
- Pienten lasten hoidossa voidaan tablettien tai kapselien sijaan käyttää nestemäistä lääkemuotoa (oraalisuspensiota).
- Tetrasykliini voi aiheuttaa kehittyvän hampaan sisäistä värjäytymistä, minkä vuoksi sen käyttöä ei suositella alle 8-vuotiaille lapsille eikä raskaana oleville «Kim SJ, Kim EH, Lee M, ym. Risk of Dental Discolor...»135, «Olson CA, Riley HD Jr. Complications of tetracycli...»136.
- Doksisykliiniä käytettäessä värjäytymisen riski näyttää olevan pieni «Cross R, Ling C, Day NP, ym. Revisiting doxycyclin...»127, «Pöyhönen H, Nurmi M, Peltola V, ym. Dental stainin...»128.
Seuranta
- Potilaan huolellinen seuranta ja selkeiden jatkohoito-ohjeiden ja yhteystietojen antaminen suullisesti ja kirjallisesti ovat suun ja leukojen alueen infektioiden hoidon yhteydessä erityisen tärkeitä, koska tilanteen kehittymistä on hyvin vaikea arvioida.
- Jos oireet eivät selvästi lievity 3 vuorokauden kuluessa tai pahenevat, on uusi arvio pikaisesti tarpeen.
- Nopeasti kehittyneissä infektioissa ensimmäinen seurantakäynti on hyvä ajoittaa 1 vuorokauden päähän, jolloin hoitovaste jo yleensä näkyy. Mikäli infektio on levinnyt nopeasti, sijaitsee alveoliharjanteen ulkopuolella tai potilaalla on yleisoireita, tulee infektion kehittymistä seurata yksilöllisen tilanteen mukaisesti.
- Varsinaisen infektion hoidon lisäksi tulee huolehtia myös potilaan kipulääkityksestä ja suuhygieniasta. Etenkin lasten ja vanhusten nesteen- ja ravinnonsaanti tulee varmistaa. Huomioitava on, että suun ja nielun alueen turvotus ja kivut haittaavat syömistä ja juomista ja saattavat vaikeuttaa myös lääkkeenottoa.
- Aloitetusta hoidosta huolimatta hammasperäinen infektio voi jatkaa leviämistä ja vaatia
myös sairaalahoitoa.
- Etu- ja kulmahammasalueiden infektiot vastaavat yleensä hyvin hammaslääkärin antamaan hoitoon.
- Poskihampaiden, etenkin alaleuan poskihampaiden, infektiot voivat levitä nopeastikin. Alaleuan poskihammasalueelta infektio leviää tyypillisesti suunpohjan kielenpuoleisiin pehmytkudoksiin, joista on suora yhteys nielua ja kaulaa ympäröiviin syviin rakenteisiin alas aina välikarsinaan saakka.
- Alaleuan aition infektio voi levitä myös suunpohjan flegmoniksi (angina Ludovici eli ns. Ludwigin angiina) ja edelleen kaulan syväksi infektioksi.
- Yläleuan poskihammasperäiset infektiot leviävät yleensä suulakeen tai poskeen, mutta ne voivat levitä myös poskionteloihin ja jopa silmäkuoppaan.
- Potilaan tulee ottaa yhteyttä toimenpiteen tehneeseen hammaslääkäriin tai päivystykseen aina, jos hänelle nousee kuume tai kehittyy muita vakavan infektion merkkejä (taulukko «Vakavan infektion tunnusmerkit....»1).
Porrastus ja työnjako
- Potilaat, joilla on äkillinen hammasperäinen infektio, tutkitaan ja hoidetaan aina viipymättä.
- Potilaat, joilla on vakavan infektion oireita (taulukko «Vakavan infektion tunnusmerkit....»1), tulee ohjata hoitoon päivystystapauksina suu- ja leukasairauksien erikoissairaanhoidon yksikköön.
- Potilaat, joilla on hammasperäisille infektiokomplikaatioille altistava sairaus tai lääkitys, tulee myös arvioida päivystyksellisesti.
- Terveiden potilaiden (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) suun alueen infektiot hoidetaan perusterveydenhuollossa. Sama koskee sellaisia suurentuneen infektioriskin potilaita (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2), joilla ei ole yleisoireita eikä infektio uhkaa hengitysteitä (taulukko «Vakavan infektion tunnusmerkit....»1). Suurentuneen infektioriskin potilaiden hoitolinjoista ja työnjaosta suositellaan tarvittaessa herkästi konsultoimaan lähialueen suu- ja leukasairauksien erikoissairaanhoidon yksikköä tai pitkäaikaissairauden hoidosta vastuussa olevaa lääkäriä.
- Septisten potilaiden (tunnistettu infektiofokus ja systeeminen elimistön vaste siihen: kuume, suurentunut syke ja hengitystaajuus) ja potilaiden, joilla on muita vakavan infektion merkkejä, hoito kuuluu aina erikoissairaanhoitoon (taulukko «Vakavan infektion tunnusmerkit....»1).
- Huomattavasti suurentuneen infektioriskin potilaiden (taulukko «Mahdollisia potilaskohtaisia infektiokomplikaatioiden riskitekijöitä. (Avaa taulukon PDF-versio tästä linkistä )...»2) ensisijainen hoitopaikka on erikoissairaanhoidossa, mutta niin sovittaessa heidän hoitonsa voidaan toteuttaa yhteistyössä perusterveydenhuollon kanssa.
Suomalaisen Lääkäriseuran Duodecimin ja Suomen Hammaslääkäriseura Apollonian asettama työryhmä
Mikrobilääkkeet hammasperäisten infektioiden hoidossa ja komplikaatioiden ehkäisyssä -suosituksen historiatiedot «Mikrobilääkkeet hammasperäisten infektioiden hoidossa ja komplikaatioiden ehkäisyssä, Käypä hoito -suosituksen historiatiedot»7
Puheenjohtaja:
Hannamari Välimaa, dosentti, suun mikrobiologian erikoishammaslääkäri, EL (kliininen mikrobiologia), kliininen opettaja; Helsingin yliopisto, erikoislääkäri; HUS suu- ja leukasairaudet, vastuulääkäri; HUS Meilahden Rokotetutkimuskeskus MeVac
Jäsenet:
Heikki Alapulli, kliinisen hammashoidon erikoishammaslääkäri, vs. apulaisylihammaslääkäri; HUS suu- ja leukasairaudet, Uusi lastensairaala
Asko Järvinen, professori, ylilääkäri; HUS infektiosairauksien klinikka
Karita Nylund, kliinisen hammashoidon erikoishammaslääkäri (parodontologia), apulaisylihammaslääkäri; HUS Pää- ja kaulakeskus, suu- ja leukasairaudet
Mataleena Parikka, HLT, immunobiologian professori; Tampereen yliopisto
Marja Pöllänen, dosentti, parodontologian erikoishammaslääkäri; Suomalainen Lääkäriseura Duodecim, Käypä hoito -toimittaja
Tero Soukka, dosentti, suu- ja leukakirurgian erikoishammaslääkäri, palvelualuejohtaja; TYKS syöpäklinikka ja pääkeskus
Leo Tjäderhane, kariologian ja endodontian professori; Helsingin yliopisto, HUS Pää- ja kaulakeskus, suu- ja leukasairaudet
Asiantuntijat:
Vesa Anttila, dosentti, sydän- ja rintaelinkirurgian erikoislääkäri, vastuualuejohtaja; TYKS Sydänkeskus kirurgia, Turku
Sakari Jokiranta, dosentti, kliinisen mikrobiologian erikoislääkäri, johtava ylilääkäri; Vita Laboratoriot Oy, Helsinki
Anna Koffert, ihotautien erikoislääkäri, haavanhoidon erityispätevyys; TYKS Ihopoliklinikka, Turku
Päivi Lintu, LT, ihotautien ja allergologian erikoislääkäri, apulaisylilääkäri; TYKS Ihopoliklinikka, Turku
Tea Nieminen, LT, lastentautien erikoislääkäri, lasten infektiolääkäri; HUS Uusi lastensairaala
Laura Pirilä, dosentti, sisätautien, reumatologian ja geriatrian erikoislääkäri, ylilääkäri, palvelualuejohtaja; TYKS Medisiininen, Turku
Pekka Porela, dosentti, sisätautien ja kardiologian erikoislääkäri; TYKS Sydänkeskus, Turku
Helena Rajala, dosentti, sisätautien ja kardiologian erikoislääkäri, vt ylilääkäri, linjajohtaja; HUS Sydän- ja keuhkokeskus, kardiologia
Kimmo Salminen, gastroenterologian ja geriatrian erikoislääkäri, ylilääkäri, vastuualuejohtaja; TYKS Vatsakeskus, Turku
Anna Vasara, dosentti, ortopedian ja traumatologian erikoislääkäri, tukielinkirurgian linjajohtaja, HUS
Sidonnaisuudet
Sidonnaisuusilmoitukset on kerätty 22.10.2025 julkaistun suosituksen laatimisen yhteydessä.
Heikki Alapulli: Sivutoimet: erikoishammaslääkäri; Mehiläinen, Töölö. Koulutustoiminta: Suomen Hammaslääkäriseura Apollonia ry, Suomen kotilääkäripalvelu Oy.
Asko Järvinen: Luentopalkkiot: Astellas, Biogen, GSK, MSD, OrionPharma, Pfizer, Sanofi, ThermoFisher, UnimedicPharma; asiantuntijapalkkio: CSL Behring. Kongressit ja seminaarit: Steripolar. Luottamustoimet terveydenhuollon alalla: puheenjohtaja, Suomen infektiolääkärit ry; hallituksen jäsen, Filha ry; president elect, Nordic Society for Clinical Microbiology and Infectious Diseases; member of board, SSAC Foundation; jäsen, STM tartuntatautien neuvottelukunta; jäsen, Lääkevahinkolautakunta ja Fine vakuutuslautakunta (lääkevahingot). Toiminta terveydenhuollon ohjaukseen pyrkivissä hankkeissa: jäsen, KELA sosiaalilääketieteellinen neuvottelukunta ja sen lääkejaosto; jäsen, STM Palko lääkejaosto; jäsen, THL kansallinen mikrobilääkeresistenssin torjunnan asiantuntijaryhmä.
Karita Nylund: Sivutoimet: parodontologi; Plusterveys. Tutkimusrahoitus: Minervasäätiö Selma och Maja-Lisa Selander, Apollonia, HUS. Luentopalkkio: Dentsply Sirona Implants, Straumann, Apollonia, ITI (International team for implantology. Luottamustoimet terveydenhuollon alalla: ITI Suomen jaos
Mataleena Parikka: Luottamustoimet terveydenhuollon alalla: hallituksen jäsen, Suomen Hammaslääkäriseura Apollonia; tieteellinen päätoimittaja, Suomen Hammaslääkärilehti ja Apollonia-lehti; hallituksen jäsen, Acta Odontologica Scandinavica Society.
Marja Pöllänen: Luentopalkkiot: Hammaslääkäriseura Apollonia, Turun hammaslääkäriseura, Denstal, Vantaan ja Keravan hyvinvointialue. Luottamustoimet terveydenhuollon alalla: jäsen, STM Palveluvalikoimaneuvosto 30.6.2023 asti; hallituksen puheenjohtaja, Meritalon Hammaslääkärit Oy.
Tero Soukka: Sivutoimet: suu- ja leukakirurgi, Oral Hammaslääkärit, Terveystalo. Luottamustoimet terveydenhuollon alalla: PALKO kuvantamisjaosto, Suun terveydenhuollon kehittämisverkoston (SUTKE) ohjausryhmä, KELA sosiaalilääketieteellinen neuvottelukunta, Valtakunnallinen uniapnean kirurgisen ja kiskohoidon työryhmä (TYKS uni- ja hengityskeskus), Suomen Hammaslääkäriliitto terveyspoliittinen valiokunta 31.12.2024 asti.
Leo Tjäderhane: Sivutoimet: ylihammaslääkäri, HUS. Luentopalkkiot: Hammaslääkäriseura Apollonia. Luottamustoimet terveydenhuollon alalla: hallituksen puheenjohtaja, Suomen Hammaslääkäriseura Apollonia.
Hanna Välimaa: Luentopalkkiot: Lääketietokeskus. Luottamustoimet terveydenhuollon alalla: asiamies, Virustautien tutkimussäätiö; varapuheenjohtaja, Suupatologian ja suulääketieteen jaosto, Suomen Hammaslääkäriseura Apollonia; asiantuntijalääkäri, Potilasvakuutuskeskus. Toiminta terveydenhuollon ohjaukseen pyrkivissä hankkeissa: Ohje suun terveydenhuollon yksiköille COVID-19-epidemian aikana, THL.
Kirjallisuusviite
Mikrobilääkkeet hammasperäisten infektioiden hoidossa ja komplikaatioiden ehkäisyssä. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Hammaslääkäriseura Apollonian asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2025 (viitattu pp.kk.vvvv). Saatavilla internetissä: www.kaypahoito.fi
Tarkemmat viittausohjeet: «http://www.kaypahoito.fi/web/kh/viittaaminen»11
Vastuun rajaus
Käypä hoito -suositukset ja Vältä viisaasti -suositukset ovat asiantuntijoiden laatimia yhteenvetoja yksittäisten sairauksien diagnostiikan ja hoidon vaikuttavuudesta. Suositukset toimivat lääkärin tai muun terveydenhuollon ammattilaisen päätöksenteon tukena hoitopäätöksiä tehtäessä. Ne eivät korvaa lääkärin tai muun terveydenhuollon ammattilaisen omaa arviota yksittäisen potilaan parhaasta mahdollisesta diagnostiikasta, hoidosta ja kuntoutuksesta hoitopäätöksiä tehtäessä.
Tiedonhakukäytäntö
Systemaattinen kirjallisuushaku on hoitosuosituksen perusta. Lue lisää artikkelista khk00007
Kirjallisuutta
- 2023 ESC Guidelines for the management of endocarditis. ESC Clinical Practice Guidelines. European Society of Cardiology 2023. https://www.escardio.org/Guidelines/Clinical-Practice-Guidelines/Endocarditis-Guidelines
- Meisgeier A, Pienkohs S, Dürrschnabel F, ym. Rising incidence of severe maxillofacial space infections in Germany. Clin Oral Investig 2024;28(5):264 «PMID: 38644434»PubMed
- Robertson DD, Smith AJ. Significant increase in hospital admissions for the management of severe dental infection in England 2000-2020. J Infect 2021;83(4):496-522 «PMID: 34289400»PubMed
- Furuholm J, Rautaporras N, Uittamo J, ym. Health status in patients hospitalised for severe odontogenic infections. Acta Odontol Scand 2021;79(6):436-442 «PMID: 33502919»PubMed
- Velhonoja J, Lääveri M, Soukka T, ym. Deep neck space infections: an upward trend and changing characteristics. Eur Arch Otorhinolaryngol 2020;277(3):863-872 «PMID: 31797041»PubMed
- Chow A. Infections of the oral cavity, neck and head. Kirjassa: Principles and practice of infectious diseases. Mandell GL, Bennett JE, Dolin R (toim.). Volume 1. 6. painos. Philadelphia: Churchill Livingstone. 2005;787-802
- Jäsberg, H, Kellokoski, J. 2021. Poski turvoksissa, suu ei aukea: akuutit hammasperäiset infektiot. Suomen Lääkärilehti 2021;76(15):937-942
- Furuholm J, Uittamo J, Rautaporras N, ym. Streptococcus anginosus: a stealthy villain in deep odontogenic abscesses. Odontology 2023;111(2):522-530 «PMID: 36346473»PubMed
- García-Cabrera E, Fernández-Hidalgo N, Almirante B, ym. Neurological complications of infective endocarditis: risk factors, outcome, and impact of cardiac surgery: a multicenter observational study. Circulation 2013;127(23):2272-84 «PMID: 23648777»PubMed
- Lee JJ, Hahn LJ, Kao TP, ym. Post-tooth extraction sepsis without locoregional infection--a population-based study in Taiwan. Oral Dis 2009;15(8):602-7 «PMID: 19619196»PubMed
- Seppänen L, Lauhio A, Lindqvist C, ym. Analysis of systemic and local odontogenic infection complications requiring hospital care. J Infect 2008;57(2):116-22 «PMID: 18649947»PubMed
- Ylijoki S, Suuronen R, Jousimies-Somer H, ym. Differences between patients with or without the need for intensive care due to severe odontogenic infections. J Oral Maxillofac Surg 2001;59(8):867-72; discussion 872-3 «PMID: 11474438»PubMed
- Søndenbroe R, Markvart M, Cort ID, ym. Patients with severe odontogenic infections receive insufficient dental treatment before hospitalization - a retrospective cross-sectional study. Acta Odontol Scand 2024;83():702-711 «PMID: 39704696»PubMed
- Furuholm J, Uittamo J, Rautaporras N, ym. Are there differences between dental diseases leading to severe odontogenic infections requiring hospitalization? A retrospective study. Quintessence Int 2022;53(6):484-491 «PMID: 35274510»PubMed
- Mahmoodi B, Weusmann J, Azaripour A, ym. Odontogenic Infections: A 1-year Retrospective Study. J Contemp Dent Pract 2015;16(4):253-8 «PMID: 26067725»PubMed
- Melnick, P, Takei, H. Diagnosis and Management of Periodontal Abscesses, kirjassa Newman and Carranza's Clinical Periodontology and Implantology, Chapter 69, 813-818.e2
- Herrera D, Roldán S, González I, ym. The periodontal abscess (I). Clinical and microbiological findings. J Clin Periodontol 2000;27(6):387-94 «PMID: 10883867»PubMed
- Herrera D, Retamal-Valdes B, Alonso B, ym. Acute periodontal lesions (periodontal abscesses and necrotizing periodontal diseases) and endo-periodontal lesions. J Clin Periodontol 2018;45 Suppl 20():S78-S94 «PMID: 29926493»PubMed
- Flores MT, Andersson L, Andreasen JO, ym. Guidelines for the management of traumatic dental injuries. I. Fractures and luxations of permanent teeth. Dent Traumatol 2007;23(2):66-71 «PMID: 17367451»PubMed
- Flores MT, Andersson L, Andreasen JO, ym. Guidelines for the management of traumatic dental injuries. II. Avulsion of permanent teeth. Dent Traumatol 2007;23(3):130-6 «PMID: 17511833»PubMed
- Flores MT, Malmgren B, Andersson L, ym. Guidelines for the management of traumatic dental injuries. III. Primary teeth. Dent Traumatol 2007;23(4):196-202 «PMID: 17635351»PubMed
- Hinckfuss SE, Messer LB. An evidence-based assessment of the clinical guidelines for replanted avulsed teeth. Part II: prescription of systemic antibiotics. Dent Traumatol 2009;25(2):158-64 «PMID: 19290893»PubMed
- Andreasen JO, Jensen SS, Schwartz O, ym. A systematic review of prophylactic antibiotics in the surgical treatment of maxillofacial fractures. J Oral Maxillofac Surg 2006;64(11):1664-8 «PMID: 17052593»PubMed
- Esposito M, Grusovin MG, Worthington HV. Interventions for replacing missing teeth: treatment of peri-implantitis. Cochrane Database Syst Rev 2012;1(1):CD004970 «PMID: 22258958»PubMed
- Siqueira JF Jr, Rôças IN. Microbiology and treatment of acute apical abscesses. Clin Microbiol Rev 2013;26(2):255-73 «PMID: 23554416»PubMed
- Lou Y, Sun Z, Ma H, ym. Odontogenic infections in the antibiotic era: approach to diagnosis, management, and prevention. Infection 2024;52(2):301-311 «PMID: 37926767»PubMed
- Lee JJ, Hahn LJ, Kao TP, ym. Post-tooth extraction sepsis without locoregional infection--a population-based study in Taiwan. Oral Dis 2009;15(8):602-7 «PMID: 19619196»PubMed
- Parahitiyawa NB, Jin LJ, Leung WK, ym. Microbiology of odontogenic bacteremia: beyond endocarditis. Clin Microbiol Rev 2009;22(1):46-64, Table of Contents «PMID: 19136433»PubMed
- Delgado, V, Marsan, N, de Waha, S ym. ESC Scientific Document Group, 2023 ESC Guidelines for the management of endocarditis: Developed by the task force on the management of endocarditis of the European Society of Cardiology (ESC) Endorsed by the European Association for Cardio-Thoracic Surgery (EACTS) and the European Association of Nuclear Medicine (EANM), European Heart Journal, Volume 44, Issue 39, 14 October 2023, Pages 3948–4042, https://doi.org/10.1093/eurheartj/ehad193
- Listgarten M, Socransky, S. Ultrastructural characteristics of a spirochete in the lesion of acute necrotizing ulcerative gingivostomatitis (Vincent's infection). Arch Oral Biol 1964;9():95-6 «PMID: 14104906»PubMed
- Loesche WJ, Syed SA, Laughon BE, ym. The bacteriology of acute necrotizing ulcerative gingivitis. J Periodontol 1982;53(4):223-30 «PMID: 6122728»PubMed
- Gmür R, Wyss C, Xue Y, ym. Gingival crevice microbiota from Chinese patients with gingivitis or necrotizing ulcerative gingivitis. Eur J Oral Sci 2004;112(1):33-41 «PMID: 14871191»PubMed
- Rihtniemi L, Tjäderhane L, Kotiranta A ym. Juurikanavien mikrobilyödökset Suomessa ja niiden merkitys. Suom Hammaslääkäril 2010;1:18-26
- Hjelm K, Seppänen L, Richardson R. Hammasperäisten paiseiden mikrobiologia. Suom Hammaslääkäril 2012;9:20-9
- WHO; Antimicrobial resistance: A global report on surveillance, 2014. https://www.who.int/drugresistance/documents/surveillancereport/en/.
- WHO: Antimicrobial resistance, 2023. https://www.who.int/news-room/fact-sheets/detail/antimicrobial-resistance
- Tamma PD, Cosgrove SE. Addressing the Appropriateness of Outpatient Antibiotic Prescribing in the United States: An Important First Step. JAMA 2016;315(17):1839-41 «PMID: 27139055»PubMed
- Maunuksela T, Huovinen P, Vuopio J. Suomessa käytetään Pohjoismaista eniten mikrobilääkkeitä avohoidossa. Suom Lääkäril 2015;36:2259-63
- Velhonoja J, Lääveri M, Soukka T, ym. Risk factors and preventive measures for severe orofacial and neck infections: a three-year observational study. BMC Oral Health 2025;25(1):136 «PMID: 39856655»PubMed
- Aksoy A, Demirkıran BB, Bora A, ym. Comprehensive evaluation of deep neck infections: A retrospective analysis of 111 cases. Laryngoscope Investig Otolaryngol 2024;9(5):e70027 «PMID: 39464792»PubMed
- Opitz D, Camerer C, Camerer DM, ym. Incidence and management of severe odontogenic infections-a retrospective analysis from 2004 to 2011. J Craniomaxillofac Surg 2015;43(2):285-9 «PMID: 25555896»PubMed
- Seppänen L, Lemberg KK, Lauhio A, ym. Is dental treatment of an infected tooth a risk factor for locally invasive spread of infection? J Oral Maxillofac Surg 2011;69(4):986-93 «PMID: 20950917»PubMed
- Dou K, Shi Y, Yang B, ym. Risk factors for life-threatening complications of head and neck space infections: A systematic review and meta-analysis. J Stomatol Oral Maxillofac Surg 2024;125(4S):101954 «PMID: 38908479»PubMed
- Grubeck-Loebenstein B, Wick G. The aging of the immune system. Adv Immunol 2002;80():243-84 «PMID: 12078483»PubMed
- Albandar JM. Aggressive and acute periodontal diseases. Periodontol 2000 2014;65(1):7-12 «PMID: 24738583»PubMed
- Yamagata K, Onizawa K, Yanagawa T, ym. A prospective study to evaluate a new dental management protocol before hematopoietic stem cell transplantation. Bone Marrow Transplant 2006;38(3):237-42 «PMID: 16850033»PubMed
- Bergmann OJ. Oral infections and septicemia in immunocompromised patients with hematologic malignancies. J Clin Microbiol 1988;26(10):2105-9 «PMID: 3182997»PubMed
- Melkos AB, Massenkeil G, Arnold R, ym. Dental treatment prior to stem cell transplantation and its influence on the posttransplantation outcome. Clin Oral Investig 2003;7(2):113-5 «PMID: 12768464»PubMed
- Elad S, Raber-Durlacher JE, Brennan MT, ym. Basic oral care for hematology-oncology patients and hematopoietic stem cell transplantation recipients: a position paper from the joint task force of the Multinational Association of Supportive Care in Cancer/International Society of Oral Oncology (MASCC/ISOO) and the European Society for Blood and Marrow Transplantation (EBMT). Support Care Cancer 2015;23(1):223-36 «PMID: 25189149»PubMed
- Bamias A, Kastritis E, Bamia C, ym. Osteonecrosis of the jaw in cancer after treatment with bisphosphonates: incidence and risk factors. J Clin Oncol 2005;23(34):8580-7 «PMID: 16314620»PubMed
- Dodson TB. The Frequency of Medication-related Osteonecrosis of the Jaw and its Associated Risk Factors. Oral Maxillofac Surg Clin North Am 2015;27(4):509-16 «PMID: 26362367»PubMed
- Klokkevold, PR, Carranza, FA. Acute Gingival Infections and Management. Kirjassa: Newman and Carranza's Clinical Periodontology and Implantology, 14. painos, 2023, p.238-250.e4
- Póvoa P, Almeida E, Moreira P, ym. C-reactive protein as an indicator of sepsis. Intensive Care Med 1998;24(10):1052-6 «PMID: 9840239»PubMed
- HUS. Mikrobilääke-hoito-opas. 2024. https://www.hus.fi/sites/default/files/2024-09/mikrobilaakehoito-opas-8_2024.pdf
- Anttila, V-J. Moniresistentit bakteerit. Helsinki: Kustannus Oy Duodecim, 2025. [online] Saatavilla internetissä (vaatii käyttäjätunnuksen): https://www.terveysportti.fi/apps/dna/ltk/article/ykt00009/search/resistentit%20bakteerit
- Anttila, V-J. MRSA (metisilliinille resistentti Staphylococcus aureus). Helsinki: Kustannus Oy Duodecim, 2024. [online]. Saatavilla internetissä (vaatii käyttäjätunnuksen): https://www.terveyskirjasto.fi/dlk00586
- Kirchner M, Mafura M, Hunt T, ym. Antimicrobial resistance characteristics and fitness of Gram-negative fecal bacteria from volunteers treated with minocycline or amoxicillin. Front Microbiol 2014;5():722 «PMID: 25566232»PubMed
- Zaura E, Brandt BW, Teixeira de Mattos MJ, ym. Same Exposure but Two Radically Different Responses to Antibiotics: Resilience of the Salivary Microbiome versus Long-Term Microbial Shifts in Feces. mBio 2015;6(6):e01693-15 «PMID: 26556275»PubMed
- Abeles SR, Jones MB, Santiago-Rodriguez TM, ym. Microbial diversity in individuals and their household contacts following typical antibiotic courses. Microbiome 2016;4(1):39 «PMID: 27473422»PubMed
- Khalil D, Hultin M, Rashid MU, ym. Oral microflora and selection of resistance after a single dose of amoxicillin. Clin Microbiol Infect 2016;22(11):949.e1-949.e4 «PMID: 27569711»PubMed
- Ugwumba CU, Adeyemo WL, Odeniyi OM, ym. Preoperative administration of 0.2% chlorhexidine mouthrinse reduces the risk of bacteraemia associated with intra-alveolar tooth extraction. J Craniomaxillofac Surg 2014;42(8):1783-8 «PMID: 25028067»PubMed
- Duvall NB, Fisher TD, Hensley D, ym. The comparative efficacy of 0.12% chlorhexidine and amoxicillin to reduce the incidence and magnitude of bacteremia during third molar extractions: a prospective, blind, randomized clinical trial. Oral Surg Oral Med Oral Pathol Oral Radiol 2013;115(6):752-63 «PMID: 23453612»PubMed
- Barbosa M, Prada-López I, Álvarez M, ym. Post-tooth extraction bacteraemia: a randomized clinical trial on the efficacy of chlorhexidine prophylaxis. PLoS One 2015;10(5):e0124249 «PMID: 25955349»PubMed
- Maharaj B, Coovadia Y, Vayej AC. A comparative study of amoxicillin, clindamycin and chlorhexidine in the prevention of post-extraction bacteraemia. Cardiovasc J Afr 2012;23(9):491-4 «PMID: 23108516»PubMed
- Arteagoitia I, Rodriguez Andrés C, Ramos E. Does chlorhexidine reduce bacteremia following tooth extraction? A systematic review and meta-analysis. PLoS One 2018;13(4):e0195592 «PMID: 29684028»PubMed
- Rajasuo A, Nyfors S, Kanervo A, ym. Bacteremia after plate removal and tooth extraction. Int J Oral Maxillofac Surg 2004;33(4):356-60 «PMID: 15145038»PubMed
- Kinane DF, Riggio MP, Walker KF, ym. Bacteraemia following periodontal procedures. J Clin Periodontol 2005;32(7):708-13 «PMID: 15966875»PubMed
- Lou Y, Sun Z, Ma H, ym. Odontogenic infections in the antibiotic era: approach to diagnosis, management, and prevention. Infection 2024;52(2):301-311 «PMID: 37926767»PubMed
- Thornhill MH, Gibson TB, Yoon F, ym. Antibiotic Prophylaxis Against Infective Endocarditis Before Invasive Dental Procedures. J Am Coll Cardiol 2022;80(11):1029-1041 «PMID: 35987887»PubMed
- Arteagoitia I, Diez A, Barbier L, ym. Efficacy of amoxicillin/clavulanic acid in preventing infectious and inflammatory complications following impacted mandibular third molar extraction. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2005;100(1):e11-8 «PMID: 15953905»PubMed
- Lacasa JM, Jiménez JA, Ferrás V, ym. Prophylaxis versus pre-emptive treatment for infective and inflammatory complications of surgical third molar removal: a randomized, double-blind, placebo-controlled, clinical trial with sustained release amoxicillin/clavulanic acid (1000/62.5 mg). Int J Oral Maxillofac Surg 2007;36(4):321-7 «PMID: 17229548»PubMed
- Halpern LR, Dodson TB. Does prophylactic administration of systemic antibiotics prevent postoperative inflammatory complications after third molar surgery? J Oral Maxillofac Surg 2007;65(2):177-85 «PMID: 17236918»PubMed
- Lee JY, Do HS, Lim JH, ym. Correlation of antibiotic prophylaxis and difficulty of extraction with postoperative inflammatory complications in the lower third molar surgery. Br J Oral Maxillofac Surg 2014;52(1):54-7 «PMID: 24029441»PubMed
- Chuang SK, Perrott DH, Susarla SM, ym. Risk factors for inflammatory complications following third molar surgery in adults. J Oral Maxillofac Surg 2008;66(11):2213-8 «PMID: 18940482»PubMed
- Sonbol H, Spratt D, Roberts GJ, ym. Prevalence, intensity and identity of bacteraemia following conservative dental procedures in children. Oral Microbiol Immunol 2009;24(3):177-82 «PMID: 19416445»PubMed
- Mougeot FK, Saunders SE, Brennan MT, ym. Associations between bacteremia from oral sources and distant-site infections: tooth brushing versus single tooth extraction. Oral Surg Oral Med Oral Pathol Oral Radiol 2015;119(4):430-5 «PMID: 25758845»PubMed
- Tomás I, Diz P, Tobías A, ym. Periodontal health status and bacteraemia from daily oral activities: systematic review/meta-analysis. J Clin Periodontol 2012;39(3):213-28 «PMID: 22092606»PubMed
- Zhang W, Daly CG, Mitchell D, ym. Incidence and magnitude of bacteraemia caused by flossing and by scaling and root planing. J Clin Periodontol 2013;40(1):41-52 «PMID: 23137266»PubMed
- Lucas VS, Gafan G, Dewhurst S, ym. Prevalence, intensity and nature of bacteraemia after toothbrushing. J Dent 2008;36(7):481-7 «PMID: 18448227»PubMed
- Lockhart PB, Brennan MT, Sasser HC, ym. Bacteremia associated with toothbrushing and dental extraction. Circulation 2008;117(24):3118-25 «PMID: 18541739»PubMed
- Forner L, Larsen T, Kilian M, ym. Incidence of bacteremia after chewing, tooth brushing and scaling in individuals with periodontal inflammation. J Clin Periodontol 2006;33(6):401-7 «PMID: 16677328»PubMed
- Martins CC, Lockhart PB, Firmino RT, ym. Bacteremia following different oral procedures: Systematic review and meta-analysis. Oral Dis 2024;30(3):846-854 «PMID: 36750413»PubMed
- Shelburne SA, Sahasrabhojane P, Saldana M, ym. Streptococcus mitis strains causing severe clinical disease in cancer patients. Emerg Infect Dis 2014;20(5):762-71 «PMID: 24750901»PubMed
- Whimbey E, Kiehn TE, Brannon P, ym. Clinical significance of colony counts in immunocompromised patients with Staphylococcus aureus bacteremia. J Infect Dis 1987;155(6):1328-30 «PMID: 3572043»PubMed
- Laine, J, Ryödi, E. Bakteeriendokardiitin ehkäisy [online]. Helsinki: Kustannus Oy Duodecim, 2022. Saatavilla internetissä (vaatii käyttöoikeuden): https://www.terveysportti.fi/apps/dna/ltk/article/ykt00136/search/endokardiitti
- Cahill TJ, Harrison JL, Jewell P, ym. Antibiotic prophylaxis for infective endocarditis: a systematic review and meta-analysis. Heart 2017;103(12):937-944 «PMID: 28213367»PubMed
- Sperotto F, France K, Gobbo M, ym. Antibiotic Prophylaxis and Infective Endocarditis Incidence Following Invasive Dental Procedures: A Systematic Review and Meta-Analysis. JAMA Cardiol 2024;9(7):599-610 «PMID: 38581643»PubMed
- Thornhill MH, Gibson TB, Yoon F, ym. Endocarditis, invasive dental procedures, and antibiotic prophylaxis efficacy in US Medicaid patients. Oral Dis 2024;30(3):1591-1605 «PMID: 37103475»PubMed
- Rutherford SJ, Glenny AM, Roberts G, ym. Antibiotic prophylaxis for preventing bacterial endocarditis following dental procedures. Cochrane Database Syst Rev 2022;5(5):CD003813 «PMID: 35536541»PubMed
- Vähäsarja, N. 2023. Antibiotic prophylaxis in dentistry for the prevention of infective endocarditis. Karolinska Institutet. https://hdl.handle.net/10616/48534
- Rademacher WMH, Walenkamp GHIM, Moojen DJF, ym. Antibiotic prophylaxis is not indicated prior to dental procedures for prevention of periprosthetic joint infections. Acta Orthop 2017;88(5):568-574 «PMID: 28639846»PubMed
- Thornhill MH, Crum A, Rex S, ym. Analysis of Prosthetic Joint Infections Following Invasive Dental Procedures in England. JAMA Netw Open 2022;5(1):e2142987 «PMID: 35044470»PubMed
- McGregor JC, Wilson GM, Gibson G, ym. The effect of antibiotic premedication on postoperative complications following dental extractions. J Public Health Dent 2024;84(4):343-350 «PMID: 39134053»PubMed
- Ren YF, Malmstrom HS. Effectiveness of antibiotic prophylaxis in third molar surgery: a meta-analysis of randomized controlled clinical trials. J Oral Maxillofac Surg 2007;65(10):1909-21 «PMID: 17884515»PubMed
- Terveysportti. Lääkkeet ja hinnat 2025. https://www.terveysportti.fi/apps/laakkeetjahinnat/
- Brennan MT, Runyon MS, Batts JJ, ym. Odontogenic signs and symptoms as predictors of odontogenic infection: a clinical trial. J Am Dent Assoc 2006;137(1):62-6 «PMID: 16457000»PubMed
- Rautaporras N, Uittamo J, Furuholm J, ym. Severe infections after teeth removal - are we doing enough in preventing them? J Clin Exp Dent 2022;14(3):e254-e262 «PMID: 35317298»PubMed
- Ribeiro ED, de Santana IHG, Viana MRM, ym. Optimal treatment time with systemic antimicrobial therapy in odontogenic infections affecting the jaws: a systematic review. BMC Oral Health 2025;25(1):253 «PMID: 39966906»PubMed
- Cooper L, Stankiewicz N, Sneddon J, ym. Indications for the use of metronidazole in the treatment of non-periodontal dental infections: a systematic review. JAC Antimicrob Resist 2022;4(4):dlac072 «PMID: 35959239»PubMed
- Cachovan G, Böger RH, Giersdorf I, ym. Comparative efficacy and safety of moxifloxacin and clindamycin in the treatment of odontogenic abscesses and inflammatory infiltrates: a phase II, double-blind, randomized trial. Antimicrob Agents Chemother 2011;55(3):1142-7 «PMID: 21173173»PubMed
- Lindeboom JA, Frenken JW, Valkenburg P, ym. The role of preoperative prophylactic antibiotic administration in periapical endodontic surgery: a randomized, prospective double-blind placebo-controlled study. Int Endod J 2005;38(12):877-81 «PMID: 16343114»PubMed
- Lindeboom JA, Tuk JG, Kroon FH, ym. A randomized prospective controlled trial of antibiotic prophylaxis in intraoral bone grafting procedures: single-dose clindamycin versus 24-hour clindamycin prophylaxis. Mund Kiefer Gesichtschir 2005;9(6):384-8 «PMID: 16270222»PubMed
- Segura-Egea JJ, Gould K, Şen BH, ym. Antibiotics in Endodontics: a review. Int Endod J 2017;50(12):1169-1184 «PMID: 28005295»PubMed
- Matthews DC, Sutherland S, Basrani B. Emergency management of acute apical abscesses in the permanent dentition: a systematic review of the literature. J Can Dent Assoc 2003;69(10):660 «PMID: 14611715»PubMed
- Lang PM, Jacinto RC, Dal Pizzol TS, ym. Resistance profiles to antimicrobial agents in bacteria isolated from acute endodontic infections: systematic review and meta-analysis. Int J Antimicrob Agents 2016;48(5):467-474 «PMID: 27742205»PubMed
- Parodontiitti. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Hammaslääkäriseura Apollonia ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2025 (viitattu 25.1.2025). Saatavilla internetissä: www.kaypahoito.fi
- Herrera D, Alonso B, de Arriba L, ym. Acute periodontal lesions. Periodontol 2000 2014;65(1):149-77 «PMID: 24738591»PubMed
- Klokkevold, P, Carranza, F. Acute Periodontal Infections and Management. Kirjassa: Newman and Carranza's Clinical Periodontology and Implantology. 14. painos. USA: St Louis, MO. Elsavier 2024, s. 435-39.
- Leroy R, Bourgeois J, Verleye L, ym. Should systemic antibiotics be prescribed in periodontal abscesses and pericoronitis? A systematic review of the literature. Eur J Oral Sci 2022;130(4):e12884 «PMID: 35781706»PubMed
- Heitz-Mayfield LJ. Systemic antibiotics in periodontal therapy. Aust Dent J 2009;54 Suppl 1():S96-101 «PMID: 19737272»PubMed
- Slots J, Research, Science and Therapy Committee. Systemic antibiotics in periodontics. J Periodontol 2004;75(11):1553-65 «PMID: 15633334»PubMed
- Herrera D, Roldán S, O'Connor A, ym. The periodontal abscess (II). Short-term clinical and microbiological efficacy of 2 systemic antibiotic regimes. J Clin Periodontol 2000;27(6):395-404 «PMID: 10883868»PubMed
- Melnick, P, Takei, H. Diagnosis and Management of Periodontal Abscesses. Kirjassa: Newman and Carranza's Clinical Periodontology and Implantology. 14. painos. USA: St Louis, MO. Elsavier 2024, s. 813-18.
- Preshaw PM. Antibiotics in the treatment of periodontitis. Dent Update 2004;31(8):448-50, 453-4, 456 «PMID: 15554049»PubMed
- Holmstrup P WJ. Necrotizing periodontal disease. Kirjassa: Clinical periodontology and implant dentistry. Lindhe J, Lang NP, Karring T (toim). Volume I, 5. painos. Blackwell Munksgaard, Oxford, UK . 2008;459-74
- Dufty J, Gkranias N, Donos N. Necrotising Ulcerative Gingivitis: A Literature Review. Oral Health Prev Dent 2017;15(4):321-327 «PMID: 28761942»PubMed
- Hartnett AC, Shiloah J. The treatment of acute necrotizing ulcerative gingivitis. Quintessence Int 1991;22(2):95-100 «PMID: 2068255»PubMed
- Marucha PT. Treatment of acute gingival disease. Kirjassa: Carranza's clinical periodontology. Newman MG, Takei HH, Klokkevold PR, Carranza FA (toim.). 10. painos. Saunders Elsevier, St. Louis, MO, USA. 2006b;706-13
- Ahl DR, Hilgeman JL, Snyder JD. Periodontal emergencies. Dent Clin North Am 1986;30(3):459-72 «PMID: 3459680»PubMed
- Johnson BD, Engel D. Acute necrotizing ulcerative gingivitis. A review of diagnosis, etiology and treatment. J Periodontol 1986;57(3):141-50 «PMID: 3514841»PubMed
- American Academy on Pediatric Dentistry Council on Clinical Affairs. Guideline on appropriate use of antibiotic therapy for pediatric dental patients. Pediatr Dent 2008;30(7 Suppl):212-4 «PMID: 19216423»PubMed
- Dar-Odeh N, Atef A, Flaifl Y, ym. Evaluation of metronidazole oral monotherapy in anaerobic oral infections. Int J Clin Pharmacol Ther 2024;62(11):517-524 «PMID: 39120079»PubMed
- Bourgeois J, Carvalho JC, De Bruyne M, ym. Antibiotics at replantation of avulsed permanent teeth? A systematic review. J Evid Based Dent Pract 2022;22(2):101706 «PMID: 35718435»PubMed
- Bourguignon C, Cohenca N, Lauridsen E, ym. International Association of Dental Traumatology guidelines for the management of traumatic dental injuries: 1. Fractures and luxations. Dent Traumatol 2020;36(4):314-330 «PMID: 32475015»PubMed
- Fouad AF, Abbott PV, Tsilingaridis G, ym. International Association of Dental Traumatology guidelines for the management of traumatic dental injuries: 2. Avulsion of permanent teeth. Dent Traumatol 2020;36(4):331-342 «PMID: 32460393»PubMed
- Day PF, Flores MT, O'Connell AC, ym. International Association of Dental Traumatology guidelines for the management of traumatic dental injuries: 3. Injuries in the primary dentition. Dent Traumatol 2020;36(4):343-359 «PMID: 32458553»PubMed
- Cross R, Ling C, Day NP, ym. Revisiting doxycycline in pregnancy and early childhood--time to rebuild its reputation? Expert Opin Drug Saf 2016;15(3):367-82 «PMID: 26680308»PubMed
- Pöyhönen H, Nurmi M, Peltola V, ym. Dental staining after doxycycline use in children. J Antimicrob Chemother 2017;72(10):2887-2890 «PMID: 29091225»PubMed
- Leroy R, Bourgeois J, Verleye L, ym. Are systemic antibiotics indicated in children presenting with an odontogenic abscess in the primary dentition? A systematic review of the literature. Clin Oral Investig 2021;25(5):2537-2544 «PMID: 33791867»PubMed
- Joachim MV, Abdo M, Alkeesh K, ym. Factors associated with prolonged hospitalizations from odontogenic infections in children. J Clin Pediatr Dent 2022;46(6):40-44 «PMID: 36624903»PubMed
- American Academy of Pediatric Dentistry. Antibiotic prophylaxis for dental patients at risk for infection. The Reference Manual of Pediatric Dentistry. Chicago, Ill.: American Academy of Pediatric Dentistry; 2022:500-6.
- American Academy of Pediatric Dentistry. Use of antibiotic therapy for pediatric dental patients. The Reference Manual of Pediatric Dentistry. Chicago, Ill.: American Academy of Pediatric Dentistry; 2024:533-7.
- Thikkurissy S, Rawlins JT, Kumar A, ym. Rapid treatment reduces hospitalization for pediatric patients with odontogenic-based cellulitis. Am J Emerg Med 2010;28(6):668-72 «PMID: 20637381»PubMed
- Kara A, Ozsurekci Y, Tekcicek M, ym. Length of hospital stay and management of facial cellulitis of odontogenic origin in children. Pediatr Dent 2014;36(1):18E-22E «PMID: 24717702»PubMed
- Kim SJ, Kim EH, Lee M, ym. Risk of Dental Discoloration and Enamel Dysplasia in Children Exposed to Tetracycline and Its Derivatives. Yonsei Med J 2022;63(12):1113-1120 «PMID: 36444547»PubMed
- Olson CA, Riley HD Jr. Complications of tetracycline therapy. J Pediatr 1966;68(5):783-91 «PMID: 5325961»PubMed


