Keuhkoahtaumatauti
Miten viitata Käypä hoito -suositukseen? «K1»1
Keskeinen sanoma
- Tehokkain tapa ehkäistä keuhkoahtaumatautia on savuttomuus.
- Diagnostiikkaa tulee parantaa, ja siihen tulee liittää tupakasta vieroitus.
- Tupakoinnin lopettaminen ja liikunta ovat keskeinen osa hoitoa.
- Lääkehoidolla vähennetään oireita, kuten rasituksessa ilmenevää hengenahdistusta, ja estetään pahenemisvaiheita.
- Liitännäissairaudet huonontavat ennustetta, ja niiden toteaminen sekä suositusten mukainen hoito ovat osa kokonaisvaltaista lähestymistapaa.
- Pitkään tupakoineiden henkilöiden keuhkoahtaumatautia voidaan seuloa oirekyselyllä ja mikrospirometrialla terveydenhuoltokäyntien yhteydessä.
- Keuhkoahtaumataudin diagnostiikka perustuu riskitekijöiden arvioon, oireisiin ja spirometriaan. Spirometriassa todetaan palautumaton obstruktio, ja avaavan lääkkeen antamisen jälkeen FEV1/FVC on < 0,7. Taudin vaikeuden luokittelevat oireet, pahenemisvaiheet ja FEV1-suureen Z-arvo.
Tiivistelmä ja potilasversio
- Suosituksen tiivistelmä «Keuhkoahtaumatauti»1 ja lyhyt abstrakti englanniksi «Chronic obstructive pulmonary disease (COPD)»2
- Suosituksen yleiskielinen potilasversio suomeksi «Keuhkoahtaumatauti – salaa etenevä kansantauti»3 ja ruotsiksi «Kroniskt obstruktiv lungsjukdom – en lömskt framskridande folksjukdom»4
Kohderyhmät ja tavoite
- Suositus on tarkoitettu perusterveydenhuoltoon (työterveyshuolto mukaan luettuna) ja erikoissairaanhoitoon. Tavoitteena on parantaa keuhkoahtaumataudin diagnostiikkaa ja luoda yhtenäinen hoito- ja seurantakäytäntö sekä tukea osaamista.
Määritelmiä
- Keuhkoahtaumatauti (Chronic Obstructive Pulmonary Disease, COPD) on yleinen estettävissä oleva sairaus, jota tulee hoitaa. Sille ovat tyypillisiä jatkuvat hengitystieoireet, etenevä ilmateiden ahtaus ja krooninen tulehdus, joka syntyy, kun ihminen hengittäessään altistuu haitallisille hiukkasille ja kaasuille «Global Strategy for the Diagnosis, Management and ...»1.
- Sairauteen vaikuttaa kolme osatekijää, joiden keskinäinen merkitys vaihtelee potilaittain:
- krooninen keuhkoputkitulehdus
- uloshengitysvirtauksen hidastuminen, joka johtuu ilmateiden ahtaumasta ja keuhkorakkuloiden tuhoutumisesta, emfyseemasta
- keuhkojen ulkopuoliset vaikutukset (ks. kohta Keuhkoahtaumataudin kokonaisvaltainen arvio «A3»2).
- Krooninen keuhkoputkitulehdus määritellään pitkäaikaiseksi limannousuksi, jota ilmenee vähintään kolmena kuukautena vuodessa ainakin kahtena peräkkäisenä vuotena, kun taustalla ei ole muuta keuhkosairautta (esim. bronkiektasiatautia eli keuhkoputkien laajentumatautia). Krooninen keuhkoputkitulehdus voi edeltää keuhkoahtaumatautia. Kroonisessa keuhkoputkitulehduksessa (ilman ahtaumaa) spirometrian tulos on normaali.
- Keuhkoputkien ahtaumassa uloshengitysvirtaus on hidastunut paitsi hengitysteiden ahtauman myös emfyseemaan liittyvän keuhkojen kimmovoimien pienenemisen vuoksi.
- Keuhkoahtaumatautiin liittyy myös keuhkojen ulkopuolisia muutoksia, joiden taustalla lienee systeeminen tulehdus «MacNee W. Systemic inflammatory biomarkers and co-...»2. Sydän- ja verisuonisairaudet, aivoverenkierron sairaudet, diabetes, verenpainetauti, psykiatriset sairaudet, suolisto- ja munuaissairaudet, osteoporoosi ja syöpä ovat keuhkoahtaumatautipotilailla yleisempiä kuin ikäkaltaistetulla väestöllä. Edenneeseen tautiin voi liittyä hauraus-raihnausoireyhtymä, jolle tyypillisiä ovat lihaskato ja laihtuminen. Taudin myötä potilaan liikkuminen vähenee ja hän kokee terveydentilansa heikoksi «Donaldson AV, Maddocks M, Martolini D ym. Muscle f...»3.
- Keuhkoahtaumataudin ilmiasu vaihtelee esimerkiksi pahenemisvaiheiden esiintymisen, kroonisen keuhkoputkitulehduksen oireiden, obstruktion ja emfyseeman vaikeusasteen sekä samanaikaisen astman tai eosinofiilimäärän mukaan. Ilmiasu vaikuttaa ennusteeseen, taudin kulkuun ja hoidon valintaan.
Epidemiologia
- Keuhkoahtaumatautia sairastaa arviolta 200 000 suomalaista. FinTerveys 2017 -kyselytutkimuksessa keuhkoahtaumatauti oli melko harvinainen työikäisillä «Koponen P, Borodulin K, Lundqvist A ym. (toim).Ter...»4. Lääkärin toteamaa keuhkoahtaumatautia raportoi sairastavansa 60–69-vuotiaista miehistä 5 % ja naisista 2 %. 80 vuotta täyttäneillä tautia sairastavien osuudet olivat 9 % ja 4 %.
- Terveys 2000 -tutkimuksessa spirometriassa todetun obstruktion perusteella keuhkoahtaumataudin esiintyvyys vuosina 2000–2001 oli miehillä 4,3 % ja naisilla 3,1 % «Vasankari TM, Impivaara O, Heliövaara M ym. No inc...»5. Keuhkoahtaumatautia oli 65–74-vuotiaista miehistä 13 %:lla, 55–64-vuotiaista 5 %:lla ja 30–54-vuotiaista 2 %:lla. Naisilla esiintyvyys oli 2–3 %.
- Helsinkiläisessä väestöotannassa vuonna 2006 esiintyvyys oli tupakoimattomilla 3 %, alle 20 askivuotta tupakoineilla 4 %, 20–29,9 askivuotta tupakoineilla 12 % ja ≥ 30 askivuotta tupakoineilla 27 % «Alpha 1-antitrypsin deficiency: memorandum from a ...»6.
- Keuhkoahtaumataudin ikävakioitu esiintyvyys on pysynyt 1990-luvulta 2000-luvulle ennallaan «Vasankari TM, Impivaara O, Heliövaara M ym. No inc...»5, «Kainu A, Pallasaho P, Piirilä P ym. Increase in pr...»7. Keuhkoahtaumatautiin sopivat oireet, kuten pitkäaikainen limainen yskä, toistuva hengitysteiden vinkuminen, rasitukseen liittyvät hengitysteiden oireet ja hengenahdistus, eivät lisääntyneet vuodesta 1996 vuoteen 2006 «Kainu A, Pallasaho P, Pietinalho A. No change in p...»8.
- THL:n tilastojen mukaan Suomessa oli vuosina 2000–2009 yhteensä 101 000 hoitojaksoa keuhkoahtaumataudin takia. Seuranta-aikana keuhkoahtaumatautipotilailla oli keskimäärin 3,4 hoitojaksoa, ja samanaikaisesti astmaa ja keuhkoahtaumatautia sairastavilla hoitojaksojen määrä oli lähes kaksinkertainen (6,0) «Andersén H, Lampela P, Nevanlinna A ym. High hospi...»9. Helsingissä vuonna 2014 keuhkoahtaumataudin vaikean pahenemisvaiheen takia vuodeosastolla hoidetuista yli 400 potilaasta 13 % menehtyi 90 päivän ja 36 % vuoden seuranta-aikana «Katajisto M, Laitinen T. Estimating the effectiven...»10.
- Suomalaisen sairaalan osastolla tai poliklinikassa hoidettujen keuhkoahtaumatautipotilaiden kohortissa kuolleisuus oli 5 vuoden seurannassa (2007–2011) 15 %. Tupakoinnin jatkaminen suurensi kuolleisuutta (12 % vs. 21 %) «Kupiainen H, Kinnula VL, Lindqvist A ym. Successfu...»11. Tilastokeskuksen mukaan Suomessa kuoli vuonna 2017 keuhkoahtaumatautiin 1 148 henkeä, joista yli kolmannes oli naisia.
Vaaratekijät
- Tupakointi on keuhkoahtaumataudin tärkein aiheuttaja. Tupakoinnin lopettaminen parantaa jo todetun taudin ennustetta «Tupakointi on keuhkoahtaumataudin tärkein aiheuttaja. Tupakoinnin lopettaminen parantaa jo todetun taudin ennustetta.»A. Tupakointi suurentaa kokonaiskuolleisuutta ja riskiä kuolla keuhkoahtaumatautiin. Riski on sitä suurempi, mitä enemmän askivuosia potilaalla on takanaan, ja tupakoinnin lopettaminen pienentää kuolleisuutta «Kupiainen H, Kinnula VL, Lindqvist A ym. Successfu...»11, «Thun MJ, Carter BD, Feskanich D ym. 50-year trends...»12, «Pirie K, Peto R, Reeves GK ym. The 21st century ha...»13.
- Mitä runsaampaa altistuminen tupakansavulle on, sitä suurempi myös keuhkoahtaumataudin vaara on.
- Keuhkoahtaumataudin yleisyys korreloi suoraan väestön tupakointitapoihin parinkymmenen vuoden viiveellä.
- Tupakointi on moniin muihin vaaratekijöihin, kuten atopiaan, pieneen syntymäpainoon ja keuhkoputkien lisääntyneeseen supistumisherkkyyteen, verrattuna hallitseva vaaratekijä.
- Ympäristön tupakansavualtistus ilmeisesti suurentaa keuhkoahtaumataudin riskiä «Ympäristön tupakansavualtistus ilmeisesti suurentaa keuhkoahtaumataudin riskiä.»B.
- Keuhkoahtaumataudin työperäiseksi syyosuudeksi arvioidaan noin 14 % «Eisner MD, Anthonisen N, Coultas D ym. An official...»14.
- Työperäinen altistuminen pölyille, kaasuille tai huuruille on yhteydessä keuhkoahtaumataudin tavallista suurempaan ilmaantuvuuteen etenkin tupakoivilla «Mehta AJ, Miedinger D, Keidel D ym. Occupational e...»15, «Trupin L, Earnest G, San Pedro M ym. The occupatio...»16, «Blanc PD, Iribarren C, Trupin L ym. Occupational e...»17, «Pallasaho P, Kainu A, Sovijärvi A ym. Combined eff...»18.
- Työperäisen altistumisen jatkuminen saattaa nopeuttaa keuhkoahtaumatautia sairastavan keuhkojen toiminnan huononemista «Harber P, Tashkin DP, Simmons M ym. Effect of occu...»19.
- Jos tupakoimattomalla tai korkeintaan 10 askivuotta tupakoineella keuhkoahtaumatautipotilaalla on takanaan pitkäkestoinen ja runsas työperäinen altistuminen orgaanisille pölyille, epäorgaanisille pölyille, kaasuille tai huuruille, voidaan keuhkoahtaumatautia epäillä työperäiseksi ja tarvittaessa käynnistää ammattitautitutkimukset «Karvala K, Leino T, Oksa P ym. Altistelähtöinen ty...»20.
- Alfa1-antitrypsiinin puutos on harvinainen keuhkoahtaumataudin (etenkin emfyseema, ZZ-genotyyppi) vaaratekijä etenkin tupakoitsijoilla «Alfa1-antitrypsiinin puutos on harvinainen keuhkoahtaumataudin (etenkin emfyseemafenotyyppi) vaaratekijä etenkin tupakoitsijoilla.»A. Se selittää noin 2 % keuhkoahtaumatautitapauksista «Gooptu B, Ekeowa UI, Lomas DA. Mechanisms of emphy...»21. Aiemmin todettu astma suurentaa keuhkoahtaumataudin esiintyvyyttä «Vasankari TM, Impivaara O, Heliövaara M ym. No inc...»5 ja ilmaantuvuutta «Pallasaho P, Kainu A, Sovijärvi A ym. Combined eff...»18.
Ehkäisy
- Tupakkatuotteiden käytön ehkäisy kaikin mahdollisin tavoin on erittäin vaikuttava keino keuhkoahtaumataudin vähentämiseksi. Aktiivista tupakoinnista kysymistä ja vieroitusta tulee toteuttaa kaikilla terveydenhuollon tasoilla ja kaikkien ammattiryhmien toimesta. Ks. lisätietoa Käypä hoito -suosituksesta Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito «Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito»5, «Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito...»22.
- Työperäistä pöly-, kaasu- ja huurualtistumista tulee välttää.
Diagnostiikka
- Keuhkoahtaumataudin diagnoosi perustuu altistushistoriaan, oireisiin ja bronkodilataation jälkeisessä spirometriassa havaittavaan keuhkoputkien ahtaumaan (obstruktioon).
Altistavien tekijöiden kartoittaminen
- Tupakkatuotteella tarkoitetaan kulutukseen sopivaa, tupakasta kokonaan tai osittain koostuvaa tuotetta. Tupakkatuotteet voidaan jakaa savuttomiin ja poltettavaksi tarkoitettuihin tupakkatuotteisiin.
- Keuhkoahtaumataudin riskitekijöistä selvitetään
- tupakointi askivuosina (päivittäin poltettujen askien määrä x tupakoinnin kesto vuosina), passiivinen tupakointi ja työperäinen altistuminen
- aiemmat hengitystieinfektiot ja astma
- suvun hengitystiesairaudet (astma, keuhkoahtaumatauti).
Oireet
- Keuhkoahtaumataudin tyypillisiä oireita ovat hengenahdistus, yskä ja limannousu «Global Strategy for the Diagnosis, Management and ...»1.
- Keuhkoahtaumataudin diagnoosia ei voi tehdä pelkästään oireiden perusteella, sillä potilas voi olla oireeton ja toisaalta oireet voivat johtua muista sairauksista «Zwar NA, Marks GB, Hermiz O ym. Predictors of accu...»23.
- Tyypilliset oireet tupakalle tai muulle vaaratekijälle altistuneella potilaalla ovat kuitenkin aihe spirometriaan ja muihin diagnostisiin tutkimuksiin.
- Keuhkoahtaumatautipotilaan oireet ja pahenemisvaiheet tulee kartoittaa, sillä ne vaikuttavat hoidon valintaan «Global Strategy for the Diagnosis, Management and ...»1.
- Ajan myötä oireet yleensä pahenevat, etenkin jos potilas tupakoi.
- Pitkälle edenneen taudin oireita ovat hengenahdistus vähäisessä rasituksessa tai levossa, yskä, laihtuminen, väsymys ja toistuvat pahenemisvaiheet «Blinderman CD, Homel P, Billings JA ym. Symptom di...»24.
Potilaan tutkiminen
- Keuhkoahtaumataudin diagnoosia ei voi tehdä pelkästään kliinisten löydösten perusteella, mutta ne voivat antaa viitteitä keuhkoahtaumataudista ja sen vaikeusasteesta «Global Strategy for the Diagnosis, Management and ...»1.
- Keuhkojen auskultaatiossa saatetaan kuulla uloshengityksen vinkunaa, rahinoita tai hengitysäänen hiljentymistä, mutta auskultaatiolöydös voi olla myös normaali.
- Vaikeaan tautimuotoon liittyvät lepohengenahdistus, hengitystaajuuden suureneminen, apuhengityslihasten käyttö, lihasmassan väheneminen ja sydämen oikean puolen vajaatoiminnan merkit.
Keuhkojen toimintakokeet
- Keuhkoahtaumataudin diagnostiikassa spirometriaan liitetään aina bronkodilataatiokoe «Sovijärvi ARA, Kainu A, Malmberg P, Guldbrand A, T...»25.
- Uloshengityksen sekuntikapasiteetin pienentynyt suhde nopeaan vitaalikapasiteettiin (FEV1/FVC) < 0,7 bronkodilataation jälkeisessä spirometriassa sopii keuhkoahtaumatautiin «Global Strategy for the Diagnosis, Management and ...»1, «LLN (lower limit of normal)»1. Lievässä obstruktiossa (FEV1/FVC 0,6–0,8) on usein biologista vaihtelua ja spirometria tulisi toistaa «Aaron SD, Tan WC, Bourbeau J ym. Diagnostic Instab...»26. Tupakoinnin lopettaneilla obstruktio saattaa hävitä usean vuoden kuluttua «Aaron SD, Tan WC, Bourbeau J ym. Diagnostic Instab...»26.
- Obstruktion vaikeus määritetään uloshengityksen sekuntikapasiteetin (FEV1) perusteella ja viitearvoina käytetään Kainun viitearvoja, joissa prosenttien tilalla ovat Z-arvot. Z-arvo ilmaisee tuloksen poikkeaman viitearvoaineiston keskihajonnan (SD) kerrannaisena «Quanjer PH, Stanojevic S, Cole TJ ym. Multi-ethnic...»27. Prosenttiarvoja käytetään toistaiseksi silloin, kun haetaan Kansaneläkelaitoksen tai muun vakuutuslaitoksen myöntämiä etuuksia. Keuhkoahtaumataudin vaikeusasteen määrityksessä obstruktion vaikeus FEV1-arvon perusteella on vain yksi osatekijä (taulukko «Keuhkoahtaumataudin kliininen vaikeusaste Suomessa...»1).
- Merkitsevä bronkodilataatiovaste (12 % ja vähintään 200 ml:n suurenema sekuntikapasiteetissa) voidaan todeta keuhkoahtaumataudissa 25–50 %:lla potilaista (ks. kohta Erotusdiagnoosi «A2»3).
| KEUHKOAHTAUMATAUDIN KLIININEN VAIKEUSASTE | |
|---|---|
| CAT-testi = COPD Assessment Test, keuhkoahtaumataudin arviointitesti FEV1 = Forced Expiratory Volume in 1 second, sekuntikapasiteetti Z-arvo = Tuloksen poikkeama viitearvoaineiston keskihajonnan (SD) kerrannaisena |
|
| Lievä |
|
| Vaikea |
|
| Erittäin vaikea |
|
Kuvantamistutkimukset
- Keuhkoahtaumatautidiagnoosia ei tehdä keuhkojen röntgenkuvauksen perusteella, mutta se kuuluu perustutkimuksiin, koska sen avulla voidaan yleensä sulkea pois muita hengitystieoireita aiheuttavia sairauksia, kuten keuhkosyöpä, tuberkuloosi, pneumonia sekä sydänsairaudet ja keuhkopussin sairaudet.
- Lievässä keuhkoahtaumataudissa keuhkojen röntgenlöydös on melkein aina normaali.
- Edenneessä taudissa radiologiset löydökset, kuten laakeat palleakaaret, tippamainen sydänvarjo, niukentunut keuhkojen ääriosien verekkyys tai emfyseemabullat, viittaavat keuhkoahtaumatautiin.
- Tietokonetomografiaa ei tarvita rutiininomaisesti keuhkoahtaumataudin diagnoosimenetelmänä, mutta sitä käytetään erikoissairaanhoidossa tarpeen mukaan ongelmatapauksissa diagnoosin tarkentamiseksi, erotusdiagnostiikassa (poikkeava röntgenkuva) sekä leikkaushoidon (keuhkojen pienennys, keuhkonsiirto) arvioinnissa «Xie X, de Jong PA, Oudkerk M ym. Morphological mea...»28.
Laboratoriotutkimukset
- Keuhkoahtaumatautidiagnoosia ei voi tehdä laboratoriokokeiden perusteella «Global Strategy for the Diagnosis, Management and ...»1.
- Laboratoriotutkimuksia käytetään muiden tautien sulkemiseen pois, akuutin infektion toteamiseen ja akuuttitilanteen arvioon taudin pahenemisvaiheen yhteydessä.
- Veren eosinofiilimäärä voi vaikuttaa kliinisen ilmiasun määritykseen ja lääkehoidon valintaan «Agusti A, Fabbri LM, Singh D ym. Inhaled corticost...»29, ja se on suositeltavaa määrittää diagnostiikkavaiheessa «Kolsum U, Southworth T, Jackson N ym. Blood eosino...»30 ja pahenemisvaiheessa ennen mahdollista systeemistä glukokortikoidia.
- Poikkeuksellisen nuorilta (alle 45-vuotiaat) tai lyhyen tupakointihistorian (alle 20 askivuotta) keuhkoahtaumatautipotilailta kannattaa määrittää seerumin alfa1-antitrypsiinipitoisuus «Alpha 1-antitrypsin deficiency: memorandum from a ...»6.
- Yskösten bakteeriviljelystä ei ole hyötyä taudin stabiilissa vaiheessa.
Keuhkoahtaumataudin kokonaisvaltainen arvio
- Oireiden ja elämänlaadun kartoittamisessa voidaan käyttää kyselylomakkeita, kuten laaja-alaisempaa CAT (COPD Assessment Test) -testiä «Jones PW, Harding G, Berry P ym. Development and f...»31, «Jones PW, Brusselle G, Dal Negro RW ym. Properties...»32 tai hengenahdistusta kartoittavaa mMRC (modified Medical Research Council dyspnea scale) -testiä «Modified Medical research council dyspnea scale (mMRC)»2.
- Keuhkoahtaumataudin vaikeusasteeseen vaikuttavat potilaan oireet, pahenemisvaiheet, ja spirometriassa todettu obstruktion vaikeusaste FEV1-mittauksen Z-arvon mukaan määritettynä (taulukko «Keuhkoahtaumataudin kliininen vaikeusaste Suomessa...»1).
- Keuhkojen ulkopuoliset muutokset sekä liitännäissairaudet, kuten sydän- ja verisuonisairaudet, metabolinen oireyhtymä ja masennus, ovat keuhkoahtaumatautipotilailla yleisempiä kuin muilla samanikäisillä yhtä kauan tupakoineilla.
- Ravitsemustila, erityisesti laihtuminen, kartoitetaan.
- Suorituskykyä arvioidaan vähintään kysymällä potilaan arviota esimerkiksi siitä, kuinka hyvin hän kykenee nousemaan portaita tai kuinka pitkän matkan hän jaksaa kävellä. Tarvittaessa suorituskyky testataan tarkemmin esimerkiksi 6 minuutin kävelytestillä tai rasitusergometrilla.
- Toimintakykyä arvioidaan vähintään kysymällä potilaan harrastuksista, kotiaskareista, raskaista töistä suoriutumisesta ja työstä poissaoloista.
Erotusdiagnoosi
- Yleisimpiä erotusdiagnostisia sairauksia ovat astma, krooninen keuhkoputkitulehdus, hengitystieinfektiot ja sydänsairaudet.
- Muista keuhkosairauksista on hyvä muistaa keuhkosyöpä, tuberkuloosi, keuhkoparenkyymin sairaudet ja bronkiektasiatauti.
- Yleinen ongelma on erottaa toisistaan keuhkoahtaumatauti ja astma. Vaikka molempia hoidetaan osittain samoilla lääkkeillä, ne ovat kuitenkin etiologialtaan, perusmekanismeiltaan, taudinkulultaan ja ennusteeltaan erilaisia sairauksia.
- Keuhkoahtaumataudin ja astman samanaikainen esiintyminen on tavallista. Erityisesti tupakoivalla astmaatikolla hengitystietulehdus ja hoitovaste muuttuvat keuhkoahtaumataudin suuntaan.
- Eräitä keuhkoahtaumataudin ja astman eroja on esitetty Käypä hoito -suosituksen Astma taulukossa 2 Astman ja keuhkoahtaumataudin eroja «Astma»6, «Astma. Käypä hoito -suositus. Suomalaisen Lääkäris...»33.
- Astman ja keuhkoahtaumataudin erotusdiagnostiikkaan eivät riitä pelkät keuhkofunktiomittaukset, vaan siinä pitää aina ottaa huomioon myös tupakointi- ja oirehistoria, liitännäissairaudet ja sukutausta «Global Strategy for the Diagnosis, Management and ...»1, «Global strategy for asthma management and preventi...»34.
- Bronkodilataatiokokeella ei voida luotettavasti erottaa astmaa keuhkoahtaumataudista «Global Strategy for the Diagnosis, Management and ...»1, koska astmapotilailla ei näy bronkodilataatiovastetta joka mittauskerralla ja toisaalta noin 25–50 %:lla keuhkoahtaumatautipotilaista on merkitsevä bronkodilataatiovaste «Calverley PM, Burge PS, Spencer S ym. Bronchodilat...»35, «Tashkin DP, Celli B, Decramer M ym. Bronchodilator...»36, «Albert P, Agusti A, Edwards L ym. Bronchodilator r...»37.
- Glukokortikoidihoitokoe (kortisonihoitokoe) ei myöskään aina erota astmaa keuhkoahtaumataudista «Broekhuizen BD, Sachs AP, Moons KG ym. Diagnostic ...»38, koska myös keuhkoahtaumatautipotilaista huomattava osa hyötyy glukokortikoidista «Callahan CM, Dittus RS, Katz BP. Oral corticostero...»39 ja toisaalta jotkut astmapotilaat eivät juuri reagoi pelkkään glukokortikoidihoitoon «Woolcock AJ. Corticosteroid-resistant asthma. Defi...»40.
- Koska keuhkoahtaumataudissa vaste suun kautta otettavaan kortisoniin ei ennusta vastetta inhaloitavaan glukokortikoidiin «Burge PS, Calverley PM, Jones PW ym. Prednisolone ...»41, «Chavannes NH, Schermer TR, Wouters EF ym. Predicti...»42, mahdollinen glukokortikoidihoitokoe kannattaa tehdä keskisuuren (tai suuren) annoksen inhaloitavaa glukortikoidia sisältävällä valmisteella (4–)8 viikon ajan.
- Jos lääkehoito normalisoi keuhkojen toiminnan, kyseessä on astma eikä keuhkoahtaumatauti. Jos taas keuhkofunktio ei parane tai se paranee vain vähän eikä normalisoidu, kyseessä on todennäköisemmin keuhkoahtaumatauti kuin astma.
Keuhkoahtaumataudin seulonta terveydenhuoltokäynnin yhteydessä
- Pitkään tupakoineiden osalta suositellaan, että keuhkoahtaumataudin mahdollisuus huomioidaan terveydenhuoltokäyntien yhteydessä teettämällä oirekysely, mikrospirometria tai spirometriatutkimus. Lievän ja oireettoman keuhkoahtaumataudin seulonnasta ei ole osoitettu terveyshyötyä. Kun seulontaan yhdistetään tehokas tupakasta vieroitus ja oireisten potilaiden hoito, seulonnasta saavutetaan paras hyöty.
- Kansainvälisesti on tutkittu useita keuhkoahtaumataudin seulontaan kehitettyjä kyselylomakkeita «Price DB, Tinkelman DG, Halbert RJ ym. Symptom-bas...»43, «Martinez FJ, Raczek AE, Seifer FD ym. Development ...»44 ja lyhennettyä CAT-testiä «Martinez CH, Murray S, Barr G ym. Respiratory Symp...»45.
- Mikrospirometria on ilmeisesti keuhkoahtaumataudin seulonnassa sensitiivisempi ja spesifisempi kuin oirekysely «Mikrospirometria on ilmeisesti keuhkoahtaumataudin seulonnassa sensitiivisempi ja spesifisempi kuin oirekysely.»B, «Rytila P, Helin T, Kinnula V. The use of microspir...»46, «Frith P, Crockett A, Beilby J ym. Simplified COPD ...»47, «Sichletidis L, Spyratos D, Papaioannou M ym. A com...»48, «Haroon S, Jordan R, Takwoingi Y ym. Diagnostic acc...»49, «Yawn BP, Duvall K, Peabody J ym. The impact of scr...»50.
- Pölyille, kaasuille ja huuruille altistuneiden työntekijöiden terveystarkastusten yhteydessä suositellaan hengitystieoireiden kartoittamista ja seulonnan perusteella oireisille työntekijöille tehdään spirometria ja bronkodilataatiokoe «Karvala K, Leino T, Oksa P ym. Altistelähtöinen ty...»20.
Hoidon tavoitteet
- Keuhkoahtaumataudin hoidon tavoitteina ovat
- oireiden ja elämänlaadun paraneminen
- taudin etenemisen hidastuminen
- pahenemisvaiheiden ehkäiseminen
- kuolleisuuden pieneneminen
- liitännäissairauksien huomioiminen ja hoito (ks. edellä kohdassa Keuhkoahtaumataudin kokonaisvaltainen arvio «A3»2)
- potilaan jatkuva tukeminen sairauden kanssa pärjäämiseksi (omahoito ja hoitoon sitoutuminen)
- oikea-aikainen elämän loppuvaiheen hoitosuunnitelman tekeminen.
Kokonaisvaltainen hoito
- Lääkkeettömään hoitoon kuuluvat tupakasta vieroitus, liikkumiseen kannustaminen ja liikunnallinen kuntoutus.
- Tehokas tupakasta vieroitus on keskeinen osa keuhkoahtaumataudin pitkäaikaishoitoa. Ks. Käypä hoito -suositus Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito «Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito»5, «Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito...»22.
Ohjattu omahoito
- Keuhkoahtaumatautipotilaan omahoidolla tarkoitetaan hänen osallistumistaan oman hoitonsa suunnitteluun ja toteutukseen terveydenhuollon ammattilaisten tukemana.
- Omahoitoon kuuluvat oman voinnin seuraaminen ja oireiden tunnistaminen, säännöllinen lääkkeiden otto sekä lääkityksen sääteleminen lääkäriltä saatujen ohjeiden mukaan infektioiden ja pahenemisvaiheiden yhteydessä.
- Yksilöllinen toimintasuunnitelma sisältää valmiiksi varalle kirjoitetut glukokortikoidi- ja antibioottireseptit sekä selkeät (kirjalliset) toimintaohjeet. Osalle potilaista omahoito sopii hyvin, mutta heikentyvän voinnin taustalla voi olla myös muita syitä, jotka jäävät tällöin toteamatta.
- Ohjattu omahoito, joka sisältää yksilöllisen toimintasuunnitelman pahenemisvaiheita varten, luultavasti pienentää hengitysongelmasta johtuvan sairaalahoidon riskiä ja parantaa elämänlaatua «Ohjattu omahoito, joka sisältää yksilöllisen toimintasuunnitelman pahenemisvaiheessa luultavasti vähentää hengitysongelmasta johtuvan sairaalahoidon riskiä ja parantaa elämänlaatua.»B.
- Edelleenkään ei ole näyttöä siitä, että omahoidon avulla voitaisiin vähentää päivystyskäyntejä ja pienentää pahenemisvaiheiden esiintyvyyttä ja kuolleisuutta.
Liikunnallinen kuntoutus
- Fyysinen inaktiivisuus mahdollisena huonomman ennusteen riskitekijänä tulisi selvittää jokaisen keuhkoahtaumatautipotilaan osalta, ja siihen tulisi puuttua neuvonnalla, ohjauksella ja tarvittaessa tarjoamalla liikunnallista kuntoutusta.
- Liikunnallinen kuntoutus vähentää merkittävästi hengenahdistusta ja voimattomuutta, lieventää depressiota ja ahdistuneisuutta, parantaa fyysistä suorituskykyä ja pienentää sairaalahoitoon joutumisen ja kuoleman riskiä. Liikunnallinen kuntoutus on ilmeisesti hyödyksi myös lievässä keuhkoahtaumataudissa, jos potilaan suorituskyky on heikentynyt «Liikunnallinen kuntoutus on ilmeisesti hyödyksi myös lievässä keuhkoahtaumataudissa, jos potilaan suorituskyky on heikentynyt.»B.
- Keuhkoahtaumatautipotilaan kuntoutuksen tulee perustua tavoitteelliseen liikuntaharjoitteluun ja tähdätä pysyvästi aktiivisempaan elämäntapaan. Liikunnallinen kuntoutus parantaa keuhkoahtaumatautipotilaan suorituskykyä ja vähentää oireita sekä pahenemisvaiheita «Keuhkoahtaumatautipotilaan kuntoutuksen tulee perustua tavoitteelliseen liikuntaharjoitteluun ja tähdätä pysyvästi aktiivisempaan elämäntapaan. Liikunnallinen kuntoutus parantaa keuhkoahtaumapotilaan suorituskykyä ja vähentää oireita sekä pahenemisvaiheita.»A.
- Liikuntaharjoitteluun perustuvaan kuntoutukseen tulee ohjata potilaat, joilla asianmukaisesta
lääkehoidosta huolimatta on jatkuvasti oireita tai jotka kärsivät suorituskyvyn heikkenemisestä
tai liikkuvat vähän.
- Liikunnallinen kuntoutus on mielekkäintä järjestää ryhmämuotoisena avokuntoutuksena «Bolton CE, Bevan-Smith EF, Blakey JD ym. British T...»51. Vain poikkeustilanteissa se kannattaa järjestää potilaan kotona tai laitoksessa.
- Liikunnallisen keuhkokuntoutuksen tulee sisältää ohjattua monipuolista liikuntaharjoittelua, esimerkiksi kuntosaliharjoittelua, ryhmävoimistelua tai vesiliikuntaa, kaikkiaan 45–90 minuuttia kolmesti viikossa, joista vähintään kahdesti ohjattuna. Kuntoutusjakson tulee kestää 6–12 viikkoa, ja kuntoutujien yksilölliset mieltymykset tulee pyrkiä huomioimaan.
- Kova harjoittelu tuo enemmän tulosta, mutta se myös lisää keskeytyksiä. Sopiva harjoittelutaso on 60–80 % oireen rajoittamasta suoritustasosta.
- Harjoittelun tulee sisältää lihaskuntoa parantavia harjoituksia ja kestävyysharjoittelua.
- Tietoa keuhkoahtaumataudista ja ohjausta omahoitoon on hyvä tarjota kuntoutuskurssin osana.
- Liikunnallisen keuhkokuntoutuksen tulokset tulee mitata vähintään suorituskykytestillä ja oirekyselyllä mutta mielellään myös elämänlaatukyselyn avulla.
- Tavoitteena ovat pysyvät liikuntatottumukset ja aktiivisempi elämä. (Ks. käytännön ohje liikunnallisen keuhkokuntoutuksen järjestämisestä Keuhkosairaudet – Diagnostiikka ja hoito -oppikirjasta) «Katajisto M, Laitinen T. Keuhkopotilaan kuntoutus....»52.
- Toistuvat pahenemisvaiheet invalidisoivat potilasta nopeasti. Liikunnallinen kuntoutus myös heti keuhkoahtaumataudin pahenemisvaiheen jälkeen on turvallista ja pienentää uuden sairaalahoidon ja kuoleman riskiä «Liikunnallinen kuntoutus myös heti keuhkoahtaumataudin pahenemisvaiheen jälkeen on turvallista ja pienentää uuden sairaalahoidon ja kuoleman riskiä.»A. Liikunnallista keuhkokuntoutusta tulisi tarjota toistuvista pahenemisvaiheista kärsiville.
- Rasitushypoksemian korjaaminen rasituksenaikaisella happilisällä saattaa parantaa yksittäisen harjoitussuorituksen tulosta silloinkin, kun pysyvää happihoitokriteerit täyttävää hypoksemiaa eli valtimoveren hapenpuutetta ei ole kehittynyt, mutta tutkimusnäyttöä rasituksenaikaisen happilisän hyödystä pidemmällä aikavälillä ei ole «Rasitushypoksemian korjaaminen rasituksenaikaisella happilisällä saattaa parantaa yksittäisen harjoitussuorituksen tulosta silloinkin, kun pysyvää happihoitokriteerit täyttävää hypoksemiaa eli valtimoveren hapenpuutetta ei ole kehittynyt, mutta tutkimusnäyttöä rasituksenaikaisen happilisän hyödystä pidemmällä aikavälillä ei ole.»C.
- Lisähapesta rasituksessa käytettäväksi ei ole hyötyä, elleivät pitkäaikaisen happihoidon kriteerit täyty «Lisähapesta rasituksessa käytettäväksi ei ole hyötyä, jos pitkäaikaisen happihoidon kriteerit eivät täyty.»A.
- Potilasohjaus, perheenjäsenten neuvonta ja potilaan psykososiaalinen tukeminen on katsottu oleelliseksi osaksi keuhkoahtaumatautipotilaiden kuntoutusta, mutta näyttö niiden itsenäisestä vaikutuksesta kuntoutuksen tulokseen on melko vähäinen «Potilasohjaus, perheenjäsenten neuvonta ja potilaan psykososiaalinen tukeminen on katsottu oleelliseksi osaksi keuhkoahtaumapotilaiden kuntoutusta, mutta näyttö niiden itsenäisestä vaikutuksesta kuntoutuksen tulokseen on melko vähäinen.»C «Gallefoss F, Bakke PS, Rsgaard PK. Quality of life...»53.
Ravitsemustilan huomioiminen
- Sairaalaan tai kuntoutuslaitokseen joutuneista vaikeaa keuhkoahtaumatautia sairastavista 25 % kärsii aliravitsemuksesta ja katabolisesta aineenvaihdunnasta. Huono ravitsemustila lisää akuutin hengitysvajauksen vaaraa ja ennustaa respiraattorihoidon tarvetta. Erityisruokavaliosta ei kuitenkaan ole hyötyä «Ferreira IM, Brooks D, Lacasse Y ym. Nutritional s...»54. Anabolisesti vaikuttavilla lääkeaineilla voidaan lisätä potilaiden lihasmassaa, mutta näyttöä niiden vaikutuksesta suorituskykyyn tai ennusteeseen ei ole.
- Jos keuhkoahtaumatautipotilaan BMI (Body Mass Index) on alle 21, kyseessä on jo aliravitsemustila. Normaalipainoisen tai hoikan potilaan tahaton yli 10 %:n laihtuminen viimeisen puolen vuoden aikana voi olla merkki riittämättömästä energiansaannista tai hengityslihasten lisääntyneen hapenkulutuksen aiheuttamasta lisääntyneestä energiankulutuksesta. Aliravittujen keuhkoahtaumatautipotilaiden paino ilmeisesti nousee kalori- ja proteiinipitoisten ja useimmiten myös hivenaineita ja vitamiineja sisältävien lisäravinteiden avulla, ja niiden käyttöä voi harkita, ellei ravitsemusta muutoin saada korjatuksi «Aliravittujen keuhkoahtaumatautipotilaiden paino ilmeisesti nousee kalori- ja proteiinipitoisten ja useimmiten myös hivenaineita ja vitamiineja sisältävien lisäravinteiden avulla ja niiden käyttöä voidaan harkita, ellei ravitsemusta muutoin saada korjatuksi.»B.
- Merkittävästi keskivartalolihavien keuhkoahtaumatautipotilaiden on syytä laihduttaa.
Rokotukset
- Yli 65-vuotiailla influenssarokotuksen on todettu yleisesti estävän keuhkokuumeita, sairaalahoitoja ja kuolemia 50–68 %. Suuri osa keuhkoahtaumatautipotilaista kuuluu juuri tähän ikäryhmään. Influenssarokote vähentää keuhkoahtaumataudin pahenemisvaiheita «Influenssarokote vähentää keuhkoahtaumataudin pahenemisvaiheita.»A. Vuosittaista influenssarokotusta suositellaan kaikille keuhkoahtaumatautia sairastaville.
- Pneumokokkirokote ilmeisesti vähentää keuhkokuumeita ja pahenemisvaiheita keuhkoahtaumatautipotilailla «Pneumokokkirokote ilmeisesti vähentää keuhkokuumeita ja pahenemisvaiheita keuhkoahtaumatautipotilailla.»B. Pneumokokkirokotusta suositellaan kaikille keuhkoahtaumatautipotilaille.
- Krooninen keuhkosairaus -riskiryhmälle THL suosittelee ensisijaisesti konjugaattirokotetta. 13-valenttinen konjugaattirokote estää ikääntyneillä vakavaa pneumokokkitautia ja keuhkokuumetta «https://thl.fi/fi/web/rokottaminen/rokotteet/pneumokokkirokote/riskiryhmien-pneumokokkirokotukset»1
Keuhkoahtaumataudin lääkehoito
Säännöllisen pitkäaikaisen lääkehoidon periaatteet
- Lääkehoidon tarkoituksena on vähentää potilaan oireita ja pahenemisvaiheiden ilmaantuvuutta. Tietyn lääkeaineen käytön peruste voi olla kumpi tahansa tavoitteista tai molemmat tavoitteet yhdessä, ja lääkityksen jatkamista tai lopettamista arvioidaan sen mukaan, minkä tavoitteen täyttymistä tavoitellaan (kuva «Keuhkoahtaumataudin hoidon tavoitteet, niiden saavuttamiseksi käytössä olevat lääkkeet ja lääkityksen jatkamisen periaatteet»1).
- Jos lääkehoito on aloitettu pahenemisvaiheiden vähentämiseksi, sitä jatketaan, vaikkei oireiden tai keuhkojen toiminnan todettaisi parantuneen. Keuhkoahtaumataudin hoidossa käytettävät inhaloitavat lääkeaineryhmät ja lääkeaineet luetellaan taulukossa «Keuhkoahtaumataudin hoidossa käytettävät lääkeaineet ryhmiteltyinä vaikutuksensa ja sen keston mukaan sekä lääkkeiden yhteiskäytön periaatteet...»2.
- Tupakoinnin lopettamisen, liikunnan ja lääkkeiden vaikutuksia kuvataan taulukossa «Tupakoinnin lopettamisen, liikunnan ja keuhkoahtaumataudin hoidossa käytettävien lääkkeiden vaikutuksia keuhkoahtaumataudissa...»3 ja tavallisimpia lääkkeiden käyttöön liittyviä näkökohtia ja haittavaikutuksia kohdassa Keuhkoahtaumataudin pitkäaikaisessa hoidossa käytettävät lääkkeet.
- Keuhkoahtaumataudin lääkehoito ja sen valinta pohjautuvat potilaan yksilölliseen sairauden ilmiasuun, oireiden määrään ja pahenemisvaiheriskiin. Potilaiden luokittelu eri ryhmiin lääkehoidon pohjaksi esitetään kuvassa «Keuhkoahtaumataudin diagnostiikka ja arviointi sekä ilmiasun ja hoidon määräytyminen»2.
- Ilmiasu ja sen mukainen lääkehoito tulee arvioida uudelleen jokaisen seurantakäynnin yhteydessä «Keuhkoahtaumataudin diagnostiikka ja arviointi sekä ilmiasun ja hoidon määräytyminen»2, koska ilmiasu saattaa taudin edetessä muuttua (erityisesti pahenemisvaiheiden riskin osalta) «Agusti A, Edwards LD, Celli B ym. Characteristics,...»55.
- Toistaiseksi minkään lääkehoidon ei ole varmasti osoitettu vaikuttavan taudin etenemiseen (vuotuinen FEV1:n pieneneminen) tai kuolleisuuteen «Decramer M, Celli B, Kesten S ym. Effect of tiotro...»56, «Jenkins CR, Jones PW, Calverley PM ym. Efficacy of...»57, «Burge PS, Calverley PM, Jones PW ym. Randomised, d...»58, «Celli BR, Thomas NE, Anderson JA ym. Effect of pha...»59, «Anthonisen NR, Connett JE, Kiley JP ym. Effects of...»60, «Pauwels RA, Löfdahl CG, Laitinen LA ym. Long-term ...»61, «Vestbo J, Sørensen T, Lange P ym. Long-term effect...»62, mutta viitteitä asiasta on julkaistu «Lipson DA, Barnhart F, Brealey N ym. Once-Daily Si...»63.
- Lääkkeiden yhdistämisen periaatteet kuvataan taulukossa «Keuhkoahtaumataudin hoidossa käytettävät lääkeaineet ryhmiteltyinä vaikutuksensa ja sen keston mukaan sekä lääkkeiden yhteiskäytön periaatteet...»2, «O'Donnell DE, Sciurba F, Celli B ym. Effect of flu...»67.
- Tarvittaessa otettava lyhytvaikutteinen avaava lääke on tarpeellinen useimmille potilaille tilanteessa, jossa peruslääkityksenä on pitkävaikutteinen avaava tai niiden yhdistelmä.
- Tämän lääkehoitosuosituksen perusteista ja taustalla olevien kliinisten tutkimusten ominaisuuksista on kerätty selittävä osio lisätietoaineistoon «Keuhkoahtaumataudin lääkehoidosta»3.
| Jos kliiniset indikaatiot puoltavat seuraavien lääkeaineryhmien yhdistämistä, siihen ei ole farmakologista estettä. Samalle potilaalle valitaan kustakin lääkeaineryhmästä vain yksi käytettävä lääkeaine. Huomioi kiinteiden yhdistelmävalmisteiden tapauksessa (ICS + LABA, LABA + LAMA, ICS + LABA + LAMA), ettei niiden rinnalle valita samoista ryhmistä toisia lääkeaineita. Lyhytvaikutteisen ja pitkävaikutteisen beeta2-agonistin yhdistämisessä ei yleensä ole ongelmia, mutta lyhytvaikutteisen ja pitkävaikutteisen antikolinergin yhdistäminen voi lisätä haittavaikutusten riskiä. |
|---|
Lyhytvaikutteiset beeta2-agonistit (Short-acting β2-agonists (SABA)):
|
Lyhytvaikutteiset antikolinergit (Short-acting muscarinic antagonist (SAMA)):
|
Pitkävaikutteiset beeta2-agonistit (Long-acting β2-agonist (LABA)):
|
Pitkävaikutteiset antikolinergit (Long-acting muscarinic antagonist (LAMA)):
|
Hengitettävät glukokortikoidit (Inhaled corticosteroids (ICS)) yhdistelmävalmisteissa:
|
Suun kautta otettavat:
|
| * Kiinteät kombinaatiot ICS + LABA tai ICS + LABA + LAMA. ** Lyhytvaikutteisen ja pitkävaikutteisen antikolinergin yhdistäminen voi lisätä haittavaikutusten riskiä (ks. tarkemmin kohta Keuhkoputkia avaavien lääkkeiden yhdistäminen «A1»4). |
| Tupakoinnin lopettaminen | Liikunta | Lyhytvaikutteinen avaava (beeta2-agonisti tai antikolinergi) | Pitkävaikutteinen beeta2-agonisti | Pitkävaikutteinen antikolinergi | Inhalaatiosteroidin lisääminen vaikeassa keuhkoahtaumataudissa * | Roflumilasti vaikeassa keuhkoahtaumataudissa | |
|---|---|---|---|---|---|---|---|
| + Selvä suotuisa vaikutus (+) Vähäinen tai mahdollinen suotuisa vaikutus - Ei vaikutusta ? Ei tutkittua tietoa * Käytännössä tarkoittaa useimmiten yhden tai kahden pitkävaikutteisen avaavan vaihtamista inhalaatiosteroidia sisältävään ns. kombinaatiovalmisteeseen |
|||||||
| Oireet | + | + | + | + | + | (+) | - |
| Obstruktion lievittyminen | + | - | + | + | + | (+) | (+) |
| Pahenemisvaiheiden väheneminen | + | + | - | + | + | + | + |
| Taudin eteneminen (vuosittainen FEV1:n pieneneminen) | + | ? | - | - | - | (+) | ? |
| Kuolleisuus | + | + | - | - | - | (+) | ? |

Keuhkoahtaumataudin hoidon tavoitteet, niiden saavuttamiseksi käytössä olevat lääkkeet ja lääkityksen jatkamisen periaatteet.
SABA = lyhytvaikutteinen beeta2-agonisti, SAMA = lyhytvaikutteinen antikolinergi, LABA = pitkävaikutteinen beeta2-agonisti, LAMA = pitkävaikutteinen antikolinergi, ICS = inhaloitava glukokortikoidi, CAT = COPD Assessment Test, FEV1 = sekuntikapasiteetti, FVC = nopea vitaalikapasiteetti, PEF = uloshengityksen huippuvirtaus.
© Suomalainen Lääkäriseura Duodecim

Keuhkoahtaumataudin diagnostiikka ja arviointi sekä ilmiasun ja hoidon määräytyminen.
SABA = lyhytvaikutteinen beeta2-agonisti, SAMA = lyhytvaikutteinen antikolinergi, LABA = pitkävaikutteinen beeta2-agonisti, LAMA = pitkävaikutteinen antikolinergi, ICS = inhaloitava glukokortikoidi, CAT= COPD Assessment Test, FEV1 = sekuntikapasiteetti.
PDF-versio «hoi06040a.pdf»
© Suomalainen Lääkäriseura Duodecim
Keuhkoahtaumataudin pitkäaikaisessa hoidossa käytettävät lääkkeet
Keuhkoputkia avaavat lääkkeet
- Lääkeaineita, jotka avaavat keuhkoputkia pääosin vähentämällä hengitysteiden sileän lihaksen supistusta, kutsutaan avaaviksi lääkkeiksi. Ne yleensä parantavat sekuntikapasiteettia (FEV1) tai muita spirometrialla mitattavia arvoja. Lisäksi ne yleensä parantavat keuhkojen tyhjentymistä ja vähentävät ansailmaa (dynaaminen hyperinflaatio tai restriktio) sekä levossa että rasituksessa «Thomas M, Decramer M, O'Donnell DE. No room to bre...»65. Näitä vaikutuksia ei kuitenkaan välttämättä pysty ennustamaan sen perusteella, miten hyvin lääke parantaa FEV1-arvoa «O'Donnell DE, Flüge T, Gerken F ym. Effects of tio...»66, «O'Donnell DE, Sciurba F, Celli B ym. Effect of flu...»67, «Berger R, Smith D. Effect of inhaled metaprotereno...»68, «Hay JG, Stone P, Carter J ym. Bronchodilator rever...»69.
- Keuhkoputkia avaavia lääkkeitä käytettäessä annoksen vähäisellä suurentamisella ei yleensä saada kasvatetuksi keuhkoputkia avaavaa tehoa kovin merkittävästi «Kankaanranta H. Keuhkoahtaumataudin uudet lääkkeet...»64, «Gross NJ, Petty TL, Friedman M ym. Dose response t...»70, «Higgins BG, Powell RM, Cooper S ym. Effect of salb...»71, «Vathenen AS, Britton JR, Ebden P ym. High-dose inh...»72. Haittavaikutukset «Keuhkoahtaumataudin lääkehoidon mahdolliset haittavaikutukset»4 riippuvat yleensä annoksesta. Inhaloidun beeta2-agonistin tai antikolinergin annoksen suurentaminen kymmenkertaiseksi, erityisesti kun se annetaan nebulisoituna, helpottaa subjektiivista hengenahdistustuntemusta akuuttitilanteissa muttei välttämättä auta stabiilin taudin hoidossa «O'Driscoll BR, Kay EA, Taylor RJ ym. A long-term p...»73, «Jenkins SC, Heaton RW, Fulton TJ ym. Comparison of...»74.
- Avaavia lääkkeitä on kahta eri ryhmää, joilla on pääosin samankaltainen keuhkoputkia avaava vaikutus mutta erilainen solutason vaikutusmekanismi. Näitä ovat beeta2-agonistit ja muskariinireseptoreita (M1, M2 ja M3) salpaavat aineet (ns. antikolinergit) «Kankaanranta H, Moilanen E. Hengitysteiden sairauk...»75, «Kankaanranta H, Mäkelä M. Tukkeavat keuhkosairaude...»76. Molemmissa lääkeaineryhmissä on sekä lyhytvaikutteisia (avaavan vaikutuksen kesto yleensä 3–6 tuntia) että pitkävaikutteisia valmisteita (avaavan vaikutuksen kesto yleensä 12–24 tuntia). Avaavia lääkkeitä annostellaan yleensä joko tarpeen mukaan akuuttien oireiden helpottamiseksi tai säännöllisesti oireiden ilmaantumisen estämiseksi.
- Useimmilla potilailla on järkevää olla äkillisten oireiden varalta tarvittaessa otettava lyhytvaikutteinen keuhkoputkia avaava lääke, vaikka heillä olisi säännöllisessä käytössä myös pitkävaikutteinen avaava lääke. Sen sijaan säännöllisen, suuriannoksisen, useasti päivässä annettavan lyhytvaikutteisen avaavan lääkkeen tai näiden yhdistelmän (nebulisoituna tms.) yhdistämisestä pitkävaikutteisiin avaaviin lääkkeisiin ei pitkäaikaishoidossa ole näyttöä «Global Strategy for the Diagnosis, Management and ...»1, «Global Initiative for chronic obstructive lung dis...»77 Tällainen yhdistelmä on myös syytä varata vain vaikeimpien potilaiden hoitoon, ja samalla on huolellisesti arvioitava pitkävaikutteisten avaavien tarve ja potilaan kyky ottaa ne oikein.
Lyhyt- ja pitkävaikutteiset beeta2-agonistit (SABA, LABA)
- Beeta2-agonistien pääasiallinen vaikutus on hengitysteiden sileän lihaksen supistustilan laukeaminen. Lyhytvaikutteisten beeta2-agonistien keuhkoputkia avaava vaikutus kestää yleensä 3–6 tuntia. Tarvittaessa tai säännöllisesti käytettävät lyhytvaikutteiset beeta2-agonistit vähentävät oireita ja parantavat keuhkofunktiota esimerkiksi FEV1- tai FVC-arvolla mitattuina «Sestini P, Renzoni E, Robinson S ym. Short-acting ...»78.
- Pitkävaikutteisten beeta2-agonistien keuhkoputkia avaava vaikutus kestää noin 12 (formoteroli ja salmeteroli) tai noin 24 tuntia (indakateroli, olodateroli, vilanteroli).
- Pitkävaikutteisten beeta2-agonistien käyttö astman hoidossa ilman samanaikaista hoitavaa lääkitystä on kielletty (ks. Käypä hoito -suositus Astma «Astma»6, «Astma. Käypä hoito -suositus. Suomalaisen Lääkäris...»33), koska on näyttöä siitä, että astman hoito pelkällä pitkävaikutteisella beeta2-agonistilla suurentaa astmakuolleisuutta «Cates CJ, Cates MJ. Regular treatment with salmete...»79. Keuhkoahtaumataudin hoidossa pitkävaikutteista beeta2-agonistia sen sijaan voidaan käyttää ainoana lääkkeenä. Keuhkoahtaumataudin hoidossa pitkävaikutteinen beeta2-agonisti ei tutkimusten mukaan suurenna kuolleisuutta «Decramer ML, Hanania NA, Lötvall JO ym. The safety...»80. Kohorttitutkimusten mukaan se saattaa jopa pienentää sitä «Lee TA, Pickard AS, Au DH ym. Risk for death assoc...»81, «Mapel DW, Nelson LS, Lydick E ym. Survival among C...»82.
Lyhyt- ja pitkävaikutteiset antikolinergit (SAMA, LAMA)
- Antikolinergit salpaavat muskariinireseptoreita ja estävät siten asetyylikoliinin aiheuttaman keuhkoputkien sileän lihaksen supistumisen. Lyhytvaikutteisen antikolinergin (ipratropium) keuhkoputkia avaava vaikutus kestää yleensä jonkin verran pidempään (jopa noin 8 tuntia) kuin lyhytvaikutteisten beeta2-agonistien, mutta vastaavasti niiden vaikutus alkaa hieman hitaammin «Kankaanranta H, Moilanen E. Hengitysteiden sairauk...»75, «Kankaanranta H, Mäkelä M. Tukkeavat keuhkosairaude...»76.
- Pitkävaikutteisten antikolinergien keuhkoputkia avaava vaikutus kestää noin 12 tuntia (aklidinium) tai noin 24 tuntia (glykopyrronium, tiotropium, umeklidinium).
- Pitkävaikutteisista antikolinergeista tiotropium on ollut kauimmin käytössä, ja se on myös laajimmin tutkittu. Tiotropium vähentää keuhkoahtaumataudin pahenemisvaiheita, parantaa keuhkofunktiota ja elämänlaatua ja vähentää keuhkoahtaumataudin oireita «Tiotropium vähentää keuhkoahtaumataudin pahenemisvaiheita, parantaa keuhkofunktiota ja elämänlaatua ja vähentää keuhkoahtaumataudin oireita.»A. Sen sijaan se ei vaikuta taudin etenemiseen, kun mittarina käytetään vuosittaista FEV1:n pienenemistä «Tashkin DP, Celli B, Senn S ym. A 4-year trial of ...»83. Tiotropium on mahdollisesti salmeterolia tehokkaampi vähentämään keuhkoahtaumataudin pahenemisvaiheita «Vogelmeier C, Hederer B, Glaab T ym. Tiotropium ve...»84. Myös muista pitkävaikutteisista antikolinergeista on julkaistu samansuuntaisia tuloksia «Sims MW, Panettieri RA Jr. Profile of aclidinium b...»85, «Ulrik CS. Once-daily glycopyrronium bromide, a lon...»86, «Jones PW, Rennard SI, Agusti A ym. Efficacy and sa...»87, «Kerwin E, Hébert J, Gallagher N ym. Efficacy and s...»88, «Poole P, Sathananthan K, Fortescue R. Mucolytic ag...»89, «Rojas-Reyes MX, García Morales OM, Dennis RJ ym. C...»90.
Keuhkoputkia avaavien lääkkeiden yhdistäminen
- Vaikutusmekanismiltaan tai vaikutusajaltaan erilaisia keuhkoputkia avaavia lääkkeitä voi melko vapaasti yhdistää (ks. taulukko «Keuhkoahtaumataudin hoidossa käytettävät lääkeaineet ryhmiteltyinä vaikutuksensa ja sen keston mukaan sekä lääkkeiden yhteiskäytön periaatteet...»2), ja yhdistäminen saattaa lisätä keuhkoputkia avaavaa tehoa «Appleton S, Jones T, Poole P ym. Ipratropium bromi...»91. Esimerkiksi lyhytvaikutteisen antikolinergin yhdistäminen joko lyhyt- tai pitkävaikutteiseen beeta2-agonistiin parantaa FEV1-arvoa paremmin kuin kumpikaan lääke yksin «Appleton S, Jones T, Poole P ym. Ipratropium bromi...»91, «Appleton S, Jones T, Poole P ym. Ipratropium bromi...»92.
- Lyhyt- tai pitkävaikutteisen beeta2-agonistin yhdistämistä pitkävaikutteiseen antikolinergiin voidaan kokeilla, jos yksittäinen lääke ei korjaa oireita riittävän tehokkaasti «Appleton S, Jones T, Poole P ym. Ipratropium bromi...»91, «Appleton S, Jones T, Poole P ym. Ipratropium bromi...»92, «Karner C, Cates CJ. Long-acting beta(2)-agonist in...»93. Tiotropiumin ja pitkävaikutteisen beeta2-agonistin yhdistelmä parantaa ilmeisesti elämänlaatua ja keuhkofunktiota hieman paremmin «Farne HA, Cates CJ. Long-acting beta2-agonist in a...»94.
- Lyhyt- ja pitkävaikutteisen antikolinergin yhteiskäyttö saattaa parantaa keuhkojen toimintakokeiden tuloksia, mutta se voi suurentaa haittavaikutusten, ainakin virtsaummen, riskiä «Cole JM, Sheehan AH, Jordan JK. Concomitant use of...»95. Lyhytvaikutteisen beeta2-agonistin yhdistäminen pitkävaikutteiseen antikolinergiin tuottaa vähintään yhtä hyvän vasteen keuhkojen toimintakokeiden tuloksiin ilman antikolinergisten haittavaikutusten riskin suurenemista, joten pitkävaikutteisen antikolinergin rinnalla on suositeltavaa tarvittaessa käyttää lyhytvaikutteista beeta2-agonistia «Cole JM, Sheehan AH, Jordan JK. Concomitant use of...»95.
Inhaloitavat glukokortikoidit (ICS)
- Inhaloitavien glukokortikoidien teho ja haittavaikutukset astman hoidossa riippuvat annoksesta «Kankaanranta H, Lahdensuo A, Moilanen E ym. Add-on...»96. Inhaloitavien glukokortikoidivalmisteiden tehon ja haittavaikutusten annosvasteisuutta keuhkoahtaumataudissa ei sen sijaan tunneta yhtä hyvin «López-Campos JL, Calero Acuña C. What is in the gu...»97, «Yang IA, Clarke MS, Sim EH ym. Inhaled corticoster...»98, mutta pienet ja keskisuuret annokset ovat todennäköisesti tehon ja haittojen suhteen parhaita «Dransfield MT, Bourbeau J, Jones PW ym. Once-daily...»99.
- Säännöllinen pitkäaikainen (> 6 kk) hoito inhaloitavalla glukokortikoidilla vähentää pahenemisvaiheita ja hidastaa elämänlaadun huononemista keuhkoahtaumataudissa «Yang IA, Clarke MS, Sim EH ym. Inhaled corticoster...»98. Vastetta inhaloituun glukokortikoidiin ei ole mahdollista ennustaa oraaliseen glukokortikoidiin ("tablettikortisoni") saatavan vasteen, bronkodilataatiokokeen tai hyperreaktiviteetin mittaamisen pohjalta «Yang IA, Clarke MS, Sim EH ym. Inhaled corticoster...»98. Inhaloitavan glukokortikoidihoidon lopettaminen voi joillakuilla potilailla aiheuttaa pahenemisvaiheen «van der Valk P, Monninkhof E, van der Palen J ym. ...»100.
- Inhaloitava glukokortikoidi ei yksin vaikuta keuhkoahtaumatautikuolleisuuteen tai keuhkofunktion (FEV1) huononemisnopeuteen «Yang IA, Clarke MS, Sim EH ym. Inhaled corticoster...»98. Sen käytön haittapuolena ovat nielun hiivatulehdusten lisääntyminen ja äänen käheys. Lisäksi on havaintoja siitä, että keuhkokuumeet ovat inhaloitavalla glukokortikoidilla hoidetuilla lisääntyneet «Yang IA, Clarke MS, Sim EH ym. Inhaled corticoster...»98, «Cazzola M, Rogliani P. In stable COPD, long-acting...»101.
- Muun hoidon lisäksi annettavaa pitkäaikaista hoitoa inhaloitavalla glukokortikoidilla suositellaan vain potilaille, joilla on astma-keuhkoahtaumatauti-ilmiasu, suurentunut veren eosinofiilimäärä tai muusta hoidosta huolimatta toistuvia pahenemisvaiheita «ICS-lääkityksen aloittaminen keuhkoahtaumataudissa»3.
- Inhaloitavan glukokortikoidin pitkäaikaista käyttöä ainoana lääkkeenä keuhkoahtaumataudin hoidossa ei suositella, koska inhaloitavan glukokortikoidin ja pitkävaikutteisen beeta2-agonistin yhdistelmä on tehokkaampi vähentämään pahenemisvaiheita ja mahdollisesti jopa pienentämään kuolleisuutta sekä parantamaan keuhkojen toimintaa ja elämänlaatua «Nannini LJ, Cates CJ, Lasserson TJ ym. Combined co...»102.
- Inhaloitavan glukokortikoidin pitkäaikaista käyttöä keuhkoahtaumataudin hoidossa ei suositella nykyisten indikaatioiden ulkopuolella, koska pitkäaikainen hoito inhaloitavalla glukokortikoidilla saattaa suurentaa keuhkokuumeen «López-Campos JL, Calero Acuña C. What is in the gu...»97, «Yang IA, Clarke MS, Sim EH ym. Inhaled corticoster...»98, osteoporoosin ja luunmurtumien riskiä «Loke YK, Cavallazzi R, Singh S. Risk of fractures ...»103.
- Inhaloitavaa glukokortikoidia kokeillaan, jos potilaalla on samanaikainen astma tai
jos on ollut vähintään kaksi keskivaikeaa pahenemisvaihetta tai yksi sairaalahoitoinen
pahenemisvaihe ja etenkin jos pahenemisvaiheiden lisäksi B-Eos taso on yli 0,3x109 solua/l.
- Veren eosinofiilien määrä ennustaa hoitovastetta inhalaatiosteroidiin pahenemisvaiheiden ehkäisyssä «Lipson DA, Barnhart F, Brealey N ym. Once-Daily Si...»63, «Bafadhel M, Peterson S, De Blas MA ym. Predictors ...»104, «Siddiqui SH, Guasconi A, Vestbo J ym. Blood Eosino...»105, «Papi A, Vestbo J, Fabbri L ym. Extrafine inhaled t...»106, «Pascoe S, Locantore N, Dransfield MT ym. Blood eos...»107, «Vestbo J, Papi A, Corradi M ym. Single inhaler ext...»108, mutta vielä ei ole riittävästi todisteita eosinofiilien käytöstä yksittäisen potilaan pahenemisvaiheriskin ennustamiseen «Casanova C, Celli BR, de-Torres JP ym. Prevalence ...»109, «Vedel-Krogh S, Nielsen SF, Lange P ym. Blood Eosin...»110.
- Vähäinen veren eosinofiilien määrä (< 0,1 x 109 solua/l) liittyy pienempään hyötyyn «Hogg JC, McDonough JE, Gosselink JV ym. What drive...»111 ja vähäisempi osuus (< 2 %) suurentuneeseen keuhkokuumeriskiin inhalaatiosteroidihoitoa saavilla «Pavord ID, Lettis S, Anzueto A ym. Blood eosinophi...»112.
- Inhalaatiosteroidin lopetukseen liittyy eniten FEV1:n pienenemistä ja pahenemisvaiheita potilailla, joiden veren eosinofiilimäärä on yli 0,3 x109 solua/l «Chapman KR, Hurst JR, Frent SM ym. Long-Term Tripl...»113.
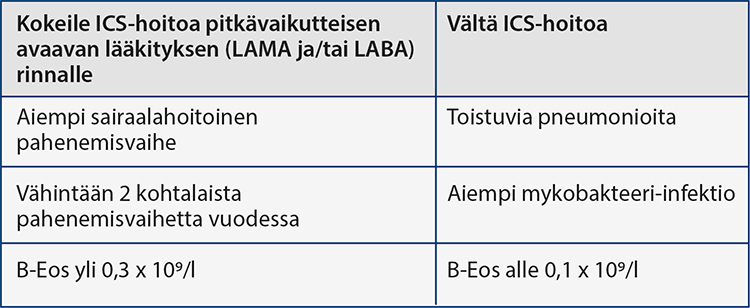
ICS-lääkityksen aloittaminen keuhkoahtaumataudissa.
ICS-lääkitys kuuluu alusta asti astma-keuhkoahtaumatauti-ilmiasua sairastavan lääkitykseen, mutta tavallisessa keuhkoahtaumataudissa sen rooli on epäselvempi. Osalla keuhkoahtaumatautipotilaista ICS-lääkitys vähentää toistuvia pahenemisvaiheita, mutta siihen voi liittyä myös haittoja. Oheisen taulukon avulla voi arvioida, milloin kannattaa aloittaa ICS-lääkitys pitkävaikutteisen avaavan lääkityksen (LAMA tai LABA) rinnalle.
© Suomalainen Lääkäriseura Duodecim
Inhaloitavan glukokortikoidin ja pitkävaikutteisen avaavan lääkkeen yhdistelmä
- Inhaloitavan glukokortikoidin ja pitkävaikutteisen beeta2-agonistin yhdistelmä vähentää keuhkoahtaumataudin pahenemisvaiheita ja parantaa keuhkofunktiota ja elämänlaatua «Inhaloitavan glukokortikoidin ja pitkävaikutteisen β2-agonistin yhdistelmä vähentää keuhkoahtaumataudin pahenemisvaiheita ja parantaa keuhkofunktiota ja elämänlaatua.»A.
- Inhaloitavan glukokortikoidin ja pitkävaikutteisen beeta2-agonistin yhdistelmä on pelkkää lumelääkettä tai sen osakomponentteja tehokkaampi parantamaan keuhkofunktiota ja terveydentilaa ja vähentämään keuhkoahtaumataudin pahenemisvaiheita «Dransfield MT, Bourbeau J, Jones PW ym. Once-daily...»99, «Nannini LJ, Cates CJ, Lasserson TJ ym. Combined co...»102, «Nannini L, Cates CJ, Lasserson TJ ym. Combined cor...»114, «Nannini LJ, Lasserson TJ, Poole P. Combined cortic...»115.
- Suuressa prospektiivisessa tutkimuksessa ei havaittu, että yhdistelmävalmisteella olisi merkittävää vaikutusta kuolleisuuteen «Calverley PM, Anderson JA, Celli B ym. Salmeterol ...»116, mutta myöhemmin tehdyssä meta-analyysissa todettiin, että sen käyttö saattaa pienentää kuolleisuutta (Number Needed to Treat NNT = 36; 95 % CI 21;258), «Nannini L, Cates CJ, Lasserson TJ ym. Combined cor...»114.
- Inhaloitavan glukokortikoidin ja pitkävaikutteisen beeta2-agonistin yhdistelmän lisääminen tiotropiumin rinnalle parantaa keuhkofunktiota ja elämänlaatua ja saattaa edelleen vähentää pahenemisvaiheita «Rojas-Reyes MX, García Morales OM, Dennis RJ ym. C...»90, «Aaron SD, Vandemheen KL, Fergusson D ym. Tiotropiu...»117, «Welte T, Miravitlles M, Hernandez P ym. Efficacy a...»118, «Cazzola M, Andò F, Santus P ym. A pilot study to a...»119, «Karner C, Cates CJ. Combination inhaled steroid an...»120, mutta asiasta tarvitaan lisää ja pidempiä tutkimuksia. Kolmen lääkkeen yhdistelmän kustannusvaikuttavuudesta pelkkään pitkävaikutteiseen antikolinergiin nähden on alustavaa näyttöä myös Suomesta «Nielsen R, Kankaanranta H, Bjermer L ym. Cost effe...»121.
Kaksoisavaavat
- Pitkävaikutteisten bronkodilaattoreiden yhdistelmä on pelkkää pitkävaikutteista beeta2-agonistia tai antikolinergia tehokkaampi keuhkoahtaumataudin pahenemisvaiheiden estossa ja saattaa vähentää oireita monoterapiaa tehokkaammin «Oba Y, Keeney E, Ghatehorde N ym. Dual combination...»122, «Pitkävaikutteisten bronkodilataattoreiden yhdistelmä on tehokkaampi kuin pitkävaikutteinen β2-agonisti tai antikolinergi yksin keuhkoahtaumataudin pahenemisvaiheiden estossa ja saattaa vähentää oireita monoterapiaa tehokkaammin.»A. Pitkävaikutteinen antikolinergi saattaa olla pitkävaikutteista beeta2-agonistia tehokkaampi pahenemisvaiheiden estossa erityisesti niillä, joilla pahenemisvaiheriski on suuri «Oba Y, Keeney E, Ghatehorde N ym. Dual combination...»122.
Kolmoisyhdistelmähoito
- Aiemmasta säännöllisestä hoidosta huolimatta edelleen oireisilla tai pahenemisvaiheista kärsivillä keuhkoahtaumatautipotilailla kolmoisyhdistelmähoidon (ICS + LABA + LAMA) on todettu olevan ICS + LABA -yhdistelmää ja avaavia lääkkeitä tehokkaampi vähentämään pahenemisvaiheita, parantamaan keuhkofunktiota ja parantamaan oireita ja elämänlaatua. Tuoreen meta-analyysin mukaan kolmoishoidon paremmuus LABA + LAMA -hoitoon nähden pahenemisvaiheiden vähentämisessä on yhteydessä veren eosinofiilimäärään (NNT 8,6 potilailla, joilla B-Eos ≥ 0,3 x 109 solua/l; NNT 46,3 potilailla, joilla B-Eos < 0,3 x 109 solua/l). Meta-analyysin mukaan pneumoniariski oli kolmoishoidolla 1,3-kertainen LABA + LAMA -hoitoon nähden, mutta ero ei ollut tilastollisesti merkitsevä «Cazzola M, Rogliani P, Calzetta L ym. Triple thera...»123.
Inhalaatiosteroidin hyödyt ja haitat
Inhaloitavan lääkehoidon keventämisen periaatteet
- Potilailla, joilla on käytössään ICS:n ja yhden tai kahden avaavan lääkkeen yhdistelmiä, voidaan joissakin tilanteissa harkita ICS:n jättämistä pois.
- ICS:n lopettamista harkitaan ja hoitoa jatketaan avaavilla lääkkeillä, jos potilaalla on toistuvia keuhkokuumeita tai jos ICS:stä ei ole ollut hyötyä pahenemisvaiheiden estoon tai oireiden lievittymiseen «ICS-lääkityksen aloittaminen keuhkoahtaumataudissa»3, «ICS-lääkityksen vähentäminen tai lopettaminen keuhkoahtaumataudissa»4.
- ICS:ää sisältävien lääkeyhdistelmien käyttäjillä, joilla veren eosinofiilitaso on ≥ 0,3 x109 solua/l, pahenemisvaiheen riski saattaa kasvaa huomattavasti ICS:n lopettamisen seurauksena «Chapman KR, Hurst JR, Frent SM ym. Long-Term Tripl...»124, «Calverley PMA, Tetzlaff K, Vogelmeier C ym. Eosino...»125.
- Potilaita, joiden lääkehoitoa on kevennetty jättämällä ICS pois, tulee seurata tiheämmin, koska tutkimusnäyttö lääkehoidon keventämisestä on niukka.

ICS-lääkityksen vähentäminen tai lopettaminen keuhkoahtaumataudissa
Osa keuhkoahtaumatautipotilaista hyötyy ICS-lääkityksestä lähinnä pahenemisvaiheiden vähenemisen myötä, mutta ICS-hoitoon voi liittyä myös haittoja. Oheisen kuvion perusteella voi arvioida, milloin ICS-hoitoa kannattaisi kokeilla vähentää tai lopettaa. Astma-keuhkoahtaumatauti-ilmiasua sairastavien hoitoon ICS kuuluu.
© Suomalainen Lääkäriseura Duodecim
Roflumilasti
- Roflumilasti vaimentaa keuhkoahtaumatautiin liittyvää tulehdusreaktiota estämällä fosfodiesteraasi-4 (PDE4) -entsyymiä ja suurentamalla solunsisäisen syklisen adenosiinimonofosfaatin (cAMP) pitoisuutta «Kankaanranta H. Keuhkoahtaumataudin uudet lääkkeet...»64.
- Roflumilasti annostellaan kerran päivässä suun kautta tablettina. Vaikka se ei suoranaisesti ole bronkodilataattori, sillä on myös jonkin verran bronkodilatoivaa vaikutusta. Salmeterolia tai tiotropiumia saavilla potilailla sen on osoitettu parantavan FEV1-arvoa keskimäärin 50–80 ml «Kankaanranta H. Keuhkoahtaumataudin uudet lääkkeet...»64, «Chong J, Poole P, Leung B ym. Phosphodiesterase 4 ...»126, «Calverley PM, Rabe KF, Goehring UM ym. Roflumilast...»127, «Fabbri LM, Calverley PM, Izquierdo-Alonso JL ym. R...»128.
- Roflumilasti vähentää keuhkoahtaumataudin pahenemisvaiheita ja parantaa keuhkojen toimintaa, mutta sillä on merkittäviä haittavaikutuksia «Roflumilasti vähentää keuhkoahtaumataudin pahenemisvaiheita ja parantaa keuhkojen toimintaa, mutta sillä on merkittäviä haittavaikutuksia.»A. Roflumilasti vähentää keskivaikeita (systeemistä glukokortikoidia vaativa) ja vaikeita (sairaalahoitoon tai kuolemaan johtava) keuhkoahtaumataudin pahenemisvaiheita potilailla, joilla on vaikea keuhkoahtaumatauti (FEV1< 50 %), krooninen keuhkoputkitulehdus ja toistuvia pahenemisvaiheita pitkävaikutteisesta avaavasta lääkityksestä huolimatta «Kankaanranta H. Keuhkoahtaumataudin uudet lääkkeet...»64, «Chong J, Poole P, Leung B ym. Phosphodiesterase 4 ...»126, «Calverley PM, Rabe KF, Goehring UM ym. Roflumilast...»127. Sen sijaan vaikutukset elämänlaatuun ja oireisiin ovat vähäisempiä «Kankaanranta H. Keuhkoahtaumataudin uudet lääkkeet...»64, «Chong J, Poole P, Leung B ym. Phosphodiesterase 4 ...»126.
Muut pitkäaikaisessa hoidossa käytettävät lääkkeet
Oraalinen glukokortikoidi
- Oraalisella glukokortikoidilla ("tablettikortisoni") tehtävää hoitokoetta ei ole suositeltavaa käyttää sen selvittämiseen, hyötyykö potilas inhaloitavasta glukokortikoidista tai muusta lääkehoidosta, koska oraaliseen glukokortikoidiin saatavan vasteen ei tiedetä ennustavan muihin lääkkeisiin saatavaa vastetta «Broekhuizen BD, Sachs AP, Moons KG ym. Diagnostic ...»38, «Callahan CM, Dittus RS, Katz BP. Oral corticostero...»39, «Woolcock AJ. Corticosteroid-resistant asthma. Defi...»40, «Burge PS, Calverley PM, Jones PW ym. Prednisolone ...»41, «Chavannes NH, Schermer TR, Wouters EF ym. Predicti...»42. Tämä ei kuitenkaan tarkoita sitä, ettei pahenemisvaiheita tulisi hoitaa kuuriluonteisesti oraalisella glukokortikoidilla tai ettei hankalasti oireilevaa potilasta voisi kokeilla hoitaa kuurilla oraalista glukokortikoidia.
- Vaikka suuriannoksinen (≥ 30 mg prednisolonia/vrk) oraalinen glukokortikoidi parantaa keuhkojen toimintaa lyhyellä aikavälillä, pitkäaikaisen, pienemmällä annoksella toteutetun hoidon pitkäaikaisista hyödyistä ei ole näyttöä «Walters JA, Walters EH, Wood-Baker R. Oral cortico...»129. Sen sijaan haittavaikutusten lisääntymisestä on viitteitä «Walters JA, Walters EH, Wood-Baker R. Oral cortico...»129.
- Oraalisen glukokortikoidin pitkäaikaiseen käyttöön keuhkoahtaumataudin hoidossa tulee suhtautua pidättyvästi, koska on viitteitä siitä, että se jopa huonontaa potilaan ennustetta «Schols AM, Wesseling G, Kester AD ym. Dose depende...»130.
Teofylliini
- Teofylliinin tarkka vaikutusmekanismi on epäselvä, mutta sillä on havaittu olevan sekä keuhkoputkia avaavia että tulehdusreaktiota rauhoittavia ominaisuuksia. Teofylliinin farmakokinetiikka vaihtelee huomattavasti yksilöittäin ja on altis lääkeaineiden yhteisvaikutuksille «Barnes PJ. Theophylline. Am J Respir Crit Care Med...»131, «Cazzola M, Page CP, Calzetta L ym. Pharmacology an...»132, joten lääkkeen veripitoisuuksia tulee seurata ja annostelu tulee sovittaa niiden mukaan. Lisäksi tiedot hitaasti vapautuvien teofylliiniyhdisteiden vaikutuksen kestosta puuttuvat «Global Initiative for chronic obstructive lung dis...»77.
- Raportit teofylliinin vaikutuksista keuhkoahtaumataudissa ovat ristiriitaisia. Teofylliini ilmeisesti parantaa keuhkofunktiota keuhkoahtaumataudissa, mutta toisaalta se lisää haittavaikutuksia «Teofylliini ilmeisesti parantaa keuhkofunktiota keuhkoahtaumataudissa, mutta haittavaikutukset lisääntyvät.»B. Lisäksi teofylliini saattaa parantaa sisäänhengityslihasten toimintaa «Barnes PJ. Theophylline. Am J Respir Crit Care Med...»131. Teofylliinin vaikutus keuhkojen toimintaan ja oireisiin keuhkoahtaumataudissa on vähäisempi kuin pitkävaikutteisten beeta2-agonistien formoterolin tai salmeterolin «Rossi A, Kristufek P, Levine BE ym. Comparison of ...»133, «ZuWallack RL, Mahler DA, Reilly D ym. Salmeterol p...»134. Teofylliinin lisääminen salmeterolin rinnalle paransi FEV1:tä ja vähensi hengenahdistusta paremmin kuin pelkkä salmeteroli «ZuWallack RL, Mahler DA, Reilly D ym. Salmeterol p...»134. Pieni annos teofylliiniä (100 mg kahdesti päivässä) vähensi pahenemisvaiheita tilastollisesti merkitsevästi muttei parantanut bronkodilataattorin annon jälkeen mitattua keuhkojen toimintaa «Zhou Y, Wang X, Zeng X ym. Positive benefits of th...»135.
- Teofylliinin terapeuttinen leveys on kapea ja laaja-alainen toksisuus helposti ongelma «Global Initiative for chronic obstructive lung dis...»77, «Barnes PJ. Theophylline. Am J Respir Crit Care Med...»131, «Cazzola M, Page CP, Calzetta L ym. Pharmacology an...»132. Tästä syystä teofylliinin käyttö on vähentynyt ja sitä suositellaan keuhkoahtaumataudin hoitoon vain lisälääkkeenä vaikeasti oireilevilla potilailla.
Makrolidit
- 11 tutkimusta sisältäneen meta-analyysin mukaan makrolidien (erytromysiini tai atsitromysiini) 6–12 kuukauden säännöllisellä käytöllä on saatu vähennetyksi keuhkoahtaumataudin pahenemisvaiheita «Cui Y, Luo L, Li C ym. Long-term macrolide treatme...»136.
- Potilailla, joilla on suuri pahenemisvaiheen riski, atsitromysiini käytettynä joko 250 mg päivässä tai 500 mg kolmena päivänä viikossa vuoden ajan vähentää pahenemisvaiheita tavanomaiseen hoitoon nähden. Aktiivisesti tupakoivilla hyöty vaikuttaa vähäisemmältä «Han MK, Tayob N, Murray S ym. Predictors of chroni...»137.
- Makrolidien laajamittaista käyttöä keuhkoahtaumataudin pahenemisvaiheiden estämiseksi hillitsee pelko niiden haittavaikutusten esiintymisestä sekä bakteerien makrolidiresistenssin lisääntymisestä «Cui Y, Luo L, Li C ym. Long-term macrolide treatme...»136. Atsitromysiinin pitkäaikaiseen käyttöön liittyy enemmän haittavaikutuksia, kuten bakteeri-resistenssin kehittyminen, pitkittynyt QTc-aika ja kuulon heikkeneminen «Cui Y, Luo L, Li C ym. Long-term macrolide treatme...»136.
- Koska makrolidin aloittaminen pitkäaikaiseksi hoidoksi vaatii edeltäviä tutkimuksia (esim. yskösviljelyt) ja riski-hyötysuhteen arviointia, suositellaan, että arvio tehdään ainoastaan erikoissairaanhoidossa.
Liman eritykseen tai koostumukseen vaikuttavat lääkkeet (mukolyytit)
- Käytössä on usealla eri mekanismilla toimivia mukolyyttejä «Kankaanranta H, Moilanen E. Hengitysteiden sairauk...»75, «Kankaanranta H, Mäkelä M. Tukkeavat keuhkosairaude...»76. Mukolyyttien säännöllistä käyttöä keuhkoahtaumataudissa on selvitetty useissa tutkimuksissa, ja tulokset ovat olleet ristiriitaisia «Global Initiative for chronic obstructive lung dis...»77, «Poole P, Black PN, Cates CJ. Mucolytic agents for ...»138.
- Mukolyytit ilmeisesti vähentävät keuhkoahtaumataudin pahenemisvaiheita ilman merkittäviä haittavaikutuksia mutteivät paranna keuhkojen toimintaa «Poole P, Sathananthan K, Fortescue R. Mucolytic ag...»89.
Fenotyypitys, lääkehoito ja vastearvio
- Keuhkoahtaumataudin lääkehoito ja sen valinta pohjautuvat kunkin potilaan yksilölliseen sairauden ilmiasuun, oireiden määrään ja pahenemisvaiheriskiin. Potilaiden luokittelu ja lääkehoito esitetään kuvassa «Keuhkoahtaumataudin diagnostiikka ja arviointi sekä ilmiasun ja hoidon määräytyminen»2.
- Säännöllinen lääkehoito aloitetaan kaikille potilaille, joilla on säännöllisesti haittaavia oireita tai suuri riski saada keuhkoahtaumataudin pahenemisvaiheita.
- Keuhkoahtaumataudin lääkehoito perustuu suurelta osin hengitettäviin lääkkeisiin, jolloin sopivan inhalaattorin valinta (taulukko «Sopivan inhalaattorin valinta...»4) ja huolellinen inhalaatio-ohjaus ovat tärkeitä.
- Kaikilla potilailla hoidon tavoitteena on vähentää oireita ja mahdollisia pahenemisvaiheita.
- Olennaista hoidon valinnassa on ilmiasun perusteella valita joko pitkävaikutteiset avaavat lääkkeet tai heti alusta saakka niiden rinnalle myös hengitettävä glukokortikoidi.
- Ilmiasu, hoitovaste ja sopiva lääkitys ja sen mukainen lääkehoito tulee arvioida uudelleen jokaisen seurantakäynnin yhteydessä «Keuhkoahtaumataudin diagnostiikka ja arviointi sekä ilmiasun ja hoidon määräytyminen»2, koska ilmiasu saattaa taudin edetessä muuttua (erityisesti pahenemisvaiheiden riskin osalta) «Agusti A, Edwards LD, Celli B ym. Characteristics,...»55.
- Aina hoitovastetta arvioidessa on syytä kiinnittää huomiota inhalaattorin valintaan, inhalaatiotekniikkaan ja erotusdiagnostiikkaan.
Inhalaatiolaitteen valinta
- Huomattava osa potilaista ei osaa käyttää inhalaattoriaan oikein «Yawn BP, Colice GL, Hodder R. Practical aspects of...»139, joten sen käyttöä on tärkeää opettaa lääkitystä aloitettaessa ja seurantakäynneillä.
- Jauheinhalaattorin käyttö ei vaadi potilaalta laitteen laukaisun ja sisäänhengityksen koordinointia, mutta se vaatii riittävän sisäänhengitysvoiman ja -nopeuden.
- Ponnekaasuaerosolin käyttö ei vaadi suurta sisäänhengitysnopeutta, mutta potilaan pitää osata koordinoida laitteen laukaisu sisäänhengityksen alkuun.
- Tilanjatkeen käyttö ponnekaasuaerosolien kanssa vähentää koordinaation tarvetta, ja osa laitteista vähentää suuhun ja nieluun jäävien suurien lääkepisaroiden määrää «Laube BL, Janssens HM, de Jongh FH ym. What the pu...»140.
- Vaikeaa keuhkoahtaumatautia sairastavilla sisäänhengitysnopeus ei aina riitä jauheinhalaattorin käyttöön «Wieshammer S, Dreyhaupt J. Dry powder inhalers: wh...»141. Tällöin tulisi käyttää ponnekaasuaerosolia. Koordinaatio-ongelmien vuoksi tarvitaan usein myös tilanjatke ja tarvittaessa naamari ja avustaja.
- Sopivan inhalaattorin valinnan periaatteet esitetään taulukossa «Sopivan inhalaattorin valinta...»4.
| Sopivan inhalaattorin valinta | |||
|---|---|---|---|
|
|||
| Hyvä koordinaatio | Huono koordinaatio | ||
| Sisäänhengitysnopeus > 30 l/min | Sisäänhengitysnopeus < 30 l/min | Sisäänhengitysnopeus > 30 l/min | Sisäänhengitysnopeus < 30 l/min |
| Jauheinhalaattori
Ponnekaasuaerosoli Soft Mist Inhaler Autohaler (Nebulisaattori) |
Ponnekaasuaerosoli Soft Mist Inhaler (Nebulisaattori) |
Jauheinhalaattori Autohaler Ponnekaasuaerosoli + tilanjatke (Soft Mist Inhaler) (Nebulisaattori) |
Ponnekaasuaerosoli + tilanjatke (Soft Mist Inhaler) (Nebulisaattori) |
| Mukailtu lähteestä «Chapman KR, Voshaar TH and Virchow JC. Inhaler cho...»142 | |||
Kotihappihoito
- Hoito aloitetaan erikoissairaanhoidossa.
- Vaikealle keuhkoahtaumataudille on tyypillistä keuhkojen toiminnan ja hemodynamiikan vähittäinen huononeminen. Lopulta seurauksena saattaa olla valtimoveren happikyllästeisyyden pysyvä väheneminen ja sen seurauksena kudosten hapenpuute.
- Krooniseen hypoksemiaan voivat liittyä muun muassa keuhkovaltimopaineen suureneminen, sekundaarinen polysytemia, neuropsykologisten toimintojen heikkeneminen ja erityisesti yöllä esiintyvät sydämen rytmihäiriöt.
- Kotihappihoito ilmeisesti pienentää kuolleisuutta keuhkoahtaumatautipotilailla, joilla on vaikea hypoksemia «Kotihappihoito ilmeisesti pienentää kuolleisuutta keuhkoahtaumatautipotilailla, joilla on vaikea hypoksemia.»B. Yöllä annettava pienivirtauksinen happihoito (vähintään 15 tuntia vuorokaudessa) vähentää valikoiduilla hypokseemisilla potilailla merkitsevästi keuhkoahtaumataudin aiheuttamaa kuolleisuutta, mutta paras vaikutus kuolleisuuteen saadaan ympärivuorokautisella (20–24 h/vrk) happihoidolla.
- Kotihappihoidosta ei ole ilmeisesti apua kuolleisuuden pienentämiseen lievässä tai keskivaikeassa hypoksemiassa «Kotihappihoidosta ei ole ilmeisesti apua kuolleisuuden pienentämiseen lievässä tai keskivaikeassa hypoksemiassa.»B.
- Rasituksenaikainen tai lyhytaikainen oireenmukainen happilisä ei ilmeisesti lievitä merkittävästi hengenahdistusoireita keuhkoahtaumatautipotilailla, joilla pitkäaikaishappihoidon kriteerit eivät täyty «Rasituksenaikainen tai lyhytaikainen oireenmukainen happilisä ei ilmeisesti lievitä merkittävästi hengenahdistusoireita keuhkoahtaumatautipotilaalla, jolla pitkäaikaishappihoidon kriteerit eivät täyty.»B.
- Pysyvässä happihoidossa olevat potilaat saattavat hyötyä rasituksessa käytettävästä, mukana kannettavasta happilisästä «Pysyvässä happihoidossa olevat potilaat saattavat hyötyä rasituksessa käytettävästä, mukana kannettavasta happilisästä.»B.
Kotihappihoidon aloittamisen kriteerit
- Potilaan tulee olla tupakoimaton ja riittävän yhteistyökykyinen. Hänellä tulee myös
olla krooninen, pitkälle edennyt keuhkosairaus. Lisäksi valtimoveren happiosapaineen
tulee kahdessa erillisessä vähintään 3 viikon välein otetussa näytteessä olla alle
7,3 kPa, kun potilas hengittää huoneilmaa ja on stabiilissa vaiheessa. Kriteeri täyttyy
myös, jos happiosapaine on 7,3–8,0 kPa ja jokin seuraavista lisäkriteereistä täyttyy:
- merkkejä kohonneesta keuhkovaltimopaineesta, esimerkiksi turvotuksia
- sekundaarinen polysytemia (hematokriitti yli 55 %)
- oksimetrian avulla todettu ja happihoidolla korjautuva merkittävä yöunen aikainen hypoksemia, joka ei johdu samanaikaisesta uniapneataudista
- merkittävät neuropsykologiset oireet, jotka korjautuvat happihoidolla.
- happihoidolla saavutettu toivottu vaste (PaO2 yli 8,0 kPa) ilman haitalliseksi katsottavaa valtimoveren hiilidioksidiosapaineen nousua.
- Happihoito toteutetaan sairaalan apuvälineyksiköstä lainattavalla happirikastimella ja kodin ulkopuolella happipullojen avulla. Kalliimpi vaihtoehto on nestehappi (kotisäiliö ja täytettävä kannettava säiliö). Nestehappi ja happipullot määrätään reseptillä. Potilas tilaa hapen kaasujen toimittajalta «http://www.linde-healthcare.fi/»2, «http://www.woikoski.fi/»3 ja saa hapesta ja laitteiden vuokrasta sairausvakuutuksen peruskorvauksen. Kuntoutusohjaaja toimii asiantuntijana happihoidon aloituksessa, ohjauksessa ja kotiseurannassa.
- Happihoidon käyttämättömyys tai tupakointi happihoidon aikana on aihe kotihappihoidon lopettamiseen, ja tämä tulee kirjata sairauskertomukseen.
- Jos keuhkoahtaumatautipotilaan happikyllästeisyys stabiilissa tilanteessa ja levossa on yli 90 %, happihoidon kriteerit eivät todennäköisesti täyty.
Noninvasiivinen ventilaatio stabiilissa keuhkoahtaumataudissa
- Yönaikainen noninvasiivinen ventilaatio (NIV, hengityksen avustaminen hengityslaitteella ilman keinoilmatietä) stabiilissa keuhkoahtaumataudissa ei hyperkapnisilla potilailla todennäköisesti vähennä pahenemisvaiheita tai sairaalahoidon tarvetta eikä paranna kaasujenvaihtoa, rasituksensietokykyä, elämän laatua, hengityslihasvoimaa tai unen tehokkuutta, mutta se saattaa pienentää kuolleisuutta «Yönaikainen noninvasiivinen ventilaatio (NIV) stabiilissa keuhkoahtaumataudissa ei hyperkapnisilla potilailla todennäköisesti vähennä pahenemisvaiheita tai sairaalahoidon tarvetta eikä paranna kaasujenvaihtoa, rasituksensietokykyä, elämänlaatua, hengityslihasvoimaa tai unen tehokkuutta, mutta se saattaa vähentää kuolleisuutta.»C.
- Jos keuhkoahtaumatautipotilaalla on adekvaatin hoidon aikana krooninen hyperkapnia ja toistuvia pahenemisvaiheita, joiden aikana hän tarvitsee noninvasiivista tai invasiivista ventilaatiota, tai voimakas hyperkapnia happihoidon aikana ja oireita yöllisestä hypoventilaatiosta, yöllistä noninvasiivista ventilaatiota voidaan harkita (joko happihoidon kera tai ilman).
- Potilailla, joilla on sekä keuhkoahtaumatauti että obstruktiivinen uniapnea, CPAP-hoito pienentää kuolleisuutta ja sairaalahoidon tarvetta «Marin JM, Soriano JB, Carrizo SJ ym. Outcomes in p...»143.
- Laitteen käyttämättömyys on aihe laitehoidon lopettamiseen, ja tämä tulee kirjata sairauskertomukseen.
Keuhkoahtaumataudin kirurginen hoito
- Keuhkonsiirron ensisijaisena tavoitteena on aina elinajan piteneminen. Tässä suhteessa keuhkonsiirtotoiminnan parhaat tulokset saavutetaan muissa sairauksissa kuin keuhkoahtaumataudissa.
- Pitkä tupakointihistoria aiheuttaa usein liitännäissairauksia ja suurentuneen syöpäriskin, jotka voivat estää keuhkonsiirron.
- Jos kyseessä ei ole alfa1-antitrypsiinin puutokseen liittyvä keuhkoahtaumatauti tai emfyseema, keuhkonsiirtokriteerit täyttävä suorituskyvyn ja keuhkofunktion pienenemä kehittyy vasta melko korkeassa iässä.
- Keuhkoahtaumatauti ei myöskään etene yhdenmukaisesti tai suoraviivaisesti loppuvaiheessaan, joten kuolleisuutta on vaikeaa ennustaa pelkän obstruktion vaikeusasteen perusteella.
- Jos tauti etenee ja oireet lisääntyvät maksimaalisesta lääkkeettömästä (mm. liikunnallinen kuntoutus) ja lääkkeellisestä hoidosta huolimatta, sopiva potilas voidaan lähettää erikoissairaanhoitoon keuhkonsiirtoarvioon. Keuhkoahtaumatautipotilaan oikeaa lähettämisen ja listalle asettamisen ajankohtaa arvioidaan BODE-indeksin avulla «Orens JB, Estenne M, Arcasoy S ym. International g...»144. BODE-indeksi on työkalu keuhkoahtaumatautipotilaan ennusteen arvioimiseksi, ja siinä otetaan huomioon painoindeksi, obstruktion vaikeusaste (FEV1, % viitearvosta), hengenahdistuksen aste (mMRC-testi) ja 6 minuutin kävelytestin tulos «Celli BR, Cote CG, Marin JM ym. The body-mass inde...»145. Ks. lisätietoa aiheesta «Keuhkoahtaumataudin kirurginen hoito»5.
- Keuhkojen pienennysleikkauksessa (Lung Volume Reduction Surgery) poistetaan vaikeaa emfyseemaa sairastavilta keuhkoista pahimmin tuhoutuneita alueita. Volyymireduktiokirurgia ilmeisesti hyödyttää oikein valittuja potilaita «Volyymireduktiokirurgia ilmeisesti hyödyttää oikein valittuja potilaita.»B.
- Endoskooppinen keuhkotilavuuden reduktio esimerkiksi keuhkoputkiin asennettavien venttiileiden avulla saattaa olla hoitomahdollisuus vaikeassa emfyseemassa. Vaikeaa keuhkoahtaumatautia sairastavan hoidossa voidaan joutua harkitsemaan keuhkonsiirtoa, jos muilla hoitokeinoilla ei ole saavutettu suotuisaa vastetta ja potilaan elinaikaennuste on alle 2 vuotta.
- Kun keuhkonsiirto tehdään yli 60-vuotiaalle, elinaikaennuste on ollut huonompi ja kroonisen hyljinnän riski suurempi kuin alle 60-vuotiailla keuhkoahtaumatautipotilailla «Inci I, Schuurmans M, Ehrsam J ym. Lung transplant...»146.
Keuhkoahtaumataudin pahenemisvaihe
- Keuhkoahtaumataudin pahenemisvaiheessa potilaan hengitystieoireet äkillisesti vaikeutuvat tavanomaisesta päivittäisestä vaihtelusta. Pahenemisvaiheessa lääkitystä joudutaan väliaikaisesti tehostamaan «Global Strategy for the Diagnosis, Management and ...»1.
- Keuhkoahtaumataudin pahenemisvaiheen diagnoosi on kliininen, ja sen merkkejä ovat
- lisääntynyt hengenahdistus
- yskä
- mahdollisesti märkäiset yskökset.
- Lääkehoidoittain ja hoitopaikoittain pahenemisvaiheet jaetaan vakavuutensa mukaan
kolmeen kategoriaan:
- lievät (lyhytvaikutteiset avaavat inhalaatiolääkkeet; avohoito, polikliinisesti)
- keskivaikeat (avaavien inhalaatiolääkkeiden lisäksi suun kautta annosteltava glukokortikoidi tai antibioottikuuri; avohoito, polikliinisesti)
- vaikeat (vaatii päivystyskäyntiä tai sairaalahoitoa; yleensä kaikki edellä mainitut lääkkeet ja happihoito; usein edellyttää hengitystukihoitoa mekaanisilla ventilaattoreilla).
- Taipumus pahenemisvaiheisiin on yksilöllinen. Kaikilla potilailla ei esiinny pahenemisvaiheita, mutta osalla pahenemisvaiheita on toistuvasti. Heikentynyt keuhkotoiminta (FEV1 alle 50 % viitearvosta) suurentaa taudin pahenemisvaiheiden riskiä. Sairastettu pahenemisvaihe on seuraavan pahenemisvaiheen merkittävin riskitekijä.
- Tärkeimmät pahenemisvaiheita laukaisevista tekijöistä ovat hengitystieinfektiot (60–80 % tapauksista) «Papi A, Bellettato CM, Braccioni F ym. Infections ...»147. Yksi mahdollinen toistuvien pahenemisvaiheiden aiheuttaja on hengitysteiden mikrobikolonisaatio. Potilaista 10 %:lla syynä on altistus ilmansaasteille.
- Pahenemisvaiheeseen ajautuneen potilaan kokonaistilaa arvioitaessa tulisi sulkea pois muut mahdolliset tilan huononemisen syyt, kuten keuhkokuume, toistuva aspiraatio, sydäninfarkti, rytmihäiriöt, sydämen vajaatoiminta, keuhkoveritulppa, ilmarinta ja keuhkopussineste. Toisaalta edellä mainitut tilat voivat yhtä hyvin laukaista pahenemisvaiheen tai pahentaa sitä. Myös lääkehoidon keskeyttäminen saattaa johtaa pahenemisvaiheeseen.
- Erityisesti sairaalahoitoon johtavat ja toistuvat pahenemisvaiheet heikentävät merkittävästi potilaan elämänlaatua ja ennustetta (sairaalahoidon jälkeen 3 ja 5 vuoden kuolleisuus 43 % ja 51 %) «Hoogendoorn M, Hoogenveen RT, Rutten-van Mölken MP...»148. Aiempi sairaalahoitoon johtanut pahenemisvaihe ja vaikeat liitännäissairaudet, kuten sydän- ja verisuonitaudit, liittyvät kuolemanriskiin pahenemisvaiheessa «Global Strategy for the Diagnosis, Management and ...»1, «Patel AR, Kowlessar BS, Donaldson GC ym. Cardiovas...»149.
Kliininen arvio ja tutkimukset
- Keuhkoahtaumataudin pahenemisen tutkimus- ja hoitoalgoritmi esitetään kuvassa «Keuhkoahtaumataudin pahenemisvaihe»5. Tilanne arvioidaan yksilöllisesti.
- Pahenemisvaiheen arvioinnissa anamneesi on avainasemassa. Siinä tulee selvittää potilaan
- glukokortikoidilla tai antibiootilla hoidettujen pahenemisvaiheiden määrä (onko ollut ≥ 2 pahenemisvaihetta vuodessa tai ≥ 1 sairaalahoitoon johtanut pahenemisvaihe?)
- hengitystieahtauman vaikeusaste (FEV1) ennen pahenemisvaihetta
- hengenahdistuksen ja uusien oireiden kesto ja voimakkuus
- muut krooniset sairaudet ja liitännäissairaudet
- nykyinen lääkitys ja lääkkeenottotekniikka.

Keuhkoahtaumataudin pahenemisvaihe. © Suomalainen Lääkäriseura Duodecim
Alkututkimukset ja sairaalahoidon tarpeen arvio
- Potilaalle tehdään kliininen tutkimus (mm. ihon syanoosi, kalpeus tai punakkuus, hengitystaajuus, sydän- ja hengitysäänet, apuhengityslihasten käyttö ja perifeeriset turvotukset).
- Happikyllästeisyys arvioidaan pulssioksimetrilla (suuntaa-antava arvo).
- Yskösnäytteen ulkonäkö arvioidaan. Märkäisyys eli purulenssi (yskös on väriltään kellertävä tai vihertävä) viittaa bakteeritulehdukseen ja on riittävä merkki antibioottikuurin aloittamiseksi «Global Strategy for the Diagnosis, Management and ...»1, vaikka CRP olisi normaali.
- Erotusdiagnostisena tutkimuksena ja keuhkokuumetta tai ilmarintaa epäiltäessä tehdään keuhkojen röntgenkuvaus.
- Potilaalle tehdään perusverikokeet (TVK, CRP, kreatiniini ja elektrolyytit) ja häneltä rekisteröidään EKG.
- Spirometriaa ei ole suositeltavaa tehdä pahenemisvaiheen yhteydessä, koska tuolloin sen tekeminen saattaa olla potilaalle vaikeaa ja tulokset ovat epäluotettavia.
- Pahenemisvaiheen vakavuuden ja potilaan perustilanteen (mm. hengitysahtauman vaikeusaste, sairastettujen pahenemisvaiheiden määrä ja liitännäissairaudet) mukaan pahenemisvaiheen hoito toteutetaan avohoidossa polikliinisesti (yli 80 % tapauksista) tai terveyskeskuksen, perusterveydenhuollon tai erikoissairaanhoidon vuodeosastolla.
Lisätutkimukset sairaalan päivystyspoliklinikalla
- Potilaalle tehdään samat perustutkimukset kuin edellä ja mahdolliset puuttuvat tutkimukset täydennetään.
- pH:n ja verikaasujen määritystä varten otetaan valtimoverinäyte.
- Harkinnan mukaan tehdään laajempia diagnoosia tukevia ja erotusdiagnostisia tutkimuksia.
Pahenemisvaiheen hoito
- Hoidon tavoitteena on
- vähentää pahenemisvaiheen haitallisia vaikutuksia potilaaseen
- ehkäistä seuraavia pahenemisvaiheita
- parantaa potilaan ennustetta «Global Strategy for the Diagnosis, Management and ...»1.
- Peruslääkehoitoon, jonka käyttö onnistuu hyvin avohoidossa, kuuluvat keuhkoputkia
avaavat lääkkeet (bronkodilataattorit), glukokortikoidi ja antibiootit.
- Hypoksemian korjaus toteutetaan hallitusti lisähapella, joka annetaan happiviiksillä tai venturinaamarilla (ks. kohta Happihoito «A4»5).
- Pahenemisvaiheen hoitona sairaalassa käytetään samoja peruslääkkeitä (bronkodilataattorit, glukokortikoidi ja antibiootit) kuin avohoidossa, mutta niiden antamistapa tai valmisteen muoto on usein erilainen (suun kautta vs. suonensisäinen; jauheinhalaattori tai ponnekaasuaerosoli vs. nebulisaattori). Lisäksi potilaiden heikentyneen yleistilan ja pahenemisvaiheen vaikeuden perusteella (kuva «Keuhkoahtaumataudin pahenemisvaihe»5) käyttöön otetaan tarvittaessa lisähappihoito ja noninvasiivinen tai invasiivinen ventilaatiohoito mekaanisilla ventilaattoreilla.
- Keuhkoahtaumataudin pahenemisvaiheeseen liittyy yleistynyt tukosalttius, minkä vuoksi sairaalassa hoidetuille potilaille tulee harkita laskimotukoksen estohoitoa. Ks. Käypä hoito -suositus Laskimotukos ja keuhkoembolia «Syvä laskimotukos ja keuhkoembolia»7, «Laskimotukos ja keuhkoembolia. Käypä hoito -suosit...»150, «Bertoletti L, Quenet S, Laporte S ym. Pulmonary em...»151.
Bronkodilataattorit
- Pahenemisvaiheen hoidon perusta ovat lyhytvaikutteiset beeta2-agonistit (salbutamoli, terbutaliini tai fenoteroli) ja antikolinergi (ipratropium) joko yksin tai lyhytvaikutteisen beeta2-agonistin ja antikolinergin yhdistelmävalmisteena.
- Sairaalaoloissa käytetään inhaloitavaa lyhytvaikutteista beeta2-agonistia (salbutamolia 5–10 mg) yksin tai yhdistettynä inhaloitavaan antikolinergiin (ipratropium 0,5 mg) tai fenoterolin ja ipratropiumin (1,25 mg / 0,5 mg) yhdistelmää. Inhaloitavan ipratropiumin liittämisestä salbutamoliin ei ilmeisesti ole hyötyä keuhkoahtaumataudin pahenemisvaiheen hoidossa «Inhaloitavan ipratropiumin liittämisestä salbutamoliin ei ilmeisesti ole hyötyä keuhkoahtaumataudin pahenemisvaiheen hoidossa.»B.
- Ponnekaasuaerosolin (salbutamoli (100 µg yhteensä 4 sumutusta ad 400 µg) anto tilanjatkeella lienee vähintään yhtä tehokasta kuin sen anto jatkuvatoimisella sumuttimella (nebulisaattori) «Hendeles L, Hatton RC, Coons TJ ym. Automatic repl...»152.
- Inhaloitava keuhkoputkia laajentava lääkitys voidaan toistaa alkuun tarvittaessa jopa 20–60 min välein 3 kertaa ja sitten 4–6 tunnin välein.
- Suonensisäisestä teofylliinista ei ole hyötyä keuhkoahtaumataudin pahenemisvaiheen hoidossa «Suonensisäisestä teofylliinista ei ole hyötyä keuhkoahtaumataudin pahenemisvaiheen hoidossa.»A.
Glukokortikoidi
- Hengitystieinfektion (nuhakuumeen) oireiden alkaessa inhaloitavan glukokortikoidin ja pitkävaikutteisen avaavan lääkeannoksen kaksinkertaistaminen 10 vuorokaudeksi ilmeisesti pienentää vaikean pahenemisvaiheen riskiä erityisesti potilailla, joilla on suuri pahenemisvaiheen riski «Hengitystieinfektion (nuhakuumeen) oireiden alkaessa inhaloitavan glukokortikoidin ja pitkävaikutteisen avaavan lääkeannoksen kaksinkertaistaminen 10 vuorokaudeksi ilmeisesti pienentää vaikean pahenemisvaiheen riskiä erityisesti suuren pahenemisvaiheen riskin potilailla.»B.
- Systeeminen glukokortikoidi nopeuttaa toipumista keuhkoahtaumataudin pahenemisvaiheesta, parantaa keuhkojen toimintaa (FEV1) ja valtimoveren hypoksemiaa, vähentää uusiutumisvaaraa ja hoidon epäonnistumisia ja lyhentää sairaalahoidon pituutta lumelääkitykseen verrattuna. Suun kautta annettavan glukokortikoidin teho on samankaltainen kuin suonensisäisesti annettavan valmisteen «Systeeminen glukokortikoidi nopeuttaa toipumista keuhkoahtaumataudin pahenemisvaiheesta, parantaa keuhkojen toimintaa (FEV1) ja valtimoveren hypoksemiaa, vähentää uusiutumisvaaraa ja hoidon epäonnistumista ja lyhentää sairaalahoidon pituutta lumelääkitykseen verrattuna. Suun kautta annettavan glukokortikoidin teho on samankaltainen kuin suonensisäisesti annettavan valmisteen.»A. Glukokortikoidikuuri aloitetaan suun kautta, ja suositeltava annos on 30–40 mg/vrk.
- 5 vuorokauden glukokortikoidikuuri suun kautta annosteltuna (esim. prednisoloni 40 mg:n vuorokausiannoksina) on ilmeisesti yhtä tehokas pahenemisvaiheen hoidossa kuin pidempi kuuri samalla annoksella «Viiden vuorokauden glukokortikoidikuuri suun kautta annosteltuna (esimerkiksi prednisoloni 40 mg:n vuorokausiannoksella) on ilmeisesti yhtä tehokas pahenemisvaiheen hoidossa kuin pidempi kuuri samalla annoksella.»B.
- Jos potilaan yleistila on heikentynyt tai jos hän ei voi niellä tai oksentelee, kuuri voidaan aloittaa suonensisäisesti antamalla 40 mg metyyliprednisolonia 6–8 tunnin välein.
Antibioottihoito
- Keuhkoahtaumataudin pahenemisvaiheessa, jolle ominaisia piirteitä ovat lisääntynyt hengenahdistus, yskösten määrä ja ysköksen märkäisyys, antibioottihoidosta saattaa olla hyötyä lumelääkkeeseen nähden. Pahenemisvaiheen vakavuudesta ja hoitopaikasta riippuvasti antibioottihoito vähentää hoidon epäonnistumista. Antibioottihoidon vaikutus kuolleisuuteen on havaittu vain teho-osastolla hoidetuilla, vaikean pahenemisvaiheen potilailla «Keuhkoahtaumataudin pahenemisvaiheessa, jolle ominaisia piirteitä ovat lisääntynyt hengenahdistus, yskösten määrä ja ysköksen märkäisyys, antibioottihoidosta saattaa olla hyötyä verrattuna lumelääkkeeseen. Riippuen pahenemisvaiheen vakavuudesta ja hoitopaikasta antibioottihoito vähentää hoidon epäonnistumista.»C.
- Todennäköisiä patogeenejä pahenemisvaiheissa ovat sekä bakteerit (H. influenzae, S. pneumoniae ja M. catarrhalis) että virukset (rino-, korona-, influenssa-, parainfluenssa-, adeno- ja RS (respiratory syncytial) -virus).
- Antibioottihoito aloitetaan keuhkoahtaumataudin pahenemisvaiheessa, jos potilaalla
esiintyy «Global Strategy for the Diagnosis, Management and ...»1, «Miravitlles M, Anzueto A. Antibiotics for acute an...»153
- lisääntynyttä yskösten märkäisyyttä ja
- hengenahdistusta tai ysköksiä.
- Keskivaikeassa pahenemisvaiheessa suun kautta annosteltavan glukokortikoidin lisäksi antibioottikuurin aloittamista tukee yskösten tyypistä riippumatta yli 40 mg/L:n CRP-arvo, kun taas alle 20 mg/L:n CRP-arvo ei puolla sitä «Butler CC, Gillespie D, White P ym. C-Reactive Pro...»155.
- Antibioottihoidossa käytetään tavanomaisia hengitysteiden infektioihin tehoavia antibiootteja ja noudatetaan alueellista antibioottien käyttöpolitiikkaa. Kuurin pituudeksi suositellaan 5–7 päivää. Empiiriseksi ensilinjan antibiootiksi voidaan valita amoksisilliini, amoksisilliinin ja klavulaanihapon yhdistelmä, doksisykliini, sulfa-trimetopriimi tai toistuvissa pahenemisvaiheissa harkinnan jälkeen moksifloksasiini «Miravitlles M, Anzueto A. Antibiotics for acute an...»153. Jos moksifloksasiinia käytetään pahenemisvaiheessa, tuberkuloosin mahdollisuus tulee huomioida ja se tulee sulkea pois ennen hoidon aloitusta.
- Jos keuhkoahtaumataudin pahenemisvaihetta komplisoi keuhkokuume, mikrobilääkityksen valinnassa noudatetaan Käypä hoito -suosituksen Alahengitystieinfektiot (aikuiset) periaatteita. Ks. Käypä hoito -suositus Alahengitystieinfektiot (aikuiset) «Aikuisten kotisyntyinen bakteerikeuhkokuume»8, «Alahengitystieinfektiot (aikuiset). Käypä hoito -s...»154.
- Jos vaikea pahenemisvaihe edellyttää tehohoitoa, hoidon epäonnistumisen riskin pienenemisen lisäksi antibioottihoito pienentää kuolleisuutta ja lyhentää sairaalahoidon pituutta «Nouira S, Marghli S, Belghith M ym. Once daily ora...»156.
- Mekaanisilla ventilaattoreilla hoidetuilta ja sellaisilta potilailta, joilla on toistuvia pahenemisvaiheita ja vaikea hengitystieahtauma, pyritään ottamaan yskösnäytteitä bakteeriviljelyä varten. Yksi mahdollinen vaikean tai toistuvien pahenemisvaiheiden aiheuttaja on hengitysteiden gramnegatiivisten (esim. Pseudomonas-laji) tai tavallisille antibiooteille resistenttien patogeenien mikrobikolonisaatio.
Fysioterapia
- Keuhkoputkien liman aktiivinen tyhjentäminen saattaa jonkin verran hyödyttää osaa keuhkoahtaumatautipotilaista «Keuhkoputkien liman aktiivinen tyhjentäminen saattaa jonkin verran hyödyttää osaa keuhkoahtaumatautipotilaista.»C.
- Liikunnallinen kuntoutus myös heti keuhkoahtaumataudin pahenemisvaiheen jälkeen on turvallista ja pienentää uuden sairaalahoidon ja kuoleman riskiä «Liikunnallinen kuntoutus myös heti keuhkoahtaumataudin pahenemisvaiheen jälkeen on turvallista ja pienentää uuden sairaalahoidon ja kuoleman riskiä.»A.
Happihoito
- Pahenemisvaiheessa valtimoveren hapenpuute eli hypoksemia on tavallinen löydös. Potilaan aikaisempi (pahenemisvaihetta edeltänyt) happeutumistilanne pyritään selvittämään.
- Koska hypoksemian aiheuttama hengityksen stimulaatio on keskeinen seikka hypokseemisen potilaan hengityksen säätelyssä, lisähappea tulee antaa varovasti tai hallitusti, mutta samalla tulee kuitenkin pyrkiä 88–92 %:n happikyllästeisyyteen. Riittämätön hapenanto pitkittää kudosten hapenpuutetta.
- Keuhkoahtaumataudin pahenemisvaiheessa hallitusti nenäviiksien avulla toteutettu hapen anto, joka tehdään happikyllästeisyyttä seuraten tavoitteeseen 88–92 %, ilmeisesti vähentää komplikaatioita ja pienentää kuolleisuutta suurivirtauksiseen happihoitoon verrattuna «Keuhkoahtaumataudin pahenemisvaiheessa happikyllästeisyyttä seuraten hallitusti nenäviiksien avulla toteutettu hapen anto tavoitteeseen 88–92 % ilmeisesti vähentää komplikaatioita ja pienentää kuolleisuutta suurivirtauksiseen happihoitoon verrattuna.»B.
- Jos hiilidioksidin kertymisen riski arvioidaan merkittäväksi, lisähappihoidon aloittamisen jälkeen on suositeltavaa tehdä verikaasuanalyysi 30–60 minuutin kuluttua tyydyttävän happikyllästeisyyden (PaO2 > 8 kPa) varmistamiseksi ja asidoosin (pH ≤ 7,35) ja hiilidioksidin kertymisen (PaCO2 > 6,0 kPa) sulkemiseksi pois. Jos hiilidioksidia kertyy merkittävästi, on suositeltavaa aloittaa NIV.
- Osalla potilailla on jo normaalitilanteessa lievä hyperkapnia (PaCO2 > 6,0 kPa), joka voi pahenemisvaiheessa merkitsevästi pahentua (PaCO2 > 7,5–8,0 kPa), mikä johtaa hiilidioksidikertymän oireiden (uneliaisuus, päänsärky, desorientaatio ja ihon punakkuus) lisääntymiseen. Oireilevien, erityisesti tajunnan häiriöistä kärsivien, potilaiden hoidossa on suositeltavaa aloittaa NIV «Global Strategy for the Diagnosis, Management and ...»1.
- Potilailla, joilla ei ole taipumusta hiilidioksidin kertymiseen, happiosapaine pyritään nostamaan arvoon 8–10 kPa «O'Driscoll BR, Howard LS, Davison AG ym. BTS guide...»157.
- Venturinaamarit (sininen venttiili 2 l/min = 24 %; valkoinen 4 l/min = 28 %; keltainen 8 l/min = 35 %; punainen 10 l/min = 40 %; vihreä 15 l/min = 60 %) takaavat luotettavimmin riittävän hapensaannin ja antavat parhaiten ennakoitavissa olevan happipitoisuuden.
- Suurivirtauksinen kostutetun hapen anto nenäkanyylilla (NHF = Nasal High-Flow) lienee hieman tavanomaista happiviiksien avulla annettavaa hoitoa tehokkaampi, mutta riittävä tutkimusnäyttö sen käytöstä pahenemisvaiheessa puuttuu «Kostutetun hapen anto suurella virtauksella nenäkanyylilla (NHF = Nasal High Flow) lienee hieman tavanomaista happiviiksien avulla annettavaa hoitoa tehokkaampi, mutta riittävä tutkimusnäyttö pahenemisvaiheessa käytöstä puuttuu.»D.
Noninvasiivinen ventilaatio (NIV)
- Sairaalaoloissa NIV:n käyttö pahenemisvaiheiden hoidossa on yleistynyt merkitsevästi ja hoito onnistuu 80–85 %:lla.
- NIV-hoitoa annetaan päivystyspoliklinikoissa ja kevyen tai tehostetun valvonnan osastoilla. Usein NIV-hoitoa jatketaan vuodeosastolla akuuteimman vaiheen jälkeen.
- Keuhkoahtaumataudin pahenemisvaiheen akuutissa hengityksen vajaatoiminnassa NIV tulee aloittaa mahdollisimman varhain. Varhain standardihoidon ohella ensilinjan interventiona aloitettu NIV helpottaa hengenahdistusta, korjaa akuuttiin tilanteeseen liittyvää respiraattorista asidoosia (suurentaa pH:ta ja vähentää PaCO2:ta), vähentää intubaation tarvetta, pienentää hoidon epäonnistumisen riskiä, lyhentää sairaalahoidon pituutta ja pienentää kuolleisuutta «Varhain standardihoidon ohella ensilinjan interventiona aloitettu NIV helpottaa hengenahdistusta, korjaa akuuttiin tilanteeseen liittyvää respiratorista asidoosia (nostaa pH:ta ja vähentää PaCO2:ta), vähentää intubaation tarvetta, pienentää hoidon epäonnistumisen riskiä, lyhentää sairaalahoidon pituutta ja pienentää kuolleisuutta.»A.
- Hoidon epäonnistumisen riski on suurentunut, jos hengitysvajauksen oireet, löydökset ja potilaan yleistila eivät kohene ensimmäisen 2 tunnin aikana NIV:n aloittamisesta.
- Kun potilaan tila pysyy NIV-hoidolla vakaana vähintään 4 tunnin ajan, hoidon saa suoraan lopettaa ilman laitteesta vieroittamisen menettelyn tarvetta «Sellares J, Ferrer M, Anton A ym. Discontinuing no...»158.
- NHF-happihoidon (suurivirtauksinen happihoito nenäkanyylilla) näyttö hyperkapnisen akuutin hengityksen vajaatoiminnan hoidossa on niin vähäistä, ettei sitä voi suositella NIV-hoidon sijaan «Frat JP, Coudroy R, Thille AW. Non-invasive ventil...»159.
Invasiivinen ventilaatiohoito
- Invasiivisen mekaanisen ventilaatiohoidon (hengityslaitehoito intubaatioputken tai henkitorviavanteen kautta) aloittaminen edellyttää aina perusteellista potilaskohtaista harkintaa. Hoito annetaan tehostetun valvonnan osastolla tai tehovalvonnassa.
- Jos potilaalla on pitkälle edennyt keuhkoahtaumatauti eikä akuutin heikkenemisen takana ole korjattavissa olevaa tekijää, tehohoitoon tulee suhtautua pidättyvästi.
Sairaalan vuodeosastolta kotiutuminen
- Vuodeosastolla annettuun hoitoon ja hoitojakson pituuteen vaikuttavat pahenemisvaiheen syy ja vaikeusaste, aiemmin sairastetut pahenemisvaiheet sekä liitännäissairaudet.
- Hoidon tavoitteet ja rajoitukset huomioon ottaen suositellaan, että ennen kotiutumista otetaan kantaa inhalaatiolääkehoidon optimointiin, liitännäissairauksien tunnistamiseen ja hoitosuunnitelmaan, kotihappihoidon tarpeen arviointiin sekä yksilöllisesti liikunnallisen kuntoutuksen suunnitteluun.
- Kotiutumisvaiheen hyvään käytäntöön sisältyvät omahoito-ohjaus, inhalaatiotekniikan tarkistus, jatkoseurannan tarpeen arviointi sekä sen ajankohdan ja paikan määrittäminen.
- Varhainen seurantakäynti (kuukauden sisällä) pienentää riskiä joutua uuden pahenemisvaiheen vuoksi sairaalahoitoon «Gavish R, Levy A, Dekel OK ym. The Association Bet...»160.
Palliatiivinen hoito
- Palliatiivisella hoidolla tarkoitetaan kuolemaan johtavaa tai henkeä uhkaavaa sairautta sairastavan potilaan ja hänen läheistensä aktiivista kokonaisvaltaista hoitoa, jolla pyritään ehkäisemään ja lievittämään kärsimystä ja vaalimaan elämänlaatua. Ks. Käypä hoito -suositus Palliatiivinen hoito ja saattohoito «Palliatiivinen hoito ja saattohoito»9, «Palliatiivinen hoito ja saattohoito. Käypä hoito -...»161.
- Keuhkoahtaumatautia voidaan pitää pitkälle edenneenä, kun potilaalla on optimaalisesta
hoidosta huolimatta useita seuraavista «Curtis JR. Palliative and end-of-life care for pat...»162, «Rocker GM, Sinuff T, Horton R ym. Advanced chronic...»163:
- huono suorituskyky
- hengenahdistusta levossa tai alle 100 m tasamaata kävellessä
- useita sairaalahoitoisia pahenemisvaiheita vuodessa
- hypoksemia tai hyperkapnia
- FEV1 alle 30 % viitearvosta
- tahatonta laihtumista
- keuhkoverenpaineen nousu
- useita muita sairauksia.
- Vaikeassakin keuhkoahtaumataudissa ennusteen määrittely on vaikeaa, joten palliatiivisen hoidon keinoja ja ajattelutapaa on mielekästä hyödyntää osana potilaan kokonaisvaltaista hoitoa ilman jyrkkiä rajoja «Pinnock H, Kendall M, Murray SA ym. Living and dyi...»164, «Patel K, Janssen DJ, Curtis JR. Advance care plann...»165.
- Pitkälle edenneen keuhkoahtaumataudin ennakoivaan hoitosuunnitelmaan (Advanced Care Planning) tulisi kuulua keskustelu potilaan toiveista ja peloista sairauden edetessä ja kuoleman lähestyessä, hoidon tavoitteista (hoitolinjaus), hoidon rajoista (esim. suhtautuminen invasiiviseen respiraattorihoitoon) sekä hoitosuunnitelmasta elämän loppuvaiheessa «Patel K, Janssen DJ, Curtis JR. Advance care plann...»165, «Curtis JR, Engelberg RA, Nielsen EL ym. Patient-ph...»166.
- Ennakoiva hoitosuunnitelma tulisi tehdä riittävän ajoissa, esimerkiksi potilaan jouduttua toistuvasti sairaalaan pahenemisvaiheiden vuoksi.
- Yleisimpiä oireita pitkälle edenneessä keuhkoahtaumataudissa ovat (% potilaista) «Blinderman CD, Homel P, Billings JA ym. Symptom di...»24, «Solano JP, Gomes B, Higginson IJ. A comparison of ...»167, «Elkington H, White P, Addington-Hall J ym. The hea...»168
- hengenahdistus (n. 90–95 %)
- yskä (n. 50–80 %)
- kipu (n. 30–70 %)
- väsymysoireyhtymä (n. 70–80 %)
- depressio (n. 35–70 %).
- Opioidi saattaa lievittää hengenahdistusta vaikeassa keuhkoahtaumataudissa, kun muut hoidot eivät tuo riittävää apua «Opioidi ilmeisesti lievittää hengenahdistusta vaikeassa keuhkoahtaumataudissa, kun muut hoidot eivät tuo riittävää apua.»C.
- Keuhkoahtaumatautipotilaiden kipua tulee hoitaa kivun hoitosuositusten mukaisesti. Elämän loppuvaiheessa tulee tarvittaessa käyttää myös opioideja. Ks. Käypä hoito -suositukset Palliatiivinen hoito ja saattohoito «Palliatiivinen hoito ja saattohoito»9, «Palliatiivinen hoito ja saattohoito. Käypä hoito -...»161ja Kipu «Kipu»10, «Kipu. Käypä hoito -suositus. Suomalaisen Lääkärise...»169.
- Hengitysvajauksen riski on pieni, kunhan opioideja annostellaan vain sen verran kuin oireiden (kipu tai hengenahdistus) lievittämiseksi on tarpeen «Jennings AL, Davies AN, Higgins JP ym. Opioids for...»170, «Abernethy AP, Currow DC, Frith P ym. Randomised, d...»171.
- Happihoito ei yleisesti ottaen lievitä hengenahdistusta enempää kuin ilmavirta, ellei potilaalla esiinny pitkäaikaisen happihoidon kriteereitä täyttävää hypoksemiaa «Abernethy AP, McDonald CF, Frith PA ym. Effect of ...»172.
- Potilas voi selvitä NIV:n avulla pahenemisvaiheesta, vaikka olisi päädytty pidättäytymään invasiivisesta ventilaattorihoidosta. Ks. kohta Pahenemisvaiheen hoito «A5»6. NIV:n tavoitteet ja tarve tulisi kuitenkin määritellä etukäteen. Palliatiivisessa mielessä hoito on mielekästä vain, jos sillä saavutetaan oirehyöty (hengenahdistuksen helpotus tai pahenemisvaiheen väistyminen) ilman, että kuolinprosessi pitkittyy «Curtis JR, Cook DJ, Sinuff T ym. Noninvasive posit...»173.
- Keuhkoahtaumatautipotilaiden muiden fyysisten ja psykososiaalisten oireiden hoidon osalta ks. Käypä hoito -suositus Palliatiivinen hoito ja saattohoito «Palliatiivinen hoito ja saattohoito»9, «Palliatiivinen hoito ja saattohoito. Käypä hoito -...»161.
Hoidon porrastus
- Primaaridiagnostiikka tehdään perus- ja työterveyshuollossa, ja sen tavoitteena ovat varhainen diagnoosi ja onnistunut erotusdiagnostiikka.
- Diagnostiikka perustuu anamneesiin (erityisesti tupakointianamneesiin), oireisiin ja spirometriatutkimukseen.
- Epäselvät tapaukset, kliinisesti merkittävät erotusdiagnostiset ongelmat ja vaikeat tautimuodot sekä poikkeuksellisen nuorena sairastuneet kuuluvat erikoissairaanhoidon selvittelyyn.
- Hoito ja seuranta toteutetaan pääosin perusterveydenhuollossa, niin että huomioidaan potilaiden monisairastavuus, ikärakenne ja sairauden yleisyys.
- Ks. lisätietoa sosiaaliturvasta (lääkekorvaukset, hoito- tai vammaistuki sekä ammatillinen ja lääkinnällinen kuntoutus) osoitteessa www.kela.fi «http://www.kela.fi/»4.
Perusterveydenhuollon ja työterveyshuollon tehtävät
- Keuhkoahtaumataudin ehkäisyssä keskeisintä ovat tupakkatuotteiden käytön ehkäisy, tupakoinnin ja nikotiiniriippuvuuden selvittäminen vastaanotolla ja tupakoinnin lopettaminen. Ks. Käypä hoito -suositus Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito «Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito»5, «Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito...»22.
- Tupakointitiedot kirjataan potilaskertomukseen.
- Tupakoinnin lopettamista tuetaan kaikissa kontakteissa. Spirometria on tärkein diagnostinen tutkimus ja tarpeellinen taudin etenemisen kliinisen arvion osana. Oirekyselyä ja mikrospirometriaa voi käyttää seulontatutkimuksena.
- Työterveyshuollossa on aiheellista pyrkiä vähentämään työntekijöiden altistumista erityisesti pölyille. Spirometria tehdään yksilöllisen tarpeen mukaan.
- Ilmiasu ja sen mukainen lääkehoito arvioidaan jokaisella seurantakäynnillä. Seurannassa ja ohjauksessa hyödynnetään astma- tai keuhkoahtaumatautihoitajien osaamista.
- Pahenemisvaiheissa turvataan riittävän varhainen hoito omahoito-ohjeilla ja tarvittaessa nopealla hoitoon pääsyllä.
- Merkittävä osa sairaalahoitoa vaativista pahenemisvaiheista hoidetaan terveyskeskusten vuodeosastoilla. Tarvittaessa potilas lähetetään erikoissairaanhoitoon, jos katsotaan, että hän kokonaisuuden kannalta hyötyy siirrosta.
- Pitkälle edenneen keuhkoahtaumataudin hoito toteutetaan kokonaisvaltaisesti niin, että hyödynnetään myös palliatiivisen hoidon mahdollisuuksia.
- Liikunnallisen ohjauksen tulee sisältyä olennaisena osana potilaskontakteihin.
- Liikunnallista kuntoutusta toteutetaan sekä yksilö- että ryhmäohjauksessa.
- Rokotukset pyritään saamaan mahdollisimman kattaviksi sekä kausi-influenssan että pneumokokin osalta.
- Työkykyarvion tekee ensisijaisesti (työterveys)lääkäri, joka tuntee potilaan työolot ja työn vaatimukset. Epäselvissä tapauksissa pyydetään lisälausunto keuhkosairauksien erikoislääkäriltä.
Erikoissairaanhoidon tehtävät
- Erikoissairaanhoidon vastuulla ovat
- tupakasta vieroittaminen kaikissa potilaskontakteissa ja vieroittamisen ohjausmenetelmien alueellinen koordinaatio
- vaativa erotusdiagnostiikka
- happihoidon ja hengityslaitehoidon tarpeen arviointi, aloitus ja seurannan koordinointi
- poikkeuksellisen nuorena sairastuneet
- ammattitautiepäilyt (ohjaaminen Työterveyslaitoksen tutkimuksiin)
- työ- ja toimintakykyarvio
- vaativa akuuttihoito
- liikunnallisen kuntoutuksen suunnittelu ja alueellinen koordinaatio sekä vaikeimmin sairaiden potilaiden kuntouttaminen
- kirurgiset hoidot (keuhkonsiirtoarviot mukaan luettuina).
- vaativat työkykyarviot
- koulutus ja hoidon alueellinen koordinointi, (spirometriatutkimusten laadunvalvonta mukaan luettuna)
- pitkälle edenneiden sairauksien hoitosuunnitelmien teko.
Suomalaisen Lääkäriseuran Duodecimin ja Suomen Keuhkolääkäriyhdistys ry:n asettama työryhmä
Keuhkoahtaumatauti-suosituksen historiatiedot «Keuhkoahtaumatauti, Käypä hoito -suosituksen historiatiedot»6
Puheenjohtaja:
Terttu Harju, dosentti, keuhkosairauksien erikoislääkäri, apulaisylilääkäri; OYS:n medisiininen tulosalue, sisätaudit ja keuhkosairaudet
Jäsenet:
Hannu Kankaanranta, professori, keuhkosairauksien erikoislääkäri, ylilääkäri; Seinäjoen keskussairaala ja Tampereen yliopisto
Milla Katajisto, LL, keuhkosairauksien erikoislääkäri, osastonlääkäri; HYKS, Sydän- ja keuhkokeskus
Maritta Kilpeläinen, dosentti, keuhkosairauksien ja keuhkoallergologian erikoislääkäri, ylilääkäri, vastuualuejohtaja, vs.; TYKS:n keuhkosairauksien vastuualue
Lauri Lehtimäki, dosentti, keuhkosairauksien ja allergologian erikoislääkäri, keuhkosairausopin apulaisprofessori; Tampereen yliopisto ja TAYS
Juho Lehto, LT, keuhkosairauksien erikoislääkäri, palliatiivisen lääketieteen erityispätevyys, ylilääkäri; TAYS ja Tampereen yliopisto
Witold Mazur, dosentti, keuhkosairauksien ja allergologian erikoislääkäri, osastonylilääkäri; HYKS, Sydän- ja keuhkokeskus
Tuula Meinander, LL, BSc, sisätautien ja kardiologian erikoislääkäri, terveydenhuoltoon erikoistuva lääkäri; TAYS Sydänsairaala, Käypä hoito -toimittaja
Sidonnaisuudet
Sidonnaisuusilmoitukset on kerätty 21.11.2019 julkaistun suosituksen laatimisen yhteydessä.
Terttu Harju: Korvaukset koulutus- ja kongressikuluista: Actelion, Boehringer-Ingelheim, Chiesi, Orion, AstraZeneca, Roche, GSK. Luento-, koulutus- ja asiantuntijapalkkiot: Actelion, Boehringer-Ingelheim, Chiesi, Orion, AstraZeneca, Roche, Mundipharma. Sivutoimet: yksityislääkäri Lääkärikeskus Mehiläinen.
Hannu Kankaanranta: Tutkimusrahoitus: AstraZeneca (maksettu instituutille). Korvaukset koulutus- ja kongressikuluista: AstraZeneca, Boehringer-Ingelheim, Orion Pharma. Luento-, koulutus- ja asiantuntijapalkkiot: AstraZeneca, Boehringer-Ingelheim, Chiesi Pharma AB, GlaxoSmithKline, Mundipharma, Novartis, Orion Pharma, SanofiGenzyme. Luottamustoimet: European Respiratory Society (College of Experts; apuraha arviointi), Pirkanmaan kulttuurirahasto (apuraha-arviointi), Allergiatutkimussäätiö (apuraha-arviointi), Nordic Severe Asthma Network (vaikean astman pohjoismainen hoitosuositus työryhmä).
Milla Katajisto: Korvaukset koulutus- ja kongressikuluista: ESMO SMT-Pharma, ERS, Mundipharma, Boehringer-ingelheim. Luento-, koulutus- ja asiantuntijapalkkiot: Orion, Boehringer, Roche, Chiesi.
Maritta Kilpeläinen: Tutkimusrahoitus: Boehringer-Ingelheim. Korvaukset koulutus- ja kongressikuluista: AstraZeneca, Roche, Boehringer-Ingelheim, Novartis. Luento-, koulutus- ja asiantuntijapalkkiot: Chiesi, Boehringer-Ingelheim, Sanofi-Genzyme, Orionpharma, Teva. Luottamustoimet: Valvira, pysyvä asiantuntija. Muut sidonnaisuudet: SKLY, hallituksen jäsen, varapj.; SAIY, apurahatoimikunnan jäsen. Sivutoimet: Erityisasiantuntija, Turun yliopisto, Kliininen laitos, Keuhkosairausopin ja kliinisen allergologian oppiaine 2019.
Lauri Lehtimäki: Korvaukset koulutus- ja kongressikuluista: AstraZeneca, GSK, Mundipharma. Luento-, koulutus- ja asiantuntijapalkkiot: ALK, AstraZeneca, Boehringer Ingelheim, Chiesi, GSK, Mundipharma, Novartis, Orion, SanofiGenzyme, Teva.
Juho Lehto: Korvaukset koulutus- ja kongressikuluista: Bristol-Myers Squibb, Kyowa Kiri. Luento-, koulutus- ja asiantuntijapalkkiot: Kyowa Kiri, Orion, Roche, Lilly, Mundipharma, Amgen, Boehringer-Ingelheim. Ohjaushankkeet: OKM, Palliatiivisen hoitotyön ja lääketieteen koulutuksen monialainen ja työelämälähtöinen kehittäminen – hanke; STM Palliatiivisen hoidon ja saattohoidon kehittämisen ohjausryhmä.
Witold Mazur: Tutkimusrahoitus: HUS. Korvaukset koulutus- ja kongressikuluista: AstraZeneca, GlaxoSmithKline, Boehringer Ingelheim, Actelion. Luento-, koulutus- ja asiantuntijapalkkiot: Boehringer Ingelheim, Chiesi, GlaxoSmithKline, Novartis, AstraZeneca, Orion.
Tuula Meinander: Korvaukset koulutus- ja kongressikuluista: Bayer. Luento-, koulutus- ja asiantuntijapalkkiot: Suomen Lääkäriliitto, Suomalainen Lääkäriseura Duodecim, Suomen Kardiologinen Seura, Bayer; Boehringer Ingelheim, Terve Media Oy. Luottamustoimet: Neuvottelukunta: Sepelvaltimotauti neuvottelukunta, sihteeri ja jäsen, Käypä hoito, Diabetes neuvottelukunta, sihteeri ja jäsen, Käypä hoito; Sydänääni-lehden toimittaja ja nettitoimittaja, Suomen Kardiologinen Seura; Eurooppalaisen kardiologikoulutuksen opetussuunnitelman päivitystoimikunnan nuorten kardiologien edustaja, European Society of Cardiology; Pohjoismaisen työryhmän jäsen, Guidelines International Network; Tays Sydänsairaala, luottamusvaltuutettu, 2018–2020.
Kirjallisuusviite
Keuhkoahtaumatauti. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Keuhkolääkäriyhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2020 (viitattu pp.kk.vvvv). Saatavilla internetissä: www.kaypahoito.fi
Tarkemmat viittausohjeet: «http://www.kaypahoito.fi/web/kh/viittaaminen»5
Vastuun rajaus
Käypä hoito -suositukset ja Vältä viisaasti -suositukset ovat asiantuntijoiden laatimia yhteenvetoja yksittäisten sairauksien diagnostiikan ja hoidon vaikuttavuudesta. Suositukset toimivat lääkärin tai muun terveydenhuollon ammattilaisen päätöksenteon tukena hoitopäätöksiä tehtäessä. Ne eivät korvaa lääkärin tai muun terveydenhuollon ammattilaisen omaa arviota yksittäisen potilaan parhaasta mahdollisesta diagnostiikasta, hoidosta ja kuntoutuksesta hoitopäätöksiä tehtäessä.
Tiedonhakukäytäntö
Systemaattinen kirjallisuushaku on hoitosuosituksen perusta. Lue lisää artikkelista khk00007
Kirjallisuutta
- Global Strategy for the Diagnosis, Management and Prevention of Chronic Obstructive Lung Disease (2019 report), Global Initiative for Chronic Obstructive Lung Disease (GOLD) 2019. Available from: http://www.goldcopd.org/ «http://www.goldcopd.org/»6
- MacNee W. Systemic inflammatory biomarkers and co-morbidities of chronic obstructive pulmonary disease. Ann Med 2013;45:291-300 «PMID: 23110517»PubMed
- Donaldson AV, Maddocks M, Martolini D ym. Muscle function in COPD: a complex interplay. Int J Chron Obstruct Pulmon Dis 2012;7:523-35 «PMID: 22973093»PubMed
- Koponen P, Borodulin K, Lundqvist A ym. (toim).Terveys, toimintakyky ja hyvinvointi Suomessa. FinTerveys 2017-tutkimus. Raportti 4/2018. http://URN:ISBN:978-952-343-105-8
- Vasankari TM, Impivaara O, Heliövaara M ym. No increase in the prevalence of COPD in two decades. Eur Respir J 2010;36:766-73 «PMID: 20693258»PubMed
- Alpha 1-antitrypsin deficiency: memorandum from a WHO meeting. Bull World Health Organ 1997;75:397-415 «PMID: 9447774»PubMed
- Kainu A, Pallasaho P, Piirilä P ym. Increase in prevalence of physician-diagnosed asthma in Helsinki during the Finnish Asthma Programme: improved recognition of asthma in primary care? A cross-sectional cohort study. Prim Care Respir J 2013;22:64-71 «PMID: 23299455»PubMed
- Kainu A, Pallasaho P, Pietinalho A. No change in prevalence of symptoms of COPD between 1996 and 2006 in Finnish adults - a report from the FinEsS Helsinki Study. Eur Clin Respir J 2016;3:31780 «PMID: 27534614»PubMed
- Andersén H, Lampela P, Nevanlinna A ym. High hospital burden in overlap syndrome of asthma and COPD. Clin Respir J 2013;7:342-6 «PMID: 23362945»PubMed
- Katajisto M, Laitinen T. Estimating the effectiveness of pulmonary rehabilitation for COPD exacerbations: reduction of hospital inpatient days during the following year. Int J Chron Obstruct Pulmon Dis 2017;12:2763-2769 «PMID: 28989279»PubMed
- Kupiainen H, Kinnula VL, Lindqvist A ym. Successful Smoking Cessation in COPD: Association with Comorbidities and Mortality. Pulm Med 2012;2012:725024 «PMID: 23213517»PubMed
- Thun MJ, Carter BD, Feskanich D ym. 50-year trends in smoking-related mortality in the United States. N Engl J Med 2013;368:351-64 «PMID: 23343064»PubMed
- Pirie K, Peto R, Reeves GK ym. The 21st century hazards of smoking and benefits of stopping: a prospective study of one million women in the UK. Lancet 2013;381:133-41 «PMID: 23107252»PubMed
- Eisner MD, Anthonisen N, Coultas D ym. An official American Thoracic Society public policy statement: Novel risk factors and the global burden of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2010;182:693-718 «PMID: 20802169»PubMed
- Mehta AJ, Miedinger D, Keidel D ym. Occupational exposure to dusts, gases, and fumes and incidence of chronic obstructive pulmonary disease in the Swiss Cohort Study on Air Pollution and Lung and Heart Diseases in Adults. Am J Respir Crit Care Med 2012;185:1292-300 «PMID: 22492989»PubMed
- Trupin L, Earnest G, San Pedro M ym. The occupational burden of chronic obstructive pulmonary disease. Eur Respir J 2003;22:462-9 «PMID: 14516136»PubMed
- Blanc PD, Iribarren C, Trupin L ym. Occupational exposures and the risk of COPD: dusty trades revisited. Thorax 2009;64:6-12 «PMID: 18678700»PubMed
- Pallasaho P, Kainu A, Sovijärvi A ym. Combined effect of smoking and occupational exposure to dusts, gases or fumes on the incidence of COPD. COPD 2014;11:88-95 «PMID: 24111617»PubMed
- Harber P, Tashkin DP, Simmons M ym. Effect of occupational exposures on decline of lung function in early chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2007;176:994-1000 «PMID: 17626912»PubMed
- Karvala K, Leino T, Oksa P ym. Altistelähtöinen työterveysseuranta. Kustannus Oy Duodecim, 2019, 1. painos
- Gooptu B, Ekeowa UI, Lomas DA. Mechanisms of emphysema in alpha1-antitrypsin deficiency: molecular and cellular insights. Eur Respir J 2009;34:475-88 «PMID: 19648523»PubMed
- Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Yleislääketieteen yhdistyksen asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2018 (viitattu 19.6.2019). Saatavilla internetissä: www.kaypahoito.fi
- Zwar NA, Marks GB, Hermiz O ym. Predictors of accuracy of diagnosis of chronic obstructive pulmonary disease in general practice. Med J Aust 2011;195:168-71 «PMID: 21843115»PubMed
- Blinderman CD, Homel P, Billings JA ym. Symptom distress and quality of life in patients with advanced chronic obstructive pulmonary disease. J Pain Symptom Manage 2009;38:115-23 «PMID: 19232893»PubMed
- Sovijärvi ARA, Kainu A, Malmberg P, Guldbrand A, Timonen K, Piirilä P. Spirometrian suorittaminen ja tulkinta – uudet suomalaiset ja monikansalliset viitearvot käyttöön. Suomen Kliinisen Fysiologian yhdistyksen ja Suomen Keuhkolääkäriyhdistyksen suositus 2015. Suom Lääkäril 2016;71:1673-81
- Aaron SD, Tan WC, Bourbeau J ym. Diagnostic Instability and Reversals of Chronic Obstructive Pulmonary Disease Diagnosis in Individuals with Mild to Moderate Airflow Obstruction. Am J Respir Crit Care Med 2017;196:306-314 «PMID: 28267373»PubMed
- Quanjer PH, Stanojevic S, Cole TJ ym. Multi-ethnic reference values for spirometry for the 3-95-yr age range: the global lung function 2012 equations. Eur Respir J 2012;40:1324-43 «PMID: 22743675»PubMed
- Xie X, de Jong PA, Oudkerk M ym. Morphological measurements in computed tomography correlate with airflow obstruction in chronic obstructive pulmonary disease: systematic review and meta-analysis. Eur Radiol 2012;22:2085-93 «PMID: 22699870»PubMed
- Agusti A, Fabbri LM, Singh D ym. Inhaled corticosteroids in COPD: friend or foe? Eur Respir J 2018;52: «PMID: 30190269»PubMed
- Kolsum U, Southworth T, Jackson N ym. Blood eosinophil counts in COPD patients compared to controls. Eur Respir J 2019;54: «PMID: 31221811»PubMed
- Jones PW, Harding G, Berry P ym. Development and first validation of the COPD Assessment Test. Eur Respir J 2009;34:648-54 «PMID: 19720809»PubMed
- Jones PW, Brusselle G, Dal Negro RW ym. Properties of the COPD assessment test in a cross-sectional European study. Eur Respir J 2011;38:29-35 «PMID: 21565915»PubMed
- Astma. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Keuhkolääkäriyhdistys ry:n, Suomen Lastenlääkäriyhdistys ry:n ja Suomen Kliinisen Fysiologian Yhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2012 (viitattu 19.6.2019. Saatavilla internetissä: www.kaypahoito.fi
- Global strategy for asthma management and prevention, Global Initiative for Asthma (GINA) 2012. Available from http://www.ginasthma.org/. «http://www.ginasthma.org/»7
- Calverley PM, Burge PS, Spencer S ym. Bronchodilator reversibility testing in chronic obstructive pulmonary disease. Thorax 2003;58:659-64 «PMID: 12885978»PubMed
- Tashkin DP, Celli B, Decramer M ym. Bronchodilator responsiveness in patients with COPD. Eur Respir J 2008;31:742-50 «PMID: 18256071»PubMed
- Albert P, Agusti A, Edwards L ym. Bronchodilator responsiveness as a phenotypic characteristic of established chronic obstructive pulmonary disease. Thorax 2012;67:701-8 «PMID: 22696176»PubMed
- Broekhuizen BD, Sachs AP, Moons KG ym. Diagnostic value of oral prednisolone test for chronic obstructive pulmonary disorders. Ann Fam Med 2011;9:104-9 «PMID: 21403135»PubMed
- Callahan CM, Dittus RS, Katz BP. Oral corticosteroid therapy for patients with stable chronic obstructive pulmonary disease. A meta-analysis. Ann Intern Med 1991;114:216-23 «PMID: 1824614»PubMed
- Woolcock AJ. Corticosteroid-resistant asthma. Definitions. Am J Respir Crit Care Med 1996;154:S45-8 «PMID: 8756787»PubMed
- Burge PS, Calverley PM, Jones PW ym. Prednisolone response in patients with chronic obstructive pulmonary disease: results from the ISOLDE study. Thorax 2003;58:654-8 «PMID: 12885977»PubMed
- Chavannes NH, Schermer TR, Wouters EF ym. Predictive value and utility of oral steroid testing for treatment of COPD in primary care: the COOPT study. Int J Chron Obstruct Pulmon Dis 2009;4:431-6 «PMID: 20037682»PubMed
- Price DB, Tinkelman DG, Halbert RJ ym. Symptom-based questionnaire for identifying COPD in smokers. Respiration 2006;73:285-95 «PMID: 16330875»PubMed
- Martinez FJ, Raczek AE, Seifer FD ym. Development and initial validation of a self-scored COPD Population Screener Questionnaire (COPD-PS). COPD 2008;5:85-95 «PMID: 18415807»PubMed
- Martinez CH, Murray S, Barr G ym. Respiratory Symptoms items from the COPD assessment test identify ever-smokers with preserved lung function at higher risk for poor respiratory outcomes. An analysis of the subpopulations and intermediate outcome measures in COPD Study Cohort. Annals Am Thorax Soc 2017;14:636-42
- Rytila P, Helin T, Kinnula V. The use of microspirometry in detecting lowered FEV1 values in current or former cigarette smokers. Prim Care Respir J 2008;17:232-7 «PMID: 18830521»PubMed
- Frith P, Crockett A, Beilby J ym. Simplified COPD screening: validation of the PiKo-6® in primary care. Prim Care Respir J 2011;20:190-8, 2 p following 198 «PMID: 21597667»PubMed
- Sichletidis L, Spyratos D, Papaioannou M ym. A combination of the IPAG questionnaire and PiKo-6® flow meter is a valuable screening tool for COPD in the primary care setting. Prim Care Respir J 2011;20:184-9, 1 p following 189 «PMID: 21597666»PubMed
- Haroon S, Jordan R, Takwoingi Y ym. Diagnostic accuracy of screening tests for COPD: a systematic review and meta-analysis. BMJ Open 2015;5:e008133 «PMID: 26450427»PubMed
- Yawn BP, Duvall K, Peabody J ym. The impact of screening tools on diagnosis of chronic obstructive pulmonary disease in primary care. Am J Prev Med 2014;47:563-75 «PMID: 25241196»PubMed
- Bolton CE, Bevan-Smith EF, Blakey JD ym. British Thoracic Society guideline on pulmonary rehabilitation in adults. Thorax 2013;68 Suppl 2:ii1-30 «PMID: 23880483»PubMed
- Katajisto M, Laitinen T. Keuhkopotilaan kuntoutus. Kirjassa: Keuhkosairaudet – Diagnostiikka ja hoito , ss. 464-70, Kustannus Oy Duodecim, 2013
- Gallefoss F, Bakke PS, Rsgaard PK. Quality of life assessment after patient education in a randomized controlled study on asthma and chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1999;159:812-7 «PMID: 10051255»PubMed
- Ferreira IM, Brooks D, Lacasse Y ym. Nutritional support for individuals with COPD: a meta-analysis. Chest 2000;117:672-8 «PMID: 10712990»PubMed
- Agusti A, Edwards LD, Celli B ym. Characteristics, stability and outcomes of the 2011 GOLD COPD groups in the ECLIPSE cohort. Eur Respir J 2013;42:636-46 «PMID: 23766334»PubMed
- Decramer M, Celli B, Kesten S ym. Effect of tiotropium on outcomes in patients with moderate chronic obstructive pulmonary disease (UPLIFT): a prespecified subgroup analysis of a randomised controlled trial. Lancet 2009;374:1171-8 «PMID: 19716598»PubMed
- Jenkins CR, Jones PW, Calverley PM ym. Efficacy of salmeterol/fluticasone propionate by GOLD stage of chronic obstructive pulmonary disease: analysis from the randomised, placebo-controlled TORCH study. Respir Res 2009;10:59 «PMID: 19566934»PubMed
- Burge PS, Calverley PM, Jones PW ym. Randomised, double blind, placebo controlled study of fluticasone propionate in patients with moderate to severe chronic obstructive pulmonary disease: the ISOLDE trial. BMJ 2000;320:1297-303 «PMID: 10807619»PubMed
- Celli BR, Thomas NE, Anderson JA ym. Effect of pharmacotherapy on rate of decline of lung function in chronic obstructive pulmonary disease: results from the TORCH study. Am J Respir Crit Care Med 2008;178:332-8 «PMID: 18511702»PubMed
- Anthonisen NR, Connett JE, Kiley JP ym. Effects of smoking intervention and the use of an inhaled anticholinergic bronchodilator on the rate of decline of FEV1. The Lung Health Study. JAMA 1994;272:1497-505 «PMID: 7966841»PubMed
- Pauwels RA, Löfdahl CG, Laitinen LA ym. Long-term treatment with inhaled budesonide in persons with mild chronic obstructive pulmonary disease who continue smoking. European Respiratory Society Study on Chronic Obstructive Pulmonary Disease. N Engl J Med 1999;340:1948-53 «PMID: 10379018»PubMed
- Vestbo J, Sørensen T, Lange P ym. Long-term effect of inhaled budesonide in mild and moderate chronic obstructive pulmonary disease: a randomised controlled trial. Lancet 1999;353:1819-23 «PMID: 10359405»PubMed
- Lipson DA, Barnhart F, Brealey N ym. Once-Daily Single-Inhaler Triple versus Dual Therapy in Patients with COPD. N Engl J Med 2018;378:1671-1680 «PMID: 29668352»PubMed
- Kankaanranta H. Keuhkoahtaumataudin uudet lääkkeet indakateroli ja roflumilasti. Suom Lääkäril 2013;68:299-306
- Thomas M, Decramer M, O'Donnell DE. No room to breathe: the importance of lung hyperinflation in COPD. Prim Care Respir J 2013;22:101-11 «PMID: 23429861»PubMed
- O'Donnell DE, Flüge T, Gerken F ym. Effects of tiotropium on lung hyperinflation, dyspnoea and exercise tolerance in COPD. Eur Respir J 2004;23:832-40 «PMID: 15218994»PubMed
- O'Donnell DE, Sciurba F, Celli B ym. Effect of fluticasone propionate/salmeterol on lung hyperinflation and exercise endurance in COPD. Chest 2006;130:647-56 «PMID: 16963658»PubMed
- Berger R, Smith D. Effect of inhaled metaproterenol on exercise performance in patients with stable "fixed" airway obstruction. Am Rev Respir Dis 1988;138:624-9 «PMID: 3202416»PubMed
- Hay JG, Stone P, Carter J ym. Bronchodilator reversibility, exercise performance and breathlessness in stable chronic obstructive pulmonary disease. Eur Respir J 1992;5:659-64 «PMID: 1628722»PubMed
- Gross NJ, Petty TL, Friedman M ym. Dose response to ipratropium as a nebulized solution in patients with chronic obstructive pulmonary disease. A three-center study. Am Rev Respir Dis 1989;139:1188-91 «PMID: 2523681»PubMed
- Higgins BG, Powell RM, Cooper S ym. Effect of salbutamol and ipratropium bromide on airway calibre and bronchial reactivity in asthma and chronic bronchitis. Eur Respir J 1991;4:415-20 «PMID: 1830277»PubMed
- Vathenen AS, Britton JR, Ebden P ym. High-dose inhaled albuterol in severe chronic airflow limitation. Am Rev Respir Dis 1988;138:850-5 «PMID: 2462383»PubMed
- O'Driscoll BR, Kay EA, Taylor RJ ym. A long-term prospective assessment of home nebulizer treatment. Respir Med 1992;86:317-25 «PMID: 1448587»PubMed
- Jenkins SC, Heaton RW, Fulton TJ ym. Comparison of domiciliary nebulized salbutamol and salbutamol from a metered-dose inhaler in stable chronic airflow limitation. Chest 1987;91:804-7 «PMID: 3556051»PubMed
- Kankaanranta H, Moilanen E. Hengitysteiden sairauksien hoidossa käytettävät lääkeaineet. [Drugs used to treat respiratory diseases]. Kirjassa: Farmakologia ja Toksikologia [In: Pharmacology and Toxicology]. Koulu M., Tuomisto J. (Eds.). 8th ed. Kustannusosakeyhtiö Medicina Oy, 2012, pp. 513-40
- Kankaanranta H, Mäkelä M. Tukkeavat keuhkosairaudet. [Obstructive lung diseases]. Kirjassa: Kliininen farmakologia ja Lääkehoito [In: Clinical Pharmacology and Drug Treatment]. Neuvonen PJ, Backman JT, HimbergJ-J, Huupponen R, Keränen T, Kivistö KT. (Eds.). 2nd ed. Kandidaattikustannus Oy, 2011, pp. 323-45
- Global Initiative for chronic obstructive lung disease. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (revised 2013). http://www.goldcopd.org «http://www.goldcopd.org»8
- Sestini P, Renzoni E, Robinson S ym. Short-acting beta 2 agonists for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2002;3:CD001495 «PMID: 12519559»PubMed
- Cates CJ, Cates MJ. Regular treatment with salmeterol for chronic asthma: serious adverse events. Cochrane Database Syst Rev 2008;3:CD006363 «PMID: 18646149»PubMed
- Decramer ML, Hanania NA, Lötvall JO ym. The safety of long-acting ß2-agonists in the treatment of stable chronic obstructive pulmonary disease. Int J Chron Obstruct Pulmon Dis 2013;8:53-64 «PMID: 23378756»PubMed
- Lee TA, Pickard AS, Au DH ym. Risk for death associated with medications for recently diagnosed chronic obstructive pulmonary disease. Ann Intern Med 2008;149:380-90 «PMID: 18794557»PubMed
- Mapel DW, Nelson LS, Lydick E ym. Survival among COPD patients using fluticasone/salmeterol in combination versus other inhaled steroids and bronchodilators alone. COPD 2007;4:127-34 «PMID: 17530506»PubMed
- Tashkin DP, Celli B, Senn S ym. A 4-year trial of tiotropium in chronic obstructive pulmonary disease. N Engl J Med 2008;359:1543-54 «PMID: 18836213»PubMed
- Vogelmeier C, Hederer B, Glaab T ym. Tiotropium versus salmeterol for the prevention of exacerbations of COPD. N Engl J Med 2011;364:1093-1103 «PMID: 21428765»PubMed
- Sims MW, Panettieri RA Jr. Profile of aclidinium bromide in the treatment of chronic obstructive pulmonary disease. Int J Chron Obstruct Pulmon Dis 2011;6:457-66 «PMID: 22003291»PubMed
- Ulrik CS. Once-daily glycopyrronium bromide, a long-acting muscarinic antagonist, for chronic obstructive pulmonary disease: a systematic review of clinical benefit. Int J Chron Obstruct Pulmon Dis 2012;7:673-8 «PMID: 23055716»PubMed
- Jones PW, Rennard SI, Agusti A ym. Efficacy and safety of once-daily aclidinium in chronic obstructive pulmonary disease. Respir Res 2011;12:55 «PMID: 21518460»PubMed
- Kerwin E, Hébert J, Gallagher N ym. Efficacy and safety of NVA237 versus placebo and tiotropium in patients with COPD: the GLOW2 study. Eur Respir J 2012;40:1106-14 «PMID: 23060624»PubMed
- Poole P, Sathananthan K, Fortescue R. Mucolytic agents versus placebo for chronic bronchitis or chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2019;5:CD001287 «PMID: 31107966»PubMed
- Rojas-Reyes MX, García Morales OM, Dennis RJ ym. Combination inhaled steroid and long-acting beta2-agonist in addition to tiotropium versus tiotropium or combination alone for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2016;6:CD008532 «PMID: 27271056»PubMed
- Appleton S, Jones T, Poole P ym. Ipratropium bromide versus short acting beta-2 agonists for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2006;2:CD001387 «PMID: 16625543»PubMed
- Appleton S, Jones T, Poole P ym. Ipratropium bromide versus long-acting beta-2 agonists for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2006;3:CD006101 «PMID: 16856113»PubMed
- Karner C, Cates CJ. Long-acting beta(2)-agonist in addition to tiotropium versus either tiotropium or long-acting beta(2)-agonist alone for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2012;4:CD008989 «PMID: 22513969»PubMed
- Farne HA, Cates CJ. Long-acting beta2-agonist in addition to tiotropium versus either tiotropium or long-acting beta2-agonist alone for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2015;10:CD008989 «PMID: 26490945»PubMed
- Cole JM, Sheehan AH, Jordan JK. Concomitant use of ipratropium and tiotropium in chronic obstructive pulmonary disease. Ann Pharmacother 2012;46:1717-21 «PMID: 23170031»PubMed
- Kankaanranta H, Lahdensuo A, Moilanen E ym. Add-on therapy options in asthma not adequately controlled by inhaled corticosteroids: a comprehensive review. Respir Res 2004;5:17 «PMID: 15509300»PubMed
- López-Campos JL, Calero Acuña C. What is in the guidelines about the pharmacological treatment of chronic obstructive pulmonary disease? Expert Rev Respir Med 2013;7:43-51 «PMID: 23551023»PubMed
- Yang IA, Clarke MS, Sim EH ym. Inhaled corticosteroids for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2012;7:CD002991 «PMID: 22786484»PubMed
- Dransfield MT, Bourbeau J, Jones PW ym. Once-daily inhaled fluticasone furoate and vilanterol versus vilanterol only for prevention of exacerbations of COPD: two replicate double-blind, parallel-group, randomised controlled trials. Lancet Respir Med 2013;1:210-23 «PMID: 24429127»PubMed
- van der Valk P, Monninkhof E, van der Palen J ym. Effect of discontinuation of inhaled corticosteroids in patients with chronic obstructive pulmonary disease: the COPE study. Am J Respir Crit Care Med 2002;166:1358-63 «PMID: 12406823»PubMed
- Cazzola M, Rogliani P. In stable COPD, long-acting muscarinic antagonist plus long-acting beta-agonists resulted in less exacerbations, pneumonia and larger improvement in FEV 1 than long-acting beta-agonists plus inhaled corticosteroids. Evid Based Med 2017;22:183-184 «PMID: 28801320»PubMed
- Nannini LJ, Cates CJ, Lasserson TJ ym. Combined corticosteroid and long-acting beta-agonist in one inhaler versus inhaled steroids for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2007;4:CD006826 «PMID: 17943917»PubMed
- Loke YK, Cavallazzi R, Singh S. Risk of fractures with inhaled corticosteroids in COPD: systematic review and meta-analysis of randomised controlled trials and observational studies. Thorax 2011;66:699-708 «PMID: 21602540»PubMed
- Bafadhel M, Peterson S, De Blas MA ym. Predictors of exacerbation risk and response to budesonide in patients with chronic obstructive pulmonary disease: a post-hoc analysis of three randomised trials. Lancet Respir Med 2018;6:117-126 «PMID: 29331313»PubMed
- Siddiqui SH, Guasconi A, Vestbo J ym. Blood Eosinophils: A Biomarker of Response to Extrafine Beclomethasone/Formoterol in Chronic Obstructive Pulmonary Disease. Am J Respir Crit Care Med 2015;192:523-5 «PMID: 26051430»PubMed
- Papi A, Vestbo J, Fabbri L ym. Extrafine inhaled triple therapy versus dual bronchodilator therapy in chronic obstructive pulmonary disease (TRIBUTE): a double-blind, parallel group, randomised controlled trial. Lancet 2018;391:1076-1084 «PMID: 29429593»PubMed
- Pascoe S, Locantore N, Dransfield MT ym. Blood eosinophil counts, exacerbations, and response to the addition of inhaled fluticasone furoate to vilanterol in patients with chronic obstructive pulmonary disease: a secondary analysis of data from two parallel randomised controlled trials. Lancet Respir Med 2015;3:435-42 «PMID: 25878028»PubMed
- Vestbo J, Papi A, Corradi M ym. Single inhaler extrafine triple therapy versus long-acting muscarinic antagonist therapy for chronic obstructive pulmonary disease (TRINITY): a double-blind, parallel group, randomised controlled trial. Lancet 2017;389:1919-1929 «PMID: 28385353»PubMed
- Casanova C, Celli BR, de-Torres JP ym. Prevalence of persistent blood eosinophilia: relation to outcomes in patients with COPD. Eur Respir J 2017;50: «PMID: 29167301»PubMed
- Vedel-Krogh S, Nielsen SF, Lange P ym. Blood Eosinophils and Exacerbations in Chronic Obstructive Pulmonary Disease. The Copenhagen General Population Study. Am J Respir Crit Care Med 2016;193:965-74 «PMID: 26641631»PubMed
- Hogg JC, McDonough JE, Gosselink JV ym. What drives the peripheral lung-remodeling process in chronic obstructive pulmonary disease? Proc Am Thorac Soc 2009;6:668-72 «PMID: 20008873»PubMed
- Pavord ID, Lettis S, Anzueto A ym. Blood eosinophil count and pneumonia risk in patients with chronic obstructive pulmonary disease: a patient-level meta-analysis. Lancet Respir Med 2016;4:731-741 «PMID: 27460163»PubMed
- Chapman KR, Hurst JR, Frent SM ym. Long-Term Triple Therapy De-escalation to Indacaterol/Glycopyrronium in Patients with Chronic Obstructive Pulmonary Disease (SUNSET): A Randomized, Double-Blind, Triple-Dummy Clinical Trial. Am J Respir Crit Care Med 2018;198:329-339 «PMID: 29779416»PubMed
- Nannini L, Cates CJ, Lasserson TJ ym. Combined corticosteroid and long-acting beta-agonist in one inhaler versus placebo for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2007;4:CD003794 «PMID: 17943798»PubMed
- Nannini LJ, Lasserson TJ, Poole P. Combined corticosteroid and long-acting beta(2)-agonist in one inhaler versus long-acting beta(2)-agonists for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2012;9:CD006829 «PMID: 22972099»PubMed
- Calverley PM, Anderson JA, Celli B ym. Salmeterol and fluticasone propionate and survival in chronic obstructive pulmonary disease. N Engl J Med 2007;356:775-89 «PMID: 17314337»PubMed
- Aaron SD, Vandemheen KL, Fergusson D ym. Tiotropium in combination with placebo, salmeterol, or fluticasone-salmeterol for treatment of chronic obstructive pulmonary disease: a randomized trial. Ann Intern Med 2007;146:545-55 «PMID: 17310045»PubMed
- Welte T, Miravitlles M, Hernandez P ym. Efficacy and tolerability of budesonide/formoterol added to tiotropium in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2009;180:741-50 «PMID: 19644045»PubMed
- Cazzola M, Andò F, Santus P ym. A pilot study to assess the effects of combining fluticasone propionate/salmeterol and tiotropium on the airflow obstruction of patients with severe-to-very severe COPD. Pulm Pharmacol Ther 2007;20:556-61 «PMID: 16914336»PubMed
- Karner C, Cates CJ. Combination inhaled steroid and long-acting beta(2)-agonist in addition to tiotropium versus tiotropium or combination alone for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2011;3:CD008532 «PMID: 21412920»PubMed
- Nielsen R, Kankaanranta H, Bjermer L ym. Cost effectiveness of adding budesonide/formoterol to tiotropium in COPD in four Nordic countries. Respir Med 2013;107:1709-21 «PMID: 23856511»PubMed
- Oba Y, Keeney E, Ghatehorde N ym. Dual combination therapy versus long-acting bronchodilators alone for chronic obstructive pulmonary disease (COPD): a systematic review and network meta-analysis. Cochrane Database Syst Rev 2018;12:CD012620 «PMID: 30521694»PubMed
- Cazzola M, Rogliani P, Calzetta L ym. Triple therapy versus single and dual long-acting bronchodilator therapy in COPD: a systematic review and meta-analysis. Eur Respir J 2018;52: «PMID: 30309975»PubMed
- Chapman KR, Hurst JR, Frent SM ym. Long-Term Triple Therapy De-escalation to Indacaterol/Glycopyrronium in Patients with Chronic Obstructive Pulmonary Disease (SUNSET): A Randomized, Double-Blind, Triple-Dummy Clinical Trial. Am J Respir Crit Care Med 2018;198:329-339 «PMID: 29779416»PubMed
- Calverley PMA, Tetzlaff K, Vogelmeier C ym. Eosinophilia, Frequent Exacerbations, and Steroid Response in Chronic Obstructive Pulmonary Disease. Am J Respir Crit Care Med 2017;196:1219-1221 «PMID: 28306321»PubMed
- Chong J, Poole P, Leung B ym. Phosphodiesterase 4 inhibitors for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2011;5:CD002309 «PMID: 21563134»PubMed
- Calverley PM, Rabe KF, Goehring UM ym. Roflumilast in symptomatic chronic obstructive pulmonary disease: two randomised clinical trials. Lancet 2009;374:685-94 «PMID: 19716960»PubMed
- Fabbri LM, Calverley PM, Izquierdo-Alonso JL ym. Roflumilast in moderate-to-severe chronic obstructive pulmonary disease treated with longacting bronchodilators: two randomised clinical trials. Lancet 2009;374:695-703 «PMID: 19716961»PubMed
- Walters JA, Walters EH, Wood-Baker R. Oral corticosteroids for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2005;3:CD005374 «PMID: 16034972»PubMed
- Schols AM, Wesseling G, Kester AD ym. Dose dependent increased mortality risk in COPD patients treated with oral glucocorticoids. Eur Respir J 2001;17:337-42 «PMID: 11405508»PubMed
- Barnes PJ. Theophylline. Am J Respir Crit Care Med 2013;188:901-6 «PMID: 23672674»PubMed
- Cazzola M, Page CP, Calzetta L ym. Pharmacology and therapeutics of bronchodilators. Pharmacol Rev 2012;64:450-504 «PMID: 22611179»PubMed
- Rossi A, Kristufek P, Levine BE ym. Comparison of the efficacy, tolerability, and safety of formoterol dry powder and oral, slow-release theophylline in the treatment of COPD. Chest 2002;121:1058-69 «PMID: 11948033»PubMed
- ZuWallack RL, Mahler DA, Reilly D ym. Salmeterol plus theophylline combination therapy in the treatment of COPD. Chest 2001;119:1661-70 «PMID: 11399688»PubMed
- Zhou Y, Wang X, Zeng X ym. Positive benefits of theophylline in a randomized, double-blind, parallel-group, placebo-controlled study of low-dose, slow-release theophylline in the treatment of COPD for 1 year. Respirology 2006;11:603-10 «PMID: 16916334»PubMed
- Cui Y, Luo L, Li C ym. Long-term macrolide treatment for the prevention of acute exacerbations in COPD: a systematic review and meta-analysis. Int J Chron Obstruct Pulmon Dis 2018;13:3813-3829 «PMID: 30538443»PubMed
- Han MK, Tayob N, Murray S ym. Predictors of chronic obstructive pulmonary disease exacerbation reduction in response to daily azithromycin therapy. Am J Respir Crit Care Med 2014;189:1503-8 «PMID: 24779680»PubMed
- Poole P, Black PN, Cates CJ. Mucolytic agents for chronic bronchitis or chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2012;8:CD001287 «PMID: 22895919»PubMed
- Yawn BP, Colice GL, Hodder R. Practical aspects of inhaler use in the management of chronic obstructive pulmonary disease in the primary care setting. Int J Chron Obstruct Pulmon Dis 2012;7:495-502 «PMID: 22888221»PubMed
- Laube BL, Janssens HM, de Jongh FH ym. What the pulmonary specialist should know about the new inhalation therapies. Eur Respir J 2011;37:1308-31 «PMID: 21310878»PubMed
- Wieshammer S, Dreyhaupt J. Dry powder inhalers: which factors determine the frequency of handling errors? Respiration 2008;75:18-25 «PMID: 17911976»PubMed
- Chapman KR, Voshaar TH and Virchow JC. Inhaler choice in primary practice Eur Respir rev 2005;14:117-22
- Marin JM, Soriano JB, Carrizo SJ ym. Outcomes in patients with chronic obstructive pulmonary disease and obstructive sleep apnea: the overlap syndrome. Am J Respir Crit Care Med 2010;182:325-31 «PMID: 20378728»PubMed
- Orens JB, Estenne M, Arcasoy S ym. International guidelines for the selection of lung transplant candidates: 2006 update--a consensus report from the Pulmonary Scientific Council of the International Society for Heart and Lung Transplantation. J Heart Lung Transplant 2006;25:745-55 «PMID: 16818116»PubMed
- Celli BR, Cote CG, Marin JM ym. The body-mass index, airflow obstruction, dyspnea, and exercise capacity index in chronic obstructive pulmonary disease. N Engl J Med 2004;350:1005-12 «PMID: 14999112»PubMed
- Inci I, Schuurmans M, Ehrsam J ym. Lung transplantation for emphysema: impact of age on short- and long-term survival. Eur J Cardiothorac Surg 2015;48:906-9 «PMID: 25602056»PubMed
- Papi A, Bellettato CM, Braccioni F ym. Infections and airway inflammation in chronic obstructive pulmonary disease severe exacerbations. Am J Respir Crit Care Med 2006;173:1114-21 «PMID: 16484677»PubMed
- Hoogendoorn M, Hoogenveen RT, Rutten-van Mölken MP ym. Case fatality of COPD exacerbations: a meta-analysis and statistical modelling approach. Eur Respir J 2011;37:508-15 «PMID: 20595157»PubMed
- Patel AR, Kowlessar BS, Donaldson GC ym. Cardiovascular risk, myocardial injury, and exacerbations of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2013;188:1091-9 «PMID: 24033321»PubMed
- Laskimotukos ja keuhkoembolia. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Kardiologisen Seuran asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2016 (viitattu 19.6.2019). Saatavilla internetissä: www.kaypahoito.fi
- Bertoletti L, Quenet S, Laporte S ym. Pulmonary embolism and 3-month outcomes in 4036 patients with venous thromboembolism and chronic obstructive pulmonary disease: data from the RIETE registry. Respir Res 2013;14:75 «PMID: 23865769»PubMed
- Hendeles L, Hatton RC, Coons TJ ym. Automatic replacement of albuterol nebulizer therapy by metered-dose inhaler and valved holding chamber. Am J Health Syst Pharm 2005;62:1053-61 «PMID: 15901590»PubMed
- Miravitlles M, Anzueto A. Antibiotics for acute and chronic respiratory infection in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2013;188:1052-7 «PMID: 23924286»PubMed
- Alahengitystieinfektiot (aikuiset). Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Keuhkolääkäriyhdistyksen, Suomen Infektiolääkärit ry:n ja Suomen Yleislääketieteen Yhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2015 (viitattu 19.6.2019). Saatavilla internetissä: www.kaypahoito.fi
- Butler CC, Gillespie D, White P ym. C-Reactive Protein Testing to Guide Antibiotic Prescribing for COPD Exacerbations. N Engl J Med 2019;381:111-120 «PMID: 31291514»PubMed
- Nouira S, Marghli S, Belghith M ym. Once daily oral ofloxacin in chronic obstructive pulmonary disease exacerbation requiring mechanical ventilation: a randomised placebo-controlled trial. Lancet 2001;358:2020-5 «PMID: 11755608»PubMed
- O'Driscoll BR, Howard LS, Davison AG ym. BTS guideline for emergency oxygen use in adult patients. Thorax 2008;63 Suppl 6:vi1-68 «PMID: 18838559»PubMed
- Sellares J, Ferrer M, Anton A ym. Discontinuing noninvasive ventilation in severe chronic obstructive pulmonary disease exacerbations: a randomised controlled trial. Eur Respir J 2017;50: «PMID: 28679605»PubMed
- Frat JP, Coudroy R, Thille AW. Non-invasive ventilation or high-flow oxygen therapy: When to choose one over the other? Respirology 2019;24:724-731 «PMID: 30406954»PubMed
- Gavish R, Levy A, Dekel OK ym. The Association Between Hospital Readmission and Pulmonologist Follow-up Visits in Patients With COPD. Chest 2015;148:375-381 «PMID: 25611698»PubMed
- Palliatiivinen hoito ja saattohoito. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Palliatiivisen Lääketieteen yhdistyksen asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2019 (viitattu 19.6.2019). Saatavilla internetissä: www.kaypahoito.fi
- Curtis JR. Palliative and end-of-life care for patients with severe COPD. Eur Respir J 2008;32:796-803 «PMID: 17989116»PubMed
- Rocker GM, Sinuff T, Horton R ym. Advanced chronic obstructive pulmonary disease: innovative approaches to palliation. J Palliat Med 2007;10:783-97 «PMID: 17592991»PubMed
- Pinnock H, Kendall M, Murray SA ym. Living and dying with severe chronic obstructive pulmonary disease: multi-perspective longitudinal qualitative study. BMJ 2011;342:d142 «PMID: 21262897»PubMed
- Patel K, Janssen DJ, Curtis JR. Advance care planning in COPD. Respirology 2012;17:72-8 «PMID: 22008225»PubMed
- Curtis JR, Engelberg RA, Nielsen EL ym. Patient-physician communication about end-of-life care for patients with severe COPD. Eur Respir J 2004;24:200-5 «PMID: 15332385»PubMed
- Solano JP, Gomes B, Higginson IJ. A comparison of symptom prevalence in far advanced cancer, AIDS, heart disease, chronic obstructive pulmonary disease and renal disease. J Pain Symptom Manage 2006;31:58-69 «PMID: 16442483»PubMed
- Elkington H, White P, Addington-Hall J ym. The healthcare needs of chronic obstructive pulmonary disease patients in the last year of life. Palliat Med 2005;19:485-91 «PMID: 16218161»PubMed
- Kipu. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Anestesiologiyhdistyksen ja Suomen Yleislääketieteen yhdistyksen asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2015 (viitattu 19.6.2019). Saatavilla internetissä: www.kaypahoito.fi
- Jennings AL, Davies AN, Higgins JP ym. Opioids for the palliation of breathlessness in terminal illness. Cochrane Database Syst Rev 2001;4:CD002066 «PMID: 11687137»PubMed
- Abernethy AP, Currow DC, Frith P ym. Randomised, double blind, placebo controlled crossover trial of sustained release morphine for the management of refractory dyspnoea. BMJ 2003;327:523-8 «PMID: 12958109»PubMed
- Abernethy AP, McDonald CF, Frith PA ym. Effect of palliative oxygen versus room air in relief of breathlessness in patients with refractory dyspnoea: a double-blind, randomised controlled trial. Lancet 2010;376:784-93 «PMID: 20816546»PubMed
- Curtis JR, Cook DJ, Sinuff T ym. Noninvasive positive pressure ventilation in critical and palliative care settings: understanding the goals of therapy. Crit Care Med 2007;35:932-9 «PMID: 17255876»PubMed
- Ahmadi Z, Currow DC, Ekström M. Palliative oxygen for chronic breathlessness: what new evidence? Curr Opin Support Palliat Care 2017;11:159-164 «PMID: 28644301»PubMed
- Alfageme I, Vazquez R, Reyes N ym. Clinical efficacy of anti-pneumococcal vaccination in patients with COPD. Thorax 2006;61:189-95 «PMID: 16227328»PubMed
- Austin MA, Wills KE, Blizzard L ym. Effect of high flow oxygen on mortality in chronic obstructive pulmonary disease patients in prehospital setting: randomised controlled trial. BMJ 2010;341:c5462 «PMID: 20959284»PubMed
- Barnes H, McDonald J, Smallwood N ym. Opioids for the palliation of refractory breathlessness in adults with advanced disease and terminal illness. Cochrane Database Syst Rev 2016;3:CD011008 «PMID: 27030166»PubMed
- Barr RG, Rowe BH, Camargo CA. Methylxanthines for exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2003;2:CD002168 «PMID: 12804425»PubMed
- Booth S. Improving research methodology in breathlessness: a meeting convened by the MRC clinical trials unit and the Cicely Saunders Foundation. Palliat Med 2006;20:219-20 «PMID: 16764228»PubMed
- Bradley JM, O'Neill B. Short-term ambulatory oxygen for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2005;4:CD004356 «PMID: 16235359»PubMed
- Budweiser S, Hitzl AP, Jörres RA ym. Impact of noninvasive home ventilation on long-term survival in chronic hypercapnic COPD: a prospective observational study. Int J Clin Pract 2007;61:1516-22 «PMID: 17686094»PubMed
- Burrows B. Predictors of loss of lung function and mortality in obstructive lung diseases. Eur Respir Rev 1991;1:340-5
- Casanova C, Celli BR, Tost L ym. Long-term controlled trial of nocturnal nasal positive pressure ventilation in patients with severe COPD. Chest 2000;118:1582-90 «PMID: 11115443»PubMed
- Chaouat A, Weitzenblum E, Kessler R ym. A randomized trial of nocturnal oxygen therapy in chronic obstructive pulmonary disease patients. Eur Respir J 1999;14:1002-8 «PMID: 10596681»PubMed
- Clini E, Sturani C, Rossi A ym. The Italian multicentre study on noninvasive ventilation in chronic obstructive pulmonary disease patients. Eur Respir J 2002;20:529-38 «PMID: 12358325»PubMed
- Continuous or nocturnal oxygen therapy in hypoxemic chronic obstructive lung disease: a clinical trial. Nocturnal Oxygen Therapy Trial Group. Ann Intern Med 1980;93:391-8
- Cranston JM, Crockett AJ, Moss JR ym. Domiciliary oxygen for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2005;4:CD001744 «PMID: 16235285»PubMed
- Currow DC, Ekström M, Johnson MJ. The strength of evidence: low dose morphine for chronic breathlessness. Intern Med J 2018;48:102-103 «PMID: 29314519»PubMed
- Currow DC, McDonald C, Oaten S ym. Once-daily opioids for chronic dyspnea: a dose increment and pharmacovigilance study. J Pain Symptom Manage 2011;42:388-99 «PMID: 21458217»PubMed
- de Jong YP, Uil SM, Grotjohan HP ym. Oral or IV prednisolone in the treatment of COPD exacerbations: a randomized, controlled, double-blind study. Chest 2007;132:1741-7 «PMID: 17646228»PubMed
- Devine EC, Pearcy J. Meta-analysis of the effects of psychoeducational care in adults with chronic obstructive pulmonary disease. Patient Educ Couns 1996;29:167-78 «PMID: 9006233»PubMed
- Díaz O, Bégin P, Torrealba B ym. Effects of noninvasive ventilation on lung hyperinflation in stable hypercapnic COPD. Eur Respir J 2002;20:1490-8 «PMID: 12503709»PubMed
- Doll R, Peto R, Wheatley K ym. Mortality in relation to smoking: 40 years' observations on male British doctors. BMJ 1994;309:901-11 «PMID: 7755693»PubMed
- Duffy N, Walker P, Diamantea F ym. Intravenous aminophylline in patients admitted to hospital with non-acidotic exacerbations of chronic obstructive pulmonary disease: a prospective randomised controlled trial. Thorax 2005;60:713-7 «PMID: 15939732»PubMed
- Eisner MD, Balmes J, Katz PP ym. Lifetime environmental tobacco smoke exposure and the risk of chronic obstructive pulmonary disease. Environ Health 2005;4:7 «PMID: 15890079»PubMed
- Ekström M, Ahmadi Z, Bornefalk-Hermansson A ym. Oxygen for breathlessness in patients with chronic obstructive pulmonary disease who do not qualify for home oxygen therapy. Cochrane Database Syst Rev 2016;11:CD006429 «PMID: 27886372»PubMed
- Ekström M, Nilsson F, Abernethy AA ym. Effects of opioids on breathlessness and exercise capacity in chronic obstructive pulmonary disease. A systematic review. Ann Am Thorac Soc 2015;12:1079-92 «PMID: 25803110»PubMed
- Ferreira IM, Brooks D, White J ym. Nutritional supplementation for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2012;12:CD000998 «PMID: 23235577»PubMed
- Fletcher C, Peto R. The natural history of chronic airflow obstruction. Br Med J 1977;1:1645-8 «PMID: 871704»PubMed
- Forey BA, Thornton AJ, Lee PN. Systematic review with meta-analysis of the epidemiological evidence relating smoking to COPD, chronic bronchitis and emphysema. BMC Pulm Med 2011;11:36 «PMID: 21672193»PubMed
- Górecka D, Gorzelak K, Sliwinski P ym. Effect of long-term oxygen therapy on survival in patients with chronic obstructive pulmonary disease with moderate hypoxaemia. Thorax 1997;52:674-9 «PMID: 9337824»PubMed
- Henningfield JE. Nicotine medications for smoking cessation. N Engl J Med 1995;333:1196-203 «PMID: 7565976»PubMed
- Hersh CP, Dahl M, Ly NP ym. Chronic obstructive pulmonary disease in alpha1-antitrypsin PI MZ heterozygotes: a meta-analysis. Thorax 2004;59:843-9 «PMID: 15454649»PubMed
- Hersh CP, Hokanson JE, Lynch DA ym. Family history is a risk factor for COPD. Chest 2011;140:343-350 «PMID: 21310839»PubMed
- Holland AE, Hill CJ, Rasekaba T ym. Updating the minimal important difference for six-minute walk distance in patients with chronic obstructive pulmonary disease. Arch Phys Med Rehabil 2010;91:221-5 «PMID: 20159125»PubMed
- Huang W, Wang WR, Deng B ym. Several clinical interests regarding lung volume reduction surgery for severe emphysema: meta-analysis and systematic review of randomized controlled trials. J Cardiothorac Surg 2011;6:148 «PMID: 22074613»PubMed
- Jaakkola MS, Jaakkola JJ. Effects of environmental tobacco smoke on the respiratory health of adults. Scand J Work Environ Health 2002;28 Suppl 2:52-70 «PMID: 12058803»PubMed
- Jindal SK, Aggarwal AN, Chaudhry K ym. A multicentric study on epidemiology of chronic obstructive pulmonary disease and its relationship with tobacco smoking and environmental tobacco smoke exposure. Indian J Chest Dis Allied Sci 2006;48:23-9 «PMID: 16482948»PubMed
- Johannessen A, Bakke PS, Hardie JA ym. Association of exposure to environmental tobacco smoke in childhood with chronic obstructive pulmonary disease and respiratory symptoms in adults. Respirology 2012;17:499-505 «PMID: 22248329»PubMed
- Johnson MJ, Bland JM, Oxberry SG ym. Clinically important differences in the intensity of chronic refractory breathlessness. J Pain Symptom Manage 2013;46:957-63 «PMID: 23608121»PubMed
- Karner C, Chong J, Poole P. Tiotropium versus placebo for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2012;7:CD009285 «PMID: 22786525»PubMed
- Kim ES, Lee H, Kim SJ ym. Effectiveness of high-flow nasal cannula oxygen therapy for acute respiratory failure with hypercapnia. J Thorac Dis 2018;10:882-888 «PMID: 29607161»PubMed
- Kolodziej MA, Jensen L, Rowe B ym. Systematic review of noninvasive positive pressure ventilation in severe stable COPD. Eur Respir J 2007;30:293-306 «PMID: 17459893»PubMed
- Kopsaftis Z, Wood-Baker R, Poole P. Influenza vaccine for chronic obstructive pulmonary disease (COPD). Cochrane Database Syst Rev 2018;6:CD002733 «PMID: 29943802»PubMed
- McCrory DC, Brown CD. Anti-cholinergic bronchodilators versus beta2-sympathomimetic agents for acute exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2002;4:CD003900 «PMID: 12519615»PubMed
- McEvoy RD, Pierce RJ, Hillman D ym. Nocturnal non-invasive nasal ventilation in stable hypercapnic COPD: a randomised controlled trial. Thorax 2009;64:561-6 «PMID: 19213769»PubMed
- Moore RP, Berlowitz DJ, Denehy L ym. A randomised trial of domiciliary, ambulatory oxygen in patients with COPD and dyspnoea but without resting hypoxaemia. Thorax 2011;66:32-7 «PMID: 20880870»PubMed
- Nici L, Donner C, Wouters E ym. American Thoracic Society/European Respiratory Society statement on pulmonary rehabilitation. Am J Respir Crit Care Med 2006;173:1390-413 «PMID: 16760357»PubMed
- Nonoyama ML, Brooks D, Lacasse Y ym. Oxygen therapy during exercise training in chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2007;2:CD005372 «PMID: 17443585»PubMed
- O'Driscoll BR, Neill J, Pulakal S ym. A crossover study of short burst oxygen therapy (SBOT) for the relief of exercise-induced breathlessness in severe COPD. BMC Pulm Med 2011;11:23 «PMID: 21569473»PubMed
- Osadnik CR, McDonald CF, Jones AP ym. Airway clearance techniques for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2012;3:CD008328 «PMID: 22419331»PubMed
- Osadnik CR, Tee VS, Carson-Chahhoud KV ym. Non-invasive ventilation for the management of acute hypercapnic respiratory failure due to exacerbation of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2017;7:CD004104 «PMID: 28702957»PubMed
- Peat JK, Woolcock AJ, Cullen K. Decline of lung function and development of chronic airflow limitation: a longitudinal study of non-smokers and smokers in Busselton, Western Australia. Thorax 1990;45:32-7 «PMID: 2321175»PubMed
- Peto R, Lopez AD, Boreham J ym. Mortality from tobacco in developed countries: indirect estimation from national vital statistics. Lancet 1992;339:1268-78 «PMID: 1349675»PubMed
- Pilcher J, Eastlake L, Richards M ym. Physiological effects of titrated oxygen via nasal high-flow cannulae in COPD exacerbations: A randomized controlled cross-over trial. Respirology 2017;22:1149-1155 «PMID: 28470831»PubMed
- Puhan M, Scharplatz M, Troosters T ym. Pulmonary rehabilitation following exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2009;1:CD005305 «PMID: 19160250»PubMed
- Puhan MA, Gimeno-Santos E, Scharplatz M ym. Pulmonary rehabilitation following exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2011;10:CD005305 «PMID: 21975749»PubMed
- Quantrill SJ, White R, Crawford A ym. Short burst oxygen therapy after activities of daily living in the home in chronic obstructive pulmonary disease. Thorax 2007;62:702-5 «PMID: 17311844»PubMed
- Ram FS, Jones PW, Castro AA ym. Oral theophylline for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2002;4:CD003902 «PMID: 12519617»PubMed
- Ries AL. Minimally clinically important difference for the UCSD Shortness of Breath Questionnaire, Borg Scale, and Visual Analog Scale. COPD 2005;2:105-10 «PMID: 17136970»PubMed
- Ryrsø CK, Godtfredsen NS, Kofod LM ym. Lower mortality after early supervised pulmonary rehabilitation following COPD-exacerbations: a systematic review and meta-analysis. BMC Pulm Med 2018;18:154 «PMID: 30219047»PubMed
- Seersholm N, Kok-Jensen A, Dirksen A. Survival of patients with severe alpha 1-antitrypsin deficiency with special reference to non-index cases. Thorax 1994;49:695-8 «PMID: 8066566»PubMed
- Stolz D, Hirsch HH, Schilter D ym. Intensified Therapy with Inhaled Corticosteroids and Long-Acting ß2-Agonists at the Onset of Upper Respiratory Tract Infection to Prevent Chronic Obstructive Pulmonary Disease Exacerbations. A Multicenter, Randomized, Double-Blind, Placebo-controlled Trial. Am J Respir Crit Care Med 2018;197:1136-1146 «PMID: 29266965»PubMed
- Struik FM, Lacasse Y, Goldstein R ym. Nocturnal non-invasive positive pressure ventilation for stable chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2013;6:CD002878 «PMID: 23766138»PubMed
- Tanash HA, Nilsson PM, Nilsson JA ym. Clinical course and prognosis of never-smokers with severe alpha-1-antitrypsin deficiency (PiZZ). Thorax 2008;63:1091-5 «PMID: 18682522»PubMed
- Tashkin DP, Clark VA, Coulson AH ym. The UCLA population studies of chronic obstructive respiratory disease. VIII. Effects of smoking cessation on lung function: a prospective study of a free-living population. Am Rev Respir Dis 1984;130:707-15 «PMID: 6497153»PubMed
- Walters JA, Gibson PG, Wood-Baker R ym. Systemic corticosteroids for acute exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2009;1:CD001288 «PMID: 19160195»PubMed
- Walters JA, Tang JN, Poole P ym. Pneumococcal vaccines for preventing pneumonia in chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2017;1:CD001390 «PMID: 28116747»PubMed
- van Agteren JE, Carson KV, Tiong LU ym. Lung volume reduction surgery for diffuse emphysema. Cochrane Database Syst Rev 2016;10:CD001001 «PMID: 27739074»PubMed
- van Wetering CR, Hoogendoorn M, Mol SJ ym. Short- and long-term efficacy of a community-based COPD management programme in less advanced COPD: a randomised controlled trial. Thorax 2010;65:7-13 «PMID: 19703824»PubMed
- Vineis P, Airoldi L, Veglia F ym. Environmental tobacco smoke and risk of respiratory cancer and chronic obstructive pulmonary disease in former smokers and never smokers in the EPIC prospective study. BMJ 2005;330:277 «PMID: 15681570»PubMed
- Vollenweider DJ, Frei A, Steurer-Stey CA ym. Antibiotics for exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2018;10:CD010257 «PMID: 30371937»PubMed
- www.nice.org.uk/guidance/CG101 (accessed 19.11.2012) National Institute for Health and Clinical Excellence. Chronic Obstructive Pulmonary Disease. NICE Clinical Guideline 201. 2010
- Yin P, Jiang CQ, Cheng KK ym. Passive smoking exposure and risk of COPD among adults in China: the Guangzhou Biobank Cohort Study. Lancet 2007;370:751-7 «PMID: 17765524»PubMed
- Lenferink A, Brusse-Keizer M, van der Valk PD ym. Self-management interventions including action plans for exacerbations versus usual care in patients with chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2017;8:CD011682 «PMID: 28777450»PubMed
- Lee TA, Weaver FM, Weiss KB. Impact of pneumococcal vaccination on pneumonia rates in patients with COPD and asthma. J Gen Intern Med 2007;22:62-7 «PMID: 17351841»PubMed
- Nannini L, Poole P, Milan SJ ym. Combined corticosteroid and long-acting beta2-agonist in one inhaler versus placebo for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2013;11:CD003794 «PMID: 24214176»PubMed
- Chong J, Leung B, Poole P. Phosphodiesterase 4 inhibitors for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2013;:CD002309 «PMID: 24190161»PubMed
- Long term domiciliary oxygen therapy in chronic hypoxic cor pulmonale complicating chronic bronchitis and emphysema. Report of the Medical Research Council Working Party. Lancet 1981;1:681-6 «PMID: 6110912»PubMed
- Long-Term Oxygen Treatment Trial Research Group., Albert RK, Au DH ym. A Randomized Trial of Long-Term Oxygen for COPD with Moderate Desaturation. N Engl J Med 2016;375:1617-1627 «PMID: 27783918»PubMed
- Leuppi JD, Schuetz P, Bingisser R ym. Short-term vs conventional glucocorticoid therapy in acute exacerbations of chronic obstructive pulmonary disease: the REDUCE randomized clinical trial. JAMA 2013;309:2223-31 «PMID: 23695200»PubMed
- Lightowler JV, Wedzicha JA, Elliott MW ym. Non-invasive positive pressure ventilation to treat respiratory failure resulting from exacerbations of chronic obstructive pulmonary disease: Cochrane systematic review and meta-analysis. BMJ 2003;326:185 «PMID: 12543832»PubMed

