Eteisvärinä
Miten viitata Käypä hoito -suositukseen? «K1»1
Keskeinen sanoma
- Eteisvärinä on yleisin pitkäkestoinen rytmihäiriö. Se aiheuttaa yli kolmanneksen rytmihäiriöihin liittyvistä sairaalahoitojaksoista ja kuormittaa suuresti myös avoterveydenhuoltoa.
- Iän ohella merkittävimmät eteisvärinälle altistavat tekijät ovat kohonnut verenpaine, sydänsairaudet, diabetes ja ylipaino.
- Hoitamattomana eteisvärinä lisää kuolleisuutta, altistaa aivohalvaukselle ja muille tromboembolisille komplikaatiolle, huonontaa elämänlaatua ja voi aiheuttaa sydämen vajaatoiminnan (ns. takykardiamyopatia).
- Eteisvärinän hoito valitaan yksilöllisesti niin, että huomioidaan rytmihäiriön aiheuttamat
oireet sekä potilaan perussairaudet ja toiveet. Keskeisimmät hoitomuodot ovat
- perussairauden ja muiden rytmihäiriölle altistavien tekijöiden hoito
- tromboembolisia komplikaatioita estävä antikoagulaatiohoito
- kammiotaajuuden optimointi (sykkeenhallinta)
- sinusrytmin palauttaminen sähköisellä tai lääkkeellisellä rytminsiirrolla ja rytmihäiriön uusiutumisen estäminen (rytminhallinta).
- Potilaan ennusteen kannalta tärkeimpiä ovat perussairauksien hyvä hoito ja oikein toteutettu antikoagulaatiohoito.
Tiivistelmä ja potilasversio
- Suosituksen tiivistelmä «Eteisvärinä»1
- Suosituksen yleiskielinen potilasversio suomeksi «Eteisvärinä»2 ja ruotsiksi «Förmaksflimmer»3
Suosituksen tavoitteet
- Suosituksen tavoitteena on antaa tuoreeseen tutkimustietoon perustuva käytännönläheinen ohje eteisvärinän hoidosta, selventää yksilöllisen hoitolinjan valintaperusteita ja täsmentää perusterveydenhuollon ja erikoissairaanhoidon välistä työnjakoa.
Kohderyhmät
- Ensisijainen kohderyhmä ovat eteisvärinän hoitoon osallistuvat perusterveydenhuollon ja erikoissairaanhoidon lääkärit, mutta suositus soveltuu myös muiden terveydenhuoltoalan ammattilaisten käyttöön.
Aiheen rajaus
- Suositus koskee aikuisten eteisvärinän hoitoa muttei sellaisenaan sovellu erityistilanteisiin, kuten sydäninfarktiin tai kajoaviin toimenpiteisiin (mm. sydänleikkaus, sepelvaltimoiden pallolaajennus) liittyvän eteisvärinän hoitoon.
- Eteislepatusta ja muita eteisvärinään läheisesti liittyviä supraventrikulaarisia rytmihäiriöitä käsitellään vain eteisvärinän hoitoon oleellisesti liittyviltä osin.
Määritelmä ja luokitus
- Eteisvärinä on supraventrikulaarinen rytmihäiriö, jota luonnehtii eteisten nopea, järjestymätön sähköinen ja mekaaninen toiminta.
- Eteisvärinä voidaan uusiutumistaipumuksensa ja kestonsa mukaan jakaa kolmeen päätyyppiin «Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHR...»1, «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, (kuva «Eteisvärinän luokittelu uusiutumistaipumuksen ja keston mukaan jaoteltuna»1):
- Kohtauksittainen (paroxysmal) eteisvärinä (ICD-10-koodi I48.0): sinusrytmi palautuu itsestään tai se palautetaan sähköisesti tai lääkkeellisesti rytminsiirrolla 7 vuorokauden kuluessa.
- Jatkuva (persistent) eteisvärinä (I48.1): sinusrytmi ei palaudu 7 vuorokauden kuluessa, tai se palautetaan sähköisesti tai lääkkeellisesti rytmihäiriön kestettyä yli 7 vuorokautta. Erityistilanteissa, joissa hoitolinjaksi valitaan rytminhallinta, vaikka eteisvärinä on ollut vallitsevana rytminä yli vuoden, voidaan käyttää nimitystä pitkään jatkunut (long-standing persistent) eteisvärinä erotuksena pysyvästä eteisvärinästä.
- Pysyvä (permanent) eteisvärinä (I48.2): rytmihäiriö hyväksytään, koska rytminsiirto ei onnistu tai sitä ei pidetä aiheellisena.
- Piilevä eteisvärinä (silent, subclinial) tarkoittaa tilannetta, jossa potilaalla on eteisvärinään sopivia oireita, mutta sitä ei ole saatu vielä diagnosoitua EKG:llä, tai oireettomalla potilaalla on todettavissa lyhytkestoisia eteisperäisiä rytmihäiriöitä esimerkiksi tahdistinlaitteen muistissa.
- Termiä itsenäinen eteisvärinä (lone atrial fibrillation) termiä voidaan käyttää muuten
terveillä alle 60-vuotiailla potilailla esiintyvästä eteisvärinästä «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Kopecky SL, Gersh BJ, McGoon MD ym. The natural hi...»3.
- Jos potilaalle ilmaantuu ikääntymisen myötä liitännäissairauksia, kyseessä ei enää ole itsenäinen eteisvärinä.
- Akuutti eteisvärinä tarkoittaa vastikään alkanutta oireista eteisvärinäkohtausta. Akuutin eteisvärinäkohtauksen keston arviointi (alle 12 tuntia, 12–24 tuntia tai 24–48 tuntia) on tärkeää arvioitaessa, voidaanko tehdä varhainen rytminsiirto.
- Eteisvärinäkuorma (atrial fibrillation burden) tarkoittaa osuutta, jonka ajan potilas oli eteisvärinässä monitoroinnin aikana.

Eteisvärinän luokittelu uusiutumistaipumuksen ja keston mukaan jaoteltuna. Kohtauksittaisella eteisvärinällä on taipumus muuttua ajan myötä vaikeammin hoidettavaksi jatkuvaksi ja edelleen pysyväksi eteisvärinäksi.
© Suomalainen Lääkäriseura Duodecim
Esiintyvyys ja ilmaantuvuus
Esiintyvyys
- Eteisvärinä on yleisin pitkäkestoinen rytmihäiriö. Sen esiintyvyys aikuisilla on keskimäärin
2–4 % ja sen odotetaan kasvavan 2,3-kertaiseksi vuoteen 2060 mennessä «Chugh SS, Havmoeller R, Narayanan K ym. Worldwide ...»4.
- Suomessa eteisvärinän esiintyvyys on keskimäärin 4,1 % ja eteisvärinäpotilaita arvioidaan olevan nykyään lähes 230 000 «Lehto M, Haukka J, Aro A, ym. Comprehensive nation...»5.
- Esiintyvyys vaihtelee suuresti potilaiden iän ja perussairauksien mukaan «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Alle 60-vuotiailla eteisvärinä on harvinainen (0,4 %), mutta se yleistyy nopeasti iän myötä niin, että yli 75-vuotiaista sitä sairastaa jopa yli 20 % «Lehto M, Haukka J, Aro A, ym. Comprehensive nation...»5.
- Potilaiden keski-ikä on 75 vuotta, ja noin 70 % potilaista on yli 65-vuotiaita «Feinberg WM, Blackshear JL, Laupacis A ym. Prevale...»6.
- Eteisvärinää esiintyy erityisesti sydämen vajaatoimintaa sairastavilla.
- Lievää vajaatoimintaa sairastavista noin 4 %:lla ja vaikeaa, lepo-oireista vajaatoimintaa (NYHA IV) potevista jopa puolella on eteisvärinä «Savelieva I, John Camm A. Atrial fibrillation and ...»7.
Ilmaantuvuus
- Eteisvärinää ilmaantuu vuodessa 0,1 %:lle alle 40-vuotiaista mutta miltei 2 %:lle
yli 80-vuotiaista «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Yli 55-vuotiaista joka kolmas kokee eteisvärinän elämänsä aikana «Lloyd-Jones DM, Wang TJ, Leip EP ym. Lifetime risk...»8, «Magnussen C, Niiranen TJ, Ojeda FM ym. Sex Differe...»9.
- Eteisvärinän ilmaantuvuus lisääntyy väestön ikääntymisen ja liitännäissairauksien yleistymisen myötä «Miyasaka Y, Barnes ME, Gersh BJ ym. Secular trends...»10.
- Miehillä on samanikäisiin naisiin nähden lähes kaksinkertainen riski sairastua eteisvärinään «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
Syntymekanismit
- Eteisvärinä syntyy, kun tiheään toistuvat lisälyönnit johtavat (ns. pesäkealkuinen
eteisvärinä) usean järjestymättömän kiertoaktivaatiorintaman syntyyn eteiskudoksessa
«Rensma PL, Allessie MA, Lammers WJ ym. Length of e...»12, «Allessie MA, Boyden PA, Camm AJ ym. Pathophysiolog...»13, «Nattel S. New ideas about atrial fibrillation 50 y...»14, «Tieleman RG. The pathophysiology of maintenance of...»15.
- Lisälyönnit ovat useimmiten lähtöisin keuhkolaskimoiden tyvialueelta «Haïssaguerre M, Jaïs P, Shah DC ym. Spontaneous in...»16, «Chen SA, Chen YJ, Yeh HI ym. Pathophysiology of th...»17, «Nattel S. Basic electrophysiology of the pulmonary...»18.
- Monet rakenteelliset muutokset, kuten eteismyopatia, eteisen koon kasvu ja sidekudoksen
kertyminen, sekä toiminnalliset seikat (esim. autonomisen hermoston tonus), vaikuttavat
eteisvärinän syntyyn ja jatkumiseen (kuva «Eteisvärinän syntymekanismit»2).
- Vagaalinen eteisvärinä alkaa tyypillisesti sykkeen hidastuessa yöllä ja levossa rasituksen tai ruokailun jälkeen.
- Sympatikotoninen eteisvärinä ilmaantuu yleensä sykkeen nopeutuessa fyysisen tai psyykkisen rasituksen vaikutuksesta.
- Eteisvärinä ruokkii itse itseään siten, että se muovaa eteisten sähköistä «Wijffels MC, Kirchhof CJ, Dorland R ym. Atrial fib...»19, «Allessie M, Ausma J, Schotten U. Electrical, contr...»20 ja mekaanista toimintaa «Sparks PB, Mond HG, Vohra JK ym. Mechanical remode...»21, «Schotten U, Duytschaever M, Ausma J ym. Electrical...»22 sekä rakenteita «Nattel S, Li D, Yue L. Basic mechanisms of atrial ...»23, «Burstein B, Nattel S. Atrial fibrosis: mechanisms ...»24 niin, että rytmihäiriö pitkittyy ja sinusrytmin palauttaminen vaikeutuu (remodeling eli uudelleen muotoutuminen) (kuva «Eteisvärinän luonnollinen kulku»3).

Eteisvärinän syntymekanismit. Eteisvärinän syntyyn ja ylläpitoon vaikuttavat monet rakenteelliset ja toiminnalliset tekijät. Eteisvärinä ruokkii itse itseään aiheuttamalla eteisten sähköisessä ja mekaanisessa toiminnassa sekä rakenteissa muutoksia, jotka altistavat rytmihäiriön synnylle ja ylläpitävät häiriötä (remodeling eli muovautuminen).

Eteisvärinän luonnollinen kulku. Eteisvärinä ruokkii itse itseään, minkä takia kohtauksittaisella eteisvärinällä on taipumus muuttua vaikeammin hoidettavaksi jatkuvaksi ja edelleen pysyväksi eteisvärinäksi. Useimmissa tapauksissa potilaalla on ollut useita “piileviä” eteisvärinäepisodeja ennen kuin rytmihäiriö “saadaan kiinni”.
© Suomalainen Lääkäriseura Duodecim
Altistavat tekijät
- Merkittävin eteisvärinälle altistava yksittäinen tekijä on ikä.
- Yli 50-vuotiailla eteisvärinään sairastumisen vaara kasvaa jokaista kymmentä ikävuotta kohden yli kaksinkertaiseksi «Benjamin EJ, Levy D, Vaziri SM ym. Independent ris...»11.
- Yli 70 %:lla eteisvärinäpotilaista on todettavissa rakenteellinen sydänsairaus tai muu rytmihäiriölle altistava systeemisairaus (taulukko «Eteisvärinälle altistavia tekijöitä...»1).
- Tärkeimpiä sydän- ja verenkiertoperäisiä eteisvärinälle altistavia tekijöitä ovat
«Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2
- kohonnut verenpaine
- sydämen vajaatoiminta
- sydämen läppäviat
- sepelvaltimotauti.
- Lisäksi monet supraventrikulaariset takykardiat, kuten eteislepatus, eteis-kammiosolmukkeen kiertoaktivaatiotakykardia ja synnynnäiseen oikorataan liittyvä takykardia, voivat pitkittyessään laukaista eteisvärinän.
- Sydämen ulkopuolisista syistä eteisvärinälle altistavat etenkin diabetes, lihavuus ja uniapnea, mutta myös kilpirauhasen toimintahäiriöt, munuaisten vajaatoiminta ja krooniset keuhkosairaudet lisäävät eteisvärinään sairastumisen vaaraa «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Schoonderwoerd BA, Smit MD, Pen L ym. New risk fac...»25.
- Pitkään jatkunut säännöllisesti toistuva poikkeuksellisen kuormittava kestävyysharjoittelu
(> 1 500 tunnin kumulatiivinen harjoituskuorma) altistaa myöhemmin kehittyvälle eteisvärinälle
«Elosua R, Arquer A, Mont L ym. Sport practice and ...»26, «Mont L, Sambola A, Brugada J ym. Long-lasting spor...»27, «Abdulla J, Nielsen JR. Is the risk of atrial fibri...»28, «Wilhelm M, Roten L, Tanner H ym. Atrial remodeling...»29, «Andersen K, Farahmand B, Ahlbom A ym. Risk of arrh...»30, «Karjalainen J, Kujala UM, Kaprio J ym. Lone atrial...»31, «Turagam MK, Flaker GC, Velagapudi P ym. Atrial Fib...»32, «Calvo N, Ramos P, Montserrat S ym. Emerging risk f...»33.
- Liikunnan suotuisat vaikutukset ovat kuitenkin sydän-verenkiertosairauksien kannalta niin suuria, ettei liikunnan lopettaminen eteisvärinän estämiseksi yleensä ole järkevää «Aizer A, Gaziano JM, Cook NR ym. Relation of vigor...»34.
- Fyysisesti heikkokuntoisilla ja ylipainoisilla liikunta estää eteisvärinän ilmaantumista «Manolis AS, Manolis AA. Exercise and Arrhythmias: ...»35.
- Akuutteja, väliaikaisia eteisvärinää laukaisevia tekijöitä ovat muun muassa alkoholin
liikakäyttö ("krapulaflimmeri"), akuutti sydäninfarkti, perikardiitti, myokardiitti
ja keuhkoembolia.
- Aiheuttavan tekijän hoitaminen palauttaa näissä tiloissa usein sinusrytmin.
- Monien eteisvärinälle altistavien tekijöiden, kuten sepelvaltimo- ja verenpainetaudin,
vaara periytyy.
- Myös itsenäinen eteisvärinätaipumus saattaa kulkea suvuittain, ja yksittäisiä eteisvärinälle altistavia ionikanavan mutaatioita on löydetty «Brugada R, Tapscott T, Czernuszewicz GZ ym. Identi...»36, «Troughton RW, Asher CR, Klein AL. The role of echo...»37, «Andalib A, Brugada R, Nattel S. Atrial fibrillatio...»38.
- Geneettiset tutkimukset eivät ole nykykäsityksen mukaan aiheellisia.
| Sydänperäiset syyt | Muut syyt |
|---|---|
| Kohonnut verenpaine | Diabetes |
| Sydämen vajaatoiminta | Lihavuus |
| Sydämen läppäviat | Uniapnea |
| Sepelvaltimotauti | Kilpirauhasen toimintahäiriöt |
| Akuutti tai aiempi sydäninfarkti | Munuaisten vajaatoiminta |
| Perikardiitti | Tulehdukselliset sairaudet |
| Myokardiitti | Dyslipidemia |
| Synnynnäinen sydänvika | Elektrolyyttihäiriöt |
| Hypertrofinen kardiomyopatia | Akuutti tai krooninen keuhkosairaus
|
| Laajentava kardiomyopatia | Feokromosytooma |
| Sairas sinus -oireyhtymä | Runsas alkoholinkäyttö ("krapulaflimmeri") |
| Muut supraventrikulaariset rytmihäiriöt | Tupakka- ja nikotiinivalmisteiden käyttö |
| Sydänleikkauksen jälkitila | Huumeidenkäyttö (esimerkiksi kokaiini) |
Seuraukset
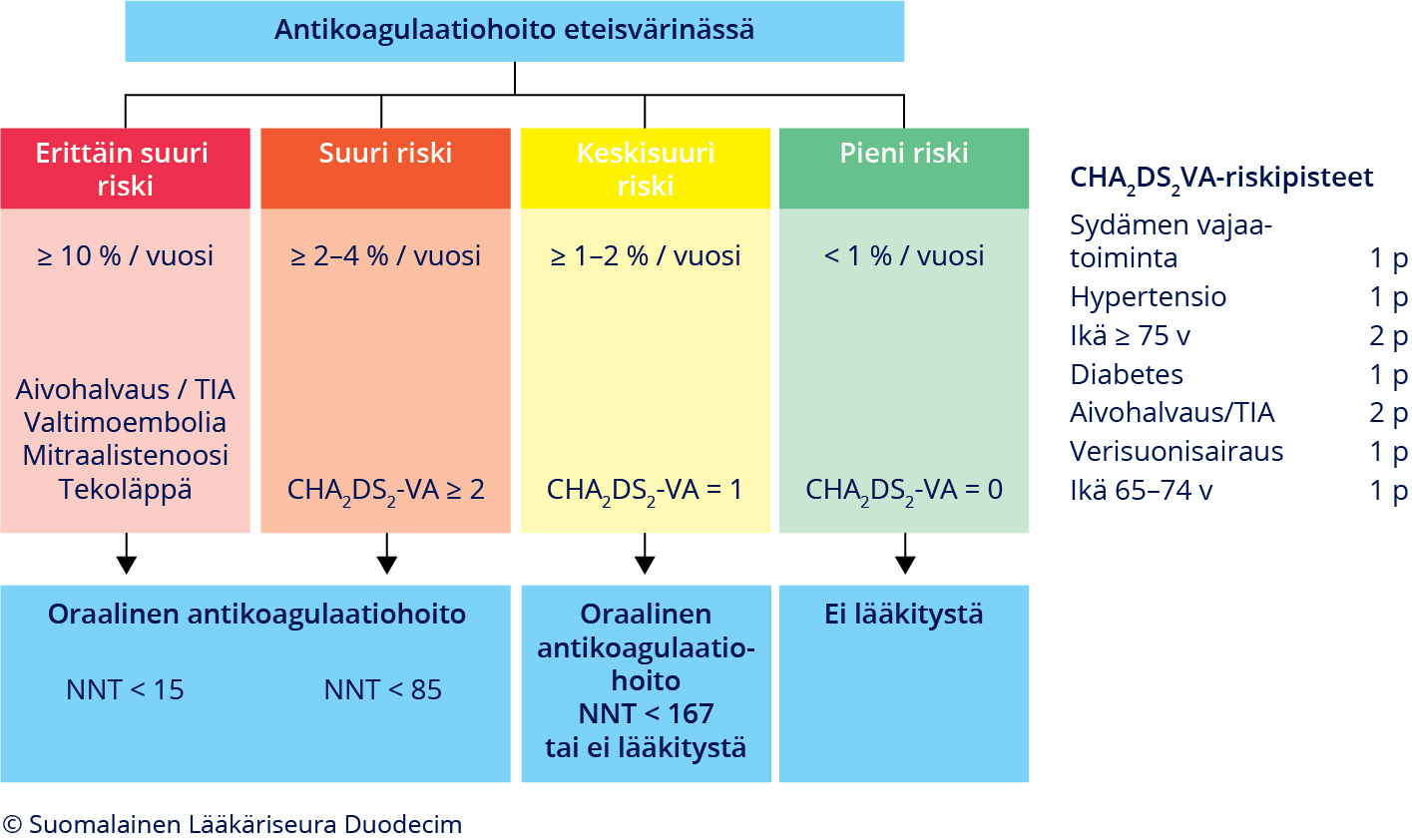
Antitromboottinen hoito eteisvärinässä. Pysyvän antikoaglaatiohoidon (AK) aiheellisuus arvioidaan suhteutettuna potilaan yksilölliseen aivohalvauksen vaaraan CHA2DS2VA-riskipisteytystä käyttämällä. Suuren riskin potilailla (CHA2DS2VA ≥ 2) AK-hoito (yleensä suora antikoaglantti) on aiheellinen lähes poikkeuksetta. Keskisuuren riskin potilailla (CHA2DS2VA = 1) AK-hoidon tarve arvioidaan yksilöllisesti. Siitä voidaan luopua, jos vuotovaara on suuri, potilas ei halua käyttää AK-hoitoa, vaaratekijä (esim. verenpaine) on hoidettu hyvin eikä potilaalla ole muita pienempiä vaaratekijöitä (mm. tupakointi, dyslipidemia, munuaisten vajaatoiminta). Pienen riskin potilaille (CHA2DS2VA = 0) antikoagulaatiohoitoa ei anneta, koska sen hyöty on heillä haittoja vähäisempi. ASA ja ADP-reseptorin salpaajat eivät sovellu heikon tehonsa ja haittavaikutustensa takia eteisvärinään liittyvien tukosten estoon. NNT (number needed to treat) on niiden potilaiden lukumäärä, joista yksi välttää aivohalvauksen lumelääkettä saaneisiin verrattuna yhden vuoden hoidon aikana (ks. lisätietoaineisto «Antitromboottisen hoidon valinta eteisvärinässä»). Vuotovaaran aiheuttavien toimenpiteiden ja leikkausten ajaksi AK-hoito voidaan tarvittaessa tauottaa suurimman riskin potilaita lukuun ottamatta.
© Suomalainen Lääkäriseura Duodecim
Kuolleisuus
- Rytmihäiriönä eteisvärinä on harvoin henkeä uhkaava.
- Laajoissa epidemiologisissa tutkimuksissa eteisvärinäpotilaiden kuolleisuus sinusrytmissä olleisiin nähden on todettu noin kaksinkertaiseksi «Krahn AD, Manfreda J, Tate RB ym. The natural hist...»39, «Benjamin EJ, Wolf PA, D'Agostino RB ym. Impact of ...»40, «Stevenson WG, Stevenson LW, Middlekauff HR ym. Imp...»41.
- Eteisvärinäpotilaiden kuolleisuus liittyy niin läheisesti sydänsairauden vaikeusasteeseen ja eteisvärinän lääkitykseen, että on epävarmaa, onko eteisvärinä itsenäinen vaaratekijä vai merkki vaikeasta kardiovaskulaarisesta sairaudesta tai käytetystä rytmihäiriölääkityksestä «Eteisvärinään liittyy lisääntynyt kuolleisuus, mutta on epäselvää johtuuko se rytmihäiriöstä sinänsä, taustalla olevasta sydänsairaudesta tai muusta sairaudesta vai käytetystä lääkityksestä.»C.
Tromboemboliset komplikaatiot
- Eteisvärinä on merkittävin sydänperäiselle embolisaatiolle altistava tekijä.
- Keskimäärin 20–30 %:lla iskeemisen aivohalvauksen saaneista potilaista on todettavissa eteisvärinä, ja eteisvärinä selittää noin 10 % salasyntyisistä (kryptogeenisistä) aivohalvauksista.
- Osa iskeemisistä aivoembolioista voi ilmetä pelkästään dementiana tai kognitiivisten toimintojen heikkenemisenä «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Knecht S, Oelschläger C, Duning T ym. Atrial fibri...»42.
- Embolian vaara on erityisen suuri kardioversiota seuraavien 1–2 viikon aikana.
- Eteisvärinäpotilailla aivoinfarktin ilmaantuvuus sinusrytmissä oleviin nähden on vaaratekijöiden
mukaan noin kaksinkertainen «Aivohalvaus ilmaantuu keskimäärin 5 %:lle eteisvärinäpotilaista vuodessa, mutta vaaratekijöistä riippuen ilmaantuvuus vaihtelee 1–12 %.»A.
- Reumaattiseen läppävikaan liittyvässä eteisvärinässä iskeemisen aivohalvauksen vaara on jopa 17-kertainen «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Riskitekijöiden hyvän hoidon ja tehostuneen antikoagulaatiohoidon ansiosta aivohalvauksen ilmaantuvuus pieneni viime vuosikymmenen aikana alle puoleen «Teppo K, Airaksinen KEJ, Jaakkola J, ym. Trends in...»43. .
- Merkittävimmät aivoinfarktille altistavat tekijät eteisvärinässä ovat
- aiempi aivohalvaus tai TIA
- ≥ 75 vuoden ikä
- mitraaliläpän kohtalainen tai vaikea ahtauma tai mekaaninen tekoläppä
- hypertrofinen kardiomyopatia.
- Muita CHA2DS2VA-pisteytyksessä huomioituja vaaratekijöitä ovat
- sydämen vajaatoiminta
- kohonnut verenpaine
- diabetes
- 65–74 vuoden ikä
- valtimosairaus (mm. merkittävä sepelvaltimotauti, aortankaaren tai kaulavaltimon plakki tai perifeerinen valtimosairaus).
- Muita kliinisesti merkittäviä vaaratekijöitä ovat
- munuaisten vajaatoiminta
- dyslipidemia
- tupakointi.
- Nykytiedon perusteella naissukupuoli ei ole itsenäinen tukosvaaratekijä eikä sukupuoli vaikuta antikoagulaatiohoidon aiheellisuuteen «Teppo K, Lip GYH, Airaksinen KEJ, ym. Comparing CH...»44, «Penttilä T, Lehto M, Niiranen J, ym. Differences i...»45.
- Käytännössä tromboembolisten komplikaatioiden vaaraa arvioidaan CHA2DS2VA-pisteytyksen (taulukko «Tromboembolisten komplikaatioiden vaaran arviointi CHA2DS2VA-pisteytyksen avulla....»2) avulla «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Lip GY, Nieuwlaat R, Pisters R ym. Refining clinic...»46, «Van Staa TP, Setakis E, Di Tanna GL ym. A comparis...»47.
- Kohtauksittaisessa eteisvärinässä tukosvaara on hieman pienempi kuin jatkuvassa tai pysyvässä eteisvärinässä «Steinberg BA, Hellkamp AS, Lokhnygina Y ym. Higher...»48, «Vanassche T, Lauw MN, Eikelboom JW ym. Risk of isc...»49, mutta riskitekijät ja hoitosuositus ovat kaikissa tapauksissa samanlaiset.
- Hypertrofisessa kardiomyopatiassa, merkittävässä mitraaliläpän ahtaumassa ja sydänamyloidoosissa pysyvä antikoagulaatiohoito on aiheellinen eteisvärinään liittyvien tukosten estossa CHA2DS2VA-pisteistä riippumatta «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
| Riskitekijä | Pisteet | |
|---|---|---|
| Punaisella merkittyihin vaaratekijöihin ei voida vaikuttaa, mutta muihin tekijöihin
liittyvää vaaraa voidaan pienentää niiden hyvällä hoidolla. Dekompensaation aiheuttanut
sydämen vajaatoiminta altistaa tukoksille riippumatta vasemman kammion ejektiofraktiosta. Maksimipisteet ovat 8, koska iästä saa yhden tai kaksi pistettä. Pisteytykseen perustuva suositus antitromboottisen hoidon valinnasta on esitetty kuvassa «Antitromboottinen hoito eteisvärinässä»4. 1Merkittävä sepelvaltimotauti (sepelvaltimotaudin aiheuttamia oireita ja/tai kuvantamistutkimuksessa todettu merkittävä ahtauma), aortankaaren plakki, kaulavaltimon ahtauma tai vaikea perifeerinen valtimosairaus. |
||
| Chronic heart failure | Sydämen vajaatoiminta | 1 |
| Hypertension | Kohonnut verenpaine | 1 |
| A2ge ≥ 75 years | Ikä ≥ 75 vuotta | 2 |
| Diabetes | Diabetes | 1 |
| S2troke or TIA | Aiempi aivohalvaus tai TIA | 2 |
| Vascular disease | Valtimosairaus 1 | 1 |
| Age 65–74 years | Ikä 65–74 vuotta | 1 |
Hemodynaamiset vaikutukset
- Sydämen minuuttitilavuus pienenee eteisvärinän vaikutuksesta noin 15–30 % «Alboni P, Scarfò S, Fucà G ym. Hemodynamics of idi...»50, «Clark DM, Plumb VJ, Epstein AE ym. Hemodynamic eff...»51, koska
- eteissupistukset puuttuvat ja eteiset ja kammiot toimivat eri tahtiin
- kammiovaste on tilanteeseen nähden liian nopea ja epäsäännöllinen.
- Minuuttitilavuuden pienenemisen merkitys on vähäinen, jos vasemman kammion supistumisvireys on normaali, mutta sydämen vajaatoiminnassa eteisvärinä voi johtaa äkillisiin hemodynaamisiin ongelmiin «Lau CP, Leung WH, Wong CK ym. Haemodynamics of ind...»52.
- Eteisvärinä voi aiheuttaa sydämen vajaatoiminnan (ns. takykardiamyopatia), jos kammiovaste on jatkuvasti liian nopea «Shinbane JS, Wood MA, Jensen DN ym. Tachycardia-in...»53.
Elämänlaatu
- Eteisvärinän tyypistä (kohtauksittainen, jatkuva tai pysyvä) riippumatta potilaiden
elämänlaatu on rytmihäiriön aikana huonompi kuin sinusrytmin aikana «Dorian P, Jung W, Newman D ym. The impairment of h...»54, «Lüderitz B. Dirk Durrer (1918-1984). J Interv Card...»55, «van den Berg MP, Hassink RJ, Tuinenburg AE ym. Qua...»56.
- Rytmin- ja sykkeenhallintaan satunnaistettujen potilaiden välillä ei kontrolloiduissa tutkimuksissa havaittu elämänlaatueroja, mutta kummassakin hoitolinjassa elämänlaatu oli parempi sinusrytmissä olevilla «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Eteisvärinäpotilaiden elämänlaatu on monilta osin huonompi kuin sepelvaltimoiden pallolaajennuksiin
tulevilla ja sydäninfarktin sairastaneilla ja keskimäärin samaa tasoa kuin sydämen
vajaatoimintaa potevilla «van den Berg MP, Hassink RJ, Tuinenburg AE ym. Qua...»56.
- Elämänlaatu näyttää huononevan naisilla enemmän kuin miehillä «Paquette M, Roy D, Talajic M ym. Role of gender an...»57, «Hekkala AM. Suomalaisten eteisvärinäpotilaiden kok...»58.
Diagnostiikka
- Eteisvärinän diagnoosi pitää aina varmistaa EKG:llä (12-kytkentäinen EKG tai mikä tahansa riittävän pitkä ja hyvälaatuinen lääkärin tarkastama EKG-tallenne).
Oireet ja kliiniset löydökset
- Eteisvärinän aiheuttamat oireet ja kliiniset löydökset vaihtelevat sydän- ja muiden liitännäissairauksien, rytmihäiriön keston ja kammiotaajuuden sekä potilaan kunnon ja vireystilan mukaan.
- Eteisvärinä saattaa olla täysin oireeton, mikä vaikeuttaa diagnostiikkaa.
- Tavallisimpia eteisvärinän aiheuttamia oireita ovat
- sydämentykytystuntemus (palpitaatio)
- väsymys ja suorituskyvyn heikkeneminen
- huimaus
- rintakipu
- hengenahdistus
- polyuria.
- Oireiden vaikeusasteen arvioinnissa suositellaan käytettäväksi European Heart Rhythm Associationin kehittämää EHRA-luokitusta (ks. taulukko «Eteisvärinän aiheuttamien oireiden EHRA-luokitus ...»3), «Kirchhof P, Bax J, Blomstrom-Lundquist C ym. Early...»59.
- Synkopee on harvinaista ja herättää epäilyn vakavasta liitännäissairaudesta, kuten sinus- tai eteis-kammiosolmukkeen toimintahäiriöstä, aorttaläpän ahtaumasta tai Wolff–Parkinson–Whiten (WPW) oireyhtymästä.
- Kliinisistä löydöksistä tyypillisin on epäsäännöllinen kammiotaajuus, joka voidaan helposti todeta sydäntä
auskultoimalla tai valtimosykettä tunnustelemalla.
- "Pulssivajeen" takia ranteessa tuntuva syke on usein hitaampi kuin stetoskoopilla kuuntelemalla laskettu tai EKG:stä mitattu.
| EHRA-luokka | Kriteerit |
|---|---|
| 1 | Ei oireita |
| 2 | Lieviä oireita, jotka eivät vaikuta päivittäiseen elämään |
| 3 | Vaikeita oireita, joiden takia päivittäinen elämä vaikeutuu |
| 4 | Sietämättömiä oireita, joiden takia päivittäistä elämää on pitänyt muuttaa |
EKG-löydökset
- Eteisten tiheän (450–600/min) ja organisoitumattoman sähköisen toiminnan vuoksi normaali P-aalto ei erotu ja EKG:n perusviiva on epätasainen (kuva «Eteisvärinän aikana rekisteröity 12-kytkentäinen EKG»5).
- Kammiotaajuus on epäsäännöllinen sähköimpulssien edetessä eteisistä kammioihin vaihtelevalla nopeudella.
- QRS-heilahdus on yleensä kapea, mutta se saattaa olla leveä toiminnallisessa (aberraatio) ja pysyvässä haarakatkoksessa tai WPW-oireyhtymässä.
- Erittäin nopea (yli 200/min) leveäkompleksinen eteisvärinä on harvinainen ja viittaa WPW-oireyhtymään (kuva «Nuorella naisella havaittu WPW-oireyhtymään liittyvä nopea eteisvärinä»6).
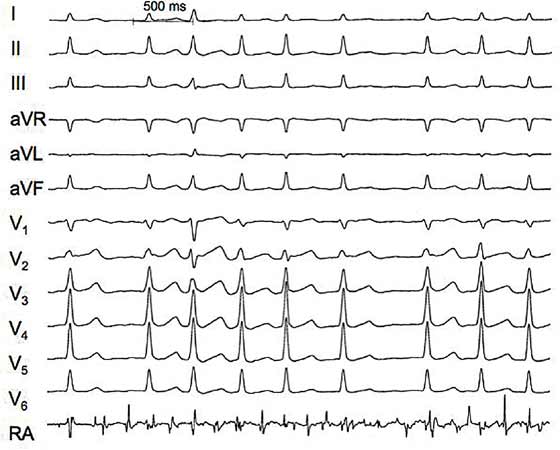
Eteisvärinän aikana rekisteröity 12-kytkentäinen EKG. Huomaa lyöntivälien epäsäännöllisyys, vaihteleva perusviiva ja P-aaltojen puuttuminen. Eteisvärinän kammiovaste on tällä potilaalla selvästi tihentynyt (noin 120–150/min). Alimmaisena on oikean eteisen sisältä rekisteröity EKG, jossa näkyy erittäin nopea ja epätasainen eteisrytmi.
© Suomalainen Lääkäriseura Duodecim

Nuorella naisella havaittu WPW-oireyhtymään liittyvä nopea eteisvärinä. Huomaa delta-aallon takia leveä QRS-heilahdus ja erittäin nopea kammiotaajuus (yli 350/min). Sinusrytmi palautettiin kardioversiolla, ja potilaalle tehtiin onnistunut katetriablaatio, jossa katkaistiin kaksi oikorataa.
© Suomalainen Lääkäriseura Duodecim
Rytmihallintalaitteiden ja rytmivalvurin EKG-tallenteet
- Rytminhallintalaitteet (hitaan sykkeen tahdistin, vajaatoimintatahdistin, rytmihäiriötahdistin)
ja ihon alle asennettava rytmivalvuri seuraavat sydämen rytmiä jatkuvasti ja paljastavat
siten piilevän eteisvärinän herkemmin kuin 12-kytkentäinen EKG, Holter-nauhoitus tai oire-EKG.
- Yksikanavaisessa rekisteröinnissä tai tahdistinlaitteen tallentamassa rekisteröinnissä eteisvärinän diagnoosi edellyttää vähintään 30 sekunnin kestoista rytmihäiriötä (vertaa rekisteröintiä sinusrytmin aikaiseen tallenteeseen) «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- On kuitenkin vielä epäselvää, kuinka pitkä laitteen muistiin tallentunut eteisperäinen rytmihäiriö on jatkuvassa seurannassa merkityksellinen antikoagulaatiohoidon tarpeen kannalta.
- Viimeaikaisten tutkimusten perusteella potilailla, joilla on todettu lyhyitä (> 6 minuuttia, mutta ≤ 24 tuntia) eteisperäisiä rytmihäiriöitä (ns. AHRE, atrial high rate episode) tahdistinlaitteen muistissa, rutiinimainen antikoagulaatiohoito saattaa olla jopa haitallista «Kirchhof P, Toennis T, Goette A, ym. Anticoagulati...»60, «Healey JS, Lopes RD, Granger CB, ym. Apixaban for ...»61.
- Käytännössä antikoagulaatiohoitoa harkittaessa on otettavat huomioon rytmihäiriökuorman lisäksi myös mahdolliset tukosvaaratekijät eikä antikoagulaatiohoitoa pidä aloittaa ilman rekisteröintiä, jossa nähdään eteisvärinä.
- Rytminhallintalaitteiden diagnostisia ominaisuuksia kannattaa hyödyntää suuressa tukosvaarassa olevilla potilailla oireettoman eteisvärinän etsimisessä, ja tarvittaessa salasyntyisen aivoinfarktin jälkeen eteisvärinää voidaan etsiä asentamalla rytmivalvuri «Toni D, Lorenzano S, Strano S ym. Detection of Sil...»62, ks. Käypä hoito -suositus Aivoinfarkti ja TIA «Aivoinfarkti ja TIA»4, «Aivoinfarkti ja TIA. Käypä hoito -suositus. Suomal...»63.
Älypuhelinsovellukset ja muut omatoimiseen rytmiseurantaan tarkoitetut laitteet
- Käytössä on useita erilaisia laitteita ja älypuhelinsovelluksia, joiden avulla voidaan
rekisteröidä EKG tai seurata sykettä ja pulssiaaltoa esimerkiksi ranteesta tai sormenpäästä
ilman kajoavia toimenpiteitä «Fung E, Järvelin MR, Doshi RN ym. Electrocardiogra...»64.
- Laitteiden käyttö on yksinkertaista, ja niiden avulla sydämen sykettä voidaan helposti seurata usean viikon ajan tai pitempäänkin.
- Erityisen suuressa eteisvärinäriskissä olevat potilaat (esim. ikä yli 75 vuotta, kohonnut verenpaine, uniapnea) voivat käyttää niitä omatoimisessa havainnoinnissa. Aihetta tutkitaan vilkkaasti, ja siitä saadaan jatkuvasti lisätietoa.
- Osassa laitteista eteisvärinän tunnistus perustuu pelkästään sykevälin vaihtelun analysointiin,
eivätkä ne tallenna varsinaista EKG:tä.
- Tunnistusalgoritmien kehittymisestä huolimatta eteisvärinän diagnoosi vaatii aina lääkärin tarkastaman EKG-otoksen.
Pulssin tunnustelu
- Pulssin tunnustelu ranteesta tai kaulalta on eteisvärinän seulonnan perustyökalu.
- Se kannattaa opettaa vastaanottokäyntien yhteydessä kaikille iäkkäille tai muuten suuressa eteisvärinäriskissä oleville potilaille.
- Pulssin tunnustelussa kiinnitetään huomiota syketaajuuden lisäksi myös sykkeen säännöllisyyteen.
- Jos syke on toistetussa mittauksessakin poikkeuksellisen nopea tai epäsäännöllinen, on EKG aiheellinen.
Erotusdiagnostiikka
- Eteisvärinän tärkeimpiä erotusdiagnostisia vaihtoehtoja ovat muut eteisperäiset rytmihäiriöt,
kuten eteislepatus (EKG-tietokanta «Tyypillinen eteislepatus»1 (vaatii käyttöoikeuden)) ja supraventrikulaarinen takykardia (EKG-tietokanta «Eteis-kammiosolmukkeen kiertoaktivaatiotakykardia»2 (vaatii käyttöoikeuden)).
- Yhtäkkiä alkava ja loppuva tasainen nopealyöntisyys viittaa supraventrikulaariseen takykardiaan.
- Vähitellen alkava ja loppuva tasainen tykytys sopii paremmin sinustakykardiaan kuin eteisvärinään.
- Aberroitunut tai pysyvään haarakatkokseen ja kammioiden varhaisaktivaatioon liittyvä eteisvärinä voi muistuttaa kammiotakykardiaa (EKG-tietokanta «Sydäninfarktin arven aiheuttama takykardia»3 (vaatii käyttöoikeuden)).
Tutkimukset
- Suositus eteisvärinäpotilaalle tehtävistä tutkimuksista esitetään taulukossa «Suositus eteisvärinäpotilaalle tehtävistä tutkimuksista...»4.
- Perustutkimukset pitää tehdä kaikille potilaille eteisvärinän etiologiaa selvitettäessä ja pitkäaikaishoitoa suunniteltaessa, mutta laajat laboratorio- ja kuvantamistutkimukset eivät akuuttia kohtausta hoidettaessa yleensä ole tarpeen.
| Perustutkimukset | |
|---|---|
| 1. Anamneesi ja kliininen tutkimus | |
|
|
| 2. EKG | |
|
|
| 3. Laboratoriotutkimukset | |
|
|
| 4. Sydämen kaikututkimus | |
|
|
| Lisätutkimukset | |
| 1. Muut kuvantamistutkimukset | |
|
|
| 2. EKG:n pitkäaikaisrekisteröinti tai tapahtuma-EKG | |
|
|
| 3. Kliininen rasituskoe | |
|
|
| 4. Ruokatorven kautta tehtävä sydämen kaikututkimus | |
|
|
| 5. Elektrofysiologinen tutkimus | |
|
|
Anamneesi ja kliininen tutkimus
- Anamneesi:
- kohonnut verenpaine ja muut eteisvärinälle altistavat sairaudet ja tekijät
- tukoksille (CHA2DS2VA-pisteet) ja verenvuodolle altistavat tekijät (HAS-BLED-pisteet)
- oireet rytmihäiriön aikana (EHRA-luokitus)
- karkea arvio kognitiivisesta toimintakyvystä (tarvittaessa muistitesti)
- rytmihäiriön kesto ja kohtausten esiintymistaajuus (eteisvärinän tyyppi)
- rytmihäiriön alkamis- ja loppumistapa (yhtäkkiä vai vähitellen)
- laukaisevat tekijät
- lääkkeet ja muut hoidot
- lähisukulaisilla esiintyneet rytmihäiriöt ja sydänsairaudet
- Kliininen tutkimus:
- viitteet eteisvärinälle ja tromboembolisille komplikaatioille altistavista tekijöistä ja muista sydänsairauksista
- huolellinen kardiovaskulaarinen tutkimus: valtimosykkeen tunnustelu, sydämen ja keuhkojen auskultaatio, verenpaineen mittaus ja aiempien mittaustulosten tarkistus
- eteisvärinän vaikutus hemodynamiikkaan (verenpaine) ja sydänlihaksen hapensaantiin (ST-T-muutokset)
EKG
- Rytmihäiriön aikana rekisteröidyssä EKG:ssä kiinnitetään huomiota P-aallon puuttumisen lisäksi kammiotaajuuteen ja sydänsairauksiin viittaaviin löydöksiin.
- Normaalin sinusrytmin aikana rekisteröity EKG voi paljastaa monia eteisvärinän hoidon kannalta oleellisia seikkoja:
- P-aallon muoto ja kesto: pitkittynyt, kaksihuippuinen P-aalto on merkki eteisvärinälle altistavasta eteisensisäisen tai eteistenvälisen johtumisen tai molempien hidastumisesta tai eteisten kuormituksesta
- QRS-heilahduksen muoto ja kesto: vasemman kammion hypertrofia, infarktiarpi, haarakatkos, delta-aalto
- PQ-aika: lyhentynyt WPW-oireyhtymässä, pidentynyt eteis-kammiojohtumisen häiriöissä.
- QT-aika: pitkä QT -oireyhtymä ja muut repolarisaatiohäiriöt.
- EKG:tä voidaan käyttää myös lääkevaikutuksen seurantaan analysoimalla lääkityksen
aiheuttamia muutoksia
- syketaajuudessa
- PQ-ajassa
- QRS-heilahduksen muodossa ja kestossa
- QT-ajan pituudessa.
Laboratoriotutkimukset
- Kun ensimmäisen kohtauksen jälkeen suunnitellaan estohoitoa tai kun eteisvärinä toistuu
yllättävästi hoidon aikana, tehdään seuraavat perustutkimukset:
- perusverenkuva
- plasman elektrolyytit
- plasman glukoosi
- seerumin lipidit
- kilpirauhasen toimintakokeet
- virtsan seulontakoe (proteinuria, glukosuria)
- antikoagulaatiohoidon ja estolääkityksen aloitukseen ja seurantaan liittyvät tutkimukset.
Sydämen kaikututkimus
- Sydämen kaikututkimus on mahdollisten rakenteellisten sydänsairauksien toteamiseksi
suositeltavaa tehdä kertaalleen kaikille potilaille, joilla todetaan eteisvärinä.
- Iäkkäillä potilailla, joilla ei todeta viitteitä sydänsairauksista, siitä voidaan kuitenkin luopua, jos hoitolinjaksi valitaan sykkeenhallinta ja eteisvärinän kammiotaajuus on "taloudellinen".
- Erityisen tärkeä sydämen kaikututkimus on, kun
- suunnitellaan varsinaisen rytmihäiriölääkityksen (ryhmien I tai III lääkkeet) aloittamista tai
- muissa tutkimuksissa todetaan rakenteelliseen sydänsairauteen viittaavia oireita tai löydöksiä.
- Sydämen kaikututkimuksessa erityistä huomiota kiinnitetään seikkoihin, jotka vaikuttavat
hoitolinjan, estohoidon (rytmihäiriölääkitys, kajoava hoito) ja antikoagulaatiohoidon
valintaan «Troughton RW, Asher CR, Klein AL. The role of echo...»37, «McNamara RL, Tamariz LJ, Segal JB ym. Management o...»65:
- vasemman kammion koko ja toiminta
- vasemman eteisen koko
- muut sydämen rakenteelliset poikkeavuudet, kuten infarktiarpi, läppäviat ja seinämähypertrofia
- sydämen sisäiset hyytymät.
- Ruokatorven kautta tehtävä sydämen kaikututkimus (TEE) sulkee luotettavasti pois sydämensisäiset
trombit «Manning WJ, Weintraub RM, Waksmonski CA ym. Accura...»66, «Saarela E, Koskela V, Strandberg M ym. Ruokatorven...»67.
- TEE-tutkimus on välttämätön, kun suunnitellaan välitöntä rytminsiirtoa antikoaguloimattomalla potilaalla, jolla eteisvärinän kesto on yli 24–48 tuntia tai epäselvä «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
Sydämen ja keuhkojen röntgenkuvaus
- Sydämen ja keuhkojen röntgenkuva tutkitaan, jos epäillään, että eteisvärinän syynä on krooninen keuhkosairaus tai muu röntgenkuvasta havaittava sairaus tai tekijä.
Muut tutkimukset
- EKG:n pitkäaikaisrekisteröintiä, tapahtuma-EKG:tä tai EKG:n rekisteröiviä älypuhelin- tai muita sovelluksia voidaan käyttää diagnostiikan lisäksi myös hoitovasteen arvioinnissa.
- Kliininen rasituskoe on käyttökelpoinen rasituksen aikana ilmenevän eteisvärinän diagnostiikassa, pysyvän eteisvärinän sykkeenhallinnan arvioinnissa ja iskemian sulkemisessa pois, kun suunnitellaan IC-ryhmän rytmihäiriölääkkeen käytön aloittamista.
- Sepelvaltimoiden ja sydämen kuvantaminen (varjoainekuvaus, tietokonetomografia, magneettitutkimus, isotooppitutkimus) voi olla aiheellinen, jos eteisvärinään liittyy rintakipua, hengenahdistusta tai muita sydänoireita. Kuvantamista voidaan käyttää myös vasemman eteisen anatomian selvittämiseen ennen katetriablaatiota (tietokonetomografia, magneettitutkimus) ja vasemman eteisen trombin poissulkemiseen (tietokonekuvaus).
- Pulssin omatoiminen tunnustelu auttaa oireettoman eteisvärinän tunnistamisessa. Siitä samoin kuin edellä mainituista älypuhelin- ja muista sovelluksista voi olla hyötyä suuren riskin potilaiden seulonnassa ja hoidon seurannassa «Camm AJ, Lip GY, De Caterina R ym. 2012 focused up...»68.
Hoitolinjan valinta: sykkeen- vai rytminhallinta
- Eteisvärinä on monitahoinen tila, jonka hoito vaatii usein moniammatillista osaamista ja hyvää yhteistyötä eri erikoisalojen (mm. kardiologia, sisätaudit, neurologia, kirurgia ja hematologia) sekä perusterveydenhuollon välillä.
- Eteisvärinän yksilöllistä hoitoa (taulukko «Eteisvärinän kokonaisvaltainen hoito...»5) valittaessa huomioidaan
- muut (sydän)sairaudet
- tromboembolisten komplikaatioiden vaaratekijät
- potilaan oireet (EHRA-luokitus)
- rytmihäiriön kesto
- hoidon odotettavissa olevat hyödyt ja haitat
- potilaan toiveet.
- Ensimmäinen oireisen eteisvärinäkohtauksen ilmaannuttua kannattaa lähes poikkeuksetta yrittää sinusrytmin palauttamista.
- Sinusrytmi palautuu itsestään 1–2 vuorokauden kuluessa ilman toimenpiteitä 50–70 %:ssa eteisvärinäkohtauksista «Danias PG, Caulfield TA, Weigner MJ ym. Likelihood...»69, «Dell'Orfano JT, Patel H, Wolbrette DL ym. Acute tr...»70, «Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoit...»71.
- Oireettomilla ja lieväoireisilla (EHRA 1–2) iäkkäillä potilailla ennuste ja elämänlaatu
ovat vähintään yhtä hyvät sykkeenhallinnan kuin lääkkeelliseen rytminhallinnan aikana
«Sykkeenhallinta on eteisvärinässä parempi vaihtoehto kuin rytminhallinta aivohalvauksien ja kokonaiskuolleisuuden suhteen, mutta hoidot ovat samanarvoisia kuolleisuuden ja potilaiden elämänlaadun suhteen.»A.
- Näissä tapauksissa rytminsiirrosta voidaan luopua ja keskittyä kohonneen verenpaineen, sydämen vajaatoiminnan, diabeteksen ja muiden mahdollisten vaaratekijöiden hoitoon sekä antikoagulaatiohoitoon ja sykkeenhallintaan «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Hohnloser SH, Kuck KH, Lilienthal J. Rhythm or rat...»72, «Wyse DG, Waldo AL, DiMarco JP ym. A comparison of ...»73, «Van Gelder IC, Hagens VE, Bosker HA ym. A comparis...»74, «Carlsson J, Miketic S, Windeler J ym. Randomized t...»75, «Opolski G, Torbicki A, Kosior DA ym. Rate control ...»76, «Roy D, Talajic M, Nattel S ym. Rhythm control vers...»77. Ks. myös Vältä viisaasti -suositus Vältä eteisvärinän rytminsiirtoa lieväoireisilla iäkkäillä potilailla «Eteisvärinän rytminsiirto lieväoireisilla iäkkäillä potilailla»1.
- Työikäisille kannattaa yleensä tehdä rytminsiirto kertaalleen, vaikka potilas olisi oireeton.
- Muita sykkeenhallintaa puoltavia tekijöitä ovat
- oireiden hallittavuus kammiovastetta hidastavilla lääkkeillä
- eteisvärinän uusiutuminen nopeasti (alle 1–2 kuukauden kuluessa rytminsiirrosta) estohoidosta huolimatta
- kookas vasen eteinen: rytminsiirron onnistuminen ja sinusrytmin säilyminen ovat epätodennäköisiä, jos vasemman eteisen poikkimitta on yli 5 cm «McNamara RL, Tamariz LJ, Segal JB ym. Management o...»65
- eteisvärinän yhtäjaksoinen kestäminen yli 6–12 kuukautta
- vähäinen fyysinen aktiivisuus.
- Rytminhallinta on ensisijainen vaihtoehto potilaan perussairauksista riippumatta, jos
- kammiotaajuutta hidastavasta lääkityksestä huolimatta todetaan vaikeita oireita (EHRA 3–4) tai hemodynaamisia ongelmia
- vaste rytmihäiriön estohoitoon on hyvä
- vasen eteinen on normaalikokoinen
- rytmihäiriö on kestänyt alle 6 kuukautta
- potilas on fyysisesti aktiivinen.
- Seuraavissa kappaleissa rytmihäiriölääkkeet esitetään Vaughan-Williamsin jaon mukaisesti (kuva «Rytmihäiriölääkkeiden jako Vaughan-Williamsin mukaan»7).

Rytmihäiriölääkkeiden jako Vaughan–Williamsin mukaan. Osalla lääkkeistä on useamman kuin yhden ryhmän mukaisia vaikutuksia. Digoksiini ja vernakalantti eivät sovi suoraan mihinkään näistä ryhmistä. Suluissa olevat lääkkeet ovat saatavana Suomessa ainoastaan erityisluvalla.
© Suomalainen Lääkäriseura Duodecim
Eteisvärinän kokonaisvaltainen hoito
- Eteisvärinän kokonaisvaltaisen hoidon osa-alueet on esitetty taulukossa «Eteisvärinän kokonaisvaltainen hoito...»5.
- Ennusteen kannalta tärkeintä on perussairauksien hyvä hoito ja tromboembolisten komplikaatioiden esto.
| 1. Perussairauksien hyvä hoito ja rytmihäiriöille altistavien ja laukaisevien tekijöiden eliminointi | |
| 2. Tromboembolisten komplikaatioiden esto | |
|
|
| 3. Sykkeenhallinta eli kammiotaajuuden optimointi | |
|
|
| 4. Rytminhallinta | |
A. Rytminsiirto eli sinusrytmin palauttaminen
|
|
B. Sinusrytmin ylläpito
|
|
Perussairauksien hoito
- Yhteenveto eteisvärinän tavallisimmista taustatekijöistä ja niiden hoidosta on esitetty
taulukossa «Eteisvärinän tavallisimpien taustatekijöiden hoitotavoitteita ja hoitomuotoja....»6.
- Näiden tilojen näyttöön perustuvaa diagnostiikkaa ja hoitoa käsitellään tarkemmin Käypä hoito -suosituksissa Kohonnut verenpaine «Kohonnut verenpaine»5, «Kohonnut verenpaine. Käypä hoito -suositus. Suomal...»78, Sydämen vajaatoiminta «Sydämen vajaatoiminta»6, «Sydämen vajaatoiminta. Käypä hoito -suositus. Suom...»79, Tyypin 2 diabetes «Tyypin 2 diabetes»7, «Tyypin 2 diabetes. Käypä hoito -suositus. Suomalai...»80, Lihavuus (lapset, nuoret ja aikuiset) «Lihavuus (lapset, nuoret ja aikuiset)»8, «Lihavuus (lapset, nuoret ja aikuiset). Käypä hoito...»81, Uniapnea «Uniapnea (obstruktiivinen uniapnea aikuisilla)»9, «Uniapnea (obstruktiivinen uniapnea aikuisilla). Kä...»82 ja Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito «Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito»10, «Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito...»83.
| Taustatekijä | Hoidon tavoite | Hoitokeinot |
|---|---|---|
| * beetasalpaaja, angiotensiinikovertaasientsyymin (ACE) estäjä, angiotensiinreseptorin (ATR) salpaaja, mineralokortikoidireseptorin salpaaja (MRA), ATR-salpaajan ja neprilysiinin estäjän yhdistelmä, natriumin- ja glukoosinkuljettajaproteiini 2:n (SGLT2) estäjä. | ||
| Kohonnut verenpaine | < 130 mmHg / 80 mmHg | ACE:n estäjä / ATR-salpaaja yleensä ensisijainen vaihtoehto |
| Sydämen vajaatoiminta | Nestekertymän välttäminen Oireiden hallinta |
Hoitosuositusten mukainen lääkitys* ja muu hoito Optimaalinen diureettien käyttö |
| Tyypin 2 diabetes | HbA1c < 48–53 mmol/mol Paastosokeri < 6–7 mmo/l | Hoitosuositusten mukainen diabeteslääkitys (erityisesti SGLT2:n estäjä tai GLP-1-reseptoriagonisti) |
| Lihavuus (obesiteetti) | BMI < 27 kg/m2 tai vähintään 10 %:n painonpudotus | Ravitsemusohjeet Lääkehoito Lihavuusleikkaus |
| Obstruktiivinen uniapnea | Apneajaksojen minimointi | CPAP-hoito |
| Vähäinen fyysinen rasitus | Yksilöllinen ohjaus säännölliseen liikuntaan | Liikkumisresepti |
| Alkoholin liikakäyttö | Korkeintaan 3 alkoholiannosta viikossa | Ohjaus ja vertaistuki |
| Tupakointi | Täysi tupakoimattomuus | Ohjaus ja vertaistuki Vierotusoireiden lääkehoito |
| Muut taustatekijät | Varhainen tunnistaminen | Suositusten mukainen hoito |
Kohonnut verenpaine ja sydämen vajaatoiminta
- Kohonneen verenpaineen ja sydämen vajaatoiminnan hyvä hoito vähentää eteisvärinän
ilmaantuvuutta ja estää eteisvärinän uusiutumista.
- Seitsemän satunnaistetun tutkimuksen meta-analyysissä ACE:n estäjät ja ATR-salpaajat vähensivät eteisvärinän ilmaantuvuutta vajaatoiminta- ja verenpainepotilailla 43 % «Madrid AH, Peng J, Zamora J ym. The role of angiot...»171.
- Verenpaineen hoidon tavoitteena on systolinen verenpaine < 130 mmHg ja diastolinen verenpaine < 80 mmHg.
- Ensisijaisia lääkkeitä ovat ACE:n estäjät ja ATR-salpaajat, jotka vähentävät eteisvärinän ilmaantumista kohonneessa verenpaineessa ja sydämen vajaatoiminnassa «ACE:n estäjät ja angiotensiinireseptorin (AT) salpaajat saattavat vähentää eteisvärinän ilmaantumista vajaatoiminta- ja verenpainepotilailla.»C.
- Sydämen vajaatoiminnassa on tärkeää optimoida vajaatoiminnan ennustetta parantava lääke- ja laitehoito ja estää ylimääräisen nesteen kertyminen (turvotukset, keuhkokongestio) diureeteilla. Valikoiduille potilaille voidaan tehdä eteisvärinän katetriablaatio (ks. tarkemmin myöhemmin).
Diabetes
- Noin 25 %:lla eteisvärinäpotilaista on todettavissa tyypin 2 diabetes «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Diabeteksen huono hoitotasapaino (suuri HbA1c-arvo) lisää eteisvärinän ilmaantuvuutta, ja vastaavasti hyvä sokeritasapaino ehkäisee eteisvärinää ja vähentää sen aiheuttamia oireita sekä parantaa rytminhallinnan tuloksia.
- Diabeteslääkkeiden vaikutus eteisvärinään vaihtelee.
- Paras näyttö eteisvärinän suhteen on SGLT2:n estäjistä ja GLP-1-reseptoriagonisteista «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
Lihavuuden hoito
- Ylipainon ja eteisvärinän välillä on selvä yhteys, ja laihduttamisella on suotuisa
vaikutus eteisvärinän ilmaantumiseen ja hoidon tehoon «Schnabel RB, Yin X, Gona P ym. 50 year trends in a...»174.
- Ylipainoisilla eteisvärinän ilmaantuminen vähenee suorassa suhteessa painon vähenemiseen, mutta sen vaikutus potilaiden ennusteeseen on kiistanalainen ("obesity paradox") «Miller JD, Aronis KN, Chrispin J ym. Obesity, Exer...»175, «Nalliah CJ, Sanders P, Kottkamp H ym. The role of ...»176, «Cambeiro G, Cristina M, Mañero R ym. Review Of Obe...»177, «Goudis CA, Korantzopoulos P, Ntalas IV ym. Obesity...»178.
- Ylipainoisilla tavoitteena on BMI < 27 kg/m2 tai vähintään 10 %:n painonpudotus.
Uniapnea
- Uniapnea lisää eteisvärinän ilmaantumista ja heikentää eteisvärinän estohoidon tehoa.
- CPAP-hoito saattaa parantaa joidenkin potilaiden hoidon tehoa, mutta tulokset ovat ristiriitaisia.
Dyslipidemia
- Dyslipidemian ja dyslipidemialääkityksen vaikutus eteisvärinän ilmaantuvuuteen ja uusiutumisen on vähäinen «Yao Y, Liu F, Wang Y, ym. Lipid levels and risk of...»179.
- Toisaalta statiineilla on suotuisa vaikutus sepelvaltimotautiin ja ne saattavat vähentää eteisvärinän ilmaantumista sydänleikkauksen jälkeen, mutta tutkimusten tulokset ovat ristiriitaisia «Savelieva I, Camm J. Statins and polyunsaturated f...»172.
Ruokavalio
- Eteisvärinäpotilaille suositellaan sydänystävällistä ruokavaliota «https://sydan.fi/sydantietoa/ruoka-ravitsemus/»1.
- Kalaöljyvalmisteet eivät nykykäsityksen mukaan estä eteisvärinän uusiutumista «Savelieva I, Camm J. Statins and polyunsaturated f...»172, «Kowey PR, Reiffel JA, Ellenbogen KA ym. Efficacy a...»173.
- Kalaöljyt saattavat suurentaa verenvuotoriskiä, jos niitä käytetään yhdessä antikoagulaatiohoidon kanssa.
Akuutin kohtauksen hoito
- Sähköinen rytminsiirto on rytmihäiriön kestosta ja antikoagulaatiohoidon toteutuksesta riippumatta tehtävä heti, jos eteisvärinä romahduttaa potilaan hemodynamiikan.
- Hemodynaamisesti vakaiden potilaiden sinusrytmi palautuu itsestään vuorokauden kuluessa
lähes 70 %:ssa tapauksista, minkä takia vähäoireisten potilaiden rytminsiirrolla ei
ole välitöntä kiirettä, vaan alkuvaiheessa voidaan keskittyä sykkeenhallintaan.
- Pienessä tai keskisuuressa tukosvaarassa olevien (CHA2DS2VA ≤ 1) spontaania sinusrytmin palautumista ei kuitenkaan pidä odottaa yli 48:aa tuntia,
jotta rytminsiirtoa ei jouduta lykkäämään, kunnes tehokas antikoagulaatiohoito on
ollut käytössä vähintään 3 viikon ajan.
- Suuressa tukosvaarassa olevien antikoaguloimattomien (CHA2DS2VA ≥ 2) potilaiden sinusrytmin spontaania palautumista ei pidä odottaa yli 24:ää tuntia, jotta rytminsiirtoa ei jouduta lykkäämään.
- Pysyvää terapeuttisella tasolla olevaa antikoagulaatiohoitoa käyttävien välitön rytminsiirto voidaan tehdä riippumatta rytmihäiriön kestosta.
- Pienessä tai keskisuuressa tukosvaarassa olevien (CHA2DS2VA ≤ 1) spontaania sinusrytmin palautumista ei kuitenkaan pidä odottaa yli 48:aa tuntia,
jotta rytminsiirtoa ei jouduta lykkäämään, kunnes tehokas antikoagulaatiohoito on
ollut käytössä vähintään 3 viikon ajan.
- Jos eteisvärinän syynä on akuutti sydäninfarkti, sydämen vajaatoiminnan äkillinen paheneminen, sydänlihastulehdus, kilpirauhasen liikatoiminta, elektrolyyttihäiriö tai jokin muu hoidettavissa oleva tekijä, hoito kohdistetaan ensin perussyyhyn ja sinusrytmi palautetaan vasta sen jälkeen «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoit...»71.
- Antikoagulaatiohoidon tarve «Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä»8, «Antitromboottinen hoito eteisvärinässä»4 on arvioitava, vaikka sinusrytmi palautuisi itsestään.
- Suuren riskin potilaiden (CHA2DS2VA ≥ 2) pysyvä antikoagulaatiohoito on aiheellinen, myös näissä tapauksissa.
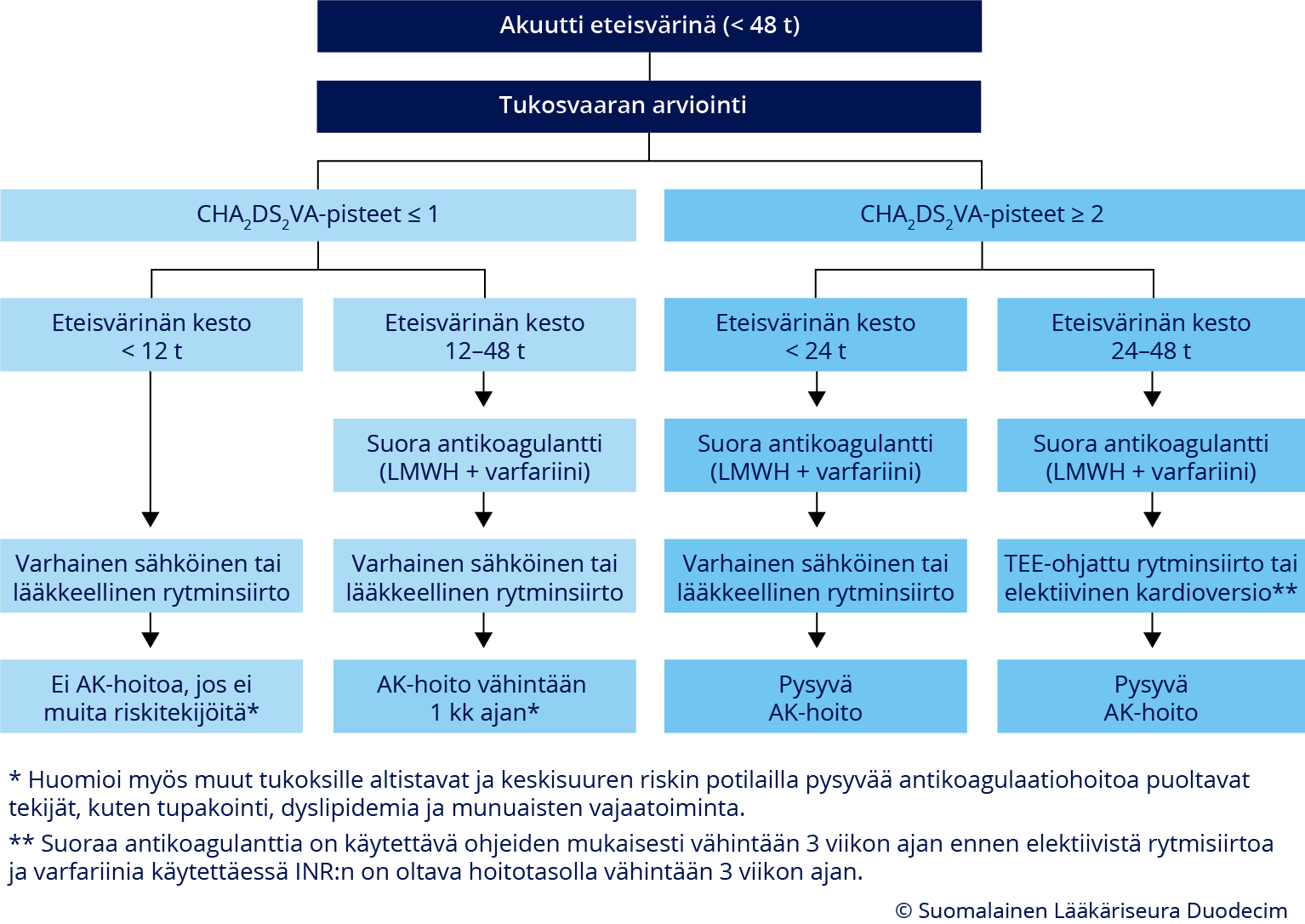
Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä. Akuutissa eteisvärinässä varhaisen rytminsiirron mahdollisuus arvioidaan tukosvaaratekijöiden ja rytmihäiriön keston perusteella. Pienen ja keskisuuren riskin potilailla eteisvärinän kardioversioon liittyvä tulosvaara on niin pieni, että antikoagulaatiohoitoa ei tarvita ennen eikä jälkeen rytminsiirron, jos rytmihäiriön kesto on alle 12 tuntia. Jos rytmihäiriön kesto on 12–48 tuntia myös heille annetaan ensimmäinen annos suoraa antikoagulantti (tai pieni molekyylistä hepariinia ja varfariina) jo ennen rytminsiirtoa, kuten suuren riskin potilaille ja rytminsiirron jälkeen AK-hoitoa jatketaan riskitekijöiden mukaan vähintään 1 kuukauden ajan tai pysyvästi (ks. tarkemmin teksti).
© Suomalainen Lääkäriseura Duodecim
Kammiovasteen hidastaminen akuutissa eteisvärinässä
- Hemodynaamisesti vakaan eteisvärinäkohtauksen alkuvaiheessa keskitytään lievittämään
potilaan oireita hidastamalla kammiotaajuutta eteis-kammiojohtumista jarruttavilla
lääkkeillä (taulukko «Akuutin eteisvärinäkohtauksen kammiovasteen hidastamisessa tehokkaiksi osoittautuneita
suoneen annettavia lääkkeitä...»7). Tavoitteena on alle 110/min:n taajuus «Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoit...»71.
- Vaikutus ilmaantuu nopeasti, kun lääke annetaan laskimoon.
- Beetasalpaajat hidastavat tehokkaasti akuutin eteisvärinän kammiotaajuutta estämällä adrenergista
järjestelmää «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Segal JB, McNamara RL, Miller MR ym. The evidence ...»84, «Snow V, Weiss KB, LeFevre M ym. Management of newl...»85, «Grönefeld GC, Hohnloser SH. Beta-blocker therapy i...»86.
- Ne ovat turvallisia sepelvaltimotaudissa ja oikein annosteltuina myös sydämen vajaatoiminnassa.
- Kalsiuminestäjät (verapamiili ja diltiatseemi) hidastavat akuutin eteisvärinän kammiovastetta vaikuttamalla
suoraan eteis-kammiosolmukkeeseen «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Segal JB, McNamara RL, Miller MR ym. The evidence ...»84, «Snow V, Weiss KB, LeFevre M ym. Management of newl...»85.
- Ne ovat hyvin siedettyjä potilailla, joilla ei ole todettu sydänsairauksia.
- Niitä on kuitenkin varottava sydämen vajaatoiminnassa, koska ne voivat aiheuttaa vaikean hypotension heikentämällä vasemman kammion pumppausvoimaa.
- Digoksiini hidastaa kammiovastetta akuutissa eteisvärinässä, mutta sen vaikutus alkaa hitaammin
ja teho on huonompi kuin beetasalpaajien ja kalsiuminestäjien «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Segal JB, McNamara RL, Miller MR ym. The evidence ...»84.
- Se on akuutissa sydämen vajaatoiminnassa (esim. keuhkopöhössä) hemodynamiikan kannalta turvallisempi kuin beetasalpaajat tai kalsiuminestäjät.
- Kalsiuminestäjät, digoksiini ja beetasalpaajat lisäävät kilpailevaa johtumista oikoradassa, minkä takia niitä ei suositella eteisvärinäkohtauksen hoitoon potilailla, joilla on todettu kammioiden varhaisaktivaatio (delta-aalto).
- Amiodaroni hidastaa kammiovastetta akuutissa eteisvärinässä estämällä sekä adrenergista järjestelmää
että hitaiden kalsiumkanavien toimintaa «Singh BN. Antiarrhythmic actions of amiodarone: a ...»87, «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88
- Amiodaroni ei ole ensisijainen lääke akuutin eteisvärinän kammiovasteen hidastamiseen, vaikka sydämenulkoiset haittavaikutukset ja proarytmia ovat lyhytaikaisessa käytössä harvinaisia.
- Vähäisen negatiivisen inotrooppisen vaikutuksensa ansiosta amiodaroni on usein hyvä vaihtoehto postoperatiivisten, kriittisesti sairaiden tai muuten hemodynaamisesti epävakaiden potilaiden eteisperäisten rytmihäiriöiden hoitoon «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Clemo HF, Wood MA, Gilligan DM ym. Intravenous ami...»89.
- Amiodaroni hidastaa johtumista myös oikoradoissa, joten sitä voidaan harkitusti käyttää myös WPW-oireyhtymässä.
- Dronedaronia ei ole tutkittu akuutin eteisvärinän kammiovasteen hidastamisessa.
- Vakavien haittavaikutustensa takia se on vasta-aiheinen pysyvässä eteisvärinässä, vaikka se hidastaa kammiovastetta tehokkaasti «Page RL, Hamad B, Kirkpatrick P. Dronedarone. Nat ...»90, «Hoy SM, Keam SJ. Dronedarone. Drugs 2009;69:1647-6...»91.
- Sotaloli hidastaa kammiovastetta, mutta sitä ei pidä kääntyvien kärkien kammiotakykardian vaaran takia käyttää kammiovasteen hidastamiseen.
- Ibutilidilla ja vernakalantilla ei ole vaikutusta kammiotaajuuteen «Murray KT. Ibutilide. Circulation 1998;97:493-7 ...»92, «Cheng JW. Vernakalant in the management of atrial ...»93.
- Ryhmän I lääkkeillä ei WPW-oireyhtymää lukuun ottamatta ole käyttöä kammiovasteen säätelyssä «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Tavanomaisessa eteisvärinässä ne saattavat paradoksaalisesti nopeuttaa kammiovastetta hidastamalla eteistaajuutta.
- WPW-oireyhtymässä ne hidastavat kammiovastetta estämällä johtumista oikoradassa.
- Beetasalpaajien ja kalsiuminestäjien yhteiskäyttö ei ole suositeltavaa akuutin eteisvärinän kammiovasteen hidastamisessa. Sen sijaan digoksiinia voidaan käyttää sekä beetasalpaajan että kalsiuminestäjän kanssa.
| Lääke | Annossuositus |
|---|---|
| Sykkeenhallintaan voidaan kiireettömissä tilanteissa käyttää myös suun kautta annettavia valmisteita. | |
| Beetasalpaajat | |
| Esmololi | Alkuannos 10–50 mg nopeana ruiskeena, jatkoinfuusio 1–4 mg/min syketaajuuden ja verenpaineen mukaan |
| Metoprololi | 5 mg hitaana ruiskeena; voidaan uusia 2–3 kertaa viiden minuutin välein |
| Kalsiuminestäjät | |
| Verapamiili | 2,5–5 mg hitaana ruiskeena; tarvittaessa toistetaan 10 mg:n kokonaisannokseen asti |
| Muut lääkkeet | |
| Digoksiini | 0,25–0,5 mg hitaana ruiskeena; voidaan uusia 2–3 kertaa 1–2 tunnin välein (kokonaisannos enintään 1 mg/vrk) |
| Amiodaroni | Alkuannos 150–300 mg infuusiona 10–60 minuutissa, jatkoinfuusio 1 200–1 800 mg/vrk |
Rytminsiirto
- Rytminsiirto (sähköinen) on tehtävä heti, jos eteisvärinä romahduttaa potilaan hemodynamiikan.
- Muissa tapauksissa rytmisiirron tarve arvioidaan yksilöllisesti edellä esitettyjä ohjeita noudattaen (ks. kohta Hoitolinjan valinta «A1»2).
- Akuutissa (< 24–48 tuntia kestäneessä) eteisvärinässä antikoagulaatiohoidon tarve riippuu muista tukosvaaratekijöistä ja rytmihäiriön kestosta «Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä»8.
- Jos tukosvaaratekijöiden määrä tai rytmihäiriön kesto on epäselvä, turvallisinta on aloittaa antikoagulaatiohoito.
- Suuren riskin potilaille (CHA2DS2VA ≥ 2) aloitetaan joko suora antikoagulantti tai pienimolekyylinen hepariini ja varfariini
ennen rytminsiirtoa, ja heillä antikoagulaatiohoitoa jatketaan pysyvästi.
- Varfariinia käytettäessä pienimolekyylistä hepariinia jatketaan painonmukaisella hoitoannoksella, kunnes INR on hoitotasolla «Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä»8.
- Pienen ja keskisuuren riskin potilaiden (CHA2DS2VA ≤ 1) tukosvaara on niin pieni, että rytminsiirto voidaan tehdä ilman antikoagulaatiohoitoa, jos rytmihäiriön kesto on alle 12 tuntia. Jos rytmihäiriön kesto on 12–48 tuntia, aloitetaan antikoagulaatiohoito ennen rytminsiirtoa, kuten suuren riskin potilaille, ja sitä jatketaan vaaratekijöistä riippuen vähintään kuukauden ajan tai pysyvästi.
- Pitkittyneessä (vähintään 48 tuntia) tai kestoltaan epäselvässä eteisvärinässä rytminsiirron edellytyksenä on jokin seuraavista «Nagarakanti R, Ezekowitz MD, Oldgren J ym. Dabigat...»94, «Piccini JP, Stevens SR, Lokhnygina Y ym. Outcomes ...»95, «Flaker G, Lopes RD, Al-Khatib SM ym. Efficacy and ...»96, «Cappato R, Ezekowitz MD, Klein AL ym. Rivaroxaban ...»97, «Caldeira D, Costa J, Ferreira JJ ym. Non-vitamin K...»98:
- Suora antikoagulantti (apiksabaani, dabigatraani, edoksabaani, rivaroksabaani) on ollut säännöllisessä käytössä vähintään 3 viikon ajan.
- Antikoagulaatiohoito varfariinilla on ollut hoitotasolla (INR > 2) vähintään 3 viikon ajan ennen rytminsiirtoa.
- Ruokatorven kautta tehdyssä sydämen kaikututkimuksessa tai sydämen tietokonekuvauksessa ei havaita sydämensisäisiä trombeja.
Sähköinen rytminsiirto
- Sähköistä rytminsiirtoa eli kardioversiota voidaan käyttää sekä akuutin eteisvärinäkohtauksen
hoidossa että elektiivisesti.
- Alle 48 tuntia kestäneessä eteisvärinässä kardioversion teho on yli 90 %.
- Eteisvärinän pitkittyessä rytminsiirron teho huononee, minkä takia elektiivisessä rytminsiirrossa pitää välttää turhia viiveitä.
- Sähköisessä rytminsiirrossa sinusrytmi palautetaan QRS-heilahdukseen synkronoidulla
bifaasisella tasavirtaiskulla kevyen anestesian aikana (kuva «Sähköinen rytminsiirto»9). Ks. Lääkärin käsikirjan artikkeli Sähköisen rytminsiirron suoritus «Sähköisen rytminsiirron suoritus»4 (vaatii käyttöoikeuden).
- Lääkkeisiin verrattuna sähköisen rytminsiirron etuina ovat hyvä teho ja turvallisuus «Sähköinen rytminsiirto on lääkkein tehtyä rytminsiirtoa tehokkaampi ja turvallinen.»A.
- Sähköisessä rytminsiirrossa suositellaan käytettävän suoraan maksimaalista energiaa, sillä se tehoaa paremmin kuin pienemmällä teholla aloitettu ja asteittain nostettu defibrillaatioenergia «Schmidt AS, Lauridsen KG, Torp P ym. Maximum-fixed...»99.
- Jos sinusrytmi ei palaudu maksimienergiallakaan, voidaan
- harkinnan mukaan antaa ibutilidia (1 mg 10 minuutin infuusiona), ellei sille ole vasta-aiheita, ja toistaa kardioversioyritys sen jälkeen saman anestesian aikana «Oral H, Souza JJ, Michaud GF ym. Facilitating tran...»100
- aloittaa rytmihäiriölääkitys suun kautta ja toistaa kardioversioyritys myöhemmin lääkkeen vaikutuksen vakiinnuttua (antikoagulaation on oltava hoitotasolla) «Marcus GM, Sung RJ. Antiarrhythmic agents in facil...»101, «Van Noord T, Van Gelder IC, Crijns HJ. How to enha...»102.
- Sähköinen rytminsiirto on vasta-aiheinen, jos
- eteisvärinän syy on hoidettavissa (esim. elektrolyyttihäiriö, digitalismyrkytys tai vaikea kilpirauhasen liikatoiminta on korjattava ennen rytminsiirtoa)
- potilaalla on sinus- tai eteis-kammiosolmukkeen vaikea toimintahäiriö eikä hänellä ole tahdistinta
- rytmi vaihtelee spontaanisti sinusrytmin ja eteisvärinän välillä (rytmihäiriölääkkeitä voidaan käyttää).

Sähköinen rytminsiirto. Sähkövirta ohjautuu parhaiten sydämen läpi, jos toinen defibrillaatioelektrodeista asetetaan potilaan selkäpuolelle (apex-posterior tai anterior-posterior). Ellei käytössä ole elektrodia, joka voidaan asettaa potilaan selkäpuolelle, on suositeltavaa asettaa toinen elektrodi sydämen kärjen seutuun ja toinen ylös, hiukan rintalastan oikealle puolelle (apex-anterior). Naisilla elektrodia ei saa asettaa rinnan päälle. Elektrodien alle on laitettava riittävästi pastaa, ja käsielektrodeja on painettava tarpeeksi voimakkaasti. Kardioversiossa käytetään bifaasista defibrillaattoria ja heti ensimmäisessä kardioversioiskussa käytetään laitteen maksimitehoa. Uusi rytminsiirtoyritys voidaan tehdä heti verenpaineen ja eteisvärinärytmin vakiinnuttua eli käytännössä noin minuutin kuluttua edellisestä yrityksestä. Kun rytminsiirtoa tehdään tahdistinpotilaalle, elektrodit sijoitetaan siten, että niiden välinen akseli sijaitsee poikittain tahdistimen ja sydämen kärjen akseliin nähden. Rytmihäiriötahdistinpotilaille eteisvärinän rytminsiirto on turvallisinta tehdä ohjelmoimalla laite antamaan synkronoitu isku sydämensisäisesti kevyessä anestesiassa. Ellei tämä tehoa, rytminsiirto tehdään kuten tahdistinpotilaalle. Kuvan lähde: Heikkilä J ym. (toim.) Kardiologia. Kustannus Oy Duodecim 2008, s. 544.
Lääkkeellinen rytminsiirto
- Lääkkeellinen rytminsiirto tehoaa hyvin akuutissa eteisvärinässä, mutta sitä ei pidä
käyttää elektiivisessä rytminsiirrossa, koska lääkkeet menettävät nopeasti tehoaan
eteisvärinän pitkittyessä «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Lääkkeellisessä rytminsiirrossa ei tarvita anestesiaa eikä edeltävää paastoa, minkä ansiosta se on helpommin toteutettavissa kuin sähköinen rytminsiirto.
- Haittapuolia ovat sähköistä rytminsiirtoa huonompi teho «Sähköinen rytminsiirto on lääkkein tehtyä rytminsiirtoa tehokkaampi ja turvallinen.»A, proarytmian vaara ja muut lääkkeiden haittavaikutukset.
- Ohje lääkkeellisen rytminsiirron toteuttamisesta esitetään taulukossa «Lääkkeellisen rytminsiirron toteutus...»8.
- Eteisvärinän rytmisiirtoon nykyään käytettävissä olevat lääkkeet esitetään taulukossa «Akuutin eteisvärinän rytminsiirrossa käytettäviä lääkkeitä. ...»9.
- Flekainidi «Flekainidi palauttaa sinusrytmin akuutissa eteisvärinässä tehokkaammin kuin lumelääke.»A on lumelääkettä tehokkaampi eteisvärinän rytminsiirrossa.
- Suun kautta annettuna flekainidi soveltuu myös perusterveydenhuollossa käytettäväksi, jos sydän on aiemmin todettu terveeksi.
- Kammioperäiset proarytmiat ovat harvinaisia, mutta kammiovasteen paradoksaalisen nopeutumisen välttämiseksi potilaalle suositellaan annettavaksi beetasalpaajaa tai muuta eteis-kammiojohtumista hidastavaa lääkettä ennen flekainidin antoa «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Flekainidia voidaan harkitusti käyttää myös WPW-oireyhtymään liittyvässä eteisvärinäkohtauksessa, koska se hidastaa johtumista oikoradassa «Crozier I. Flecainide in the Wolff-Parkinson-White...»103.
- Flekainidia ei pidä käyttää eteisvärinän rytminsiirrossa «Raatikainen MJP, Sigurd B. Atrial fibrillation - t...»104, jos
- rytmihäiriö liittyy akuuttiin sydäninfarktiin tai sydämen vajaatoiminnan pahenemiseen
- potilaalla on todettu sydäninfarkti tai sydämen vajaatoiminta
- potilaalla on todettu sinussolmukkeen toimintahäiriö, toisen tai kolmannen asteen eteis-kammiokatkos tai haarakatkos (tai QRS-heilahdus on muuten leventynyt) eikä sydäntä ole mahdollista tahdistaa
- potilaalla on eteislepatus (altistaa 1:1-eteis-kammiojohtumiselle).
- Tavallisimpia flekainidin aiheuttamia haittavaikutuksia ovat «Capucci A, Villani GQ, Aschieri D ym. Safety of or...»105, «Aliot E, De Roy L, Capucci A ym. Safety of a contr...»106, «Kishore AG, Camm AJ. Guidelines for the use of pro...»107
- lievät neurologiset oireet, kuten huimaus ja näköhäiriöt
- verenpaineen ohimenevä lasku
- kammiovasteen paradoksaalinen nopeutuminen
- sinusrytmin palautumista seuraava bradykardia.
- Suoneen annettu vernakalantti on lumelääkettä tehokkaampi akuutin (< 48 tuntia kestäneen) eteisvärinän rytminsiirrossa
«Suonensisäisesti annettu vernakalantti on lumelääkettä tehokkaampi kääntämään eteisvärinän sinusrytmiin.»A. Teho huononee yli 72 tuntia kestäneessä eteisvärinässä selvästi.
- Vernakalantti salpaa sydänlihassolujen ultranopeita kalium- ja natriumkanavia, joten sen vaikutus kohdistuu pääasiassa eteisiin eikä QT-aika pitene merkittävästi «Naccarelli GV, Wolbrette DL, Samii S ym. Vernakala...»108.
- Etuna on nopea vaikutus: sinusrytmi palautuu keskimäärin 11 minuutin kuluttua infuusion aloittamisesta «Roy D, Pratt CM, Torp-Pedersen C ym. Vernakalant h...»109, «Kowey PR, Dorian P, Mitchell LB ym. Vernakalant hy...»110.
- Yleisimpiä haittavaikutuksia ovat ohimenevät makutuntemukset, puutumisoireet, pahoinvointi ja aivastelu «Naccarelli GV, Wolbrette DL, Samii S ym. Vernakala...»108
- Vakavat haittavaikutukset ovat harvinaisia, mutta hypotonia on mahdollinen.
- Vernakalantti on vasta-aiheinen vaikeassa sydämen vajaatoiminnassa, aorttaläpän ahtaumassa ja tuoreessa sepelvaltimotautikohtauksessa.
- Amiodaroni on lumelääkettä tehokkaampi eteisvärinän rytminsiirrossa, mutta sen vaikutus on hitaampi
kuin muiden eteisvärinän rytminsiirtoon käytettävien lääkkeiden «Amiodaroni palauttaa sinusrytmin akuutissa eteisvärinässä tehokkaammin kuin lumelääke.»B.
- Amiodaronia voidaan valikoivasti käyttää myös postoperatiivisten, kriittisesti sairaiden tai muuten hemodynaamisesti epävakaiden potilaiden eteisperäisten rytmihäiriöiden hoitoon «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Clemo HF, Wood MA, Gilligan DM ym. Intravenous ami...»89.
- Pitkäaikaiselle amiodaronihoidolle ominaiset sydämenulkoiset haittavaikutukset ovat akuuttihoidossa harvinaisia.
- Ibutilidi on lumelääkettä tehokkaampi akuutin eteisvärinän rytminsiirrossa «Ibutilidi on lumelääkettä tehokkaampi eteisvärinän rytminsiirrossa.»A.
- Ibutilidin etuna on hyvä teho eteislepatukseen «Raatikainen MJ, Lindgren K. Uusien ryhmän III lääk...»111.
- Kääntyvien kärkien kammiotakykardian vaaran takia ibutilidin käyttö on syytä rajata rytmihäiriöiden hoitoon perehtyneiden erikoislääkäreiden vastuulle.
- Ibutilidi on vasta-aiheinen, jos potilaalla on todettu sairas sinus -oireyhtymä, toisen tai kolmannen asteen eteis-kammiokatkos, monimuotoinen kammiotakykardia tai pieni kaliumpitoisuus tai jos korjattu QT-aika (QTc) on yli 0,44 s tai kammiotaajuus alle 50/min «Murray KT. Ibutilide. Circulation 1998;97:493-7 ...»92, «Raatikainen MJ, Lindgren K. Uusien ryhmän III lääk...»111.
- Beetasalpaajien tehosta akuutin eteisvärinän rytminsiirrossa ei ole näyttöä, mutta ne helpottavat oireita hidastamalla kammiovastetta.
- Kalsiuminestäjät «Kalsiuminestäjät eivät ilmeisesti palauta sinusrytmiä akuutissa eteisvärinässä.»B, digoksiini ja sotaloli «Suonensisäisesti tai suun kautta annettu sotaloli ei ole merkitsevästi parempi kuin lumelääke akuutin eteisvärinän rytminsiirrossa (alle 7 vuorokautta).»B ovat tehottomia eteisvärinän rytminsiirrossa, mutta ne voivat helpottaa oireita hidastamalla
kammiovastetta.
- Kalsiumestäjät ja digoksiini saattavat pitkittää eteisvärinäkohtausta ja altistaa sen uusiutumiselle «McNamara RL, Tamariz LJ, Segal JB ym. Management o...»65, «Snow V, Weiss KB, LeFevre M ym. Management of newl...»85, «Raatikainen MJ. Is verapamil a double-edged sword ...»112.
- Hoito, jossa potilas ottaa flekainidia itsenäisesti heti rytmihäiriön alettua ("pill
in the pocket"), vaatii erikoislääkärin arviota «Alboni P, Botto GL, Baldi N ym. Outpatient treatme...»113.
- Edellytyksenä on aiemmin sairaalassa samalla valmisteella turvallisesti suoritettu rytminsiirto.
| 1. Varmista, että käytettävissä on riittävät seurantavälineet (EKG-valvonta, verenpaineen mittaus, happisaturaation mittaus) ja valmius mahdollisen proarytmian hoitoon (defibrillaattori). |
| 2. Kytke potilas EKG-monitoriin. |
| 3. Avaa suoniyhteys ja tarvittaessa aloita nesteytys esimerkiksi fysiologisella keittosuolaliuoksella. |
| 4. Hidasta kammiovastetta beetasalpaajalla (tai kalsiuminestäjällä tai digoksiinilla). |
| 5. Valitse rytminsiirtoon käytettävä lääke yksilöllisesti niin, että huomioit eri lääkkeiden edut ja haitat. |
|
| 6. Sinusrytmin palautumisen jälkeen EKG-valvontaa jatketaan lääkkeen mukaan vähintään 3–4 tunnin ajan, minkä jälkeen hyväkuntoiset potilaat voidaan kotiuttaa. |
| 7. Ellei sinusrytmi palaudu lääkkeen annon jälkeen, potilas pitää ohjata sähköiseen rytminsiirtoon eikä yrittää lääkkeellistä rytminsiirtoa toisella valmisteella. |
| Lääke | Annossuositus | Näytönaste |
|---|---|---|
| 1) Erityistapauksissa voidaan käyttää myös suurempia annoksia. | ||
| Tehokkaiksi todetut | ||
| Flekainidi | Suoneen 1–2 mg/kg 10–30 minuutin infuusiona (enintään 150 mg) Suun kautta 300 mg:n kerta-annoksena |
«Flekainidi palauttaa sinusrytmin akuutissa eteisvärinässä tehokkaammin kuin lumelääke.»A |
| Vernakalantti | Suoneen 3 mg/kg 10 minuutin infuusiona (enintään 339 mg), tarvittaessa 15 minuutin kuluttua 2 mg/kg 10 minuutin infuusiona (enintään 226 mg) |
«Suonensisäisesti annettu vernakalantti on lumelääkettä tehokkaampi kääntämään eteisvärinän sinusrytmiin.»A |
| Amiodaroni | Alkuannos 150–300 mg suoneen, jatkoinfuusio 1 200–1 800 mg/vrk1) | «Amiodaroni palauttaa sinusrytmin akuutissa eteisvärinässä tehokkaammin kuin lumelääke.»B |
| Ibutilidi | Suoneen 1 mg / 10 min (voidaan toistaa kertaalleen 10 minuutin kuluttua) | «Ibutilidi on lumelääkettä tehokkaampi eteisvärinän rytminsiirrossa.»A |
| Tehosta ei riittävästi tietoa | ||
| Beetasalpaajat | ||
| Dronedaroni | ||
| Tehottomiksi todetut | ||
| Digoksiini | Tehoton sekä suun kautta että suoneen annettuna | |
| Kalsiuminestäjät | Tehoton sekä suun kautta että suoneen annettuna | «Kalsiuminestäjät eivät ilmeisesti palauta sinusrytmiä akuutissa eteisvärinässä.»B |
| Sotaloli | Tehoton sekä suun kautta että suoneen annettuna | «Suonensisäisesti tai suun kautta annettu sotaloli ei ole merkitsevästi parempi kuin lumelääke akuutin eteisvärinän rytminsiirrossa (alle 7 vuorokautta).»B |
Antikoagulaatiohoito eteisvärinän rytminsiirron yhteydessä
- Myös akuutin eteisvärinän rytminsiirtoon voi liittyä huomattava tukosvaara.
- Tukosvaara riippuu eteisvärinäkohtauksen kestosta ja CHA2DS2VA-pisteytyksen avulla arvioitavista tukosvaaratekijöistä «Airaksinen KE, Grönberg T, Nuotio I ym. Thromboemb...»114, «Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä»8.
- Tromboembolisten komplikaatioiden vaara on erityisen suuri ensimmäisten rytminsiirtoa seuraavien päivien aikana. Mediaaniaika tukoksen ilmaantumiseen on 2 vuorokautta rytminsiirrosta «Airaksinen KE, Grönberg T, Nuotio I ym. Thromboemb...»114.
- Varhaisen rytminsiirron jälkeen ilmenevien tukosten välttämiseksi kaikille suuren riskin potilaille annetaan ensimmäinen annos suoraa antikoagulanttia (tai pienimolekyylistä hepariinia ja varfariinia) jo ennen rytminsiirtoa ja antikoagulaatiohoitoa jatketaan pysyvästi.
- Suorien antikoagulanttien vaikutus alkaa nopeasti, eikä pienimolekyylistä hepariinia tarvita «Nagarakanti R, Ezekowitz MD, Oldgren J ym. Dabigat...»94, «Piccini JP, Stevens SR, Lokhnygina Y ym. Outcomes ...»95, «Flaker G, Lopes RD, Al-Khatib SM ym. Efficacy and ...»96, «Cappato R, Ezekowitz MD, Klein AL ym. Rivaroxaban ...»97, «Caldeira D, Costa J, Ferreira JJ ym. Non-vitamin K...»98, «Steffel J, Verhamme P, Potpara TS ym. The 2018 Eur...»116.
- Varfariinia käytettäessä pienimolekyylistä hepariinia jatketaan painonmukaisella hoitoannoksella, kunnes INR on hoitotasolla «European Heart Rhythm Association., European Assoc...»115. Pienimolekyylisten hepariinien hoitoannokset esitetään lisätietoaineistossa «Pienimolekyylisten hepariinien annostelu eteisvärinän rytmisiirron yhteydessä»2.
- Pienen riskin potilaille rytminsiirto voidaan tehdä ilman antikoagulaatiohoitoa, jos rytmihäiriön kesto on alle 12 tuntia. Jos rytmihäiriön kesto on 12–48 tuntia, toimitaan kuvassa «Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä»8 esitettyjen ohjeiden mukaisesti.
- Yli 48 tuntia jatkuneessa tai tuntemattoman ajan kestäneessä eteisvärinässä ilman antikoagulaatiohoitoa tehtyyn rytminsiirtoon liittyy
5–7 %:n emboliavaara «Bjerkelund CJ, Orning OM. The efficacy of anticoag...»117, «Arnold AZ, Mick MJ, Mazurek RP ym. Role of prophyl...»118 eikä rytminsiirtoa saa tehdä, jos
- suora antikoagulaatiohoito (apiksabaani, dabigatraani, edoksabaani, rivaroksabaani) ei ole ollut säännöllisessä käytössä vähintään 3 viikon ajan tai
- varfariinihoito ei ole ollut terapeuttisella tasolla (INR > 2,0) vähintään 3 viikon ajan tai
- sydämensisäisiä trombeja ei ole suljettu pois ruokatorven kautta tehdyllä sydämen kaikututkimuksella tai sydämen tietokonekuvauksella (ks. tarkemmin jäljempää).
- Elektiivisen rytminsiirron jälkeen antikoagulaatiohoitoa jatketaan (ks. tarkemmin kohta Antikoagulaatiohoito
«A2»3) seuraavasti:
- Suuren riskin potilaiden antikoagulaatiohoitoa jatketaan pysyvästi (CHA2DS2VA ≥ 2), vaikka sinusrytmi näyttäisi pysyvän «European Heart Rhythm Association., European Assoc...»115, «Thibault B, Talajic M, Dubuc M ym. Thromboembolic ...»119.
- Pienen ja keskisuuren riskin potilaiden (CHA2DS2VA = 1) antikoagulaatiohoitoa jatketaan vähintään 1 kuukauden ajan tai pysyvästi. Tukosvaaraa lisääviä ja pysyvää antikoagulaatiohoitoa puoltavia tekijöitä ovat muun muassa tupakointi, dyslipidemia ja munuaisten vajaatoiminta.
- On erittäin tärkeää varmistaa, että varfariinia käyttävien INR pysyy yli 2,0 myös rytminsiirron jälkeen.
- Eteislepatuksen rytminsiirrossa noudatetaan samoja ohjeita kuin eteisvärinässä «Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoit...»71, «European Heart Rhythm Association., European Assoc...»115, «Biblo LA, Yuan Z, Quan KJ ym. Risk of stroke in pa...»120.
Ruokatorven kautta tehtävä sydämen kaikukuvaus eteisvärinän rytminsiirrossa
- Rytminsiirto voidaan tehdä ilman terapeuttisella tasolla olevaa antikoagulaatiohoitoa
myös yli 24–48 tuntia kestäneessä eteisvärinässä, jos ruokatorven kautta tehdyssä sydämen kaikututkimuksessa
(TEE) ei havaita sydämensisäistä trombia «Eteisvärinän rytminsiirto voidaan tehdä ilman edeltävää antikoagulaatiohoitoa, jos ruokatorven kautta tehtävässä sydämen kaikututkimuksessa (TEE) ei havaita sydämen sisäistä verihyytymää.»A, (kuva «Ruokatorven kautta suoritetun sydämen kaikututkimuksen perusteella tehtävä eteisvärinän rytminsiirto»10).
- TEE-ohjauksessa tehtävää rytminsiirtoa kannattaa harkita, jos sinusrytmin nopea palauttaminen on tarpeen vaikeiden oireiden takia (EHRA 3–4).
- Vähäoireisille (EHRA 1) "taloudellista" eteisvärinää sairastaville TEE-tutkimus ja varhainen rytminsiirto eivät yleensä ole tarpeen.
- Sydämensisäinen trombi (kuva «Sydämensisäinen trombi»11) on ehdoton vasta-aihe ja "savuilmiö" (kuva «Sydämen kaikututkimuksessa havaittava savuilmiö»12) ja vasemman eteiskorvakkeen hidastunut virtaus (kuva «Sydämen kaikututkimuksessa havaittava eteiskorvakkeen hidastunut tyhjenemisnopeus»13) suhteellisia vasta-aiheita varhaiselle rytminsiirrolle «Troughton RW, Asher CR, Klein AL. The role of echo...»37, «Saarela E, Koskela V, Strandberg M ym. Ruokatorven...»67.
- Ennen TEE-ohjattua kardioversiota kaikille potilaille annetaan tukosvaaratekijöistä riippumatta joko suoraa antikoagulanttia tai pienimolekyylistä hepariinia ja varfariinia.
- TEE-ohjattu rytminsiirto nopeuttaa sinusrytmin palautumista, minkä ansiosta
- eteisten uudelleen muotoutuminen (remodeling) rytmihäiriötä suosivaksi estyy
- rytminsiirron onnistumismahdollisuudet paranevat «Saarela E, Koskela V, Strandberg M ym. Ruokatorven...»67, «Corrado G, Santarone M, Beretta S ym. Early cardio...»121, «Klein AL, Grimm RA, Murray RD ym. Use of transesop...»122 «Weigner MJ, Thomas LR, Patel U ym. Early cardiover...»123, «Roijer A, Eskilsson J, Olsson B. Transoesophageal ...»124, mutta vaikutus sinusrytmin säilymiseen on epävarmaa «Bartel T, Erbel R, Acute Trial Investigators.. Tra...»125, «Klein AL, Murray RD, Grimm RA. Role of transesopha...»126
- hoidon kustannukset pienenevät «Seto TB, Taira DA, Tsevat J ym. Cost-effectiveness...»127, «Klein AL, Murray RD, Becker ER ym. Economic analys...»128.
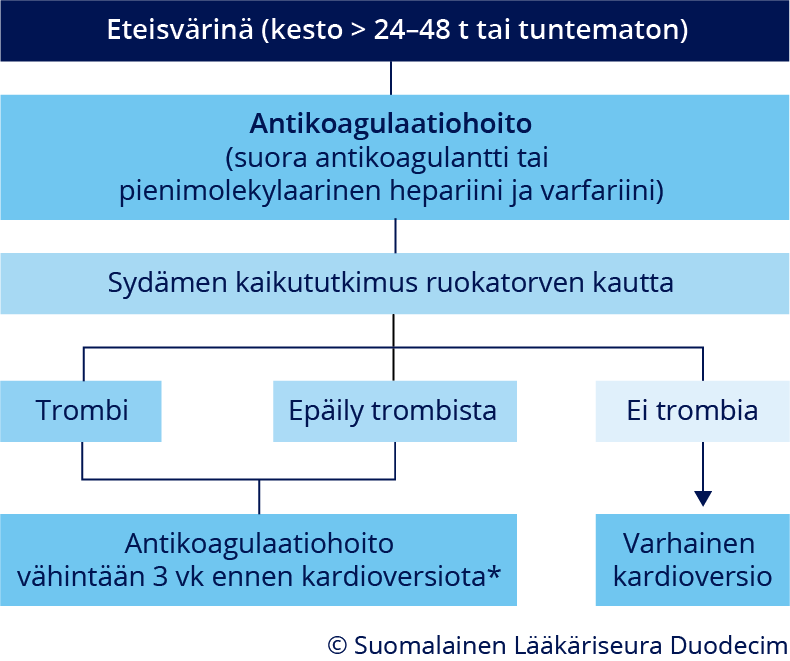
Ruokatorven kautta suoritetun sydämen kaikututkimuksen perusteella tehtävä eteisvärinän rytminsiirto. Eteisvärinän rytminsiirto voidaan tehdä ilman edeltävää antikoagulaatiohoitoa, jos ruokatorven kautta tehdyssä sydämen kaikututkimuksessa (TEE) ei havaita sydämen sisäistä trombia. Ennen varhaista rytminsiirtoa aloitetaan antikoagulaatiohoito joko suoralla antikoagulantilla tai pienimolekulaarisella hepariinilla (LMWH) ja varfariinilla. Jälkimmäisessä tapauksessa LMWH-pistoksia jatketaan sinusrytmin palautuessa, kunnes INR on hoitotasolla. Suoraa antikoagulanttia käytettäessä LMWH:ta ei tarvita. Antikoagulaatiohoitoa jatketaan muiden riskitekijöiden mukaan vähintään kuukauden ajan tai pysyvästi. TEE-tutkimus edellyttää tekijältä hyvää kokemusta, mikä rajoittaa sen käyttöä

Sydämensisäinen trombi. Ruokatorven kautta tehdyssä sydämen kaikututkimuksessa havaittu trombi on ehdoton vasta-aihe varhaiselle rytminsiirrolle. Rintakehän päältä tehtävän sydämen tavallisen kaikututkimuksen erottelukyky ei riitä varhaisen rytminsiirron ohjaukseen.

Sydämen kaikututkimuksessa havaittava savuilmiö. Ruokatorven kautta tehdyssä sydämen kaikututkimuksessa havaittava “savuilmiö” on merkki lisääntyneestä trombivaarasta, mutta ei ehdoton vasta-aihe varhaiselle rytminsiirrolle.

Sydämen kaikututkimuksessa havaittava eteiskorvakkeen hidastunut tyhjenemisnopeus. Ruokatorven kautta tehdyssä sydämen kaikututkimuksessa havaittava eteiskorvakkeen hidastunut tyhjenemisnopeus on merkki lisääntyneestä trombivaarasta, mutta ei ehdoton vasta-aihe varhaiselle rytminsiirrolle.
Estohoito (rytminhallinta)
- Jatkuva eteisvärinä uusiutuu rytminsiirron jälkeen ilman hoitoa jopa 80–90 %:lla potilaista
vuoden kuluessa «Lévy S, Breithardt G, Campbell RW ym. Atrial fibri...»129.
- Kohtauksittaisessa eteisvärinässä uusiutumisen vaara on suurempi kuin jatkuvassa.
- Estohoitoa on harkittava, jos potilas sietää eteisvärinää huonosti.
- Estolääkitys on yleensä pitkäkestoinen, mutta joissain tapauksissa voidaan käyttää myös lyhytkestoista lääkitystä (esim. flekainidia 4 viikkoa rytminsiirron jälkeen).
- Lyhytkestoinen lääkitys vähentää varhaisia relapseja muttei ole yhtä tehokas kuin pitkäkestoinen lääkitys «Kirchhof P, Andresen D, Bosch R ym. Short-term ver...»131.
- Estohoidon varhainen aloittaminen parantaa hoidon tehoa «Kirchhof P, Camm AJ, Goette A ym. Early Rhythm-Con...»130.
- Estohoito suunnitellaan yksilöllisesti unohtamatta rytmihäiriölle altistavien perussairauksien hoitoa ja invasiivisen hoidon mahdollisuuksia (taulukko «Eteisvärinän kokonaisvaltainen hoito...»5).
Estolääkitys
- Estolääkityksen valintaan vaikuttavat etenkin potilaan muut sydänsairaudet (kuva «Eteisvärinän estolääkityksen valinta»14) ja niiden lääkitys «Raatikainen MJ. Rytmihäiriölääkkeiden kliininen kä...»132.
- Beetasalpaajahoito voidaan yleensä aloittaa perusterveydenhuollossa taulukossa «Suositus eteisvärinäpotilaalle tehtävistä tutkimuksista...»4 mainittavien perustutkimusten jälkeen.
- Varsinaisten rytmihäiriölääkkeiden (amiodaroni, dronedaroni, flekainidi ja sotaloli)
käytön aloitus kuuluu kardiologille tai sisätautien erikoislääkärille, mutta perusterveydenhuollon
lääkärit voivat useimmiten vastata potilaiden seurannasta.
- Flekainidin, dronedaronin ja amiodaronin käyttö voidaan yleensä aloittaa polikliinisesti riittävien sydäntutkimusten (taulukko «Suositus eteisvärinäpotilaalle tehtävistä tutkimuksista...»4) jälkeen.
- Sotalolin käyttö suositellaan aloitettavaksi telemetriaseurannassa sairaalassa.
- Rytmihäiriölääkkeiden annokset eteisvärinän estohoidossa ja annokseen vaikuttavat
tekijät esitetään taulukossa «Yleisimmin käytössä olevien rytmihäiriölääkkeiden annokset eteisvärinän estohoidossa.
Estohoidossa kannattaa suosia pitkävaikutteisia kerran vuorokaudessa otettavia valmisteita
aina, kun sellainen on saatavana....»10.
- Ennen annoksen muuttamista tai lääkityksen lopettamista tehottomana on varmistettava, että lääkkeen vaikutus on ehtinyt vakiintua «Raatikainen MJ. Rytmihäiriölääkkeiden kliininen kä...»132.
- Objektiivista näyttöä lääkityksen tehosta saadaan esimerkiksi EKG:n pitkäaikaisrekisteröinnillä tai kliinisellä rasituskokeella.
- Lääkeaineen pitoisuus korreloi huonosti kliiniseen vasteeseen, mutta pitoisuusmäärityksiä voidaan käyttää esimerkiksi myrkytystä tai lääkeaineinteraktioita epäiltäessä.
- Rytmihäiriölääkitys estää vain harvoin eteisvärinän kokonaan.
- Realistinen tavoite on subjektiivisten oireiden lievittyminen ja kohtausten harventuminen.
- Sydämen kohdistuvista haittavaikutuksista ongelmallisimpia ovat proarytmia (taulukko «Eteisvärinän hoidossa käytettyjen rytmihäiriölääkkeiden aiheuttamia proarytmisia vaikutuksia ja niiden hoito ja ehkäisy...»11) ja negatiivisen inotrooppisen vaikutuksen aiheuttama vajaatoiminnan paheneminen.
- Tavallisimmat rytmihäiriölääkityksen aiheuttamat sydämenulkoiset haitat esitetään taulukossa «Eteisvärinän hoidossa käytettävien rytmihäiriölääkkeiden aiheuttamia sydämenulkoisia haittavaikutuksia. Kaikki rytmihäiriölääkkeet voivat lisäksi aiheuttaa erilaisina iho- tai muina oireina ilmeneviä allergisia reaktioita. Suluissa olevat lääkkeet ovat saatavana Suomessa vain erityisluvalla....»12.
| Lääke | Suositeltava ylläpitoannos/vrk | Näytön aste | Annoksen muuttaminen vajaatoiminnan yhteydessä | ||
|---|---|---|---|---|---|
| 1) Beetasalpaajaa on käytettävä varovasti sydämen vajaatoiminnassa, ja annosta on suurennettava
hitaasti valmistajan ohjeiden mukaisesti. 2) Dronedaroni on vasta-aiheinen munuaisten ja maksan vaikeassa vajaatoiminnassa, mutta lievissä toimintahäiriöissä annosta ei tarvitse muuttaa. |
|||||
| Munuaiset | Maksa | Sydän | |||
| Tehokkaiksi osoittautuneet | |||||
| Flekainidi | 100–200 mg x 1 | «Flekainidi estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A | Pienennä | Vasta-aiheinen | |
| Beetasalpaajat1) | «Beetasalpaajat näyttävät vähentävän eteisvärinän uusiutumista rytminsiirron jälkeen verrattuna lumelääkkeeseen.»B | ||||
| atenololi | 50–100 mg x 1 | Pienennä | |||
| bisoprololi | 5–10 mg x 1 | ||||
| karvediloli | 25–50 mg x 1 | ||||
| metoprololi | 95–190 mg x 1 | Pienennä | |||
| Amiodaroni | 100–200 mg x 1 | «Amiodaroni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A | Pienennä | ||
| Dronedaroni2) | 400 mg x 2 | «Dronedaroni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A | Vasta-aiheinen | ||
| Sotaloli | 80–160 mg x 2 | «Sotaloli estää kohtauksittaisen ja jatkuvan (persistoivan) eteisvärinän uusiutumisen rytminsiirron jälkeen tehokkaammin kuin lumelääke.»A | Pienennä | Varo käyttöä | |
| Tehottomiksi osoittautuneet tai riittämättömästi tutkitut | |||||
| Diltiatseemi | «Kalsiuminestäjät yksinään eivät estä eteisvärinän uusiutumista.»C | Pienennä | Vältä käyttöä | ||
| Verapamiili | «Kalsiuminestäjät yksinään eivät estä eteisvärinän uusiutumista.»C | Pienennä | Vältä käyttöä | ||
| Digoksiini | Pienennä | ||||
| Proarytmia | Tyypillisiä aiheuttajia | Kliinisiä piirteitä | Hoito ja ehkäisy |
|---|---|---|---|
| Eteisperäinen nopealyöntisyys | |||
| Eteislepatus kammiovasteella 1:1 | Ryhmien IA ja IC lääkkeet | Nopea ja tasainen kammiovaste (150–220/min), usein leveä QRS-heilahdus | Eteis-kammiojohtumisen hidastaminen (beetasalpaaja, kalsiuminestäjä tai digoksiini) Eteislepatuksen katetriablaatio |
| Eteisvärinän kammiovasteen nopeutuminen | Ryhmien IA ja IC lääkkeet | Kammiovaste nopeutuu, ja joskus eteisvärinä muuttuu eteislepatukseksi | Eteis-kammiojohtumisen hidastaminen |
| Kammioperäinen nopealyöntisyys | |||
| Yhdenmuotoinen kammiotakykardia | Ryhmän IC lääkkeet | Laukaisevana tekijänä yleensä iskemia tai sydämen vajaatoiminta.
Takykardia voi olla lähes jatkuva (vallitseva) ja suhteellisen hidas |
Vältä käyttöä, jos potilaalla on rakenteellinen sydänvika.
Katetriablaatio |
| Kääntyvien kärkien kammiotakykardia | Ryhmien IA ja III lääkkeet | Monimuotoinen kammiotakykardia, jossa QRS-heilahduksen polariteetti vaihtelee sukkulamaisesti, "lyhyt-pitkä-lyhyt"-alkusekvenssi, QT-ajan ja QT-dispersion kasvu | Elektrolyyttihäiriöiden korjaus, magnesium, isoprenaliini, ylitahdistus ja sen suojassa beetasalpaaja tai kalsiuminestäjä |
| Muita | |||
| Sinusbradykardia | Beetasalpaajat, sotaloli, kalsiuminestäjät, digoksiini, amiodaroni ja dronedaroni | Etenkin sinusrytmin palautuessa | Lääkityksen lopettaminen, tarvittaessa tahdistus |
| Eteis-kammiokatkos | Beetasalpaajat, sotaloli, kalsiuminestäjät, digoksiini, amiodaroni ja dronedaroni, flekainidi | Eteisvärinän aikana hidas ja tasainen kammiovaste | Lääkityksen lopettaminen, tarvittaessa tahdistus |
| Lääke | Yleisiä haittavaikutuksia | Harvinaisia haittavaikutuksia |
|---|---|---|
| Flekainidi | huimaus, näköhäiriöt | pahoinvointi, oksentelu |
| (Propafenoni) | ummetus, pahoinvointi, suun puutuminen ja kuivuminen, karvas maku, hypotensio | ihottuma, leukopenia, maksavaurio, anoreksia, ekstrapyramidaalioireet, näköhäiriöt, unihäiriöt |
| Beetasalpaajat | fyysisen suorituskyvyn heikentyminen, väsymys, raajojen kylmyys, klaudikaation paheneminen, unihäiriöt | bronkusspasmi, hypoglykemia, depressio, lihaskouristukset, impotenssi |
| Amiodaroni | kilpirauhasen toimintahäiriöt, maksa-arvojen suurentuminen, herkkyys valolle, huimaus, unihäiriöt, pahoinvointi, oksentelu, sarveiskalvon samentuma | alveoliitti, keuhkofibroosi, maksavaurio, perifeerinen neuropatia, huimaus, unihäiriöt, pahoinvointi, oksentelu |
| Dronedaroni | ruoansulatuselimistön häiriöt (ripuli, oksentelu, pahoinvointi, vatsakipu, dyspepsia), ihottuma, väsymys, heikkous | valoherkkyys, makuhäiriöt |
| Ibutilidi | pahoinvointi | |
| Sotaloli | samat kuin beetasalpaajilla | pahoinvointi, oksentelu, ripuli |
| Vernakalantti | makuhäiriöt, tuntoharhat, huimaus, bradykardia, hypotensio, pahoinvointi, oksentelu, suun kuivuminen, aivastelu, infuusiopaikan kipu | kirvelyn tunne, hajuaistin häiriöt, uneliaisuus, silmien ärsytys, johtumishäiriöt, hengenahdistus, ripuli, raajakipu |
| Diltiatseemi | nilkkaturvotus, ihon punoitus, päänsärky, pahoinvointi, ummetus, huimaus | ihottuma, maksavaurio |
| Verapamiili | ummetus, nilkkaturvotus, päänsärky, huimaus, hypotensio | ihon punoitus, päänsärky, pahoinvointi, oksentelu, huimaus |
| Digoksiini | ruokahaluttomuus, pahoinvointi, oksentelu, ripuli | gynekomastia, trombosytopenia, eosinofilia, näköhäiriöt, väsymys, päänsärky |
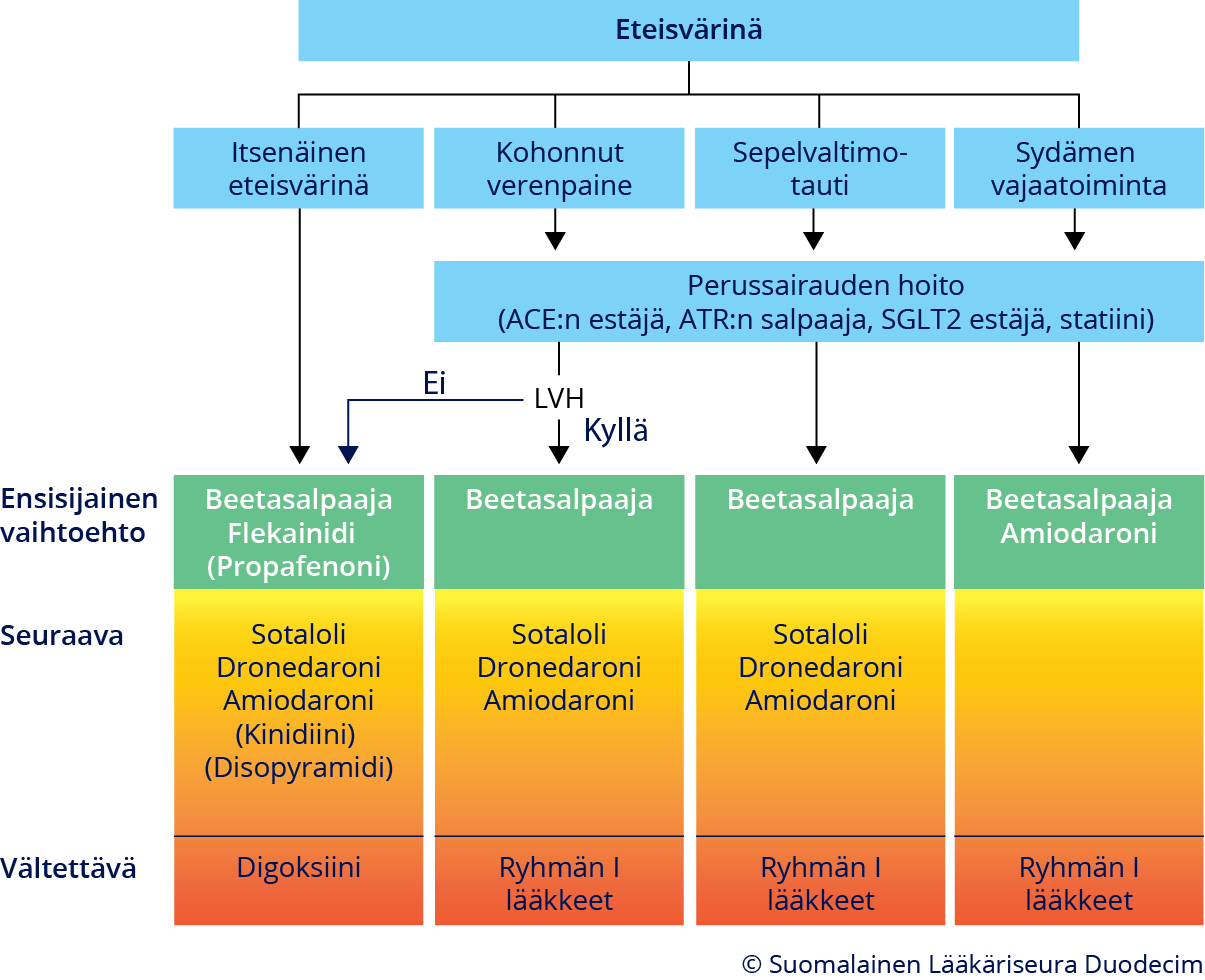
Eteisvärinän estolääkityksen valinta. Estolääkityksen valintaan vaikuttavat oleellisesti potilaan muut (sydän)sairaudet. Avohoidossa ensisijainen lääkevaihtoehto on yleensä beetasalpaaja. Varsinaisista rytmihäiriölääkkeistä itsenäisessä eteisvärinässä ensisijaisia ovat ryhmän IC lääkkeet (flekainidi). Kinidiini ja disopyramidi sopivat etenkin vagaalisen eteisvärinän hoitoon. Rakenteellinen sydänsairaus on vasta-aihe ryhmän I rytmihäiriölääkkeille. Sotalolin käyttöä rajoittaa kääntyvien kärkien kammiotakykardian vaara. Amiodaroni ja dronedaroni aiheuttavat monia sydämen ulkoisia haittoja, mikä rajoittaa niiden käyttöä. ACE:n estäjät ja angiotensiini II -reseptorin (AR-) salpaajat näyttävät estävän eteisvärinän ilmaantumista sydämen vajaatoiminnassa ja verenpainetaudissa ja SGLT2-estäjillä on suotuisa vaikutus etenkin sydämen vajaatoiminnassa. Suluissa olevat lääkkeet ovat nykyään saatavana Suomessa ainoastaan erityisluvalla.
Ryhmän II lääkkeet (beetasalpaajat)
- Beetasalpaajat estävät eteisvärinää tehokkaammin kuin lumelääke «Beetasalpaajat näyttävät vähentävän eteisvärinän uusiutumista rytminsiirron jälkeen verrattuna lumelääkkeeseen.»B.
- Ne ovat erityisen tehokkaita kohonnutta verenpainetta «Van Noord T, Tieleman RG, Bosker HA ym. Beta-block...»133 ja sydämen vajaatoimintaa potevilla «Meng F, Yoshikawa T, Baba A ym. Beta-blockers are ...»134.
- Ne ovat turvallisia myös sydäninfarktin jälkeen «Kühlkamp V, Bosch R, Mewis C ym. Use of beta-block...»135.
- Ne vahvistavat muiden rytmihäiriölääkkeiden vaikutusta ja vähentävät niiden aiheuttamaa proarytmiaa «Grönefeld GC, Hohnloser SH. Beta-blocker therapy i...»86.
- Ne saattavat muuttaa oireisen eteisvärinän oireettomaksi hidastamalla kammiovastetta «Page RL, Reiffel JA, Tavel ME. Asymptomatic atrial...»136, «Page RL. beta-blockers for atrial fibrillation: mu...»137.
- Varsinaisista rytmihäiriölääkkeistä poikkeavasti hoito voidaan aloittaa perusterveydenhuollossa.
Ryhmän IC rytmihäiriölääkkeet
- Flekainidi estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke «Flekainidi estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A tai ryhmän IA lääkkeet «Lévy S, Breithardt G, Campbell RW ym. Atrial fibri...»129, «Naccarelli GV, Dorian P, Hohnloser SH ym. Prospect...»138, «Lee SH, Chen SA, Chiang CE ym. Comparisons of oral...»139, «Grey E, Silverman DI. Efficacy of type 1C antiarrh...»140.
- Flekainidi on turvallinen itsenäisen eteisvärinän hoidossa mutta vasta-aiheinen sydäninfarktin
sairastaneilla, oireisessa sepelvaltimotaudissa, sydämen vajaatoiminnassa ja muissa vaikeissa rakenteellisissa sydänsairauksissa.
- Sydäninfarktin sairastaneilla flekainidi suurentaa kuolleisuuden noin 2,5-kertaiseksi lumelääkkeeseen verrattuna «Echt DS, Liebson PR, Mitchell LB ym. Mortality and...»141.
- Tervesydämisillä flekainidi ei vaikuta kuolleisuuteen ja sen vakavat haittavaikutukset ovat harvinaisia «Hughes MM, Trohman RG, Simmons TW ym. Flecainide t...»142, «Chimienti M, Cullen MT Jr, Casadei G. Safety of lo...»143, «Anderson JL, Platt ML, Guarnieri T ym. Flecainide ...»144, «Wehling M. Meta-analysis of flecainide safety in p...»145.
- Verenpainetautia sairastavilla flekainidia voidaan käyttää, jos kammioseinämät eivät ole hypertrofiset (yli 14 mm) «Joglar JA, Chung MK, Armbruster AL, ym. 2023 ACC/A...»146.
- Flekainidia voidaan harkitusti käyttää myös WPW-oireyhtymään liittyvän eteisvärinän hoidossa «Crozier I. Flecainide in the Wolff-Parkinson-White...»103.
- Ennen ryhmän IC lääkityksen aloittamista
- sydämen rakenteet ja toiminta on tarkistettava kaikututkimuksella
- kliininen rasituskoe (tai sepelvaltimoiden kuvantaminen) voidaan tehdä, ellei sydänlihasiskemiaa voida sulkea pois riittävän varmasti (kuva «Ryhmän IC rytmihäiriölääkityksen aloittaminen ja potilaan seuranta»15).
- Proarytmisten vaikutusten (taulukko «Eteisvärinän hoidossa käytettyjen rytmihäiriölääkkeiden aiheuttamia proarytmisia vaikutuksia ja niiden hoito ja ehkäisy...»11) vähentämiseksi flekainidiin on suositeltavaa yhdistää beetasalpaaja tai jokin muu eteis-kammiojohtumista hidastava lääke «Raatikainen MJP, Sigurd B. Atrial fibrillation - t...»104.
- Propafenoni «Propafenoni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A on nykyään saatavana vain erityisluvalla.

Ryhmän IC rytmihäiriölääkityksen aloittaminen ja potilaan seuranta. Ennen ryhmän IC lääkityksen aloittamista on varmistettava sydämen kaikututkimuksella, että sydän on rakenteellisesti terve. Kliininen rasituskoe tehdään aina, jos sepelvaltimotautia ei muutoin voida sulkea varmasti pois. Erityistapauksissa voidaan käyttää lääkityksen vakiinnuttua tehtävää rasituskoetta proarytmialle alttiiden potilaiden ja hitaiden metaboloijien löytämiseksi. VES = kammiolisälyönti.
Ryhmän III lääkkeet (kaliumkanavan salpaajat)
- Amiodaroni estää eteisvärinän uusiutumista merkitsevästi paremmin kuin lumelääke «Amiodaroni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A.
- Satunnaistetuissa kaksoissokkotutkimuksissa amiodaroni on osoittautunut tehokkaammaksi kuin dronedaroni «Le Heuzey JY, De Ferrari GM, Radzik D ym. A short-...»147, sotaloli, propafenoni «Roy D, Talajic M, Dorian P ym. Amiodarone to preve...»148 ja kinidiini «Vitolo E, Tronci M, Larovere MT ym. Amiodarone ver...»149.
- Meta-analyysin perusteella amiodaroni näyttää olevan myös flekainidia tehokkaampi eteisvärinän estohoidossa «Zarembski DG, Nolan PE Jr, Slack MK ym. Treatment ...»150.
- Amiodaronin käyttö edellyttää monia varotoimia ja huolellista seurantaa «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Raatikainen MJ. Rytmihäiriölääkkeiden kliininen kä...»132, «Singh BN. Amiodarone: the expanding antiarrhythmic...»151, «Siddoway LA. Amiodarone: guidelines for use and mo...»152.
- Pitkäaikaiskäyttöä vaikeuttavat monet sydämenulkoiset haittavaikutukset ja yhteisvaikutukset muiden lääkkeiden (esim. varfariinin ja suorien antikoagulanttien) kanssa, minkä takia amiodaronia ei voida pitää ensivaiheen lääkkeenä eteisvärinän hoidossa «European Heart Rhythm Association., European Assoc...»115, «Connolly SJ. Evidence-based analysis of amiodarone...»153.
- Toisaalta se aiheuttaa vain harvoin proarytmiaa «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Hohnloser SH, Klingenheben T, Singh BN. Amiodarone...»154, ja sitä voidaan käyttää myös sydäninfarktin sairastaneilla ja sydämen vajaatoimintaa potevilla «Julian DG, Camm AJ, Frangin G ym. Randomised trial...»155, «Cairns JA, Connolly SJ, Roberts R ym. Randomised t...»156, «Doval HC, Nul DR, Grancelli HO ym. Randomised tria...»157, «Deedwania PC, Singh BN, Ellenbogen K ym. Spontaneo...»158.
- Eteisvärinän estohoidossa latausannoksen (esim. 600 mg/vrk 2 viikon ajan) jälkeen on pyrittävä käyttämään mahdollisimman pientä annosta (100–200 mg/vrk), jotta vältyttäisiin vakavilta haittavaikutuksilta.
- Dronedaroni (400 mg x 2/vrk) estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke «Dronedaroni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A.
- Dronedaronilla on kaikkien Vaughan–Williamsin luokkien mukaista vaikutusta kuten amiodaronillakin.
- Dronedaronin teho on heikompi kuin amiodaronin «Le Heuzey JY, De Ferrari GM, Radzik D ym. A short-...»147, «Piccini JP, Hasselblad V, Peterson ED ym. Comparat...»159 ja mahdollisesti myös muiden rytmihäiriölääkkeiden «Lafuente-Lafuente C, Mouly S, Longas-Tejero MA ym....»160, «Freemantle N, Lafuente-Lafuente C, Mitchell S ym. ...»161.
- Rytmihäiriön uusiutumista estävän vaikutuksen lisäksi dronedaroni ilmeisesti vähentää
valikoitujen eteisvärinäpotilaiden sairaalahoidon tarvetta ja kuolleisuutta «Dronedaroni saattaa parantaa valikoitujen eteisvärinäpotilaiden ennustetta ja vähentää sairaalahoidon tarvetta.»B.
- Ennustevaikutus on selvin sepelvaltimotautia sairastavilla.
- Dronedaroni on vasta-aiheinen
- sydämen vajaatoiminnassa (lisää kuolleisuutta) «Køber L, Torp-Pedersen C, McMurray JJ ym. Increase...»162
- pysyvässä eteisvärinässä (lisää kuolleisuutta) «Connolly SJ, Camm AJ, Halperin JL ym. Dronedarone ...»163
- potilailla, joilla on todettu maksan tai keuhkojen toksisuus amiodaronihoidon aikana
- dabigatraanihoidon aikana.
- Dronedaronilääkitys edellyttää huolellista potilasvalintaa ja säännöllistä seurantaa
(ks. kuva «Dronedaronin käyttö eteisvärinän estohoidossa»16).
- Ennen lääkityksen aloittamista on harkittava muita hoitovaihtoehtoja.
- Lääkitys on aloitettava erikoislääkärin toimesta, ja sitä on seurattava erikoislääkärin ohjeiden mukaisesti.
- Hoidon aikana sydämen rytmiä (EKG 6 kuukauden välein) ja pumppauskykyä sekä maksan toimintaa on seurattava säännöllisesti.
- Lääkitys pitää lopettaa, jos eteisvärinä kroonistuu tai ilmenee muita vasta-aiheita.
- Sotaloli estää eteisvärinän uusiutumista rytminsiirron jälkeen tehokkaammin kuin lumelääke
«Sotaloli estää kohtauksittaisen ja jatkuvan (persistoivan) eteisvärinän uusiutumisen rytminsiirron jälkeen tehokkaammin kuin lumelääke.»A.
- Ryhmän III mukainen vaikutus tulee esille vain silloin, kun käytetään suuria annoksia (yli 160 mg/vrk). Pienempinä annoksina lääke toimii tavallisen beetasalpaajan tavoin.
- Vertailevissa tutkimuksissa sotaloli on ollut eteisvärinän estossa yhtä tehokas kuin kinidiini «Juul-Möller S, Edvardsson N, Rehnqvist-Ahlberg N. ...»164, propafenoni «Bellandi F, Simonetti I, Leoncini M ym. Long-term ...»165 ja bisoprololi «Plewan A, Lehmann G, Ndrepepa G ym. Maintenance of...»166 mutta huonompi kuin amiodaroni «Roy D, Talajic M, Dorian P ym. Amiodarone to preve...»148.
- Kääntyvien kärkien kammiotakykardian vaaran «Brendorp B, Pedersen O, Torp-Pedersen C ym. A bene...»167 takia sotalolin käytön aloittaminen pitäisi rajoittaa rytmihäiriöiden hoitoon perehtyneille erikoislääkäreille.

Dronedaronin käyttö eteisvärinän estohoidossa. Dronedaronin turvallinen käyttö eteisvärinän estohoidossa edellyttää huolellista potilasvalintaa ja säännöllistä seurantaa. Ennen hoidon aloittamista on sydämen kaikututkimuksen avulla varmistettava, ettei potilaalla ole sydämen vajaatoimintaa. Lisäksi tehdään maksan ja munuaisten toimintakokeet. Jos seerumin alaniiniaminotransferaasin (S-ALAT) pitoisuus on yli kolminkertainen normaalialueen ylärajaan verrattuna, dronedaronia ei pidä aloittaa. Jos ALAT-arvo suurenee seurannan aikana ≥ 3 × normaalin ylärajan, seurantakoe on tehtävä 2–3 vuorokauden kuluessa. Jos arvo on edelleen suurentunut, lääkitys on lopetettava. Dronedaroni ei juuri vaikuta munuaisten toimintaan, mutta seerumin kreatiniinipitoisuus saattaa suurentua, koska lääke kilpailee munuaisissa kreatiniinin erittymisen kanssa. Kreatiniinipitoisuus mitataan ennen hoidon aloittamista ja viikon kuluttua sen jälkeen. Jos arvo on suurentunut, mittaus toistetaan 2 viikon kohdalla. Kliininen arvio on tehtävä enintään 6 kuukauden välein ja samalla on otettava myös EKG. Maksa-arvoja (ALAT) seurataan aluksi tiheään määrittämällä ALAT hoidon aloituksen jälkeen 1 viikon sekä 1, 2, 3, 4, 5, 6, 9 ja 12 kk:n kuluttua. Sen jälkeen kokeet voidaan ottaa harvemmin. Jos seurannan aikana todetaan sydämen vajaatoimintaan tai keuhkojen toimintahäiriöön viittaavia oireita tai löydöksiä, sydämen kaikututkimus tai keuhkojen toimintakokeet on tehtävä viivyttelemättä ja tarvittaessa lääkitys on lopetettava. Dronedaroni on vasta-aiheinen pysyvässä eteisvärinässä, ja sen käyttö on lopetettava, jos eteisvärinä kroonistuu hoidon aikana. Käytännössä myös INR-arvojen sekä digoksiinin pitoisuuden seurantaa on tehostettava dronedaronin aloituksen jälkeen.
© Suomalainen Lääkäriseura Duodecim
Ryhmän IA rytmihäiriölääkkeet
- Vain erityisluvalla saatavina olevia kinidiiniä «Kinidiini vähentää eteisvärinän ilmaantumista merkittävästi enemmän kuin lumelääke tai lääkkeetön hoito ja yhtä tehokkaasti kuin IC-luokan lääkkeet ja sotaloli, mutta huonommin kuin amiodaroni.»A ja disopyramidia «Disopyramidi estää paremmin toistuvia eteisvärinäkohtauksia kuin lumelääke ja yhtä hyvin kuin IC-luokan lääkkeet, mutta sen teho on huonompi kuin amiodaronin.»A käytetään nykyään harvoin eteisvärinän estohoidossa «Coplen SE, Antman EM, Berlin JA ym. Efficacy and s...»168.
- Ne tehoavat parhaiten vagaaliseen eteisvärinään.
- Tyypillisiä haittavaikutuksia ovat kinidiinin aiheuttama ripuli ja disopyramidin voimakkaaseen antikolinergiseen vaikutukseen liittyvät suun kuivuminen, virtsaumpi ja ummetus.
- Ryhmän IB rytmihäiriölääkkeillä (meksiletiini ja lidokaiini) ei ole käyttöä eteisvärinän estohoidossa.
Ryhmän IV lääkkeet (kalsiuminestäjät)
- Verapamiili ja diltiatseemi eivät estä eteisvärinän uusiutumista «Kalsiuminestäjät yksinään eivät estä eteisvärinän uusiutumista.»C, mutta ne saattavat tehostaa muiden rytmihäiriölääkkeiden vaikutusta ja vähentää proarytmian vaaraa «Patten M, Maas R, Bauer P ym. Suppression of parox...»169, «Fetsch T, Bauer P, Engberding R ym. Prevention of ...»170.
Digoksiini
- Digoksiini ei estä eteisvärinän uusiutumista vaan saattaa jopa lisätä ja pidentää vagaalisia eteisvärinäkohtauksia «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Eteisvärinän uusiutuessa digoksiini voi kuitenkin estää nopean kammiovasteen, mikä puoltaa sen käyttöä sellaisilla sydämen vajaatoimintaa potevilla, jotka sietävät huonosti muita sykettä hidastavia lääkkeitä «European Heart Rhythm Association., European Assoc...»115.
Tahdistinhoito eteisvärinän estossa
- Tahdistinhoidon ei ole voitu osoittaa ehkäisevän eteisvärinän uusiutumista «Tahdistinhoidon ei ole voitu osoittaa toimivan itsenäisesti eteisvärinän ehkäisyssä.»B.
- Kun tahdistimen asennus on muiden syiden takia aiheellinen, tahdistintyypin valinnalla
voidaan vaikuttaa eteisvärinän ilmaantumiseen.
- Sinussolmukkeen toimintahäiriössä kannattaa suosia eteistahdistusta ja välttää kammiotahdistusta «Jos potilaalla on todettu perinteinen tahdistinhoidon indikaatio, eteistahdistus näyttää vähentävän eteisvärinän ilmaantuvuutta verrattaessa kammiotahdistukseen.»B, «Andersen HR, Nielsen JC, Thomsen PE ym. Long-term ...»180, «Kerr CR, Connolly SJ, Abdollah H ym. Canadian Tria...»181, «Nielsen JC, Kristensen L, Andersen HR ym. A random...»182.
- Vajaatoimintatahdistinhoito «Vajaatoimintatahdistinhoito saattaa palauttaa sinusrytmin joillakin eteisvärinästä kärsivillä potilailla.»D ja johtoratatahdistus «Wijesuriya N, Mehta V, De Vere F, ym. The role of ...»183 voivat parantaa vasemman kammion toimintaa ja vähentää mitraalivuotoa, millä saattaa olla suotuisa vaikutus eteisvärinään.
- Sinusbradykardiaan taipuvaisilla potilailla tahdistinhoito helpottaa rytmihäiriölääkityksen toteuttamista ja voi siten estää eteisvärinää.
- Sydämensisäiset eteisdefibrillaattorit ovat jääneet pois käytöstä «Burns JL, Sears SF, Sotile R ym. Do patients accep...»184, «Boodhoo LE, Mitchell AR, Sulke N. The clinical and...»185.
Katetriablaatio eteisvärinän estossa
- Katetriablaation tavoitteena on vähentää potilaan oireita ja parantaa elämänlaatua.
- Yleisesti ottaen katetriablaatio ei paranna eteisvärinäpotilaiden ennustetta «Packer DL, Mark DB, Robb RA ym. Effect of Catheter...»186.
- Vaikeassa sydämen systolisessa vajaatoiminnassa se saattaa kuitenkin parantaa valikoitujen potilaiden ennustetta «Packer DL, Mark DB, Robb RA ym. Effect of Catheter...»186, «Sohns C, Fox H, Marrouche NF, ym. Catheter Ablatio...»187, ks. Käypä hoito -suositus Sydämen vajaatoiminta «Sydämen vajaatoiminta»6, «Sydämen vajaatoiminta. Käypä hoito -suositus. Suom...»79.
- Eteisvärinän katetriablaatiohoidossa keuhkolaskimoiden tyvialueella sijaitsevat rytmihäiriöpesäkkeet eristetään muusta eteiskudoksesta (keuhkolaskimoiden isolaatio) joko pareittain tekemällä yhtenäinen ablaatiolinja radiotaajuusenergialla «Eteisvärinän katetriablaatiohoito»17tai yksitellen ns. kryopallolla tai pulssikenttäablaatiolla «Eteisvärinän ablaatiohoito kryopallolla»18, «Eteisvärinän pulssikenttäablaatio (pulsed field ablation, PFA)»19.
- Katetriablaation pääaiheena on voimakasoireinen, lääkehoitoon reagoimaton kohtauksittainen
tai jatkuva eteisvärinä.
- Ensivaiheen hoitona ablaatiota voidaan harkita itsenäistä kohtauksittaista eteisvärinää sairastavalle, jos hän niin haluaa «Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHR...»1, «Cosedis Nielsen J, Johannessen A, Raatikainen P ym...»188.
- Parhaiten ablaatiohoitoon sopivat potilaat, joilla
- on kohtauksittainen eteisvärinä
- ei ole todettu merkittävää sydänsairautta
- vasen eteinen ei ole huomattavasti laajentunut (poikkimitta alle 5 cm)
- todetaan runsaasti T-aallon päälle ajoittuvia eteislisälyöntejä ("P-on-T"-ilmiö) (kuva «Pesäkealkuiselle eteisvärinälle ominaisia T-aallon päälle osuvia (P-on-T) lisälyöntejä»20).
- Eteisvärinän katetriablaatiohoito estää kohtauksittaisen ja jatkuvan eteisvärinän
uusiutumista tehokkaammin kuin lääkehoito «Katetriablaatiohoito estää eteisvärinän uusiutumista tehokkaammin kuin lääkehoito.»A ja parantaa merkitsevästi potilaiden elämänlaatua «Hakalahti A, Biancari F, Nielsen JC ym. Radiofrequ...»189, «Mark DB, Anstrom KJ, Sheng S ym. Effect of Cathete...»190, «Blomström-Lundqvist C, Gizurarson S, Schwieler J y...»191. Nykyisin näyttöä on 5 vuoden seurannasta «Nielsen JC, Johannessen A, Raatikainen P ym. Long-...»192, «Raatikainen MJ, Hakalahti A, Uusimaa P ym. Radiofr...»193.
- Katetriablaatiohoito tehoaa 60–85 %:lla itsenäistä kohtauksittaista eteisvärinää sairastavista potilaista, joilla lääkehoito on osoittautunut tehottomaksi «Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHR...»1, «European Heart Rhythm Association., European Assoc...»115, «Cappato R, Calkins H, Chen SA ym. Updated worldwid...»194, «Piccini JP, Lopes RD, Kong MH ym. Pulmonary vein i...»195, «Gjesdal K, Vist GE, Bugge E ym. Curative ablation ...»196, «Calkins H, Reynolds MR, Spector P ym. Treatment of...»197, «Blomström-Lundqvist C, Gizurarson S, Schwieler J y...»191.
- Kohtauksittaisessa eteisvärinässä radiotaajuusenergialla tehtävän ablaation, kryohoidon ja pulssikenttäablaation tehossa ei ole merkittävää eroa «Schmidt M, Dorwarth U, Andresen D ym. Cryoballoon ...»198, «Reddy VY, Gerstenfeld EP, Natale A, ym. Pulsed Fie...»199.
- Rakenteellisessa sydänviassa, pitkään jatkuneessa eteisvärinässä ja selvästi ylipainoisilla katetriablaation tulokset ovat edellä esitettyä huonompia. Ylipainoisille suositellaan laihduttamista ennen toimenpidettä «Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHR...»1, «European Heart Rhythm Association., European Assoc...»115.
- Ablaatiohoidon kustannukset ovat alussa suuremmat, mutta ilmeisesti jo 3–5 vuoden kuluttua sen kokonaiskustannukset ovat pienemmät kuin lääkehoidon «Weerasooriya R, Jaïs P, Le Heuzey JY ym. Cost anal...»200, «Andrikopoulos G, Tzeis S, Maniadakis N ym. Cost-ef...»201. Etu on suurin nuorilla potilailla «Aronsson M, Walfridsson H, Janzon M ym. The cost-e...»202.
- Eteisvärinän ablaatiohoito on monimutkainen elektrofysiologinen toimenpide, johon
liittyy harvinaisten mutta vakavien komplikaatioiden vaara «European Heart Rhythm Association., European Assoc...»115, «Cappato R, Calkins H, Chen SA ym. Updated worldwid...»194, «Spragg DD, Dalal D, Cheema A ym. Complications of ...»203.
- Haittavaikutuksia on vähemmän, mutta ne ovat vakavampia kuin lääkehoitoon liittyvät ongelmat «Calkins H, Reynolds MR, Spector P ym. Treatment of...»197.
- Vakavia haittavaikutuksia ovat muun muassa tamponaatio (1–2 %), keuhkolaskimon ahtautuminen (alle 1 %), tromboemboliset komplikaatiot (alle 1 %), palleahermon halvaantuminen (1–2%) ja ruokatorven puhkeaminen (alle 0,1 %).
- Ablaatiohoidon haittavaikutukset ilmenevät yleensä nopeasti toimenpiteen jälkeen, mutta lääkehoidon haitat saattavat tulla esille vuosienkin jälkeen.
- Antikoagulaatio eteisvärinän ablaatiohoidon yhteydessä:
- Katetriablaatio ei ole vaihtoehto antikoagulaatiohoidolle, vaan antikoagulaatiossa noudatetaan samoja periaatteita kuin muissakin potilasryhmissä.
- Toimenpiteeseen liittyvien tromboembolisten komplikaatioiden välttämiseksi myös pienen riskin potilaille suositellaan aloitettavaksi suora antikoagulantti viimeistään 3 viikkoa ennen toimenpidettä (varfariinia käyttäessä INR:n on oltava hoitotasolla vähintään 3 viikkoa).
- Toimenpiteen jälkeen antikoagulaatiohoitoa jatketaan pienen riskin potilailla 2–3 kuukautta ja suuressa tukosvaarassa oleville (CHA2DS2VA ≥ 2) suositellaan pysyvää antikoagulaatiohoitoa.
- Tarkempia ohjeita antikoagulaatiohoidon toteutuksesta annetaan toimenpiteitä tekevistä sairaaloista.
- Jos eteisvärinän laukaisijana toimii jokin muu rytmihäiriö (esim. eteis-kammiosolmukkeen
kiertoaktivaatiotakykardia, eteis-kammiokiertoaktivaatiotakykardia, eteistakykardia
tai eteislepatus), sen katetriablaatiohoito saattaa estää myös eteisvärinän «European Heart Rhythm Association., European Assoc...»115, «Blomström-Lundqvist C, Scheinman MM, Aliot EM ym. ...»204.
- Eteislepatuksen katetriablaatiohoito vähentää eteisvärinää muttei poista sitä kokonaan «Nabar A, Rodriguez LM, Timmermans C ym. Effect of ...»205, «Ahvenvaara T, Uusimaa P, Huikuri HV, Raatikainen M...»206.
- WPW-oireyhtymään liittyvä nopea eteisvärinä on hengenvaarallinen. Sitä poteville pitäisi ehdottomasti tehdä oikoradan katetriablaatio «European Heart Rhythm Association., European Assoc...»115, «Blomström-Lundqvist C, Scheinman MM, Aliot EM ym. ...»204.

Eteisvärinän katetriablaatiohoito. Kuvassa A nähdään elektroanatomista kartoituslaitteistoa (CartoTM) käyttämällä tehty kolmiulotteinen malli vasemmasta eteisestä ja keuhkolaskimoista takaapäin katsottuna. Keuhkolaskimot on merkitty välillisillä putkilla ja katetriablaatiokohteet punaisilla pallukoilla. Kuvassa B nähdään, kuinka sähköinen aktiviteetti häviää oikean puoleisesta yläkeuhkolaskimoista ablaation vaikutuksesta. Tämä on merkki siitä, että keuhkolaskimo on eristetty eikä sen sisällä sijaitseva rytmihäiriöpesäke pysty enää käynnistämään eteisvärinää. Myös muut laskimot tarkastettiin toimenpiteen aikana eikä niissä yhdessäkään havaittu sähköistä aktiviteettia, joka olisi pystynyt käynnistämään eteisvärinän.
kuva A © Pekka Raatikainen
kuva B © Suomalainen Lääkäriseura Duodecim

Eteisvärinän ablaatiohoito kryopallolla. Tässä menetelmässä kaikki keuhkolaskimot käsitellään erikseen ja tulos varmistetaan pallokatetrin lävitse keuhkolaskimon sisälle viedyllä sirkulaarisella diagnostisella katetrilla samaan tapaan kuin radiotaajuusenergialla tehdyssä ablaatiossa. Kuvassa näkyy kryopallo täytettynä vasemmassa yläkeuhkolaskimossa. Pallo tukkii suonen hyvin, sillä sen läpi ruiskutettu varjoaine ei vapaudu lainkaan eteisen puolella. Hyvä “okkluusio” on onnistuneen kryoablaation edellytys.
© Pekka Raatikainen
Eteisvärinän pulssikenttäablaatio (pulsed field ablation, PFA)
Kuvassa nähdään PFA-katetri vasemmassa yläkeuhkolaskimossa ensin ns. korimuodossa (AP-suunta) hieman laskimon sisäpuolelle ulottuen ja toisessa kuvassa sama katetri hieman laskimon suuaukon ulkopuolella ns. kukkamuodossa (LAO 60 -suunta). Tällä katetrilla keuhkolaskimot eristetään yksitellen tekemällä jokaiseen laskimoon vähintään kahdeksan lyhytkestoista (4 s) hoitoa. Menetelmän etuna on nopeuden lisäksi myös turvallisuus, sillä PFA-energia kohdistuu enimmäkseen sydänlihakseen ja vaara muiden rakenteiden, kuten palleahermon tai ruokatorven, vaurioitumisesta on pienempi kuin radiotaajuusenergialla tai jäädyttämällä tehtävässä ablaatiossa.
© Pekka Raatikainen

Pesäkealkuiselle eteisvärinälle ominaisia T-aallon päälle osuvia (P-on-T) lisälyöntejä. Nämä ovat yleensä lähtöisin keuhkolaskimoista ja laukaisevat usein kohtauksittaisen eteisvärinän.
Kirurginen hoito eteisvärinän estossa
- Sydänkirurgian yhteydessä tehtävä eteisvärinän poistoon tähtäävä lisätoimenpide estää
tehokkaasti eteisvärinän uusiutumista «Sydänkirurgian yhteydessä tehtävä erillinen eteisvärinän poistoon suuntautuva lisätoimenpide estää eteisvärinän uusiutumista.»A.
- Viime vuosina eteisvärinän kirurgisessa hoidossa on käytetty sokkeloleikkauksen (kuva «Perinteinen Coxin sokkeloleikkaus (MAZE-leikkaus)»21), «Prasad SM, Maniar HS, Camillo CJ ym. The Cox maze ...»207 sijasta lähes yksinomaan radiotaajuus- tai kryotekniikoita, joiden ansiosta toimenpide on tullut nopeammaksi ja turvallisemmaksi «Cox JL. Cardiac surgery for arrhythmias. J Cardiov...»208, (kuva «Eteisvärinän kirurginen epikardiaalinen ablaatiohoito»22).
- Kirurgista hoitoa voidaan harkita, jos eteisvärinäpotilas joutuu sydänleikkaukseen
muusta syystä, ja valikoiduilla potilailla muiden hoitojen osoittauduttua tuloksettomiksi
tai vasta-aiheisiksi.
- Rakenteellinen sydänvika ei ole este eteisvärinän kirurgiselle hoidolle – päinvastoin mitraaliläppäviassa eteisvärinän ilmaantuminen saattaa kiirehtiä leikkauspäätöstä.
- Vakavat komplikaatiot ovat harvinaisia, mutta yksittäistapauksissa kirurgisen ablaation on kuvattu aiheuttaneen ruokatorven puhkeamia «McLellan CS, Abdollah H, Brennan FJ ym. Atrial fib...»209 ja sepelvaltimoahtaumia.
- Kokemukset mini-invasiivisista ja tähystyksen avulla tehtävistä toimenpiteistä sekä ns. hybriditoimenpiteistä ovat lupaavia. Niitä voidaan harkita ainoana toimenpiteenä, jos katetriablaatiohoito eivät ole tuottanut tulosta ja oireet ovat edelleen vaikeita tai on syytä pidättäytyä transseptaalisesta katetrihoidosta esimerkiksi eteisväliseinän sulkulaitteen takia «Boersma LV, Castella M, van Boven W ym. Atrial fib...»210, «Castellá M, Pereda D, Mestres CA ym. Thoracoscopic...»212.

Perinteisessä Coxin sokkeloleikkausessa (MAZE-leikkaus) kirurgi leikkasi eteisen pienempiin osiin ja ompeli sen sitten uudelleen kasaan. Tällä menetelmällä sinusrytmi on saatu palautettua jopa 90 %:lla potilaista. Menetelmä on kuitenkin työläs ja aikaavievä ja siitä on suurelta osin luovuttu ja siirrytty käyttämään kirurgista ablaatiohoitoa.

Eteisvärinän kirurginen epikardiaalinen ablaatiohoito. Menetelmä on tavanomaista MAZE-leikkausta helpommin toteutettavissa, sillä leesiot tehdään radiotaajuusenergialla, jäädytyksellä tai mikroaaltoanturilla. Toimenpide voidaan tehdä myös tähystysleikkauksena, joka soveltunee paremmin pelkän eteisvärinän hoitoon.
Kammiovasteen hidastaminen pysyvässä eteisvärinässä (sykkeenhallinta)
- Jos päädytään pysyvään eteisvärinään ja sykkeenhallintaan, potilaalle on hyvä kertoa
hoitomyöntyvyyden parantamiseksi, että
- ennuste on lieväoireisilla potilailla (EHRA 1–2) sykkeenhallinnan aikana yhtä hyvä kuin lääkkeellisen rytminhallinnan aikana «Sykkeenhallinta on eteisvärinässä parempi vaihtoehto kuin rytminhallinta aivohalvauksien ja kokonaiskuolleisuuden suhteen, mutta hoidot ovat samanarvoisia kuolleisuuden ja potilaiden elämänlaadun suhteen.»A
- elimistö yleensä tottuu pysyvään eteisvärinään syketaajuuden optimoinnin myötä ("taloudellinen flimmeri") «Levy T, Walker S, Mason M ym. Importance of rate c...»213, «Van Gelder IC, Van Veldhuisen DJ, Crijns HJ ym. RA...»214.
- Pysyvän eteisvärinän aikana kammiotaajuus säädetään yksilöllisesti (kuva «Sykkeenhallinta pysyvässä eteisvärinässä»23).
- Tavoitteena on, että potilas on oireeton ja kammiovaste on levossa alle 110/min.
- Oireiset potilaat hyötyvät tiukemmasta sykkeenhallinnasta, jossa tavoitteellinen kammiovaste on levossa 60–80/min ja kevyessä rasituksessa, kuten kävellessä, 90–115/min.
- Systolisessa vajaatoiminnassa kannattaa varoa kammiovasteen liiallista hidastamista.
- Sykkeenhallinnan toteutuminen täytyy tarvittaessa varmistaa EKG:n pitkäaikaisrekisteröinnillä,
kliinisellä rasituskokeella tai molemmilla.
- Jatkuvasti liian nopea kammiovaste (keskimääräinen syketaajuus yli 110/min) voi johtaa sydämen vajaatoimintaan (ns. takykardiamyopatia) «Shinbane JS, Wood MA, Jensen DN ym. Tachycardia-in...»53.

Sykkeenhallinta pysyvässä eteisvärinässä. Kammiovasteen hidastamiseen käytettävä lääkitys valitaan ja annos säädetään yksilöllisesti niin, että potilas on oireeton. Minimitavoite oireettomilla potilailla on, että kammiovaste on levossa alle 110/min. Tiukempia sykerajoja käytetään oireisilla potilailla. Tällöin tavoitteena on, että syke on levossa 60–80/min ja kevyessä rasituksessa, kuten kävellessä, 90–115/min. Jos yksi lääke ei riitä, voidaan käyttää yhdistelmää, ja ellei sekään auta, potilas on ohjattava rytmikardiologin konsultaatioon invasiivisen hoidon arviota varten (tahdistin ja eteiskammiosolmukkeen katetriablaatio).
© Suomalainen Lääkäriseura Duodecim
Lääkehoito
- Kammiovasteen hidastamiseen käytettävä lääkitys (taulukko «Pysyvän eteisvärinän kammiotaajuuden optimoinnissa yleisimmin käytettäviä lääkkeitä...»13) valitaan yksilöllisesti ja annos säädetään edellä esitettyjen tavoitteiden mukaisesti.
- Beetasalpaajat ovat tehokkaita ja turvallisia eteisvärinän sykkeenhallinnassa «Beetasalpaajat ovat turvallisia ja tehokkaita pysyvän eteisvärinän kammiovasteen hidastamisessa.»A, «Olshansky B, Rosenfeld LE, Warner AL ym. The Atria...»215.
- Hoidossa kannattaa suosia valmisteita (bisoprololi, karvediloli ja metoprololi), joiden teho ja turvallisuus muissa sydänsairauksissa on dokumentoitu hyvin «Grönefeld GC, Hohnloser SH. Beta-blocker therapy i...»86.
- Beetasalpaajat (pindololi ja asebutololi), joilla on sisäinen sympatomimeettinen vaikutus (ISA), hidastavat leposykettä vähemmän kuin muut beetasalpaajat. Potilaat, joiden kammiovaste on levossa hidas mutta rasituksen aikana liian nopea, sietävät niitä usein paremmin kuin muita beetasalpaajia «Grönefeld GC, Hohnloser SH. Beta-blocker therapy i...»86, «Leclercq JF, Rosengarten MD, Kural S ym. Effects o...»216.
- Kalsiuminestäjät (verapamiili ja diltiatseemi) hidastavat pysyvässä eteisvärinässä tehokkaasti kammiovastetta
«Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Ne sopivat erityisesti paljon liikkuville potilaille, joilla ei ole todettu sydänsairauksia.
- Digoksiini hidastaa kammiovastetta levossa tehokkaammin kuin lumelääke, mutta sen teho heikkenee fyysisen tai psyykkisen rasituksen aikana «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Sethi NJ, Nielsen EE, Safi S ym. Digoxin for atria...»211.
- Se sopii lähinnä vähän liikkuville potilaille ja sydämen vajaatoimintaa sairastaville.
- Digoksiinin vaikutus eteisvärinäpotilaiden ennusteeseen on kiistanalainen «Al-Khateeb M, Qureshi WT, Odeh R ym. The impact of...»217, «Wang ZQ, Zhang R, Chen MT ym. Digoxin Is Associate...»218, «Chao TF, Liu CJ, Tuan TC ym. Rate-control treatmen...»220, «Gheorghiade M, Fonarow GC, van Veldhuisen DJ ym. L...»221.
- Amiodaroni hidastaa eteisvärinän kammiovastetta, mutta sen pitkäaikaista käyttöä pitää välttää
sydämenulkoisten haittavaikutusten takia «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Raatikainen MJ. Rytmihäiriölääkkeiden kliininen kä...»132.
- Yleensä amiodaronin käyttö pitää lopettaa, jos potilas jää pysyvään eteisvärinään, ellei sille ole muuta aihetta kuten kammiotakykardia.
- Sitä voidaan kuitenkin käyttää siltahoitona eteis-kammiosolmukkeen ablaatiota odotettaessa.
- Jos beetasalpaaja tai kalsiuminestäjä ei yksinään riitä hidastamaan kammiovastetta
optimaaliseksi, voidaan käyttää yhdistelmälääkitystä tai asentaa pysyvä tahdistin
ja tehdä eteis-kammiosolmukkeen ablaatio (kuva «Sykkeenhallinta pysyvässä eteisvärinässä»23), «Eteis-kammiojohtumisen katkaisu ja pysyvä tahdistinhoito vähentänee vaikeaoireisen eteisvärinäpotilaan oireisuutta mutta ei kuolleisuutta.»B.
- Käyttökelpoisimpia yhdistelmiä ovat beetasalpaaja ja digoksiini sekä kalsiuminestäjä ja digoksiini.
- Ongelmallisimmissa tapauksissa voidaan käyttää myös beetasalpaajan ja kalsiuminestäjän (ja digoksiinin) yhdistelmää tai amiodaronia.
- Dronedaroni on vasta-aiheinen pysyvässä eteisvärinässä, vaikka se hidastaa tehokkaasti kammiovastetta
«Davy JM, Herold M, Hoglund C ym. Dronedarone for t...»222, «Singh BN, Connolly SJ, Crijns HJ ym. Dronedarone f...»223.
- Se lisää kuolleisuutta, aivohalvauksen ja sydäntapahtumien vaaraa sekä sairaalahoidon tarvetta potilailla, joilla on pysyvä eteisvärinä ja muita vaaratekijöitä «Connolly SJ, Camm AJ, Halperin JL ym. Dronedarone ...»163.
| Lääke | Suositeltava ylläpitoannos/vrk | Näytön aste |
|---|---|---|
| Beetasalpaajat | «Beetasalpaajat ovat turvallisia ja tehokkaita pysyvän eteisvärinän kammiovasteen hidastamisessa.»A | |
| Atenololi | 50–100 mg x 1 | |
| Bisoprololi | 5–10 mg x 1 (enintään 20 mg) | |
| Karvediloli | 25–50 mg x 1 | |
| Metoprololi | 95–190 mg x 1 | |
| Kalsiuminestäjät | «Kalsiuminestäjät eivät ilmeisesti palauta sinusrytmiä akuutissa eteisvärinässä.»B | |
| Diltiatseemi | 180–360 mg (voidaan tarvittaessa jakaa kahteen annokseen) | |
| Verapamiili | 120–480 mg (voidaan tarvittaessa jakaa kahteen annokseen) | |
| Muut | ||
| Amiodaroni | 100–200 mg x 1 | |
| Digoksiini | 0,0625–0,375 mg x 1 |
Eteis-kammiosolmukkeen katetriablaatio
- Eteis-kammiosolmukkeen ablaatio parantaa elämänlaatua ja vähentää sairaalahoidon tarvetta muttei vaikuta kuolleisuuteen «Eteis-kammiojohtumisen katkaisu ja pysyvä tahdistinhoito vähentänee vaikeaoireisen eteisvärinäpotilaan oireisuutta mutta ei kuolleisuutta.»B.
- Toimenpiteessä potilaalle asennetaan ensin pysyvä sydämentahdistin ja yleensä 2–3
viikkoa sen jälkeen aiheutetaan katetriablaatiolla täydellinen eteis-kammiokatkos
«Aliot E ym. Catheter ablation or modulation of the...»224.
- Osalla potilaista sykettä hidastavan lääkityksen annosta voidaan tahdistimen asennuksen jälkeen suurentaa niin, ettei eteis-kammiosolmukkeen katkaisua tarvita.
- Eteis-kammiosolmukkeen ablaatio ei poista eteisvärinää eikä antikoagulaatiohoidon tarvetta.
- Ablaation jälkeen sydäntä on tahdistettava 1–3 kuukauden ajan tavallista nopeammin (noin 70–90/min), jotta vältytään proarytmialta «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Nowinski K, Gadler F, Jensen-Urstad M ym. Transien...»225.
- Toimenpide on aiheellinen, jos
- leposyke on maksimaalisesta lääkityksestä huolimatta yli 110/min eikä rytminhallinta ole mahdollista, vaikka potilas olisi vähäoireinen
- potilas saa nopeasta sykkeestä vaikeita oireita (palpitaatio, pyörtyminen tms.)
- sykettä hidastava lääkitys aiheuttaa vaikeita haittavaikutuksia
- potilaalla on todettu takykardiamyopatia
- kammiovaste on niin nopea, että biventrikulaarisen vajaatoimintatahdistuksen osuus jää alle 90 %:iin ajasta.
- Pysyvässä eteisvärinässä käytetään kammiotahdistusta (VVIR).
- Kohtauksittaisessa ja jatkuvassa eteisvärinässä eteis-kammiosolmukkeen katkaisua kannattaa yleensä välttää, mutta jos siihen päädytään, käytetään fysiologista tahdistusta.
- Biventrikulaarinen vajaatoimintatahdistus «Jos vasemman kammion toiminta on alentunut, olisi suositeltavaa asentaa sydämen vajaatoimintatahdistin (biventrikulaarinen tahdistin) eteis-kammiosolmukkeen katkaisun yhteydessä.»B tai johtoratatahdistus «Vijayaraman P, Chung MK, Dandamudi G ym. His Bundl...»219 on yleensä parempi vaihtoehto kuin tavanomainen oikean kammion tahdistus etenkin, jos vasemman kammion toiminta on heikentynyt.
Antikoagulaatiohoito
- Perussairauksien hyvän hoidon ohella eteisvärinäpotilaan ennusteen kannalta tärkeintä on oikein toteutettu antikoagulaatiohoito.
- Sydänperäisen embolisaation ja aivohalvauksen vaara ja hoitosuositus ovat samat oireettomassa ja oireisessa eteisvärinässä «European Heart Rhythm Association., European Assoc...»115.
- Kohtauksittaisessa eteisvärinässä hoitosuositus on sama kuin jatkuvassa ja pysyvässä eteisvärinässä, vaikka aivohalvauksen vaara on ilmeisesti hieman pienempi «Steinberg BA, Hellkamp AS, Lokhnygina Y ym. Higher...»48, «Vanassche T, Lauw MN, Eikelboom JW ym. Risk of isc...»49.
- Eteislepatuksessa hoitosuositus on sama kuin eteisvärinässä, vaikka tukosvaara on ilmeisesti hiukan pienempi kuin eteisvärinässä «European Heart Rhythm Association., European Assoc...»115, «Wood KA, Eisenberg SJ, Kalman JM ym. Risk of throm...»226.
- Antikoagulaatiohoidon tarve arvioidaan CHA2DS2VA-pisteytyksen (taulukko «Tromboembolisten komplikaatioiden vaaran arviointi CHA2DS2VA-pisteytyksen avulla....»2) avulla aina, kun potilaalla todetaan eteisvärinä «Antitromboottinen hoito eteisvärinässä»4.
- Suuren riskin potilaille (CHA2DS2VA ≥ 2) antikoagulaatiohoito on yleensä aiheellinen, vaikka vuotoriski olisi suurentunut.
- Keskisuuren riskin potilailla (CHA2DS2VA = 1) päätös antikoagulaatiohoidosta tehdään yksilöllisesti niin, että huomioidaan
- riskitekijöiden hoidon tulokset (esim. kohonneen verenpaineen merkitys on vähäinen, jos se on hyvässä hoitotasapainossa)
- pienemmät tukoksen vaaratekijät (esim. tupakointi, dyslipidemia ja munuaisten vajaatoiminta) lisäävät tukosvaaraa
- vuotovaara (antikoagulaatiohoidosta on syytä luopua, jos vuotovaara on suurentunut).
- Pienen riskin potilaille (CHA2DS2VA = 0) ei anneta antikoagulaatiohoitoa, koska sen hyöty on heillä vähäisempi kuin haitat.
- Riskipisteet näyttävät ennustavan aivohalvauksen vaaraa myös sinusrytmissä olevilla, mutta heillä antikoagulaatiohoidon tehosta ei ole näyttöä «Ilmeisesti riski-indeksit CHADS2 ja CHA2DS2-VASc ennustavat aivohalvauksen vaaraa myös sinusrytmissä.»B.
- Antikoagulaatiohoidon aikana vuotovaaraa lisäävät muun muassa
- > 65 vuoden ikä
- aiemmin todettu vakava verenvuoto
- kohonnut verenpaine (systolinen verenpaine > 160 mmHg)
- vaikea munuaisten vajaatoiminta
- vaikea maksan vajaatoiminta
- syöpä ja muut verenvuodolle altistavat sairaudet ja tilat (esim. anemia, trombosytopenia, trombosyyttien toimintahäiriö, diabetes)
- muut veren hyytymistä estävät lääkkeet (esim. ASA, tulehduskipulääkkeet) ja kalaöljyvalmisteet
- runsas alkoholin käyttö
- geneettiset tekijät
- dementia
- tapaturma-altis ammatti tai harrastus
- huono hoitomyönteisyys (INR-arvojen selittämätön vaihtelu tai epäsäännöllinen suoran antikoagulantin käyttö)
- Kliinisessä työssä verenvuotovaara voidaan arvioida HAS-BLED-pisteytyksen avulla (taulukko «Vuotovaaran arviointi HAS-BLED-pisteytyksen avulla. ...»14), «Verenvuodon vaaraa varfariinihoidon aikana lisäävät erityisesti korkea ikä, verenhyytymiseen vaikuttavat lääkkeet, INR > 4 ja lukuisat potilaan lisäsairaudet ja kliiniset ominaisuudet.»A, «Vakavien vuotokomplikaatioiden ennustaminen HAS-BLED-indeksin avulla»3.
- Suuressa tukosvaarassa olevilla antikoagulaatiohoito on lähes aina aiheellinen, vaikka vuotovaara olisi koholla.
- Antikoagulaatiohoidon aiheellisuus on arvioitava erityisen huolellisesti, jos HAS-BLED
> CHA2DS2VA.
- Huomioi myös mahdollinen anemia ja/tai trombosytopenia.
- Kallonsisäisiä vuotoja ilmaantuu suoria antikoagulantteja käytettäessä harvemmin kuin varfariinihoidossa, jossa ne liittyvät etenkin aikaisempaan aivohalvaukseen, korkeaan ikään, ASAn käyttöön sekä muuhun kuin valkoihoiseen väestöön kuulumiseen «Kallonsisäisiä vuotoja ilmeisesti ilmaantuu NOAC-hoitojen aikana harvemmin kuin varfariinihoidossa, jossa ne liittyvät aikaisempaan aivohalvaukseen, muuhun kuin valkoihoiseen väestöön kuulumiseen ja ASAn käyttöön sekä korkeaan ikään.»B.
- Kaikki hoidettavissa olevat verenvuodolle altistavat tekijät pyritään korjaamaan.
- Kohonneen verenpaineen hoidossa tavoite on < 130 / < 80 mmHg.
- Kaatuilun merkitys on arvioitava yksilöllisesti. Yleensä se ei ole este antikoagulaatiohoidolle «Cairns JA. Stroke prevention in atrial fibrillatio...»227.
| Jokainen kohta on yhden pisteen arvoinen. Punaisella merkittyihin vaaratekijöihin ei voida vaikuttaa, mutta muihin tekijöihin liittyvää vaaraa voidaan useimmissa tapauksissa pienentää niiden hyvällä hoidolla. Vuotovaara on suurentunut, jos pisteiden summa on vähintään 3. Huomioi myös mahdollinen anemia ja trombosytopenia. | ||
|---|---|---|
| 1) syöpä, anemia, trombosytopenia, trombosyyttinen toimintahäiriö, aiempi vuoto | ||
| Riskitekijä | Pisteet | |
| Hypertension | Systolinen verenpaine yli 160 mmHg | 1 |
| Abnormal liver or kidney function | Maksan tai munuaisten vaikea toimintahäiriö | 1 molemmista |
| Stroke | Aikaisempi aivohalvaus | 1 |
| Bleeding | Verenvuototaipumus 1) | 1 |
| Labile INR | INR-arvojen vaihtelu | 1 |
| Elderly | Ikä yli 65 vuotta | 1 |
| Drugs or alcohol | Vuotoriskiä lisäävä lääkitys tai alkoholin runsas käyttö | 1 molemmista |
Toimenpiteet ennen antikoagulaatiohoidon aloittamista
- Ennen suoran antikoagulantin tai varfariinin käytön aloittamista on
- varmistettava, ettei potilaalla ole antikoagulaatiohoidon tai spesifisen lääkkeen vasta-aiheita
- tutkittava, onko vuotovaara suurentunut, ja korjattava kaikki ne vuotovaaraa lisäävät
tekijät, joihin voidaan vaikuttaa.
- Jos vakavan verenvuodon vaara on tästä huolimatta suurempi kuin eteisvärinän aiheuttama tukosvaara, antikoagulaatiohoitoa ei pidä aloittaa, mutta eteiskorvakkeen sulku voi tulla kyseeseen
- selvitettävä, onko käytössä tukos- tai vuotavaaraa lisääviä lääkkeitä (yhteisvaikutukset)
- tarkistettava verenpaine sekä munuaisten ja maksan toiminta
- varmistettava hoitomyönteisyys.
- Suositeltavia laboratoriotutkimuksia ovat perusverenkuva (Hb, trombosyytit), Krea (eGFR), ALAT ja P-TT (INR).
Suorat antikoagulantit
- Suorista antikoagulanteista kliinisessä käytössä nykyisin ovat suora trombiininestäjä
dabigatraani ja tekijän Xa estäjät apiksabaani, edoksabaani ja rivaroksabaani (taulukko
«Suorien antikoagulanttien ominaisuuksia ja annosteluohjeita...»15).
- Kooste suorien antikoagulanttien eduista ja haitoista varfariiniin verrattuna esitetään taulukossa «Suorien antikoagulanttien edut ja haitat varfariiniin verrattuna...»16.
- Nykyisin kaikille suorille antikoagulanteille on olemassa spesifinen vasta-aine
- idarusitsumabi kumoaa dabigatraanin vaikutuksen «Pollack CV Jr, Reilly PA, Eikelboom J ym. Idaruciz...»228, «Connolly SJ, Crowther M, Eikelboom JW ym. Full Stu...»229 ja
- andeksaneetti alfa kumoaa tekijän Xa estäjien (rivaroksabaani, apiksabaani ja edoksabaani) vaikutuksen «Connolly SJ, Crowther M, Eikelboom JW ym. Full Stu...»229, «Siegal DM, Curnutte JT, Connolly SJ ym. Andexanet ...»230
- protrombiinikompleksikonsentraatti (PCC) kumoaa tekijän Xa estäjien, mutta ei dabigratraanin vaikutusta
- Suorat antikoagulantit ovat vasta-aiheisia kohtalaisessa tai vaikeassa mitraalistenoosissa ja potilailla, joilla on mekaaninen tekoläppä.
- Jos potilaalla on biologinen tekoläppä, joka ei vaadi varfariinihoitoa, suoria antikoagulantteja voidaan käyttää samoin kuin muillakin eteisvärinäpotilailla «Raatikainen MJP. Oraalinen antikoagulaatiohoito sy...»231.
- Eteisvärinäpotilaan vakaassa sepelvaltimotaudissa pelkkä suora antikoagulantti riittää
estämään sekä eteisvärinään että valtimotautiin liittyviä tapahtumia.
- ASAn tai ADP-reseptorin P2Y12 salpaajien yhteiskäyttö suorien antikoagulanttien kanssa lisää verenvuotovaaraa muttei paranna antitromboottista tehoa vakaassa sepelvaltimotaudissa.
- Sen sijaan sepelvaltimoiden pallolaajennuksen jälkeen suoran antikoagulantin ja antitromboottien väliaikainen yhteiskäyttö on aiheellista.
- Suoria antikoagulantteja käytettäessä rutiinimainen verenhyytymistä mittaavien kokeiden
seuranta ei ole tarpeen mutta verenkuvaa ja munuaisten toimintaa (eGFR) on seurattava
säännöllisesti «Steffel J, Verhamme P, Potpara TS ym. The 2018 Eur...»116.
- Suorien antikoagulanttien kliinisessä käytössä huomioitavia seikkoja on käsitelty yksityiskohtaisesti EHRA:n julkaisemassa ohjeessa «Steffel J, Verhamme P, Potpara TS ym. The 2018 Eur...»116, jonka tiivistelmä on julkaistu myös suomeksi ( «https://www.fincardio.fi/site/assets/files/1381/keymessages_ehra_noac_finland_bd.pdf»2), ja ESC:n hoitosuosituksessa «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Erityistilanteissa (esim. vuoto tai tukos hoidon aikana, sydäntoimenpiteet) kannattaa herkästi konsultoida hyytymisasiantuntijaa tai kardiologia.
| Dabigatraani | Apiksabaani | Edoksabaani | Rivaroksabaani | |
|---|---|---|---|---|
| * Lähes 100 % ruoan kera ** Käytössä noudatettava erityistä varovaisuutta ja harkittava muita vaihtoehtoja *** Kliininen merkitys vähäinen PCC = protrombiinikompleksikonsentraatti |
||||
| Vaikutusmekanismi | Suora trombiinin (tekijä II) estäjä | Suora tekijän Xa estäjä | Suora tekijän Xa estäjä | Suora tekijän Xa estäjä |
| Biologinen hyötyosuus | 3–7 % | 50 % | 62 % | 66 %* |
| Ruoan vaikutus imeytymiseen | Ei vaikutusta | Ei vaikutusta | 6–22 % enemmän ruoan kera | 39 % enemmän ruoan kera |
| Huippupitoisuus (tuntia) | 2 | 1–4 | 1–2 | 2–4 |
| Eliminaatio | 80 % munuaisten ja 20 % muuta kautta |
27 % munuaisten ja 73 % muuta kautta |
50 % munuaisten ja 50 % muuta kautta |
35 % munuaisten ja
65 % muuta kautta |
| Puoliintumisaika (tuntia) | 12–17 | 9–14 | 10–14 | 5–13 |
| Normaali annos eteisvärinässä | 150 mg x 2 Potilaan ikä ja paino huomioitava annostelussa | 5 mg x 2 Potilaan ikä ja paino huomioitava annostelussa | 60 mg x 1 Potilaan paino huomioitava annostelussa | 20 mg x1 Otettava ruoan kanssa |
| Annostelu munuaisten vajaatoiminnassa | ||||
| eGFR > 50 ml/min | 150 mg x 2 | 5 mg x 2 | 60 mg x 1 | 20 mg x 1 |
| eGFR 30–49 ml/min | 110 mg x 2 | 5 mg x 2 | 30 mg x 1 | 15 mg x 1 |
| eGFR 15–29 ml/min | Vasta-aiheinen | (2,5 mg x 2)** | (30 mg x 1)** | (15 mg x 1)** |
| eGFR < 15 ml/min | Vasta-aiheinen | Vasta-aiheinen | Vasta-aiheinen | Vasta-aiheinen |
| Yhteisvaikutukset | ||||
| P-glykoproteiini | Kyllä | Kyllä | Kyllä | Kyllä |
| CYP3A4 | Ei | Kyllä (kohtalainen) | Kyllä (vähäinen) | Kyllä (kohtalainen) |
| Vaikutuksen kumoaminen | Idarusitsumabi | Andeksaneetti alfa
PCC |
Andeksaneetti alfa
PCC |
Andeksaneetti alfa
PCC |
| Erityispiirteitä |
Dyspepsiaa 5–10 %:lle
Happosalpaajat heikentävät imeytymistä 12–30 %*** Säilytettävä foliopakkauksessa |
Teho voi heikentyä, jos eGFR > 95 ml/min *** | ||
| Edut |
| Vähemmän kallonsisäisiä vuotoja |
| Vakioannostelu ja ennustettavampi annosvaikutus |
| K-vitamiinin saannin vaihtelu (ravinto) ei muuta vaikutusta |
| Vähemmän lääkeinteraktioita |
| Ei rutiinimaisen lääkevaikutuksen monitoroinnin tarvetta (helpompi ja mukavampi toteuttaa) |
| Merkittävät haitat |
| Vasta-aiheisia mitraaliläpän ahtaumassa ja potilailla, joilla on mekaaninen tekoläppä |
| Vasta-aiheisia vaikeassa munuaisten vajaatoiminnassa (annoksen pienentäminen lievemmissä tapauksissa) |
| Muita huomioitavia seikkoja |
| Monitorointimenetelmien huonompi saatavuus (lääkevaikutuksen ja hoitomyönteisyyden seuranta on vaativampaa silloin kun siihen on tarvetta) |
| Potilaan ikä ja paino vaikuttavat joidenkin valmisteiden annosteluun |
| Muut haittavaikutukset kuin vuodot tavallisempia (esim. dyspepsia) |
| Hinta |
Dabigatraani
- Dabigatraani on kaksi kertaa vuorokaudessa otettava suora trombiininestäjä, joka estää aivohalvauksia
vähintään yhtä hyvin kuin varfariini «Suora trombiinin estäjä dabigatraani ilmeisesti estää aivohalvauksia yhtä hyvin kuin varfariini ja aiheuttaa vähemmän kallonsisäisiä verenvuotoja.»B.
- Vuorokausiannos 150 mg x 2 estää aivohalvauksia merkitsevästi paremmin (NNT 182) ja aiheuttaa vähemmän kallonsisäisiä verenvuotoja kuin varfariini «Connolly SJ, Ezekowitz MD, Yusuf S ym. Dabigatran ...»232.
- Annos 110 mg x 2 estää aivohalvauksia yhtä tehokkaasti kuin varfariini (NNT 718) ja aiheuttaa vähemmän verenvuotoja «Connolly SJ, Ezekowitz MD, Yusuf S ym. Dabigatran ...»232.
- Dabigatraanin suositeltava vuorokausiannos eteisvärinän aiheuttamien tukosten estossa on 150 mg x 2.
- Annoksen pienentämistä (110 mg x 2) suositellaan seuraavissa tapauksissa:
- Potilas on yli 80-vuotias.
- Potilas käyttää verapamiilia.
- Kreatiniinipuhdistuma (eGFR) on 30–50 ml/min.
- Dabigatraanin tärkeimmät vasta-aiheet ovat
- yliherkkyys
- mekaaninen tekoläppä
- mitraalistenoosi
- eGFR < 30 ml/min
- ALAT > 2 x normaalin yläraja
- voimakkaiden P-glykoproteiinin estäjien (systeemisesti käytetty ketokonatsoli, siklosporiini, itrakonatsoli tai takrolimuusi) ja dronedaronin yhtäaikainen käyttö.
- Hätätilanteissa (esim. vaikea verenvuoto, kiireellinen leikkaus) dabigatraanin vaikutus voidaan kumota spesifisellä vasta-aineella (idarusitsumabi) «Pollack CV Jr, Reilly PA, Eikelboom J ym. Idaruciz...»228.
- PCC ei juurikaan kumoa dabigatraanin vaikutusta.
Apiksabaani
- Apiksabaani on kaksi kertaa vuorokaudessa otettava tekijä Xa estäjä, joka estää aivohalvauksia tehokkaammin ja aiheuttaa vähemmän kallonsisäisiä vuotoja kuin varfariini «Suora tekijä Xa:n estäjä apiksabaani ilmeisesti estää aivohalvauksia paremmin kuin varfariini ja aiheuttaa vähemmän kallonsisäisiä ja vakavia verenvuotoja.»B, «Granger CB, Alexander JH, McMurray JJ ym. Apixaban...»233.
- Apiksabaanin suositeltava vuorokausiannos eteisvärinän aiheuttamisen tukosten estossa on 5 mg x 2.
- Annoksen pienentämistä (2,5 mg x 2) suositellaan, jos vähintään kaksi seuraavista
ominaisuuksista täyttyy:
- Potilas on ≥ 80-vuotias.
- Potilas painaa ≤ 60 kg.
- Seerumin kreatiniinipitoisuus on ≥ 130 mikromol/l.
- Apiksabaanin tärkeimmät vasta-aiheet ovat
- yliherkkyys
- mekaaninen tekoläppä
- mitraalistenoosi
- vaikea maksasairaus
- voimakkaiden CYP3A4:n ja P-glykoproteiinin estäjien (esim. atsoliryhmän sienilääkkeet) yhteiskäyttö.
- Hätätilanteissa apiksabaanin vaikutus voidaan kumota spesifisellä vasta-aineella (andeksaneetti alfa). Myös PCC kumoaa apiksabaanin vaikutusta.
Edoksabaani
- Edoksabaani on kerran päivässä otettava tekijä Xa:n estäjä, joka estää aivohalvauksia vähintään yhtä hyvin kuin varfariini «Suora tekijä Xa -estäjä edoksabaani ilmeisesti estää aivohalvauksia vähintään yhtä hyvin ja aiheuttaa vähemmän kallonsisäisiä verenvuotoja kuin varfariini.»B, «Giugliano RP, Ruff CT, Braunwald E ym. Edoxaban ve...»234.
- Suositeltava annos eteisvärinän aiheuttamien tukosten estossa on 60 mg x 1.
- Lääkkeen teho heikkenee, jos munuaisten toiminta on poikkeuksellisen hyvä «Bohula EA, Giugliano RP, Ruff CT ym. Impact of Ren...»235.
- Annosta on pienennettävä (30 mg x 1), jos
- eGFR on 15–49 ml/min (GFR-laskuri «GFR-laskuri»1) tai
- paino on alle 60 kg.
- Edoksabaanin tärkeimmät vasta-aiheet ovat
- yliherkkyys
- mekaaninen tekoläppä
- mitraalistenoosi
- eGFR < 15 ml/min
- voimakkaiden CYP3A4:n ja P-glykoproteiinin estäjien yhteiskäyttö (esim. atsoliryhmän sienilääkkeet).
- Hätätilanteissa edoksabaanin vaikutus voidaan kumota spesifisellä vasta-aineella (andeksaneetti alfa). Myös PCC kumoaa edoksabaanin vaikutusta.
Rivaroksabaani
- Rivaroksabaani on kerran vuorokaudessa otettava tekijän Xa estäjä, joka estää aivohalvauksia yhtä hyvin ja aiheuttaa vähemmän kallonsisäisiä vuotoja kuin varfariini «Suora hyytymistekijä Xa:n estäjä rivaroksabaani ilmeisesti estää aivohalvauksia paremmin kuin varfariini. Hoito aiheuttaa vakavia verenvuotoja saman verran ja kallonsisäisiä verenvuotoja vähemmän kuin varfariini.»B, «Patel MR, Mahaffey KW, Garg J ym. Rivaroxaban vers...»236.
- Rivaroksabaanin suositeltava vuorokausiannos eteisvärinän aiheuttamien tukosten estohoidossa on 20 mg x 1 potilaan iästä ja painosta riippumatta.
- Annoksen pienentämistä (15 mg x 1) suositellaan, jos eGFR = 30–49 ml/min.
- Rivaroksabaanin tärkeimmät vasta-aiheet ovat
- yliherkkyys
- mekaaninen tekoläppä
- mitraalistenoosi
- eGFR < 15 ml/min
- vaikea maksasairaus
- voimakkaiden CYP3A4:n ja P-glykoproteiinin estäjien yhteiskäyttö.
- Hätätilanteissa rivaroksabaanin vaikutus voidaan kumota spesifisellä vasta-aineella (andeksaneetti alfa). Myös PCC kumoaa rivaroksabaanin vaikutusta.
Varfariini
- Varfariini estää aivohalvauksia merkitsevästi paremmin kuin lumelääke «Oraalinen antikoagulaatiohoito estää hyvin aivohalvauksien ilmaantumista eteisvärinäpotilailla primaaripreventiossa (vaaran väheneminen 59 %) ja sekundaaripreventiossa (68 %, yhdistettynä 62 %) (95 % luottamusvälit 48–72 %) lumeeseen verrattuna.»A ja ASA «Varfariini estää aivohalvauksia merkittävästi paremmin kuin ASA.»A.
- Yhden aivohalvaustapauksen estämiseksi on riskin suuruuden mukaan hoidettava varfariinilla vuoden ajan 15–238 potilasta (kuva «Antitromboottinen hoito eteisvärinässä»4). Ks. lisätietoaineisto «Antikoagulaatiohoidon hyöty suhteessa aivoinfarktin riskin suuruuteen»4.
- Varfariinin annos on yksilöllinen, ja se säädetään INR-mittausten perusteella
- Aivohalvauksen eston ja verenvuotokomplikaatioiden kannalta INR 2–3 on ihanteellinen hoitotaso «Varfariinihoito estää tehokkaasti aivohalvauksia, kun hoitotasapaino on hyvä.»A, (kuva «INR-arvon vaikutus»24).
- Pitkäaikaishoidossa INR määritetään yleensä kerran kuukaudessa ja mittauksia tihennetään, jos arvot heittelevät tai potilaan muu lääkitys tai tila muuttuu.
- Lisätietoa varfariinihoidon toteutuksesta on lisätietoaineistossa «Varfariinin annosteluohje»5 ja internetissä «https://www.julkari.fi/bitstream/handle/10024/120375/antikoagluaatiohoidon%20k%c3%a4sikirja.pdf?sequence=1&isAllowed=y»3, ja lisätietoa antikoagulaatiohoidon toteutuksesta erityistilanteissa on ESC:n hoitosuosituksessa «European Heart Rhythm Association., European Assoc...»115.
- Varfariinihoidon tasapainoa kuvaava TTR ("time in therapeutic range") -arvo ilmaisee
ajan (%), jona lääkitys on ollut hoitotasolla (INR = 2–3). TTR-laskuri on osoitteessa «http://www.terveyskirjasto.fi/xmedia/pgr/200.054.html»4.
- Varfariinihoidon teho ja turvallisuus ovat parhaat, kun TTR on yli 70 % «Lehto M, Luojus A, Halminen O, ym. Time-in-therape...»237.
- Poikkeuksellisen suuret tai pienet yksittäiset INR-arvot altistavat tukos- ja vuotokomplikaatioille TTR:stä riippumatta «Varfariinihoito estää tehokkaasti aivohalvauksia, kun hoitotasapaino on hyvä.»A, «European Heart Rhythm Association., European Assoc...»115, «Nilsson GH, Björholt I, Krakau I. Anticoagulant tr...»238.
- Eteisvärinäpotilaan sepelvaltimotaudissa pelkkä varfariinihoito riittää yleensä estämään
sekä eteisvärinään että valtimotautiin liittyviä tapahtumia «European Heart Rhythm Association., European Assoc...»115.
- ASAn tai ADP-reseptorin P2Y12 salpaajien käyttö yhdessä varfariinin kanssa lisää verenvuotovaaraa muttei paranna antitromboottista tehoa vakaassa sepelvaltimotaudissa.
- Poikkeuksia ovat potilaat, joilla on mekaaninen mitraalitekoläppä (pysyvä yhteiskäyttö) tai sepelvaltimoiden pallolaajennuksen jälkitila (väliaikainen yhteiskäyttö).
- Hätätilanteissa varfariinin vaikutus voidaan kumota PCC:lla tai K-vitamiinilla.

INR-arvon vaikutus aivohalvausten ja kallonsisäisten verenvuotojen vaaraan varfafiinihoidon aikana. INR = 2–3 on ihanteellinen hoidon tehon ja vuotokomplikaatioden suhteen.
© Suomalainen Lääkäriseura Duodecim
Asetyylisalisyylihappo (ASA)
- ASAa ei pidä käyttää eteisvärinään liittyvien tromboembolisten komplikaatioiden estoon, koska
- suuren ja keskisuuren riskin potilailla sen teho eteisvärinään liittyvien tukosten estossa on merkitsevästi huonompi kuin varfariinin «Varfariini estää aivohalvauksia merkittävästi paremmin kuin ASA.»A ja suorien antikoagulanttien «Connolly SJ, Eikelboom J, Joyner C ym. Apixaban in...»239
- pienen riskin potilailla ASAn hyöty on vähäisempi kuin sen haitat «ASA estää aivohalvauksia eteisvärinäpotilailla noin 20 % lumelääkkeeseen verrattuna. Teho antikoagulaatiohoitoon verrattuna on kuitenkin matala.»A.
- ASAn käyttö suositellaan yleensä lopetettavaksi, kun aloitetaan suora antikoagulantti
tai varfariini.
- Yhteiskäyttö lisää verenvuotovaaraa muttei paranna antitromboottista tehoa.
- Poikkeuksina ovat potilaat, joilla on sepelvaltimoiden pallolaajennuksen jälkitila (väliaikainen yhteiskäyttö).
ADP-reseptorin P2Y12 salpaajat
- ADP-reseptorin P2Y12 salpaajia (klopidogreeli, prasugreeli, tikagreloli, tiklodipiini) ei yksinään ole tutkittu eteisvärinään liittyvän aivohalvauksen estossa, joten niitä ei pidä käyttää eteisvärinään liittyvän aivohalvauksen estoon.
- Klopidogreelin ja ASAn yhdistelmä estää aivohalvauksia paremmin kuin pelkkä ASA, mutta se lisää verenvuotokomplikaatioita «Klopidogreeli-ASA -yhdistelmähoidon aivohalvauksia estävä teho on parempi kuin pelkän ASA-hoidon, mutta kliinistä hyötyä ei ole yhdistelmän aiheuttamien verenvuotojen vuoksi.»B ja sen teho on merkitsevästi huonompi kuin varfariinin «Klopidogreeli-ASA -yhdistelmähoidon aivohalvauksia estävä teho on parempi kuin pelkän ASA-hoidon, mutta kliinistä hyötyä ei ole yhdistelmän aiheuttamien verenvuotojen vuoksi.»B.
- Väliaikainen yhteiskäyttö suorien antikoagulanttien tai varfariinin kanssa voi olla aiheellista sepelvaltimoiden pallolaajennuksen yhteydessä.
Oraalisen antikoagulantin valinta
- Valinta suorien antikoagulanttien ja varfariinin välillä tehdään yksilöllisesti niin, että huomioidaan lääkkeiden edut ja haitat (taulukko «Suorien antikoagulanttien edut ja haitat varfariiniin verrattuna...»16), potilaan toiveet ja alla mainittavat seikat.
- Paremman hoitomyönteisyyden ja turvallisuuden takia suora antikoagulantti on ensisijainen
valinta useimmille uusille eteisvärinäpotilaille «Zalesak M, Siu K, Francis K ym. Higher persistence...»240, «Gorst-Rasmussen A, Skjøth F, Larsen TB ym. Dabigat...»241.
- Suorat antikoagulantit ovat vähintään yhtä tehokkaita ja etenkin kallonsisäisten verenvuotojen kannalta turvallisempia kuin varfariini eteisvärinään liittyvien aivohalvausten estossa «Suorat antikoagulatit ovat tehokkaampia ja turvallisempia kuin varfariini eteisvärinään liittyvien aivohalvauksien estossa.»A.
- Suorien antikoagulanttien etuna lyhytaikaisessa hoidossa (mm. kardioversion tai ablaatiohoidon yhteydessä) on se, että vaikutus alkaa nopeasti ja hoitovaikutus saavutetaan huomattavasti nopeammin kuin varfariinia käytettäessä.
- Pitkäaikaishoidossa hyvin toteutettua varfariinihoitoa voidaan jatkaa «Joosten LPT, van Doorn S, van de Ven PM, ym. Safet...»242, sillä rutiinimainen vaihto suoraan antikoagulanttiin saattaa olla jopa haitallista etenkin iäkkäillä
ja haurailla potilailla.
- Iäkkäillä ja monisairailla INR-seurantaan liittyvät säännölliset terveydenhuollon kontaktit voivat olla hyödyllisiä.
- Pikainen vaihto suoraan antikoagulanttiin on aiheellinen, jos
- varfariinia ei voida jatkaa allergian tai muun haitan takia
- INR-seuranta ei onnistu.
- Jos TTR on < 70 %, selvitetään huonon tasapainon syy ja arvioidaan, voidaanko tilanne korjata varfariinihoitoa tehostamalla tai vaihtamalla suoraan antikoagulanttiin.
- Suoria antikoagulantteja ei ole vertailtu keskenään, eikä valintaan niiden välillä voida tässä vaiheessa ottaa kantaa.
Eteiskorvakkeen sulku
- Perkutaanisella sydämen sisältä katetriteitse asennettavalla sulkulaitteella tehtävä
vasemman eteiskorvakkeen sulku ilmeisesti estää tromboembolisia aivotapahtumia yhtä
tehokkaasti kuin varfariinihoito «Vasemman eteiskorvakkeen sulku perkutaanisella sydämen sisältä katetriteitse asennettavalla sulkulaitteella estää tromboembolisia aivotapahtumia todennäköisesti yhtä tehokkaasti kuin varfariinihoito korkean tromboembolian ja korkean vuotoriskin potilailla.»B.
- Komplikaatiovaarasta huolimatta toimenpidettä voidaan harkita suuren tukosriskin potilaille, joilla oraalinen antikoagulaatiohoito on vasta-aiheinen.
- Lisäksi toimenpidettä voidaan harkita, jos suuren riskin potilaalla ilmenee vakava vuotokomplikaatio terapeuttisen antikoagulaatiohoidon aikana.
- Sydänleikkauksen yhteydessä tehtävä vasemman eteiskorvakkeen täydellinen sulku vähentänee
eteisvärinäpotilaan tromboembolisia komplikaatioita yhtä tehokkaasti kuin varfariinihoito
«Muun sydänkirurgian yhteydessä tehtävä vasemman eteiskorvakkeen täydellinen sulku vähentänee eteisvärinäpotilaan tromboembolisia komplikaatioita yhtä tehokkaasti kuin varfariinihoito.»B.
- Epätäydellinen kirurginen eteiskorvakkeen sulku saattaa olla haitallisempi kuin sulkematta jättäminen «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Aryana A, Singh SK, Singh SM ym. Association betwe...»243.
- Toimenpidettä voidaan harkita muun sydänleikkauksen yhteydessä, jos eteisvärinäalttius on ilmeinen ja potilaalla on myös muita aivoverenkierron häiriön vaaratekijöitä.
- Sydänleikkauksen yhteydessä tehty eteiskorvakkeen sulku tai poisto ei poista antikoagulaatiohoidon tarvetta. Yhdistettynä antikoagulaatiohoitoon se ilmeisesti vähentää tromboembolisia komplikaatiota enemmän kuin antikoagulaatiohoito yksinään «Whitlock RP, Belley-Cote EP, Paparella D, ym. Left...»244.
Seuranta
- Eteisvärinä on krooninen sairaus, joka edellyttää säännöllistä seurantaa.
- Ensimmäinen seurantakäynti on yleensä aiheellinen noin puolen vuoden kuluttua eteisvärinän toteamisesta, ja sen jälkeen seurantakäyntien ajoitus riippuu potilaan taustasairauksista ja kokonaistilanteesta sekä rytmihäiriöiden esiintymisestä.
- Valtaosalla potilaista seuranta voidaan toteuttaa perusterveydenhuollossa.
- Seurantakäynnin aikana selvitetään
- onko perussairauksien tilanne tai hoito muuttunut ja tarvittaessa tehostetaan hoitoa tai järjestetään tarvittavat lisätutkimukset
- ovatko aivoverenkierron häiriöiden ja verenvuotojen vaaratekijät muuttuneet (CHA2DS2VA- ja HAS-BLED-pisteytys)
- onko potilaalla ollut aivoverenkierron häiriöön viittaavia oireita
- onko antikoagulaatiohoito toteutunut suositusten mukaisesti (varfariinihoidon aikana TTR:n tavoite on yli 70 %)
- ovatko potilaan rytmihäiriöoireet helpottuneet hoidon vaikutuksesta (EHRA-luokka)
- onko käytössä olevalle rytmihäiriölääkitykselle ilmaantunut vasta-aiheita (QRS-heilahduksen leveneminen, QT-ajan piteneminen, vasemman kammion hypertrofia, iskemia, vajaatoiminta)
- onko eteisvärinän tyyppi muuttunut kohtauksittaisesta jatkuvaksi tai pysyväksi eteisvärinäksi
- onko pysyvän eteisvärinän kammiovaste "taloudellinen".
- Anamneesin ja kliinisen tutkimuksen lisäksi tarkistetaan rutiinimaisesti 12-kytkentäinen EKG, jossa kiinnitetään huomiota muun muassa taulukossa «Suositus eteisvärinäpotilaalle tehtävistä tutkimuksista...»4 esitettäviin seikkoihin.
- Muiden tutkimusten tarve arvioidaan yksilöllisesti. Mahdollisia tutkimuksia ovat muun
muassa:
- laboratoriotutkimukset (esim. pieni verenkuva, trombosyytit, elektrolyytit, kreatiniini, glukoosi, lipidit, antikoagulaatiohoidon ja rytmihäiriölääkityksen turvakokeet)
- sydämen kaikututkimus
- thorax-röntgenkuvaus
- EKG:n pitkäaikaisrekisteröinti
- rasitus-EKG
- invasiiviset tutkimukset
- tarkemmat neurologiset selvittelyt.
- Eteisvärinä ei yleensä aiheuta pitkäaikaista työkyvyttömyyttä eikä estä autolla ajoa.
- Lyhytkestoinen sairausloma voi kuitenkin olla aiheellinen rytmihäiriökohtauksen, rytminsiirron tai esimerkiksi katetriablaatiohoidon takia.
- Ammattiautoilun jatkaminen edellyttää suositusten mukaan toteutuvaa antikoagulaatiohoitoa.
Hoidon porrastus
- Eteisvärinän hoito on monimutkaista ja vaatii moniammatillista osaamista ja hyvää yhteistyötä eri erikoisalojen (mm. kardiologia, sisätaudit, neurologia ja hyytymisasiantuntijat) ja perusterveydenhuollon välillä.
- Erikoissairaanhoidon velvollisuutena on varmistaa alueellisten hoitoketjujen toimivuus ja järjestää oman alueensa hoitohenkilökunnalle koulutusta ja riittävät konsultaatiomahdollisuudet.
- Perusterveydenhuollon lääkäreillä on oltava hyvät perustiedot eteisvärinäpotilaan
- antikoagulaatiohoidon aiheista ja toteutuksesta
- hoitolinjan (sykkeen- vai rytminhallinta) valintaan vaikuttavista tekijöistä
- kammiotaajuuden optimoinnista
- estolääkityksen aiheista ja seurannasta
- invasiivisen hoidon aiheista
- Potilaiden opastukseen löytyy runsaasti materiaalia ja oppaita muun muassa Sydänliiton «https://sydan.fi/»5 ja Terveyskylän «https://www.terveyskyla.fi/»6 verkkosivustoilta, ja potilasjärjestöt tarjoavat myös vertaistukea.
- Perussairauksien ja altistavien tekijöiden hoito
- Perussairauksien hyvä hoito on eteisvärinän hoidon kulmakivi riippumatta valitusta hoitolinjasta (taulukko «Eteisvärinän tavallisimpien taustatekijöiden hoitotavoitteita ja hoitomuotoja....»6).
- Päävastuu yleisimpien eteisvärinälle ja tromboembolisille komplikaatioille altistavien liitännäissairauksien, kuten hypertension ja diabeteksen, diagnostiikasta ja hoidosta on perusterveydenhuollon lääkäreillä.
- Erikoissairaanhoidossa on syytä hoitaa tavanomaiseen lääkitykseen huonosti reagoivat ja sellaiset potilaat, joiden liitännäissairaus vaatii invasiivisia tutkimuksia tai hoitoa.
- Akuutin eteisvärinäkohtauksen hoito
- Hoitolinja (sykkeen- tai rytminhallinta) voidaan yleensä valita perusterveydenhuollossa. Ongelmatapauksissa on aiheellista konsultoida kardiologia.
- Sähköinen rytminsiirto vaatii anestesian, minkä takia se soveltuu vain harvoin perusterveydenhuollossa tehtäväksi.
- Lääkkeellinen rytminsiirto voidaan tehdä myös hyvin varustetussa terveyskeskuksessa.
- Eteisvärinän estohoito (rytminhallinta)
- Beetasalpaajalääkitys voidaan aloittaa perusterveydenhuollossa.
- Varsinaisen rytmihäiriölääkityksen (ryhmien I ja III lääkkeet) aloittaa kardiologi tai sydänsairauksien hoitoon perehtynyt sisätautilääkäri.
- Terveyskeskus- tai työterveyslääkäri voi huolehtia potilaan jatkoseurannasta erikoislääkärin ohjeiden mukaisesti.
- Invasiivisen hoidon suunnittelu ja toteutus kuuluvat rytmikardiologille.
- Kammiotaajuuden optimointi (sykkeenhallinta)
- Pysyvän eteisvärinän kammiotaajuuden optimoinnissa ja seurannassa päävastuu on perusterveydenhuollon lääkäreillä.
- Erikoissairaanhoidossa on syytä hoitaa tavanomaiseen lääkitykseen huonosti reagoivat ja sellaiset potilaat, joiden liitännäissairaus vaatii erikoissairaanhoitoa.
- Antikoagulaatiohoito
- Perusterveydenhuollon lääkäreillä on päävastuu antikoagulaatiohoidon toteutuksesta.
- Edellä esitetyt suositukset ovat ohjeellisia, ja niitä voidaan muokata paikallisesti niin, että alueellinen hoitoketju toimii mahdollisimman tehokkaasti.
Suomalaisen Lääkäriseuran Duodecimin ja Suomen Kardiologisen Seuran asettama työryhmä
Eteisvärinä-suosituksen historiatiedot «Eteisvärinä, Käypä hoito -suosituksen historiatiedot»6
Puheenjohtaja
Pekka Raatikainen, dosentti, ylilääkäri, kardiologian ja sisätautien erikoislääkäri; HUS Sydän- ja keuhkokeskus
Jäsenet
Kari Askonen, LL, yleislääketieteen erikoislääkäri; Mehiläinen
Juhani Junttila, professori, kardiologian erikoislääkäri; OYS ja Oulun yliopisto
Tuomas Kiviniemi, kardiologian apulaisprofessori, kardiologian erikoislääkäri; TYKS Sydänkeskus, Turun Yliopisto
Riho Luite, LL, kardiologian erikoislääkäri, KYS Sydänkeskus
Annukka Marjamaa, dosentti, kardiologian erikoislääkäri; HUS Sydän- ja keuhkokeskus
Tero Penttilä, LT, kardiologian erikoislääkäri; TAYS Sydänsairaala
Tuula Meinander, LL, BSc, kardiologian ja sisätautien erikoislääkäri, terveydenhuoltoon erikoistuva lääkäri, Käypä hoito -toimittaja
Sidonnaisuudet
Sidonnaisuusilmoitukset on tarkistettu 26.2.2025 julkaistun kohdennetun päivityksen yhteydessä.
Kari Askonen: Sivutoimet: Mehiläinen, oma vastaanotto, yksityislääkäri. Luento-, koulutus- ja asiantuntijapalkkiot: Divicon Oy. Luottamustoimet: Lääkäriliiton professiovaliokunnan jäsen, Oulu. Ohjaushankkeet: Sote. Muut sidonnaisuudet: Divicon Oy.
Juhani Junttila: Sivutoimet: Oulun yliopistollinen sairaala, ylilääkäri. Tutkimusrahoitus: Abbot Medical Finland, Boehringer Ingelheim. Luento-, koulutus- ja asiantuntijapalkkiot: Astra Zeneca, Boehringer Ingelheim, Bayer, Pfizer, MSD, Sanofi, Novo Nordisk. Korvaukset koulutus- ja kongressikuluista: Novo Nordisk. Luottamustoimet: Valtakunnallinen terveyden tutkimuksen arviointiryhmän jäsen; Sydäntutkimussäätiön tieteellisen asiantuntijavaliokunnan jäsen. Muut sidonnaisuudet: Oulun Sydänkeskus Oy osakas.
Tuomas Kiviniemi: Tutkimusrahoitus: EU/H2020-ECSEL-2019-IA-876190 Moore4Medical, EU/EIC Pathfinder Miracle, Suomen Akatemia LAA-CLOSURE, Sydäntutkimussäätiö, Emil Aaltosen säätiö, Atricure ltd, USA; Vifor Pharma, Sveitsi. Luento-, koulutus- ja asiantuntijapalkkiot: AstraZeneca, Bayer, BMS-Pfizer, Boehringer-Ingelheim, MSD, Orion Pharma. Luottamustoimet: Suomen Kardiologinen Seura, hallituksen jäsen
Riho Luite: Sivutoimet: Luento-, koulutus- ja asiantuntijapalkkiot: BMS/Pfizer, Bayer, Biosense Webster. Korvaukset koulutus- ja kongressikuluista: Biosense Webster, Stereotaxis.
Annukka Marjamaa: Sivutoimet: Terveystalo, RemoTest, yksityislääkäri. Luento-, koulutus- ja asiantuntijapalkkiot: Abbott, Medtronic.
Tuula Meinander: Sivutoimet: Käypä hoito -toimittaja, Suomalainen Lääkäriseura Duodecim; Yksityislääkäri (Mehiläinen Finlayson, Pihlajalinna Koskikeskus, Aava Ratina); Väitöskirjatutkija, Tampereen yliopisto, Oikeuslääketiede. Koulutustoiminta: Suomalainen Lääkäriseura Duodecim, Suomen Lääkäriliitto, Suomen Kardiologinen Seura, Bayer Oy. Kongressit ja seminaarit: Suomen Kardiologinen Seura, Bayer Oy, Orion Oyj. Luottamustoimet: Käyvän hoidon Sepelvaltimotauti-neuvottelukunnan puheenjohtaja; Käyvän hoidon Diabetes-neuvottelukunnan puheenjohtaja; Suomen Lääkäriliiton luottamuslääkäri ja Tampereen Terveyspoliittisen valiokunnan jäsen; Suomen Kardiologisen Seuran Sydänääni-lehden toimittaja ja tromboosijaoksen puheenjohtaja; Guidelines International Network (G-I-N) Pohjoismaisen työryhmän jäsen.
Tero Penttilä: Luento-, koulutus- ja asiantuntijapalkkiot: BMS-Pfizer, Boehringer-Ingelheim. Muut sidonnaisuudet: Orionin osakeomistus.
Pekka Raatikainen: Sivutoimet: Orton Oy, TAYS Sydänsairaala, Coronaria Analyysipalvelut, yksityislääkäri. Tutkimusrahoitus: Biosense Webster. Luento-, koulutus- ja asiantuntijapalkkiot: Biosense Webster, BMS/Pfizer, Stereotaxis. Luottamustoimet: Valviran pysyvä asiantuntija. Muut sidonnaisuudet: Orion osakeomistus.
Kirjallisuusviite
Eteisvärinä. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Kardiologisen Seuran asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2025 (viitattu pp.kk.vvvv). Saatavilla internetissä: www.kaypahoito.fi
Tarkemmat viittausohjeet: «http://www.kaypahoito.fi/web/kh/viittaaminen»7
Vastuun rajaus
Käypä hoito -suositukset ja Vältä viisaasti -suositukset ovat asiantuntijoiden laatimia yhteenvetoja yksittäisten sairauksien diagnostiikan ja hoidon vaikuttavuudesta. Suositukset toimivat lääkärin tai muun terveydenhuollon ammattilaisen päätöksenteon tukena hoitopäätöksiä tehtäessä. Ne eivät korvaa lääkärin tai muun terveydenhuollon ammattilaisen omaa arviota yksittäisen potilaan parhaasta mahdollisesta diagnostiikasta, hoidosta ja kuntoutuksesta hoitopäätöksiä tehtäessä.
Tiedonhakukäytäntö
Systemaattinen kirjallisuushaku on hoitosuosituksen perusta. Lue lisää artikkelista khk00007
Kirjallisuutta
- Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHRA/ECAS/APHRS/SOLAECE expert consensus statement on catheter and surgical ablation of atrial fibrillation: Executive summary. Europace 2018;20:157-208 «PMID: 29016841»PubMed
- Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ESC Guidelines for the management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2024;45(36):3314-3414 «PMID: 39210723»PubMed
- Kopecky SL, Gersh BJ, McGoon MD ym. The natural history of lone atrial fibrillation. A population-based study over three decades. N Engl J Med 1987;317:669-74 «PMID: 3627174»PubMed
- Chugh SS, Havmoeller R, Narayanan K ym. Worldwide epidemiology of atrial fibrillation: a Global Burden of Disease 2010 Study. Circulation 2014;129:837-47 «PMID: 24345399»PubMed
- Lehto M, Haukka J, Aro A, ym. Comprehensive nationwide incidence and prevalence trends of atrial fibrillation in Finland. Open Heart 2022;9(2): «PMID: 36414332»PubMed
- Feinberg WM, Blackshear JL, Laupacis A ym. Prevalence, age distribution, and gender of patients with atrial fibrillation. Analysis and implications. Arch Intern Med 1995;155:469-73 «PMID: 7864703»PubMed
- Savelieva I, John Camm A. Atrial fibrillation and heart failure: natural history and pharmacological treatment. Europace 2004;5 Suppl 1:S5-19 «PMID: 15450275»PubMed
- Lloyd-Jones DM, Wang TJ, Leip EP ym. Lifetime risk for development of atrial fibrillation: the Framingham Heart Study. Circulation 2004;110:1042-6 «PMID: 15313941»PubMed
- Magnussen C, Niiranen TJ, Ojeda FM ym. Sex Differences and Similarities in Atrial Fibrillation Epidemiology, Risk Factors, and Mortality in Community Cohorts: Results From the BiomarCaRE Consortium (Biomarker for Cardiovascular Risk Assessment in Europe). Circulation 2017;136:1588-1597 «PMID: 29038167»PubMed.
- Miyasaka Y, Barnes ME, Gersh BJ ym. Secular trends in incidence of atrial fibrillation in Olmsted County, Minnesota, 1980 to 2000, and implications on the projections for future prevalence. Circulation 2006;114:119-25 «PMID: 16818816»PubMed
- Benjamin EJ, Levy D, Vaziri SM ym. Independent risk factors for atrial fibrillation in a population-based cohort. The Framingham Heart Study. JAMA 1994;271:840-4 «PMID: 8114238»PubMed
- Rensma PL, Allessie MA, Lammers WJ ym. Length of excitation wave and susceptibility to reentrant atrial arrhythmias in normal conscious dogs. Circ Res 1988;62:395-410 «PMID: 3338122»PubMed
- Allessie MA, Boyden PA, Camm AJ ym. Pathophysiology and prevention of atrial fibrillation. Circulation 2001;103:769-77 «PMID: 11156892»PubMed
- Nattel S. New ideas about atrial fibrillation 50 years on. Nature 2002;415:219-26 «PMID: 11805846»PubMed
- Tieleman RG. The pathophysiology of maintenance of atrial fibrillation. Pacing Clin Electrophysiol 2003;26:1569-71 «PMID: 12914604»PubMed
- Haïssaguerre M, Jaïs P, Shah DC ym. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. N Engl J Med 1998;339:659-66 «PMID: 9725923»PubMed
- Chen SA, Chen YJ, Yeh HI ym. Pathophysiology of the pulmonary vein as an atrial fibrillation initiator. Pacing Clin Electrophysiol 2003;26:1576-82 «PMID: 12914606»PubMed
- Nattel S. Basic electrophysiology of the pulmonary veins and their role in atrial fibrillation: precipitators, perpetuators, and perplexers. J Cardiovasc Electrophysiol 2003;14:1372-5 «PMID: 14678116»PubMed
- Wijffels MC, Kirchhof CJ, Dorland R ym. Atrial fibrillation begets atrial fibrillation. A study in awake chronically instrumented goats. Circulation 1995;92:1954-68 «PMID: 7671380»PubMed
- Allessie M, Ausma J, Schotten U. Electrical, contractile and structural remodeling during atrial fibrillation. Cardiovasc Res 2002;54:230-46 «PMID: 12062329»PubMed
- Sparks PB, Mond HG, Vohra JK ym. Mechanical remodeling of the left atrium after loss of atrioventricular synchrony. A long-term study in humans. Circulation 1999;100:1714-21 «PMID: 10525491»PubMed
- Schotten U, Duytschaever M, Ausma J ym. Electrical and contractile remodeling during the first days of atrial fibrillation go hand in hand. Circulation 2003;107:1433-9 «PMID: 12642366»PubMed
- Nattel S, Li D, Yue L. Basic mechanisms of atrial fibrillation--very new insights into very old ideas. Annu Rev Physiol 2000;62:51-77 «PMID: 10845084»PubMed
- Burstein B, Nattel S. Atrial fibrosis: mechanisms and clinical relevance in atrial fibrillation. J Am Coll Cardiol 2008;51:802-9 «PMID: 18294563»PubMed
- Schoonderwoerd BA, Smit MD, Pen L ym. New risk factors for atrial fibrillation: causes of 'not-so-lone atrial fibrillation'. Europace 2008;10:668-73 «PMID: 18480076»PubMed
- Elosua R, Arquer A, Mont L ym. Sport practice and the risk of lone atrial fibrillation: a case-control study. Int J Cardiol 2006;108:332-7 «PMID: 15963583»PubMed
- Mont L, Sambola A, Brugada J ym. Long-lasting sport practice and lone atrial fibrillation. Eur Heart J 2002;23:477-82 «PMID: 11863350»PubMed
- Abdulla J, Nielsen JR. Is the risk of atrial fibrillation higher in athletes than in the general population? A systematic review and meta-analysis. Europace 2009;11:1156-9 «PMID: 19633305»PubMed
- Wilhelm M, Roten L, Tanner H ym. Atrial remodeling, autonomic tone, and lifetime training hours in nonelite athletes. Am J Cardiol 2011;108:580-5 «PMID: 21658663»PubMed
- Andersen K, Farahmand B, Ahlbom A ym. Risk of arrhythmias in 52 755 long-distance cross-country skiers: a cohort study. Eur Heart J 2013;34:3624-31 «PMID: 23756332»PubMed
- Karjalainen J, Kujala UM, Kaprio J ym. Lone atrial fibrillation in vigorously exercising middle aged men: case-control study. BMJ 1998;316:1784-5 «PMID: 9624065»PubMed
- Turagam MK, Flaker GC, Velagapudi P ym. Atrial Fibrillation In Athletes: Pathophysiology, Clinical Presentation, Evaluation and Management. J Atr Fibrillation 2015;8:1309 «PMID: 27957228»PubMed
- Calvo N, Ramos P, Montserrat S ym. Emerging risk factors and the dose-response relationship between physical activity and lone atrial fibrillation: a prospective case-control study. Europace 2016;18:57-63 «PMID: 26333377»PubMed
- Aizer A, Gaziano JM, Cook NR ym. Relation of vigorous exercise to risk of atrial fibrillation. Am J Cardiol 2009;103:1572-7 «PMID: 19463518»PubMed
- Manolis AS, Manolis AA. Exercise and Arrhythmias: A Double-Edged Sword. Pacing Clin Electrophysiol 2016;39:748-62 «PMID: 27120033»PubMed
- Brugada R, Tapscott T, Czernuszewicz GZ ym. Identification of a genetic locus for familial atrial fibrillation. N Engl J Med 1997;336:905-11 «PMID: 9070470»PubMed
- Troughton RW, Asher CR, Klein AL. The role of echocardiography in atrial fibrillation and cardioversion. Heart 2003;89:1447-54 «PMID: 14617563»PubMed
- Andalib A, Brugada R, Nattel S. Atrial fibrillation: evidence for genetically determined disease. Curr Opin Cardiol 2008;23:176-83 «PMID: 18382204»PubMed
- Krahn AD, Manfreda J, Tate RB ym. The natural history of atrial fibrillation: incidence, risk factors, and prognosis in the Manitoba Follow-Up Study. Am J Med 1995;98:476-84 «PMID: 7733127»PubMed
- Benjamin EJ, Wolf PA, D'Agostino RB ym. Impact of atrial fibrillation on the risk of death: the Framingham Heart Study. Circulation 1998;98:946-52 «PMID: 9737513»PubMed
- Stevenson WG, Stevenson LW, Middlekauff HR ym. Improving survival for patients with atrial fibrillation and advanced heart failure. J Am Coll Cardiol 1996;28:1458-63 «PMID: 8917258»PubMed
- Knecht S, Oelschläger C, Duning T ym. Atrial fibrillation in stroke-free patients is associated with memory impairment and hippocampal atrophy. Eur Heart J 2008;29:2125-32 «PMID: 18667399»PubMed
- Teppo K, Airaksinen KEJ, Jaakkola J, ym. Trends in treatment and outcomes of atrial fibrillation during 2007-17 in Finland. Eur Heart J Qual Care Clin Outcomes 2023;9(7):673-679 «PMID: 36542420»PubMed
- Teppo K, Lip GYH, Airaksinen KEJ, ym. Comparing CHA(2)DS(2)-VA and CHA(2)DS(2)-VASc scores for stroke risk stratification in patients with atrial fibrillation: a temporal trends analysis from the retrospective Finnish AntiCoagulation in Atrial Fibrillation (FinACAF) cohort. Lancet Reg Health Eur 2024;43():100967 «PMID: 39171253»PubMed
- Penttilä T, Lehto M, Niiranen J, ym. Differences in the risk of stroke, bleeding events, and mortality between female and male patients with atrial fibrillation during warfarin therapy. Eur Heart J Cardiovasc Pharmacother 2019;5(1):29-36 «PMID: 30052822»PubMed
- Lip GY, Nieuwlaat R, Pisters R ym. Refining clinical risk stratification for predicting stroke and thromboembolism in atrial fibrillation using a novel risk factor-based approach: the euro heart survey on atrial fibrillation. Chest 2010;137:263-72 «PMID: 19762550»PubMed
- Van Staa TP, Setakis E, Di Tanna GL ym. A comparison of risk stratification schemes for stroke in 79,884 atrial fibrillation patients in general practice. J Thromb Haemost 2011;9:39-48 «PMID: 21029359»PubMed
- Steinberg BA, Hellkamp AS, Lokhnygina Y ym. Higher risk of death and stroke in patients with persistent vs. paroxysmal atrial fibrillation: results from the ROCKET-AF Trial. Eur Heart J 2015;36:288-96 «PMID: 25209598»PubMed
- Vanassche T, Lauw MN, Eikelboom JW ym. Risk of ischaemic stroke according to pattern of atrial fibrillation: analysis of 6563 aspirin-treated patients in ACTIVE-A and AVERROES. Eur Heart J 2015;36:281-7a «PMID: 25187524»PubMed
- Alboni P, Scarfò S, Fucà G ym. Hemodynamics of idiopathic paroxysmal atrial fibrillation. Pacing Clin Electrophysiol 1995;18:980-5 «PMID: 7659571»PubMed
- Clark DM, Plumb VJ, Epstein AE ym. Hemodynamic effects of an irregular sequence of ventricular cycle lengths during atrial fibrillation. J Am Coll Cardiol 1997;30:1039-45 «PMID: 9316536»PubMed
- Lau CP, Leung WH, Wong CK ym. Haemodynamics of induced atrial fibrillation: a comparative assessment with sinus rhythm, atrial and ventricular pacing. Eur Heart J 1990;11:219-24 «PMID: 2318225»PubMed
- Shinbane JS, Wood MA, Jensen DN ym. Tachycardia-induced cardiomyopathy: a review of animal models and clinical studies. J Am Coll Cardiol 1997;29:709-15 «PMID: 9091514»PubMed
- Dorian P, Jung W, Newman D ym. The impairment of health-related quality of life in patients with intermittent atrial fibrillation: implications for the assessment of investigational therapy. J Am Coll Cardiol 2000;36:1303-9 «PMID: 11028487»PubMed
- Lüderitz B. Dirk Durrer (1918-1984). J Interv Card Electrophysiol 2000;4:547 «PMID: 11203445»PubMed
- van den Berg MP, Hassink RJ, Tuinenburg AE ym. Quality of life in patients with paroxysmal atrial fibrillation and its predictors: importance of the autonomic nervous system. Eur Heart J 2001;22:247-53 «PMID: 11161936»PubMed
- Paquette M, Roy D, Talajic M ym. Role of gender and personality on quality-of-life impairment in intermittent atrial fibrillation. Am J Cardiol 2000;86:764-8 «PMID: 11018197»PubMed
- Hekkala AM. Suomalaisten eteisvärinäpotilaiden kokemuksia sairautensa hoidosta. Suom Lääkäril 2021;76(10):650-2
- Kirchhof P, Bax J, Blomstrom-Lundquist C ym. Early and comprehensive management of atrial fibrillation: proceedings from the 2nd AFNET/EHRA consensus conference on atrial fibrillation entitled 'research perspectives in atrial fibrillation'. Europace 2009;11:860-85 «PMID: 19531542»PubMed
- Kirchhof P, Toennis T, Goette A, ym. Anticoagulation with Edoxaban in Patients with Atrial High-Rate Episodes. N Engl J Med 2023;389(13):1167-1179 «PMID: 37622677»PubMed
- Healey JS, Lopes RD, Granger CB, ym. Apixaban for Stroke Prevention in Subclinical Atrial Fibrillation. N Engl J Med 2024;390(2):107-117 «PMID: 37952132»PubMed
- Toni D, Lorenzano S, Strano S ym. Detection of Silent Atrial Fibrillation aFter Ischemic StrOke (SAFFO) guided by implantable loop recorder: multicentre Italian trial based on stroke unit network with paired cardio-arrhythmology units (Italian Neurocardiology Unit Network). Int J Stroke 2016;11:361-7 «PMID: 26873942»PubMed
- Aivoinfarkti ja TIA. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Neurologinen yhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2024 (viitattu 15.1.2025). Saatavilla internetissä: www.kaypahoito.fi
- Fung E, Järvelin MR, Doshi RN ym. Electrocardiographic patch devices and contemporary wireless cardiac monitoring. Front Physiol 2015;6:149 «PMID: 26074823»PubMed
- McNamara RL, Tamariz LJ, Segal JB ym. Management of atrial fibrillation: review of the evidence for the role of pharmacologic therapy, electrical cardioversion, and echocardiography. Ann Intern Med 2003;139:1018-33 «PMID: 14678922»PubMed
- Manning WJ, Weintraub RM, Waksmonski CA ym. Accuracy of transesophageal echocardiography for identifying left atrial thrombi. A prospective, intraoperative study. Ann Intern Med 1995;123:817-22 «PMID: 7486462»PubMed
- Saarela E, Koskela V, Strandberg M ym. Ruokatorven kautta tehtävä sydämen kaikukuvaus eteisvärinän rytminsiirrossa. Duodecim 2004;120:1575-81 «http://www.duodecimlehti.fi/web/guest/etusivu/artikkeli?tunnus=duo94376»8
- Camm AJ, Lip GY, De Caterina R ym. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: an update of the 2010 ESC Guidelines for the management of atrial fibrillation--developed with the special contribution of the European Heart Rhythm Association. Europace 2012;14:1385-413 «PMID: 22923145»PubMed
- Danias PG, Caulfield TA, Weigner MJ ym. Likelihood of spontaneous conversion of atrial fibrillation to sinus rhythm. J Am Coll Cardiol 1998;31:588-92 «PMID: 9502640»PubMed
- Dell'Orfano JT, Patel H, Wolbrette DL ym. Acute treatment of atrial fibrillation: spontaneous conversion rates and cost of care. Am J Cardiol 1999;83:788-90, A10 «PMID: 10080441»PubMed
- Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoito. Suom Lääkäril 2002;57:5029-36
- Hohnloser SH, Kuck KH, Lilienthal J. Rhythm or rate control in atrial fibrillation--Pharmacological Intervention in Atrial Fibrillation (PIAF): a randomised trial. Lancet 2000;356:1789-94 «PMID: 11117910»PubMed
- Wyse DG, Waldo AL, DiMarco JP ym. A comparison of rate control and rhythm control in patients with atrial fibrillation. N Engl J Med 2002;347:1825-33 «PMID: 12466506»PubMed
- Van Gelder IC, Hagens VE, Bosker HA ym. A comparison of rate control and rhythm control in patients with recurrent persistent atrial fibrillation. N Engl J Med 2002;347:1834-40 «PMID: 12466507»PubMed
- Carlsson J, Miketic S, Windeler J ym. Randomized trial of rate-control versus rhythm-control in persistent atrial fibrillation: the Strategies of Treatment of Atrial Fibrillation (STAF) study. J Am Coll Cardiol 2003;41:1690-6 «PMID: 12767648»PubMed
- Opolski G, Torbicki A, Kosior DA ym. Rate control vs rhythm control in patients with nonvalvular persistent atrial fibrillation: the results of the Polish How to Treat Chronic Atrial Fibrillation (HOT CAFE) Study. Chest 2004;126:476-86 «PMID: 15302734»PubMed
- Roy D, Talajic M, Nattel S ym. Rhythm control versus rate control for atrial fibrillation and heart failure. N Engl J Med 2008;358:2667-77 «PMID: 18565859»PubMed
- Kohonnut verenpaine. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Verenpaineyhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2020 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Sydämen vajaatoiminta. Käypä hoito -suositus. Suomalaisen Lääkäriseura Duodecimin ja Suomen Kardiologisen Seuran asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2023 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Tyypin 2 diabetes. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Sisätautilääkärien yhdistyksen ja Diabetesliiton Lääkärineuvoston asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2024 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Lihavuus (lapset, nuoret ja aikuiset). Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Lihavuustutkijat ry:n ja Suomen Lastenlääkäriyhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2024 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Uniapnea (obstruktiivinen uniapnea aikuisilla). Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Keuhkolääkäriyhdistyksen ja Suomen Unitutkimusseura ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2022 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Yleislääketieteen yhdistyksen asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2024 (viitattu 15.1.2025). Saatavilla internetissä: www.kaypahoito.fi
- Segal JB, McNamara RL, Miller MR ym. The evidence regarding the drugs used for ventricular rate control. J Fam Pract 2000;49:47-59 «PMID: 10678340»PubMed
- Snow V, Weiss KB, LeFevre M ym. Management of newly detected atrial fibrillation: a clinical practice guideline from the American Academy of Family Physicians and the American College of Physicians. Ann Intern Med 2003;139:1009-17 «PMID: 14678921»PubMed
- Grönefeld GC, Hohnloser SH. Beta-blocker therapy in atrial fibrillation. Pacing Clin Electrophysiol 2003;26:1607-12 «PMID: 12914610»PubMed
- Singh BN. Antiarrhythmic actions of amiodarone: a profile of a paradoxical agent. Am J Cardiol 1996;78:41-53 «PMID: 8780328»PubMed
- Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiriöiden hoidossa. Duodecim 1998;114:1923-36 «http://www.duodecimlehti.fi/web/guest/etusivu/artikkeli?tunnus=duo80400»9
- Clemo HF, Wood MA, Gilligan DM ym. Intravenous amiodarone for acute heart rate control in the critically ill patient with atrial tachyarrhythmias. Am J Cardiol 1998;81:594-8 «PMID: 9514456»PubMed
- Page RL, Hamad B, Kirkpatrick P. Dronedarone. Nat Rev Drug Discov 2009;8:769-70 «PMID: 19794441»PubMed
- Hoy SM, Keam SJ. Dronedarone. Drugs 2009;69:1647-63 «PMID: 19678715»PubMed
- Murray KT. Ibutilide. Circulation 1998;97:493-7 «PMID: 9490245»PubMed
- Cheng JW. Vernakalant in the management of atrial fibrillation. Ann Pharmacother 2008;42:533-42 «PMID: 18334607»PubMed
- Nagarakanti R, Ezekowitz MD, Oldgren J ym. Dabigatran versus warfarin in patients with atrial fibrillation: an analysis of patients undergoing cardioversion. Circulation 2011;123:131-6 «PMID: 21200007»PubMed
- Piccini JP, Stevens SR, Lokhnygina Y ym. Outcomes after cardioversion and atrial fibrillation ablation in patients treated with rivaroxaban and warfarin in the ROCKET AF trial. J Am Coll Cardiol 2013;61:1998-2006 «PMID: 23500298»PubMed
- Flaker G, Lopes RD, Al-Khatib SM ym. Efficacy and safety of apixaban in patients after cardioversion for atrial fibrillation: insights from the ARISTOTLE Trial (Apixaban for Reduction in Stroke and Other Thromboembolic Events in Atrial Fibrillation). J Am Coll Cardiol 2014;63:1082-7 «PMID: 24211508»PubMed
- Cappato R, Ezekowitz MD, Klein AL ym. Rivaroxaban vs. vitamin K antagonists for cardioversion in atrial fibrillation. Eur Heart J 2014;35:3346-55 «PMID: 25182247»PubMed
- Caldeira D, Costa J, Ferreira JJ ym. Non-vitamin K antagonist oral anticoagulants in the cardioversion of patients with atrial fibrillation: systematic review and meta-analysis. Clin Res Cardiol 2015;104:582-90 «PMID: 25643952»PubMed
- Schmidt AS, Lauridsen KG, Torp P ym. Maximum-fixed energy shocks for cardioverting atrial fibrillation. Eur Heart J 2020;41:626-631 «PMID: 31504412»PubMed
- Oral H, Souza JJ, Michaud GF ym. Facilitating transthoracic cardioversion of atrial fibrillation with ibutilide pretreatment. N Engl J Med 1999;340:1849-54 «PMID: 10369847»PubMed
- Marcus GM, Sung RJ. Antiarrhythmic agents in facilitating electrical cardioversion of atrial fibrillation and promoting maintenance of sinus rhythm. Cardiology 2001;95:1-8 «PMID: 11385184»PubMed
- Van Noord T, Van Gelder IC, Crijns HJ. How to enhance acute outcome of electrical cardioversion by drug therapy: importance of immediate reinitiation of atrial fibrillation. J Cardiovasc Electrophysiol 2002;13:822-5 «PMID: 12212706»PubMed
- Crozier I. Flecainide in the Wolff-Parkinson-White syndrome. Am J Cardiol 1992;70:26A-32A «PMID: 1509995»PubMed
- Raatikainen MJP, Sigurd B. Atrial fibrillation - the role of flecainide. Oy Sevenprint Ltd, Rovaniemi 2008
- Capucci A, Villani GQ, Aschieri D ym. Safety of oral propafenone in the conversion of recent onset atrial fibrillation to sinus rhythm: a prospective parallel placebo-controlled multicentre study. Int J Cardiol 1999;68:187-96 «PMID: 10189007»PubMed
- Aliot E, De Roy L, Capucci A ym. Safety of a controlled-release flecainide acetate formulation in the prevention of paroxysmal atrial fibrillation in outpatients. Ann Cardiol Angeiol (Paris) 2003;52:34-40 «PMID: 12710293»PubMed
- Kishore AG, Camm AJ. Guidelines for the use of propafenone in treating supraventricular arrhythmias. Drugs 1995;50:250-62 «PMID: 8521758»PubMed
- Naccarelli GV, Wolbrette DL, Samii S ym. Vernakalant--a promising therapy for conversion of recent-onset atrial fibrillation. Expert Opin Investig Drugs 2008;17:805-10 «PMID: 18447605»PubMed
- Roy D, Pratt CM, Torp-Pedersen C ym. Vernakalant hydrochloride for rapid conversion of atrial fibrillation: a phase 3, randomized, placebo-controlled trial. Circulation 2008;117:1518-25 «PMID: 18332267»PubMed
- Kowey PR, Dorian P, Mitchell LB ym. Vernakalant hydrochloride for the rapid conversion of atrial fibrillation after cardiac surgery: a randomized, double-blind, placebo-controlled trial. Circ Arrhythm Electrophysiol 2009;2:652-9 «PMID: 19948506»PubMed
- Raatikainen MJ, Lindgren K. Uusien ryhmän III lääkkeiden asema rytmihäiriöiden hoidossa. Suom Lääkäril 2001;56:5101-6
- Raatikainen MJ. Is verapamil a double-edged sword in rate control of paroxysmal atrial fibrillation? Heart Rhythm 2010;7:584-5 «PMID: 20189494»PubMed
- Alboni P, Botto GL, Baldi N ym. Outpatient treatment of recent-onset atrial fibrillation with the "pill-in-the-pocket" approach. N Engl J Med 2004;351:2384-91 «PMID: 15575054»PubMed
- Airaksinen KE, Grönberg T, Nuotio I ym. Thromboembolic complications after cardioversion of acute atrial fibrillation: the FinCV (Finnish CardioVersion) study. J Am Coll Cardiol 2013;62:1187-92 «PMID: 23850908»PubMed
- European Heart Rhythm Association., European Association for Cardio-Thoracic Surgery., Camm AJ ym. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010;31:2369-429 «PMID: 20802247»PubMed
- Steffel J, Verhamme P, Potpara TS ym. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J 2018;39:1330-1393 «PMID: 29562325»PubMed
- Bjerkelund CJ, Orning OM. The efficacy of anticoagulant therapy in preventing embolism related to D.C. electrical conversion of atrial fibrillation. Am J Cardiol 1969;23:208-16 «PMID: 4180019»PubMed
- Arnold AZ, Mick MJ, Mazurek RP ym. Role of prophylactic anticoagulation for direct current cardioversion in patients with atrial fibrillation or atrial flutter. J Am Coll Cardiol 1992;19:851-5 «PMID: 1545081»PubMed
- Thibault B, Talajic M, Dubuc M ym. Thromboembolic events occur despite sinus rhythm maintenance in patients treated for atrial fibrillation: The Canadian Trial of Atrial Fibrillation experience. Can J Cardiol 2004;20:195-9 «PMID: 15010743»PubMed
- Biblo LA, Yuan Z, Quan KJ ym. Risk of stroke in patients with atrial flutter. Am J Cardiol 2001;87:346-9, A9 «PMID: 11165976»PubMed
- Corrado G, Santarone M, Beretta S ym. Early cardioversion of atrial fibrillation and atrial flutter guided by transoesophageal echocardiography: a single centre 8.5-year experience. Europace 2000;2:119-26 «PMID: 11225938»PubMed
- Klein AL, Grimm RA, Murray RD ym. Use of transesophageal echocardiography to guide cardioversion in patients with atrial fibrillation. N Engl J Med 2001;344:1411-20 «PMID: 11346805»PubMed
- Weigner MJ, Thomas LR, Patel U ym. Early cardioversion of atrial fibrillation facilitated by transesophageal echocardiography: short-term safety and impact on maintenance of sinus rhythm at 1 year. Am J Med 2001;110:694-702 «PMID: 11403753»PubMed
- Roijer A, Eskilsson J, Olsson B. Transoesophageal echocardiography-guided cardioversion of atrial fibrillation or flutter. Selection of a low-risk group for immediate cardioversion. Eur Heart J 2000;21:837-47 «PMID: 10781356»PubMed
- Bartel T, Erbel R, Acute Trial Investigators.. Transoesophageal echocardiography for immediate and safe cardioversion in patients with atrial fibrillation. Eur Heart J 2001;22:2041-4 «PMID: 11686658»PubMed
- Klein AL, Murray RD, Grimm RA. Role of transesophageal echocardiography-guided cardioversion of patients with atrial fibrillation. J Am Coll Cardiol 2001;37:691-704 «PMID: 11693739»PubMed
- Seto TB, Taira DA, Tsevat J ym. Cost-effectiveness of transesophageal echocardiographic-guided cardioversion: a decision analytic model for patients admitted to the hospital with atrial fibrillation. J Am Coll Cardiol 1997;29:122-30 «PMID: 8996304»PubMed
- Klein AL, Murray RD, Becker ER ym. Economic analysis of a transesophageal echocardiography-guided approach to cardioversion of patients with atrial fibrillation: the ACUTE economic data at eight weeks. J Am Coll Cardiol 2004;43:1217-24 «PMID: 15063433»PubMed
- Lévy S, Breithardt G, Campbell RW ym. Atrial fibrillation: current knowledge and recommendations for management. Working Group on Arrhythmias of the European Society of Cardiology. Eur Heart J 1998;19:1294-320 «PMID: 9792255»PubMed
- Kirchhof P, Camm AJ, Goette A ym. Early Rhythm-Control Therapy in Patients with Atrial Fibrillation. N Engl J Med 2020;383:1305-1316 «PMID: 32865375»PubMed
- Kirchhof P, Andresen D, Bosch R ym. Short-term versus long-term antiarrhythmic drug treatment after cardioversion of atrial fibrillation (Flec-SL): a prospective, randomised, open-label, blinded endpoint assessment trial. Lancet 2012;380:238-46 «PMID: 22713626»PubMed
- Raatikainen MJ. Rytmihäiriölääkkeiden kliininen käyttö. Kirjassa: Heikkilä J ym. (toim). Kardiologia. Kustannus Oy Duodecim, 2008; 2:s. 692-711
- Van Noord T, Tieleman RG, Bosker HA ym. Beta-blockers prevent subacute recurrences of persistent atrial fibrillation only in patients with hypertension. Europace 2004;6:343-50 «PMID: 15172659»PubMed
- Meng F, Yoshikawa T, Baba A ym. Beta-blockers are effective in congestive heart failure patients with atrial fibrillation. J Card Fail 2003;9:398-403 «PMID: 14583902»PubMed
- Kühlkamp V, Bosch R, Mewis C ym. Use of beta-blockers in atrial fibrillation. Am J Cardiovasc Drugs 2002;2:37-42 «PMID: 14727997»PubMed
- Page RL, Reiffel JA, Tavel ME. Asymptomatic atrial fibrillation: problems of management. Chest 2001;119:628-31 «PMID: 11171747»PubMed
- Page RL. beta-blockers for atrial fibrillation: must we consider asymptomatic arrhythmias? J Am Coll Cardiol 2000;36:147-50 «PMID: 10898426»PubMed
- Naccarelli GV, Dorian P, Hohnloser SH ym. Prospective comparison of flecainide versus quinidine for the treatment of paroxysmal atrial fibrillation/flutter. The Flecainide Multicenter Atrial Fibrillation Study Group. Am J Cardiol 1996;77:53A-59A «PMID: 8607392»PubMed
- Lee SH, Chen SA, Chiang CE ym. Comparisons of oral propafenone and quinidine as an initial treatment option in patients with symptomatic paroxysmal atrial fibrillation: a double-blind, randomized trial. J Intern Med 1996;239:253-60 «PMID: 8772625»PubMed
- Grey E, Silverman DI. Efficacy of type 1C antiarrhythmic agents for treatment of resistant atrial fibrillation. Pacing Clin Electrophysiol 1993;16:2235-40 «PMID: 7508600»PubMed
- Echt DS, Liebson PR, Mitchell LB ym. Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial. N Engl J Med 1991;324:781-8 «PMID: 1900101»PubMed
- Hughes MM, Trohman RG, Simmons TW ym. Flecainide therapy in patients treated for supraventricular tachycardia with near normal left ventricular function. Am Heart J 1992;123:408-12 «PMID: 1736577»PubMed
- Chimienti M, Cullen MT Jr, Casadei G. Safety of long-term flecainide and propafenone in the management of patients with symptomatic paroxysmal atrial fibrillation: report from the Flecainide and Propafenone Italian Study Investigators. Am J Cardiol 1996;77:60A-75A «PMID: 8607393»PubMed
- Anderson JL, Platt ML, Guarnieri T ym. Flecainide acetate for paroxysmal supraventricular tachyarrhythmias. The Flecainide Supraventricular Tachycardia Study Group. Am J Cardiol 1994;74:578-84 «PMID: 8074041»PubMed
- Wehling M. Meta-analysis of flecainide safety in patients with supraventricular arrhythmias. Arzneimittelforschung 2002;52:507-14 «PMID: 12189773»PubMed
- Joglar JA, Chung MK, Armbruster AL, ym. 2023 ACC/AHA/ACCP/HRS Guideline for the Diagnosis and Management of Atrial Fibrillation: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation 2024;149(1):e1-e156 «PMID: 38033089»PubMed
- Le Heuzey JY, De Ferrari GM, Radzik D ym. A short-term, randomized, double-blind, parallel-group study to evaluate the efficacy and safety of dronedarone versus amiodarone in patients with persistent atrial fibrillation: the DIONYSOS study. J Cardiovasc Electrophysiol 2010;21:597-605 «PMID: 20384650»PubMed
- Roy D, Talajic M, Dorian P ym. Amiodarone to prevent recurrence of atrial fibrillation. Canadian Trial of Atrial Fibrillation Investigators. N Engl J Med 2000;342:913-20 «PMID: 10738049»PubMed
- Vitolo E, Tronci M, Larovere MT ym. Amiodarone versus quinidine in the prophylaxis of atrial fibrillation. Acta Cardiol 1981;36:431-44 «PMID: 7039195»PubMed
- Zarembski DG, Nolan PE Jr, Slack MK ym. Treatment of resistant atrial fibrillation. A meta-analysis comparing amiodarone and flecainide. Arch Intern Med 1995;155:1885-91 «PMID: 7677555»PubMed
- Singh BN. Amiodarone: the expanding antiarrhythmic role and how to follow a patient on chronic therapy. Clin Cardiol 1997;20:608-18 «PMID: 9220176»PubMed
- Siddoway LA. Amiodarone: guidelines for use and monitoring. Am Fam Physician 2003;68:2189-96 «PMID: 14677664»PubMed
- Connolly SJ. Evidence-based analysis of amiodarone efficacy and safety. Circulation 1999;100:2025-34 «PMID: 10556230»PubMed
- Hohnloser SH, Klingenheben T, Singh BN. Amiodarone-associated proarrhythmic effects. A review with special reference to torsade de pointes tachycardia. Ann Intern Med 1994;121:529-35 «PMID: 8067651»PubMed
- Julian DG, Camm AJ, Frangin G ym. Randomised trial of effect of amiodarone on mortality in patients with left-ventricular dysfunction after recent myocardial infarction: EMIAT. European Myocardial Infarct Amiodarone Trial Investigators. Lancet 1997;349:667-74 «PMID: 9078197»PubMed
- Cairns JA, Connolly SJ, Roberts R ym. Randomised trial of outcome after myocardial infarction in patients with frequent or repetitive ventricular premature depolarisations: CAMIAT. Canadian Amiodarone Myocardial Infarction Arrhythmia Trial Investigators. Lancet 1997;349:675-82 «PMID: 9078198»PubMed
- Doval HC, Nul DR, Grancelli HO ym. Randomised trial of low-dose amiodarone in severe congestive heart failure. Grupo de Estudio de la Sobrevida en la Insuficiencia Cardiaca en Argentina (GESICA) Lancet 1994;344:493-8 «PMID: 7914611»PubMed
- Deedwania PC, Singh BN, Ellenbogen K ym. Spontaneous conversion and maintenance of sinus rhythm by amiodarone in patients with heart failure and atrial fibrillation: observations from the veterans affairs congestive heart failure survival trial of antiarrhythmic therapy (CHF-STAT). The Department of Veterans Affairs CHF-STAT Investigators. Circulation 1998;98:2574-9 «PMID: 9843465»PubMed
- Piccini JP, Hasselblad V, Peterson ED ym. Comparative efficacy of dronedarone and amiodarone for the maintenance of sinus rhythm in patients with atrial fibrillation. J Am Coll Cardiol 2009;54:1089-95 «PMID: 19744618»PubMed
- Lafuente-Lafuente C, Mouly S, Longas-Tejero MA ym. Antiarrhythmics for maintaining sinus rhythm after cardioversion of atrial fibrillation. Cochrane Database Syst Rev 2007;4:CD005049 «PMID: 17943835»PubMed
- Freemantle N, Lafuente-Lafuente C, Mitchell S ym. Mixed treatment comparison of dronedarone, amiodarone, sotalol, flecainide, and propafenone, for the management of atrial fibrillation. Europace 2011;13:329-45 «PMID: 21227948»PubMed
- Køber L, Torp-Pedersen C, McMurray JJ ym. Increased mortality after dronedarone therapy for severe heart failure. N Engl J Med 2008;358:2678-87 «PMID: 18565860»PubMed
- Connolly SJ, Camm AJ, Halperin JL ym. Dronedarone in high-risk permanent atrial fibrillation. N Engl J Med 2011;365:2268-76 «PMID: 22082198»PubMed
- Juul-Möller S, Edvardsson N, Rehnqvist-Ahlberg N. Sotalol versus quinidine for the maintenance of sinus rhythm after direct current conversion of atrial fibrillation. Circulation 1990;82:1932-9 «PMID: 2242519»PubMed
- Bellandi F, Simonetti I, Leoncini M ym. Long-term efficacy and safety of propafenone and sotalol for the maintenance of sinus rhythm after conversion of recurrent symptomatic atrial fibrillation. Am J Cardiol 2001;88:640-5 «PMID: 11564387»PubMed
- Plewan A, Lehmann G, Ndrepepa G ym. Maintenance of sinus rhythm after electrical cardioversion of persistent atrial fibrillation; sotalol vs bisoprolol. Eur Heart J 2001;22:1504-10 «PMID: 11482924»PubMed
- Brendorp B, Pedersen O, Torp-Pedersen C ym. A benefit-risk assessment of class III antiarrhythmic agents. Drug Saf 2002;25:847-65 «PMID: 12241126»PubMed
- Coplen SE, Antman EM, Berlin JA ym. Efficacy and safety of quinidine therapy for maintenance of sinus rhythm after cardioversion. A meta-analysis of randomized control trials. Circulation 1990;82:1106-16 «PMID: 2144796»PubMed
- Patten M, Maas R, Bauer P ym. Suppression of paroxysmal atrial tachyarrhythmias--results of the SOPAT trial. Eur Heart J 2004;25:1395-404 «PMID: 15321697»PubMed
- Fetsch T, Bauer P, Engberding R ym. Prevention of atrial fibrillation after cardioversion: results of the PAFAC trial. Eur Heart J 2004;25:1385-94 «PMID: 15302102»PubMed
- Madrid AH, Peng J, Zamora J ym. The role of angiotensin receptor blockers and/or angiotensin converting enzyme inhibitors in the prevention of atrial fibrillation in patients with cardiovascular diseases: meta-analysis of randomized controlled clinical trials. Pacing Clin Electrophysiol 2004;27:1405-10 «PMID: 15511250»PubMed
- Savelieva I, Camm J. Statins and polyunsaturated fatty acids for treatment of atrial fibrillation. Nat Clin Pract Cardiovasc Med 2008;5:30-41 «PMID: 18094671»PubMed
- Kowey PR, Reiffel JA, Ellenbogen KA ym. Efficacy and safety of prescription omega-3 fatty acids for the prevention of recurrent symptomatic atrial fibrillation: a randomized controlled trial. JAMA 2010;304:2363-72 «PMID: 21078810»PubMed
- Schnabel RB, Yin X, Gona P ym. 50 year trends in atrial fibrillation prevalence, incidence, risk factors, and mortality in the Framingham Heart Study: a cohort study. Lancet 2015;386:154-62 «PMID: 25960110»PubMed
- Miller JD, Aronis KN, Chrispin J ym. Obesity, Exercise, Obstructive Sleep Apnea, and Modifiable Atherosclerotic Cardiovascular Disease Risk Factors in Atrial Fibrillation. J Am Coll Cardiol 2015;66:2899-906 «PMID: 26718677»PubMed
- Nalliah CJ, Sanders P, Kottkamp H ym. The role of obesity in atrial fibrillation. Eur Heart J 2016;37:1565-72 «PMID: 26371114»PubMed
- Cambeiro G, Cristina M, Mañero R ym. Review Of Obesity And Atrial Fibrillation: Exploring The Paradox. J Atr Fibrillation 2015;8:1259 «PMID: 27957191»PubMed
- Goudis CA, Korantzopoulos P, Ntalas IV ym. Obesity and atrial fibrillation: A comprehensive review of the pathophysiological mechanisms and links. J Cardiol 2015;66:361-9 «PMID: 25959929»PubMed
- Yao Y, Liu F, Wang Y, ym. Lipid levels and risk of new-onset atrial fibrillation: A systematic review and dose-response meta-analysis. Clin Cardiol 2020;43(9):935-943 «PMID: 32720403»PubMed
- Andersen HR, Nielsen JC, Thomsen PE ym. Long-term follow-up of patients from a randomised trial of atrial versus ventricular pacing for sick-sinus syndrome. Lancet 1997;350:1210-6 «PMID: 9652562»PubMed
- Kerr CR, Connolly SJ, Abdollah H ym. Canadian Trial of Physiological Pacing: Effects of physiological pacing during long-term follow-up. Circulation 2004;109:357-62 «PMID: 14707022»PubMed
- Nielsen JC, Kristensen L, Andersen HR ym. A randomized comparison of atrial and dual-chamber pacing in 177 consecutive patients with sick sinus syndrome: echocardiographic and clinical outcome. J Am Coll Cardiol 2003;42:614-23 «PMID: 12932590»PubMed
- Wijesuriya N, Mehta V, De Vere F, ym. The role of conduction system pacing in patients with atrial fibrillation. Front Cardiovasc Med 2023;10():1187754 «PMID: 37304966»PubMed
- Burns JL, Sears SF, Sotile R ym. Do patients accept implantable atrial defibrillation therapy? Results from the Patient Atrial Shock Survey of Acceptance and Tolerance (PASSAT) Study. J Cardiovasc Electrophysiol 2004;15:286-91 «PMID: 15030417»PubMed
- Boodhoo LE, Mitchell AR, Sulke N. The clinical and electrophysiological implications of asymptomatic atrial fibrillation. Minerva Cardioangiol 2004;52:547-52 «PMID: 15729215»PubMed
- Packer DL, Mark DB, Robb RA ym. Effect of Catheter Ablation vs Antiarrhythmic Drug Therapy on Mortality, Stroke, Bleeding, and Cardiac Arrest Among Patients With Atrial Fibrillation: The CABANA Randomized Clinical Trial. JAMA 2019;321:1261-1274 «PMID: 30874766»PubMed
- Sohns C, Fox H, Marrouche NF, ym. Catheter Ablation in End-Stage Heart Failure with Atrial Fibrillation. N Engl J Med 2023;389(15):1380-1389 «PMID: 37634135»PubMed
- Cosedis Nielsen J, Johannessen A, Raatikainen P ym. Radiofrequency ablation as initial therapy in paroxysmal atrial fibrillation. N Engl J Med 2012;367:1587-95 «PMID: 23094720»PubMed
- Hakalahti A, Biancari F, Nielsen JC ym. Radiofrequency ablation vs. antiarrhythmic drug therapy as first line treatment of symptomatic atrial fibrillation: systematic review and meta-analysis. Europace 2015;17:370-8 «PMID: 25643988»PubMed
- Mark DB, Anstrom KJ, Sheng S ym. Effect of Catheter Ablation vs Medical Therapy on Quality of Life Among Patients With Atrial Fibrillation: The CABANA Randomized Clinical Trial. JAMA 2019;321:1275-1285 «PMID: 30874716»PubMed
- Blomström-Lundqvist C, Gizurarson S, Schwieler J ym. Effect of Catheter Ablation vs Antiarrhythmic Medication on Quality of Life in Patients With Atrial Fibrillation: The CAPTAF Randomized Clinical Trial. JAMA 2019;321:1059-1068 «PMID: 30874754»PubMed
- Nielsen JC, Johannessen A, Raatikainen P ym. Long-term efficacy of catheter ablation as first-line therapy for paroxysmal atrial fibrillation: 5-year outcome in a randomised clinical trial. Heart 2017;103:368-376 «PMID: 27566295»PubMed
- Raatikainen MJ, Hakalahti A, Uusimaa P ym. Radiofrequency catheter ablation maintains its efficacy better than antiarrhythmic medication in patients with paroxysmal atrial fibrillation: On-treatment analysis of the randomized controlled MANTRA-PAF trial. Int J Cardiol 2015;198:108-14 «PMID: 26163901»PubMed
- Cappato R, Calkins H, Chen SA ym. Updated worldwide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation. Circ Arrhythm Electrophysiol 2010;3:32-8 «PMID: 19995881»PubMed
- Piccini JP, Lopes RD, Kong MH ym. Pulmonary vein isolation for the maintenance of sinus rhythm in patients with atrial fibrillation: a meta-analysis of randomized, controlled trials. Circ Arrhythm Electrophysiol 2009;2:626-33 «PMID: 20009077»PubMed
- Gjesdal K, Vist GE, Bugge E ym. Curative ablation for atrial fibrillation: a systematic review. Scand Cardiovasc J 2008;42:3-8 «PMID: 18273730»PubMed
- Calkins H, Reynolds MR, Spector P ym. Treatment of atrial fibrillation with antiarrhythmic drugs or radiofrequency ablation: two systematic literature reviews and meta-analyses. Circ Arrhythm Electrophysiol 2009;2:349-61 «PMID: 19808490»PubMed
- Schmidt M, Dorwarth U, Andresen D ym. Cryoballoon versus RF ablation in paroxysmal atrial fibrillation: results from the German Ablation Registry. J Cardiovasc Electrophysiol 2014;25:1-7 «PMID: 24134539»PubMed
- Reddy VY, Gerstenfeld EP, Natale A, ym. Pulsed Field or Conventional Thermal Ablation for Paroxysmal Atrial Fibrillation. N Engl J Med 2023;389(18):1660-1671 «PMID: 37634148»PubMed
- Weerasooriya R, Jaïs P, Le Heuzey JY ym. Cost analysis of catheter ablation for paroxysmal atrial fibrillation. Pacing Clin Electrophysiol 2003;26:292-4 «PMID: 12687831»PubMed
- Andrikopoulos G, Tzeis S, Maniadakis N ym. Cost-effectiveness of atrial fibrillation catheter ablation. Europace 2009;11:147-51 «PMID: 19098290»PubMed
- Aronsson M, Walfridsson H, Janzon M ym. The cost-effectiveness of radiofrequency catheter ablation as first-line treatment for paroxysmal atrial fibrillation: results from a MANTRA-PAF substudy. Europace 2015;17:48-55 «PMID: 25341739»PubMed
- Spragg DD, Dalal D, Cheema A ym. Complications of catheter ablation for atrial fibrillation: incidence and predictors. J Cardiovasc Electrophysiol 2008;19:627-31 «PMID: 18462327»PubMed
- Blomström-Lundqvist C, Scheinman MM, Aliot EM ym. ACC/AHA/ESC guidelines for the management of patients with supraventricular arrhythmias--executive summary. a report of the American college of cardiology/American heart association task force on practice guidelines and the European society of cardiology committee for practice guidelines (writing committee to develop guidelines for the management of patients with supraventricular arrhythmias) developed in collaboration with NASPE-Heart Rhythm Society. J Am Coll Cardiol 2003;42:1493-531 «PMID: 14563598»PubMed
- Nabar A, Rodriguez LM, Timmermans C ym. Effect of right atrial isthmus ablation on the occurrence of atrial fibrillation: observations in four patient groups having type I atrial flutter with or without associated atrial fibrillation. Circulation 1999;99:1441-5 «PMID: 10086967»PubMed
- Ahvenvaara T, Uusimaa P, Huikuri HV, Raatikainen MJP. Eteislepatuksen katetriablaatiohoito. Suom Lääkäril 2004;59:2355-61
- Prasad SM, Maniar HS, Camillo CJ ym. The Cox maze III procedure for atrial fibrillation: long-term efficacy in patients undergoing lone versus concomitant procedures. J Thorac Cardiovasc Surg 2003;126:1822-8 «PMID: 14688693»PubMed
- Cox JL. Cardiac surgery for arrhythmias. J Cardiovasc Electrophysiol 2004;15:250-62 PMID: 15028063
- McLellan CS, Abdollah H, Brennan FJ ym. Atrial fibrillation in the pacemaker clinic. Can J Cardiol 2003;19:492-4 «PMID: 12717483»PubMed
- Boersma LV, Castella M, van Boven W ym. Atrial fibrillation catheter ablation versus surgical ablation treatment (FAST): a 2-center randomized clinical trial. Circulation 2012;125:23-30 «PMID: 22082673»PubMed
- Sethi NJ, Nielsen EE, Safi S ym. Digoxin for atrial fibrillation and atrial flutter: A systematic review with meta-analysis and trial sequential analysis of randomised clinical trials. PLoS One 2018;13:e0193924 «PMID: 29518134»PubMed
- Castellá M, Pereda D, Mestres CA ym. Thoracoscopic pulmonary vein isolation in patients with atrial fibrillation and failed percutaneous ablation. J Thorac Cardiovasc Surg 2010;140:633-8 «PMID: 20117799»PubMed
- Levy T, Walker S, Mason M ym. Importance of rate control or rate regulation for improving exercise capacity and quality of life in patients with permanent atrial fibrillation and normal left ventricular function: a randomised controlled study. Heart 2001;85:171-8 «PMID: 11156667»PubMed
- Van Gelder IC, Van Veldhuisen DJ, Crijns HJ ym. RAte Control Efficacy in permanent atrial fibrillation: a comparison between lenient versus strict rate control in patients with and without heart failure. Background, aims, and design of RACE II. Am Heart J 2006;152:420-6 «PMID: 16923407»PubMed
- Olshansky B, Rosenfeld LE, Warner AL ym. The Atrial Fibrillation Follow-up Investigation of Rhythm Management (AFFIRM) study: approaches to control rate in atrial fibrillation. J Am Coll Cardiol 2004;43:1201-8 «PMID: 15063430»PubMed
- Leclercq JF, Rosengarten MD, Kural S ym. Effects of intrinsic sympathetic activity of beta-blockers on SA and AV nodes in man. Eur J Cardiol 1981;12:367-75 «PMID: 6113145»PubMed
- Al-Khateeb M, Qureshi WT, Odeh R ym. The impact of digoxin on mortality in patients with chronic systolic heart failure: A propensity-matched cohort study. Int J Cardiol 2017;228:214-218 «PMID: 27865188»PubMed
- Wang ZQ, Zhang R, Chen MT ym. Digoxin Is Associated With Increased All-cause Mortality in Patients With Atrial Fibrillation Regardless of Concomitant Heart Failure: A Meta-analysis. J Cardiovasc Pharmacol 2015;66:270-5 «PMID: 26348825»PubMed
- Vijayaraman P, Chung MK, Dandamudi G ym. His Bundle Pacing. J Am Coll Cardiol 2018;72:927-947 «PMID: 30115232»PubMed
- Chao TF, Liu CJ, Tuan TC ym. Rate-control treatment and mortality in atrial fibrillation. Circulation 2015;132:1604-12 «PMID: 26384160»PubMed
- Gheorghiade M, Fonarow GC, van Veldhuisen DJ ym. Lack of evidence of increased mortality among patients with atrial fibrillation taking digoxin: findings from post hoc propensity-matched analysis of the AFFIRM trial. Eur Heart J 2013;34:1489-97 «PMID: 23592708»PubMed
- Davy JM, Herold M, Hoglund C ym. Dronedarone for the control of ventricular rate in permanent atrial fibrillation: the Efficacy and safety of dRonedArone for the cOntrol of ventricular rate during atrial fibrillation (ERATO) study. Am Heart J 2008;156:527.e1-9 «PMID: 18760136»PubMed
- Singh BN, Connolly SJ, Crijns HJ ym. Dronedarone for maintenance of sinus rhythm in atrial fibrillation or flutter. N Engl J Med 2007;357:987-99 «PMID: 17804843»PubMed
- Aliot E ym. Catheter ablation or modulation of the atrioventricular node. Kirjassa: Zipes DP, Haissaguerre M (toim.). Armonk: Futura Publishing Company, Inc., 2002; s. 205-23
- Nowinski K, Gadler F, Jensen-Urstad M ym. Transient proarrhythmic state following atrioventricular junctional radiofrequency ablation. Pacing Clin Electrophysiol 2002;25:291-9 «PMID: 11990658»PubMed
- Wood KA, Eisenberg SJ, Kalman JM ym. Risk of thromboembolism in chronic atrial flutter. Am J Cardiol 1997;79:1043-7 «PMID: 9114761»PubMed
- Cairns JA. Stroke prevention in atrial fibrillation trial. Circulation 1991;84:933-5 «PMID: 1860238»PubMed
- Pollack CV Jr, Reilly PA, Eikelboom J ym. Idarucizumab for Dabigatran Reversal. N Engl J Med 2015;373:511-20 «PMID: 26095746»PubMed
- Connolly SJ, Crowther M, Eikelboom JW ym. Full Study Report of Andexanet Alfa for Bleeding Associated with Factor Xa Inhibitors. N Engl J Med 2019;380:1326-1335 «PMID: 30730782»PubMed
- Siegal DM, Curnutte JT, Connolly SJ ym. Andexanet Alfa for the Reversal of Factor Xa Inhibitor Activity. N Engl J Med 2015;373:2413-24 «PMID: 26559317»PubMed
- Raatikainen MJP. Oraalinen antikoagulaatiohoito sydänsairauksissa. Suom Lääkäril 2019:74:443-8
- Connolly SJ, Ezekowitz MD, Yusuf S ym. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009;361:1139-51 «PMID: 19717844»PubMed
- Granger CB, Alexander JH, McMurray JJ ym. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2011;365:981-92 «PMID: 21870978»PubMed
- Giugliano RP, Ruff CT, Braunwald E ym. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2013;369:2093-104 «PMID: 24251359»PubMed
- Bohula EA, Giugliano RP, Ruff CT ym. Impact of Renal Function on Outcomes With Edoxaban in the ENGAGE AF-TIMI 48 Trial. Circulation 2016;134:24-36 «PMID: 27358434»PubMed
- Patel MR, Mahaffey KW, Garg J ym. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med 2011;365:883-91 «PMID: 21830957»PubMed
- Lehto M, Luojus A, Halminen O, ym. Time-in-therapeutic-range defined warfarin and direct oral anticoagulants in atrial fibrillation: a Nationwide Cohort Study. Ann Med 2024;56(1):2364825 «PMID: 38873855»PubMed
- Nilsson GH, Björholt I, Krakau I. Anticoagulant treatment of patients with chronic atrial fibrillation in primary health care in Sweden--a retrospective study of incidence and quality in a registered population. Fam Pract 2004;21:612-6 «PMID: 15465879»PubMed
- Connolly SJ, Eikelboom J, Joyner C ym. Apixaban in patients with atrial fibrillation. N Engl J Med 2011;364:806-17 «PMID: 21309657»PubMed
- Zalesak M, Siu K, Francis K ym. Higher persistence in newly diagnosed nonvalvular atrial fibrillation patients treated with dabigatran versus warfarin. Circ Cardiovasc Qual Outcomes 2013;6:567-74 «PMID: 23922182»PubMed
- Gorst-Rasmussen A, Skjøth F, Larsen TB ym. Dabigatran adherence in atrial fibrillation patients during the first year after diagnosis: a nationwide cohort study. J Thromb Haemost 2015;13:495-504 «PMID: 25594442»PubMed
- Joosten LPT, van Doorn S, van de Ven PM, ym. Safety of Switching From a Vitamin K Antagonist to a Non-Vitamin K Antagonist Oral Anticoagulant in Frail Older Patients With Atrial Fibrillation: Results of the FRAIL-AF Randomized Controlled Trial. Circulation 2024;149(4):279-289 «PMID: 37634130»PubMed
- Aryana A, Singh SK, Singh SM ym. Association between incomplete surgical ligation of left atrial appendage and stroke and systemic embolization. Heart Rhythm 2015;12:1431-7 «PMID: 25998141»PubMed
- Whitlock RP, Belley-Cote EP, Paparella D, ym. Left Atrial Appendage Occlusion during Cardiac Surgery to Prevent Stroke. N Engl J Med 2021;384(22):2081-2091 «PMID: 33999547»PubMed

