Atooppinen ekseema
Miten viitata Käypä hoito -suositukseen? «K1»1
Keskeinen sisältö
- Atooppinen ekseema on krooninen ja kutiseva tulehduksellinen ihotauti, jolle tyypillisiä ovat vaikeasti ennustettavat pahenemisvaiheet. Atooppista ekseemaa sairastavat kokevat usein myös ihon kipua ja kosketusarkuutta.
- Atooppisessa ekseemassa ihon läpäisyesteen toiminta on heikompaa kuin terveessä ihossa.
- Atooppisessa ekseemassa voidaan erottaa useita ilmiasuja (fenotyyppejä) taustalla olevien geneettisten tekijöiden, esimerkiksi potilaan etnisen taustan, ja tulehdusmekanismien mukaan. Taudin kliininen kuva ja tulehdusvaste muuttuvat iän myötä.
- Diagnoosi on kliininen, joten laboratorio- tai allergiatutkimukset eivät yleensä ole
tarpeen.
- Osalla alle vuoden ikäisistä keskivaikeaa tai vaikeaa ekseemaa sairastavista lapsista voi taustalla olla ruoka-allergia. Muissa potilasryhmissä ruoka-allergiaa ei yleensä tarvitse etsiä.
- Atooppisen ekseeman ehkäisyyn ei tunneta kiistattomia keinoja.
- Suurimmalla osalla sairaus on lievä ja sen ennuste hyvä. Vaikea atooppinen ekseema heikentää elämänlaatua ja työ- ja toimintakykyä.
- Hoidon tavoitteena on pitkäkestoinen oireiden hallinta: oireiden minimointi, pahenemisvaiheiden
määrän väheneminen ja vaikeusasteen lieveneminen sekä potilaan elämänlaadun ja työ-
ja toimintakyvyn paraneminen.
- Ekseeman vaikeusasteen arviointiin ja sairauden elämänlaatuvaikutuksen mittaamiseen voidaan käyttää validoituja mittareita. Erityisesti erikoissairaanhoidossa sairauden vaikeusastetta ja vaikutuksia kuvaavien mittareiden käyttö on suositeltavaa myös hoitovasteen seurannassa.
- Atooppisen ekseeman vaikeusaste vaikuttaa hoidon valintaan, ja ihottuman asianmukainen
hoito lievittää parhaiten kutinaa. Ks. hoitoalgoritmi «Atooppisen ekseeman hoitoalgoritmi»1.
- Perusvoiteilla hoidetaan atooppiseen ekseemaan liittyvää ihon kuivuutta. Ihon tulehdusta
(inflammaatiota) hoidetaan lääkevoiteilla ja tarvittaessa systeemisellä lääkehoidolla
tai UV-hoidolla.
- Useimmat potilaat pärjäävät perusvoiteilla ja ajoittaisella paikalliskortikosteroidien käytöllä.
- Ellei oikein käytetyillä paikalliskortikosteroideilla saada aikaan riittävää vastetta, käytetään paikallisia kalsineuriinin estäjiä pitkäaikaishoitona tai UV-hoitoa.
- Herkästi uusivassa ihottumassa suositellaan ylläpitohoitoa kortikosteroidivoiteella tai takrolimuusivoiteella kahdesti viikossa.
- Huomioi ikärajat ja kortikosteroidivoiteiden erilainen vahvuus hoitaessasi lapsia.
- Vaikeassa taudissa tarvitaan usein pitkäaikaista systeemistä lääkehoitoa, joka voidaan
toteuttaa perinteisillä immunosuppressiivisilla lääkkeillä, biologisilla lääkkeillä
tai januskinaasin (JAK) estäjillä.
- Biologisten lääkkeiden ja JAK-estäjien hoitovasteen lääkekustannukset on esitetty taulukossa, ks. «https://www.terveysportti.fi/apps/laake/laakekustannus/hoi50077»1.
- Perusvoiteilla hoidetaan atooppiseen ekseemaan liittyvää ihon kuivuutta. Ihon tulehdusta
(inflammaatiota) hoidetaan lääkevoiteilla ja tarvittaessa systeemisellä lääkehoidolla
tai UV-hoidolla.
- Atooppisen ekseeman hoidon onnistumisen edellytys on potilaiden ja lapsipotilaiden
vanhempien riittävä tieto atooppisesta ekseemasta ja sen hoidosta.
- Ohje vanhemmille atooppisesta ekseemasta «Ohje vanhemmille atooppisesta ekseemasta»1
- Perusvoiteiden säännöllinen käyttö, ihoa ärsyttävien tekijöiden välttäminen ja lääkevoiteiden
käyttö aktiivisen ekseeman aikana ovat omahoidon kulmakiviä.
- Atooppisen ekseeman ohjattu omahoito aikuisilla «hoi50077c.pdf»1
- Atooppisen ekseeman ohjattu omahoito lapsilla «hoi50077d.pdf»2
- Videot: Aikuisten «Atooppinen ekseema -suosituksen videot (aikuiset)»2 ja lasten «Atooppinen ekseema -suosituksen videot (lapset)»3 atooppisen ekseeman paikallishoidosta
- Atooppisen ekseeman liitännäissairauksien ja monimuotoisen tautitaakan vuoksi voidaan tarvita moniammatillista hoito-otetta.
- Erikoislääkärin konsultaatiota tarvitaan, jos sairaus on laaja-alainen tai vaikeahoitoinen.
Tiivistelmä ja potilasversio
- Suosituksen tiivistelmä «Atooppinen ekseema»1
- Suosituksen yleiskielinen potilasversio suomeksi «Atooppinen ihottuma (atooppinen ekseema)»2 ja ruotsiksi «Atopiskt eksem (atopisk dermatit)»3
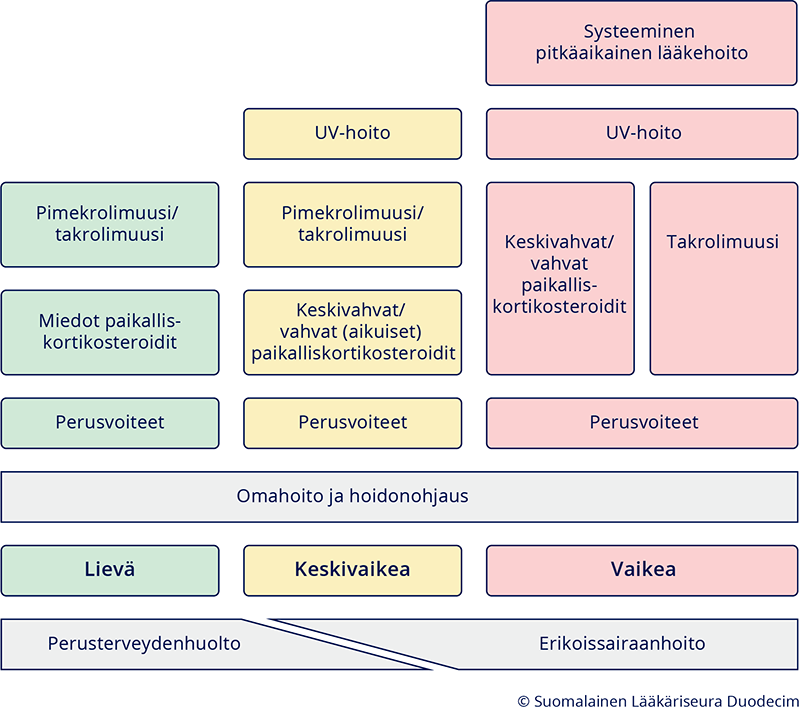
Atooppisen ekseeman hoitoalgoritmi
Hoidossa käytetään perusvoiteita, erivahvuisia kortikosteroidivoiteita, kalsineuriinin salpaajia ja UV-hoitoa ihottuman vaikeusasteen mukaan. Vaikeassa ekseemassa saatetaan tarvita sisäisiä lääkehoitoja.
© Suomalainen Lääkäriseura Duodecim
Suosituksen tavoitteet
- Suosituksen tavoitteena on luoda yhtenäiset käytännöt atooppisen ekseeman diagnostiikkaan ja hoitoon sekä selkeyttää diagnostiikan ja hoidon porrastusta. Tavoitteena on, että atooppisen ekseeman hoito perustuu tutkimusnäyttöön, on yhdenvertaista ja toteutuu onnistuneesti.
Kohderyhmä
- Suosituksen kohderyhmänä ovat atooppista ekseemaa sairastavia hoitavat terveydenhuollon ammattihenkilöt.
Määritelmä
- Atooppinen ekseema (atooppinen ihottuma, atooppinen dermatiitti, taiveihottuma, "maitorupi") on krooninen ja kutiseva tulehduksellinen ihotauti, jolle tyypillisiä ovat vaikeasti ennustettavat pahenemisvaiheet.
- Atooppista ekseemaa sairastavan iho on yleensä kuiva, vaikka ihottumaa ei aina ole havaittavissa. Ihosta voidaan tällöin käyttää nimitystä atooppinen iho.
- Noin 20–30 prosentilla atooppista ekseemaa sairastavista ei ole atooppista allergiataipumusta eli IgE-välitteisiä allergioita tai herkistymistä tavallisimmille allergeeneille «Tokura Y, Hayano S. Subtypes of atopic dermatitis:...»1, «Johansson EK, Bergström A, Kull I ym. Prevalence a...»2.
Esiintyvyys ja ennuste
- Atooppisen ekseeman vallitsevuus lapsilla on 10–20 % «Williams H, Stewart A, von Mutius E ym. Is eczema ...»3. Kansainvälisessä, standardoidussa allergisten sairauksien esiintyvyyttä selvittäneessä tutkimuksessa 13–14-vuotiaista lapsista 24 %:lla oli joskus ollut atooppista ekseemaa, 17 %:lla oli ollut viimeisen vuoden aikana ekseemaa ja 0,9 %:lla oli ollut viimeisen vuoden aikana vaikeaa ekseemaa «Williams H, Stewart A, von Mutius E ym. Is eczema ...»3. Eurooppalaisessa syntymäkohorttitutkimuksessa, jossa oli mukana myös suomalaisia lapsia, atooppisen ekseeman vallitsevuus 4 vuoden iässä oli 27 % «Roduit C, Frei R, Loss G ym. Development of atopic...»4. Lapsuudessa puhkeava atooppinen ekseema alkaa oireilla puolella potilaista ensimmäisen ikävuoden aikana ja 85 %:lla viidenteen ikävuoteen mennessä «Vakharia PP, Silverberg JI. Adult-Onset Atopic Der...»5.
- Aikuisista atooppista ekseemaa on joskus elämänsä aikana sairastanut 25–30 %, ja noin puolella heistä ekseemaa oli esiintynyt edeltävän vuoden aikana «Vartiainen E, Petäys T, Haahtela T ym. Allergic di...»6, «von Hertzen L, Mäkelä MJ, Petäys T ym. Growing dis...»7, «Mortz CG, Andersen KE, Dellgren C ym. Atopic derma...»8. Aikuisilla atooppisen ekseeman vallitsevuus eri tutkimuksissa on 2–10 % «Silverberg JI, Hanifin JM. Adult eczema prevalence...»9, «Barbarot S, Auziere S, Gadkari A ym. Epidemiology ...»10. Suomalaisessa syntymäkohorttiaineistossa atooppinen ekseema todettiin tutkimushetkellä 4,8 %:lla keski-ikäisistä aikuisista «Sinikumpu SP, Huilaja L, Jokelainen J ym. High pre...»11. Joka neljäs aikuinen atooppista ekseemaa sairastava potilas ilmoitti ihottuman alkaneen vasta aikuisiässä «Lee HH, Patel KR, Singam V ym. A systematic review...»12.
- Atooppista ekseemaa sairastavista noin 10 %:lla arvioidaan olevan vaikea tautimuoto. Lapsilla vaikea tautimuoto on harvinaisempi «Langan SM, Irvine AD, Weidinger S. Atopic dermatit...»13, «Barbarot S, Auziere S, Gadkari A ym. Epidemiology ...»10.
- Atooppinen ekseema on yleistynyt viime vuosikymmeninä kuten muutkin atooppiseen ekseemaan liittyvät sairaudet (astma, allerginen nuha) ja IgE-välitteinen allergia. Suomalaisessa varusmiehillä tehdyssä tutkimuksessa atooppisen ekseeman vallitsevuus kymmenkertaistui vuosien 1966–1987 aikana ja edelleen vuonna 2020 esiintyvyyden todettiin hieman lisääntyneen «Reijula J, Latvala J, Mäkelä M ym. Long-term trend...»14.
- On oletettu, että suurella osalla lapsipotilaista taudinkulku noudattaisi niin sanottua atooppista marssia eli oireiden esiintymistä seuraavassa järjestyksessä: ihottuma, ruoka-allergiat, astma ja hengitystieallergiat. Uusien laajojen kohorttitutkimusten valossa vain pienellä osalla oireet noudattavat atooppista marssia. Väestötutkimusten perusteella lapsuusiän atooppinen ekseema kuitenkin kaksin–kolminkertaistaa astmaan ja allergiseen nuhaan sairastumisen riskin «Dharmage SC, Lowe AJ, Matheson MC ym. Atopic derma...»15, «Haider S, Fontanella S, Ullah A ym. Evolution of E...»16.
- Suurella osalla lapsista atooppinen ekseema paranee tai lievenee vuosien kuluessa mutta voi pahentua uudelleen nuoruus- tai aikuisiässä «IIlli S, von Mutius E, Lau S ym. The natural cours...»17, «Williams HC, Strachan DP. The natural history of c...»18.
- Ks. lisätietoa atooppisen ekseeman luonnollisesta kulusta «Atooppisen ekseeman luonnollinen kulku»4.
Etiologia ja patogeneesi
- Atooppisen ekseeman taustalla on perimän, ihon läpäisyesteen puutteellisen toiminnan ja immunologisten reaktioiden yhdessä aikaansaama tulehdussolujen aktivaatio sekä ihossa että systeemisesti, mistä seuraavat ihon kuivuus, kutina ja tulehdus (inflammaatio). Atooppisessa ekseemassa on käynnissä useita toisiaan voimistavia prosesseja.
- Atooppinen ekseema on väestö- ja kaksostutkimuksien perusteella osittain perinnöllistä «Bieber T. Atopic dermatitis. N Engl J Med 2008;358...»19. Atooppisen ekseeman esiintyminen lähisuvussa on sen tärkein tunnistettu riskitekijä «Langan SM, Irvine AD, Weidinger S. Atopic dermatit...»13. Saksalaisessa tutkimuksessa äidin tai isän sairastaman atooppisen ekseeman todettiin noin kolminkertaistavan lapsen riskin sairastua atooppiseen ekseemaan «Apfelbacher CJ, Diepgen TL, Schmitt J. Determinan...»20. Jos molemmilla vanhemmilla on atooppinen ekseema, riski voi olla jopa viisinkertainen.
- Atooppisen ekseeman alttiusgeenikandidaatteja on löydetty perimänlaajuisissa assosiaatiotutkimuksissa ihon läpäisyestettä rakentavien ja muokkaavien proteiinien geeneistä ja puolustusjärjestelmän toimintaa ohjaavista geeneistä «Sliz E, Huilaja L, Pasanen A ym. Uniting biobank r...»21.
- Epidermiksen sarveiskerroksen filaggriini on yksi tärkeimmistä ihon läpäisyesteen proteiineista. Läpäisyesteen puutteelliseen toimintaan johtavat filaggriinigeenin mutaatiot ovat tunnetuin yksittäinen atooppiselle ekseemalle altistava geneettinen tekijä. Näitä mutaatioita löytyy 20–40 %:lta atooppista ekseemaa sairastavista «Palmer CN, Irvine AD, Terron-Kwiatkowski A ym. Com...»22. Vain 5,6 %:lla suomalaisista atooppista ekseemaa sairastavista erikoissairaanhoidon potilaista todettiin eurooppalaisen potilasaineiston yleisimmät filaggriinimutaatiot «Luukkonen TM, Kiiski V, Ahola M ym. The Value of F...»23.
- Atooppista ekseemaa sairastavan ihossa keratiinikerroksen rasvahappokoostumus poikkeaa terveihoisen lipidikoostumuksesta «van Smeden J, Bouwstra JA. Stratum Corneum Lipids:...»24, «Joo KM, Hwang JH, Bae S ym. Relationship of cerami...»25.
- Terve iho on hapan, pH-arvoltaan 4–6, mutta atooppinen iho on emäksinen. Atooppisen ihon vähäinen hikoilu ja poikkeava rasvahappokoostumus suurentavat pH-arvoa «Geoghegan JA, Irvine AD, Foster TJ: Staphylococcu...»26.
- Atooppisen ihon bakteerikanta (mikrobiomi) on vähemmän monimuotoinen kuin terveen ihon «Atooppista ekseemaa sairastavilla on suurella osalla Staphylococcus aureus -bakteeri sekä ekseema-alueilla että terveeltä näyttävällä iholla. Atooppisessa ekseemassa bakteerikannan monimuotoisuus on vähäisempi kuin terveellä iholla.»A. Tämä johtaa siihen, että suurella osalla atooppista ekseemaa sairastavista on Staphylococcus aureus -bakteerin yliedustus sekä ekseema-alueilla että terveeltä näyttävällä iholla.
- Epidermiksen läpäisyeste on atooppisessa ihossa puutteellinen sekä ihottuma-alueella että terveeltä näyttävässä ihossa. Geneettisten tekijöiden lisäksi läpäisyestettä heikentävät ihon raapimisen aiheuttama mekaaninen vaurio ja atooppista ihoa kolonisoivan Staphylococcus aureus-bakteerin toksiinit ja proteaasit. Ihoon pääsee tunkeutumaan mikrobeja, toksisia ärsykkeitä ja allergeeneja, jotka saavat aikaan tulehdussolujen aktivaation. Atooppisen ekseeman tyypilliset tulehdusvälittäjäaineet (IL-4, IL-13 ja IL-31) estävät filaggriinin ja muiden läpäisyesteen proteiinien muodostumista edelleen «Langan SM, Irvine AD, Weidinger S. Atopic dermatit...»13, «Geoghegan JA, Irvine AD, Foster TJ: Staphylococcu...»26.
- Atooppinen ekseema on aina kutiseva. Kaikissa ihon kerroksissa on sensorisia hermosoluja, jotka voivat välittää kutinasignaalin aivoihin ja laukaista siten raapimisreaktion. Atooppista ekseemaa sairastavan ihossa sensorisia hermosoluja on osoitettu olevan normaalia tiheämmässä. Merkittävimpiä kroonisen atooppisen ekseeman kutinaa laukaisevia tekijöitä (pruritogeenejä) näyttäisivät olevan tyypin 2 tulehdussytokiinit, kuten IL-4, IL-13 ja IL-31. Ihon sensorisista hermopäätteistä onkin löydetty muun muassa näiden sytokiinien reseptoreita. Osa kutinaa välittävistä hermosoluista aktivoituu histamiinin vapautuessa syöttösoluista «Legat FJ. Itch in Atopic Dermatitis - What Is New?...»27.
- Ihon kutinaa ja kipua välittävät sensoriset hermot ovat osittain päällekkäisiä. Kutina ja kiputuntemukset ovat atooppisessa ekseemassa usein yhteydessä toisiinsa, mutta osalla potilaista ihon kiputuntemus voi olla myös itsenäinen oire. Mekaaniset ihoa ärsyttävät tekijät, jotka vaurioittavat ihon läpäisyestettä ja vapauttavat tulehdusvälittäjäaineita ihosta, voivat saada aikaan lisääntyneeseen herkkyyteen johtavia rakenteellisia muutoksia ihon hermosoluissa. Oireiden kroonistuessa herkistyminen sekä kutina- että kiputunnolle tapahtuu myös keskushermostossa «Ständer S, Simpson EL, Guttman-Yassky E ym. Clinic...»28.
- Ks. kuva Atooppisen ekseeman patogeneesi pääpiirteissään «Atooppisen ekseeman patogeneesi pääpiirteissään»2.
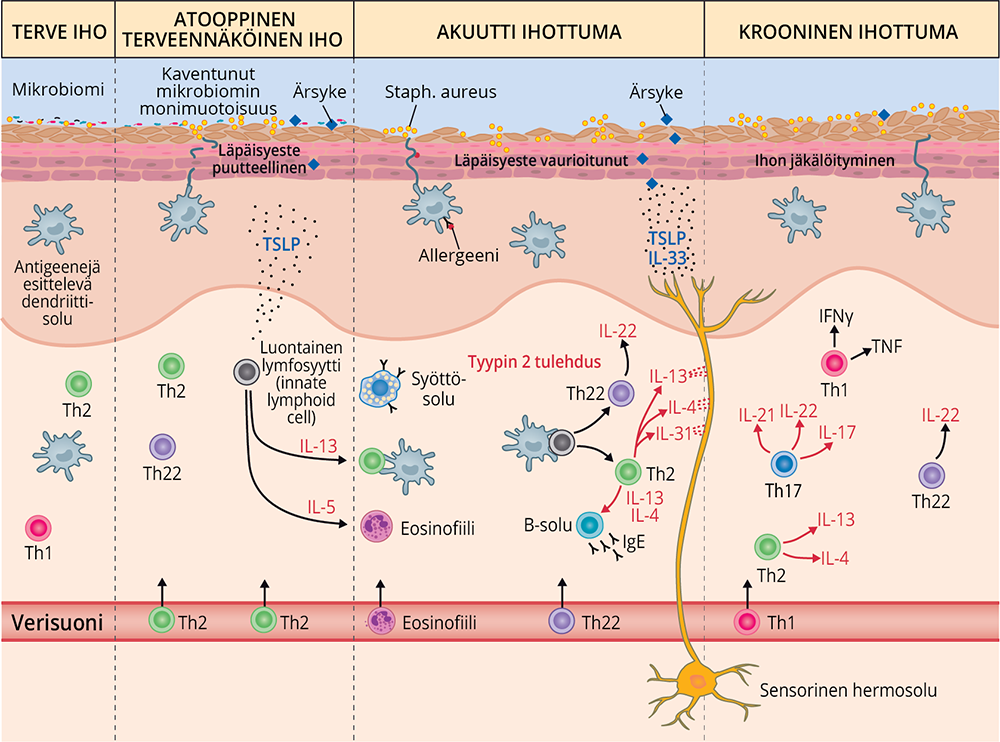
Atooppisen ekseeman patogeneesi pääpiirteissään
IFNγ = gamma-interferoni, IgE = immunoglobuliini E, IL = interleukiini, Th = auttaja-T-solu, TNF = tuumorinekroositekijä, TSLP = thymic stromal lymphopoietin.
Terve iho muodostaa fyysisen, kemiallisen ja biologisen läpäisyesteen haitallisille tekijöille (ärsykkeille, kuten bakteerit, kemikaalit ja allergeenit). Monimuotoinen ihon mikrobiomi tukee terveen immuunipuolustuksen kehittymistä aktivoimalla esimerkiksi antimikrobiaalisia mekanismeja, jotka estävät taudinaiheuttajien kasvua iholla.
Atoopikon terveennäköiselläkin iholla läpäisyeste on heikko, ihon mikrobiomin monimuotoisuus on kaventunut ja antimikrobiaalisten peptidien tuotanto vähentynyt. TSLP (thymic stromal lymphopoietin) on epiteelisolujen tuottama alarmiini (hälytysaine), joka säätelee tyypin 2 tulehdusvasteen aktivoitumista. Akuutissa ihottumavaiheessa antigeenejä esittelevät dendriittisolut, kuten Langerhansin solut ja dendriittisolut, joihin on kiinnittynyt IgE-vasta-aineita, aktivoivat tyypin 2 tulehdussoluja tuottamaan sytokiineja IL-4, IL-13 ja IL-31. Nämä toimivat kutinaa laukaisevina välittäjäaineina. Kehittyy noidankehä, jossa tyypin 2 tulehdus vaurioittaa lisää ihon läpäisyestettä ja epiteelisolut tuottavat lisää alarmiineja, kuten TSLP ja IL-33, jotka voimistavat kutinaa entisestään.
Kroonisessa atooppisessa ekseemassa Th1- ja erityisesti lapsilla ja aasialaista taustaa olevilla potilailla Th17-tulehdussolut aktivoituvat.
Kuva muokattu lähteestä: Langan SM, Irvine AD & Weidinger S. Atopic dermatitis. Lancet 2020;396:345-60
Aiheesta lisää:
Fyhrquist N. Ihon mikrobiomi ja atooppiset taudit. Duodecim 2021;137:2553-9
Beck LA, Cork MJ, Amagai M, De Benedetto A, Kabashima K, Hamilton JD, Rossi AB. Type 2 Inflammation Contributes to Skin Barrier Dysfunction in Atopic Dermatitis. JID Innovations 2022;2:100131
Ehkäisy
- Atooppista ekseemaa ei voi tehokkaasti ehkäistä.
- Yli 4 kuukautta kestävällä yksinomaisella rintaruokinnalla ei voida pienentää atooppisen ekseeman riskiä. Yleisesti suositeltu 4–6 kuukauden täysimetys sopii myös allergiariskiperheille «Greer FR, Sicherer SH, Burks AW ym. The Effects of...»29.
- Jos rintamaito ei riitä, käytetään yleensä tavallisia lehmänmaitopohjaisia korvikkeita. Ei ole riittävää näyttöä siitä, että osittain tai pitkälle pilkotun korvikkeen käyttö allergiariskiperheessä ensimmäisten 4 kuukauden aikana rintamaidon määrän ollessa riittämätön vähentäisi atooppisen ekseeman riskiä «Boyle RJ, Ierodiakonou D, Khan T ym. Hydrolysed fo...»30, «Osborn DA, Sinn JK, Jones LJ. Infant formulas cont...»31.
- Muu ruokavalio:
- Äidin raskauden tai imetyksen aikainen välttämisruokavalio ei näytä pienentävän lapsen riskiä sairastua atooppiseen ekseemaan, ja se saattaa vaikuttaa haitallisesti äidin tai sikiön ravitsemukseen «Foisy M, Boyle RJ, Chalmers JR ym. Overview of Rev...»32, «Netting MJ, Middleton PF, Makrides M. Does materna...»33. Ks. Käypä hoito -suositus Ruoka-allergia (lapset) «Ruoka-allergia (lapset)»4.
- Atooppisen ekseeman ehkäisemiseen ei suositella kiinteiden ruokien aloituksen viivästyttämistä «Greer FR, Sicherer SH, Burks AW ym. The Effects of...»29. Ei ole näyttöä siitä, että kiinteiden ruokien annon aloituksen siirtäminen 4 kuukauden iästä 6 kuukauden ikään tai myöhemmäksi vähentäisi atooppisen ekseeman ilmaantuvuutta «Zutavern A, Brockow I, Schaaf B ym. Timing of soli...»34, «Williams HC, Chalmers J. Prevention of Atopic Derm...»35.
- Yleisesti allergiaa aiheuttavien ruokien (maapähkinä, kananmuna) lisääminen ruokavalioon 4 kuukauden iästä alkaen ei lisää atooppisen ekseeman riskiä, mutta voi estää kananmuna- ja maapähkinäallergiaa «Obbagy JE, English LK, Wong YP ym. Complementary f...»36. Ks. Käypä hoito -suositus Ruoka-allergia (lapset) «Ruoka-allergia (lapset)»4.
- Probiootit ja prebiootit
- Probiootti on elävä mikrobivalmiste, joka WHO:n määritelmän mukaan riittävästi käytettynä edistää terveyttä «Pfefferle PI, Prescott SL, Kopp M. Microbial influ...»37. Prebiootti on hajoamaton ravintolisä, joka WHO:n määritelmän mukaan vaikuttaa suotuisasti stimuloimalla selektiivisesti tiettyjen bakteerien (probioottien) kasvua tai aktiivisuutta suolistossa ja edistää siten terveyttä «Kuitunen M. Probiotics and prebiotics in preventin...»38.
- Jotkin probioottiset valmisteet vähentävät atooppisen ekseeman ilmaantuvuutta allergian
riskiperheissä «Jotkut probiootit vähentävät atooppisen ekseeman ilmaantuvuutta lapsilla ainakin 2 vuoden ikään asti, kun allergian riskiperheissä äiti aloittaa probiootin käytön vähintään 4 viikkoa ennen laskettua aikaa ja käyttöä jatketaan lapsella 6 kuukauden ajan.»A. Tieto siitä, mitä probioottikantaa tai -kantojen yhdistelmää tulisi käyttää, kuinka
pitkä hoidon tulisi olla tai mikä olisi sopiva annos, on edelleen puutteellista.
- Tiedetään, että Lactobacillus rhamnosus GG:n (LGG) aloittaminen allergiariskiperheen äidille vähintään 4 viikkoa ennen laskettua aikaa ja antaminen lapselle 6 kuukauden ajan, vähentää atooppisen ekseeman ilmaantuvuutta 2 vuoden ikään saakka «Li L, Han Z, Niu X ym. Probiotic Supplementation f...»39.
- Prebiooteilla (esim. galakto- tai frukto-oligosakkaridi) saattaa olla atooppista ekseemaa vähentävää vaikutusta, mutta tutkimustietoa asiasta on vielä niukasti eikä niiden käytöstä voida toistaiseksi antaa suositusta «Osborn DA, Sinn JK. Prebiotics in infants for prev...»40, «Sestito S, D'Auria E, Baldassarre ME ym. The Role ...»41.
- Ihon läpäisyesteen poikkeavuudella on merkittävä osuus atooppisen ekseeman patogeneesissä. Perusvoiteet ovat keskeinen osa atooppisen ekseeman hoitoa, mutta niiden tehoa atooppisen ekseeman ehkäisyssä ei ole pystytty luotettavasti osoittamaan. Tutkimustieto systemaattisissa kirjallisuuskatsauksissa ja meta-analyyseissä on ristiriitaista «Kelleher MM, Cro S, Cornelius V ym. Skin care inte...»42, «Liang J, Hu F, Tang H ym. Systematic review and ne...»43. Aiemmissa pienemmissä tutkimuksissa osoitettiin atooppisen ekseeman riskin pienenevän verrokkivauvoihin verrattuna, kun suuren allergiariskin perheen vauvan ihoa rasvattiin perusvoiteella syntymän jälkeen säännöllisesti ainakin kerran vuorokaudessa 6–7 kuukauden ajan «Simpson EL, Chalmers JR, Hanifin JM ym. Emollient ...»44, «Horimukai K, Morita K, Narita M ym. Application of...»45. Myöhemmissä laajemmissa tutkimuksissa tulosta ei ole pystytty varmentamaan «Kelleher MM, Cro S, Cornelius V ym. Skin care inte...»42, «Liang J, Hu F, Tang H ym. Systematic review and ne...»43, «Skjerven HO, Rehbinder EM, Vettukattil R ym. Skin ...»46, «Chalmers JR, Haines RH, Bradshaw LE ym. Daily emol...»47.
Diagnostiikka, oireet ja löydökset
- Atooppisen ekseeman diagnoosi on kliininen.
- Diagnoosiin yleensä riittää, että potilaalla on seuraavat löydökset «Brenninkmeijer EE, Schram ME, Leeflang MM ym. Diag...»48, «Champion RH ym. (toim.) Textbook of Dermatology, 6...»49:
- kutiava ja krooninen tai jatkuvasti toistuva ekseema tyypillisillä ihoalueilla (kuva «Ihottuman tyyppialueet»3)
- ihottuma-alueella punoitusta, näppylöitä (papuloita), hilseilyä, raapimajälkiä ja ihorikkoumia. Akuuttivaiheessa iholla voi olla myös pieniä nesterakkuloita (vesikkeleitä) ja vetistystä, kroonistumisvaiheessa ihottuma-alue paksuuntuu eli jäkälöityy (likenifikaatio) raapimisen seurauksena.
- Tarkemmat diagnostiset kriteerit ovat seuraavat:
- Atooppinen ekseema on aina kutiseva – ilman kutinaa ilmenevä ihottuma ei ole atooppista ekseemaa.
- Kutinan lisäksi potilaalla pitää olla vähintään kolme viidestä seuraavasta oireesta
ja löydöksestä «Williams HC, Burney PG, Pembroke AC ym. The U.K. W...»50:
- ekseemaa tyypillisellä alueella tutkimushetkellä (kuva «Ihottuman tyyppialueet»3)
- ekseemaa tyypillisellä alueella aiemmin
- kuiva iho
- ekseema alkanut ennen toista ikävuotta
- allerginen nuha tai astma (alle 4-vuotiailla kriteerinä atooppinen sairaus perheenjäsenellä).
- Atooppiseen ekseemaan liittyy usein myös ihon kipua, eri tutkimusten mukaan jopa 43–92 %:lla potilaista. Kipu on tavallisimmin luonteeltaan polttelevaa tai ilmenee ihon aristuksena tai kosketusarkuutena. Kipuoire korreloi ihottuman vaikeusasteeseen «Ständer S, Simpson EL, Guttman-Yassky E ym. Clinic...»28, «Li JX, Dong RJ, Zeng YP. Characteristics, mechanis...»51.
- Kesällä atooppisen ekseeman oireet usein lievittyvät.
- Atooppinen ekseema voidaan kliinisessä työssä luokitella seuraavasti:
- Lievä atooppinen ekseema: potilaalla on kuivia ihoalueita, satunnaisesti kutinaa ja pienillä ihoalueilla punoitusta (kuva «Leikki-ikäisen lievä atooppinen ekseema»4). Lääkkeellistä paikallishoitoa tarvitaan ajoittain.
- Keskivaikea atooppinen ekseema: potilaalla on kuivia ihoalueita, toistuvaa kutinaa ja punoitusta ja mahdollisesti myös ihon rikkoutumista ja paksuuntumista (kuva «Atooppinen ekseema nuoren miehen ranteessa»5). Lääkkeellistä paikallishoitoa tarvitaan jatkuvasti jaksoittaisena tai ylläpitohoitona.
- Vaikea atooppinen ekseema: iho on kuiva, kutina jatkuvaa ja punoitus laaja-alaista. Lisäksi esiintyy ihorikkoumia, ihon huomattavaa paksuuntumista, verenvuotoa, vetistystä, karstoittumista ja pigmentaatiohäiriöitä (kuvat «Kouluikäisen vaikea atooppinen ekseema kaulassa ja ylävartalossa»6 ja «Kouluikäisen vaikea atooppinen ekseema yläraajoissa»7). Vaikea atooppinen ekseema voi olla erytroderminen (koko ihon ihottuma). Tarvitaan tai harkitaan pitkäaikaista systeemistä lääkitystä.
- Ekseeman vaikeusasteen kliiniseen arviointiin voidaan käyttää validoituja mittareita «Thomas KS, Apfelbacher CA, Chalmers JR ym. Recomme...»52. Erityisesti erikoissairaanhoidossa sairauden vaikeusastetta kuvaavien mittareiden käyttö on suositeltavaa. Ks. lisätietoa Atooppisen ekseeman arvioinnissa käytettäviä mittareita «Atooppisen ekseeman arvioinnissa käytettäviä mittareita»5 ja kohta Atooppisen ekseeman oireiden, vaikeusasteen ja hoitovasteen arvioinnin työkaluja «A1»2.
- Näyttää siltä, että atooppisessa ekseemassa voidaan erottaa useita ilmiasuja (fenotyyppejä)
taustalla esiintyvien geneettisten tekijöiden ja tulehdusmekanismien mukaan.
- Atooppisen ekseeman kliininen kuva muuttuu iän myötä erityisesti ihottuma-alueiden sijainnin suhteen. Myös tulehdusvaste muuttuu lapsuusiän atooppisen ekseeman Th2-, Th22- ja Th17-vallitsevuudesta Th2-, Th22- ja Th1-painotteiseksi «Czarnowicki T, He H, Krueger JG ym. Atopic dermati...»53.
- Osalla aikuisista (noin 80 %:lla) atooppista ekseemaa sairastavista seerumin IgE-pitoisuus on suurentunut. Heillä on yleensä perinnöllinen taipumus atopiaan ja filaggriinigeenin mutaatiot ovat tavallisia. Noin 20 %:lla potilaista seerumin IgE-pitoisuus on normaali. Nämä potilaat ovat usein naisia, ja heidän ihottumansa on alkanut vasta aikuisiällä «Czarnowicki T, He H, Krueger JG ym. Atopic dermati...»53, «Tokura Y, Hayano S. Subtypes of atopic dermatitis:...»54.
- Lasten taudinkulussa voidaan tunnistaa erilaisia ilmiasuja varhain puhkeavasta ja nopeasti oireettomaksi muuttuvasta taudinkuvasta krooniseen ja aikuisikään jatkuvaan tautimuotoon. Riskitekijät ja ennuste vaihtelevat geneettisten ja ympäristötekijöiden mukaan. Konsensusta eri alatyypeistä ei kuitenkaan ole «Langan SM, Irvine AD, Weidinger S. Atopic dermatit...»13, «Paternoster L, Savenije OEM, Heron J ym. Identific...»55, «Roduit C, Frei R, Depner M ym. Phenotypes of Atopi...»56.
- Atooppisen ekseeman ilmiasu ja molekyylitason mekanismit sekä immunologia ekseeman taustalla vaihtelevat potilaiden etnisen taustan mukaan «Czarnowicki T, He H, Krueger JG ym. Atopic dermati...»53.
- Toistaiseksi ei ole kliiniseen käyttöön soveltuvia geneettisiä markkereita tai biomarkkereita atooppisen ekseeman diagnostiikkaan eikä sen vaikeusasteen tai ennusteen arviointiin. Koska eri hoitojen vasteet saattavat vaihdella ekseeman ilmiasun ja sen taustalla olevien mekanismien mukaan, on tulevaisuuden tavoitteena aiempaa yksilöllisempi hoito «Renert-Yuval Y, Thyssen JP, Bissonnette R ym. Biom...»57.
- Erityispiirteitä «Akdis CA, Akdis M, Bieber T ym. Diagnosis and trea...»58:
- Ekseema alkaa vauvaiässä usein pään hilseilynä ja leviää vartaloon ja raajoihin. Vaippa-alueella ei yleensä ole ekseemaa. Ekseema voi erittää visvaa, mikä saa sen muistuttamaan märkärupea, tai muuttua erytrodermiaksi (voimakas koko ihon punoitus ja tulehdus) (kuvat «Vauvaikäisen lievä atooppinen ekseema»8 ja «Vauvan vaikea atooppinen ekseema»9). Atooppinen ekseema voi esiintyä paksuuntuneina pieninä läiskinä, jolloin sitä kutsutaan nummulaariseksi atooppiseksi ekseemaksi «Nummulaarinen ekseema»10.
- Leikki-iässä toisesta ikävuodesta alkaen atooppisen ekseeman tyyppialueet ovat kaula ja niska, kyynär- ja polvitaipeet, ranteet, pakarantaive ja nilkat. Muita tyyppialueita ovat silmien seutu, korvien taustat, korvannipukat ja suun ympäristö. Myös huulten kuiva tulehdus on yleistä. Vartalossa ja raajojen ojentajapuolilla voi esiintyä ekseemaa (kuvat «Leikki-ikäisen lievä atooppinen ekseema»4 ja «Leikki-ikäisen keskivaikea atooppinen ekseema»11).
- Kouluiässä ekseema keskittyy usein polvi- ja kyynärtaipeisiin. Ekseemaa tavataan usein myös niin sanotussa ratsupaikassa pakaroiden ja reisien alueella, käsissä, jalkaterissä, niskassa ja kasvoissa. Muita yleisiä erityismuotoja ovat atoopikon talvijalka, käsien lumipalloihottuma ja niskan neurodermatiitti. Murrosiässä ekseema leviää usein hartioihin, rintaan ja selkään (kuvat «Atooppinen ekseema pojan jalkapohjan alueella (ns. talvijalka)»12, «Kouluikäisen vaikea atooppinen ekseema kaulassa ja ylävartalossa»6 ja «Kouluikäisen vaikea atooppinen ekseema yläraajoissa»7).
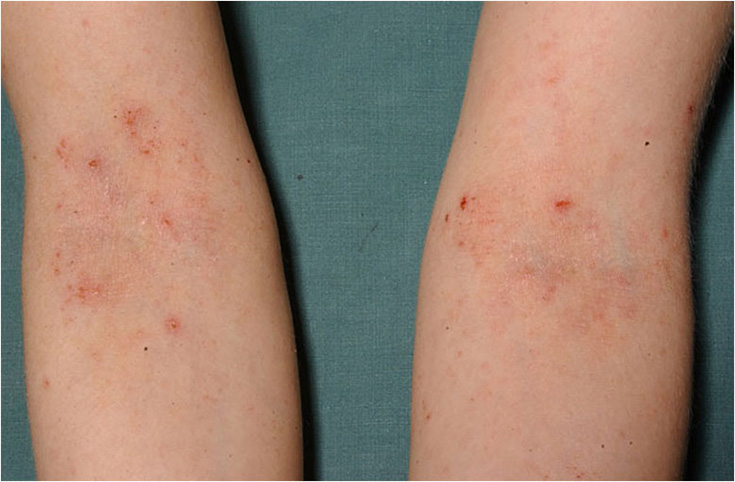
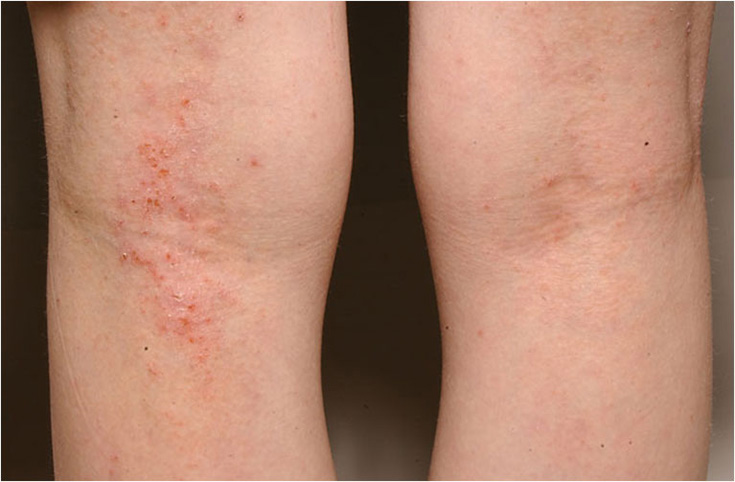
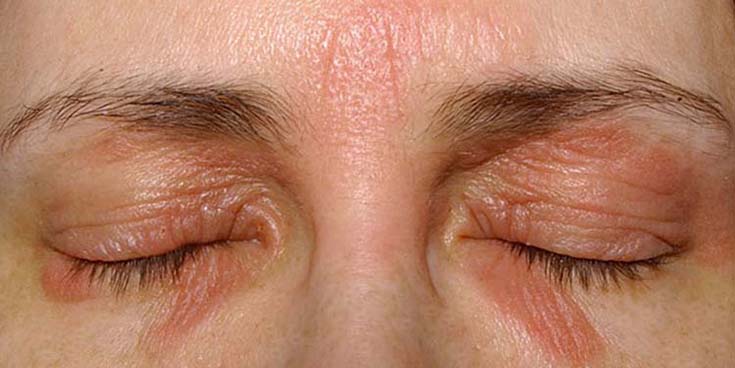
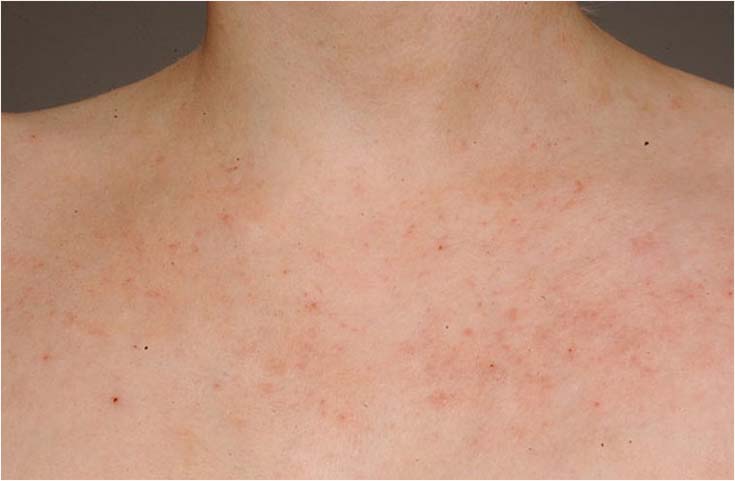
- Aikuisiällä tyypillisiä atooppisen ekseeman alueita ovat kyynär- ja polvitaipeiden lisäksi kasvot, kaula ja ylävartalo. Aikuisilla atooppinen ekseema on usein käsissä (kuvat «Atooppinen ekseema nuoren naisen kyynärtaipeissa»13, «Atooppinen ekseema polvitaipeessa»14, «Atooppinen ekseema silmäluomissa»15, «Atooppinen ekseema nuoren naisen kaulan alueella»16, «Atooppinen ekseema kaulan alueella»17, «Vaikea atooppinen ekseema niskan alueella»18, «Laaja-alainen atooppinen ekseema (erytrodermia)»19, «Atooppinen ekseema nuoren miehen ranteessa»5, «Atooppinen ekseema nuoren aikuisen kädessä»20, «Atooppinen ekseema ranteissa»21, «Vaikea atooppinen ekseema alaraajoissa»22).
- Atooppinen ekseema oireilee usein myös silmäluomilla ja blefarokonjunktiviittina.
- Tummaihoisilla potilailla iholla näkyy vähemmän ihon punoitusta kuin vaaleaihoisilla, mikä voi johtaa ihottuman vaikeusasteen aliarviointiin. Punoituksen erottaminen postinflammatorisesta hyperpigmentaatiosta voi olla haastavaa ja vaikeuttaa taudin seurantaa. EASI-mittari soveltuu kuitenkin hyvin myös tummaihoisille «Zhao CY, Hao EY, Oh DD ym. A comparison study of c...»59, «Vauvaikäisen tummaihoisen lapsen atooppinen ekseema»23, «Leikki-ikäisen tummaihoisen atooppinen ekseema»24, «Nuoren tummaihoisen atooppinen ekseema»25, «Tummaihoisen atooppinen ekseema»26.
- Erotusdiagnostiikassa on otettava huomioon erityisesti seuraavat:
- vauvoilla ja lapsilla hormoninäppylät, seborrooinen ekseema, iktyoosi, psoriaasi, ihokeliakia, keratosis pilaris, syyhy, acrodermatitis enteropathica ja immuunipuutostilat
- aikuisilla muut ekseemat (seborrooinen ekseema, nummulaarinen ekseema, infektioekseema, asteatoottinen ekseema), psoriaasi, syyhy, ihokeliakia, immuunipuutostilat, parapsoriaasi ja iholymfooma
- kaikenikäisillä allerginen kosketusekseema ja ärsytyskosketusekseema
- akuuttivaiheessa märkärupi ja erysipelas.
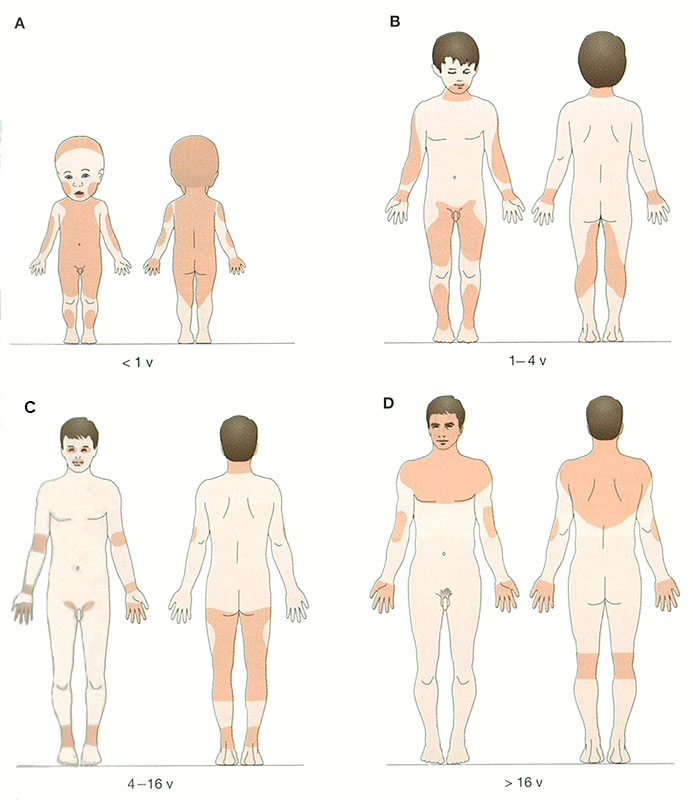
Ihottuman tyyppialueet. Atooppisen ekseeman tyypilliset ihoalueet eri ikäkausina.
Lähde: Hannuksela M, Alanko K. Atooppinen ekseema. Kirjassa: Hannuksela M, Karvonen J, Reunala T, Suhonen R (toim.). Ihotaudit. Kustannus Oy Duodecim 2003, s. 79
Lupa käyttöön saatu Kustannus Oy Duodecim/Hannele Pirttimaa 21.8.2008
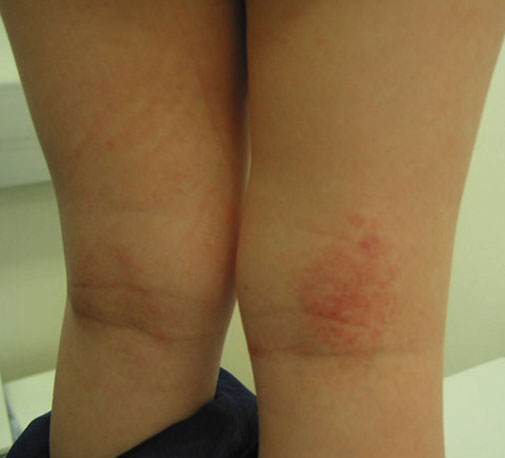
Leikki-ikäisen lievä atooppinen ekseema.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Mika Mäkelä
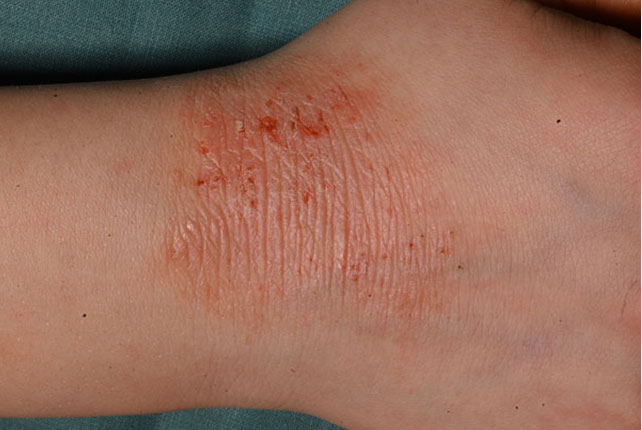
Atooppinen ekseema nuoren miehen ranteessa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
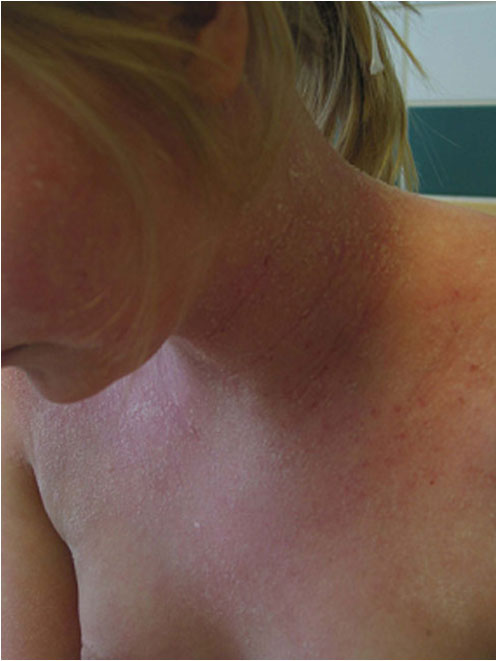
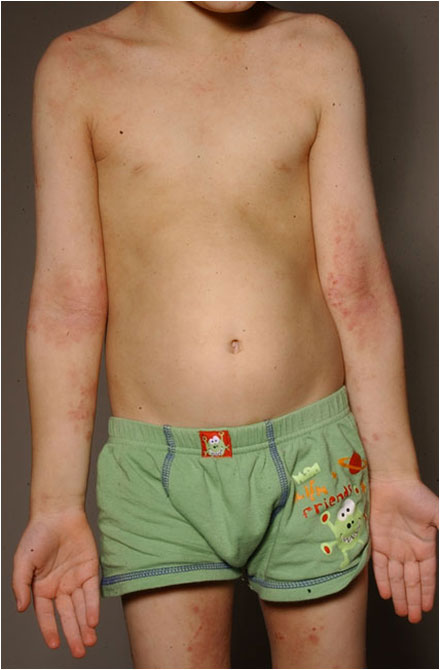
Kouluikäisen vaikea atooppinen ekseema kaulassa ja ylävartalossa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Anna Pelkonen
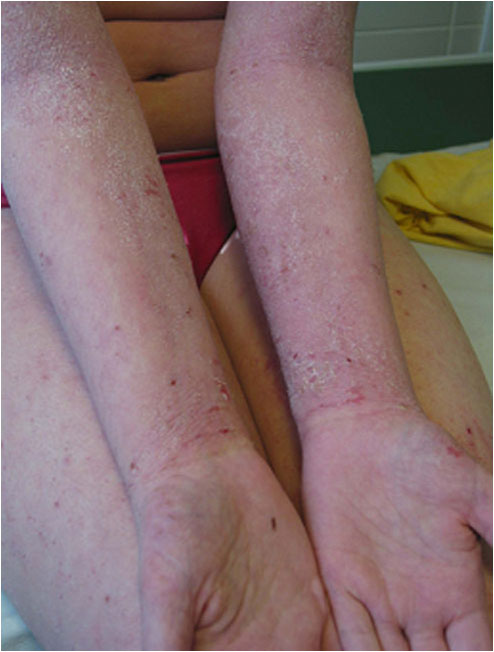
Kouluikäisen vaikea atooppinen ekseema yläraajoissa.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Anna Pelkonen.
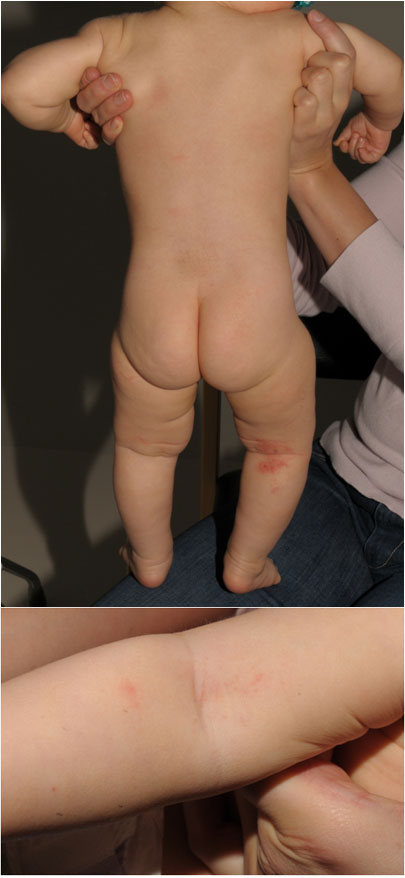
Vauvaikäisen lievä atooppinen ekseema
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Anna Pelkonen
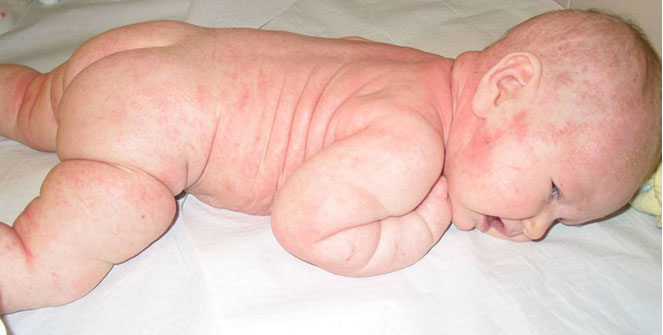
Vauvan vaikea atooppinen ekseema
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Mika Mäkelä .
Nummulaarinen ekseema.
© Hannele Heikkilä
Leikki-ikäisen keskivaikea atooppinen ekseema.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Anna Pelkonen
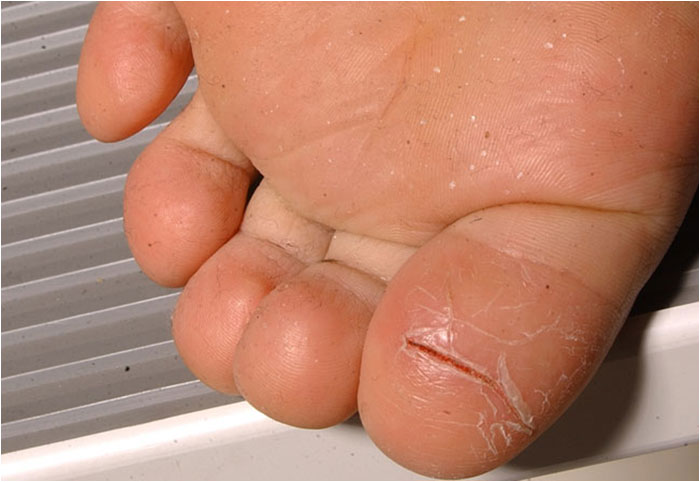
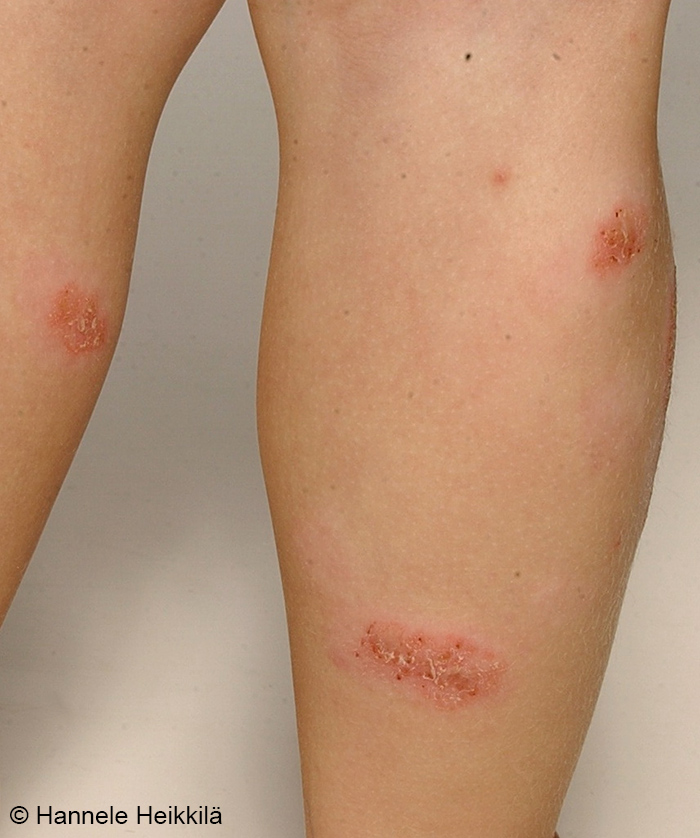
Atooppinen ekseema pojan jalkapohjan alueella (ns. talvijalka)
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
Atooppinen ekseema nuoren naisen kyynärtaipeissa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
Atooppinen ekseema polvitaipeessa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
Atooppinen ekseema silmäluomissa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
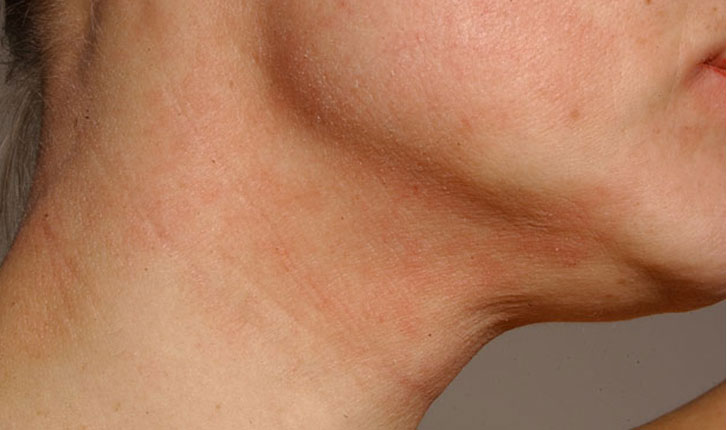
Atooppinen ekseema nuoren naisen kaulan alueella
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
Atooppinen ekseema kaulan alueella
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
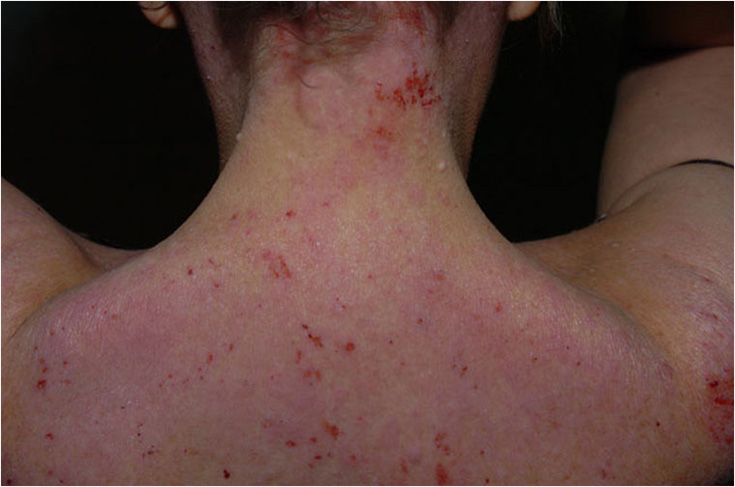
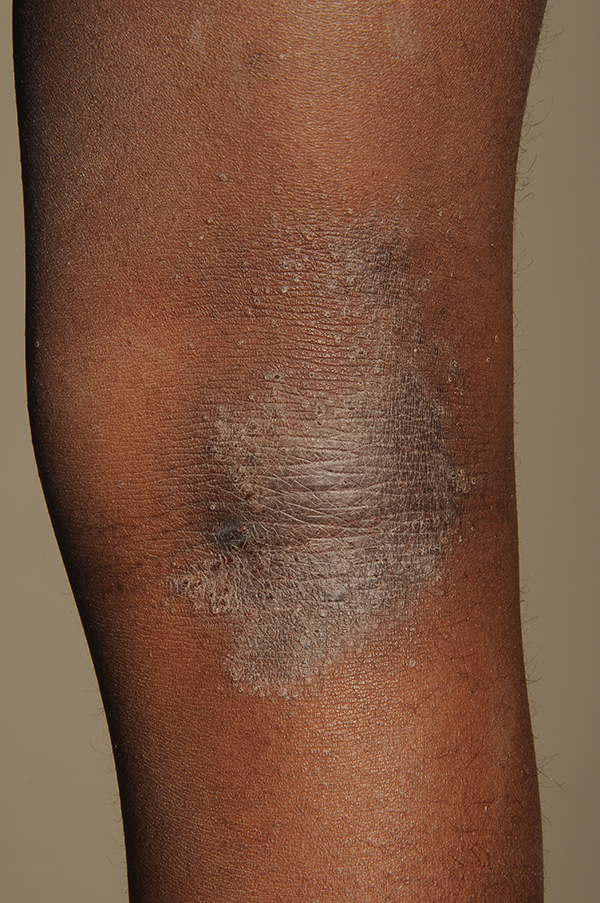
Vaikea atooppinen ekseema niskan alueella. Pitkään kestänyt, voimakkaasti kutiseva ja rikki raavittu atooppinen ekseema niskan ja yläselän alueella.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
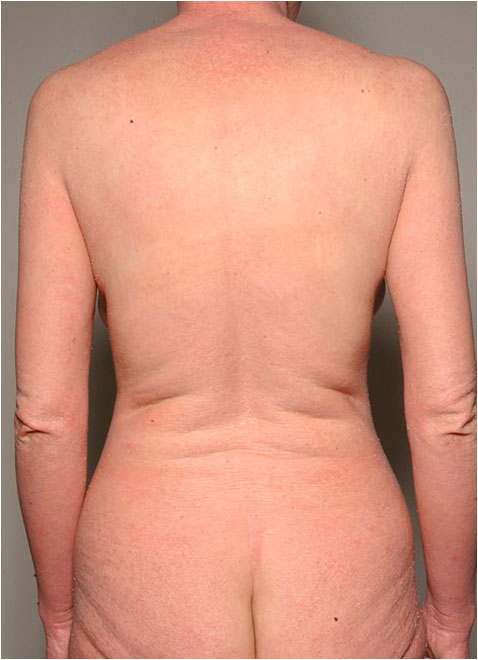
Laaja-alainen atooppinen ekseema (erytrodermia)
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
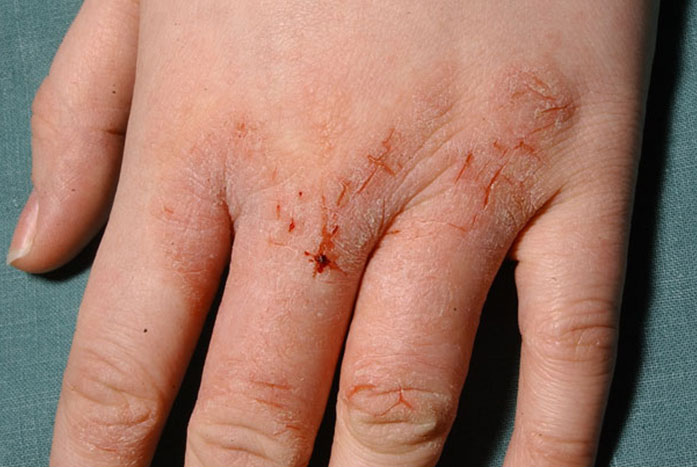
Atooppinen ekseema nuoren aikuisen kädessä
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
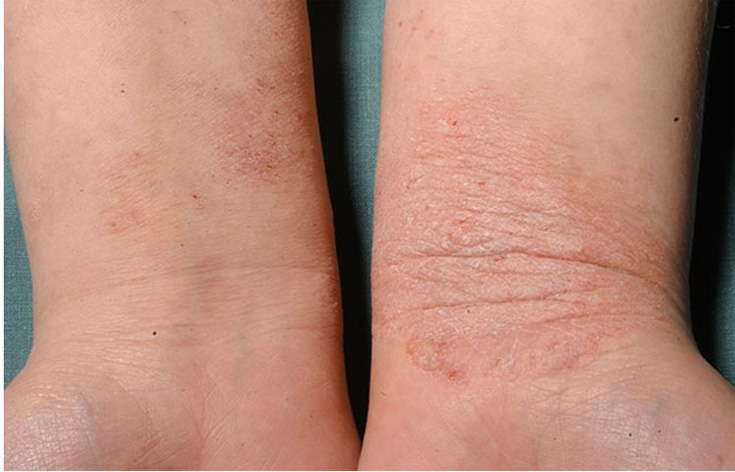
Atooppinen ekseema ranteissa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
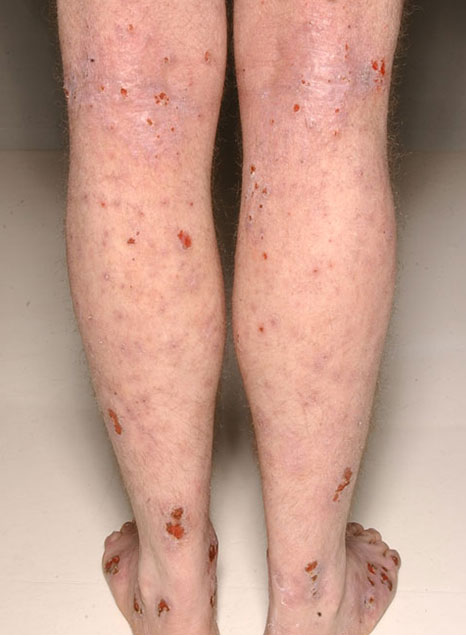
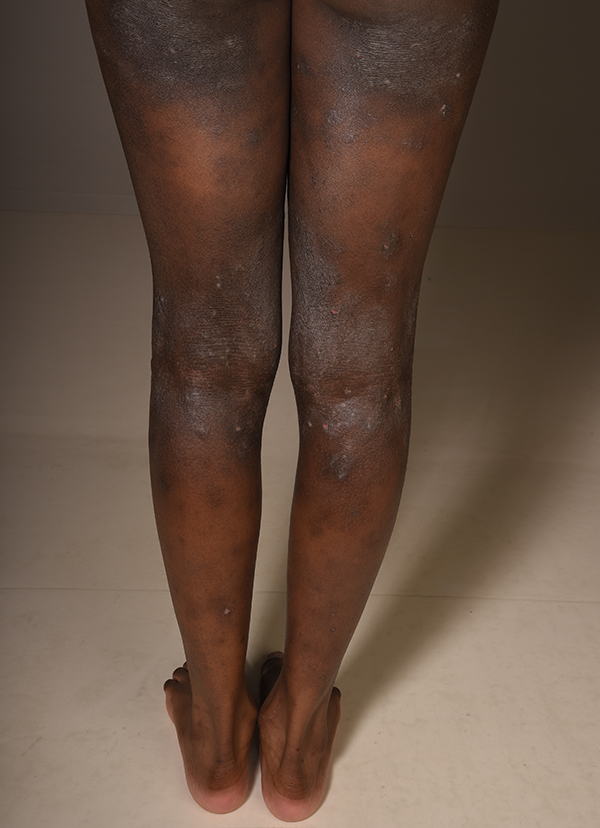
Vaikea atooppinen ekseema alaraajoissa. Pitkään kestänyt, hyvin kutiseva, jäkälöitynyt ja rikki raavittu atooppinen ekseema.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
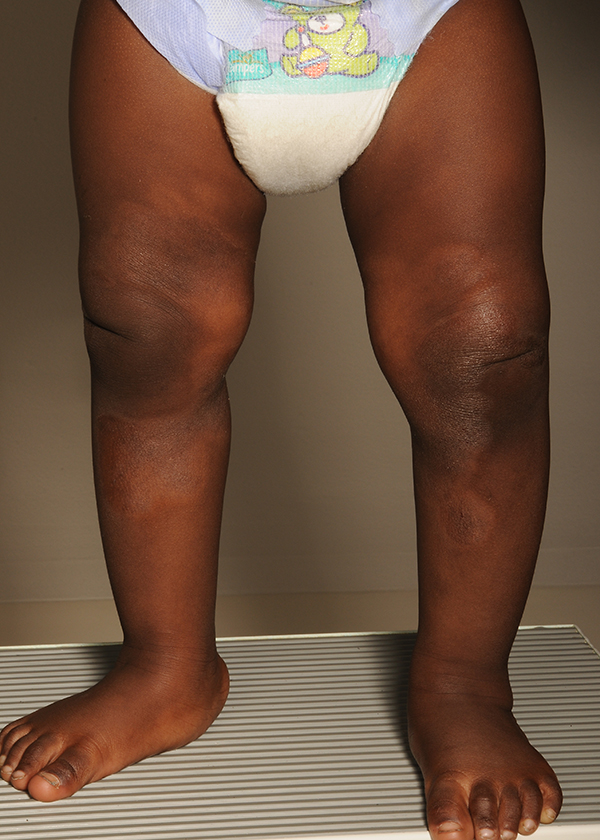
Vauvaikäisen tummaihoisen lapsen atooppinen ekseema. Tummaihoisilla ihotulehdus aiheuttaa yleisesti ihon hypo- ja hyperpigmentaatiota.
Lähde: HYKS:n iho- ja allergiasairaala
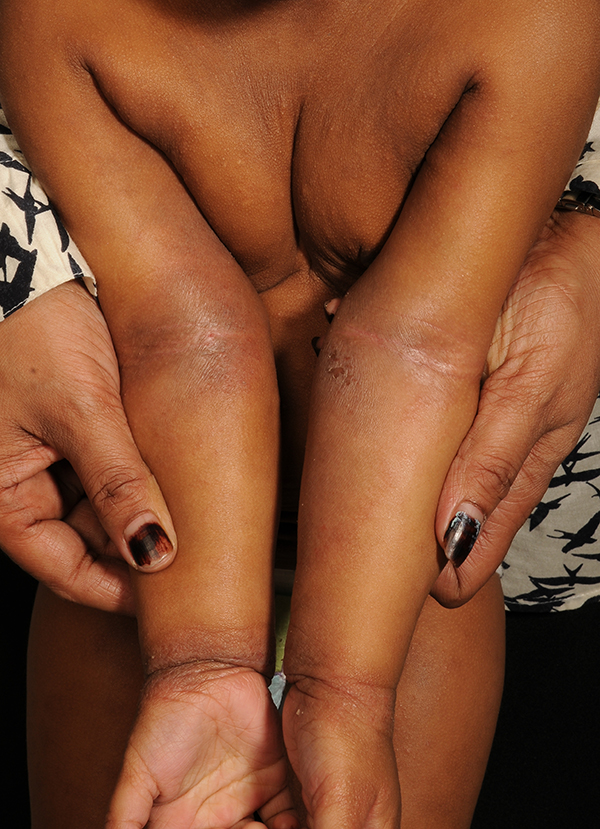
Leikki-ikäisen tummaihoisen atooppinen ekseema. Kyynärtaipeiden ja ranteiden tyypillinen atooppinen ekseema.
Lähde: HYKS:n iho- ja allergiasairaala
Nuoren tummaihoisen atooppinen ekseema. Voimakkaasta ihotulehduksesta huolimatta iholla ei näy punoitusta vaan väritys on harmahtava vaaleasta hilseilystä johtuen.
Lähde: HYKS:n iho- ja allergiasairaala
Tummaihoisen atooppinen ekseema. Polvitaipeen kuvassa näkyy tummaihoisilla yleisemmät papulaiset muutokset ja korostuneet ihon follikkeliaukot.
Lähde: HYKS:n iho- ja allergiasairaala
Allergiaselvitykset aikuisilla
- Yleensä allergiaselvitykset eivät ole tarpeen.
- Allergiaselvityksiä voidaan käyttää selvitettäessä hankalahoitoisen ekseeman pahentavia tekijöitä.
- Jos atooppiseen ekseemaan ei saada hoitovastetta tavanomaisella paikallishoidolla, kyseessä voi olla kosketusallergian kehittyminen esimerkiksi kosmetiikan tai paikallishoitojen aineosille. Tällöin epikutaanitestaus on aiheellinen.
- Aikuisen ei yleensä tarvitse eliminoida ruoka-aineita ruokavaliosta.
- Siitepölyallergioihin liittyvät ristiallergiat ruoka-aineille saattavat pahentaa atooppista ekseemaa nuorilla ja aikuisilla, mutta luotettavan tutkimuksen määrä on vähäistä «Siitepölyallergioihin liittyvät ristiallergiat ruoka-aineille saattavat pahentaa yli 12-vuotiaiden atooppista ekseemaa, mutta luotettavan tutkimuksen määrä on vähäinen.»C. Siitepölyallergisilla altistuminen siitepölylle voi pahentaa varsinkin kasvojen atooppista ekseemaa «Werfel T, Heratizadeh A, Niebuhr M ym. Exacerbatio...»60.
- Huonepölypunkkiallergian atooppista ekseemaa pahentavasta vaikutuksesta ei ole luotettavaa tutkimusnäyttöä «Nankervis H, Pynn EV, Boyle RJ ym. House dust mite...»61.
Allergiaselvitykset lapsilla
- Osalla alle vuoden ikäisistä keskivaikeaa tai vaikeaa (kuva «Vauvan vaikea atooppinen ekseema»9) atooppista ekseemaa sairastavista lapsista taustalla voi olla ruoka-allergia, tavallisimmin
lehmänmaidolle tai kananmunalle, ja allergiaselvitykset ovat aiheellisia.
- Isommilla lapsilla allergiaselvitykset ekseeman vuoksi ovat harvoin tarpeen.
- Ks. myös Vältä viisaasti -suositus Ruoka-allergiaselvitykset atooppista ekseemaa sairastavilla lapsilla «Ruoka-allergiaselvitykset atooppista ekseemaa sairastavilla lapsilla»6.
- Lasten ruoka-allergioista on erillinen Käypä hoito -suositus Ruoka-allergia (lapset) «Ruoka-allergia (lapset)»4.
- Lisätietoa ruoka-allergioista lasten atooppisessa ekseemassa on lisätietoaineistossa «Lisätietoa ruoka-allergioista lasten atooppisessa ekseemassa»7.
Atooppista ekseemaa pahentavat tekijät
- Atooppista ekseemaa sairastavan potilaan iho on herkkä ärtymään ja kutina lisääntyy erilaisten mekaanisten, fysikaalisten ja kemiallisten tekijöiden vaikutuksesta. Osa ärsyttävistä tekijöistä tunnetaan tutkimusten perusteella, mutta pääosa havainnoista perustuu kliiniseen kokemukseen.
- Hikoilu, psyykkiset tekijät (ks. kappale Elämänlaatu ja psyykkiset tekijät «A12»3), kuiva sisäilma, talviaika, ilmansaasteet, karheat vaatteet, liian kevyet tai rasvaiset voiteet sekä muut iholle laitettavat kosmetiikka- tai hygieniatuotteet voivat pahentaa ekseemaa ärsytysmekanismilla. Muita pahentavia tekijöitä voivat olla ihon bakteeri- ja virusinfektiot tai yleisinfektiot «Ring J, Alomar A, Bieber T ym. Guidelines for trea...»62.
- Ruoka-, siitepöly- ja eläinepiteeliallergiat sekä kosketusallergiat voivat myös joskus pahentaa tai ylläpitää atooppista ekseemaa (ks. kappale Allergiaselvitykset aikuisilla «A2»4 ja Käypä hoito -suositus Ruoka-allergia (lapset) «Ruoka-allergia (lapset)»4), «Werfel T, Heratizadeh A, Niebuhr M ym. Exacerbatio...»60.
- Ks. kuva Atooppinen noidankehä «Atooppinen noidankehä»27.
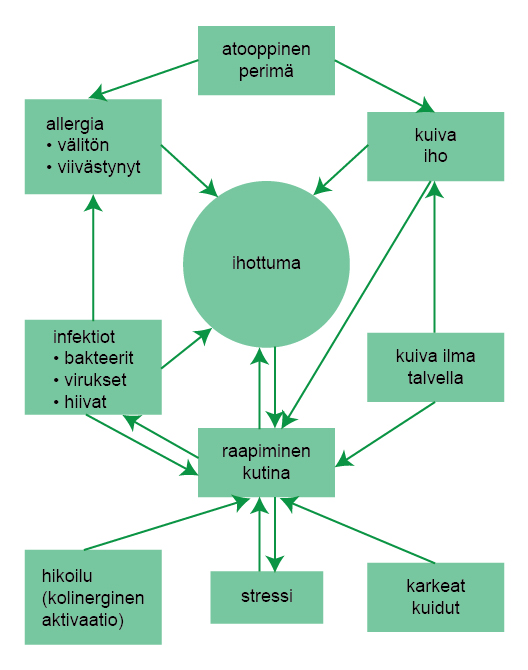
Atooppinen noidankehä
Lähde: Hannuksela M, Lauerma A. Atooppinen ekseema. Kirjassa: Hannuksela M, Peltonen S, Reunala T, Suhonen R (toim.). Ihotaudit. 2., uudistettu painos. Kustannus Oy Duodecim 2011, s. 55
Lupa käyttöön saatu Kustannus Oy Duodecim / Hannele Pirttimaa 21.3.2016
Atooppisen ekseeman liitännäissairaudet
- Atooppisen ekseeman kokonaisvaltaisessa hoidossa on tärkeää huomioida potilaan mahdolliset liitännäissairaudet, etenkin atooppiset sairaudet. Atooppisen ekseeman hoito suunnitellaan yksilöllisesti. Jos potilaalla on muita immunologisia sairauksia, voidaan, mikäli mahdollista, valita atooppisen ekseeman hoitoon sellainen lääkitys, joka tehoaa myös näihin.
- Noin neljäsosalla atooppista ekseemaa sairastavista aikuisista on astma. Vaikean atooppisen
ekseeman ja astman yhteys on selvin «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63.
- Atooppista ekseemaa sairastavilla aikuisilla on kolme kertaa todennäköisemmin astmadiagnoosi kuin muulla väestöllä.
- Aikuisten atooppisella ekseemalla näyttää olevan yhteys myös allergiseen nuhaan ja ruoka-allergioihin. Yhteys ruoka-allergioihin on vahvin vaikeaa atooppista ekseemaa sairastavilla (RR 8,5; 95 % luottamusväli, 5,4–11,5). Ruoka-allergioiden merkitys aikuisten atooppisen ekseeman oirekokonaisuudessa on kuitenkin vähäinen «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63.
- Kosketusallergiat eivät ole atooppista ekseemaa sairastavilla yleisempiä kuin muulla väestöllä «Hamann CR, Hamann D, Egeberg A ym. Association bet...»64.
- Ihoinfektioiden, erityisesti stafylokokkien ja herpes simplex -viruksen aiheuttamien infektioiden, riski on selvästi suurentunut atooppista ekseemaa
sairastavilla «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63.
- Atooppisessa ihossa virusinfektiot saattavat vaurioituneen ihon, raapimisen ja poikkeavan soluvälitteisen immuunipuolustuksen takia levitä laaja-alaisiksi. Tällaisia virustulehduksia ovat muun muassa eczema herpeticum (yleistynyt herpes simplex iholla) «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63 ja ontelosyylät. Ks. lisätietoa ihon virusinfektioista atooppisessa ekseemassa «Lisätietoa ihon virusinfektioista atooppisessa ekseemassa»8.
- Atooppisen ekseeman tehokas hoito vähentää ihoinfektioiden esiintyvyyttä «Wang V, Boguniewicz J, Boguniewicz M ym. The infec...»65.
- Iholymfooman riski on atooppista ekseemaa sairastavilla lievästi suurentunut. Vaikea atooppinen ekseema vaikuttaisi olevan merkittävä riskitekijä «Legendre L, Barnetche T, Mazereeuw-Hautier J ym. R...»66. Lisätietoa ks. «Syöpä- ja lymfoomariski kalsineuriinin estäjien paikallisen käytön yhteydessä»9.
- Atooppista ekseemaa sairastavilla on muuta väestöä useammin silmäsairauksia, kuten silmäluomen reunan tulehdus (blefariitti), sarveis- ja sidekalvotulehdus, keratokonus, glaukooma, harmaakaihi, verkkokalvon irtauma ja herpes simplex -infektio «Hsu JI, Pflugfelder SC, Kim SJ. Ocular complicatio...»67.
- Atooppista ekseemaa sairastavilla esiintyy muuta väestöä enemmän autoimmuunisairauksia, kuten pälvikaljua ja kroonista urtikariaa «Andersen YM, Egeberg A, Gislason GH ym. Autoimmune...»68, «Narla S, Silverberg JI. Association between atopic...»69, «Ivert LU, Wahlgren CF, Lindelöf B ym. Association ...»70, «Kauppi S, Jokelainen J, Timonen M ym. Atopic Derma...»71.
- Atooppista ekseemaa sairastavilla lapsilla ja aikuisilla on lisääntynyt riski sairastua
masennukseen tai ahdistuneisuushäiriöön «Rønnstad ATM, Halling-Overgaard AS, Hamann CR ym. ...»72, «Silverberg JI, Gelfand JM, Margolis DJ ym. Symptom...»73, «Kern C, Wan J, LeWinn KZ ym. Association of Atopic...»74.
- Systemaattisessa 36 alkuperäisjulkaisuun perustuvassa katsauksessa ja meta-analyysissä todettiin, että yhdellä kuudesta atooppista ekseemaa sairastavasta oli kliininen masennus ja joka neljännellä masennusoireita «Patel KR, Immaneni S, Singam V ym. Association bet...»75. Suomalaisessa kansallisessa rekisteritutkimuksessa masennusdiagnoosi oli 10,4 %:lla aikuisista atooppista ekseemaa sairastavista «Kauppi S, Jokelainen J, Timonen M ym. Adult Patien...»76. Atooppisen ekseeman vaikeusasteen ja masennuksen yhteydestä ei ole selkeää kuvaa.
- Atooppisen ekseeman ja masennuksen tai ahdistuneisuuden yhteyden syy on epäselvä. Selitys voi löytyä atooppisen ekseeman aiheuttamasta psykososiaalisesta taakasta, unihäiriöihin johtavasta kutinasta, sairauden aiheuttamasta yleisestä elämänlaadun heikkenemisestä tai näiden yhdistelmästä. Kliinisissä lääketutkimuksissa myös masennus- ja ahdistuneisuusoireet ovat voineet lievittyä keskivaikean tai vaikean atooppisen ekseeman fyysisten oireiden ja löydösten paranemisen lisäksi «de Bruin-Weller M, Thaçi D, Smith CH ym. Dupilumab...»77, «Simpson EL, Wollenberg A, Bissonnette R ym. Patien...»78.
- Lapsilla, joilla on tai on ollut atooppista ekseemaa, näyttää olevan muita lapsia
useammin aktiivisuuden ja tarkkaavaisuuden häiriöitä.
- Kuuteen alkuperäisjulkaisuun perustuvassa meta-analyysissä atooppista ekseemaa sairastaneilla lapsilla ja nuorilla todettiin noin 30 % suurempi todennäköisyys sairastua ADHD:hen kuin atooppista ekseemaa sairastamattomilla verrokeilla «Schans JV, Çiçek R, de Vries TW ym. Association of...»79. Selitykseksi on esitetty yleisen yliherkkyyden, ihottuman aiheuttaman stressin, univajeen ja väsymyksen sekä tulehdusvälittäjäaineiden vaikutusta aivojen kehitykseen.
- Aktivoitunut Th2-tulehdusvaste on mahdollinen etiologinen selitys atooppiseen ekseemaan liittyville neuropsykologisille liitännäissairauksille «Jackson-Cowan L, Cole EF, Arbiser JL ym. TH2 sensi...»80.
- Yhdysvaltalaisessa väestötutkimuksessa todettiin myös aikuisilla atooppista ekseemaa sairastavilla suurentunut ADHD-diagnoosin riski «Fan R, Leasure AC, Damsky W ym. Association of ato...»81.
- Atooppista ekseemaa sairastavien osteoporoosi- ja murtumariski on suurentunut. Tarkkaa syytä tähän ei tunneta, mutta on mahdollista, että se liittyy krooniseen tulehdukseen, muuta väestöä yleisempään D-vitamiinin puutteeseen tai systeemisten kortikosteroidien käyttöön «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63.
- Yhteys atooppisen ekseeman ja sydän- ja verisuonisairauksien sekä niihin liittyvien riskitekijöiden välillä on vielä epäselvä. Vaikeaa ekseemaa sairastavilla on ilmeisesti enemmän sydän- ja verisuonitauteja, mutta absoluuttinen riski on kuitenkin pieni «Silverberg JI. Comorbidities and the impact of ato...»82, «Ascott A, Mulick A, Yu AM ym. Atopic eczema and ma...»83. Toistaiseksi ei ole löytynyt viitteitä siitä, että atooppisen ekseeman tehokas hoito vähentäisi riskiä «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63. Tavanomaista ikään liittyvää seurantaa tarkemmasta seulonnan tarpeesta ei voida antaa suositusta «Pandher K, Ghamrawi RI, Heron CE ym. Controversial...»84.
Elämänlaatu ja psyykkiset tekijät
- Vaikea atooppinen ekseema heikentää merkittävästi elämänlaatua «Rehal B, Armstrong AW. Health outcome measures in ...»85. Ks. Atooppinen ekseema: vaikutus eri elämänalueisiin «Atooppinen ekseema: vaikutus eri elämänalueisiin»10.
- Atooppista ekseemaa sairastavilla on muuta väestöä enemmän unihäiriöitä ja kroonista väsymystä «Silverberg JI, Garg NK, Paller AS ym. Sleep distur...»86. Ruotsalaistutkimuksessa todettiin, että vaikeaa atooppista ekseemaa sairastavien todennäköisyys vakaviin unihäiriöihin oli 7,9-kertainen ja vaikeaan krooniseen väsymykseen 10,2-kertainen verrattuna verrokkeihin, jotka eivät sairastaneet atooppista ekseemaa «Theodosiou G, Montgomery S, Metsini A ym. Burden o...»87. Selittävä tekijä lienee kutina. Univaje ja väsymys voivat vaikuttaa myös keskittymiskykyyn.
- Ihottuman vaikeusaste, koettu stigma ja ihottuman aiheuttama mielialan lasku näyttävät olevan merkittävimmät ihottumaan liittyvää elämänlaatua heikentävät tekijät aikuisilla «Wittkowski A, Richards HL, Griffiths CE ym. The im...»88.
- Lapsen laaja-alainen atooppinen ekseema vaikuttaa lapsen ja perheen elämänlaatuun ainakin yhtä paljon kuin useimmat muut lasten pitkäaikaissairaudet «Beattie PE, Lewis-Jones MS. A comparative study of...»89. Lapsilla kutina, raapiminen ja ihon arkuus ovat haitallisimmin elämänlaatuun vaikuttavat seikat «Gånemo A, Svensson A, Lindberg M ym. Quality of li...»90.
- Ks. myös Aikakauskirja Duodecimin artikkeli Atooppinen ihottuma vaikuttaa elämänlaatuun ja elämänhaluun «Koulu L. Atooppinen ihottuma vaikuttaa elämänlaatu...»91, «https://www.duodecimlehti.fi/lehti/2020/22/duo15895»2.
- Psyykkiset tekijät ja stressi ovat tärkeitä atooppista ekseemaa pahentavia tekijöitä. Suomalaisessa seurantatutkimuksessa «Lammintausta K, Kalimo K, Raitala R ym. Prognosis ...»92 45–67 % erikoissairaanhoidossa hoidetuista vaikeaa atooppista ekseemaa sairastavista potilaista ilmoitti stressin suurimmaksi ekseemaansa pahentavaksi tekijäksi. Stressin mekanismit atooppisen ekseeman laukaisijana tunnetaan huonosti. Osa atooppista ekseemaa sairastavista potilaista voi hyötyä psykologisista hoitokeinoista (käyttäytymisterapeuttiset lähestymistavat, psykoedukaatio ja stressin vähentämiseen tähtäävät toimet) lääketieteellisen hoidon tukena «Chida Y, Steptoe A, Hirakawa N ym. The effects of ...»93, «Ersser SJ, Cowdell F, Latter S ym. Psychological a...»94.
- Atooppista ekseemaa sairastavan potilaan ja lapsipotilaan vanhempien hyvä sopeutuminen sairauteen auttaa sitoutumaan hoitoon ja takaa mahdollisimman onnistuneen hoitotuloksen. Potilasohjauksella pyritään parantamaan sairauden psyykkistä hallintaa ja voidaan ilmeisesti vähentää atooppisen ekseeman vaikeusastetta «Potilasohjauksella voidaan ilmeisesti vähentää atooppisen ekseeman vaikeusastetta.»B.
- Hoitoväsymys voi heikentää atooppisen ekseeman hoitotulosta, joten sen tunnistaminen on tarpeellista. Hoidon toteuttaminen voi alkaa tuntua turhauttavalta ja kuormittavalta, jolloin omahoitoon sitoutuminen heikkenee. Lääkärin ja hoitajan on hyvä ottaa hoitoväsymys puheeksi niin hoidon alussa kuin seurantakäynneilläkin etenkin, jos ilmenee, että hoidon toteutuksessa on ongelmia.
Atooppisen ekseeman hoidon yleisiä periaatteita
- Hoidon tavoitteena on pitkäkestoinen oireiden hallinta: oireiden minimointi, pahenemisvaiheiden määrän väheneminen ja vaikeusasteen lieveneminen sekä potilaan elämänlaadun ja työ- ja toimintakyvyn paraneminen.
- Hoito valitaan yksilöllisesti, ja siihen vaikuttavat muun muassa ihottuman laajuus
ja vaikeusaste, aiempien hoitojen vaste ja mahdolliset haittavaikutukset, potilaan
mahdollisuudet hoidon toteutukseen, hoitojen vasta-aiheet sekä potilaan muut sairaudet
ja lääkitykset.
- Suurimmalle osalle potilaista riittää paikallishoito.
- Atooppisen ekseeman hoitovaihtoehtojen porrastuksesta ks. kuva Atooppisen ekseeman hoitoalgoritmi «Atooppisen ekseeman hoitoalgoritmi»1.
- Lasten hoidon erityispiirteet kuvataan kappaleessa Lasten (0–16-vuotiaiden) atooppisen ekseeman hoidon erityispiirteet «A3»5.
Atooppisen ekseeman oireiden, vaikeusasteen ja hoitovasteen arvioinnin työkaluja
- Ekseeman vaikeusasteen kliiniseen arviointiin voidaan käyttää validoituja mittareita. Erityisesti erikoissairaanhoidossa sairauden vaikeusastetta kuvaavien mittareiden käyttö on suositeltavaa myös hoitovasteen seurannassa.
- Käypä hoito -työryhmä suosittelee ihottuman vaikeusasteen mittaamiseen Suomessa ensisijaisesti
EASI-mittaria.
- EASI (Eczema Area and Severity Index): atooppisen ekseeman vaikeusasteen määrityksessä käytettävä lääkärin tekemä arvio, joka huomioi ihottuman laajuuden (prosenttiosuutena) pään, vartalon ja ylä- ja alaraajojen alueilta erikseen arvioituna sekä ihottuman punoituksen, papulat (näppylät), turvotuksen, raapimisjäljet ja ihon jäkälöitymisen.
- EASI-75: EASI pienentynyt vähintään 75 % lähtötilanteesta.
- EASI-laskin ks. «hoi50077e.xlsx»3
- Taudin vaikeusasteen arvioinnissa on hyvä huomioida myös potilaan oma arvio taudin
oireista. POEM soveltuu hyvin kliinisessä työssä käytettäväksi «Leshem YA, Chalmers JR, Apfelbacher C ym. Measurin...»95.
- POEM (Patient Oriented Eczema Measure): potilaan omaan arvioon perustuva ihottumaoireita mittaava kysymyssarja. Ks. «https://www.nottingham.ac.uk/research/groups/cebd/documents/methodological-resources/ao-av153560-poem-for-self-completion-finnish-finland-version-1-25aug2016.pdf»3.
- Kutinaa ja kipua seurataan luotettavimmin NRS-mittarilla.
- NRS (numerical rating scale): potilas arvioi numeerisesti (0–10) ihon maksimikutinan tai -kivun viimeisten 24 tunnin aikana.
- Elämänlaadun mittarina käytetään ensisijaisesti DLQI-kyselyä. 4–16-vuotiaiden lasten
elämänlaadun mittarina käytetään CDLQI-kyselyä ja alle 4-vuotiaiden IDQOL-kyselyä.
- DLQI (Dermatology Life Quality Index): ihotauteihin liittyvä elämänlaatumittarina käytettävä kysymyssarja aikuisille. Ks. «https://www.cardiff.ac.uk/medicine/resources/quality-of-life-questionnaires/dermatology-life-quality-index»4 (ks. kohta Different language versions, other languages).
- CDLQI (Children's Dermatology Life Quality Index): ihotauteihin liittyvä elämänlaatumittarina käytettävä kysymyssarja 4–16-vuotiaille.
- IDQOL (Infant's Dermatology Quality of Life Index): alle 4-vuotiaiden atooppista ekseemaa sairastavien lasten vanhemmille suunnattu elämänlaatumittarina käytettävä kysymyssarja.
- DLQI-, CDLQI- ja IDQOL-kyselyissä arvioidaan ihotaudin vaikutusta elämänlaatuun viimeisen viikon aikana.
- Atooppisen ekseeman hoitotasapainon arvioimiseksi voidaan käyttää ADCT- tai RECAP-kyselyjä,
joista ADCT löytyy suomen- ja ruotsinkielisenä «Simpson E, Eckert L, Gadkari A ym. Validation of t...»96.
- ADCT (Atopic Dermatitis Control Tool): kyselyssä arvioidaan atooppisen ekseeman hoitotasapainoa edeltävän viikon ajalta. Ks. «https://www.adcontroltool.com/»5 (ks. kohta Information for patients ja valitse kielivalikosta suomi tai ruotsi).
- RECAP (Recap of atopic eczema) (4/2023 ei käännöstä suomeksi tai ruotsiksi).
- Ks. lisätietoa Atooppisen ekseeman arvioinnissa käytettävistä mittareista «Atooppisen ekseeman arvioinnissa käytettäviä mittareita»5.
Omahoito ja potilasohjaus
- Omahoito on atooppisen ekseeman hoidon kulmakivi. Omahoitoon kuuluvat
- aina perusvoiteet ja lääkevoiteet lääkärin ohjeiden mukaan
- pahentavien tekijöiden välttäminen (ks. kappale Pahentavat tekijät «A4»6).
- Päivittäinen pesu ei pahenna atooppista ekseemaa «Päivittäinen pesu lienee hyväksi atoopikon ekseemaiselle iholle.»C.
- Pesu poistaa iholta likaa, hikeä, karstaa ja bakteereita, jotka ärsyttävät ihoa.
- Pesuun käytetään tarvittaessa hajusteetonta, hapanta tai neutraalia pesunestettä tai
saippuaa.
- Atooppisen ihon puhdistuksessa käytetään usein saippuan sijasta perusvoiteita. Tämän käytännön hyödyistä ei kuitenkaan ole tutkimusnäyttöä «Tarr A, Iheanacho I. Should we use bath emollients...»97.
- Perusvoiteen käyttö pesun jälkeen estää ihon kuivumista ja voi sitoa ihoon kosteutta «Chiang C, Eichenfield LF. Quantitative assessment ...»98.
- Potilasohjaus on osa kokonaisvaltaista, moniammatillista pitkäaikaisen sairauden hoitoa.
Ohjauksen tavoitteena on parantaa potilaiden ja perheiden selviytymistaitoja ja hoitoon
sitoutumista lisäämällä ymmärrystä kroonisesta sairaudesta ja sen hoidosta.
- Potilasohjauksella voidaan ilmeisesti vähentää atooppisen ekseeman vaikeusastetta «Potilasohjauksella voidaan ilmeisesti vähentää atooppisen ekseeman vaikeusastetta.»B, ja ohjauksella on ollut mahdollista tehostaa muun muassa perusvoiteiden asianmukaista käyttöä «Cork MJ, Britton J, Butler L ym. Comparison of par...»99.
- Potilasohjauksen laadun ja määrän tarve vaihtelevat yksilöllisesti, eikä vaikuttavasta potilasohjauksesta voi antaa yksityiskohtaisia suosituksia.
- Ihon rasvauksesta on erityisen tärkeää antaa ohjeet potilaalle.
- Ks. omahoito-ohjeet
- Atooppisen ekseeman ohjattu omahoito aikuisilla «hoi50077c.pdf»1
- Atooppisen ekseeman ohjattu omahoito lapsilla «hoi50077d.pdf»2
- Ohje vanhemmille atooppisesta ekseemasta «Ohje vanhemmille atooppisesta ekseemasta»1
- Videot: Atooppinen ekseema aikuiset «Atooppinen ekseema -suosituksen videot (aikuiset)»2 ja «Yleistä atooppisesta ekseemasta (aikuiset) video»11 ja lapset «Atooppinen ekseema -suosituksen videot (lapset)»3 ja «Yleistä atooppisesta ekseemasta (lapset) video»12.
- Ks. omahoito-ohjeet
Paikallishoito
- Atooppisen ekseeman ensisijainen hoito on paikallishoito. Siihen kuuluu
- ihon säännöllinen rasvaus perusvoiteella 1–2 kertaa päivässä
- ekseema-alueiden hoito lääkevoiteilla ja perusvoiteilla.
- Paikallishoitoa tarvitaan yleensä myös UV-hoidon ja systeemisen lääkityksen yhteydessä.
Perusvoiteet
- Perusvoiteet voidaan jaotella tavanomaisiin perusvoiteisiin ja perusvoiteisiin, jotka sisältävät ihoon kosteutta sitovia aineita eli humektantteja (mm. karbamidi eli urea, glyseroli ja propyleeniglykoli).
- Perusvoiteilla hoidetaan ihon kuivuutta. Ne voivat sitoa ihoon kosteutta ja pehmentävät ihoa. Tavoitteena on ekseeman parempi hallinta ja uusiutumisen ehkäisy.
- Perusvoiteet ovat lievän atooppisen ekseeman pääasiallinen hoito ja aina osa myös
keskivaikean tai vaikean atooppisen ekseeman hoitoa. Yleensä 1–2 voitelukertaa päivässä
riittää.
- Jos iho on kuiva, atooppista ekseemaa sairastavan on oleellista käyttää perusvoidetta säännöllisesti varsinkin talvisin, vaikkei ihottumaa olisikaan.
- Perusvoidetta ja lääkevoidetta ei laiteta samanaikaisesti samalle ihoalueelle, vaan niiden käytön välillä on hyvä pitää tauko, jotta ensimmäisenä laitettu voide ehtii imeytyä.
- Perusvoiteet ilmeisesti vähentävät atooppisen ekseeman oireita, kuten ihon kutinaa,
ja pahenemisvaiheiden määrää «Perusvoiteet ilmeisesti vähentävät atooppisen ekseeman oireita.»B. Ne kosteuttavat ihoa ja vähentävät veden haihtumista ihosta. Kosteutta sitovat perusvoiteet
(sisältävät karbamidia tai glyserolia) saattavat vähentää pelkkää perusvoidetta (tai ei perusvoidetta) tehokkaammin ihottuman vaikeusastetta ja pahenemisvaiheiden
määrää «van Zuuren EJ, Fedorowicz Z, Christensen R ym. Emo...»100.
- Karbamidia sisältävät perusvoiteet saattavat aiheuttaa ihon kirvelyä, erityisesti akuutin, rikkiraavitun ekseeman hoidossa.
- Karbamidin käytöstä pienten lasten atooppisen ekseeman hoidossa ei ole tutkimustietoa. Kansainväliset hoitosuositukset suosittelevat välttämään karbamidia imeväisillä. Leikki-ikäisillä voidaan käyttää pienempiä pitoisuuksia kuin aikuisten hoidossa «Wollenberg A, Kinberger M, Arents B ym. EuroGuiDer...»101.
- Voidetyypin valinta riippuu yksilöllisistä tekijöistä.
- Potilaan on hyvä valita itse hänelle sopiva perusvoide «Williams HC. Clinical practice. Atopic dermatitis....»102, koska se parantaa hoitoon sitoutumista.
- Hoitoa aloitettaessa voi olla hyvä aloittaa keskirasvaisella perusvoiteella, joka useimmilla potilailla soveltuu parhaiten perushoitoon. Jos tunnin kuluttua perusvoiteen levittämisestä potilaasta tuntuu jo siltä, ettei ihoa olisi rasvattu lainkaan, tulisi siirtyä rasvaisempaan tai enemmän humektantteja sisältävään voiteiseen. Jos taas voide tuntuu liian rasvaiselta, saattaa olla hyvä siirtyä kevyempään.
- Jos jokin voidetyyppi aiheuttaa ihon kirvelyä, voidaan vaihtaa rasvaisempaan voiteeseen.
- Voidetyypin valinta vaihtelee myös vuodenajan mukaan: talvella tarvitaan rasvaisempia perusvoiteita, ja kesällä kevyemmät riittävät. Osa potilaista voi pärjätä kesäajan vähemmällä rasvauksella.
- Karvaisille ihoalueille tulisi käyttää kevyempiä, vähemmän öljypitoisia voiteita.
- Takyfylaksiasta eli ihon "väsymisestä" yhteen perusvoiteeseen pidemmän käytön aikana ei ole näyttöä «Hoare C, Li Wan Po A, Williams H. Systematic revie...»103.
- Reseptille tulisi kirjoittaa riittävän suuri määrä perusvoidetta. Jos voidellaan kaikki ihoalueet, voiteluun kuluu aikuisella 1,0–1,5 kiloa perusvoidetta kuukaudessa «Hannuksela-Svahn A, Hannuksela M. Ihotautien paika...»104.
- Jotta potilas saa Kela-korvattavasta perusvoiteesta peruskorvauksen, reseptiin merkitään "pitkäaikainen ihotauti".
- Lisätietoa perusvoiteiden ominaisuuksista ja käytöstä atooppisessa ekseemassa on lisätietoaineistossa «Lisätietoa perusvoiteiden ominaisuuksista ja humektanttien vaikutuksista»13.
Paikalliskortikosteroidit
- Paikalliskortikosteroidit ovat atooppisen ekseeman ensisijaiset lääkkeet.
- Tavallisesti atooppisen ekseeman hoitoon riittävät miedot tai keskivahvat paikalliskortikosteroidit, mutta hankalassa tai jäkälöityneessä ihottumassa voidaan käyttää vahvojakin paikalliskortikosteroideja. Ks. taulukko «Kokemukseen ja kliiniseen käyttöön perustuva työryhmän suositus siitä, minkä teholuokan kortikosteroidivoidetta käytetään aikuisilla (yli 16-vuotiailla) eri ihoalueille. Yli 75-vuotiailla suositellaan kortikosteroidien varovaisempaa käyttöä....»1.
- Kortikosteroidivoiteita saa käyttää ihottumasta johtuviin ihorikkoihin, ja niitä voi käyttää kesäisin ja UV-hoidon aikana.
- Paikalliskortikosteroidit jaetaan Suomessa neljään ryhmään: mietoihin, keskivahvoihin,
vahvoihin ja erittäin vahvoihin (ks. lisätietoa aiheesta «Paikalliskortikosteroidien luokittelu vaikutuksen voimakkuuden mukaan»14).
- Siirtyminen vahvempaan valmisteeseen lisää steroidin imeytymistä ihoon ja suorassa suhteessa haittavaikutuksia.
- Paikalliskortikosteroidien pääsy ihon läpi vaihtelee ja on runsainta ohuen ihon (kasvot, kaula, genitaalit) alueilla.
- Miedompia paikalliskortikosteroideja suositellaan helposti läpäisevälle ohuelle iholle ja vahvempia huonommin läpäiseville paksun ihon alueille (ks. taulukko «Kokemukseen ja kliiniseen käyttöön perustuva työryhmän suositus siitä, minkä teholuokan kortikosteroidivoidetta käytetään aikuisilla (yli 16-vuotiailla) eri ihoalueille. Yli 75-vuotiailla suositellaan kortikosteroidien varovaisempaa käyttöä....»1).
- Paikallisten kortikosteroidien pohjana on tavallisesti voide tai emulsiovoide, mutta markkinoilla on myös liuoksia karvaisten ihoalueiden, kuten hiuspohjan, hoitoon. Voidepohjalla on jonkin verran vaikutusta hoitotehoon. Rasvaisemmat voiteet voivat olla tehokkaampia «Nesbitt LT. Glucocorticoids. In: Bologna JL, Joriz...»105.
- Kortikosteroidivoiteiden käyttö lapsilla, ks. «A5»7.
- Kortikosteroidivoiteita käytetään jaksoittaisena hoitona ja lisäksi tarvittaessa ylläpitohoitona.
Ylläpitohoitoa kannattaa suosia etenkin keskivaikeassa ja vaikeassa sekä päivittäisen
hoitojakson jälkeen nopeasti uusiutuvassa atooppisessa ekseemassa. Ks. ohje «Atooppisen ekseeman hoito lääkevoiteella»28.
- Aikuisten jaksoittaisessa hoidossa kortikosteroidivoiteita käytetään yleensä 1–3 viikon
yhtämittaisina kuureina «Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106. Kasvoille käytetään yleensä lyhyempiä 1–2 viikon kuureja.
- Atooppisen ekseeman hoidossa pidetään taukoja kuurien välillä. Tauot ovat vähintään hoitojakson pituisia. Vaikeimmissa tapauksissa tämä voi kuitenkin johtaa ekseeman nopeaan uusiutumiseen. Uusiutumista voi jarruttaa keskivaikeassa ja vaikeassa atooppisessa ekseemassa ylläpitohoidolla.
- Ylläpitohoito: Ihottuman parannuttua keskivahvaa tai vahvaa kortikosteroidivoidetta
käytetään kerran päivässä kahdesti viikossa niille ihoalueille, joille ihottumaa tyypillisesti
tulee. Ylläpitohoitoa voidaan tarvittaessa käyttää usean kuukauden ajan. Ks. ohje
«Atooppisen ekseeman hoito lääkevoiteella»28.
- Kuurin jälkeinen ylläpitohoito paikallisella vahvalla kortikosteroidilla (vartalo ja raajat) kaksi kertaa viikossa näyttää estävän atooppisen ekseeman relapseja «Ylläpitohoito 2 kertaa viikossa vahvalla paikalliskortikosteroidilla näyttää ehkäisevän atooppisen ekseeman relapsia.»B ilman merkittävää ihon ohenemisen riskiä «Danby SG, Chittock J, Brown K ym. The effect of ta...»107.
- Kahdessa laajassa (n = yli 600) 4–5 kuukautta kestäneessä ylläpitohoitotutkimuksessa vahvalla kortikosteroidivoiteella ei havaittu olevan merkittäviä haittavaikutuksia «Hanifin J, Gupta AK, Rajagopalan R. Intermittent d...»108, «Berth-Jones J, Damstra RJ, Golsch S ym. Twice week...»109.
- Kliinisen kokemuksen perusteella ylläpitohoitoa voidaan toteuttaa myös keskivahvalla kortikosteroidivoiteella, mutta miedolla kortikosteroidivoiteella teho jää yleensä riittämättömäksi «Wollenberg A, Kinberger M, Arents B ym. EuroGuiDer...»101.
- Aikuisten jaksoittaisessa hoidossa kortikosteroidivoiteita käytetään yleensä 1–3 viikon
yhtämittaisina kuureina «Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106. Kasvoille käytetään yleensä lyhyempiä 1–2 viikon kuureja.
- Keskivahvaa tai vahvaa kortikosteroidia käytetään yleensä kerran päivässä. Ei ole näyttöä siitä, että useampi voitelukerta lisäisi hoidon tehoa «Williams HC. Established corticosteroid creams sho...»110, «Woods MT, Brown PA, Baig-Lewis SF ym. Effects of a...»111, «Bieber T, Vick K, Fölster-Holst R ym. Efficacy and...»112.
- Ei ole näyttöä siitä, että paikalliskortikosteroidit menettäisivät tehoaan pitkäaikaisessa jaksoittaisessa käytössä.
- Pelkkä kortikosteroidivoide vähentää myös ihon stafylokokkeja. Mitä vahvempi kortikosteroidi on, sitä tehokkaammin bakteeripitoisuus saadaan pienenemään «Stalder JF, Fleury M, Sourisse M ym. Local steroid...»113, «Nilsson EJ, Henning CG, Magnusson J. Topical corti...»114.
- Paikalliskortikosteroidien käyttöä rajoittavat niiden aiheuttamat haittavaikutukset,
joista tärkein on ihon oheneminen ihossa olevan kollageenin määrän vähentyessä «Oikarinen A, Autio P, Kiistala U ym. A new method ...»115.
- Ihon pysyvä oheneminen edellyttää usein kuukausien yhtäjaksoista käyttöä.
- Ohenemiselle alttiita ovat erityisesti jo valmiiksi ohuet ihoalueet ja vanhusten iho.
- Muita hoidon mahdollisia ihohaittavaikutuksia ovat striat, telangiektasiat ja mustelmat.
- Keskivahvojen tai vahvojen kortikosteroidivoiteiden pitkäaikainen, suositusten vastainen käyttö kasvoille voi aiheuttaa ruusufinnin kaltaisen ihottuman tai ihon pysyvän punoituksen, polttelun ja pistelyn, kun lääkitys tauotetaan ("paikallissteroidiaddiktio"). Ilmiötä esiintyy eniten naisilla kasvoissa ja genitaalialueella «Hajar T, Leshem YA, Hanifin JM ym. A systematic re...»116.
- Pitkäaikainen käyttö silmäluomiin voi aiheuttaa harmaakaihia ja glaukoomaa «Haeck IM, Rouwen TJ, Timmer-de Mik L ym. Topical c...»117.
- Systeemihaittavaikutukset, kuten hypokortisolismi, ovat harvinaisia mutta mahdollisia etenkin lasten laaja-alaista ekseemaa hoidettaessa «Axon E, Chalmers JR, Santer M ym. Safety of topica...»118.
| Ihoalue | Voiteen teholuokka | |||
|---|---|---|---|---|
| * Silmänympärysekseeman hoidossa kalsineuriinin estäjät ovat ensisijaisia. Plusmerkit kuvaavat työryhmän suosituksen vahvuutta. - = ei suositella |
||||
| I | II | III | IV | |
| Kasvot, kaula | +++ | + | - | - |
| Silmäluomet | +* | - | - | - |
| Taipeet, genitaalit | +++ | ++ | - | - |
| Vartalo, raajat | + | +++ | ++ | - |
| Kämmenet, jalkapohjat | - | ++ | +++ | + |
| Päänahka, niska | - | +++ | ++ | + |
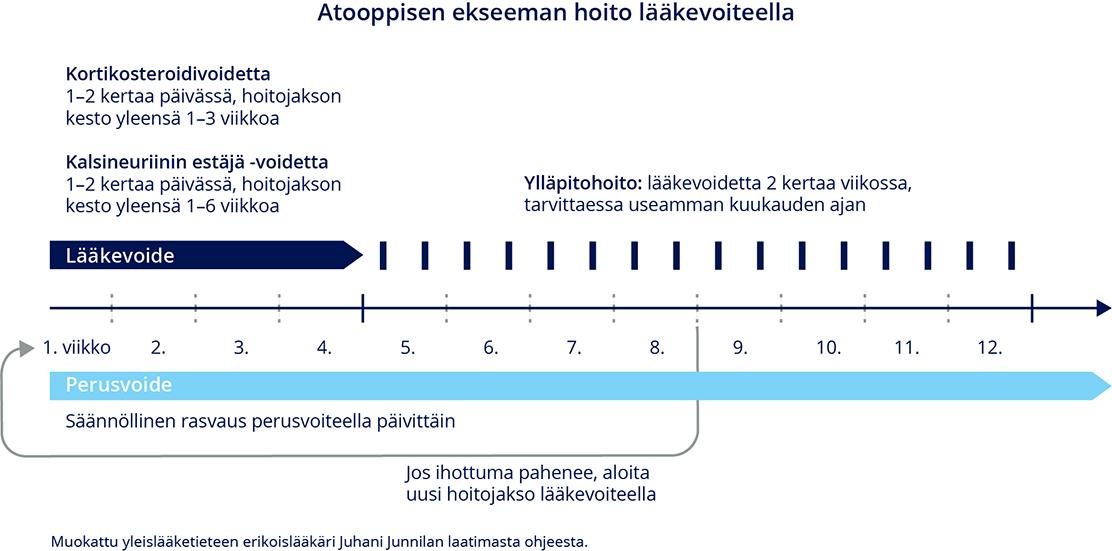
Atooppisen ekseeman hoito lääkevoiteella
Paikalliset kalsineuriinin estäjät (takrolimuusi ja pimekrolimuusi)
- Kalsineuriinin estäjät ovat atooppisen ekseeman toissijaisia lääkkeitä. Jos paikalliskortikosteroidilla
ei saada riittävää pitkäaikaista vastetta, käytetään takrolimuusivoidetta tai pimekrolimuusiemulsiovoidetta.
- Poikkeuksena ovat ohuen ihon alueet (esim. kasvot), joilla kalsineuriinin estäjiä voidaan käyttää myös ensisijaisina lääkevoiteina «Kang S, Paller A, Soter N ym. Safe treatment of he...»119, «Doss N, Reitamo S, Dubertret L ym. Superiority of ...»120.
- Silmänympäryksen atooppisen ekseeman hoidossa kalsineuriinin estäjät ovat ensisijaisia
kortikosteroideihin liittyvien haittavaikutusten vuoksi «Kang S, Paller A, Soter N ym. Safe treatment of he...»119, «Murrell DF, Calvieri S, Ortonne JP ym. A randomize...»121.
- Kalsineuriinin estäjät eivät vaikuta ihon kollageenisynteesiin eivätkä sen vuoksi ohenna ihoa pitkäaikaisessakaan hoidossa «Reitamo S, Rissanen J, Remitz A ym. Tacrolimus oin...»122, «Kyllönen H, Remitz A, Mandelin JM ym. Effects of 1...»123.
- Takrolimuusin käyttöaihe on keskivaikea tai vaikea atooppinen ekseema kahden vuoden
iästä alkaen.
- 0,03-prosenttinen takrolimuusivoide on tarkoitettu aikuisten, nuorten ja 2-vuotiaiden tai sitä vanhempien lasten hoitoon.
- 0,1-prosenttinen takrolimuusivoide on tarkoitettu aikuisten ja nuorten (16-vuotiaiden tai sitä vanhempien) hoitoon.
- Pimekrolimuusin käyttöaihe on lievä tai keskivaikea atooppinen ekseema 3 kuukauden iästä alkaen.
- Paikalliset kalsineuriinin estäjät lapsilla, ks. kohta «A5»7.
- Takrolimuusivoidetta tai pimekrolimuusiemulsiovoidetta käytetään ekseema-alueille
kahdesti päivässä, kunnes ekseema on parantunut. Ekseeman parannuttua pidetään tauko
voiteen käytössä. Oireiden ilmaantuessa aloitetaan heti uusi hoitojakso.
- Ylläpitohoito takrolimuusivoiteella on tehokas pahenemisvaiheiden estoon sekä lapsilla että aikuisilla. Ihottumaa hoidetaan kahdesti päivässä, kunnes se on rauhoittunut, minkä jälkeen voitelua jatketaan 2–3 kertaa viikossa. Ylläpitohoito on yhtä hyvin siedetty kuin voidepohjahoito «Ylläpitohoito takrolimuusivoiteella 2–3 kertaa viikossa alueille, joissa ihottumaa yleensä on esiintynyt, vähentää merkittävästi pahenemisvaiheita ja kortikosteroidivoiteiden käyttöä perusvoiteisiin verrattuna.»A. Ks. ohje «Atooppisen ekseeman hoito lääkevoiteella»28.
- Kortikosteroidivoiteen ja paikallisen kalsineuriinin estäjän samanaikainen käyttö samoille ihoalueille ei ilmeisesti paranna hoitotulosta pelkkään kortikosteroidivoiteeseen verrattuna. Tutkimuksessa, jossa pimekrolimuusiemulsiovoide yhdistettiin vahvaan kortikosteroidivoiteeseen samalle hoidettavalle alueelle, hoitotulokset eivät parantuneet pelkkään vahvaan kortikosteroidivoiteeseen verrattuna vaikeaa atooppista ekseemaa sairastavilla lapsilla «Meurer M, Eichenfield LF, Ho V ym. Addition of pim...»124.
- Herkkien ihoalueiden, kuten kasvojen, hoitaminen paikallisilla kalsineuriinin estäjillä ja muiden ihoalueiden hoitaminen kortikosteroidivoiteilla voi olla käytännöllinen ja kustannustehokas hoitovaihtoehto «Wollenberg A, Kinberger M, Arents B ym. EuroGuiDer...»101.
- 0,03-prosenttinen takrolimuusivoide on voidepohjaa ja mietoa kortikosteroidivoidehoitoa (hydrokortisoniasetaatti) tehokkaampi «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125.
- 0,1-prosenttinen takrolimuusivoide on voidepohjaa tehokkaampi ja on samantehoinen kuin keskivahva kortikosteroidivoide aikuisten atooppisen ekseeman hoidossa «Takrolimuusivoide (0,1-prosenttinen ja 0,03-prosenttinen) on tehokkaampi (EASI-pisteiden merkittävä väheneminen ja kutinan väheneminen) kuin voidepohja, ja 0,1-prosenttinen takrolimuusivoide on yhtä tehokas (mEASI pisteiden väheneminen) kuin hydrokortisoni-17-butyraattivoide atooppisen ekseeman hoidossa.»A. 0,1-prosenttinen takrolimuusivoide vaikuttaa 1-prosenttista pimekrolimuusiemulsiovoidetta tehokkaammalta aikuisten atooppisen ekseeman hoidossa «0,1-prosenttinen takrolimuusivoide on ilmeisesti 1-prosenttista pimekrolimuusiemulsiovoidetta tehokkaampi (EASI-alenema 54 % vs. 35 %) aikuisten atooppisen ekseeman lyhytaikaisessa hoidossa.»B, «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125.
- Pimekrolimuusiemulsiovoide on perusvoidetta tehokkaampi aikuisten lievän ja keskivaikean atooppisen ekseeman hoidossa «Pimekrolimuusiemulsiovoide on voidepohjaa tehokkaampi aikuisten atooppisen ekseeman hoidossa.»A. Pimekrolimuusiemulsiovoiteen ja miedon hydrokortisonipaikallishoidon välisiä vertailututkimuksia ei ole julkaistu. Pimekrolimuusi on atooppisen ekseeman hoidossa tehottomampi kuin keskivahva tai vahva paikalliskortikosteroidi (triamsinoloniasetonidi ja beetametasonivaleraatti) «Ashcroft DM, Chen LC, Garside R ym. Topical pimecr...»126.
- 0,1-prosenttinen takrolimuusivoide aiheuttaa noin 50–60 %:lle potilaista hoidon alkuvaiheessa ihon kuumotusta «Takrolimuusivoide aiheuttaa ihon kuumotusta hoidon alkuvaiheessa.»A. Se on hankalinta hoidon ensimmäisinä päivinä ja helpottaa useimmilla muutamassa vuorokaudessa voiteen säännöllisen käytön myötä «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125, «Ashcroft DM, Chen LC, Garside R ym. Topical pimecr...»126. Kuumotus on usein sitä voimakkaampaa, mitä hankalampi ihottuma on hoitoa aloitettaessa.
- 0,03- ja 0,1-prosenttisella takrolimuusivoiteella hoidettujen välillä ei vaikuttaisi olevan haittavaikutusten suhteen merkitsevää eroa 3 viikkoa ja 12 viikkoa kestäneiden tutkimusten perusteella «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125.
- 0,1-prosenttisella takrolimuusivoiteella ja 1-prosenttisella pimekrolimuusiemulsiovoiteella hoidettujen välillä ei näyttäisi 6 viikon kohdalla olevan haittavaikutusten suhteen merkitsevää eroa «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125.
- Ihon kuumotusta hoidon alkuvaiheessa voidaan usein lievittää hoitamalla ihottumaa paikalliskortikosteroidilla 1–2 viikon ajan, minkä jälkeen aloitetaan heti kalsineuriinin estäjä. Mikäli kuumotus tästä huolimatta on voimakasta ja vaikeuttaa hoidon jatkamista, voi tuntia ennen rasvausta otetusta asetyylisalisyylihaposta tai mahdollisesti ibuprofeenista olla apua kuumotuksen lievittämiseen «Mandelin J, Remitz A, Reitamo S. Effect of oral ac...»127. Ylläpitohoito on yhtä hyvin siedetty kuin voidepohjahoito, ja sillä voidaan ilmeisesti estää ihon kuumotuksen uusiutuminen «Ylläpitohoito takrolimuusivoiteella 2–3 kertaa viikossa alueille, joissa ihottumaa yleensä on esiintynyt, vähentää merkittävästi pahenemisvaiheita ja kortikosteroidivoiteiden käyttöä perusvoiteisiin verrattuna.»A.
- Takrolimuusin ja pimekrolimuusin imeytyminen verenkiertoon on vähäistä «Reitamo S, Wollenberg A, Schöpf E ym. Safety and e...»128, «Hanifin JM, Ling MR, Langley R ym. Tacrolimus oint...»129, «Ling M, Gottlieb A, Pariser D ym. A randomized stu...»130, eikä niiden käyttöön yleensä liity ihon bakteeri-, virus- tai sieni-infektioiden lisääntymistä «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125, «Ashcroft DM, Dimmock P, Garside R ym. Efficacy and...»131.
- Nykytiedon perusteella ei ole voitu osoittaa syöpäriskin lisääntyneen merkittävästi paikallisten kalsineuriinin estäjien käytön yhteydessä. Pisin seuranta-ajan mediaani on 27 vuotta «Legendre L, Barnetche T, Mazereeuw-Hautier J ym. R...»66. Ks. lisätietoa aiheesta «Syöpä- ja lymfoomariski kalsineuriinin estäjien paikallisen käytön yhteydessä»9.
- Kalsineuriinin estäjien korvattavuus, ks. Kelan sivusto «https://www.kela.fi/laake317»6.
Sidokset ja hauteet
- Joustavat sidokset suojaavat ihoa raapimiselta, mikä voi nopeuttaa ekseeman rauhoittumista. Sidokset soveltuvat raajojen rikkiraavitun ekseeman hoitoon. Sidoksen alla käytetään paikalliskortikosteroidia tai perusvoidetta. Kun hoidetaan erittäin sitkeää ihottumaa, paikallishoidon lisänä voidaan käyttää sinkkioksidipastaa sisältävää sidosta, joka saa olla paikallaan muutaman päivän.
- Paikalliskortikosteroidin imeytyminen ja teho voivat lisääntyä peittohoidolla eli okkluusiolla. Peittohoito soveltuu erityisesti pienialaisen paksuuntuneen ihottuman hoitoon. Peittosidoksena käytetään tavallisesti hydrokolloidilevyä, joka saa olla paikallaan jopa viikon. Hydrokolloidilevy kiinnittyy parhaiten, jos kortikosteroidi on liuospohjassa.
- Keittosuola- tai 0,25-prosenttinen sinkkisulfaattihaude soveltuu vetistävän ekseeman alkuvaiheen hoitoon. Hauteiden käyttö lopetetaan ihottuman kuivahdettua. Ks. potilasohjeet kostean kääreen käytöstä atooppisen ekseeman hoidossa suomeksi «Potilasohje kostean kääreen käytöstä atooppisen ekseeman hoidossa»15 ja ruotsiksi «Patientinformation om fuktigt bandage vid vård av atopiskt exem»16.
- Ks. videot Atooppisen ekseeman peittohoito (kääreet) lapsilla «Atooppisen ekseeman peittohoito (video)»17 ja Atooppisen ekseeman peittohoito aikuisilla «Atooppisen ekseeman peittohoito (video)»18.
Paikalliset antimikrobiset aineet
- Paikallisten antimikrobisten aineiden hyödystä yksinään käytettynä ei ole näyttöä atooppisen ekseeman hoidossa «George SM, Karanovic S, Harrison DA ym. Interventi...»132.
- Yhdistelmävalmisteet, jotka sisältävät paikalliskortikosteroidin ja antibiootin tai
antimikrobisen aineen, saattavat olla tehokkaampia kuin pelkkä paikalliskortikosteroidi
ihottumaoireiden lievittämisessä, mutta lisäteho on hyvin vähäinen «George SM, Karanovic S, Harrison DA ym. Interventi...»132.
- Paikallisia antiseptisiä aineita (klooriheksidiini, kaliumpermanganaatti) yhdistettynä kortikosteroidivoidehoitoon käytetään vetistävän tai infektoituneen atooppisen ekseeman hoitoon, mutta kontrolloituja tutkimuksia aiheesta ei ole tehty.
- Pitkäaikaista paikallisantibioottien käyttöä suositellaan vältettäväksi, jotta ei
kehity resistenttejä bakteerikantoja.
- Pelkkä kortikosteroidivoide vähentää ihon stafylokokkien määrää. Mitä vahvempi kortikosteroidi on, sitä tehokkaammin bakteeripitoisuus saadaan pienenemään «Stalder JF, Fleury M, Sourisse M ym. Local steroid...»113, «Nilsson EJ, Henning CG, Magnusson J. Topical corti...»114.
- Myös takrolimuusin on osoitettu vähentävän stafylokokkien määrää atooppisessa ekseemassa «Remitz A, Kyllönen H, Granlund H ym. Tacrolimus oi...»133.
- Ks. lisätietoa bakteereista atooppisessa ekseemassa «Lisätietoa bakteereista atooppisessa ekseemassa»19.
- Ks. myös Käypä hoito -suositus Ihoinfektiot «Ihoinfektiot»5.
- Sieni-infektiot:
- Ihon normaaliflooraan kuuluvien Malassezia-hiivojen merkitys atooppisessa ekseemassa on epäselvä ja antimykoottisten systeemisten tai paikallisten lääkkeiden tehosta ei ole riittävää näyttöä «Mayser P, Kupfer J, Nemetz D ym. Treatment of head...»134, «Kaffenberger BH, Mathis J, Zirwas MJ. A retrospect...»135, «Svejgaard El, Larsen PØ, Deleuran M ym. Treatment ...»136.
- Ks. lisätietoa ihon sieni-infektioista atooppisessa ekseemassa «Lisätietoa ihon sieni-infektioista atooppisessa ekseemassa»20.
UV-hoidot
- UV-hoitoa voidaan käyttää aikuisten keskivaikean ja vaikean atooppisen ekseeman hoidossa, ellei paikallishoidoilla saada riittävää vastetta. UV-hoitoa annetaan 2–3 kertaa viikossa 15–20 hoitokerran jaksoina. Suositeltava yläraja vuosittaiselle hoidolle on 2 jaksoa.
- Laitteet luokitellaan UV-spektrin mukaan «Eri valohoitolamppujen emittoiman UV-säteilyn aallonpituusspektrit»29. Suomessa atooppisen ekseeman hoitoon käytetään pääasiassa kapeakaistaista UVB-hoitoa
ja toissijaisesti SUP-hoitoa.
- SUP-hoito (selektiivinen UV-hoito, aallonpituusalue vastaa suomalaista kesäaurinkoa) on väistyvä hoitomuoto.
- UV-hoitoja antavien laitosten tulee noudattaa viranomaisten antamia ohjeita.
- UV-hoidon vaikutus perustuu immunologisen tulehdusprosessin vaimentamiseen. UV-säteily vaikuttaa tulehdussoluihin, tulehdusvälittäjäaineisiin ja antimikrobiaalisiin peptideihin «Krutmann J, Morita A. Mechanisms of ultraviolet (U...»137, «Tintle S, Shemer A, Suárez-Fariñas M ym. Reversal ...»138, «Gambichler T, Skrygan M, Tomi NS ym. Changes of an...»139.
- Aikuispotilaiden ensisijainen UV-hoito on kapeakaistainen UVB (loisteputki TL01, aallonpituusalue 311 ± 2 nm) «Lübbe J. Secondary infections in patients with ato...»140, «Garritsen FM, Brouwer MW, Limpens J ym. Photo(chem...»141. Tutkimustietoa UV-hoidon annoksista, hoidon kestosta, hoitovasteen pysyvyydestä ja mahdollisista pitkäaikaishaitoista atooppisen ekseeman hoidossa on vähän. UV-hoitoon liittyviä elämänlaatututkimuksia ei ole. Jotta UV-hoito pystytään asemoimaan oikein hoidon porrastukseen, erityisesti kapeakaistaisen UVB-hoidon pitkäaikaisturvallisuudesta ja hoitovasteista tarvittaisiin lisätutkimuksia, joissa käytetään yhtenäisiä mittareita «Musters AH, Mashayekhi S, Harvey J ym. Phototherap...»142. Kapeakaistainen UVB-hoito ilmeisesti vähentää atooppisen ekseeman oireita ja löydöksiä aikuisilla «Kapeakaistainen UVB-hoito ilmeisesti vähentää aikuisten atooppisen ekseeman oireita ja löydöksiä. Hoitovasteen pituudesta ei ole tietoa.»B.
- Remission kestosta on melko vähän tietoa: 3 kuukauden kuluttua hoidon päättymisestä suotuisa vaste on ilmeisesti nähtävissä noin puolella potilaista «Reynolds NJ, Franklin V, Gray JC ym. Narrow-band u...»143.
- Mahdollisia akuutteja haittavaikutuksia ovat punekynnyksen ylittävästä annoksesta johtuva ihon punoitus (UV-eryteema) ja herpes simplex -infektion aktivoituminen iholla.
- Ihosyöpäriskiä suurentavasta vaikutuksesta ei ole tietoa.
- Teoreettisen mallinnuksen perusteella 450 hoitokertaa kapeakaistaista UVB-hoitoa saattaisi sopia hoitokertojen ylärajaksi «Ibbotson SH, Bilsland D, Cox NH ym. An update and ...»144, «Diffey BL. Factors affecting the choice of a ceili...»145. Konsensusta asiasta ei kuitenkaan ole.
- Suomen Ihotautilääkäriyhdistyksen valojaos on laatinut suomalaisille ihotyypeille sovelletut ohjeelliset annoskaaviot (ks. lisätietoa aiheesta Ihosairauksien hoito kapeakaistaisella UVB:llä «hoi50062a.pdf»4).
- Katso kapeakaistaisen UVB-hoidon potilasohje suomeksi «https://hoito-ohjeet.fi/OhjepankkiVSSHP/Kapeakaista-UVB%20valohoito.pdf»7 ja ruotsiksi «https://hoito-ohjeet.fi/OhjepankkiVSSHPRuotsi/UV311.pdf»8.
- UV-hoitojen vasta-aiheita ovat
- infektoitunut (bakteeri- ja virusinfektiot) tai hyvin ärtynyt ekseema
- ihottuman akuutti tilanne tulee ensin rauhoittaa
- valoherkkyys (suhteellinen vasta-aihe)
- aiempi ihosyöpä (suhteellinen vasta-aihe)
- tiettyjen lääkkeiden käyttö (valoherkistäjät, immunosuppressiiviset lääkkeet, kalsineuriinin estäjät) (suhteellinen vasta-aihe)
- siklosporiinihoito.
- infektoitunut (bakteeri- ja virusinfektiot) tai hyvin ärtynyt ekseema
- UV-hoitojen käyttöä rajoittavat
- hoidon sitovuus (tyypillinen hoitotiheys 2–3 kertaa viikossa yhteensä 15–20 kertaa)
- hoidon saatavuus, matkat hoitoon
- hoidon kustannukset.
- UVA1-hoitoa (aallonpituusalue 340–400 nm) ei Suomessa käytetä atooppisen ekseeman hoitoon.
- Lasten UV-hoitojen pitkäaikaisturvallisuudesta ei ole luotettavaa tutkimusnäyttöä. Lapsille UV-hoitoa (kapeakaistainen UVB tai SUP) käytetään vain harkiten erikoislääkärin valvonnassa.
- Ilmastohoito (auringonvalohoito, helioterapia) saattaa lievittää atooppista ekseemaa ja parantaa potilaiden elämänlaatua. Suotuisan vaikutuksen kestosta ei ole luotettavaa näyttöä «Ilmastohoito saattaa lievittää atooppista ihottumaa ja parantaa potilaiden elämänlaatua. Suotuisan vaikutuksen kestosta ei ole luotettavaa näyttöä.»C. Ilmastohoitoa ei kustanneta julkisin varoin.
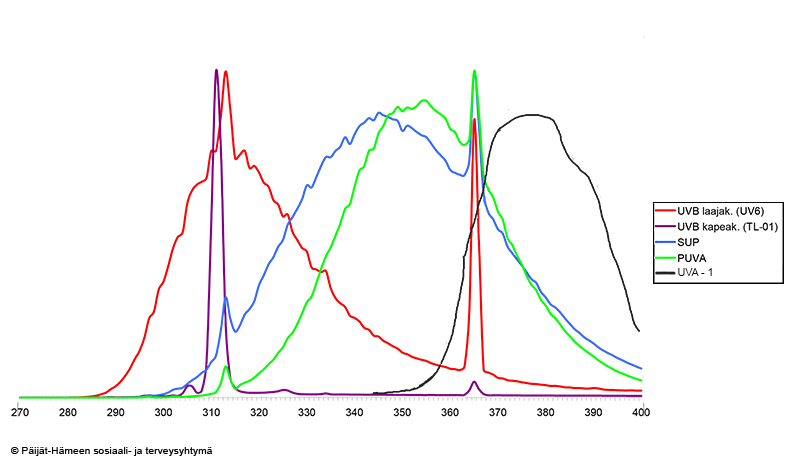
Eri valohoitolamppujen emittoiman UV-säteilyn aallonpituusspektrit
© Tapio Rantanen
Systeeminen pitkäaikainen lääkehoito
- Atooppisen ekseeman systeemisen lääkityksen tavoitteena on ekseeman pitkäaikainen hallinta. Lääkityksen aloittaa ja sitä seuraa ihotautien tai lastentautien erikoislääkäri. Ekseeman pitkäaikaishallintaan käytettäviä lääkkeitä ovat perinteiset immunosuppressiiviset lääkkeet, biologiset lääkkeet ja JAK-estäjät. Systeemisen lääkehoidon aloitusta harkitaan vaikeaa atooppista ekseemaa sairastavilla potilailla, joilla ei saada riittävää hoitovastetta hyvin toteutuneella paikallishoidolla ja mahdollisella UV-hoidolla.
- Perinteisistä immunosuppressiivisista lääkkeistä vain siklosporiinilla on virallisena käyttöaiheena atooppinen ekseema. Abrositinibin, barisitinibin, dupilumabin, tralokinumabin ja upadasitinibin virallisena käyttöaiheena on keskivaikea ja vaikea atooppinen ekseema.
- Systeemisen lääkehoidon hoitovastetta ja haittoja tulee seurata säännöllisesti.
- Hoitovaste suositellaan arvioitavaksi ensimmäisen kerran 12–16 viikon kuluttua hoidon aloittamisesta ja sen jälkeen säännöllisesti.
- Hyvässä hoitovasteessa todetaan yleensä systemaattista paranemista sekä potilaan kokemissa oireissa että ihottuman objektiivisessa vaikeusasteessa.
- Systeemiset lääkkeet eroavat toisistaan tehon, haittavaikutusten, vasta-aiheiden,
hoidon vaatiman seurannan sekä yksilölle ja yhteiskunnalle aiheutuvien kustannusten
osalta. Potilaalle sopiva lääkitys valitaan yksilöllisesti.
- Myös lääkkeiden peruskorvattavuuden kriteerit vaikuttavat usein lääkehoidon käytännön toteuttamismahdollisuuksiin. Ks. Lääkekohtaiset ajantasaiset korvausehdot Kelan sivustolta «https://www.kela.fi/yhteistyokumppanit-laakekorvaukset-laakkeiden-korvausoikeudet»9.
- Biologisten lääkkeiden ja JAK-estäjien hoitovasteen lääkekustannukset esitetään lisätietomateriaalissa «The number needed to treat (NNT) and cost per responder for systemic therapies for moderate-to-severe atopic dermatitis»21.
- Tämä luku käsittelee aikuispotilaita. Lasten systeeminen lääkehoito ks. kohta Lasten (0–16-vuotiaiden) atooppisen ekseeman hoidon erityispiirteet «A3»5.
- Terveyskylän reumataloon on koottu ohjeita useimmista atooppisen ekseeman hoidossa
käytettävistä systeemisistä lääkkeistä «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeiden-ohjeet»10. Sivuilta löytyy ohjeita infektioalttiuden arvioinnista, rokotuksista ja seurantaverikokeista
«https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeisiin-liittyv%C3%A4t-seurantakokeet»11. Ks. Myös kansallinen rokotusohjelma «https://thl.fi/fi/web/infektiotaudit-ja-rokotukset/tietoa-rokotuksista/kansallinen-rokotusohjelma»12.
- Ohjeistettu verikoeseuranta voidaan toteuttaa myös perusterveydenhuollossa.
- Ennen systeemisten lääkkeiden aloittamista päivitetään tarvittaessa kansalliseen rokotusohjelmaan
kuuluvat rokotukset ja selvitetään immuniteetti vesirokolle ja tarvittaessa tuhkarokolle.
- Kausi-influenssarokotetta suositellaan kaikille.
- Pneumokokkirokotetta suositellaan yli 65-vuotiaille ja lääkärin harkinnan mukaan muillekin.
- Vyöruusurokotetta voidaan harkita erityisesti yli 50-vuotiaille potilaille, joille suunnitellaan JAK-estäjien aloitusta.
- Immunosuppressiivista lääkitystä käytettäessä
- Suun ja hampaiden hyvästä terveydestä on huolehdittava koko lääkityksen ajan.
- Lääkitys tauotetaan tarvittaessa äkillisissä infektioissa ja leikkausten yhteydessä.
- Ihon säännöllistä paikallishoitoa tulee yleensä jatkaa systeemisen lääkehoidon rinnalla.
Perinteiset immunosuppressiiviset lääkkeet
- Kelvollisia hoitotutkimuksia immunosuppressiivisista lääkkeistä atooppisen ekseeman
hoidossa on tehty vain vähän.
- Hoitovasteen arviointi on vaihdellut, ja potilasmäärät ovat olleet pieniä.
- Lääkkeiden tehosta tarvitaan lisää tutkimusnäyttöä.
- Siklosporiini
- Siklosporiini näyttää lievittävän hoitoresistentin atooppisen ekseeman oireita lyhytaikaisessa hoidossa «Siklosporiini saattaa vähentää aikuisten atooppisen ekseeman kliinisiä löydöksiä lyhytaikaisessa (6–8 viikkoa) hoidossa.»C.
- Pitkäaikaishoitoa (yli 1–2 vuotta) pyritään välttämään siklosporiiniin liittyvien haittavaikutusten vuoksi.
- Siklosporiinihoitoa ei tule yhdistää UV-hoitoihin suurentuneen fotokarsinogeneesiriskin vuoksi «Sugie N, Fujii N, Danno K. Cyclosporin-A suppresse...»146.
- Siklosporiinin annostus, vasta-aiheet, haittavaikutukset ja seurantakokeet on esitetty Käypä hoito -suosituksen Psoriaasi ja nivelpsoriaasi taulukossa 5: Siklosporiinilääkityksessä huomioon otettavia asioita «Psoriaasi ja nivelpsoriaasi»6.
- Metotreksaatti
- Metotreksaatti saattaa olla tehokas atooppisen ekseeman hoidossa, vaikka tutkimusnäyttö on vähäistä eikä lumekontrolloituja tutkimuksia ole «Metotreksaatti saattaa vähentää atooppisen ekseeman aktiivisuutta lyhytaikaisessa hoidossa yhtä paljon kuin atsatiopriini ja siklosporiini, mutta löydöksen kliinistä merkitystä on vaikea arvioida ilman lumevertailua.»C.
- Hoitovaste saavutetaan hitaasti, useiden viikkojen aikana.
- Metotreksaatti sopii pitkäaikaishoitoon.
- Metotreksaatti on teratogeeninen.
- Lääkityksen toteuttaminen vaatii poikkeuksellisen annostelunsa vuoksi erityistä huolellisuutta.
- Metotreksaatti voidaan annostella myös ihonalaisena injektiona, jolloin sen hyötyosuus ja siedettävyys ovat paremmat (pahoinvointi on vähäisempää).
- Metotreksaatin annokset, vasta-aiheet, haittavaikutukset ja seurantakokeet on esitetty Käypä hoito- suosituksen Psoriaasi ja nivelpsoriaasi taulukossa 4: Metotreksaattilääkityksessä huomioon otettavia asioita «Psoriaasi ja nivelpsoriaasi»6
- Atsatiopriini
- Atsatiopriini saattaa olla tehokas atooppisen ekseeman hoidossa, mutta tutkimusnäyttö
on vähäistä «Atsatiopriini saattaa vähentää aikuisten atooppisen ekseeman aktiivisuutta lumelääkkeeseen verrattuna, mutta tehon kliinistä suuruutta on vaikea arvioida.»C
- Yhdessä pienessä RCT-tutkimuksessa atsatiopriini ja metotreksaatti olivat yhtä tehokkaita atooppisen ekseeman hoidossa «Schram ME, Roekevisch E, Leeflang MM ym. A randomi...»147.
- Atsatiopriini saattaa soveltua pitkäaikaiskäyttöön.
- Tiopuriinimetyylitransferaasi (TPMT) -geenin polymorfioiden tutkimista suositellaan ennen atsatiopriinihoidon aloittamista.
- Hoidon tyypillisimpiä haittavaikutuksia ovat maha-suolikanavan oireet, verenkuvamuutokset ja maksa-arvojen suureneminen.
- Lisätietoa atsatiopriinihoidosta ja seurantaverikokeista löytyy Terveyskylän Reumatalon ohjeista «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeiden-ohjeet»10 ja «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeisiin-liittyv%C3%A4t-seurantakokeet»11.
- Atsatiopriini saattaa olla tehokas atooppisen ekseeman hoidossa, mutta tutkimusnäyttö
on vähäistä «Atsatiopriini saattaa vähentää aikuisten atooppisen ekseeman aktiivisuutta lumelääkkeeseen verrattuna, mutta tehon kliinistä suuruutta on vaikea arvioida.»C
- Mykofenolaattimofetiili
- Mykofenolaattimofetiili saattaa vähentää atooppisen ekseeman oireita, mutta luotettava tutkimusnäyttö puuttuu «Mykonefolaattimofetiili saattaa vähentää atooppisen ekseeman aktiivisuutta yhtä paljon kuin siklosporiini, mutta luotettava näyttö puuttuu ja kliinistä merkitystä on vaikea arvioida ilman lumevertailua.»D.
- Käyttökokemus mykofenolaattimofetiilista atooppisen ekseeman hoidossa Suomessa on vähäistä.
- Lisätietoa mykofenolaattihoidosta ja seurantaverikokeista löytyy Terveyskylän Reumatalon ohjeista «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeiden-ohjeet»10 ja «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeisiin-liittyv%C3%A4t-seurantakokeet»11.
Biologiset lääkkeet
Dupilumabi
- Dupilumabi on IL-4Rα-vasta-aine, joka estää sytokiini IL-4:n ja IL-13:n vaikutusta.
- Dupilumabi vähentää atooppisen ekseeman vaikeusastetta.
- Viikolla 16 EASI-75-vasteen saavutti ilman samanaikaista lääkevoiteiden käyttöä dupilumabiannoksella 300 mg joka toinen viikko 48 % potilaista ja lumeella 13 % potilaista «Dupilumab (initial dose of 600 mg followed by 300 mg every other week) alone or in combination with topical treatments compared to placebo increases the proportion of adults with moderate to severe atopic dermatitis reaching EASI-75 at week 16 when compared to placebo (48–66% vs. 13–25%).»A. Samanaikaisen lääkevoiteen käytön aikana vastaavat luvut olivat 66 % ja 25 %.
- Dupilumabi vähentää ihon kutinaa ja parantaa potilaiden elämänlaatua.
- Lumekontrolloidussa tutkimuksessa dupilumabin teho näytti säilyvän vuoden seurannassa «Blauvelt A, de Bruin-Weller M, Gooderham M ym. Lon...»148.
- Dupilumabi näyttää olevan tehokas myös 6–17-vuotiailla lapsilla ja nuorilla «In children (6-11 years) with severe atopic dermatitis dupilumab (100 mg every two weeks for children with weight of 15 to <30 kg and 200 mg every two weeks for children with weight of ≥30 kg) with topical corticosteroids appears to increase the proportion of patients reaching EASI-75 at week 16 when compared to placebo (67–70% vs. 27%).»B, «Simpson EL, Paller AS, Siegfried EC ym. Efficacy a...»149.
- Dupilumabin teho on osoitettu myös vaikeassa tyypin 2 astmassa (ks. Käypä hoito -suositus Astma «Astma»7), vaikeassa kroonisessa polypoottisessa rinosinuiitissa ja prurigo nodulariksessa «Husein-ElAhmed H, Steinhoff M. Dupilumab in prurig...»150.
- Dupilumabin tehoa ja turvallisuutta on tutkittu suorissa vertailevissa tutkimuksissa, joissa dupilumabia verrattiin upadasitinibiin «Blauvelt A, Teixeira HD, Simpson EL ym. Efficacy a...»151 ja abrositinibiin «Reich K, Thyssen JP, Blauvelt A ym. Efficacy and s...»152, «Bieber T, Simpson EL, Silverberg JI ym. Abrocitini...»153.
- 16 viikon seurannassa suurempi osa potilaista saavutti EASI-75-vasteen upadasitinibilla
annoksella 30 mg/vrk kuin dupilumabilla annoksella 300 mg joka toinen viikko (71 %
vs. 61 %) «Blauvelt A, Teixeira HD, Simpson EL ym. Efficacy a...»151. Upadasitinibi tehosi nopeammin kutinaan.
- Viikolla 16 EASI-90-vasteen saavutti upadasitinibilla 61 % ja dupilumabilla 39 % potilaista.
- Viikolla 24 EASI-75-vasteen saavuttaneiden osuudet olivat dupilumabiryhmässä 60 % (95 % luottamusväli 54–65) ja upadasitinibiryhmässä 64 % (95 % luottamusväli 59–69).
- Kun verrattiin abrositinibia annoksella 200 mg/vrk ja dupilumabia annoksella 300 mg
joka toinen viikko, abrositinibin todettiin tehoavan nopeammin kutinaan «Reich K, Thyssen JP, Blauvelt A ym. Efficacy and s...»152, «Bieber T, Simpson EL, Silverberg JI ym. Abrocitini...»153. Viikolla 16 EASI-75-vasteissa ei ollut tilastollisesti merkitsevää eroa «Bieber T, Simpson EL, Silverberg JI ym. Abrocitini...»153.
- Viikolla 16 EASI-90-vasteen saavutti 54 % abrositinibilla ja 42 % dupilumabilla «Reich K, Thyssen JP, Blauvelt A ym. Efficacy and s...»152.
- Dupilumabilla hoitovaste saavutetaan tyypillisesti hitaammin kuin JAK-estäjillä; vaste näkyy 1–2 kuukauden kuluttua hoidon alusta ja paranee edelleen useiden kuukausien ajan.
- 16 viikon seurannassa suurempi osa potilaista saavutti EASI-75-vasteen upadasitinibilla
annoksella 30 mg/vrk kuin dupilumabilla annoksella 300 mg joka toinen viikko (71 %
vs. 61 %) «Blauvelt A, Teixeira HD, Simpson EL ym. Efficacy a...»151. Upadasitinibi tehosi nopeammin kutinaan.
- Vuoden seurannassa dupilumabin haitat ovat pääosin verrattavissa lumeeseen «Blauvelt A, de Bruin-Weller M, Gooderham M ym. Lon...»148, «Blauvelt A, Guttman-Yassky E, Paller AS ym. Long-T...»154. Dupilumabi-hoidon yleisin haittavaikutus on silmän sidekalvotulehdus, joka on yleensä lievä tai keskivaikea «Siegels D, Heratizadeh A, Abraham S ym. Systemic t...»155. Sen hoitoon käytetään yleensä kostutustippoja ja -geelejä, syöttösolun vakauttajia tippoina ja antihistamiinisilmätippoja. Jos oireet ovat vaikeat, suositellaan silmälääkärin konsultaatiota «Thyssen JP, Heegaard S, Ivert L ym. Management of ...»156.
- Dupilumabi ei lisää yleistä infektioherkkyyttä, eikä sitä käytettäessä tarvita laboratorioseurantaa.
Tralokinumabi
- Tralokinumabi on IL-13-vasta-aine. Sitä ei tällä hetkellä ole saatavilla Suomessa.
- Ks. lisätietoa «Tralokinumab in the treatment of adult atopic dermatitis»22.
JAK-estäjät
- JAK-estäjät ovat tablettimuotoisia lääkkeitä, joiden vaikutusmekanismi perustuu solunsisäisen JAK-STAT-signalointireitin estämiseen, mikä johtaa useiden sytokiinien vaikutuksen vähenemiseen. Ks. lisätietoa JAK-estäjistä «Janus-kinaasin estäjät (JAK-estäjät)»23.
- JAK-estäjien hoitovaste atooppisessa ekseemassa alkaa nopeasti, tyypillisesti viikoissa.
- JAK-estäjät näyttävät lisäävän infektioalttiutta. Erityisesti herpes simplex -infektioiden ja vyöruusun riski on tutkimuksissa ollut suurentunut. Lisäksi JAK-estäjien haittavaikutuksina voi esiintyä muun muassa aknen kaltaista ihottumaa, pahoinvointia, verenkuvamuutoksia ja rasva-arvojen suurenemista.
- JAK-estäjillä on interaktioita, jotka on syytä huomioida.
- Lisätietoa barisitinibi- ja upadasitinibi-hoidosta ja seurantaverikokeista löytyy
Terveyskylän Reumatalon ohjeista «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeiden-ohjeet»10 ja «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeisiin-liittyv%C3%A4t-seurantakokeet»11.
- Abrositinibilla voidaan noudattaa samansuuntaisia lääkitys- ja verikoeseurantaohjeita kuin barisitinibilla ja upadasitinibilla.
- Nivelreumapotilailla, joilla on tiettyjä riskitekijöitä, on havaittu suurentunut haittavaikutusten
riski JAK-estäjähoidossa verrattuna hoitoon TNF-alfan estäjillä. Ks. Fimea «https://fimea.fi/documents/147152901/159465460/AK+inhibitors+DHPC+Final-FI+2023-03-15.pdf/8481297f-801a-0bf7-9ca3-cb4a5cf096be/AK+inhibitors+DHPC+Final-FI+2023-03-15.pdf?t=1678882468734»13.
- Näitä haittoja ovat merkittävät sydän- ja verisuonitapahtumat, laskimotromboembolia, syövät, vakavat infektiot ja kuolleisuus.
- Suosituksen mukaan JAK-estäjiä tulisi käyttää seuraavilla potilasryhmillä vain, jos muita soveltuvia hoitovaihtoehtoja ei ole käytettävissä: ≥ 65-vuotiaat, nykyisin tupakoivat tai aiemmin pitkään tupakoineet, potilaat, joilla on muita sydän- tai verisuonitapahtumien riskitekijöitä tai syöpään liittyviä riskitekijöitä.
- JAK-estäjien käytössä on noudatettava varovaisuutta, jos potilaalla on muita kuin yllä mainittuja laskimotromboembolian riskitekijöitä.
- Ylläpitohoidossa on harkittava pienimmän tehokkaan annoksen käyttöä.
- Toistaiseksi ei ole olemassa suoria vertailevia tutkimuksia eri JAK-estäjien tehosta ja turvallisuudesta atooppisen ekseeman hoidossa.
Abrositinibi
- Abrositinibi vähentää atooppisen ekseeman vaikeusastetta.
- Viikolla 12 EASI-75-vasteen saavutti ilman samanaikaista lääkevoiteiden käyttöä 200 mg:n päiväannoksella 61–63 % ja lumeryhmässä 10–12 % potilaista «Abrocitinib in dose of 100 or 200 mg once daily alone or in combination with topical treatment increases the proportion of patients (age at least 12 years) with moderate-to-severe atopic dermatitis achieving EASI-75 response at week 12, when compared to placebo (100 mg: 40-58.7%, 200 mg: 61.»A. Vastaavat luvut samanaikaisen lääkevoiteen käytön aikana olivat 70 % ja 27 %.
- Lumeeseen verrattuna abrositinibi ilmeisesti vähentää kutinaa ja parantaa potilaiden elämänlaatua.
- Abrositinibin ja dupilumabin suora vertailu, ks. kohta Dupilumabi «A6»8.
- RCT-tutkimuksissa abrositinibille ominaisena haittavaikutuksena on esiintynyt pahoinvointia (abrositinibiryhmässä 15 % vs. lumeryhmässä 2 %) «Simpson EL, Silverberg JI, Nosbaum A ym. Integrate...»157.
Barisitinibi
- Barisitinibi näyttää vähentävän atooppisen ekseeman vaikeusastetta.
- Viikolla 16 EASI-75-vasteen saavutti ilman samanaikaista lääkevoiteiden käyttöä 4 mg:n päiväannoksella 21–25 % ja lumeryhmässä 6–9 % potilaista «Baricitinib (2-4 mg/day) treatment alone or in combination with topical treatment appears to increase the proportion of adult patients with moderate-to-severe atopic dermatitis achieving EASI-75 response at week 16, when compared to placebo (2 mg: 18-43%, 4 mg: 21-48%, and placebo 6-23%).»B. Vastaavat luvut samanaikaisen lääkevoiteen käytön aikana olivat 48 % ja 23 %.
- Barisitinibi saattaa vähentää ihon kutinaa ja parantaa potilaiden elämänlaatua.
- RCT-tutkimuksissa havaittiin JAK-estäjille tyypillisiä haittavaikutuksia, ks. kohta JAK-estäjät «A11»9.
- Barisitinibilla on käyttöaihe myös nivelreuman ja pälvikaljun hoitoon.
Upadasitinibi
- Upadasitinibi vähentää atooppisen ekseeman vaikeusastetta.
- Viikolla 16 EASI-75-vasteen saavutti ilman samanaikaista lääkevoiteiden käyttöä 30 mg:n päiväannoksella 73–80 % ja lumeryhmässä 13–16 % potilaista «Oral upadacitinib at the dose of 15-30mg daily alone or in combination with topical treatment increases the proportion of adult patients with moderate-to-severe atopic dermatitis achieving EASI75 response at week 16, when compared to placebo (15 mg: 60.1-69.»A. Samanaikainen lääkevoiteen käyttö ei näytä lisäävän hoitovasteen saaneiden määrää.
- Upadasitinibi vähentää ihon kutinaa ja parantaa potilaiden elämänlaatua.
- Alaryhmäanalyyseissa 12–17-vuotiaiden nuorten tulokset vastasivat aikuisten tuloksia «Guttman-Yassky E, Teixeira HD, Simpson EL ym. Once...»158.
- Upadasitinibin ja dupilumabin suora vertailu, ks. kohta Dupilumabi «A6»8.
- RCT-tutkimuksissa upadasitinibin yleisenä haittavaikutuksena on esiintynyt aknen kaltaista ihottumaa (30 mg:n annoksella 15 % ja lumeella 2 %) «Mendes-Bastos P, Ladizinski B, Guttman-Yassky E ym...»159.
- Upadasitinibilla on käyttöaihe myös nivelreumaan, nivelpsoriaasiin, aksiaaliseen spondylartriittiin, haavaiseen paksusuolitulehdukseen ja Crohnin tautiin.
| Lääke | Dupilumabi | Abrositinibi | Barisitinibi | Upadasitinibi |
|---|---|---|---|---|
| EASI = Eczema Area and Severity Index, IL= interleukiini, JAK = januskinaasi * Atooppisen ekseeman kliinisissä lääketutkimuksissa lumeryhmien vasteet ovat kohtalaisen suuria. Eri tutkimuksissa EASI-75-vasteen on saavuttanut lumeryhmässä 10–30 % potilaista. Osassa tutkimuksista potilaat saivat käyttää paikallista lääkevoidetta. Kun potilas osallistuu kliiniseen lääketutkimukseen, hänen vointiinsa kiinnitetään kokonaisvaltaisesti huomiota, mikä saattaa parantaa esimerkiksi sitoutumista paikallishoidon (perusvoide tai lääkevoide) toteuttamiseen. ** Vasteet viikolla 12. |
||||
| Tyyppi | humaani mono-klonaalinen vasta-aine (IgG4) | JAK-estäjä | JAK-estäjä | JAK-estäjä |
| Vaikutuskohde | IL-4Rα | JAK 1 | JAK 1 JAK 2 |
JAK 1 |
| Annos | Aloitusannos 600 mg, jonka jälkeen 300 mg 2 viikon välein s.c. |
Aloitusannos 200 mg x 1, p.o. Jatkohoito potilaan yksilöllisen vasteen mukaan. ≥ 65-vuotiaille 100 mg x 1. |
Aloitusannos 4 mg x 1, p.o. Jatkohoito potilaan yksilöllisen vasteen mukaan. 2 mg x 1 soveltuu ≥ 75-vuotiaille. |
Aloitusannos 15 mg tai 30 mg x 1, p.o. Jatkohoito potilaan yksilöllisen vasteen mukaan. 12–17-vuotiaille ja ≥ 65-vuotiaille 15 mg x 1. |
| Saavutettu EASI-75-vaste* viikolla 16 (% potilaista), ilman lääkevoidetta |
48 | 100 mg: 40–45** 200 mg: 61–63 ** |
2 mg: 18–19 4 mg: 21–25 |
15 mg: 60–70 30 mg: 73–80 |
| lumelääke: 13 |
lumelääke: 10–12** |
lumelääke: 6–9 |
lumelääke: 13–16 |
|
| Saavutettu EASI-75-vaste* viikolla 16 (% potilaista), lääkevoiteen kanssa |
66 | 100 mg: 59** 200 mg: 70** |
2 mg: 43 4 mg: 48 |
15 mg: 65 30 mg: 77 |
| lumelääke: 25 |
lumelääke: 27** |
lumelääke: 23 |
lumelääke: 26 |
|
| Saavutettu EASI-90-vaste* viikolla 16 (% potilaista), ilman lääkevoidetta |
30–36 | 100 mg: 19–24** 200 mg: 38–39** |
2 mg: 9–11 4 mg: 13–16 |
15 mg: 42–53 30 mg: 59–66 |
| lumelääke: 7–8 |
lumelääke: 4–5** |
lumelääke: 2,5–5 |
lumelääke: 5–8 |
|
Muu systeeminen lääkehoito
Sisäiset antibiootit
- Atooppisen ekseeman tehokas hoito eli ihon läpäisyesteen korjaaminen ja inflammaation vaimentaminen vähentävät ihoinfektioiden esiintyvyyttä «Wang V, Boguniewicz J, Boguniewicz M ym. The infec...»65.
- Sisäisiä antibiootteja ei käytetä infektoitumattoman atooppisen ekseeman hoidossa
«Bath-Hextall FJ, Birnie AJ, Ravenscroft JC ym. Int...»160, «Sidbury R, Davis DM, Cohen DE ym. Guidelines of ca...»161. Ks. Vältä viisaasti -suositus «Paikalliset antimikrobiset aineet ja sisäiset antibiootit atooppisen ekseeman hoidossa»24.
- Infektoitumattomassa atooppisessa ekseemassa sisäinen antibioottihoito ei vaikuta kliinisiin oireisiin, vaikka ihon stafylokokkipitoisuus pieneneekin antibioottihoidon aikana väliaikaisesti «Boguniewicz M, Sampson H, Leung SB ym. Effects of ...»162, «Ewing CI, Ashcroft C, Gibbs AC ym. Flucloxacillin ...»163.
- Stafylokokkipitoisuus palautuu lääkehoidon jälkeen nopeasti ennalleen «Boguniewicz M, Sampson H, Leung SB ym. Effects of ...»162, «Ewing CI, Ashcroft C, Gibbs AC ym. Flucloxacillin ...»163, «Lübbe J. Secondary infections in patients with ato...»140.
- Atooppista ekseemaa sairastavista suurella osalla on Staphylococcus aureus -bakteereja sekä ekseema-alueilla että terveeltä näyttävällä iholla, joten päätöstä mahdollisesta antibioottihoidosta ei pidä tehdä vain ihon bakteeriviljelyn perusteella.
- Läpäisyesteen puutteellinen toiminta atooppisessa ihossa altistaa kuitenkin ihottuman sekundaariselle infektoitumiselle.
- Antibioottihoito on aiheellinen vain, jos ekseemaan kehittyy sekundaarinen infektio. Infektoituneen ihottuman ensisijainen antibioottihoito on flukloksasilliini tai ensimmäisen polven kefalosporiini. Ks. Käypä hoito -suositus Ihoinfektiot «Ihoinfektiot»5.
- Tavanomaista paikallishoitoa jatketaan infektoituneessa atooppisessa ekseemassa antibioottihoidon rinnalla.
- Potilaat on hyvä opettaa tunnistamaan infektoituneen ihottuman oireet ja löydökset (ihottuma-alueen märkäinen erite, märkärakkulat, ruvet, nopeasti hankaloituva atooppinen ekseema, kuume ja sairauden tunne).
- Ks. myös tämän suosituksen kappale Paikalliset antimikrobiset aineet «A7»10.
Antihistamiinit
- Älä ilman erityistä syytä käytä antihistamiineja atooppisen ekseeman aiheuttaman kutinan
hoitoon. Ks. Vältä viisaasti -suositus «Antihistamiinit atooppisen ekseeman aiheuttaman kutinan hoidossa»25. Ihottuman tehokas hoito lievittää parhaiten atooppisen ekseeman kutinaa.
- Atooppisen ekseeman kutinassa merkittäviä välittäjäaineita ovat useat tulehdussytokiinit «Atooppisen ekseeman patogeneesi pääpiirteissään»2. Histamiinin merkitys on vähäinen.
- Väsyttämättömillä antihistamiineilla ei liene tehoa atooppisen ekseeman kutinaan «Antihistamiineilla paikallishoidon lisänä ei liene vaikutusta atooppisen ekseeman kutinaan.»C.
- Väsyttävien antihistamiinien vaikutus kutinaan perustuu niiden sedatiiviseen vaikutukseen eikä antihistamiinivaikutukseen «Klein PA, Clark RA. An evidence-based review of th...»164.
Sisäiset kortikosteroidit
- Systeemihaittojen vuoksi sisäisten kortikosteroidien käyttöä ei suositella.
- Vaikean atooppisen ekseeman akuutissa pahenemisvaiheessa voidaan valikoiduissa tapauksissa
käyttää lyhytaikaisia sisäisiä kortikosteroidikuureja «Hoare C, Li Wan Po A, Williams H. Systematic revie...»103. Tällöin on aina huolehdittava samanaikaisen riittävän tehokkaan paikallishoidon
toteutumisesta.
- Sisäisten kortikosteroidien teho on nopea mutta väliaikainen. Niiden käytöstä atooppisen ekseeman hoidossa ei kuitenkaan ole lumekontrolloituja kliinisiä tutkimuksia.
- Toistuvien sisäisten kortikosteroidikuurien tarve on merkki riittämättömästä ihottuman
hoitotasapainosta.
- Asianmukaisen lääkevoidehoidon toteutuminen tulee varmistaa ja tarvittaessa tehostaa paikallishoitoa.
- Tarvittaessa potilas tulee lähettää erikoislääkärille systeemisen pitkäaikaisen lääkehoidon aloituksen arvioon.
- Ks. lisätietoa sisäisten kortikosteroidien käytöstä atooppisen ekseeman hoidossa «Lisätietoa sisäisten kortikosteroidien käytöstä atooppisen ekseeman hoidossa»26.
Vakiintumattomat ja vaihtoehtoiset hoidot
- D-vitamiinin rooli atooppisessa ekseemassa on tutkimuksen kohteena. Tarvitaan kuitenkin
lisätutkimuksia osoittamaan D-vitamiinin vaikutusten syy-seuraussuhdetta atooppisen
ekseeman patogeneesissä ja D-vitamiinilisän mahdollisesta hyödystä atooppisen ekseeman
hoidossa «Ng JC, Yew YW. Effect of Vitamin D Serum Levels an...»165. Atooppista ekseemaa sinänsä ei ainakaan toistaiseksi voi suositella D-vitamiinilisän
käyttöaiheeksi «Vestita M, Filoni A, Congedo M ym. Vitamin D and a...»166, «Ong PY, Boguniewicz M. Investigational and unprove...»167.
- D-vitamiinilla on vaikutuksia luonnolliseen ja adaptiiviseen immuniteettiin, antimikrobiaalisten peptidien muodostumiseen ihossa sekä ihosolujen erilaistumiseen ja kasvuun.
- Veren kalsidiolipitoisuus (25(OH)D) on atooppista ekseemaa sairastavilla merkittävästi pienempi kuin terveihoisilla verrokeilla. Vaikeaa ihottumaa sairastavilla kalsidiolipitoisuus on pienempi kuin lievää tai keskivaikeaa ihottumaa sairastavilla «Ng JC, Yew YW. Effect of Vitamin D Serum Levels an...»165.
- Ihotautipotilaat käyttävät paljon vakiintumattomia ja vaihtoehtoisia hoitoja. Käytön
elinikäinen esiintyvyys on eri tutkimuksissa ollut 35–69 % «Ernst E, Pittler MH, Stevinson C. Complementary/al...»168, «Kim GW, Park JM, Chin HW ym. Comparative analysis ...»169.
- Lähetteellä yliopistoklinikkaan tulleista atooppista ekseemaa sairastavista potilaista 50 % käytti myös vaihtoehtoisia hoitoja ihottumaansa «Simpson EL, Basco M, Hanifin J. A cross-sectional ...»170. Irlannissa lähetteellä ihotautiklinikkaan tulleista atooppista ekseemaa sairastavista lapsista 42,5 %:lle oli käytetty vaihtoehtoisia hoitoja «Hughes R, Ward D, Tobin AM ym. The use of alternat...»171.
- Tavallisimmin käytetyt vaihtoehtoiset hoidot ovat kiinalaiset yrttivalmisteet, ravintolisä välttämättömillä rasvahapoilla, homeopatia ja akupunktio.
- Tyytymättömyys tavanomaisiin hoitoihin ja turhautuminen atooppisen ekseeman krooniseen luonteeseen johtavat potilaita kokeilemaan vaihtoehtoisia hoitoja.
- Anamneesiin on hyvä sisällyttää kysymys vakiintumattomien ja vaihtoehtoisten hoitojen käytöstä, sillä potilaat tai lapsipotilaiden vanhemmat harvoin kertovat näistä hoidoista spontaanisti.
- Kiinalaisten yrttivalmisteiden tehoa selvittävissä tutkimuksissa harhan riski on suuri erityisesti sokkouttamisen osalta. Tutkimuksissa ei ole pystytty selkeästi osoittamaan, että kiinalaiset yrttivalmisteet paikallisesti tai systeemisesti käytettyinä olisivat tehokkaita atooppisen ekseeman hoidossa «Gu S, Yang AW, Xue CC ym. Chinese herbal medicine ...»172, «Tan HY, Zhang AL, Chen D ym. Chinese herbal medici...»173, «Gu S, Yang AW, Li CG ym. Topical application of Ch...»174. Kiinalaisilla lääkeyrteillä on kuvattu olevan useita haittavaikutuksia, ja osa niistä on vakavia (laajentava kardiomyopatia, maksatoksisuus) «Hoare C, Li Wan Po A, Williams H. Systematic revie...»103, «Sheehan MP, Atherton DJ. One-year follow up of chi...»175.
- Vaihtoehtoisista paikallishoitovalmisteista on löydetty merkittäviä määriä potentteja kortikosteroideja «Boneberger S, Rupec RA, Ruzicka T. Complementary t...»176.
- Välttämättömillä rasvahapoilla ei ole todettu olevan tehoa atooppiseen ekseemaan «Välttämättömillä rasvahapoilla ei ole tehoa atooppisen ekseeman hoidossa.»A, «Hoare C, Li Wan Po A, Williams H. Systematic revie...»103, «Bath-Hextall F, Williams H. Atopic eczema. Clin Ev...»177.
- Homeopatian tehosta atooppisen ekseeman hoidossa ei ole näyttöä «Boneberger S, Rupec RA, Ruzicka T. Complementary t...»176, «Torley D, Futamura M, Williams HC ym. What's new i...»178.
- Meta-analyysin perusteella akupunktiota ei voi suositella atooppisen ekseeman hoidoksi «Jiao R, Yang Z, Wang Y ym. The effectiveness and s...»179.
- Lisätietoa vakiintumattomista hoidoista ks. «Vakiintumattomat ja vaihtoehtoiset hoidot»27.
Käsien atooppinen ekseema
- Atooppisen ekseeman yksi tyyppipaikka on kädet. Käsi-ihottumaan on tärkeä puuttua
varhaisvaiheessa ennen ekseeman kroonistumista.
- Kuiva atooppinen iho ärtyy herkästi muun muassa kosteudesta ja kosketuksesta saippuoihin, ruoka-aineisiin, veteen, likaan ja pölyyn.
- Käsien suojaus kosteudelta ja ärsyttäviltä tekijöiltä on tärkeää, jos käsissä on ollut ekseemaa (ks. ohjeet «https://www.terveyskyla.fi/ihotautitalo/ihotaudit/k%C3%A4si-ihottuma»14).
- Atooppisen käsiekseeman hoidon perusta on säännöllinen rasvaus perusvoiteella tarvittaessa
useita kertoja päivässä ja jaksoittainen paikallishoito kortikosteroideilla «Thyssen JP, Schuttelaar MLA, Alfonso JH ym. Guidel...»180.
- Käsiekseeman hoidossa tarvitaan usein vahvoja III ryhmän ja joskus erittäin vahvoja IV ryhmän kortikosteroidivoiteita. Kuurit ovat pidempiä kuin muilla ihoalueilla, yleensä 2–4 viikkoa. Kuuria voidaan jatkaa tarvittaessa 6 viikkoon asti.
- Ihottuman parannuttua tarvitaan usein ylläpitohoitoa vahvalla kortikosteroidivoiteella kahdesti viikossa uusimisen ehkäisyyn.
- Kortikosteroidivoiteiden haittavaikutukset ovat samat kuin muilla ihoalueilla.
- Kämmenten ekseemassa kalsineuriinin estäjät eivät pääse kunnolla vaikuttamaan ihon paksuuden vuoksi.
- Perusvoidetta suositellaan saippuan tilalle käsien voidepesuihin. Ks. Ihotautitalon ohje «https://www.terveyskyla.fi/ihotautitalo/Documents/Voidepesu_potilasohje.pdf»15.
- Käsiekseema tulee ottaa huomioon ammatinvalinnassa (ks. kappale Ammatinvalinta «A8»11).
Hoito raskauden ja imetyksen aikana
- Atooppinen ekseema on yleisin raskauden aikainen ihotauti «Koutroulis I, Papoutsis J, Kroumpouzos G. Atopic d...»181.
- Noin 20 %:lla atooppista ekseemaa sairastavista ihottuma lievittyy raskauden aikana, mutta muilla ihottuma pysyy ennallaan tai vaikeutuu «Balakirski G, Novak N. Atopic dermatitis and pregn...»182. Raskaudenaikainen atooppisen ekseeman vaikeutuminen voi selittyä immunologisilla tekijöillä, kuten Th2-vasteen voimistumisella, sekä raskauden aiheuttamalla lisääntyneellä fyysisellä ja psyykkisellä stressillä. Aktiivisten hoitojen välttäminen on myös yleistä, mikä voi johtaa odottavan äidin ekseeman alihoitoon «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183, «Weatherhead S, Robson SC, Reynolds NJ. Eczema in p...»184.
- Raskauden aikana voidaan jatkaa perusvoiteiden lisäksi mietojen, keskivahvojen ja
vahvojen paikalliskortikosteroidien käyttöä tavanomaiseen tapaan «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183.
- Potilas ohjataan erikoissairaanhoitoon, mikäli keskivahvat tai vahvat kortikosteroidivoiteet eivät ole riittävän tehokkaita tai potilas käyttää niitä yli 200 g kuukaudessa.
- Takrolimuusin tai pimekrolimuusin paikalliskäytölle raskauden aikana ei ole estettä. Käyttö tulisi rajata vain hoitoa vaativille ihoalueille ja hoidon kesto rajoittaa lyhimpään riittävään. Paikalliskäytössä imeytyminen on hyvin vähäistä, mutta voi lisääntyä, jos iho on rikki. Rajoitetusta paikallishoidosta ei ole odotettavissa sellaista altistumista, joka vaikuttaisi sikiön kehitykseen «Malm H. Teratologinen palvelu. Henkilökohtainen ti...»185.
- Kortikosteroidivoiteiden tai paikallisten kalsineuriinin estäjien käyttö ei ole este imettämiselle. Jos hoitoa tarvitaan rinnan alueelle, tulee noudattaa erityistä varovaisuutta, ettei imeväinen joudu suoraan kontaktiin lääkevoiteen kanssa. Käytännössä voide tulee levittää nännin tai nännipihan alueelle heti imetyksen jälkeen ja huolehtia nännin alueen hellävaraisesta mutta huolellisesta puhdistuksesta ennen imetystä «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183, «Weatherhead S, Robson SC, Reynolds NJ. Eczema in p...»184.
- Raskauden aikana voidaan käyttää kapeakaistaista UVB-hoitoa tai SUP-hoitoa «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183, «Weatherhead S, Robson SC, Reynolds NJ. Eczema in p...»184.
- Systeemistä lääkitystä vaativa atooppinen ekseema hoidetaan aina erikoissairaanhoidossa.
- Systeemihaittojen vuoksi sisäisten kortikosteroidien käyttöä atooppisessa ekseemassa ei suositella, mutta poikkeustapauksissa voidaan raskaana oleville käyttää prednisolonia. Tällöin tulisi käyttää korkeintaan 0,5 mg/kg/vrk mahdollisimman lyhyenä kuurina (yleensä alle 2–3 viikkoa) «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183, «Weatherhead S, Robson SC, Reynolds NJ. Eczema in p...»184.
- Siklosporiinia voidaan harkitusti ja tarkkaan seuraten käyttää vaikeassa ekseemassa raskauden ja imetyksen aikana.
- Atsatiopriinihoidon jatkamista voidaan harkita raskauden aikana «Mahadevan U, Long MD, Kane SV ym. Pregnancy and Ne...»186. Imetystä suositellaan vältettäväksi neljän tunnin ajan lääkkeen ottamisesta «Bar-Gil Shitrit A, Grisaru-Granovsky S, Ben Ya'aco...»187.
- Dupilumabin käyttöä ei suositella raskauden tai imetyksen aikana vähäisen tutkimustiedon vuoksi.
- Metotreksaatin, mykofenolaattimofetiilin ja JAK-estäjien käyttö on kontraindisoitu raskauden tai imetyksen aikana. Naisten tulee tauottaa metotreksaatti 3 kuukautta, mykofenolaattimofetiili 6 viikkoa ja JAK-estäjät 2–4 viikkoa ennen raskautta «Russell MD, Dey M, Flint J ym. British Society for...»188.
- Miesten ei tarvitse tauottaa atooppisen ekseeman annoksilla käytettävää metotreksaattia, siklosporiinia, atsatiopriinia, biolologisia lääkkeitä tai JAK-estäjiä perheenlisäystä suunniteltaessa «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kehoito-raskauden-ja-imetyksen-aikana»16.
| Hoito | Raskaus | Lisätietoa | Imetys | Lisätietoa |
|---|---|---|---|---|
| Perusvoiteet | Sallittu | Sallittu | ||
| Kortikosteroidivoiteet | Sallittu | Sallittu | ||
| Kalsineuriinin estäjät | Sallittu | Sallittu | ||
| Kapeakaistainen UVB-hoito ja SUP-hoito | Sallittu | Sallittu | ||
| Systeemiset lääkkeet: | ||||
| Systeemiset kortikosteroidit | Sallittu | Pienin mahdollinen annos | Sallittu | |
| Atsatiopriini | Sallittu | Sallittu rajoituksin | Imetys aikaisintaan 4 tuntia lääkkeen otosta | |
| Siklosporiini | Sallittu | Sallittu | ||
| Metotreksaatti | Kielletty | Teratogeeninen, varoaika 3 kuukautta | Kielletty | |
| Mykofenolaattimofetiili | Kielletty | Teratogeeninen, varoaika 6 viikkoa | Kielletty | |
| Dupilumabi | Ei suositella | Ei vielä riittävästi tutkimustietoa | Ei suositella | |
| JAK-estäjät | Kielletty | Lääkekohtainen varoaika 2–4 viikkoa | Kielletty | |
| Miesten ei tarvitse tauottaa (atooppisen ekseeman annoksilla käytettäviä) systeemilääkkeitä perheenlisäystä suunniteltaessa. | ||||
Lasten (0–16-vuotiaiden) atooppisen ekseeman hoidon erityispiirteet
- Lapsen atooppisen ekseeman hoidon tavoitteena on pitkäkestoinen oireiden hallinta: oireiden minimointi, pahenemisvaiheiden määrän väheneminen ja vaikeusasteen lieveneminen sekä potilaan elämänlaadun ja toimintakyvyn paraneminen.
- Vanhempien hyvä perehdytys atooppisen ekseeman syihin liittyviin asioihin, hoitojen tehon ja haittavaikutusten läpikäyminen, hoidon ohjaus ja ennusteen arvioiminen ovat hoidon onnistumisen kannalta oleellisen tärkeitä. Lapset tulee ottaa mukaan ohjauskeskusteluihin ikätasonsa mukaisesti. Hoitajan antaman perusteellisen ohjauksen on todettu parantavan hoitotulosta ja lisäävän voiteiden käyttöä «Cork MJ, Britton J, Butler L ym. Comparison of par...»99, «García-Soto L, Martín-Masot R, Espadafor-López B y...»189.
- Suosituksen liitteenä on lyhyt lisätietomateriaali vanhemmille, omahoito-ohje ja rasvausvideo lääkäreille, hoitajille ja vanhemmille «Ohje vanhemmille atooppisesta ekseemasta»1, (Atooppisen ekseeman ohjattu omahoito lapsilla «hoi50077d.pdf»2, videot «Atooppinen ekseema -suosituksen videot (lapset)»3).
- Säännöllinen rasvaus perusvoiteella 1–2 kertaa päivässä ja jaksoittainen hoito paikalliskortikosteroidivoiteella
ovat lapsen atooppisen ekseeman ensisijainen hoito.
- Lapsilla käytetään yleensä mietoja tai keskivahvoja kortikosteroidivoiteita. Vahvoja kortikosteroidivoiteita käytetään vain erikoistilanteissa erikoislääkärin määräämänä.
- Tutkimustulokset korostavat atooppisen ekseeman paikallishoidon tärkeyttä «Miyaji Y, Yang L, Yamamoto-Hanada K ym. Earlier ag...»190, «Kelleher MM, Dunn-Galvin A, Gray C ym. Skin barrie...»191. Tutkimusten mukaan imeväisiän vaikea atooppinen ekseema ja kotipölyssä oleva pähkinäproteiini suurentavat pähkinäallergian riskiä kouluiässä «Brough HA, Simpson A, Makinson K ym. Peanut allerg...»192. Yksi mahdollinen selitys on, että imeväinen herkistyy pähkinälle rikkinäisen ihon kautta.
- Atooppisen ekseeman uusiutumista ehkäisevä ylläpitohoito kalsineuriinin estäjillä, erityisesti takrolimuusilla, lapsen keskivaikeassa tai vaikeassa atooppisessa ekseemassa, jossa ei ole saatu riittävää hoitotehoa kortikosteroidivoiteilla, on osoittautunut tehokkaaksi pahenemisvaiheita vähentäväksi ja turvalliseksi hoitomuodoksi «Ylläpitohoito takrolimuusivoiteella 2–3 kertaa viikossa alueille, joissa ihottumaa yleensä on esiintynyt, vähentää merkittävästi pahenemisvaiheita ja kortikosteroidivoiteiden käyttöä perusvoiteisiin verrattuna.»A.
Paikalliskortikosteroidit
- Ekseeman ilmaantuessa käytetään paikalliskortikosteroideja kuuriluonteisesti. Ks.
taulukko «Kokemukseen ja kliiniseen käyttöön perustuva työryhmän suositus siitä, minkä teholuokan
kortikosteroidivoidetta käytetään eri-ikäisillä lapsilla ja eri ihoalueille. ...»4.
- Tutkimuksessa miedon ja keskivahvan kortikosteroidivoiteen käyttö 3–5 vuorokauden kuureina 1–3-vuotiaille keskivaikeaa tai vaikeaa atooppista ekseemaa sairastaville todettiin tehokkaaksi ja turvalliseksi «Salava A, Perälä M, Pelkonen A ym. Safety of tacro...»193, «Perälä M, Salava A, Malmberg P ym. Topical tacroli...»194.
- Eurooppalaisessa hoitosuosituksessa annetaan mahdollisuus ylläpitohoitoon kaiken vahvuisilla kortikosteroidivoiteilla. Näyttöä mietojen tai keskivahvojen kortikosteroidivoiteiden tehosta ylläpitohoidossa ei ole minkään ikäisillä potilailla «Wollenberg A, Kinberger M, Arents B ym. EuroGuiDer...»101.
- Ylläpitohoidosta kahdesti viikossa käytettävällä vahvalla kortikosteroidivoiteella on saatu jonkin verran tutkimusnäyttöä «Hanifin J, Gupta AK, Rajagopalan R. Intermittent d...»108, «Thomas KS, Armstrong S, Avery A ym. Randomised con...»195, «Ylläpitohoito 2 kertaa viikossa vahvalla paikalliskortikosteroidilla näyttää ehkäisevän atooppisen ekseeman relapsia.»B. Hoito soveltuu vain vartalolle ja raajoihin.
- Alle 1-vuotiaan hoidossa käytetään 1-prosenttista hydrokortisonivoidetta 1–2 kertaa
vuorokaudessa 3–7 vuorokauden jaksoissa «Akdis CA, Akdis M, Bieber T ym. Diagnosis and trea...»58, minkä jälkeen pidetään tauko haittavaikutusten minimoimiseksi.
- Hoito voidaan aloittaa hydrokortisonivoiderasvauksella kaksi kertaa päivässä. Vaikka voiteen annostelusta pienille lapsille kerran päivässä ei ole vielä tutkimustietoa, kliinisen kokemuksen perusteella lievemmissä ekseemoissa rasvaus kerran päivässä riittää.
- Hoitoa voidaan tehostaa käyttämällä paikallisesti sidoksia, peittävää okkluusiota tai kosteita kääreitä «Devillers AC, Oranje AP. Efficacy and safety of 'w...»196, «Nicol NH, Boguniewicz M, Strand M ym. Wet wrap the...»197. Ks. myös kappale Sidokset ja hauteet «A9»12.
- 1–7-vuotiaan hoidossa voidaan käyttää mietoa tai keskivahvaa kortikosteroidivoidetta
kerran vuorokaudessa 3–7 vuorokauden jaksoina (ks. taulukko «Kokemukseen ja kliiniseen käyttöön perustuva työryhmän suositus siitä, minkä teholuokan
kortikosteroidivoidetta käytetään eri-ikäisillä lapsilla ja eri ihoalueille. ...»4). Koululaisilla hoitojakson pituus voi tarvittaessa olla 1–2 viikkoa «Ainley-Walker PF, Patel L, David TJ. Side to side ...»198. Hoitotauko on vähintään yhtä pitkä kuin hoitojakso.
- Hoitoa voidaan tehostaa käyttämällä paikallisesti sidoksia, peittävää okkluusiota tai kosteita kääreitä «Devillers AC, Oranje AP. Efficacy and safety of 'w...»196, «Nicol NH, Boguniewicz M, Strand M ym. Wet wrap the...»197.
- Vahvaa kortikosteroidivoidetta käytetään vain erikoislääkärin ohjeen mukaan.
- Varsinkin jos käytetään vahvoja kortikosteroidivoiteita ohuille ihoalueille pitkiä aikoja (yli 2 viikkoa), paikallisten (ihon atrofia) ja myös systeemisten haittavaikutusten (hypotalamus-aivolisäke-lisämunuaiskuoriakselin suppressio) riski suurenee lapsilla «Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106, «Davallow Ghajar L, Wood Heickman LK, Conaway M ym....»199. Lapsilla, joilla on laaja-alaista ekseemaa, on miedoillakin kortikosteroidivoiteilla todettu lyhytaikaista, hoidon alkuun ajoittuvaa kortikosteroidin systeemistä imeytymistä «Davallow Ghajar L, Wood Heickman LK, Conaway M ym....»199, «Axon E, Chalmers JR, Santer M ym. Safety of topica...»118.
| Voiteen teholuokka | ||||
|---|---|---|---|---|
| * Silmänympärysekseeman hoidossa kalsineuriinin estäjät ovat ensisijaisia. Plusmerkit kuvaavat työryhmän suosituksen vahvuutta. - = ei suositella |
||||
| Potilaan ikä (v) | I | II | III | IV |
| Alle 1 | +++ | - | - | - |
| 1–6 | +++ | ++ | - | - |
| 7–16 | +++ | ++ | + | - |
| Ihoalue | ||||
| Kasvot, kaula* | +++ | - | - | - |
| Vartalo, raajat | +++ | ++ | - | - |
| Kämmenet, jalkapohjat | + | +++ | + | - |
| Kainalot, nivusseutu | +++ | + | - | - |
| Päänahka | ++ | + | - | - |
Paikalliset kalsineuriinin estäjät
- Jos paikalliskortikosteroidivoiteilla ei saada riittävää vastetta, yli 2-vuotiaiden hoidossa käytetään takrolimuusivoidetta tai yli 3 kuukauden ikäisten hoidossa pimekrolimuusiemulsiovoidetta ohuelti ekseema-alueille kahdesti päivässä, kunnes ekseema on parantunut. Ks. video Kalsineuriinin estäjät atooppisen ekseeman paikallishoidossa «Kalsineuriinin estäjät atooppisen ekseeman paikallishoidossa (video) (kesto 1:41)»28.
- Kalsineuriinin estäjät ovat tehokkaita ja turvallisia lasten atooppisen ekseeman hoidossa.
- Pimekrolimuusiemulsiovoiteen käyttöaihe yli 3 kuukauden ikäisillä on lievä tai keskivaikea atooppinen ekseema.
- 0,03-prosenttisen takrolimuusin käyttöaihe 2–15-vuotiailla on keskivaikea tai vaikea atooppinen ekseema. Vahvempaa (0,1-prosenttista) takrolimuusivoidetta käytetään erikoislääkärin harkinnan mukaan «Reitamo S, Rustin M, Harper J ym. A 4-year follow-...»200, «Wahn U, Bos JD, Goodfield M ym. Efficacy and safet...»201.
- Kalsineuriinin estäjien teho lapsilla on osoitettu.
- 1-prosenttinen pimekrolimuusiemulsiovoide on tehokkaampi kuin perusvoide lasten lievän tai keskivaikean atooppisen ekseeman sekä lyhyessä että pitkäkestoisessa (12 kk) hoidossa. Se on tehokas ja turvallinen myös kasvojen alueen ihottuman hoitoon ja imeväisille «1-prosenttinen pimekrolimuusiemulsiovoide on tehokkaampi kuin perusvoide lasten atooppisen ekseeman hoidossa. Se on tehokas ja turvallinen myös imeväisillä ja kasvojen alueen ihottuman hoidossa ja vähentää kortikosteroidivoiteen tarvetta.»A.
- Lievässä ja keskivaikeassa atooppisessa ekseemassa 1-prosenttinen pimekrolimuusiemulsiovoide vähentää kortikosteroidin käyttöä «Wahn U, Bos JD, Goodfield M ym. Efficacy and safet...»201.
- 0,03- ja 0,1-prosenttinen takrolimuusivoide ovat tehokkaampia kuin hydrokortisonivoide lasten keskivaikean tai vaikean atooppisen ekseeman hoidossa ja yhtä tehokkaita kuin keskivahva kortikosteroidivoide «0,03-prosenttinen ja 0,1-prosenttinen takrolimuusivoide ovat tehokkaampia kuin sekä perusvoide että hydrokortisonivoide lasten keskivaikean tai vaikean atooppisen ekseeman hoidossa. 0,03-prosenttinen takrolimuusivoide on yhtä tehokas kuin 0,005-prosenttinen flutikasonivoide lasten keskivaikean tai vaikean atooppisen ekseeman hoidossa.»A.
- Pimekrolimuusiemulsiovoidetta käytetään ekseema-alueille kahdesti vuorokaudessa, kunnes oireet häviävät. Tähän voi mennä useita viikkoja. Ekseeman uusituessa hoito tulee aloittaa uudelleen heti ensioireiden ilmaantuessa «Sigurgeirsson B, Ho V, Ferrándiz C ym. Effectivene...»202.
- Takrolimuusivoidetta käytetään ihottuma-alueille 1–2 kertaa päivässä, kunnes ihottuma on parantunut. Ekseeman uusiutuessa hoito aloitetaan uudelleen.
- Jos ekseema uusiutuu tiheästi, päivittäisen takrolimuusivoidehoidon jälkeen voidaan
jatkaa ylläpitohoidolla, kunnes ihottuma on parantunut täysin tai lähes täysin. Ylläpitohoidossa
takrolimuusivoidetta käytetään kahdesti viikossa kerran päivässä korkeintaan 12 kuukauden
ajan alueille, joilla ihottumaa yleensä esiintyy. Tämän jälkeen lääkärin tulee arvioida
potilaan vointi ja päättää, jatketaanko ylläpitohoitoa. Jos ihottuma pahenee ylläpitohoidon
aikana, voidetta käytetään jälleen kahdesti päivässä «Schmitt J, von Kobyletzki L, Svensson A ym. Effica...»203.
- Ylläpitohoito takrolimuusivoiteella 2–3 kertaa viikossa alueille, joissa ihottumaa yleensä on esiintynyt, vähentää merkittävästi pahenemisvaiheita ja kortikosteroidivoiteiden käyttöä perusvoiteisiin verrattuna «Ylläpitohoito takrolimuusivoiteella 2–3 kertaa viikossa alueille, joissa ihottumaa yleensä on esiintynyt, vähentää merkittävästi pahenemisvaiheita ja kortikosteroidivoiteiden käyttöä perusvoiteisiin verrattuna.»A.
- Ellei pimekrolimuusiemulsiovoiteen teho ole riittävä, siirrytään pahenemisvaiheessa käyttämään mietoa tai keskivahvaa kortikosteroidivoidetta lyhyenä kuurina ja ihon rauhoituttua palataan takaisin pelkkään kalsineuriinin estäjään «Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106.
- Takrolimuusivoidetta käytetään yleensä ainoana lääkevoiteena. Jos teho yksin käytettynä
ei ole riittävä, voidaan pahenemisvaiheessa siirtyä käyttämään keskivahvaa kortikosteroidivoidetta
ja ihon rauhoituttua palata takaisin pelkkään kalsineuriinin estäjään «Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106.
- Takrolimuusipaikallishoitoa edeltävä, voimakkaimmin oireilevaa ihottumaa lievittävä hoitojakso kortikosteroidivoiteella saattaa lisätä hoitoon sitoutumista.
- Perusvoiteet saattavat haitata kalsineuriinin estäjien imeytymistä, joten perusvoidetta ja lääkevoidetta ei laiteta samanaikaisesti samalle ihoalueelle. Voiteiden käytön välillä on hyvä pitää tauko, jotta ensimmäisenä laitettu voide ehtii imeytyä. Ks. omahoito-ohje Atooppisen ekseeman ohjattu omahoito lapsilla «hoi50077d.pdf»2.
- Takrolimuusivoidetta ja pimekrolimuusiemulsiovoidetta ei yhdistetä UV-hoitoihin.
- Kalsineuriinin estäjien yleinen haittavaikutus on hoidettujen ihoalueiden kuumoitus. Se on voimakkaimmillaan ensimmäisillä hoitokerroilla ja vähenee sekä useimmiten häviää hoidon jatkuessa. On tärkeää kertoa tämä potilaalle tai potilaan vanhemmille ennen hoidon aloitusta.
- Kalsineuriinin estäjät eivät aiheuta ihoatrofiaa «Reitamo S, Rissanen J, Remitz A ym. Tacrolimus oin...»122.
- Ei ole selkeää näyttöä siitä, että kalsineuriinin estäjä -hoito lisäisi herpes simplexin aiheuttamien ihotulehdusten tai ontelosyylien määrää lapsilla «Paul C, Cork M, Rossi AB ym. Safety and tolerabili...»204, «Kapp A, Papp K, Bingham A ym. Long-term management...»205, «Koo JY, Fleischer AB Jr, Abramovits W ym. Tacrolim...»206.
- Lapsilla ei ole osoitettu esiintyneen systeemisiä haittavaikutuksia tai merkittävää systeemistä imeytymistä kalsineuriinin estäjien käytön yhteydessä «Staab D, Pariser D, Gottlieb AB ym. Low systemic a...»207, «Alaiti S, Kang S, Fiedler VC ym. Tacrolimus (FK506...»208, «Remitz A, Harper J, Rustin M ym. Long-term safety ...»209, «Salava A, Perälä M, Pelkonen A ym. Safety of tacro...»193.
- Pimekrolimuusi- ja takrolimuusihoidolla ei ole todettu olevan vaikutusta rokotevasteisiin «Stiehm ER, Roberts RL, Kaplan MS ym. Pneumococcal ...»210, «Papp KA, Breuer K, Meurer M ym. Long-term treatmen...»211.
- Kalsineuriinin estäjät ovat rajoitetusti peruskorvattavia. Ks. «https://www.kela.fi/laake317»6.
Systeemiset pitkäaikaiset lääkkeet
- Kun lapsen vaikea atooppinen ekseema ei reagoi asianmukaisesti toteutettuun paikallishoitoon, potilas tulee lähettää erikoislääkärin arvioon. Systeemisen lääkehoidon aloitusta harkitaan vaikeaa atooppista ekseemaa sairastavilla lapsilla, joilla ei saada riittävää hoitovastetta hyvin toteutetulla paikallishoidolla ja mahdollisesti UV-hoidolla. Mahdollisia lääkkeitä ovat perinteiset immunosuppressiiviset lääkkeet, biologiset lääkkeet ja JAK-estäjät (ks. kohta (aikuisten) Systeeminen pitkäaikainen lääkehoito «A10»13).
- Systeemisten lääkkeiden ajantasaiset korvattavuudet, ks. Kelan sivut «https://www.kela.fi/yhteistyokumppanit-laakekorvaukset-laakkeiden-korvausoikeudet»9.
- Metotreksaatti ja siklosporiini
- Luotettavaa lumekontrolloitua tutkimusnäyttöä siklosporiinin ja metotreksaatin tehosta lasten vaikean atooppisen ekseeman hoidossa ei ole.
- Pienessä aineistossa metotreksaatti oli yhtä tehokas kuin siklosporiini lasten vaikean atooppisen ekseeman hoidossa. Ks. myös «Siklosporiini lasten atooppisen ekseeman hoidossa»29.
- Haittavaikutukset rajoittavat siklosporiinin pitkäaikaiskäyttöä.
- Dupilumabi
- Dupilumabi näyttää olevan tehokas 6–17-vuotiailla lapsilla ja nuorilla, jotka sairastavat
keskivaikeaa tai vaikeaa atooppista ekseemaa. Teho ja turvallisuus olivat 16 viikkoa
kestäneessä tutkimuksessa samankaltaiset kuin aikuisilla.
- Viikolla 16 EASI-75-vasteen saavutti 6–11-vuotiaista dupilumabiryhmässä (painonmukaisella annostelulla) 67–70 % ja lumeryhmässä 27 % potilaista, kun molemmat ryhmät käyttivät myös paikallista kortikosteroidia «In children (6-11 years) with severe atopic dermatitis dupilumab (100 mg every two weeks for children with weight of 15 to <30 kg and 200 mg every two weeks for children with weight of ≥30 kg) with topical corticosteroids appears to increase the proportion of patients reaching EASI-75 at week 16 when compared to placebo (67–70% vs. 27%).»B. Nuorilla (12–17-vuotiailla) vastaavat luvut ilman samanaikaista lääkevoiteen käyttöä olivat 42 % ja 8 % «Simpson EL, Paller AS, Siegfried EC ym. Efficacy a...»149.
- Dubilumabi näyttää olevan tehokas 0,5–5-vuotiaiden lasten keskivaikean ja vaikean
atooppisen ekseeman hoidossa. Teho ja turvallisuus olivat 16 viikkoa kestäneessä tutkimuksessa
samankaltaisia kuin vanhemmilla lapsilla ja aikuisilla «Paller AS, Simpson EL, Siegfried EC ym. Dupilumab ...»212.
- Viikolla 16 EASI-75-vasteen saavutti 0,5–5-vuotiaista dupilumabiryhmässä 53 % ja lumeryhmässä 11 %, kun molemmat ryhmät käyttivät myös paikallista kortikosteroidia.
- Dupilumabi näyttää olevan tehokas 6–17-vuotiailla lapsilla ja nuorilla, jotka sairastavat
keskivaikeaa tai vaikeaa atooppista ekseemaa. Teho ja turvallisuus olivat 16 viikkoa
kestäneessä tutkimuksessa samankaltaiset kuin aikuisilla.
- Upadasitinibi
- Upadasitinibi näyttää olevan tehokas 12–17-vuotiailla nuorilla.
- Alaryhmäanalyysissä 12–17-vuotiaiden nuorten (n = 228) EASI-75-tulokset vastasivat aikuisten tuloksia «Guttman-Yassky E, Teixeira HD, Simpson EL ym. Once...»158.
- Abrositinibi
- Abrositinibilla ei ole virallista käyttöaihetta alle 18-vuotiailla (4/2023), mutta sitä on tutkittu myös lasten ja nuorten atooppisen ekseeman hoidossa.
- Abrositinibi näyttää olevan tehokas 12–17-vuotiailla lapsilla ja nuorilla.
- Teho ja turvallisuus olivat 12 viikkoa kestäneessä tutkimuksessa samankaltaiset kuin
aikuisilla.
- Viikolla 12 EASI-75-vasteen saavutti abrositinibi 200 mg -ryhmässä 72 %, abrositinibi 100 mg -ryhmässä 69 % ja lumeryhmässä 42 % potilaista, kun samanaikaisesti käytettiin lääkevoiteita «Eichenfield LF, Flohr C, Sidbury R ym. Efficacy an...»213.
Muut hoidot lapsilla
- Probiooteilla ei näytä olevan tehoa atooppisen ekseeman hoidossa «Boyle RJ, Bath-Hextall FJ, Leonardi-Bee J ym. Prob...»214, «Baquerizo Nole KL, Yim E, Keri JE. Probiotics and ...»215.
- Prebioottien tehosta ekseeman hoidossa ei ole riittävästi näyttöä «van der Aa LB, Heymans HS, van Aalderen WM ym. Eff...»216.
- Systeemihaittojen vuoksi sisäisten kortikosteroidien käyttöä ei suositella.
- UV-hoidon tehoa lasten atooppisen ekseeman hoidossa ei ole selvitetty kontrolloiduin ja satunnaistetuin tutkimuksin, mutta hoitovaste ja haitat todennäköisesti vastaavat aikuisilla saatuja tuloksia.
- Lasten UV-hoidon pitkäaikaisturvallisuudesta ei ole luotettavaa näyttöä.
- UV-hoitoa (SUP tai kapeakaistainen UVB) voidaan käyttää keskivaikeassa ja vaikeassa atooppisessa ekseemassa kaikenikäisille lapsille harkitusti erikoislääkärin valvonnassa «Collins P, Ferguson J. Narrowband (TL-01) UVB air-...»217.
Taloudellista tietoa
- Ks. Lääkkeiden vaikuttavuuden (EASI-75 -vaste), kustannusten ja hoitovasteen kustannusten vertailu atooppisen ekseeman hoidossa «https://www.terveysportti.fi/apps/laake/laakekustannus/hoi50077»1 (vaatii käyttöoikeuden), lisätietoa «The number needed to treat (NNT) and cost per responder for systemic therapies for moderate-to-severe atopic dermatitis»21 ja opasvideo taulukon lukemisesta «Hoitovasteen kustannukset Käypä hoito -suosituksissa: näin luen taulukoita (video)»30.
Hoidon porrastus
- Ks. kuva Atooppisen ekseeman hoitoalgoritmi «Atooppisen ekseeman hoitoalgoritmi»1.
- Hoidon porrastuksen käytännöt sovitaan alueellisesti sen mukaan, miten tietoa ja taitoa on eri tasoilla saatavilla.
- Perusterveydenhuollossa ilman ihotautien ja allergologian tai lastentautien erikoislääkärin
konsultaatiota järjestetään
- diagnostiikka anamneesin ja kliinisen kuvan perusteella
- aikuisten lievän ja keskivaikean atooppisen ekseeman hoito suosituksen mukaisesti ja hoidonohjaus
- lasten lievän atooppisen ekseeman hoito suosituksen mukaisesti ja hoidonohjaus
- atooppista ekseemaa ylläpitävien ja pahentavien tekijöiden sekä mahdollisten liitännäissairauksien
kartoittaminen.
- Allergiatestaukset eivät yleensä ole tarpeen.
- Hoidonohjaus: Ks. omahoito-ohjeet Atooppisen ekseeman ohjattu omahoito aikuisilla
«hoi50077c.pdf»1, Atooppisen ekseeman ohjattu omahoito lapsilla «hoi50077d.pdf»2, «Ohje vanhemmille atooppisesta ekseemasta»1 ja videot rasvausohjauksesta, aikuiset «Atooppinen ekseema -suosituksen videot (aikuiset)»2 ja lapset «Atooppinen ekseema -suosituksen videot (lapset)»3.
- Kalsineuriinin estäjät ovat rajoitetusti peruskorvattavia. Ks. «https://www.kela.fi/laake317»6.
- Perusterveydenhuollossa voidaan aloittaa paikallinen kalsineuriinin estäjä -hoito kasvojen alueen ihottumaan, mikäli lääkärillä on kokemusta atooppisen ekseeman hoidosta.
- Erikoislääkärin konsultaation aiheet
- vähintään keskivaikea atooppinen ekseema lapsella
- epäily lapsen perusruoka-allergiasta (ks. Käypä hoito -suositus Ruoka-allergia (lapset) «Ruoka-allergia (lapset)»4)
- aikuisen vaikea atooppinen ekseema: ihottuma oireilee laaja-alaisena tai vaikea-asteisena asianmukaisesti toteutetusta lääkevoidehoidosta huolimatta
- lievemmätkin ekseemat, joissa on hoidon toteutumisen ongelma tai huono hoitovaste
- ihottuma vaikuttaa potilaan työ- tai toimintakykyyn
- erotusdiagnostinen ongelma
- UV-hoitojen tai systeemisen pitkäaikaisen lääkityksen harkinta
- tarvittaessa liitännäissairauksien tutkimus ja hoito eri erikoisaloilla
- Erikoislääkärikonsultaation jälkeen
- jatkohoito tapahtuu yleensä perusterveydenhuollossa
- uusintakonsultaatiot tehdään tarvittaessa, mikäli sairaus ei ole hallinnassa.
- Vaikeaa hoitoresistenttiä tai laaja-alaista ekseemaa sairastavia kaikenikäisiä potilaita seurataan erikoissairaanhoidossa.
- Systeemistä pitkäaikaista lääkehoitoa saavia seurataan erikoislääkärin toimesta.
Rajoitukset, etuudet ja kuntoutus
Ammatinvalinta
- Atooppinen ekseema on tärkein työperäisen käsi-ihottuman riskitekijä. Lapsuudessa
atooppista ekseemaa sairastaneilla on lisääntynyt taipumus saada käsi-ihottumaa aikuisiässä
työstä riippumatta «Bryld LE, Hindsberger C, Kyvik KO ym. Risk factors...»218, «Johannisson A, Pontén A, Svensson Å. Prevalence, i...»219. Atooppisen ihon rakenteeseen eli läpäisyesteen puutteelliseen toimintaan liittyy
lisääntynyt riski saada ärsytysihottumaa käsiin «Coenraads P-J, Diepgen TL. Risk for hand eczema i...»220.
- Työn ihoa ärsyttävät tekijät lisäävät käsi-ihottuman puhkeamisen riskiä.
- Käsi-ihottumaa pahentavia tekijöitä ovat märkätyö, elintarvikkeiden käsittely, runsas käsienpesu, suojakäsineiden hautova vaikutus, likaiset ja pölyiset työtehtävät, ihoa ärsyttävien kemikaalien, kuten liuottimien, öljyjen ja pesuaineiden, käsittely sekä runsas mekaaninen ärsytys.
- Atooppista ekseemaa sairastavalla ei kuitenkaan ole suurentunutta riskiä saada käsi-ihottumana ilmenevää allergista kosketusihottumaa. Allerginen kosketusihottuma voi syntyä altistumisesta allergisoiville kemikaaleille työssä tai vapaa-aikana.
- Työn ihoa ärsyttävät tekijät lisäävät käsi-ihottuman puhkeamisen riskiä.
- Ammatinvalinnasta on hyvä keskustella ammatinvalinnanohjaajan kanssa. Työntekijälle on syytä selvittää ihoa ärsyttäviin töihin liittyvät riskit «Työperäiset sairaudet. Työterveyslaitos 2008. www....»221, «http://www.ttl.fi»17.
- Ammatinvalintaan on ohjeita Työterveyslaitoksen Töissä terveenä -sivustolla «https://www.ttl.fi/teemat/tyoterveys/toissa-terveena-ammatinvalinta-allergia-ihottuma-ja-astma»18 ja «https://www.ttl.fi/teemat/tyoterveys/toissa-terveena-ammatinvalinta-allergia-ihottuma-ja-astma/riskialttiit-ammatit»19.
- Työhön liittyvät rajoitukset:
- Lievää atooppista ekseemaa sairastavilla, joita ekseema vaivaa lähinnä talvella ja joilla sitä ei esiinny käsissä, ei ole ehdottomia rajoituksia. Heidän olisi kuitenkin parempi valita kuiva ja puhdas työ.
- Atooppista ekseemaa sairastavat, joilla on ollut käsi-ihottumaa, sopivat huonosti kaikenlaiseen käsien ihoa rasittavaan työhön, kuten jatkuvaan märkään ja likaiseen tai mekaanisesti ärsyttävään työhön, kemikaaleille altistavaan työhön sekä töihin, joissa edellytetään tiheää käsienpesua tai tiiviiden kumi- tai muovikäsineiden jatkuvaa käyttöä «Lindström I, Mäkelä M, Pelkonen A ym. Astma, atoop...»222.
Asepalvelus
- Lievä atooppinen ekseema ei vaikuta yleiseen palveluskelpoisuuteen, mutta vaikeampi atooppinen ekseema, joka vaatii päivittäistä paikallishoitoa, on usein este palvelukselle «Lindström I, Mäkelä M, Pelkonen A ym. Astma, atoop...»222.
- Palveluskelpoisuuden luokitukset ja niiden yleisperusteet esitetään lisätietoaineistossa (TTO-ohje «https://puolustusvoimat.fi/documents/1948673/2258811/PEVIESTOS-Terveystarkastusohje2012.pdf/d8fec7e9-1178-44bf-8b6e-cdd9fd585ec3»20).
Kansaneläkelaitoksen etuuksista
- Ks. atooppisen ekseeman hoidossa käytettävien lääkkeiden ajantasaiset korvattavuustiedot Kelan sivustolta «https://www.kela.fi/yhteistyokumppanit-laakekorvaukset-laakkeiden-korvausoikeudet»9.
- Alle 16-vuotiaan vammaistukea maksetaan korvaukseksi vähintään 6 kuukautta kestäneestä tavanomaista suuremmasta rasituksesta ja sidonnaisuudesta, joka aiheutuu sairaan tai vammaisen lapsen hoidosta, huolenpidosta ja kuntoutuksesta. Tuki myönnetään yleensä määräajaksi, jonka päätyttyä tukeen voi hakea jatkoa «http://www.kela.fi/kelan-etuusohjeet_ohjeet-etuuksittain»21.
- Aikuisten vammaistukea voidaan myöntää 16 vuotta täyttäneelle henkilölle, jonka toimintakyky on sairauden, vian tai vamman vuoksi heikentynyt vähintään vuoden ajan ja joka ei ole elämäntilanteeltaan eläkeläinen. Jos perusedellytykset täyttyvät, oikeus etuuteen ja etuuden suuruus määräytyvät niin sanottujen määräytymisperusteiden mukaan «http://www.kela.fi/kelan-etuusohjeet_ohjeet-etuuksittain»21.
- Eläkettä saavan hoitotuki on tarkoitettu 16 vuotta täyttäneelle eläkeläiselle, joka saa hoitotukeen oikeuttavaa eläkettä ja tarvitsee vamman tai sairauden vuoksi apua tai ohjausta «http://www.kela.fi/kelan-etuusohjeet_ohjeet-etuuksittain»21.
- Reseptillä määrätyistä lääkkeistä, kliinisistä ravintovalmisteista ja perusvoiteista, jotka on määrätty sairauden hoitoon ja jotka lukeutuvat korvattaviin valmisteisiin, saa Kela-korvauksen. Lisätietoa vuosiomavastuusta eli lääkekatosta ks. «https://www.kela.fi/laakekustannusten-omavastuut»22 ja terveydenhuollon maksukatosta ks. «https://stm.fi/terveydenhuollon-maksukatto»23.
- Jos atooppista ekseemaa sairastavan tulot ja varat eivät riitä lääkkeisiin ja muihin hoitoihin, hän voi hakea Kelan toimeentulotukea. Jos hakija saa Kelasta hylkäävän päätöksen, kyseeseen voi tietyissä harvinaisissa tilanteissa tulla myös lääkkeiden osalta täydentävä ja ehkäisevä toimeentulotuki. Sitä haetaan hyvinvointialueelta.
- Atooppista ekseemaa sairastavan on hyvä muistaa hakea myös Kelan maksamat matkakorvaukset varsinkin, jos hän käy UV-hoidossa ja joutuu terveysperusteella käyttämään Kelan sopimustaksia sairausmatkoilla. Lisätietoa ks. «https://www.kela.fi/matkat»24
- Kelan sairauspäiväraha myönnetään tarvittaessa yleisen käytännön mukaan.
- Atooppista ekseemaa sairastava voi saada tukea vammaispalveluista esimerkiksi pyykinpesukoneen tai vaatteiden hankintaan. Ks. «https://thl.fi/fi/web/vammaispalvelujen-kasikirja»25.
Kuntoutus
- Työterveyshuollon lakisääteinen tehtävä on arvioida potilaan jäljellä oleva työkyky. Vaikeasta atooppisesta ekseemasta aiheutuu joskus tarvetta ammatilliseen tai lääkinnälliseen kuntoutukseen. Niihin hakeudutaan yleisen käytännön mukaan «http://www.kela.fi/kuntoutus»26.
- Joskus atooppista ekseemaa sairastavalla voi olla vaikea elämäntilanne ja useita pitkittyneitä ongelmia. Hänen sairautensa hoito ei välttämättä toteudu optimaalisesti. Silloin kyseeseen voi tulla sosiaalinen kuntoutus «https://stm.fi/sosiaalinen-kuntoutus»27. Palvelutarpeen arvio ja päätös asiasta tehdään hyvinvointialueen sosiaalipalveluissa.
- Vertaistukea ja muuta sosiaalista, psyykkistä ja tiedollista tukea atooppista ekseemaa sairastava saa myös potilasjärjestöistä. Allergia-, iho- ja astmaliitto järjestää vuosittain kursseja ja tarjoaa maksutonta sairaus- ja sosiaalineuvontaa. Ks. «https://www.allergia.fi/palvelut/kurssit/»28 ja «https://www.allergia.fi/palvelut/tukea-apua-tietoa/neuvontanumerot/»29.
- Tietoa potilasjärjestöjen jäsenyhdistyksistä ks. «https://www.allergia.fi/jarjesto/yhdistykset/»30
Suomalaisen Lääkäriseuran Duodecimin, Suomen yleislääketieteen yhdistyksen ja Suomen Ihotautilääkäriyhdistyksen asettama työryhmä
Atooppinen ekseema -suosituksen historiatiedot «Atooppinen ekseema, Käypä hoito -suosituksen historiatiedot»31
Puheenjohtaja:
Leena Koulu, dosentti, iho- ja sukupuolitautien ja ihoallergologian erikoislääkäri; Tyks Ihoklinikka
Jäsenet:
Laura Korhonen, LT, ihotautien ja allergologian erikoislääkäri; TAYS ihotautien poliklinikka ja allergiakeskus
Antti Lauerma, professori, iho- ja sukupuolitautien, ihoallergologian ja ammatti-ihotautien erikoislääkäri; HUS Iho- ja allergiasairaala
Janne Liimatainen, LL, yleislääketieteen erikoislääkäri, ylilääkäri; Lapin hyvinvointialue, Kittilän terveyskeskus
Johanna Mandelin, LKT, ihotautien ja allergologian erikoislääkäri; HUS Iho- ja allergiasairaala
Anna Pelkonen, dosentti, lastentautien ja lastenallergologian erikoislääkäri; HUS Iho- ja allergiasairaala
Sanna Poikonen, LT, ihotautien ja allergologian erikoislääkäri, Pihlajalinna
Raija Sipilä, LT, terveydenhuollon erikoislääkäri; Käypä hoito -toimittaja, Suomalainen Lääkäriseura Duodecim
Asiantuntijat:
Asiantuntijat eivät ole osallistuneet hoitosuosituksen sisältöä koskevaan päätöksentekoon.
Heli Malm, dosentti, naistentautien ja synnytysten erikoislääkäri; Teratologinen tietopalvelu, HUS Akuutti
Sirpa Pylkkänen-Mäkelä, sosiaalityöntekijä; HUS Iho- ja allergiasairaala
Tuovi Eskelinen, Riihimäki; viiteryhmän jäsen
Elina Gundersen, Helsinki; viiteryhmän jäsen
Jaana Halin, Turku; viiteryhmän jäsen
Jani Kytölä, Kauhajoki; viiteryhmän jäsen
Kati Ojala, Joensuu; viiteryhmän jäsen
Mari Repo, Masku; viiteryhmän jäsen
Jenny Soranoja, Turku; viiteryhmän jäsen
Kirsi Tarnanen; Suomalainen Lääkäriseura Duodecim, potilaiden osallisuutta tukeva toimittaja, viiteryhmän sihteeri
Mari Tiilikainen, Nokia; viiteryhmän jäsen
Ulla Turunen; viiteryhmän jäsen
Sidonnaisuudet
Sidonnaisuusilmoitukset on kerätty 30.5.2023 julkaistun suosituksen laatimisen yhteydessä.
Laura Korhonen: Tutkimusrahoitus: Novartis. Koulutus-, konsultointi- ja asiantuntijatoimintaa: Abbvie, Allergia-, iho- ja astmaliitto, Eli Lilly, LeoPharma, Novartis, Orion, Pfizer, Sanofi Genzyme, Sidekick Health, Tampereen seudun atopiayhdistys. Korvaukset kongressi- ja seminaarikuluista: Abbvie, Sanofi Genzyme. Luottamustoimet terveydenhuollon alalla: Suomen allergologi- ja immunologiyhdistys; hallituksen jäsen, puheenjohtaja, Suomen ihotautilääkäriyhdistyksen kontaktidermatiittiryhmä; puheenjohtaja. Ohjaushankkeet: Allergiadiagnostiikkarekisteri, vaikeat ihosairaudet -rekisteri, Atooppisen ekseeman hoitopolku.
Leena Koulu: Sivutoimet: konsultoiva ihotautilääkäri; Kaarinan terveyskeskus, yksityislääkäri; Mehiläinen. Koulutus-, konsultointi- ja asiantuntijatoimintaa: AbbVie, Boehringer Ingelheim, Bristol-Myers Squibb, Eli Lilly, Janssen-Cilag, Leo Pharma, Perrigo, Pfizer, UCB Pharma. Ohjaushankkeet: Vaikeat ihosairaudet -rekisteri.
Antti Lauerma: Sivutoimet: ihotautien ja allergologian professori; HY, yksityislääkäri; Mehiläinen, toimitusjohtaja; Medipracticum Oy. Tutkimusrahoitus: Orion Pharma. Koulutus-, konsultointi- ja asiantuntijatoimintaa: Orion Pharma. Luottamustoimet terveydenhuollon alalla: Suomen lääketieteen säätiö; hallituksen jäsen, HYKS-lnstituutti Oy; hallituksen jäsen, puheenjohtaja; Allergiatutkimussäätiö, Treasurer; European Academy of Allergology and Clinical lmmunology, Board Member; Euroopean Academy of Dermatology and Venereology Auditor, Nordic Dermatology Association.
Janne Liimatainen: Sivutoimet: yliopisto-opettaja; Oulun yliopisto, etä-tk-lääkäri ja TTH:n sairasvastaanotto; Coronaria Terveys Oy, erikoislääkärikoulutuksen koordinaattori; Oulun yliopisto, terveyskeskuslääkäri, Oulu. Koulutus-, konsultointi- ja asiantuntijatoimintaa: Yleislääkäripäivät 2019 ja 2022, GPF Pohjolan Lääkäripäivät, 2021 ja 2020 Coronaria Terveys Oy. Korvaukset kongressi- ja seminaarikuluista: NCGP 2019 Aalborg, Tanska (Oulun yliopisto). Luottamustoimet terveydenhuollon alalla: Oulun seudun paikallisosaston puheenjohtaja, SLL OYS-erva-alueen terveyspoliittisen valiokunnan puheenjohtaja, SLL terveyspoliittisen jaoksen jäsen, SLL Kansallinen lääkelista -hanke, asiantuntijapaaneelin jäsen, Kela.
Johanna Mandelin: Sivutoimet: ihotautilääkäri; Pikkujätti Kamppi. Tutkimusrahoitus: CRST Oy. Koulutus-, konsultointi- ja asiantuntijatoimintaa: Abbvie, Boehringer-Ingelheim, Leo Pharma, Lilly, Janssen, Novartis, Pfizer, Sanofi, Sidekick, Takeda, UCB Pharma. Luottamustoimet terveydenhuollon alalla: EFTAD (European Task Force on Atopic Dermatitis), hallituksen jäsen. Suomen allergologi- ja immunologiyhdistys, hallituksen jäsen. Ohjaushankkeet: Vaikeat ihosairaudet -rekisteri, Atooppisen ekseeman hoitopolku. Muut sidonnaisuudet: kliiniset lääke- ja rekisteritutkimukset: Sanofi, Amgen.
Anna Pelkonen: Sivutoimet: ammatinharjoittaja; Pikkujätti. Luento-, koulutus- ja asiantuntijapalkkiot: Orion Pharma. Luottamustoimet terveydenhuollon alalla: aluevaltuutettu; Länsi-Uudenmaan hyvinvointialue.
Sanna Poikonen: Sivutoimet: ihotautilääkärin yksityisvastaanotto; Pihlajalinna. Korvaukset kongressi- ja seminaarikuluista: Pfizer, EADV 2022. Muut sidonnaisuudet: aluejohtaja; Pihlajalinna Terveys Oy: hallinnollinen työ ja osakkeiden omistus 4000 kpl.
Raija Sipilä: Sivutoimet: yleislääkäri; Terveystalo. Tutkimusrahoitus: Potilaat mukaan Käypä hoito -suositusten laatimiseen -hanke, työnantajalle rahoitus, rahoittajana STEA (2019–2022) PROSHADE, työnantajalle rahoitus, rahoittajana STN 10/2020–. Koulutus-, konsultointi- ja asiantuntijatoimintaa: HUS, Lääkäriliitto, Medimerc (Turun yo). Luottamustoimet terveydenhuollon alalla: GIN Nordic, ohjausryhmän jäsen 2019–, Kela, sosiaalilääketieteen neuvottelukunta 2/2019–, Lääkärin tietokannat, neuvottelukunnan jäsen 2010–2021. Väestöliiton hallitus 2023–.
Kirjallisuusviite
Atooppinen ekseema. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen yleislääketieteen yhdistyksen ja Suomen Ihotautilääkäriyhdistyksen asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2023 (viitattu pp.kk.vvvv). Saatavilla internetissä: www.kaypahoito.fi
Tarkemmat viittausohjeet: «https://www.kaypahoito.fi/kaypa-hoito/kayttooikeudet/viittaaminen»31
Vastuun rajaus
Käypä hoito -suositukset ja Vältä viisaasti -suositukset ovat asiantuntijoiden laatimia yhteenvetoja yksittäisten sairauksien diagnostiikan ja hoidon vaikuttavuudesta. Suositukset toimivat lääkärin tai muun terveydenhuollon ammattilaisen päätöksenteon tukena hoitopäätöksiä tehtäessä. Ne eivät korvaa lääkärin tai muun terveydenhuollon ammattilaisen omaa arviota yksittäisen potilaan parhaasta mahdollisesta diagnostiikasta, hoidosta ja kuntoutuksesta hoitopäätöksiä tehtäessä.
Tiedonhakukäytäntö
Systemaattinen kirjallisuushaku on hoitosuosituksen perusta. Lue lisää artikkelista khk00007
Kirjallisuutta
- Tokura Y, Hayano S. Subtypes of atopic dermatitis: From phenotype to endotype. Allergol Int 2022;71:14-24 «PMID: 34344611»PubMed
- Johansson EK, Bergström A, Kull I ym. Prevalence and characteristics of atopic dermatitis among young adult females and males-report from the Swedish population-based study BAMSE. J Eur Acad Dermatol Venereol 2022;36:698-704 «PMID: 35032357»PubMed
- Williams H, Stewart A, von Mutius E ym. Is eczema really on the increase worldwide? J Allergy Clin Immunol 2008;121:947-54.e15 «PMID: 18155278»PubMed
- Roduit C, Frei R, Loss G ym. Development of atopic dermatitis according to age of onset and association with early-life exposures. J Allergy Clin Immunol 2012;130:130-6.e5 «PMID: 22521248»PubMed
- Vakharia PP, Silverberg JI. Adult-Onset Atopic Dermatitis: Characteristics and Management. Am J Clin Dermatol 2019;20:771-779 «PMID: 31140066»PubMed
- Vartiainen E, Petäys T, Haahtela T ym. Allergic diseases, skin prick test responses, and IgE levels in North Karelia, Finland, and the Republic of Karelia, Russia. J Allergy Clin Immunol 2002;109:643-8 «PMID: 11941314»PubMed
- von Hertzen L, Mäkelä MJ, Petäys T ym. Growing disparities in atopy between the Finns and the Russians: a comparison of 2 generations. J Allergy Clin Immunol 2006;117:151-7 «PMID: 16387599»PubMed
- Mortz CG, Andersen KE, Dellgren C ym. Atopic dermatitis from adolescence to adulthood in the TOACS cohort: prevalence, persistence and comorbidities. Allergy 2015;70:836-45 «PMID: 25832131»PubMed
- Silverberg JI, Hanifin JM. Adult eczema prevalence and associations with asthma and other health and demographic factors: a US population-based study. J Allergy Clin Immunol 2013;132:1132-8 «PMID: 24094544»PubMed
- Barbarot S, Auziere S, Gadkari A ym. Epidemiology of atopic dermatitis in adults: Results from an international survey. Allergy 2018;73:1284-1293 «PMID: 29319189»PubMed
- Sinikumpu SP, Huilaja L, Jokelainen J ym. High prevalence of skin diseases and need for treatment in a middle-aged population. A Northern Finland Birth Cohort 1966 study. PLoS One 2014;9:e99533 «PMID: 24911008»PubMed
- Lee HH, Patel KR, Singam V ym. A systematic review and meta-analysis of the prevalence and phenotype of adult-onset atopic dermatitis. J Am Acad Dermatol 2019;80:1526-1532.e7 «PMID: 29864464»PubMed
- Langan SM, Irvine AD, Weidinger S. Atopic dermatitis. Lancet 2020;396:345-360 «PMID: 32738956»PubMed
- Reijula J, Latvala J, Mäkelä M ym. Long-term trends of asthma, allergic rhinitis and atopic eczema in young Finnish men: a retrospective analysis, 1926-2017. Eur Respir J 2020;56: «PMID: 32764114»PubMed
- Dharmage SC, Lowe AJ, Matheson MC ym. Atopic dermatitis and the atopic march revisited. Allergy 2014;69:17-27 «PMID: 24117677»PubMed
- Haider S, Fontanella S, Ullah A ym. Evolution of Eczema, Wheeze, and Rhinitis from Infancy to Early Adulthood: Four Birth Cohort Studies. Am J Respir Crit Care Med 2022;206:950-960 «PMID: 35679320»PubMed
- IIlli S, von Mutius E, Lau S ym. The natural course of atopic dermatitis from birth to age 7 years and the association with asthma. J Allergy Clin Immunol 2004;113:925-31 «PMID: 15131576»PubMed
- Williams HC, Strachan DP. The natural history of childhood eczema: observations from the British 1958 birth cohort study. Br J Dermatol 1998;139:834-9 «PMID: 9892950»PubMed
- Bieber T. Atopic dermatitis. N Engl J Med 2008;358:1483-94 PMID: 18385500
- Apfelbacher CJ, Diepgen TL, Schmitt J. Determinants of eczema: population-based cross-sectional study in Germany. Allergy 2011;66:206-13 «PMID: 20804468»PubMed.
- Sliz E, Huilaja L, Pasanen A ym. Uniting biobank resources reveals novel genetic pathways modulating susceptibility for atopic dermatitis. J Allergy Clin Immunol 2022;149:1105-1112.e9 «PMID: 34454985»PubMed
- Palmer CN, Irvine AD, Terron-Kwiatkowski A ym. Common loss-of-function variants of the epidermal barrier protein filaggrin are a major predisposing factor for atopic dermatitis. Nat Genet 2006;38:441-6 «PMID: 16550169»PubMed
- Luukkonen TM, Kiiski V, Ahola M ym. The Value of FLG Null Mutations in Predicting Treatment Response in Atopic Dermatitis: An Observational Study in Finnish Patients. Acta Derm Venereol 2017;97:456-463 «PMID: 27840886»PubMed
- van Smeden J, Bouwstra JA. Stratum Corneum Lipids: Their Role for the Skin Barrier Function in Healthy Subjects and Atopic Dermatitis Patients. Curr Probl Dermatol 2016;49:8-26 «PMID: 26844894»PubMed
- Joo KM, Hwang JH, Bae S ym. Relationship of ceramide-, and free fatty acid-cholesterol ratios in the stratum corneum with skin barrier function of normal, atopic dermatitis lesional and non-lesional skins. J Dermatol Sci 2015;77:71-4 «PMID: 25455137»PubMed
- Geoghegan JA, Irvine AD, Foster TJ: Staphylococcus aureus and Atopic Dermatitis: A Complex and Evolving Relationship. Trends in Microbiology 2018;26:484-497
- Legat FJ. Itch in Atopic Dermatitis - What Is New? Front Med (Lausanne) 2021;8:644760 «PMID: 34026782»PubMed
- Ständer S, Simpson EL, Guttman-Yassky E ym. Clinical Relevance of Skin Pain in Atopic Dermatitis. J Drugs Dermatol 2020;19:921-926 «PMID: 33026764»PubMed
- Greer FR, Sicherer SH, Burks AW ym. The Effects of Early Nutritional Interventions on the Development of Atopic Disease in Infants and Children: The Role of Maternal Dietary Restriction, Breastfeeding, Hydrolyzed Formulas, and Timing of Introduction of Allergenic Complementary Foods. Pediatrics 2019;143: «PMID: 30886111»PubMed
- Boyle RJ, Ierodiakonou D, Khan T ym. Hydrolysed formula and risk of allergic or autoimmune disease: systematic review and meta-analysis. BMJ 2016;352:i974 «PMID: 26956579»PubMed
- Osborn DA, Sinn JK, Jones LJ. Infant formulas containing hydrolysed protein for prevention of allergic disease. Cochrane Database Syst Rev 2018;10:CD003664 «PMID: 30338526»PubMed
- Foisy M, Boyle RJ, Chalmers JR ym. Overview of Reviews The prevention of eczema in infants and children: an overview of Cochrane and non-Cochrane reviews. Evid Based Child Health 2011;6:1322-1339 «PMID: 22822349»PubMed
- Netting MJ, Middleton PF, Makrides M. Does maternal diet during pregnancy and lactation affect outcomes in offspring? A systematic review of food-based approaches. Nutrition 2014;30:1225-41 «PMID: 25280403»PubMed
- Zutavern A, Brockow I, Schaaf B ym. Timing of solid food introduction in relation to eczema, asthma, allergic rhinitis, and food and inhalant sensitization at the age of 6 years: results from the prospective birth cohort study LISA. Pediatrics 2008;121:e44-52 «PMID: 18166543»PubMed
- Williams HC, Chalmers J. Prevention of Atopic Dermatitis. Acta Derm Venereol 2020;100:adv00166 «PMID: 32419030»PubMed
- Obbagy JE, English LK, Wong YP ym. Complementary feeding and food allergy, atopic dermatitis/eczema, asthma, and allergic rhinitis: a systematic review. Am J Clin Nutr 2019;109:890S-934S «PMID: 30982864»PubMed
- Pfefferle PI, Prescott SL, Kopp M. Microbial influence on tolerance and opportunities for intervention with prebiotics/probiotics and bacterial lysates. J Allergy Clin Immunol 2013;131:1453-63; quiz 1464 «PMID: 23643095»PubMed
- Kuitunen M. Probiotics and prebiotics in preventing food allergy and eczema. Curr Opin Allergy Clin Immunol 2013;13:280-6 «PMID: 23594506»PubMed
- Li L, Han Z, Niu X ym. Probiotic Supplementation for Prevention of Atopic Dermatitis in Infants and Children: A Systematic Review and Meta-analysis. Am J Clin Dermatol 2019;20:367-377 «PMID: 30465329»PubMed
- Osborn DA, Sinn JK. Prebiotics in infants for prevention of allergy. Cochrane Database Syst Rev 2013;:CD006474 «PMID: 23543544»PubMed
- Sestito S, D'Auria E, Baldassarre ME ym. The Role of Prebiotics and Probiotics in Prevention of Allergic Diseases in Infants. Front Pediatr 2020;8:583946 «PMID: 33415087»PubMed
- Kelleher MM, Cro S, Cornelius V ym. Skin care interventions in infants for preventing eczema and food allergy. Cochrane Database Syst Rev 2021;2:CD013534 «PMID: 33545739»PubMed
- Liang J, Hu F, Tang H ym. Systematic review and network meta-analysis of different types of emollient for the prevention of atopic dermatitis in infants. J Eur Acad Dermatol Venereol 2023;37:501-510 «PMID: 36415973»PubMed
- Simpson EL, Chalmers JR, Hanifin JM ym. Emollient enhancement of the skin barrier from birth offers effective atopic dermatitis prevention. J Allergy Clin Immunol 2014;134:818-23 «PMID: 25282563»PubMed
- Horimukai K, Morita K, Narita M ym. Application of moisturizer to neonates prevents development of atopic dermatitis. J Allergy Clin Immunol 2014;134:824-830.e6 «PMID: 25282564»PubMed
- Skjerven HO, Rehbinder EM, Vettukattil R ym. Skin emollient and early complementary feeding to prevent infant atopic dermatitis (PreventADALL): a factorial, multicentre, cluster-randomised trial. Lancet 2020;395:951-961 «PMID: 32087121»PubMed
- Chalmers JR, Haines RH, Bradshaw LE ym. Daily emollient during infancy for prevention of eczema: the BEEP randomised controlled trial. Lancet 2020;395:962-972 «PMID: 32087126»PubMed
- Brenninkmeijer EE, Schram ME, Leeflang MM ym. Diagnostic criteria for atopic dermatitis: a systematic review. Br J Dermatol 2008;158:754-65 «PMID: 18241277»PubMed
- Champion RH ym. (toim.) Textbook of Dermatology, 6. painos, 1998
- Williams HC, Burney PG, Pembroke AC ym. The U.K. Working Party's Diagnostic Criteria for Atopic Dermatitis. III. Independent hospital validation. Br J Dermatol 1994;131:406-16 «PMID: 7918017»PubMed
- Li JX, Dong RJ, Zeng YP. Characteristics, mechanism, and management of pain in atopic dermatitis: A literature review. Clin Transl Allergy 2021;11:e12079 «PMID: 34962720»PubMed
- Thomas KS, Apfelbacher CA, Chalmers JR ym. Recommended core outcome instruments for health-related quality of life, long-term control and itch intensity in atopic eczema trials: results of the HOME VII consensus meeting. Br J Dermatol 2021;185:139-146 «PMID: 33393074»PubMed
- Czarnowicki T, He H, Krueger JG ym. Atopic dermatitis endotypes and implications for targeted therapeutics. J Allergy Clin Immunol 2019;143:1-11 «PMID: 30612663»PubMed
- Tokura Y, Hayano S. Subtypes of atopic dermatitis: From phenotype to endotype. Allergol Int 2022;71:14-24 «PMID: 34344611»PubMed
- Paternoster L, Savenije OEM, Heron J ym. Identification of atopic dermatitis subgroups in children from 2 longitudinal birth cohorts. J Allergy Clin Immunol 2018;141:964-971 «PMID: 29129583»PubMed
- Roduit C, Frei R, Depner M ym. Phenotypes of Atopic Dermatitis Depending on the Timing of Onset and Progression in Childhood. JAMA Pediatr 2017;171:655-662 «PMID: 28531273»PubMed
- Renert-Yuval Y, Thyssen JP, Bissonnette R ym. Biomarkers in atopic dermatitis-a review on behalf of the International Eczema Council. J Allergy Clin Immunol 2021;147:1174-1190.e1 «PMID: 33516871»PubMed
- Akdis CA, Akdis M, Bieber T ym. Diagnosis and treatment of atopic dermatitis in children and adults: European Academy of Allergology and Clinical Immunology/American Academy of Allergy, Asthma and Immunology/PRACTALL Consensus Report. J Allergy Clin Immunol 2006;118:152-69 «PMID: 16815151»PubMed
- Zhao CY, Hao EY, Oh DD ym. A comparison study of clinician-rated atopic dermatitis outcome measures for intermediate- to dark-skinned patients. Br J Dermatol 2017;176:985-992 «PMID: 28012183»PubMed
- Werfel T, Heratizadeh A, Niebuhr M ym. Exacerbation of atopic dermatitis on grass pollen exposure in an environmental challenge chamber. J Allergy Clin Immunol 2015;136:96-103.e9 «PMID: 26044854»PubMed
- Nankervis H, Pynn EV, Boyle RJ ym. House dust mite reduction and avoidance measures for treating eczema. Cochrane Database Syst Rev 2015;1:CD008426 «PMID: 25598014»PubMed
- Ring J, Alomar A, Bieber T ym. Guidelines for treatment of atopic eczema (atopic dermatitis) part I. J Eur Acad Dermatol Venereol 2012;26:1045-60 «PMID: 22805051»PubMed
- Davis DMR, Drucker AM, Alikhan A ym. American Academy of Dermatology Guidelines: Awareness of comorbidities associated with atopic dermatitis in adults. J Am Acad Dermatol 2022;86:1335-1336.e18 «PMID: 35085682»PubMed
- Hamann CR, Hamann D, Egeberg A ym. Association between atopic dermatitis and contact sensitization: A systematic review and meta-analysis. J Am Acad Dermatol 2017;77:70-78 «PMID: 28392290»PubMed
- Wang V, Boguniewicz J, Boguniewicz M ym. The infectious complications of atopic dermatitis. Ann Allergy Asthma Immunol 2021;126:3-12 «PMID: 32771354»PubMed
- Legendre L, Barnetche T, Mazereeuw-Hautier J ym. Risk of lymphoma in patients with atopic dermatitis and the role of topical treatment: A systematic review and meta-analysis. J Am Acad Dermatol 2015;72:992-1002 «PMID: 25840730»PubMed
- Hsu JI, Pflugfelder SC, Kim SJ. Ocular complications of atopic dermatitis. Cutis 2019;104:189-193 «PMID: 31675394»PubMed
- Andersen YM, Egeberg A, Gislason GH ym. Autoimmune diseases in adults with atopic dermatitis. J Am Acad Dermatol 2017;76:274-280.e1 «PMID: 27742171»PubMed
- Narla S, Silverberg JI. Association between atopic dermatitis and autoimmune disorders in US adults and children: A cross-sectional study. J Am Acad Dermatol 2019;80:382-389 «PMID: 30287311»PubMed
- Ivert LU, Wahlgren CF, Lindelöf B ym. Association between atopic dermatitis and autoimmune diseases: a population-based case-control study. Br J Dermatol 2021;185:335-342 «PMID: 33091150»PubMed
- Kauppi S, Jokelainen J, Timonen M ym. Atopic Dermatitis Is Associated with Dermatitis Herpetiformis and Celiac Disease in Children. J Invest Dermatol 2021;141:191-193.e2 «PMID: 32540248»PubMed
- Rønnstad ATM, Halling-Overgaard AS, Hamann CR ym. Association of atopic dermatitis with depression, anxiety, and suicidal ideation in children and adults: A systematic review and meta-analysis. J Am Acad Dermatol 2018;79:448-456.e30 «PMID: 30119868»PubMed
- Silverberg JI, Gelfand JM, Margolis DJ ym. Symptoms and diagnosis of anxiety and depression in atopic dermatitis in U.S. adults. Br J Dermatol 2019;181:554-565 «PMID: 30838645»PubMed
- Kern C, Wan J, LeWinn KZ ym. Association of Atopic Dermatitis and Mental Health Outcomes Across Childhood: A Longitudinal Cohort Study. JAMA Dermatol 2021;157:1200-1208 «PMID: 34468686»PubMed
- Patel KR, Immaneni S, Singam V ym. Association between atopic dermatitis, depression, and suicidal ideation: A systematic review and meta-analysis. J Am Acad Dermatol 2019;80:402-410 «PMID: 30365995»PubMed
- Kauppi S, Jokelainen J, Timonen M ym. Adult Patients with Atopic Eczema have a High Burden of Psychiatric Disease: A Finnish Nationwide Registry Study. Acta Derm Venereol 2019;99:647-651 «PMID: 30848288»PubMed
- de Bruin-Weller M, Thaçi D, Smith CH ym. Dupilumab with concomitant topical corticosteroid treatment in adults with atopic dermatitis with an inadequate response or intolerance to ciclosporin A or when this treatment is medically inadvisable: a placebo-controlled, randomized phase III clinical trial (LIBERTY AD CAFÉ). Br J Dermatol 2018;178:1083-1101 «PMID: 29193016»PubMed
- Simpson EL, Wollenberg A, Bissonnette R ym. Patient-Reported Symptoms and Disease Impacts in Adults With Moderate-to-Severe Atopic Dermatitis: Results From a Phase 2b Study With Abrocitinib. Dermatitis 2021;32:S53-S61 «PMID: 33795561»PubMed
- Schans JV, Çiçek R, de Vries TW ym. Association of atopic diseases and attention-deficit/hyperactivity disorder: A systematic review and meta-analyses. Neurosci Biobehav Rev 2017;74:139-148 «PMID: 28111269»PubMed
- Jackson-Cowan L, Cole EF, Arbiser JL ym. TH2 sensitization in the skin-gut-brain axis: How early-life Th2-mediated inflammation may negatively perpetuate developmental and psychologic abnormalities. Pediatr Dermatol 2021;38:1032-1039 «PMID: 34338364»PubMed
- Fan R, Leasure AC, Damsky W ym. Association of atopic dermatitis with attention-deficit hyperactivity disorder among US adults in the "All of Us" research program: A case-control study. J Am Acad Dermatol 2022;87:691-692 «PMID: 35283246»PubMed.
- Silverberg JI. Comorbidities and the impact of atopic dermatitis. Ann Allergy Asthma Immunol 2019;123:144-151 «PMID: 31034875»PubMed
- Ascott A, Mulick A, Yu AM ym. Atopic eczema and major cardiovascular outcomes: A systematic review and meta-analysis of population-based studies. J Allergy Clin Immunol 2019;143:1821-1829 «PMID: 30576754»PubMed
- Pandher K, Ghamrawi RI, Heron CE ym. Controversial cardiovascular and hematologic comorbidities in atopic dermatitis. Arch Dermatol Res 2022;314:317-324 «PMID: 33973062»PubMed
- Rehal B, Armstrong AW. Health outcome measures in atopic dermatitis: a systematic review of trends in disease severity and quality-of-life instruments 1985-2010. PLoS One 2011;6:e17520 «PMID: 21533286»PubMed
- Silverberg JI, Garg NK, Paller AS ym. Sleep disturbances in adults with eczema are associated with impaired overall health: a US population-based study. J Invest Dermatol 2015;135:56-66 «PMID: 25078665»PubMed
- Theodosiou G, Montgomery S, Metsini A ym. Burden of Atopic Dermatitis in Swedish Adults: A Population-based Study. Acta Derm Venereol 2019;99:964-970 «PMID: 31289842»PubMed
- Wittkowski A, Richards HL, Griffiths CE ym. The impact of psychological and clinical factors on quality of life in individuals with atopic dermatitis. J Psychosom Res 2004;57:195-200 «PMID: 15465076»PubMed
- Beattie PE, Lewis-Jones MS. A comparative study of impairment of quality of life in children with skin disease and children with other chronic childhood diseases. Br J Dermatol 2006;155:145-51 «PMID: 16792766»PubMed
- Gånemo A, Svensson A, Lindberg M ym. Quality of life in Swedish children with eczema. Acta Derm Venereol 2007;87:345-9 «PMID: 17598039»PubMed
- Koulu L. Atooppinen ihottuma vaikuttaa elämänlaatuun ja elämänhaluun. Duodecim 2020;136:2479-83
- Lammintausta K, Kalimo K, Raitala R ym. Prognosis of atopic dermatitis. A prospective study in early adulthood. Int J Dermatol 1991;30:563-8 «PMID: 1938054»PubMed
- Chida Y, Steptoe A, Hirakawa N ym. The effects of psychological intervention on atopic dermatitis. A systematic review and meta-analysis. Int Arch Allergy Immunol 2007;144:1-9 «PMID: 17449959»PubMed
- Ersser SJ, Cowdell F, Latter S ym. Psychological and educational interventions for atopic eczema in children. Cochrane Database Syst Rev 2014;2014:CD004054 «PMID: 24399641»PubMed
- Leshem YA, Chalmers JR, Apfelbacher C ym. Measuring atopic eczema symptoms in clinical practice: The first consensus statement from the Harmonising Outcome Measures for Eczema in clinical practice initiative. J Am Acad Dermatol 2020;82:1181-1186 «PMID: 31926221»PubMed
- Simpson E, Eckert L, Gadkari A ym. Validation of the Atopic Dermatitis Control Tool (ADCT©) using a longitudinal survey of biologic-treated patients with atopic dermatitis. BMC Dermatol 2019;19:15 «PMID: 31690295»PubMed
- Tarr A, Iheanacho I. Should we use bath emollients for atopic eczema? BMJ 2009;339:b4273 «PMID: 19914950»PubMed
- Chiang C, Eichenfield LF. Quantitative assessment of combination bathing and moisturizing regimens on skin hydration in atopic dermatitis. Pediatr Dermatol 2009;26:273-8 «PMID: 19706087»PubMed
- Cork MJ, Britton J, Butler L ym. Comparison of parent knowledge, therapy utilization and severity of atopic eczema before and after explanation and demonstration of topical therapies by a specialist dermatology nurse. Br J Dermatol 2003;149:582-9 «PMID: 14510993»PubMed
- van Zuuren EJ, Fedorowicz Z, Christensen R ym. Emollients and moisturisers for eczema. Cochrane Database Syst Rev 2017;2:CD012119 «PMID: 28166390»PubMed
- Wollenberg A, Kinberger M, Arents B ym. EuroGuiDerm Guideline on Atopic Eczema Version 2.1, December 2022. https://www.guidelines.edf.one/guidelines/atopic-ezcema. «https://www.guidelines.edf.one/guidelines/atopic-ezcema»32 Viitattu 30.3.2023.
- Williams HC. Clinical practice. Atopic dermatitis. N Engl J Med 2005;352:2314-24 «PMID: 15930422»PubMed
- Hoare C, Li Wan Po A, Williams H. Systematic review of treatments for atopic eczema. Health Technol Assess 2000;4:1-191 «PMID: 11134919»PubMed
- Hannuksela-Svahn A, Hannuksela M. Ihotautien paikallishoito ja ultraviolettivalohoito. Kirjassa Ihotaudit. Hannuksela, Peltonen, Reunala, Suhonen toim. Kustannus Oy Duodecim 2011
- Nesbitt LT. Glucocorticoids. In: Bologna JL, Jorizzo JL. Dermatology, 2nd edition. Mosby Elsevier 2008; 1923-34.
- Eichenfield LF, Tom WL, Berger TG ym. Guidelines of care for the management of atopic dermatitis: section 2. Management and treatment of atopic dermatitis with topical therapies. J Am Acad Dermatol 2014;71:116-32 «PMID: 24813302»PubMed
- Danby SG, Chittock J, Brown K ym. The effect of tacrolimus compared with betamethasone valerate on the skin barrier in volunteers with quiescent atopic dermatitis. Br J Dermatol 2014;170:914-21 «PMID: 24328907»PubMed
- Hanifin J, Gupta AK, Rajagopalan R. Intermittent dosing of fluticasone propionate cream for reducing the risk of relapse in atopic dermatitis patients. Br J Dermatol 2002;147:528-37 «PMID: 12207596»PubMed
- Berth-Jones J, Damstra RJ, Golsch S ym. Twice weekly fluticasone propionate added to emollient maintenance treatment to reduce risk of relapse in atopic dermatitis: randomised, double blind, parallel group study. BMJ 2003;326:1367 «PMID: 12816824»PubMed
- Williams HC. Established corticosteroid creams should be applied only once daily in patients with atopic eczema. BMJ 2007;334:1272 «PMID: 17569936»PubMed
- Woods MT, Brown PA, Baig-Lewis SF ym. Effects of a novel formulation of fluocinonide 0.1% cream on skin barrier function in atopic dermatitis. J Drugs Dermatol 2011;10:171-6 «PMID: 21283922»PubMed
- Bieber T, Vick K, Fölster-Holst R ym. Efficacy and safety of methylprednisolone aceponate ointment 0.1% compared to tacrolimus 0.03% in children and adolescents with an acute flare of severe atopic dermatitis. Allergy 2007;62:184-9 «PMID: 17298428»PubMed
- Stalder JF, Fleury M, Sourisse M ym. Local steroid therapy and bacterial skin flora in atopic dermatitis. Br J Dermatol 1994;131:536-40 «PMID: 7947206»PubMed
- Nilsson EJ, Henning CG, Magnusson J. Topical corticosteroids and Staphylococcus aureus in atopic dermatitis. J Am Acad Dermatol 1992;27:29-34 «PMID: 1619073»PubMed
- Oikarinen A, Autio P, Kiistala U ym. A new method to measure type I and III collagen synthesis in human skin in vivo: demonstration of decreased collagen synthesis after topical glucocorticoid treatment. J Invest Dermatol 1992;98:220-5 «PMID: 1732386»PubMed
- Hajar T, Leshem YA, Hanifin JM ym. A systematic review of topical corticosteroid withdrawal ("steroid addiction") in patients with atopic dermatitis and other dermatoses. J Am Acad Dermatol 2015;72:541-549.e2 «PMID: 25592622»PubMed
- Haeck IM, Rouwen TJ, Timmer-de Mik L ym. Topical corticosteroids in atopic dermatitis and the risk of glaucoma and cataracts. J Am Acad Dermatol 2011;64:275-81 «PMID: 21122943»PubMed
- Axon E, Chalmers JR, Santer M ym. Safety of topical corticosteroids in atopic eczema: an umbrella review. BMJ Open 2021;11:e046476 «PMID: 34233978»PubMed
- Kang S, Paller A, Soter N ym. Safe treatment of head/neck AD with tacrolimus ointment. J Dermatolog Treat 2003;14:86-94 «PMID: 12775315»PubMed
- Doss N, Reitamo S, Dubertret L ym. Superiority of tacrolimus 0.1% ointment compared with fluticasone 0.005% in adults with moderate to severe atopic dermatitis of the face: results from a randomized, double-blind trial. Br J Dermatol 2009;161:427-34 «PMID: 19416227»PubMed
- Murrell DF, Calvieri S, Ortonne JP ym. A randomized controlled trial of pimecrolimus cream 1% in adolescents and adults with head and neck atopic dermatitis and intolerant of, or dependent on, topical corticosteroids. Br J Dermatol 2007;157:954-9 «PMID: 17935515»PubMed
- Reitamo S, Rissanen J, Remitz A ym. Tacrolimus ointment does not affect collagen synthesis: results of a single-center randomized trial. J Invest Dermatol 1998;111:396-8 «PMID: 9740230»PubMed
- Kyllönen H, Remitz A, Mandelin JM ym. Effects of 1-year intermittent treatment with topical tacrolimus monotherapy on skin collagen synthesis in patients with atopic dermatitis. Br J Dermatol 2004;150:1174-81 «PMID: 15214906»PubMed
- Meurer M, Eichenfield LF, Ho V ym. Addition of pimecrolimus cream 1% to a topical corticosteroid treatment regimen in paediatric patients with severe atopic dermatitis: a randomized, double-blind trial. J Dermatolog Treat 2010;21:157-66 «PMID: 20394491»PubMed
- Cury Martins J, Martins C, Aoki V ym. Topical tacrolimus for atopic dermatitis. Cochrane Database Syst Rev 2015;2015:CD009864 «PMID: 26132597»PubMed
- Ashcroft DM, Chen LC, Garside R ym. Topical pimecrolimus for eczema. Cochrane Database Syst Rev 2007;2007:CD005500 «PMID: 17943859»PubMed
- Mandelin J, Remitz A, Reitamo S. Effect of oral acetylsalicylic acid on burning caused by tacrolimus ointment in patients with atopic dermatitis. Arch Dermatol 2010;146:1178-80 «PMID: 20956662»PubMed
- Reitamo S, Wollenberg A, Schöpf E ym. Safety and efficacy of 1 year of tacrolimus ointment monotherapy in adults with atopic dermatitis. The European Tacrolimus Ointment Study Group. Arch Dermatol 2000;136:999-1006 «PMID: 10926735»PubMed
- Hanifin JM, Ling MR, Langley R ym. Tacrolimus ointment for the treatment of atopic dermatitis in adult patients: part I, efficacy. J Am Acad Dermatol 2001;44:S28-38 «PMID: 11145793»PubMed
- Ling M, Gottlieb A, Pariser D ym. A randomized study of the safety, absorption and efficacy of pimecrolimus cream 1% applied twice or four times daily in patients with atopic dermatitis. J Dermatolog Treat 2005;16:142-8 «PMID: 16096179»PubMed
- Ashcroft DM, Dimmock P, Garside R ym. Efficacy and tolerability of topical pimecrolimus and tacrolimus in the treatment of atopic dermatitis: meta-analysis of randomised controlled trials. BMJ 2005;330:516 «PMID: 15731121»PubMed
- George SM, Karanovic S, Harrison DA ym. Interventions to reduce Staphylococcus aureus in the management of eczema. Cochrane Database Syst Rev 2019;2019: «PMID: 31684694»PubMed
- Remitz A, Kyllönen H, Granlund H ym. Tacrolimus ointment reduces staphylococcal colonization of atopic dermatitis lesions. J Allergy Clin Immunol 2001;107:196-7 «PMID: 11150013»PubMed
- Mayser P, Kupfer J, Nemetz D ym. Treatment of head and neck dermatitis with ciclopiroxolamine cream--results of a double-blind, placebo-controlled study. Skin Pharmacol Physiol 2006;19:153-8 «PMID: 16612143»PubMed
- Kaffenberger BH, Mathis J, Zirwas MJ. A retrospective descriptive study of oral azole antifungal agents in patients with patch test-negative head and neck predominant atopic dermatitis. J Am Acad Dermatol 2014;71:480-3 «PMID: 24925733»PubMed
- Svejgaard El, Larsen PØ, Deleuran M ym. Treatment of head and neck dermatitis comparing itraconazole 200 mg and 400 mg daily for 1 week with placebo. J Eur Acad Dermatol Venereol 2004;18:445-9 «PMID: 15196159»PubMed
- Krutmann J, Morita A. Mechanisms of ultraviolet (UV) B and UVA phototherapy. J Investig Dermatol Symp Proc 1999;4:70-2 «PMID: 10537012»PubMed
- Tintle S, Shemer A, Suárez-Fariñas M ym. Reversal of atopic dermatitis with narrow-band UVB phototherapy and biomarkers for therapeutic response. J Allergy Clin Immunol 2011;128:583-93.e1-4 «PMID: 21762976»PubMed
- Gambichler T, Skrygan M, Tomi NS ym. Changes of antimicrobial peptide mRNA expression in atopic eczema following phototherapy. Br J Dermatol 2006;155:1275-8 «PMID: 17107401»PubMed
- Lübbe J. Secondary infections in patients with atopic dermatitis. Am J Clin Dermatol 2003;4:641-54 «PMID: 12926982»PubMed
- Garritsen FM, Brouwer MW, Limpens J ym. Photo(chemo)therapy in the management of atopic dermatitis: an updated systematic review with implications for practice and research. Br J Dermatol 2014;170:501-13 «PMID: 24116934»PubMed
- Musters AH, Mashayekhi S, Harvey J ym. Phototherapy for atopic eczema. Cochrane Database Syst Rev 2021;10:CD013870 «PMID: 34709669»PubMed
- Reynolds NJ, Franklin V, Gray JC ym. Narrow-band ultraviolet B and broad-band ultraviolet A phototherapy in adult atopic eczema: a randomised controlled trial. Lancet 2001;357:2012-6 «PMID: 11438134»PubMed
- Ibbotson SH, Bilsland D, Cox NH ym. An update and guidance on narrowband ultraviolet B phototherapy: a British Photodermatology Group Workshop Report. Br J Dermatol 2004;151:283-97 «PMID: 15327535»PubMed
- Diffey BL. Factors affecting the choice of a ceiling on the number of exposures with TL01 ultraviolet B phototherapy. Br J Dermatol 2003;149:428-30 «PMID: 12932263»PubMed
- Sugie N, Fujii N, Danno K. Cyclosporin-A suppresses p53-dependent repair DNA synthesis and apoptosis following ultraviolet-B irradiation. Photodermatol Photoimmunol Photomed 2002;18:163-8 «PMID: 12390669»PubMed
- Schram ME, Roekevisch E, Leeflang MM ym. A randomized trial of methotrexate versus azathioprine for severe atopic eczema. J Allergy Clin Immunol 2011;128:353-9 «PMID: 21514637»PubMed
- Blauvelt A, de Bruin-Weller M, Gooderham M ym. Long-term management of moderate-to-severe atopic dermatitis with dupilumab and concomitant topical corticosteroids (LIBERTY AD CHRONOS): a 1-year, randomised, double-blinded, placebo-controlled, phase 3 trial. Lancet 2017;389:2287-2303 «PMID: 28478972»PubMed
- Simpson EL, Paller AS, Siegfried EC ym. Efficacy and Safety of Dupilumab in Adolescents With Uncontrolled Moderate to Severe Atopic Dermatitis: A Phase 3 Randomized Clinical Trial. JAMA Dermatol 2020;156:44-56 «PMID: 31693077»PubMed
- Husein-ElAhmed H, Steinhoff M. Dupilumab in prurigo nodularis: a systematic review of current evidence and analysis of predictive factors to response. J Dermatolog Treat 2022;33:1547-1553 «PMID: 33200955»PubMed
- Blauvelt A, Teixeira HD, Simpson EL ym. Efficacy and Safety of Upadacitinib vs Dupilumab in Adults With Moderate-to-Severe Atopic Dermatitis: A Randomized Clinical Trial. JAMA Dermatol 2021;157:1047-1055 «PMID: 34347860»PubMed
- Reich K, Thyssen JP, Blauvelt A ym. Efficacy and safety of abrocitinib versus dupilumab in adults with moderate-to-severe atopic dermatitis: a randomised, double-blind, multicentre phase 3 trial. Lancet 2022;400:273-282 «PMID: 35871814»PubMed
- Bieber T, Simpson EL, Silverberg JI ym. Abrocitinib versus Placebo or Dupilumab for Atopic Dermatitis. N Engl J Med 2021;384:1101-1112 «PMID: 33761207»PubMed
- Blauvelt A, Guttman-Yassky E, Paller AS ym. Long-Term Efficacy and Safety of Dupilumab in Adolescents with Moderate-to-Severe Atopic Dermatitis: Results Through Week 52 from a Phase III Open-Label Extension Trial (LIBERTY AD PED-OLE). Am J Clin Dermatol 2022;23:365-383 «PMID: 35567671»PubMed
- Siegels D, Heratizadeh A, Abraham S ym. Systemic treatments in the management of atopic dermatitis: A systematic review and meta-analysis. Allergy 2021;76:1053-1076 «PMID: 33074565»PubMed
- Thyssen JP, Heegaard S, Ivert L ym. Management of Ocular Manifestations of Atopic Dermatitis: A Consensus Meeting Using a Modified Delphi Process. Acta Derm Venereol 2020;100:adv00264 «PMID: 32926175»PubMed
- Simpson EL, Silverberg JI, Nosbaum A ym. Integrated Safety Analysis of Abrocitinib for the Treatment of Moderate-to-Severe Atopic Dermatitis From the Phase II and Phase III Clinical Trial Program. Am J Clin Dermatol 2021;22:693-707 «PMID: 34406619»PubMed
- Guttman-Yassky E, Teixeira HD, Simpson EL ym. Once-daily upadacitinib versus placebo in adolescents and adults with moderate-to-severe atopic dermatitis (Measure Up 1 and Measure Up 2): results from two replicate double-blind, randomised controlled phase 3 trials. Lancet 2021;397:2151-2168 «PMID: 34023008»PubMed
- Mendes-Bastos P, Ladizinski B, Guttman-Yassky E ym. Characterization of acne associated with upadacitinib treatment in patients with moderate-to-severe atopic dermatitis: A post hoc integrated analysis of 3 phase 3 randomized, double-blind, placebo-controlled trials. J Am Acad Dermatol 2022;87:784-791 «PMID: 35714786»PubMed
- Bath-Hextall FJ, Birnie AJ, Ravenscroft JC ym. Interventions to reduce Staphylococcus aureus in the management of atopic eczema: an updated Cochrane review. Br J Dermatol 2010;163:12-26 «PMID: 20222931»PubMed
- Sidbury R, Davis DM, Cohen DE ym. Guidelines of care for the management of atopic dermatitis: section 3. Management and treatment with phototherapy and systemic agents. J Am Acad Dermatol 2014;71:327-49 «PMID: 24813298»PubMed
- Boguniewicz M, Sampson H, Leung SB ym. Effects of cefuroxime axetil on Staphylococcus aureus colonization and superantigen production in atopic dermatitis. J Allergy Clin Immunol 2001;108:651-2 «PMID: 11590398»PubMed
- Ewing CI, Ashcroft C, Gibbs AC ym. Flucloxacillin in the treatment of atopic dermatitis. Br J Dermatol 1998;138:1022-9 «PMID: 9747366»PubMed
- Klein PA, Clark RA. An evidence-based review of the efficacy of antihistamines in relieving pruritus in atopic dermatitis. Arch Dermatol 1999;135:1522-5 «PMID: 10606058»PubMed
- Ng JC, Yew YW. Effect of Vitamin D Serum Levels and Supplementation on Atopic Dermatitis: A Systematic Review and Meta-analysis. Am J Clin Dermatol 2022;23:267-275 «PMID: 35246808»PubMed
- Vestita M, Filoni A, Congedo M ym. Vitamin D and atopic dermatitis in childhood. J Immunol Res 2015;2015:257879 «PMID: 25973433»PubMed
- Ong PY, Boguniewicz M. Investigational and unproven therapies in atopic dermatitis. Immunol Allergy Clin North Am 2010;30:425-39 «PMID: 20670823»PubMed
- Ernst E, Pittler MH, Stevinson C. Complementary/alternative medicine in dermatology: evidence-assessed efficacy of two diseases and two treatments. Am J Clin Dermatol 2002;3:341-8 «PMID: 12069640»PubMed
- Kim GW, Park JM, Chin HW ym. Comparative analysis of the use of complementary and alternative medicine by Korean patients with androgenetic alopecia, atopic dermatitis and psoriasis. J Eur Acad Dermatol Venereol 2013;27:827-35 «PMID: 22620682»PubMed
- Simpson EL, Basco M, Hanifin J. A cross-sectional survey of complementary and alternative medicine use in patients with atopic dermatitis. Am J Contact Dermat 2003;14:144-7 «PMID: 14744405»PubMed
- Hughes R, Ward D, Tobin AM ym. The use of alternative medicine in pediatric patients with atopic dermatitis. Pediatr Dermatol 2007;24:118-20 «PMID: 17461804»PubMed
- Gu S, Yang AW, Xue CC ym. Chinese herbal medicine for atopic eczema. Cochrane Database Syst Rev 2013;:CD008642 «PMID: 24018636»PubMed
- Tan HY, Zhang AL, Chen D ym. Chinese herbal medicine for atopic dermatitis: a systematic review. J Am Acad Dermatol 2013;69:295-304 «PMID: 23759835»PubMed
- Gu S, Yang AW, Li CG ym. Topical application of Chinese herbal medicine for atopic eczema: a systematic review with a meta-analysis. Dermatology 2014;228:294-302 «PMID: 24821063»PubMed
- Sheehan MP, Atherton DJ. One-year follow up of children treated with Chinese medicinal herbs for atopic eczema. Br J Dermatol 1994;130:488-93 «PMID: 8186115»PubMed
- Boneberger S, Rupec RA, Ruzicka T. Complementary therapy for atopic dermatitis and other allergic skin diseases: facts and controversies. Clin Dermatol 2010;28:57-61 «PMID: 20082952»PubMed
- Bath-Hextall F, Williams H. Atopic eczema. Clin Evid 2006;15:1-20
- Torley D, Futamura M, Williams HC ym. What's new in atopic eczema? An analysis of systematic reviews published in 2010-11. Clin Exp Dermatol 2013;38:449-56 «PMID: 23750610»PubMed
- Jiao R, Yang Z, Wang Y ym. The effectiveness and safety of acupuncture for patients with atopic eczema: a systematic review and meta-analysis. Acupunct Med 2020;38:3-14 «PMID: 31495184»PubMed
- Thyssen JP, Schuttelaar MLA, Alfonso JH ym. Guidelines for diagnosis, prevention, and treatment of hand eczema. Contact Dermatitis 2022;86:357-378 «PMID: 34971008»PubMed
- Koutroulis I, Papoutsis J, Kroumpouzos G. Atopic dermatitis in pregnancy: current status and challenges. Obstet Gynecol Surv 2011;66:654-63 «PMID: 22112526»PubMed
- Balakirski G, Novak N. Atopic dermatitis and pregnancy. J Allergy Clin Immunol 2022;149:1185-1194 «PMID: 35090948»PubMed
- Vestergaard C, Wollenberg A, Barbarot S ym. European task force on atopic dermatitis position paper: treatment of parental atopic dermatitis during preconception, pregnancy and lactation period. J Eur Acad Dermatol Venereol 2019;33:1644-1659 «PMID: 31231864»PubMed
- Weatherhead S, Robson SC, Reynolds NJ. Eczema in pregnancy. BMJ 2007;335:152-4 «PMID: 17641349»PubMed
- Malm H. Teratologinen palvelu. Henkilökohtainen tiedonanto. 9.2.2023
- Mahadevan U, Long MD, Kane SV ym. Pregnancy and Neonatal Outcomes After Fetal Exposure to Biologics and Thiopurines Among Women With Inflammatory Bowel Disease. Gastroenterology 2021;160:1131-1139 «PMID: 33227283»PubMed
- Bar-Gil Shitrit A, Grisaru-Granovsky S, Ben Ya'acov A ym. Management of Inflammatory Bowel Disease During Pregnancy. Dig Dis Sci 2016;61:2194-2204 «PMID: 27068171»PubMed
- Russell MD, Dey M, Flint J ym. British Society for Rheumatology guideline on prescribing drugs in pregnancy and breastfeeding: immunomodulatory anti-rheumatic drugs and corticosteroids. Rheumatology (Oxford) 2023;62:e48-e88 «PMID: 36318966»PubMed
- García-Soto L, Martín-Masot R, Espadafor-López B ym. Evaluation of atopy schools for parents. Allergol Immunopathol (Madr) 2021;49:1-5 «PMID: 33641287»PubMed
- Miyaji Y, Yang L, Yamamoto-Hanada K ym. Earlier aggressive treatment to shorten the duration of eczema in infants resulted in fewer food allergies at 2 years of age. J Allergy Clin Immunol Pract 2020;8:1721-1724.e6 «PMID: 31821918»PubMed
- Kelleher MM, Dunn-Galvin A, Gray C ym. Skin barrier impairment at birth predicts food allergy at 2 years of age. J Allergy Clin Immunol 2016;137:1111-1116.e8 «PMID: 26924469»PubMed
- Brough HA, Simpson A, Makinson K ym. Peanut allergy: effect of environmental peanut exposure in children with filaggrin loss-of-function mutations. J Allergy Clin Immunol 2014;134:867-875.e1 «PMID: 25282568»PubMed
- Salava A, Perälä M, Pelkonen A ym. Safety of tacrolimus 0.03% and 0.1% ointments in young children with atopic dermatitis: a 36-month follow-up study. Clin Exp Dermatol 2022;47:889-902 «PMID: 34798685»PubMed
- Perälä M, Salava A, Malmberg P ym. Topical tacrolimus and corticosteroids in childhood moderate-to-severe atopic dermatitis with impact on airways: A long-term randomized open-label study. Clin Exp Dermatol 2023;: «PMID: 36916653»PubMed
- Thomas KS, Armstrong S, Avery A ym. Randomised controlled trial of short bursts of a potent topical corticosteroid versus prolonged use of a mild preparation for children with mild or moderate atopic eczema. BMJ 2002;324:768 «PMID: 11923161»PubMed
- Devillers AC, Oranje AP. Efficacy and safety of 'wet-wrap' dressings as an intervention treatment in children with severe and/or refractory atopic dermatitis: a critical review of the literature. Br J Dermatol 2006;154:579-85 «PMID: 16536797»PubMed
- Nicol NH, Boguniewicz M, Strand M ym. Wet wrap therapy in children with moderate to severe atopic dermatitis in a multidisciplinary treatment program. J Allergy Clin Immunol Pract 2014;2:400-6 «PMID: 25017527»PubMed
- Ainley-Walker PF, Patel L, David TJ. Side to side comparison of topical treatment in atopic dermatitis. Arch Dis Child 1998;79:149-52 «PMID: 9797597»PubMed
- Davallow Ghajar L, Wood Heickman LK, Conaway M ym. Low Risk of Adrenal Insufficiency After Use of Low- to Moderate-Potency Topical Corticosteroids for Children With Atopic Dermatitis. Clin Pediatr (Phila) 2019;58:406-412 «PMID: 30694073»PubMed
- Reitamo S, Rustin M, Harper J ym. A 4-year follow-up study of atopic dermatitis therapy with 0.1% tacrolimus ointment in children and adult patients. Br J Dermatol 2008;159:942-51 «PMID: 18637898»PubMed
- Wahn U, Bos JD, Goodfield M ym. Efficacy and safety of pimecrolimus cream in the long-term management of atopic dermatitis in children. Pediatrics 2002;110:e2 «PMID: 12093983»PubMed
- Sigurgeirsson B, Ho V, Ferrándiz C ym. Effectiveness and safety of a prevention-of-flare-progression strategy with pimecrolimus cream 1% in the management of paediatric atopic dermatitis. J Eur Acad Dermatol Venereol 2008;22:1290-301 «PMID: 18624866»PubMed
- Schmitt J, von Kobyletzki L, Svensson A ym. Efficacy and tolerability of proactive treatment with topical corticosteroids and calcineurin inhibitors for atopic eczema: systematic review and meta-analysis of randomized controlled trials. Br J Dermatol 2011;164:415-28 «PMID: 20819086»PubMed
- Paul C, Cork M, Rossi AB ym. Safety and tolerability of 1% pimecrolimus cream among infants: experience with 1133 patients treated for up to 2 years. Pediatrics 2006;117:e118-28 «PMID: 16361223»PubMed
- Kapp A, Papp K, Bingham A ym. Long-term management of atopic dermatitis in infants with topical pimecrolimus, a nonsteroid anti-inflammatory drug. J Allergy Clin Immunol 2002;110:277-84 «PMID: 12170269»PubMed
- Koo JY, Fleischer AB Jr, Abramovits W ym. Tacrolimus ointment is safe and effective in the treatment of atopic dermatitis: results in 8000 patients. J Am Acad Dermatol 2005;53:S195-205 «PMID: 16021175»PubMed
- Staab D, Pariser D, Gottlieb AB ym. Low systemic absorption and good tolerability of pimecrolimus, administered as 1% cream (Elidel) in infants with atopic dermatitis--a multicenter, 3-week, open-label study. Pediatr Dermatol 2005;22:465-71 «PMID: 16191004»PubMed
- Alaiti S, Kang S, Fiedler VC ym. Tacrolimus (FK506) ointment for atopic dermatitis: a phase I study in adults and children. J Am Acad Dermatol 1998;38:69-76 «PMID: 9448208»PubMed
- Remitz A, Harper J, Rustin M ym. Long-term safety and efficacy of tacrolimus ointment for the treatment of atopic dermatitis in children. Acta Derm Venereol 2007;87:54-61 «PMID: 17225017»PubMed
- Stiehm ER, Roberts RL, Kaplan MS ym. Pneumococcal seroconversion after vaccination for children with atopic dermatitis treated with tacrolimus ointment. J Am Acad Dermatol 2005;53:S206-13 «PMID: 16021176»PubMed
- Papp KA, Breuer K, Meurer M ym. Long-term treatment of atopic dermatitis with pimecrolimus cream 1% in infants does not interfere with the development of protective antibodies after vaccination. J Am Acad Dermatol 2005;52:247-53 «PMID: 15692469»PubMed
- Paller AS, Simpson EL, Siegfried EC ym. Dupilumab in children aged 6 months to younger than 6 years with uncontrolled atopic dermatitis: a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2022;400:908-919 «PMID: 36116481»PubMed
- Eichenfield LF, Flohr C, Sidbury R ym. Efficacy and Safety of Abrocitinib in Combination With Topical Therapy in Adolescents With Moderate-to-Severe Atopic Dermatitis: The JADE TEEN Randomized Clinical Trial. JAMA Dermatol 2021;157:1165-1173 «PMID: 34406366»PubMed
- Boyle RJ, Bath-Hextall FJ, Leonardi-Bee J ym. Probiotics for the treatment of eczema: a systematic review. Clin Exp Allergy 2009;39:1117-27 «PMID: 19573037»PubMed
- Baquerizo Nole KL, Yim E, Keri JE. Probiotics and prebiotics in dermatology. J Am Acad Dermatol 2014;71:814-21 «PMID: 24906613»PubMed
- van der Aa LB, Heymans HS, van Aalderen WM ym. Effect of a new synbiotic mixture on atopic dermatitis in infants: a randomized-controlled trial. Clin Exp Allergy 2010;40:795-804 «PMID: 20184604»PubMed
- Collins P, Ferguson J. Narrowband (TL-01) UVB air-conditioned phototherapy for atopic eczema in children. Br J Dermatol 1995;133:653-5 «PMID: 7577604»PubMed
- Bryld LE, Hindsberger C, Kyvik KO ym. Risk factors influencing the development of hand eczema in a population-based twin sample. Br J Dermatol 2003;149:1214-20 «PMID: 14674899»PubMed
- Johannisson A, Pontén A, Svensson Å. Prevalence, incidence and predictive factors for hand eczema in young adults - a follow-up study. BMC Dermatol 2013;13:14 «PMID: 24164871»PubMed
- Coenraads P-J, Diepgen TL. Risk for hand eczema in employees with past or present atopic dermatitis. Int Arch Occup Environ Health 1998;71:7-13
- Työperäiset sairaudet. Työterveyslaitos 2008. www.ttl.fi «http://www.ttl.fi»17
- Lindström I, Mäkelä M, Pelkonen A ym. Astma, atooppinen ihottuma ja allergiat on huomioitava ammatinvalinnassa ja varusmiespalveluksessa. Suom Lääkäril 2023;78:e33929

