Psoriasis och psoriasisartrit
Hur kan man hänvisa till God medicinsk praxis-rekommendationen? «K1»1
Den här svenskspråkiga God medicinsk praxis-rekommendationen har översatts från den finska God medicinsk praxis-rekommendationen (Käypä hoito -suositus Psoriaasi ja nivelpsoriaasi «Psoriaasi ja nivelpsoriaasi»1). Om det finns skillnader i texterna gäller den uppdaterade finskspråkiga versionen.
Huvudsakligen finns evidenssammandragen och bakgrundsmaterialen samt internetlänkarna på finska.
Centrala rekommendationer
- Psoriasis är en mångformig (polymorf), kronisk och ofta familjär immunologisk inflammationssjukdom.
- Hud- och ledsymtomen är lindriga hos majoriteten av patienterna. Även lindrig psoriasis eller psoriasisartrit kan dock försämra patientens livskvalitet. Livskvaliteten försämras framför allt av svår psoriasisartrit och av hudpsoriasis om den förekommer i synliga områden eller på stora områden.
- Symtomen på psoriasis kan behandlas på många sätt trots att sjukdomen inte kan botas. Målet med behandlingen är att minimera symtomen och att förbättra livskvaliteten samt att bevara patientens arbets- och funktionsförmåga.
- Risken för artärsjukdomar och diabetes hos psoriasispatienter ska alltid beaktas när behandlingen planeras. Associerade sjukdomar kan konstateras redan hos barn. Patienten uppmuntras till sunda levnadsvanor. Eventuell ångest och depression ska beaktas och behandlas i tid.
- Behandlingen väljs alltid individuellt (se Nivåstrukturering av vården av hudpsoriasis «Nivåstrukturering av vården vid hudpsoriasis»1). Vid valet av behandling av psoriasis beaktas sjukdomens aktivitet och hur den kommer till uttryck.

Nivåstrukturering av vården vid hudpsoriasis
Bild: Tapio Rantanen
Mål
- Syftet med rekommendationen är att
- förenhetliga diagnostik och behandlingar av hudpsoriasis och psoriasisartrit på basis av tillgänglig evidens
- ge en rekommendation för nivåstruktureringen av vården till primärvården och specialsjukvården.
Målgrupp
- Rekommendationen är avsedd för alla yrkesutbildade personer inom hälso- och sjukvården som i sitt arbete vårdar eller behandlar psoriasispatienter.
Avgränsning
- Rekommendationen behandlar inte pustulosis palmoplantaris.
- När det gäller ledsjukdomar hos barn har litteratursökningarna gällt psoriasisartrit. Några omfattande sökningar har inte gjorts för barnreuma.
- I uppdateringen av rekommendationen (publicerad 8.10.2024) uppdaterades rekommendationens psoriasisartritdel.
Definitioner
- Psoriasis är en kronisk, polymorf (mångformig), immunmedierad inflammationssjukdom som vanligen tar sig uttryck i hudpsoriasis och psoriasisartrit «Mälkonen T, Suomela S. [What do we know about path...»1, «Matikainen S, Jokiranta S, Eklund KK. [Role of cyt...»2, «Global report on psoriasis. World Health Organizat...»3, «https://www.duodecimlehti.fi/lehti/2011/15/duo99684»1.
- Hos barn kommer psoriasisartrit under diagnosen barnreuma i ILAR-klassificeringen
(International League Against Rheumatism) «Petty RE, Southwood TR, Manners P ym. Internationa...»4. Psoriasisartrit hos barn definieras som en kronisk ledinflammation som utbryter
före 16 års ålder, som uppkommit av okänd anledning, som pågått i minst 6 veckor och
som är förknippad med utslag som uppfyller de diagnostiska kriterierna för psoriasis
eller, om utslag saknas, uppfyller minst 2 av dessa kriterier:
- nagelförändringar
- daktylit
- psoriasis hos släkting i första ledet.
Förkortningar
- ACR-kriterierna (American College of Rheumatology) = kriterier för bedömning av aktiviteten hos ledgångsreumatism. Kriterierna används också för att bedöma effekten av läkemedelsbehandling för psoriasisartrit «Felson DT, Anderson JJ, Boers M ym. American Colle...»5.
- BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) = verktyg för att mäta sjukdomsaktiviteten av spondylartropatier «https://www.reumatologinenyhdistys.fi/laakerekisteri-lomakkeet/»2.
- BASFI (Bath Ankylosing Spondylitis Functional Index) = verktyg som mäter spondylartropatipatientens funktion «https://www.reumatologinenyhdistys.fi/laakerekisteri-lomakkeet/»2.
- BSA (Body Surface Area) = hudområde täckt av eksem (%).
- DLQI (Dermatology Life Quality Index) = enkät som används för att mäta livskvaliteten hos patienter med hudsjukdom (enkätanvisningar «hoi50062b.pdf»1 och länk till enkäten «http://sites.cardiff.ac.uk/dermatology/files/2014/04/DLQI-Finnish.pdf»3).
- HAQ (Health Assessment Questionnaire) = mätare av funktionsförmågan som använts inom reumatologin «https://www.reumatologinenyhdistys.fi/laakerekisteri-lomakkeet/»2 (se God medicinsk praxis-rekommendationen om ledgångsreumatism (Nivelreuma «Nivelreuma»2 (på finska)).
- JADAS10-index (Juvenile Arthritis Disease Activity Score) = indikator för sjukdomsaktiviteten vid barnreuma.
- PASI (Psoriasis Area and Severity Index) = verktyg som används för att fastställa svårighetsgraden av hudpsoriasis och som beaktar eksemets omfattning (procentuell andel) på huvudet, bålen och övre och nedre extremiteterna separat samt fläckarnas rodnad, tjocklek och fjällning (se avsnittet Svårighetsgrad av hudpsoriasis) (PASI-räknare «gvr00091a.xls»2). Se även tabell «Definitioner associerade med terapisvaret för patienter med hudpsoriasis , ...»1.
- PsA (Psoriatic Arthritis) = psoriasisartrit.
- PsARC (Psoriatic Arthritis Response Criteria) = indikator för aktiviteten av psoriasisartrit.
- ACR Pedi-respons = American College of Rheumatologys rekommendation för bedömning av aktivitetsförändringar hos patienter med barnreuma «Giannini EH, Ruperto N, Ravelli A ym. Preliminary ...»6.
| Förkortning | Definition | |
|---|---|---|
| Otillräckligt terapisvar | < PASI-50 | PASI har minskat med mindre än 50 % från utgångsläget |
| Måttligt terapisvar | PASI-50 | PASI har minskat med minst 50 % från utgångsläget |
| Gott terapisvar | PASI-75 | PASI har minskat med minst 75 % jämfört med utgångsläget, motsvarar PASI-värdet ≤ 4 |
| Utmärkt terapisvar | PASI-90 | PASI har minskat med minst 90 % jämfört med utgångsläget, motsvarar PASI-värdet ≤ 2 |
| Fullständigt terapisvar | PASI-100 | PASI har minskat med 100 % från utgångsläget = huden är symtomfri |
| Relaps | Av minskningen av PASI har minst 50 % återkommit | |
| Relapstid | Tid från avslutad behandling till relaps | |
| Terapisvarets varaktighet | Tid från PASI-50 till förlust av terapisvar | |
| Rebound | PASI+125 | Försämring på minst 25 % jämfört med utgångsläget |
Prevalens
- I Europa och Nordamerika har 1,5–3 % av befolkningen hudpsoriasis «Global report on psoriasis. World Health Organizat...»3, «Parisi R, Symmons DP, Griffiths CE ym. Global epid...»9. I befolkningsenkäter har större prevalenstal publicerats «Danielsen K, Olsen AO, Wilsgaard T ym. Is the prev...»10, «Svensson A, Ofenloch RF, Bruze M ym. Prevalence of...»11 «Egeberg A, Andersen YMF, Thyssen JP. Prevalence an...»12.
- Hos personer under 18 år är förekomsten före puberteten 0,1–0,5 % och efter puberteten 0,6–1,3 % «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13.
- På 1990-talet förekom 100–140 nya fall hudpsoriasis per 100 000 invånare per år bland den vita befolkningen i USA och Europa. Den årliga incidensen bland personer under 18 år var 63/100 000 «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13, «Tollefson MM, Crowson CS, McEvoy MT ym. Incidence ...»14, «Huerta C, Rivero E, Rodríguez LA. Incidence and ri...»15, «Icen M, Crowson CS, McEvoy MT ym. Trends in incide...»16.
- Psoriasis kan uppkomma i vilken ålder som helst.
- Det finns två ålderstoppar för sjukdomsdebuten: den första är i ungdomen och den andra i 50–60 års åldern, vilket främst beror på genetiska riskfaktorer «Henseler T, Christophers E. Psoriasis of early and...»17, «Lønnberg AS, Skov L, Duffy DL ym. Genetic Factors ...»18
- Hos en tredjedel av patienterna uppkommer sjukdomens första symtom före 20 års ålder «Tollefson MM, Crowson CS, McEvoy MT ym. Incidence ...»14, «Vogel SA, Yentzer B, Davis SA ym. Trends in pediat...»19.
- Psoriasisartrit förekommer hos 0,16–0,25 % av den oselekerade befolkningen «Gelfand JM, Gladman DD, Mease PJ ym. Epidemiology ...»20, «Madland TM, Apalset EM, Johannessen AE ym. Prevale...»21, «Wilson FC, Icen M, Crowson CS ym. Time trends in e...»22. Årligen uppkommer 6–10 nya fall av psoriasis per 100 000 «Kaipiainen-Seppänen O. Incidence of psoriatic arth...»23, «Alamanos Y, Voulgari PV, Drosos AA. Incidence and ...»24, «Wilson FC, Icen M, Crowson CS ym. Incidence and cl...»25.
- Risken för psoriasisartrit hos en psoriasispatient ökar kontinuerligt med åren.
- I en befolkningsbaserad undersökning hade 2,4 % av psoriasispatienterna psoriasisartrit då sjukdomen konstaterades, och under 20 års uppföljning insjuknade ytterligare 5,1 % i psoriasisartrit «Wilson FC, Icen M, Crowson CS ym. Time trends in e...»22.
- Hos personer med svår hudpsoriasis är risken för psoriasisartrit betydligt större och uppgår till 20–35% för psoriasispatienter som behöver behandling med biologiska läkemedel «Prey S, Paul C, Bronsard V ym. Assessment of risk ...»26, «Christophers E, Barker JN, Griffiths CE ym. The ri...»27.
- Hos en liten del föregår ledsymtomen hudsymtomen «Gladman DD, Shuckett R, Russell ML ym. Psoriatic a...»28.
- Ledsymtom har rapporterats hos 0,7–10,5 % av patienterna med barnpsoriasis «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13.
- Kvinnor och män insjuknar lika ofta i psoriasisartrit, men spondylartropati är vanligare hos män «Kaipiainen-Seppänen O. Incidence of psoriatic arth...»23. Incidensen av barnreuma har i olika länder och undersökningar varit 1,6–23 «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13 och i det finländska materialet 21–23/100 000 «Berntson L, Andersson Gäre B, Fasth A ym. Incidenc...»29, «Savolainen E, Kaipiainen-Seppänen O, Kröger L ym. ...»30, «Virta R, Helenius H, Klaukka T. Lasten reuma yleis...»31. Av dessa är andelen psoriasisartrit hos barn cirka 6 % «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13. Incidensen av psoriasis hos barn är 0,3–0,5/100 000 «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13. Det har rapporterats att sjukdomen förekommer oftare hos flickor än hos pojkar «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13.
- Incidensen av både hudpsoriasis och psoriasisartrit har ökat under 30 års uppföljning «Tollefson MM, Crowson CS, McEvoy MT ym. Incidence ...»14, «Huerta C, Rivero E, Rodríguez LA. Incidence and ri...»15, «Wilson FC, Icen M, Crowson CS ym. Incidence and cl...»25, «Icen M, Crowson CS, McEvoy MT ym. Trends in incide...»32, «Dand N, Mahil SK, Capon F ym. Psoriasis and Geneti...»33.
Riskfaktorer
- Bakom psoriasis finns genetiska riskfaktorer «Dand N, Mahil SK, Capon F ym. Psoriasis and Geneti...»33.
- Om båda föräldrarna har psoriasis är risken för insjuknande 41–65 % «Lomholt G. Psoriasis. Prevalence, Spontaneous Cour...»34, «Swanbeck G, Inerot A, Martinsson T ym. Genetic cou...»35, «Mallbris L, Larsson P, Bergqvist S ym. Psoriasis p...»38.
- Om den ena föräldern har psoriasis är risken för insjuknande 14–28 % «Swanbeck G, Inerot A, Martinsson T ym. Genetic cou...»35, «Asumalahti K, Saarialho-Kere U, Kere J. [The patho...»36, «Andressen C, Henseler T. [Inheritance of psoriasis...»37.
- Hos cirka 30 % av patienterna med psoriasisartrit förekommer psoriasis i den närmaste släkten «Mallbris L, Larsson P, Bergqvist S ym. Psoriasis p...»38.
- Flera riskgener har lokaliserats i olika kromosomer, och deras funktionella samband med biologiska mekanismer har gestaltat sig småningom «Mälkonen T, Suomela S. [What do we know about path...»1, «Dand N, Mahil SK, Capon F ym. Psoriasis and Geneti...»33, «Harden JL, Krueger JG, Bowcock AM. The immunogenet...»39. Uppfattningen att psoriasis är en autoimmun sjukdom har stärkts av att tre autoantigener har identifierats «Arakawa A, Siewert K, Stöhr J ym. Melanocyte antig...»40, «Lande R, Botti E, Jandus C ym. The antimicrobial p...»41, «Cheung KL, Jarrett R, Subramaniam S ym. Psoriatic ...»42. För mer information se «Psoriaasin alttiusgeenejä»1.
- Den mest kända utlösande faktorn för droppformad psoriasis är svalginflammation orsakad av Streptococcus pyogenes «Mallbris L, Larsson P, Bergqvist S ym. Psoriasis p...»38, «Gudjonsson JE, Thorarinsson AM, Sigurgeirsson B ym...»43.
- Stress «Mallbris L, Larsson P, Bergqvist S ym. Psoriasis p...»38, «Seville RH. Stress and psoriasis: the importance o...»44, «Naldi L, Peli L, Parazzini F ym. Family history of...»45, «Li WQ, Qureshi AA, Schernhammer ES ym. Rotating ni...»46, depression «Dominguez PL, Han J, Li T ym. Depression and the r...»47, övervikt «Huerta C, Rivero E, Rodríguez LA. Incidence and ri...»15, «Wu S, Li WQ, Han J ym. Hypercholesterolemia and ri...»48, «Naldi L, Chatenoud L, Linder D ym. Cigarette smoki...»49, «Setty AR, Curhan G, Choi HK. Obesity, waist circum...»50, «Wolk K, Mallbris L, Larsson P ym. Excessive body w...»51, rökning «Huerta C, Rivero E, Rodríguez LA. Incidence and ri...»15, «Naldi L, Chatenoud L, Linder D ym. Cigarette smoki...»49, «Wolk K, Mallbris L, Larsson P ym. Excessive body w...»51, «Li W, Han J, Choi HK ym. Smoking and risk of incid...»52, «Setty AR, Curhan G, Choi HK. Smoking and the risk ...»53 och riklig alkoholkonsumtion «Poikolainen K, Reunala T, Karvonen J ym. Alcohol i...»54, «Qureshi AA, Dominguez PL, Choi HK ym. Alcohol inta...»55 ökar risken för plackpsoriasis och försvårar symtomen «Ockenfels HM. [Trigger factors for psoriasis]. Hau...»56, «Poikolainen K, Reunala T, Karvonen J. Smoking, alc...»57.
- Dessutom kan psoriasis utlösas eller försvåras av olika infektioner «Keller JJ, Wu CS, Lin HC. Increased risk of psoria...»58 (t.ex. streptokockinfektioner i svalget «Thorleifsdottir RH, Eysteinsdóttir JH, Olafsson JH...»59, parodontit och andra tandinflammationer samt HIV), trauman (Köbners fenomen) och
vissa läkemedel «Dika E, Varotti C, Bardazzi F ym. Drug-induced pso...»60.
- Klinisk erfarenhet visar att psoriasis försvåras bl.a. av litium, klorokin och terbinafin.
- Interferonerna alfa och gamma samt imikvimod påverkar immunsystemet och försvårar psoriasis.
- Psoriasis eller pustulosis palmoplantaris kan uppkomma vid användning av hämmare av tumörnekrosfaktor alfa för andra indikationer «Harrison MJ, Dixon WG, Watson KD ym. Rates of new-...»61, «Shmidt E, Wetter DA, Ferguson SB ym. Psoriasis and...»62, «Guerra I, Algaba A, Pérez-Calle JL ym. Induction o...»63.
- Betablockerare och ACE-hämmare förefaller inte att påverka psoriasisförloppet «Brauchli YB, Jick SS, Curtin F ym. Association bet...»64.
- De viktigaste riskfaktorerna och prognostiska faktorerna för psoriasisartrit är psoriasis i släkten «Karason A, Love TJ, Gudbjornsson B. A strong herit...»65 samt psoriasis i naglarna och flera olika hudområden hos patienten «Wilson FC, Icen M, Crowson CS ym. Incidence and cl...»25. Övervikt ökar risken för psoriasisartrit hos psoriasispatienter, medan viktminskning minskar denna risk lineärt under 10 års uppföljning «Green A, Shaddick G, Charlton R ym. Modifiable ris...»66, «Eder L, Harvey P, Chandran V ym. Gaps in Diagnosis...»67. Undersökningsresultaten gällande rökning som riskfaktor för psoriasisartrit är motstridiga «Li W, Han J, Choi HK ym. Smoking and risk of incid...»52, «Eder L, Shanmugarajah S, Thavaneswaran A ym. The a...»68. Hos personer med axial spondylartrit ökar rökning risken för psoriasisartrit «Pezzolo E, Naldi L. The relationship between smoki...»69, «Zhao SS, Goodson NJ, Robertson S ym. Smoking in sp...»70, «Tsuruta N, Imafuku S, Narisawa Y. Hyperuricemia is...»71.
Associerade sjukdomar
- Jämfört med den övriga befolkningen förekommer vissa sjukdomar och tillstånd oftare hos patienterna med svår hud- och ledpsoriasis. Detta gäller hjärt- och kärlsjukdomar och hjärt- och hjärninfarkter «Vaikeaa ihopsoriaasia sairastavilla on muuta väestöä useammin sydän- ja verisuonisairauksia.»A samt riskfaktorer för dessa «Neimann AL, Shin DB, Wang X ym. Prevalence of card...»72, «Mallbris L, Ritchlin CT, Ståhle M. Metabolic disor...»73, «Husted JA, Thavaneswaran A, Chandran V ym. Cardiov...»74, såsom övervikt, blodtryckssjukdom, vuxendiabetes, fettlever, förhöjda blodfettvärden, rökning «Naldi L, Chatenoud L, Linder D ym. Cigarette smoki...»49, «Li W, Han J, Choi HK ym. Smoking and risk of incid...»52, «Poikolainen K, Reunala T, Karvonen J. Smoking, alc...»57 och överkonsumtion av alkohol «Poikolainen K, Reunala T, Karvonen J ym. Alcohol i...»54, «McAleer MA, Mason DL, Cunningham S ym. Alcohol mis...»75. Kronisk inflammation i kroppen p.g.a. svår psoriasis utgör en separat riskfaktor för kranskärlssjukdom «Mehta NN, Azfar RS, Shin DB ym. Patients with seve...»76. Kranskärlssjukdom är den viktigaste orsaken till överdödlighet hos patienterna med svår psoriasis «Gelfand JM, Troxel AB, Lewis JD ym. The risk of mo...»77, «Abuabara K, Azfar RS, Shin DB ym. Cause-specific m...»78. Hos personer med metabolt syndrom är halten av urat i blodet ofta förhöjt.
- Personer med hudpsoriasis och psoriasisartrit har inflammatoriska tarmsjukdomar (Crohns sjukdom och ulcerös kolit) «Cohen AD, Dreiher J, Birkenfeld S. Psoriasis assoc...»79 samt celiaki «Ludvigsson JF, Lindelöf B, Zingone F ym. Psoriasis...»80 något oftare än den övriga befolkningen. Torra ögon och anterior uveit kan förekomma särskilt hos patienter med psoriasisartrit «Rehal B, Modjtahedi BS, Morse LS ym. Ocular psoria...»81.
- Svår psoriasis är förknippad med en lätt förhöjd risk för lymfom «Vaikeaan psoriaasiin näyttää liittyvän lievästi kohonnut lymfoomariski.»B, dermal keratinocytcancer «Vaikeaan psoriaasiin liittyy lievästi kohonnut ihon okasolusyövän riski, jonka tärkein riskitekijä on metoksaleeni-tabletti-PUVA-hoito.»A och förhöjd risk för cancersjukdomar med koppling till levnadsvanorna «Boffetta P, Gridley G, Lindelöf B. Cancer risk in ...»82, «Brauchli YB, Jick SS, Miret M ym. Psoriasis and ri...»83, «Chen YJ, Wu CY, Chen TJ ym. The risk of cancer in ...»84.
- Risken för depression, ångest och suicid är förhöjd särskilt hos personer med svår psoriasis och hos unga psoriasispatienter «Schmitt J, Ford DE. Psoriasis is independently ass...»85, «Kurd SK, Troxel AB, Crits-Christoph P ym. The risk...»86. Depressionssymtom är också vanligare hos patienter med psoriasisartrit med nagelförändringar, som har en betydande försämring av funktionsförmågan (HAQ > 0,5) och vars halt av IL-6 i serum är förhöjd «De Lorenzis E, Natalello G, Bruno D ym. Psoriatic ...»87. Den systemiska inflammationen kan stå i samband med reglering av sinnesstämningen hos patienter med psoriasisartrit.
- Associerade sjukdomar förekommer också hos barn med psoriasis. De vanligaste är uveit, förhöjt blodtryck, fetma, hyperlipidemi och depression «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13, «Augustin M, Radtke MA, Glaeske G ym. Epidemiology ...»88.
- Associerade sjukdomar ska uppföljas och beaktas vid den övergripande vården av patienten. Patienten uppmuntras till sunda levnadsvanor: normalvikt, regelbunden motion, rökfrihet och alkoholkonsumtion som får högst vara måttlig.
- Arbetsgruppen rekommenderar att helhetsrisken för hjärt- och kärlsjukdomar hos patienter med hudpsoriasis eller psoriasisartrit bedöms regelbundet, se God medicinsk praxis-rekommendationerna Dyslipidemier «Dyslipidemier»3, Högt blodtryck «Högt blodtryck»4, Typ 2-diabetes «Typ 2-diabetes»5 och Fetma (barn, unga och vuxna) «Fetma (barn, unga och vuxna)»6.
Målsättningarna för behandlingen av hudpsoriasis och psoriasisartrit
- Målet med behandlingen är att minimera patientens symtom, förbättra livskvaliteten
och bevara arbets- och funktionsförmågan. Sjukdomen kan inte botas.
- Vid psoriasisartrit eftersträvar man att släcka inflammationsreaktionen och förhindra strukturella skador.
- Behandlingen väljs alltid individuellt.
- Det är bra att förklara för patienten vad som kan uppnås med varje behandling.
- En del patienter har nytta av multiprofessionell vård.
- Valet av behandlingsform påverkas av
- eksemets svårighetsgrad och psoriasisartritens aktivitet och uttrycksformer (se punkterna Hudpsoriasis svårighetsgrad, Bedömning av aktivitet vid psoriasisartrit och Tabell «Psoriasisartritfenotyper...»15. Psoriasisfenotyper)
- patientens möjlighet och förmåga att förbinda sig till behandlingen
- patientspecifika kontraindikationer
- patientens erfarenheter av tidigare behandlingar
- patientens övriga sjukdomar.
- Tillräcklig information om sjukdomen och dess behandlingar samt effekterna av behandlingarna
och det praktiska genomförandet torde öka patientens förmåga att anpassa sig till
sin sjukdom.
- Mer information om sjukdomen finns i Ihotautitalo «https://www.terveyskyla.fi/ihotautitalo/ihotaudit/psoriaasi»4 och Reumatalo «https://www.terveyskyla.fi/reumatalo/tietoa/selk%C3%A4rankareumat/nivelpsoriaasi»5.
- Skriftliga patientanvisningar finns under Terveyskirjasto «http://www.terveyskirjasto.fi/»6 och på Psoriasisförbundets webbplats «http://www.psoriasisliitto.fi»7.
- Information om anpassningsträningskurser finns på Psoriasisförbundets webbplats «http://www.psoriasisliitto.fi»7.
Hudpsoriasis
Diagnos
- Diagnosen ställs utifrån den kliniska bilden.
- En hudbiopsi kan ibland vara till nytta ur differentialdiagnostisk synpunkt.
- Hudbiopsin tas i mitten av en obehandlad fläck (se artikel i Lääkärin käsikirja: Ihokoepalan oton aiheet ja tekniikka «Ihokoepalan oton aiheet ja tekniikka»1 (kräver åtkomsträtt)).
Sjukdomsbild och differentialdiagnostik
- Sjukdomsbilden för hudpsoriasis och differentialdiagnostiken beskrivs i tabell «Sjukdomsbild, differentialdiagnostik och behandling av hudpsoriasis...»2.
- Psoriasis förekommer i alla hudområden och i naglarna.
- Eksemets omfattning varierar från några små fläckar till utslag som täcker så gott som hela huden.
- Psoriasis kan vara förknippat med klåda och ömhet i huden.
- Typiskt för eksemet är växlingar mellan lugna och symtomatiska perioder.
- Psoriasis kan uppkomma på skadade hudområden (Köbners fenomen).
Svårighetsgrad
- Vid bedömning av svårighetsgraden ska bland annat följande faktorer beaktas:
- omfattningen och intensiteten av hudsymtom som kan konstateras objektivt
- intensiteten hos subjektiva symtom såsom klåda och smärta
- sjukdomens inverkan på patientens liv och livskvalitet «Finlay AY, Coles EC. The effect of severe psoriasi...»89, «Rapp SR, Feldman SR, Exum ML ym. Psoriasis causes ...»90
- effekten av tidigare behandlingar
- ledsymtom.
- Vanliga indikatorer på objektiva hudsymtom som endast lämpar sig för mätning av plackpsoriasis
är bland annat
- andelen av psoriasisförändringar i procent av hudytan (body surface area, BSA)
- Som hjälpmedel kan man använda närmevärdet 1 % = ytan på handavtrycket (handflatan och fingrarna) «Burden AD, Hilton Boon M, Leman J ym. Diagnosis an...»91, «Ahlehoff O, Gislason GH, Charlot M ym. Psoriasis i...»92, «Gelfand JM, Troxel AB, Lewis JD ym. The risk of mo...»93, «Daudén E, Puig L, Ferrándiz C ym. Consensus docume...»94.
- PASI (psoriasis area and severity index).
- På huvudet, kroppen och de övre och nedre extremiteterna bedöms den procentuella andelen av utslag samt psoriasisfläckarnas rodnad, tjocklek och fjällning. Värdena placeras i kalkyltabellen som ger ett siffervärde mellan 0 och 72 (PASI-räknaren «gvr00091a.xls»2).
- andelen av psoriasisförändringar i procent av hudytan (body surface area, BSA)
- Som mätare för livskvaliteten i association med psoriasis och andra hudsjukdomar har man mest använt en enkät med tio frågor som heter Dermatology Life Quality Index (DLQI) och som ger ett talvärde på skalan 0–30 (anvisningar om enkäten «hoi50062b.pdf»1, finska enkäten «http://sites.cardiff.ac.uk/dermatology/files/2014/04/DLQI-Finnish.pdf»3).
- Hudpsoriasis indelas numera i två grupper enligt svårighetsgrad på basis av flera
rekommendationer «Strober B, Ryan C, van de Kerkhof P ym. Recategori...»95, läkemedelsersättningskriterier och de flesta befolkningsbaserade epidemiologiska
undersökningarna:
- lindrig psoriasis
- Hudpsoriasis anses vara lindrig när den är begränsad och kan kontrolleras enbart med lokala behandlingar.
- svår psoriasis
- Hudpsoriasis anses vara svår när eksemets procentuella andel av hela huden (BSA) är över 10 % eller PASI är över 10 eller DLQI över 10.
- Även psoriasis med begränsad yta (eller PASI under 10) anses vara svår om den ger kraftiga symtom eller varblåsor på särskilda områden, till exempel handflatorna, fotsulorna, ansiktet eller genitalierna.
- Psoriasisen kan inte kontrolleras med lokala behandlingar.
- lindrig psoriasis
Behandling
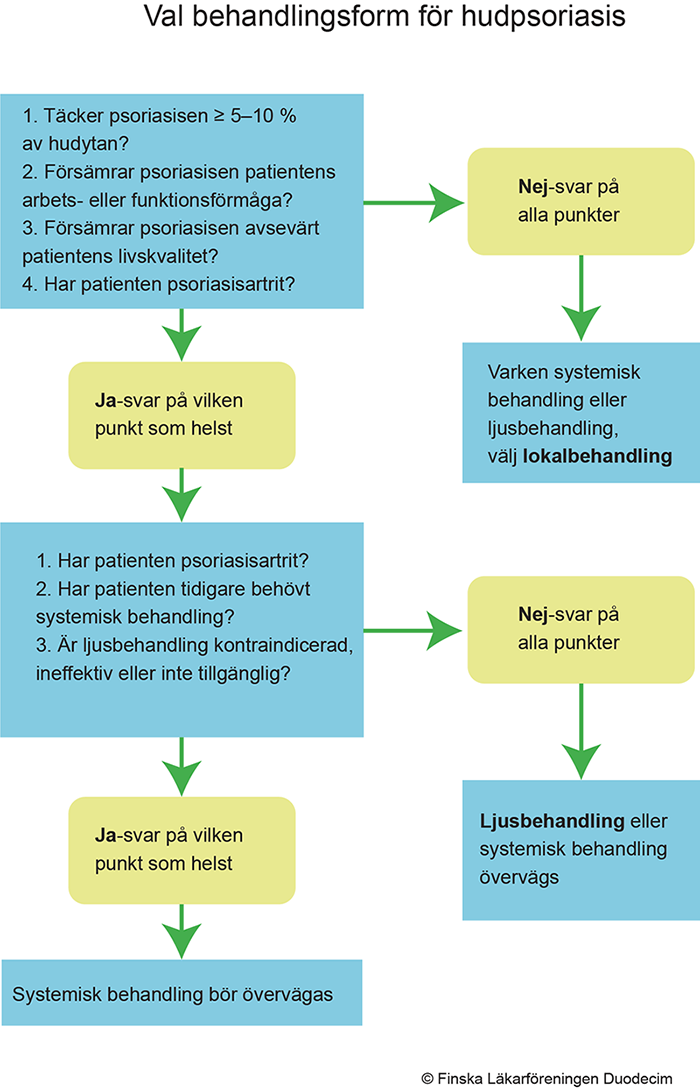
- Se behandlingsalgoritmen (diagrammet «Val av behandlingsform för hudpsoriasis»2) och tabell «Sjukdomsbild, differentialdiagnostik och behandling av hudpsoriasis...»2.
- Begränsad hudpsoriasis behöver inte behandlas om den inte stör patienten.
| Huvudtyper | Differentialdiagnostik | Behandling |
|---|---|---|
| Droppformad psoriasis (psoriasis guttata) | ||
Bilderna «Pisarapsoriaasi eli psoriasis guttata»3, «Pisarapsoriaasi eli psoriasis guttata»4, «Pisarapsoriaasi eli psoriasis guttata»5, «Pisarapsoriaasi eli psoriasis guttata»6 och «Pisarapsoriaasi eli psoriasis guttata»7
|
Bildkollage för differentialdiagnostik vid misstanke om droppformad psoriasis «Esimerkkejä pisarapsoriaasin erotusdiagnostiikasta huomioitavista ihottumista»8
|
|
| Plackpsoriasis (psoriasis vulgaris) | ||
Bilderna «Läiskäpsoriaasi eli psoriasis vulgaris»9, «Läiskäpsoriaasi eli psoriasis vulgaris»10, «Läiskäpsoriaasi eli psoriasis vulgaris»11, «Läiskäpsoriaasi eli psoriasis vulgaris»12, «Läiskäpsoriaasi eli psoriasis vulgaris»13, «Läiskäpsoriaasi eli psoriasis vulgaris»14, «Läiskäpsoriaasi eli psoriasis vulgaris»15och «Läiskäpsoriaasi eli psoriasis vulgaris»16
|
Bildkollage för differentialdiagnostik vid misstanke om plackpsoriasis «Läiskäpsoriaasin erotusdiagnostiikassa huomioitavia ihottumia»17
|
Lindrig:
Svår:
|
| Psoriasis i särskilda kroppsområden | ||
| Psoriasis i hudveck (psoriasis inversa, bilderna «Taivepsoriaasi eli psoriasis in versa»18 och «Taivepsoriaasi kainalossa eli psoriasis in versa»19) | Bildkollage för differentialdiagnostik vid misstanke om psoriasis i hudveck «Taivepsoriaasin erotusdiagnostiikassa huomioitavia ihottumia»20
|
|
| Psoriasis i hårbottnen (psoriasis capitis, bilderna «Päänahan psoriaasi»21, «Päänahan psoriaasi»22, «Päänahan psoriaasi»23, «Päänahan psoriaasi»24, «Päänahan psoriaasi»25) | Bildkollage för differentialdiagnostik vid misstanke om psoriasis i hårbottnen «Päänahan psoriaasin erotusdiagnostiikassa huomioitavia ihottumia»26
|
|
| Ansiktspsoriasis (bild «Otsan psoriaasi»27) | Bildkollage för differentialdiagnostik vid misstanke om ansiktspsoriasis «Kasvopsoriaasin erotusdiagnostiikassa huomioitavia ihottumia»28
|
|
| Psoriasis på handflator och fotsulor (bilderna «Jalkapohjien psoriaasi»29, «Jalkapohjien psoriaasi»30, «Jalkapohjien psoriaasi»31, «Kämmenten psoriaasi»32, «Kämmenten psoriaasi»33, «Kämmenten psoriaasi»34, «Kämmenten psoriaasi»35, «Kämmenten psoriaasi»36) | Bildkollage för differentialdiagnostik vid misstanke om hand- och fotpsoriasis «Kämmen- ja jalkapohjapsoriaasin erotusdiagnostiikassa huomioitavia ihottumia»37
|
|
| Psoriasis på könsorganen (bild «Genitaalialueen psoriaasi»38) | Differentialdiagnostik:
|
|
| Psoriasis med varblåsa (psoriasis pustulosa) | ||
Generaliserad form
|
|
|
lokal form
|
|
|
| Psoriasis över hela huden (psoriasis erythrodermica) | ||
Bild «Erytroderminen psoriaasi»40
|
|
|
| Nagelförändringar vid psoriasis | ||
| Bilderna «Psoriaasin kynsimuutoksia»41, «Psoriaasin kynsimuutoksia»42, «Psoriaasin kynsimuutoksia»43, «Psoriaasin kynsimuutoksia»44 |
Bildkollage för differentialdiagnostik av nagelpsoriasis «Kynsipsoriaasin erotusdiagnostiikassa huomioitavia kynsimuutoksia»45 |
|
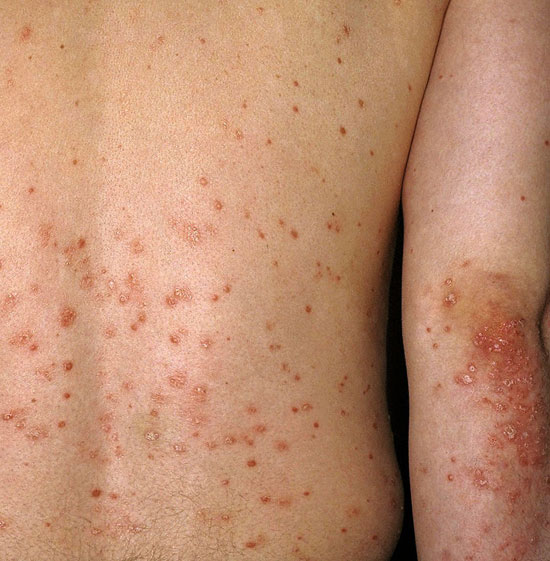
Pisarapsoriaasi eli psoriasis guttata.
© Raimo Suhonen
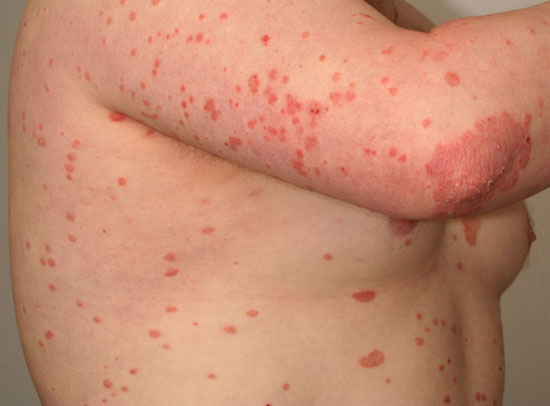
Pisarapsoriaasi eli psoriasis guttata
© Raimo Suhonen
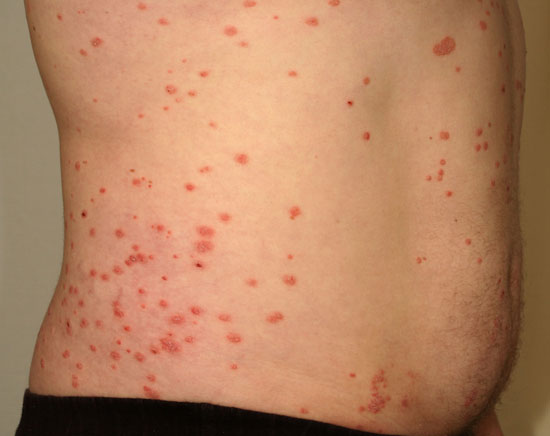
Pisarapsoriaasi eli psoriasis guttata
© Raimo Suhonen
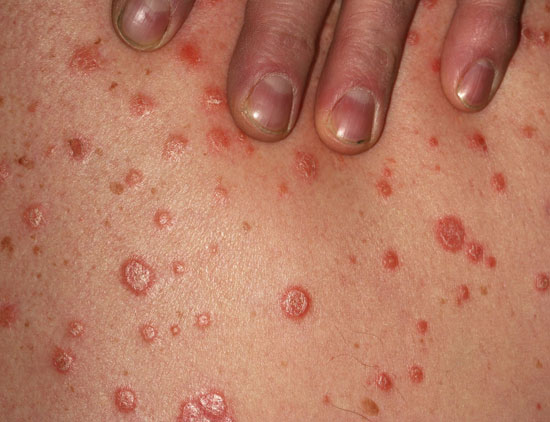
Pisarapsoriaasi eli psoriasis guttata
© Raimo Suhonen
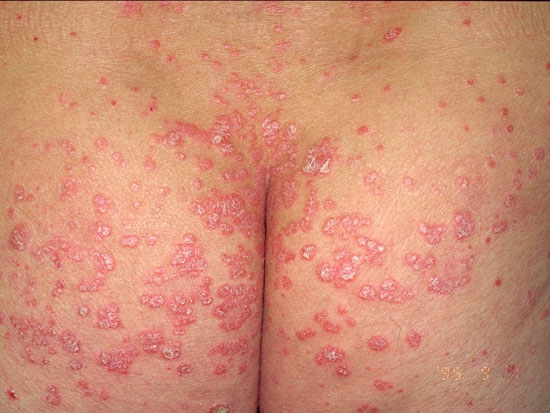
Pisarapsoriaasi eli psoriasis guttata
© Raimo Suhonen
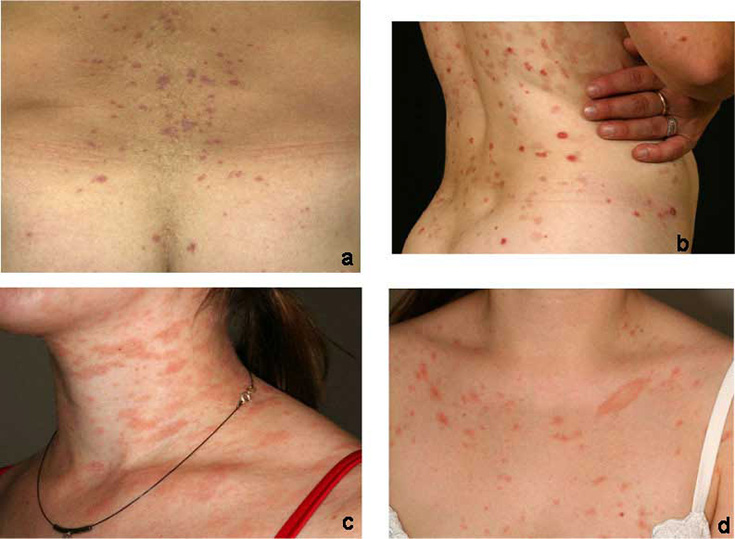
Esimerkkejä pisarapsoriaasin erotusdiagnostiikasta huomioitavista ihottumista: a= lichen planus eli punajäkälä (a), pityriasis lichenoides chronica (b), pityriasis rosea (c) ja pityriasis rosea (d).
© Raimo Suhonen
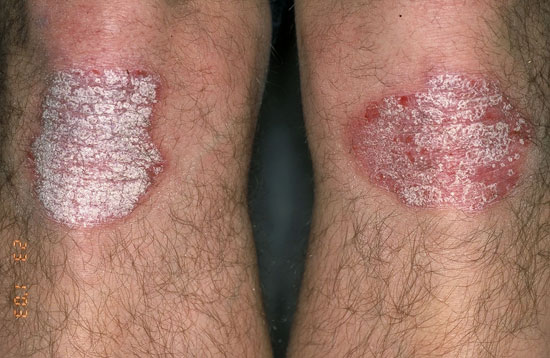
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
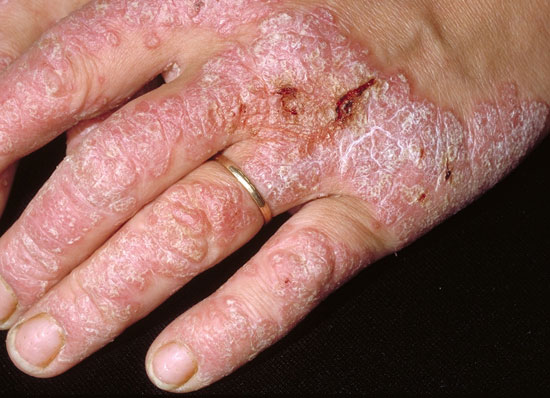
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
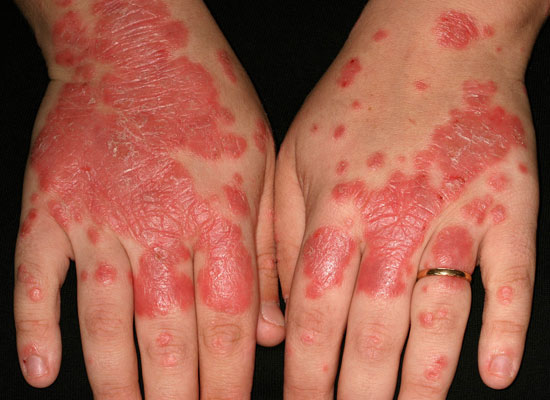
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
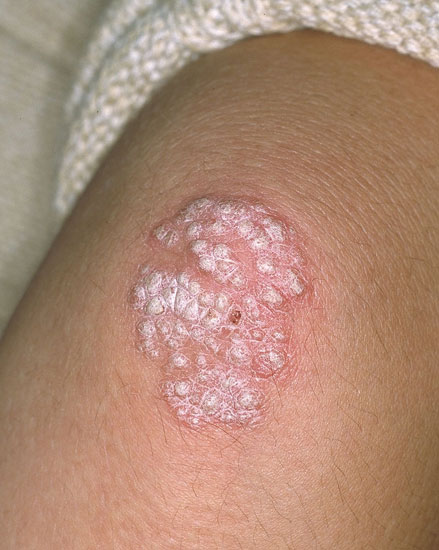
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
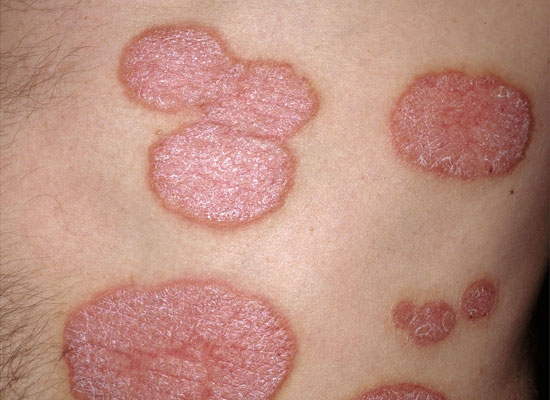
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
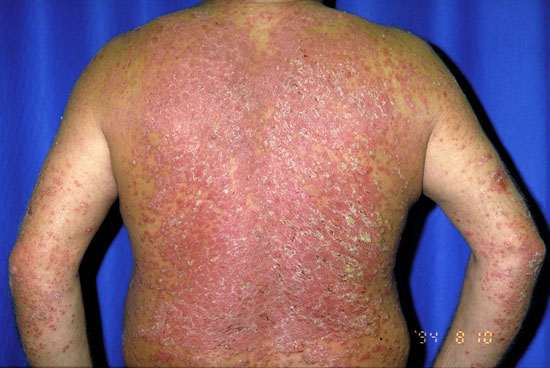
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
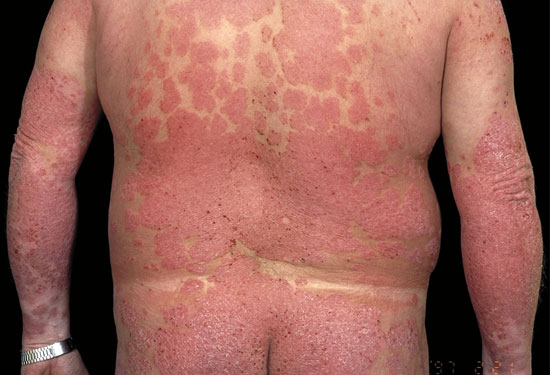
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
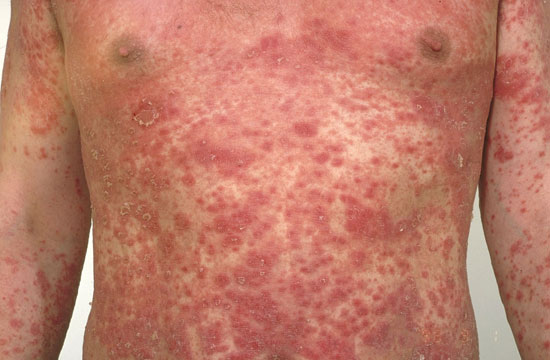
Laaja-alainen, lähes erytroderminen läiskäpsoriaasi, jossa myös pustulaarisen psoriaasin piirteitä.
© Raimo Suhonen
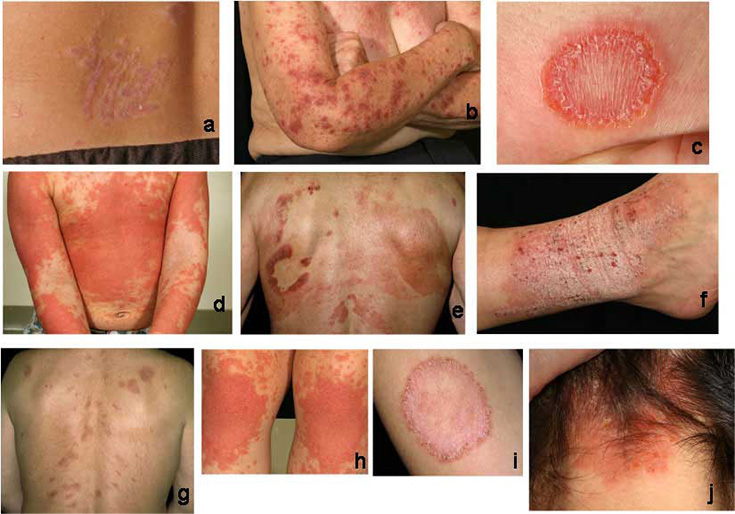
Läiskäpsoriaasin erotusdiagnostiikassa huomioitavia ihottumia: läiskäekseema (eczema nummulare) (b, c), neurodermatiitti (f, j), silsa (tinea) (i), punajäkälä (lichen planus) (a, g), ihon T-solulymfooma (Mycosis fungoides) (e), pityriasis rubra pilaris (d, h).
© Raimo Suhonen
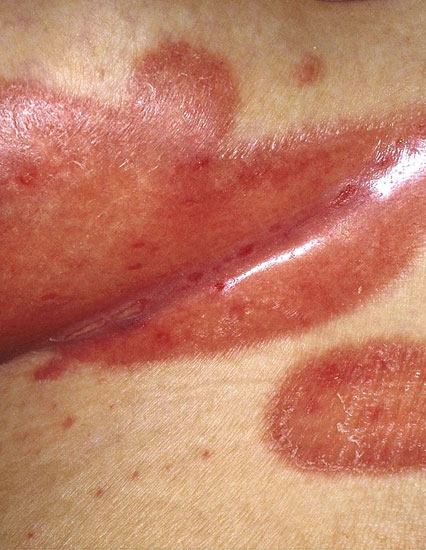
Taivepsoriaasi eli psoriasis in versa
© Raimo Suhonen
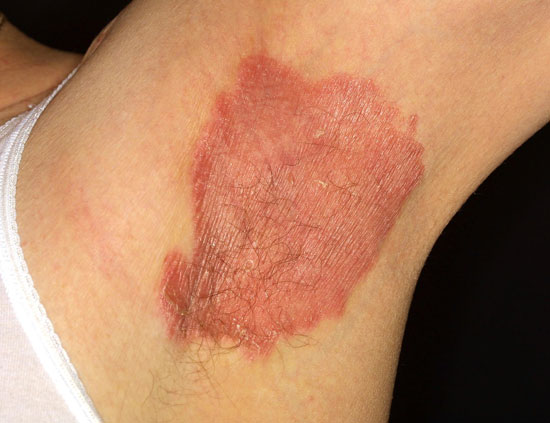
Taivepsoriaasi kainalossa eli psoriasis in versa
© Raimo Suhonen
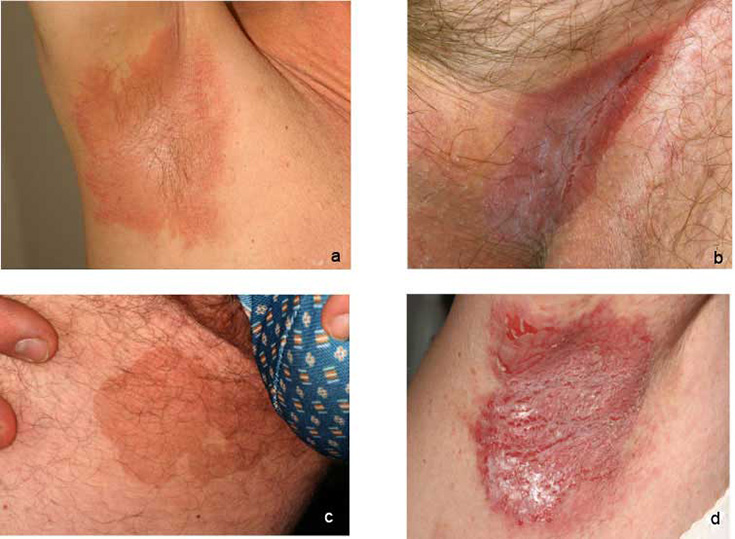
Taivepsoriaasin erotusdiagnostiikassa huomioitavia ihottumia ovat mm. hiivan aiheuttama intertrigo, seborroinen ekseema (a, b), bakteeri-infektion aiheuttama taivealueiden ihottuma (erytrasma) (c) ja Mb Hailey-Hailey (Benign chronic familial pemphigus) (d).
© Raimo Suhonen
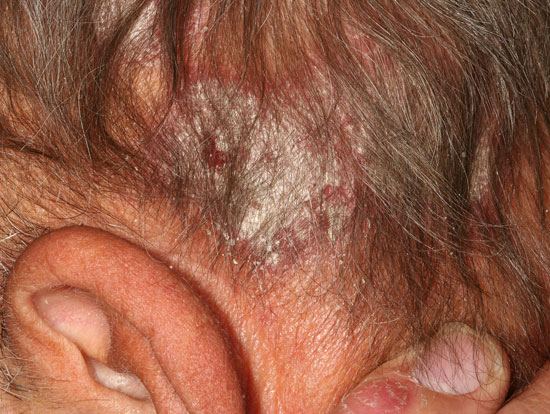
Päänahan psoriaasi
©: Raimo Suhonen

Päänahan psoriaasi
© Raimo Suhonen
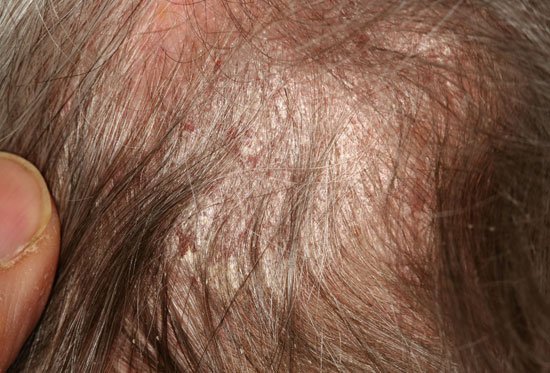
Päänahan psoriaasi
© Raimo Suhonen
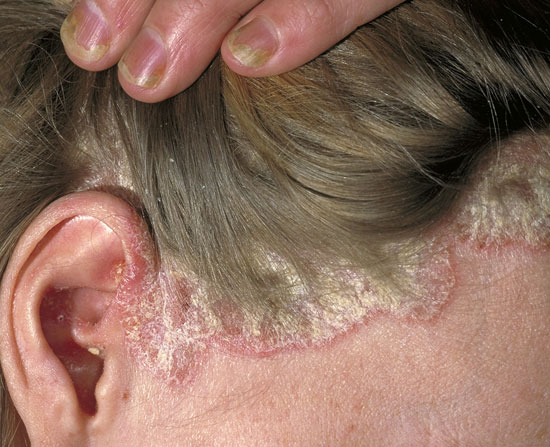
Päänahan psoriaasi
© Raimo Suhonen
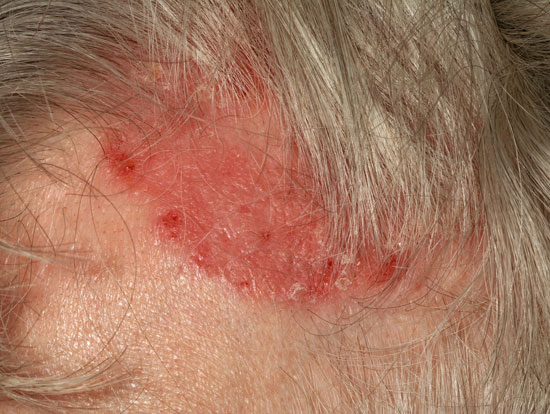
Päänahan psoriaasi
© Raimo Suhonen
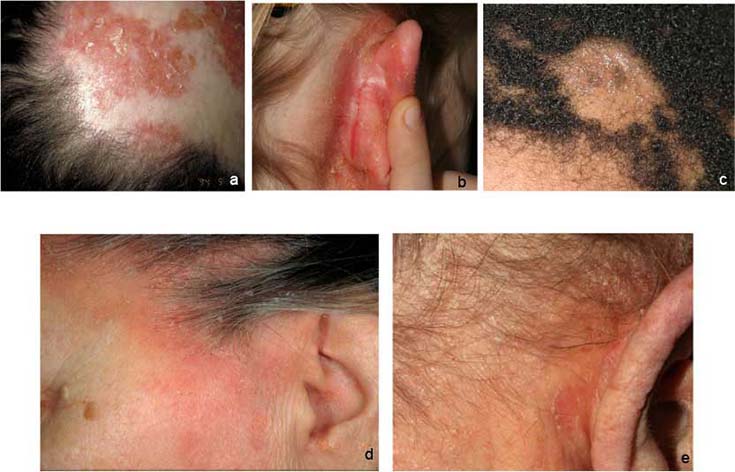
Päänahan psoriaasin erotusdiagnostiikassa huomioitavia ihottumia ovat mm. seborroinen ekseema (b, d, e), silsa (tinea) (c) ja punahukka (DLE) (a).
© Raimo Suhonen
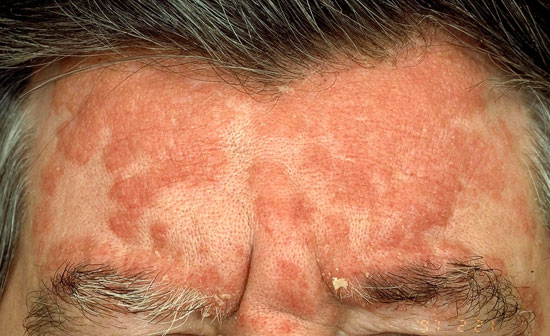
Otsan psoriaasi
© Raimo Suhonen
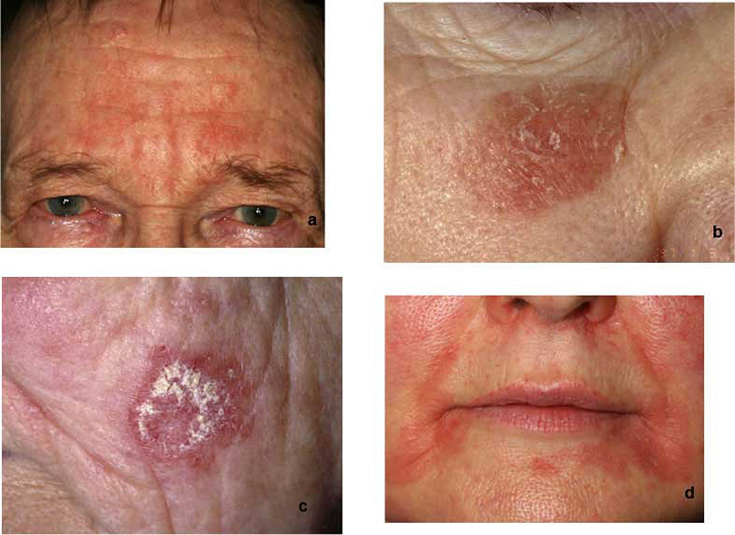
Kasvopsoriaasin erotusdiagnostiikassa huomioitavia ihottumia ovat esim. taliköhnä (seborroinen ekseema) (a, d), punahukka (DLE) (c) ja joskus myös aktiini keratoosi (b).
© Raimo Suhonen
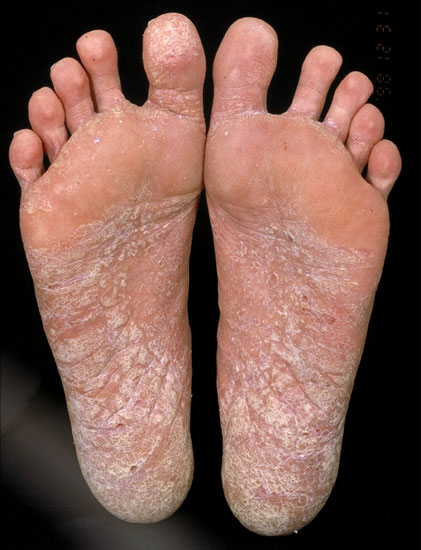
Jalkapohjien psoriaasi
© Raimo Suhonen
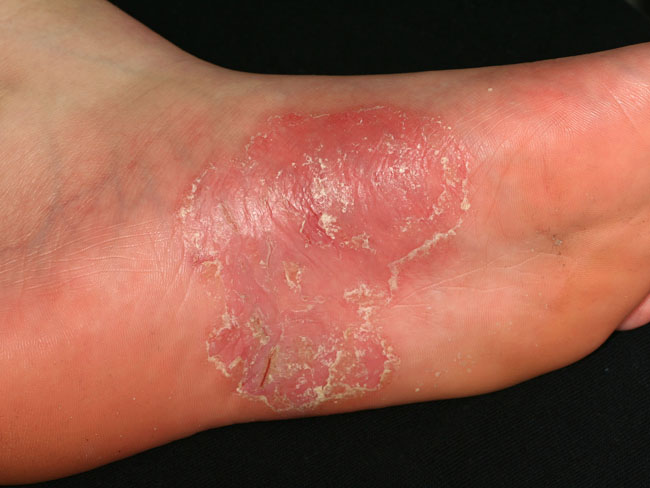
Jalkapohjien psoriaasi
© Raimo Suhonen
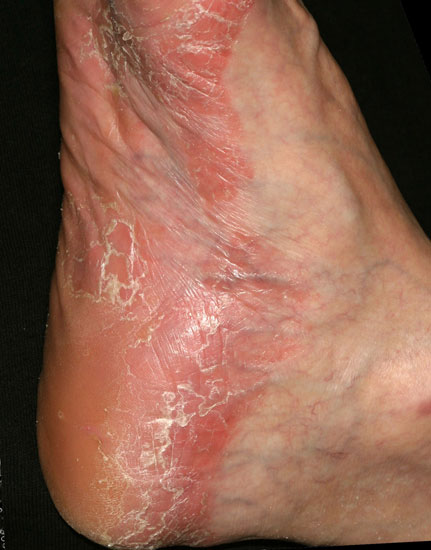
Jalkapohjien psoriaasi
© Raimo Suhonen
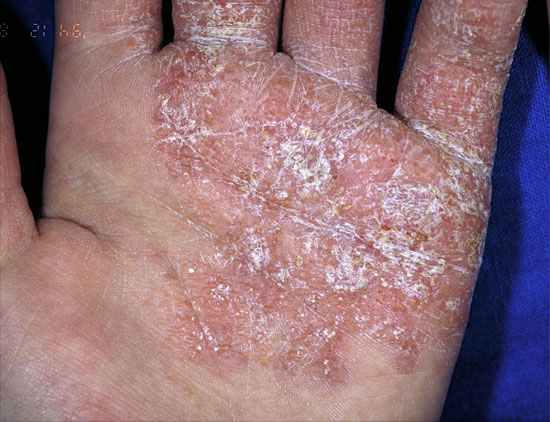
Kämmenten psoriaasi
© Raimo Suhonen
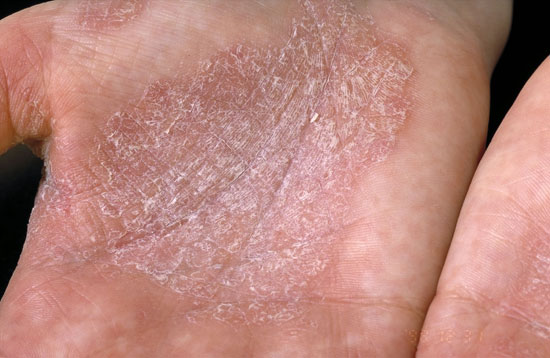
Kämmenten psoriaasi
© Raimo Suhonen
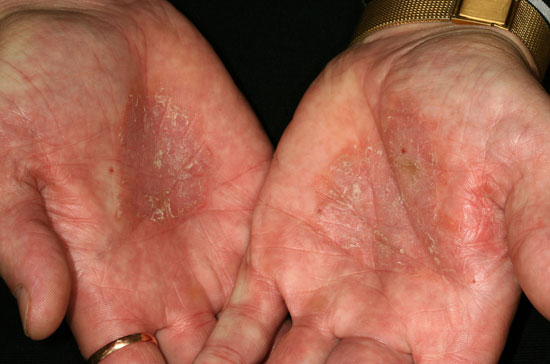
Kämmenten psoriaasi
© Raimo Suhonen
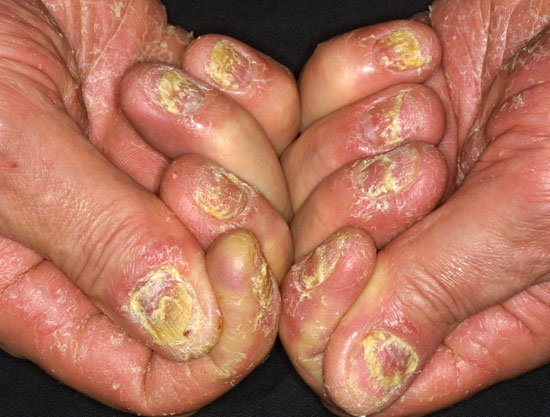
Kämmenten psoriaasi
© Raimo Suhonen
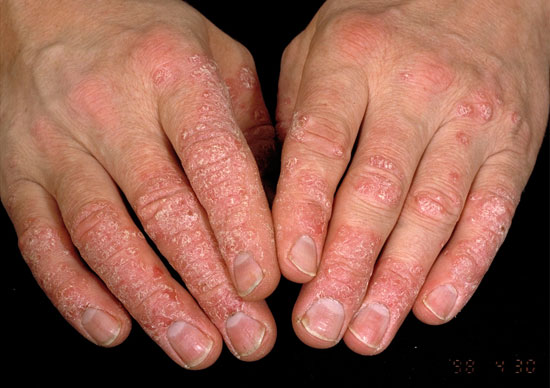
Kämmenten psoriaasi
© Raimo Suhonen
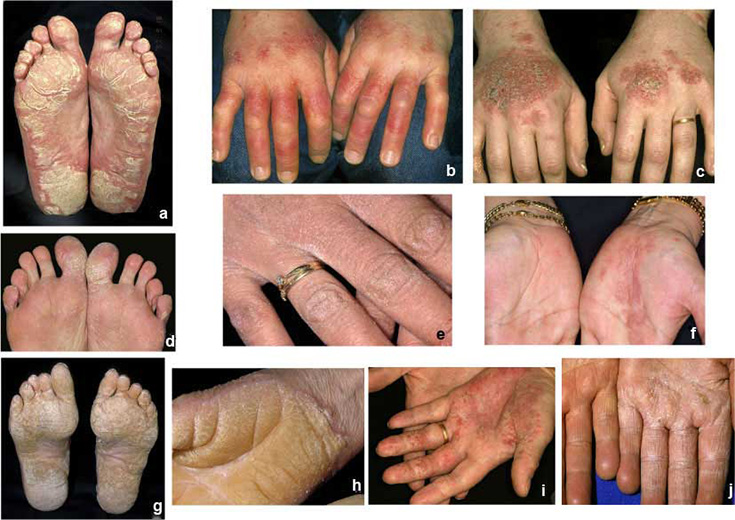
Kämmen- ja jalkapohjapsoriaasin erotusdiagnostiikassa huomioitavia ihottumia ovat muun muassa ekseemat, kuten atoopikon krooninen käsi- ja jalkaihottuma (kuva a), läiskäekseema (kuvat c ja i) tai toksinen ekseema (kuva e), silsa (tinea) (kuvat d ja j), hyperkeratoosit (keratodermat) (kuvat g ja h), punajäkälä (lichen planus) (kuva f) tai kosketusallergiat (kuva b).
© Raimo Suhonen
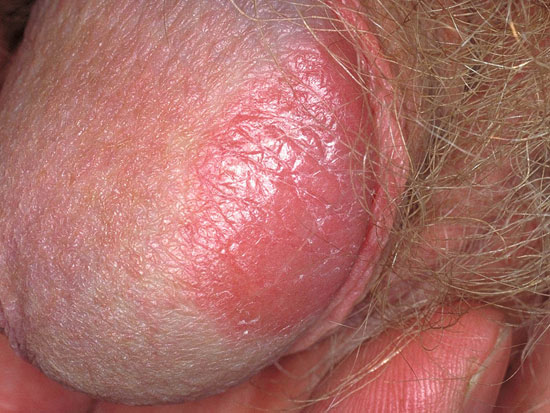
Genitaalialueen psoriaasi
© Raimo Suhonen
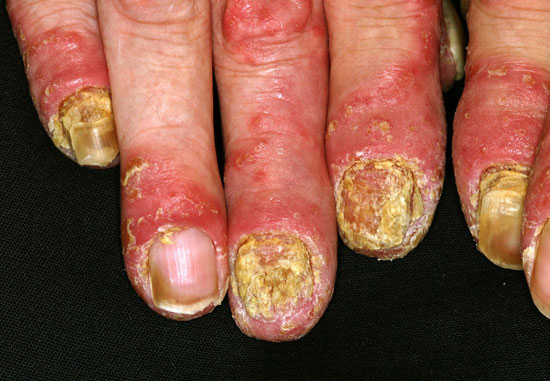
Sormien pustuloiva psoriaasi eli Acrodermatitis continua Hallopeau
© Raimo Suhonen
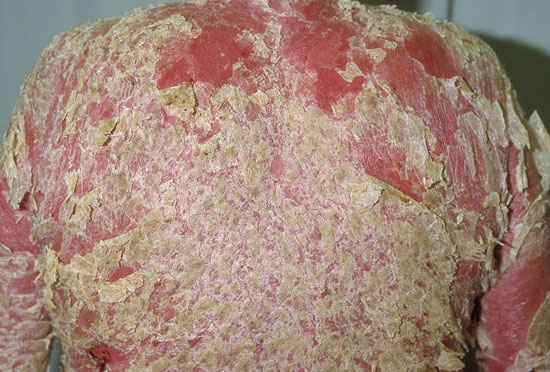
Erytroderminen psoriaasi
©: Raimo Suhonen
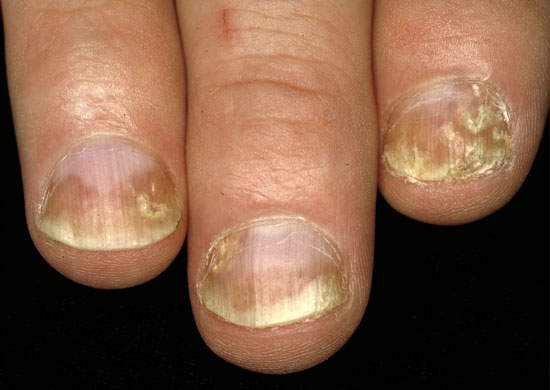
Psoriaasin kynsimuutoksia
© Raimo Suhonen
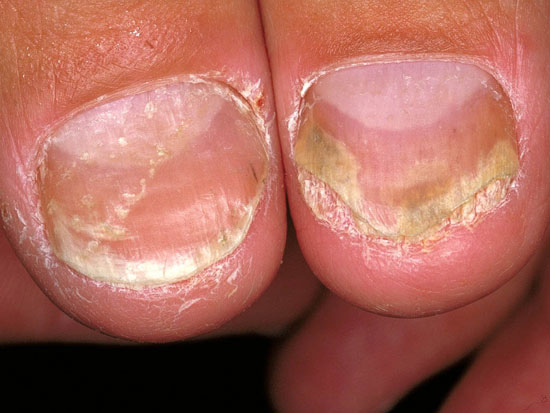
Psoriaasin kynsimuutoksia
© Raimo Suhonen
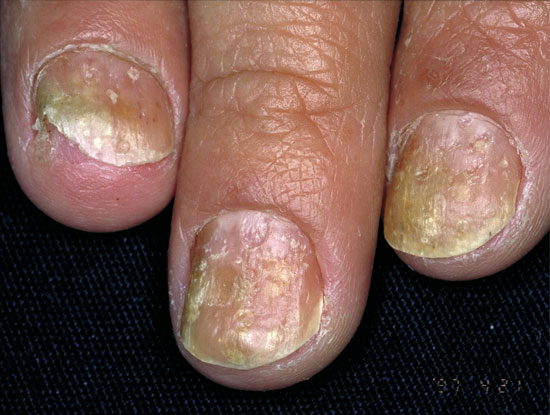
Psoriaasin kynsimuutoksia
© Raimo Suhonen
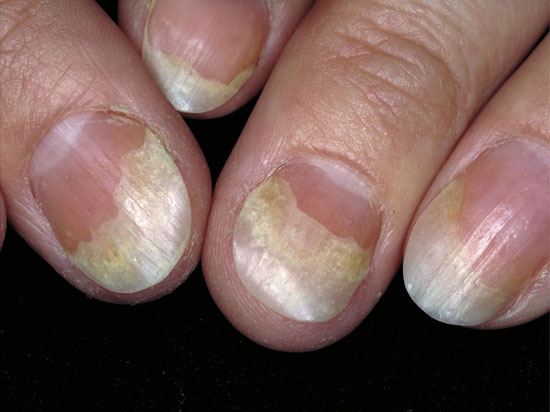
Psoriaasin kynsimuutoksia
© Raimo Suhonen
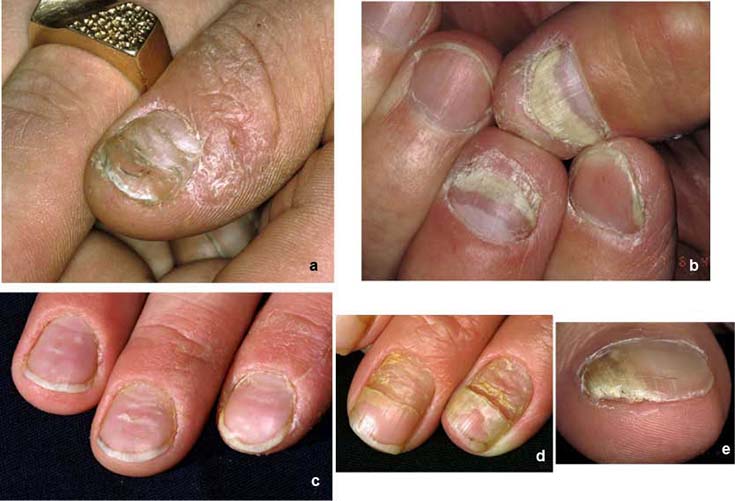
Kynsipsoriaasin erotusdiagnostiikassa huomioitavia kynsimuutoksia ovat mm. käsiekseemojen aiheuttamat kynsimuutokset (a, c, d) ja kynsisilsa (tinea) (b, e).
© Raimo Suhonen
Lokalbehandling
- För majoriteten av patienterna räcker det med lokalbehandling.
- Vid omfattande psoriasis används dessutom lokalbehandling som stöd för andra behandlingar.
- Mängden läkemedelssalva som behövs beror på storleken av hudområdet som behandlas «Lääkevoiteiden kulutus ihotautien hoidossa»2.
Bassalva
- Regelbunden användning av bassalva på ren hud lindrar torr hud, klåda och fjällande, men avlägsnar knappast ensamt eksem «Lodén M. Role of topical emollients and moisturize...»96.
Salva med salicylsyra
- Salva med salicylsyra används för att hudpeeling vid psoriasis med tjocka fjäll «Salisyylihappopitoinen voide psoriaasi-ihottuman hilseen pehmittämiseksi»3.
- Tjocka lager fjäll förhindrar absorptionen av läkemedelssalvor och bromsar upp effekten av ljusbehandling.
- Salvan kan irritera framför allt frisk hud.
- Salvan absorberas genom huden.
- Salvan lämpar sig inte för behandling av omfattande psoriasis (över 20 % av hudytan) «Lebwohl M. The role of salicylic acid in the treat...»97.
- Använd inte salvan omedelbart före ljusbehandling «Fetil E, Ozka S, Soyal MC ym. Effects of topical p...»98, «Lebwohl M, Martinez J, Weber P ym. Effects of topi...»99.
- Salva med salicylsyra absorberar UV-strålar.
Kortikosteroidsalvor
- Kortikosteroidsalvor lämpar sig för behandling av de flesta typer av psoriasis, men bör inte användas som huvudsaklig behandling för patienter med psoriasis som täcker mer än 10 % av hudytan.
- Effekten är antiinflammatorisk «Surber C, Itin PH, Bircher AJ ym. Topical corticos...»100.
- Preparat och salvbas väljs enligt typ av psoriasis och hudområde:
- preparat klass I–II i områden med tunna hudveck och i ansiktet
- preparat klass III–IV för tjocka plackliknande fläckar «Mason J, Mason AR, Cork MJ. Topical preparations f...»101.
- Salvorna doseras 1–2 gånger per dygn, förutom preparat klass IV som doseras endast
en gång per dygn.
- Maximal dos är 30–50 g i veckan.
- Behandlingstid:
- I områden med tunn hud (ansikte, hudveck) är behandlingstiden 1–2 veckor utan avbrott.
- I områden med tjockare hud (bålen, extremiteternas sträcksidor, handflator, fotsulor) är behandlingstiden 3–4 veckor.
- Särskilt kortikosteroider i grupp IV avslutas gradvis.
- Behandlingen kan ges som kurer eller som underhållsbehandling 2 dagar i veckan.
- I tunna hudområden går man snabbt över till kortikosteroidfria behandlingsalternativ. Se Skötsel av särskilda hudområden
- Kortikosteroidsalvor lämpar sig inte för långvarig daglig användning «Kortikosteroidivoiteet psoriaasin hoidossa»4.
- Behandling med kortikosteroidsalva kan ge irreversibel hudatrofi som biverkning.
- Halveringstiden för hudens kollagen är lång, och därför uppkommer hudatrofi med fördröjning.
- Även en kort behandling med kortikosteroidsalvor minskar kollagenproduktionen i huden i upp till flera veckor. Det finns inte tillförlitlig information om hur länge det tar för kollagensyntesen att återhämta sig «Haapasaari KM, Risteli J, Oikarinen A. Recovery of...»102, «Murdoch D, Clissold SP. Calcipotriol. A review of ...»103.
- Behandling med kortikosteroidsalva kan ge irreversibel hudatrofi som biverkning.
- Kortikosteroidsalvor kan orsaka binjuresuppression. Denna risk bör beaktas särskilt vid behandling av omfattande eksem, ålderstigna patienter, barn eller vid användning av starka eller extra starka kortikosteroidsalvor.
- Den symtomfria tiden efter användning av kortikosteoridsalva varar ofta bara i några veckor.
D-vitaminderivat (kalcipotriol och kalcitriol)
- D-vitaminderivat minskar aktiveringen av interleukin 36 och transkriptionsfaktor NF-κB och främjar celldifferentiering och apoptos i hudens skivepitelcellslager «Murdoch D, Clissold SP. Calcipotriol. A review of ...»103, «Liu X, Liu Y, Xu M ym. Zinc finger protein A20 is ...»104, «Germán B, Wei R, Hener P ym. Disrupting the IL-36 ...»105.
- Den bästa sättet att behandla är genom att dosera D-vitaminderivatpreparaten två gånger
om dagen tills psoriasisfläckarna läkts.
- Det kan ta upp till 6 veckor innan behandlingsresultatet är gott.
- Det finns inga tillförlitliga forskningsresultat gällande behandlingsresultatets varaktighet.
- D-vitaminderivat lämpar sig för långtidsanvändning «Barnes L, Altmeyer P, Fôrstrôm L ym. Long-term tre...»106, «Ramsay CA, Berth-Jones J, Brundin G ym. Long-term ...»107.
- Lokal hudirritation är den vanligaste biverkningen och kan begränsa användningen av D-vitaminderivat i känsliga hudområden (veck och ansikte) «Bruner CR, Feldman SR, Ventrapragada M ym. A syste...»108, «Carboni I, de Felice C, Bergamin A ym. Topical use...»109, «Ortonne JP, Humbert P, Nicolas JF ym. Intra-indivi...»110.
- För hög dos kan orsaka hyperkalcemi.
- Vid användning av doser enligt anvisning (kalcipotriol högst 100 g i veckan och kalcitriol 30 g/dygn) är inga störningar i kalciumomsättningen att förväntas «Bourke JF, Iqbal SJ, Hutchinson PE. Vitamin D anal...»111.
- Den rekommenderade dosen ska inte överskridas utan noggrann uppföljning av laboratorievärden (fP-Pi, P-Ca, dU-Ca, P-AFOS) «Berth-Jones J, Bourke JF, Iqbal SJ ym. Urine calci...»112.
Kombination av kortikosteroid och kalcipotriol
- Kombinationen är effektivare än kalcipotriol eller betametasondipropionat i monoterapi
«Kalsipotrioli-beetametasonidipropionaattiyhdistelmävoide on kuukauden hoitokuurina tehokkaampi kuin vaikuttavat aineet käytettynä erikseen.»A.
- Kombinationen finns i gel-, skum- och krämform, varav skummet är effektivast «Koo J, Tyring S, Werschler WP ym. Superior efficac...»113, «Paul C, Stein Gold L, Cambazard F ym. Calcipotriol...»114.
- Doseringen är en gång per dygn, högst 15 g per gång.
- Efter 4 veckors användning övergår man stegvis till lokalbehandling utan kortikosteroidsalva eller till underhållsbehandling 1–2 dagar i veckan.
- Kombinationspreparat med kalcipotriol och betametasondipropionat innehåller en stark
kortikosteroid.
- På grund av risken för hudatrofi gäller samma regler för användning av detta kombinationspreparat som för andra starka kortikosteroidsalvor «Kalsipotrioli-beetametasonidipropionaattivoiteen atrofogeeniset ominaisuudet vastannevat beetametasonidipropionaattia. Pitkäaikaiskäytön turvallisuutta ei ole pystytty osoittamaan.»C (se punkten Kortikosteroidsalvor).
Ditranol, d.v.s. antralin
- Numera används ditranol sällan på sjukhuspolikliniker eftersom substansen färgar av sig och fläckar.
- Ditranol kan vara lika effektivt som kalcipotriol för behandling av psoriasis «Ditranoli ja kalsipotrioli ovat todennäköisesti yhtä tehokkaita psoriaasin paikallishoitoja poliklinikan avohoito-osastolla käytettynä vähintään 12 viikon pituisessa hoidossa. Molemmat hoidot vaikuttavat positiivisesti psoriaatikon elämänlaatuun.»C, i synnerhet psoriasis med tjocka plack.
- För mer information se «Ditranoli psoriaasin hoidossa»5.
Behandling av psoriasis i särskilda hudområden
Behandling av psoriasis i hårbottnen
- Mot psoriasis i hårbottnen används periodvis preparat som innehåller antingen enbart kortikosteroid ur grupp III–IV eller kortikosteroid i kombination med salicylsyra eller kalcipotriol.
- För att lossa de tjocka fjällen i hårbottnen används 5–10-procentig salicylsyra i en vattenlöslig salvbas eller olja «Salisyylihappopitoinen voide psoriaasi-ihottuman hilseen pehmittämiseksi»3.
- Mjällschampo kan användas periodvis för att hålla Malassezia-svampen borta.
Lokalbehandling av psoriasis i andra särskilda hudområden
- Ansikte och hårfäste:
- lokalkortikosteroider grupp I–II i behandlingsperioder på 1–2 veckor
- kalcitriolsalva
- Hudirritation lindras genom att växla med kortikosteroider.
- lokala kalcineurinhämmare (takrolimus, pimekrolimus) verkar vara effektiva «Paikalliset kalsineuriinin estäjät näyttävät tehoavan kasvojen ja taivealueiden psoriaasiin.»B
- Behandling av psoriasis är dock inte en officiell indikation för kalcineurinhämmare.
- Vanliga biverkningar, särskilt i början av behandlingen, är irritation, hetta och klåda i det behandlade området.
- Kalcineurinhämmare verkar sakna effekt på plackpsoriasis på bålen «Zonneveld IM, Rubins A, Jablonska S ym. Topical ta...»115.
- Fjäll i örongångarna kan mjukas upp och avlägsnas med hudolja och öronspolning «Harth W, Caffier PP, Mayelzadeh B ym. Topical tacr...»116. Takrolimuskräm och kortikosteroidsalvor kan användas periodvis, men vetenskapliga prövningar saknas.
- Fjällfri psoriasis i hudveck och genitalområdena:
- Hudvecksområden går lätt sönder.
- En mild eller medelstark kortikosteroidsalva kan kombineras med ett antimikrobiellt ämne eller antimykotikum «Rikkipitoinen ex tempore -valmiste taivepsoriaasin hoitoon»6.
- Kalcineurinhämmare är effektiva för behandling av psoriasis i hudveck «Paikalliset kalsineuriinin estäjät näyttävät tehoavan kasvojen ja taivealueiden psoriaasiin.»B.
- Effektiv lokalbehandling av psoriasisförändringar i naglarna saknas «Crowley JJ, Weinberg JM, Wu JJ ym. Treatment of na...»117.
- Starka kortikosteroidsalvor kan testas vid begynnande onykolys och extrem förhorning av nagelbädden.
- Nagelförändringarna kan minska med systemiska läkemedelsbehandlingar «Gümüsel M, Özdemir M, Mevlitoglu I ym. Evaluation ...»118, «Jiaravuthisan MM, Sasseville D, Vender RB ym. Psor...»119, «Tosti A, Ricotti C, Romanelli P ym. Evaluation of ...»120. Enbart nagelförändringar behandlas med systemiska läkemedel dock endast i sällsynta specialfall (t.ex. för att upprätthålla arbetsförmågan).
- Det är också bra att utesluta nagelsvamp med svampodling.
- Patienten kan ha nytta av att behandling som ges av en hälso- och sjukvårdsutbildad fotvårdare eller fotterapeut.
UV-ljusbehandlingar
- Definitioner:
- Fototerapi: Ultravioletta strålar (UV-strålar) används som sådana (UVB-behandlingar och SUP-behandling).
- Fotokemoterapi (PUVA-behandlingar): Före behandlingen sensibiliseras patientens hud mot UVA-strålning med ett psoralenläkemedel systemiskt eller utvärtes.
- Indikationer:
- Indikationerna för UV-ljusbehandling är droppformad psoriasis och plackpsoriasis (bild «Esimerkkejä keskivaikeasta pisara- ja läiskäpsoriaasista»46).
- Kontraindikationer:
- Det finns inga absoluta kontraindikationer.
- Relativa kontraindikationer är
- pustulös och erytrodermisk psoriasis
- ljuskänslighet (ljuseksem, lupus erythematosus)
- tidigare hudcancer eller faktorer som ökar risken för hudcancer (bl.a. ciklosporin).
- Användningen begränsas av
- att behandlingen begränsar patientens rörlighet
- tillgång på vård och resandet till och från behandlingarna
- eventuellt förhöjd hudcancerrisk.
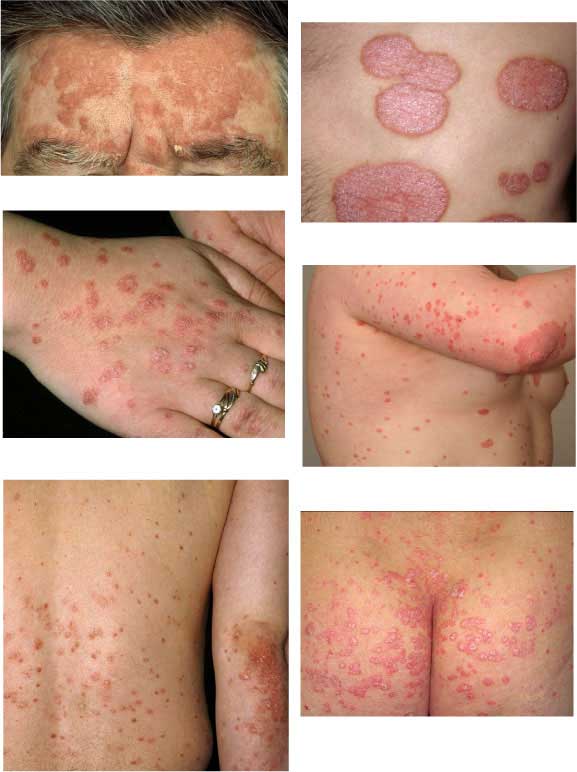
Esimerkkejä keskivaikeasta pisara- ja läiskäpsoriaasista. Näissä valohoidot ovat usein hyvä hoitovalinta.
© Raimo Suhonen
Ljusbehandlingsapparater och kvalitetshantering
- Apparaterna klassificeras enligt UV-spektrum i UVB-, UVA- och SUP-apparater (diagram «Eri valohoitolamppujen emittoiman UV-säteilyn aallonpituusspektrit»47)
- Inrättningarna som ger ljusbehandling ska följa myndigheternas anvisningar. Se Fimeas webbplats «http://www.fimea.fi/documents/160140/753095/19694_julkaisut_4_2005_UV_julkaisu_verkko_v2-rd.pdf.pdf»8. Valvira övervakar säkerheten vid användning av produkter och utrustning för hälso- och sjukvård.
- UV-ljusbehandlingar av hudsjukdomar kan endast administreras av yrkesutbildade personer
inom hälso- och sjukvården insatta i ljusbehandlingar.
- Det finns inga bestämmelser om egenvård.
- Patientens kumulativa UV-dos ska följas upp.
- Den kumulativa UV-dosen för varje vårdperiod antecknas i patientjournalen.
- Patientens kumulativa exposition för UV under hela hens liv antecknas indelat i PUVA-behandlingar, UVB-behandlingar och naturlig UV-exponering (klimatbehandlingar).
- Den rekommenderade maximigränsen för antalet årliga behandlingar är 2 perioder.
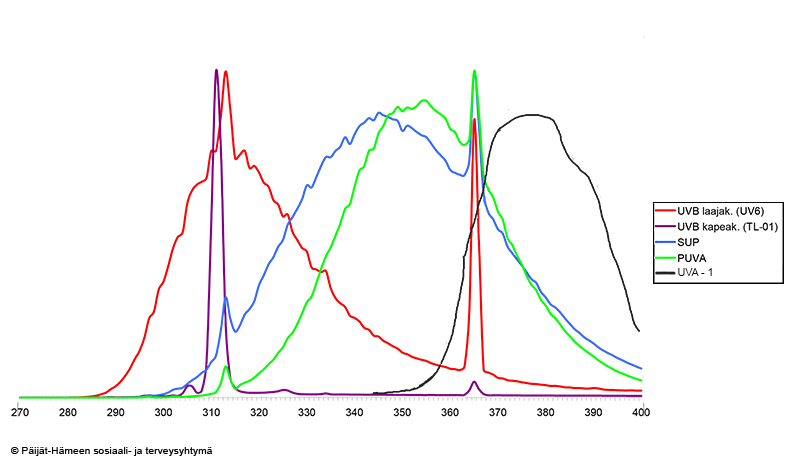
Eri valohoitolamppujen emittoiman UV-säteilyn aallonpituusspektrit
© Tapio Rantanen
UVB-behandlingar
- Smalbandig UVB-behandling (lysrörstyp TL/01, våglängdsområde 311 ± 2 nm):
- Primär UV-ljusbehandling för vuxna patienter:
- Svåra eksem blir symtomfria hos cirka 70 % av patienterna efter 20–30 behandlingar «Keskivaikea psoriaasi-ihottuma ilmeisesti paranee oireettomaksi kapeakaistaisella UVB-hoidolla noin 70 %:lla potilaista.»B.
- Det finns inga tillförlitliga jämförande undersökningar mellan metoxalen-bad-PUVA och andra terapier
- UV-sensibiliserande läkemedel orsakar i allmänhet inte problem vid smalbandig UVB-behandling, eftersom det är UVA-våglängden som ger ljuskänslighet för systemiska läkemedel.
- Mer information om behandlingen finns i tilläggsmaterialet «Psoriaasin valohoitojen toteutus»7.
- Ljussektionen vid Finlands Dermatologförening har utarbetat riktgivande dosdiagram för finländska hudtyper (smalbands-UVB, doseringsanvisning «hoi50062a.pdf»3).
- Den vanligaste behandlingsfrekvensen är 3 gånger i veckan «Kapeakaistaisen UVB-hoidon suositeltava antotiheys lienee kolme kertaa viikossa.»C.
- Remissionstid efter behandling:
- Olika undersökningar visar att 12–35 % av patienterna är i remission ännu 6 månader efter avslutad behandling «Yones SS, Palmer RA, Garibaldinos TT ym. Randomize...»121.
- En eventuell akut biverkning är rodnad (UV-erytem) som uppkommer på grund av att dosen överskrider den lägsta erytemdosen.
- Det finns ingen information huruvida behandlingen ökar risken för hudcancer eller
inte «Hearn RM, Kerr AC, Rahim KF ym. Incidence of skin ...»122.
- På basis av teoretisk modellering kunde 450 behandlingar med smalbandig UVB-behandling anges som övre gränsen för antalet behandlingar «Ibbotson SH, Bilsland D, Cox NH ym. An update and ...»123, «Diffey BL. Factors affecting the choice of a ceili...»124. Det finns dock ingen konsensus i frågan.
- Smalbandig UVB-behandling kan också vara lämplig för hemvård om lämpliga apparater kommer ut på marknaden «Koek MB, Buskens E, van Weelden H ym. Home versus ...»125, «Koek MB, Sigurdsson V, van Weelden H ym. Cost effe...»126.
- Patientanvisning för UVB-behandling: «Psoriaasin UV311-hoito»8.
- Primär UV-ljusbehandling för vuxna patienter:
- Bredbandig UVB-behandling (TL/12, över 275 nm; UV6, över 285 nm):
- Bredbandig UVB-behandling håller på att försvinna från hälso- och sjukvårdsenheterna,
men den kan användas hemma.
- En del psoriasisföreningar hyr ut UVB-ljusbehandlingsapparater till personer som fått ett behandlingsförordnande «https://psori.fi/tietoa-psoriasiksesta/psoriasiksen-hoito/hoitovaihtoehdot/»9.
- Psoriasisförbundet förutsätter remiss av hudläkare för den första vårdperioden.
- Hemvård beviljas efter särskild prövning «Koek MB, Buskens E, Bruijnzeel-Koomen CA ym. Home ...»127, «Koek MB, Buskens E, Steegmans PH ym. UVB photother...»128.
- Bredbandig UVB-behandling håller på att försvinna från hälso- och sjukvårdsenheterna,
men den kan användas hemma.
SUP-behandling (selektiv ultraviolett fototerapi)
- Effekten på psoriasis är liten eftersom andelen UVB-strålning är liten.
PUVA-behandlingar
- PUVA-behandlingar som grundar sig på utvärtes (extern) sensibilisering:
- I Finland används bad-PUVA med 8-metoxipsoralen (8-MOP). Även salva-PUVA är möjlig när eksemet finns i begränsade områden, till exempel på handflatorna eller fotsulorna.
- Patienten kan klara sig flera år på periodisk PUVA-behandling.
- Bad-PUVA är inte riskfritt och förutsätter särskilt insatt personal «Voss A, Leverkus M, Bröcker EB ym. Topical psorale...»129.
- Effekterna av långtidsbehandling är inte exakt kända «Hannuksela-Svahn A, Pukkala E, Koulu L ym. Cancer ...»130.
- För närmare information om inledning av behandlingen, se «Psoriaasin valohoitojen toteutus»7.
- PUVA-behandlingar som grundar sig på invärtes sensibilisering:
- I Finland används PUVA som grundar sig på invärtes (systemisk) sensibilisering endast i specialsituationer för behandling av psoriasis.
- Psoralenen som används är 8-metoxipsoralen (8-MOP). Långvarig behandling ökar permanent
risken för hudcancer, särskilt för skivepitelcancer, «Vaikeaan psoriaasiin liittyy lievästi kohonnut ihon okasolusyövän riski, jonka tärkein riskitekijä on metoksaleeni-tabletti-PUVA-hoito.»A.
- Risken är livslång och därför ska huden kontrolleras regelbundet «Stern RS, Liebman EJ, Väkevä L. Oral psoralen and ...»131, «Stern RS, PUVA Follow up Study.. The risk of melan...»132.
- På grund av risken för fotokarcinogenes rekommenderas maximalt 200–250 PUVA-behandlingar eller en maximal kumulativ UVA-dos på 1000 J/cm² «Griffiths CE, Clark CM, Chalmers RJ ym. A systemat...»133, «Stern RS, Lunder EJ. Risk of squamous cell carcino...»134.
Kombinationsbehandlingar med UV-ljusbehandling
- Kortikosteroidsalvor:
- Användningen av kortikosteroidsalvor avslutas gradvis i samband med ljusbehandling.
- UV-ljusbehandling inleds ofta för att avbryta behandlingen med kortikosteroidsalvor.
- Att kombinera kortikosteroidsalva med UVB-behandlingar förefaller inte att förbättra behandlingsresultatet eller at minska den nödvändiga UV-stråldosen «Griffiths CE, Clark CM, Chalmers RJ ym. A systemat...»133, «Stern RS, Lunder EJ. Risk of squamous cell carcino...»134.
- Remissionstiden kan efter kombinationsbehandling vara kortare än efter enbart UVB-behandling «Griffiths CE, Clark CM, Chalmers RJ ym. A systemat...»133, «Lebwohl M, Menter A, Koo J ym. Combination therapy...»135.
- Användningen av kortikosteroidsalvor avslutas gradvis i samband med ljusbehandling.
- Systemisk retinoid (vanligen acitretin):
- Kombinationen kan påskynda läkningen av eksemet «Asitretiinin ja UVB-valon yhdistelmähoito näyttää olevan tehokkaampi kuin pelkkä UVB-valohoito.»B och minska dosen av UV-strålning som behövs.
- Retinoidbehandling kan ha en gynnsam effekt som minskar risken för skivepitelcellscancer hos patienter som fått mycket ljusterapi. Effekten försvinner efter avslutad medicinering «Asitretiini saattaa vähentää ihon okasolusyövän riskiä hoidon aikana.»C.
- Metotrexat:
- Kombinationen kommer i fråga i specialsituationer.
- Ciklosporin:
- På grund av den ökade risken för fotokarcinogenes ska ciklosporin inte kombineras med UV-ljusbehandlingar «Sugie N, Fujii N, Danno K. Cyclosporin-A suppresse...»136.
- För personer som fått många UV-ljusbehandlingar rekommenderas inte ciklosporinbehandling «Paul CF, Ho VC, McGeown C ym. Risk of malignancies...»137, «Marcil I, Stern RS. Squamous-cell cancer of the sk...»138, «Murphy GM. Skin cancer in patients with psoriasis-...»139.
- Biologiska läkemedel, apremilast och dimetylfumarat:
- Enligt arbetsgruppens uppfattning kommer kombinationen i fråga i specialsituationer, men forskningsevidensen är ringa.
Klimatterapi
- Klimatterapi har samma effekt som UVB-ljusbehandling «Snellman E. E. Heliotherapy of psoriasis (thesis)....»140.
- Hos cirka hälften av patienterna återgår eksemet till det tidigare inom ett halvt år efter en 4 veckors klimatterapiresa «Snellman E. E. Heliotherapy of psoriasis (thesis)....»140.
- Ciklosporinbehandling kontraindicerar klimatterapi.
- Se anvisningen för solbad «Auringonotto-ohje ihopsoriaasipotilaalle»9.
Systemisk läkemedelsbehandling
- Systemisk behandling av hudpsoriasis inleds och följs upp av dermatolog.
- Till god behandlingspraxis hör uppföljning av säkerheten av patienter som får systemisk
läkemedelsbehandling «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10 samt uppföljning av effekten, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11.
- Den föreskrivna uppföljningen med blodprov kan genomföras inom primärvården.
- Anvisningarna gäller vuxna patienter.
- På webbplatsen för Reumatologisk förening i Finland «https://www.reumatologinenyhdistys.fi/ohjeet/»12 finns anvisningar för bedömning av infektionskänslighet, vaccinationer, hepatit B-virus och latent tuberkulos.
- Målet med behandlingen är ett tillstånd med så få symtom som möjligt. Som mätare används oftast förändringen i PASI-indexet (ΔPASI) eller det absoluta PASI-värdet samt livskvalitetsmätaren DLQI som kan användas för att ge grunder för behandlingsbesluten (se bild «Målorienterad behandlingsstrategi för biologisk behandling för hudpsoriasis»48).
- Målet för den biologiska behandlingen är att åtminstone nå PASI-75-respons (gott terapisvar) men gärna PASI-90-respons (utmärkt terapisvar). Patienter med PASI-90-respons har betydligt bättre livskvalitet än patienter med PASI-75-respons «Puig L. PASI90 response: the new standard in thera...»141, «Strober B, Papp KA, Lebwohl M ym. Clinical meaning...»142, «Elewski BE, Puig L, Mordin M ym. Psoriasis patient...»143.
- Sjukförsäkringsersättningen delar in systemiska psoriasisläkemedel i primära och sekundära:
- De primära psoriasisläkemedlen är de traditionella läkemedlen acitretin, metotrexat
och ciklosporin. De är grundersättningsgilla utan separat utlåtande.
- För behandling av erytrodermisk psoriasis kan dessa läkemedel på basis av utlåtande ersättas enligt den högre specialersättningsklassen (100%).
- Alla andra läkemedel är sekundära. På basis av läkarutlåtande kan de beviljas begränsad grundersättning. Förutsättningen för detta är svår psoriasis, där behandling med något primärt läkemedel inte haft effekt eller har inte kunnat användas på grund av kontraindikation eller biverkningar.
- De primära psoriasisläkemedlen är de traditionella läkemedlen acitretin, metotrexat
och ciklosporin. De är grundersättningsgilla utan separat utlåtande.

Grunderna för bedömning av terapisvar och beslut om fortsatt behandling. Som mätare fungerar PASI-förbättring (ΔPASI) eller absolut PASI och DLQI.
DLQI (Dermatology Life Quality Index)
PASI (Psoriasis Area and Severity Index)
Anpassad från artikel Mrowietz U ym. Definition of treatment goals for moderate to severe psoriasis: a European consensus Arch Dermatol Res 2011;303:1-10
Primära systemiska läkemedel
- Indikationer (bild «Esimerkkejä keskivaikeasta ja vaikeasta läiskäpsoriaasista ja erytrodermisestä psoriaasista sekä kämmen-, jalkapohja- ja hiuspohjan psoriaasista»49):
- svår plackpsoriasis
- erytrodermisk eller pustulös psoriasis
- psoriasis i handflatan eller på fotsulan som inte reagerar på lokalbehandling
- svår psoriasis i hårbottnen
- För bedömning av terapisvar se tabell «Definitioner associerade med terapisvaret för patienter med hudpsoriasis , ...»1.
- Acitretin «Sbidian E, Maza A, Montaudié H ym. Efficacy and sa...»144 (tabell «Detta bör beaktas vid acitretinbehandling...»3):
- Acitretin används för behandling av svår plackpsoriasis, psoriasis med tjocka fjäll
i handflator och på fotsulor samt generaliserad pustulös psoriasis.
- Acitretin har ingen effekt på psoriasisartrit.
- Ett gott terapisvar kan uppnås hos 22–25 % av patienterna med plackpsoriasis inom 8 veckor med dosen 10–50 mg «Gollnick H, Bauer R, Brindley C ym. Acitretin vers...»145, men effektevidensen jämfört med placebo är knapp «Tutkimusnäyttö asitretiinin tehosta näyttää olevan vähäinen.»C.
- Acitretinbehandling kombineras med UV-ljusbehandling för behandling av plackpsoriasis.
- Klinisk erfarenhet stöder uppfattningen att kombinationsbehandling med PUVA ger bättre resultat är enbart acitretin, men forskningsevidens för bättre effekt av att kombinera acitretin med PUVA-behandling saknas «Griffiths CE, Clark CM, Chalmers RJ ym. A systemat...»133.
- Kombinationsbehandling med UVB-ljus ökar effekten jämfört med enbart UV-ljus. Ett gott terapisvar kan uppnås hos 60 % av patienterna på 8 veckor «Ruzicka T, Sommerburg C, Braun-Falco O ym. Efficie...»146.
- Acitretin försvagar inte immunförsvaret.
- Incidensen av skivepitelcancer kan minska under behandlingen «Asitretiini saattaa vähentää ihon okasolusyövän riskiä hoidon aikana.»C.
- Acitretin lämpar sig för långtidsbehandling och behandlingen kan avbrytas och återinsättas.
- På grund av teratogenicitet strävar man att undvika användning av acitretin hos kvinnor i fertil ålder.
- Acitretin används för behandling av svår plackpsoriasis, psoriasis med tjocka fjäll
i handflator och på fotsulor samt generaliserad pustulös psoriasis.
- Metotrexat (tabell «Detta bör beaktas vid metotrexatbehandling...»4):
- Metotrexat används vid svår psoriasis «Warren RB, Weatherhead SC, Smith CH ym. British As...»147.
- Om patienten samtidigt har psoriasisartrit är metotrexatbehandling den primära behandlingen.
- Metotrexat är effektivt för behandling av plackpsoriasis «Metotreksaatti on tehokas hoito läiskäpsoriaasissa.»A.
- Ett gott terapisvar uppnås hos cirka 40–60 % av patienterna med en veckodos på 15–20 mg under 12 veckors behandling.
- Metotrexatbehandlingen påverkar immunförsvaret.
- Metotrexat lämpar sig för långtidsbehandling och behandlingen kan ges intermittent.
- Medicineringen kräver särskild noggrannhet på grund av den exceptionella doseringen och biverkningarna. Se «http://www.nrls.npsa.nhs.uk/resources/type/alerts/?entryid45=59800&q=0%C2%ACmethotrexate%C2%AC»13.
- Biotillgängligheten av metotrexat är bättre när den doseras subkutant eller intramuskulärt än oralt «Metotreksaatin hyötyosuus on parempi ihon alle tai lihakseen annosteltuna.»A.
- Vid en akut allvarlig infektion görs uppehåll i medicineringen «Anttila VJ, Haapamäki J, Peltomaa R ym. [Interrupt...»148.
- Latent tuberkulos och hepatit B-infektion screenas vid behov enligt anvisningen utgiven av Reumatologisk förening i Finland. Se «https://www.reumatologinenyhdistys.fi/ohjeet/»12.
- Årlig vaccination mot säsongsinfluensa rekommenderas.
- Pneumokockvaccination rekommenderas för alla personer över 65 år. För andra grupper rekommenderas detta enligt läkarens bedömning.
- Uppehåll med metotrexat behövs inte före vaccinationer «https://www.reumatologinenyhdistys.fi/ohjeet/»12. Se anvisningar när det gäller barn «https://www.reumatologinenyhdistys.fi/ohjeet/»12.
- Ciklosporin (tabell «Detta bör beaktas vid ciklosporinbehandling...»5):
- Ciklosporin kan i specialfall användas vid svår psoriasis när det behövs snabb respons eller andra primära behandlingar är olämpliga.
- Ciklosporin är effektivt för behandling av plackpsoriasis «Siklosporiini on tehokas hoito läiskäpsoriaasissa.»A.
- Ett gott terapisvar kan uppnås hos 50–70 % av patienterna med en dygnsdos på 3 mg/kg under 8–16 veckor.
- Ciklosporin försvagar immunförsvaret.
- Särskilt hos patienter som tidigare behandlats med tablett-PUVA ökar ciklosporin risken för skivepitelcancer i huden «Siklosporiini näyttää lisäävän ihon okasolusyövän riskiä psoriaasipotilailla.»B.
- Långtidsbehandling (över 2 år) bör helst undvikas på grund av njurbiverkningar «Ryan C, Amor KT, Menter A. The use of cyclosporine...»149, «Munuaishaittavaikutusten riskiä lisää yli 2 vuotta kestänyt hoito ja ≥ 5 mg/kg/vrk siklosporiiniannos.»A.
- Medicineringen kan vid behov ges intermittent.
- Vid plötsliga infektioner görs uppehåll i medicineringen.
- Hudpsoriasis återkommer vanligen inom ett par månader efter att användningen av alla systemiska läkemedel upphört «Koo J, Lebwohl M. Duration of remission of psorias...»150.
- För uppföljningsproven som ska tas vid användning av systemiska läkemedel, se tabellerna «Detta bör beaktas vid acitretinbehandling...»3, «Detta bör beaktas vid metotrexatbehandling...»4 och «Detta bör beaktas vid ciklosporinbehandling...»5.
- Systembehandlingar, såsom aciteretin eller metotrexat, kan undantagsvis behövas för behandling av psoriasis hos barn. Vid behov genomförs behandlingen i samarbete med pediater.
| Rubrik | Bör beaktas |
|---|---|
| Dos | Startdos 10–25 mg/dygn Dosen höjs vid behov med 2–4 veckors intervall till högst 50 mg/dygn «Sbidian E, Maza A, Montaudié H ym. Efficacy and sa...»144, «Gollnick H, Bauer R, Brindley C ym. Acitretin vers...»145, «Berbis P, Geiger JM, Vaisse C ym. Benefit of progr...»151. |
| Biverkningar | Fosterskador under medicineringen och i 3 år efter avslutad användning Torr hud och torra slemhinnor Eventuell ökning av håravfall Eventuellt förhöjda triglycerider, kolesterol och levervärden «Gollnick H, Bauer R, Brindley C ym. Acitretin vers...»145, «Murray HE, Anhalt AW, Lessard R ym. A 12-month tre...»152, «Roenigk HH Jr, Callen JP, Guzzo CA ym. Effects of ...»153 Inga bevis på hyperostos. |
| Interaktioner | A-vitamin och A-vitaminderivat, tetracyklin, metotrexat och fenytoin |
| Kontraindikationer | Graviditet och amning (se tabell «Patienter med psoriasis och psoriasisartrit: systemisk läkemedelsbehandling under
graviditet och amning ...»22) Kvinnor som kan bli gravida ska inte konsumera alkohol under behandlingen och inte heller 2 månader efter att behandlingen avslutats, eftersom etretinat som kan bildas kan öka risken för fosterskador. Allvarlig lever- eller njursvikt |
| Användbar kombination | UV-ljusbehandlingar «Asitretiinin ja UVB-valon yhdistelmähoito näyttää olevan tehokkaampi kuin pelkkä UVB-valohoito.»B |
| Uppföljningsprov före och under behandlingen* | Triglycerider, ALAT (och kolesterol) och kreatinin före behandlingen, en månad efter
att behandlingen påbörjats och därefter med 3–6 månaders intervall. Hos personer i fertil ålder ska graviditet uteslutas före behandlingen. Om triglyceridvärdet överstiger 4 mmol/l eller om ALAT-värdet överstiger 2 x referensvärdet, ska dosen reduceras eller medicineringen avslutas. Se även «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 |
| * Alla nämnda uppföljningsprov behöver inte nödvändigtvis tas av varje patient, utan omfattningen av uppföljningsprov bedöms individuellt. | |
| Rubrik | Bör beaktas |
|---|---|
| Dos | Som tabletter eller subkutant 7,5–25 mg en gång i veckan. Startdosen är 10–15 mg doserad oralt eller som subkutan injektion. Dosen höjs på
basis av responsen med 2–4 veckors intervall vid behov upp till 25 mg. Om läkemedlet
är ineffektivt oralt, övergår man till att använda subkutana injektioner. Subkutan dosering minskar biverkningarna i mag-tarmkanalen och kan förbättra effekten. Doseringen ska vara försiktig vid behandling av äldre personer. Hos barn inleds medicineringen vanligen direkt med underhållsdosen. Medicineringen kräver särskild noggrannhet på grund av exceptionell dosering och biverkningar. |
| Biverkningar | Illamående och diarré Nedsatt benmärgsfunktion (cytopeni)
|
| Stomatit Fettdegeneration av levern, toxiska skador på levercellerna och leverfibros:
|
|
| Interstitiell lungreaktion Hög ålder, hypoalbuminemi och nedsatt njurfunktion ökar förekomsten av biverkningar «Puig L. PASI90 response: the new standard in thera...»141, «Kent PD, Luthra HS, Michet C Jr. Risk factors for ...»158, «Alarcón GS, Kremer JM, Macaluso M ym. Risk factors...»159. |
|
| Interaktioner | Trimetoprim, probenecid och retinoider Antiinflammatoriska smärtstillande läkemedel och protonpumpshämmare bör tas vid en annan tidpunkt än metotrexat (i övrigt tillåtna). |
| Kontraindikationer | Njur-, lever- eller benmärgssvikt Signifikant lungfibros och signifikant nedsatt lungfunktion Överkonsumtion av alkohol Graviditet och amning (se tabell «Patienter med psoriasis och psoriasisartrit: systemisk läkemedelsbehandling under graviditet och amning ...»22) |
| Användbar kombination | Folsyratillskott 5 mg i veckan eller 1 mg/dygn minskar levertoxiciteten och symtomen i mag-tarmkanalen utan att minska effekten av metotrexat «Foolihapposubstituutio 5 mg/vko tai 1 mg/vrk saattaa vähentää metotreksaatin aiheuttamaa maksatoksisuutta ja gastrointestinaalioireita vähentämättä kuitenkaan metotreksaatin tehoa.»C. |
| Uppföljningsprov* | Liten blodbild + trombocyter, ALAT före behandlingen, därefter efter 3, 6 och 12 veckor
och därefter med 3–6 månaders intervall Krea var 6:e månad Vid behov då dosen höjs. |
| Hos vuxna tas lungröntgen före behandlingen, om det inte har gjorts under föregående år. | |
| Om ALAT förhöjt > 2–2,5 x referensvärdets övre gräns, görs behandlingsuppehåll för metotrexat och uppföljningsprov av ALAT tas på vuxna 2 veckor senare och hos barn 1 vecka senare. Patientens användning av alkohol och andra läkemedel samt viktindex (risk för fettlever) ska uppmärksammas. Medicineringen kan inledas på nytt när ALAT hos vuxna är tillbaka till det ursprungliga värdet och hos barn < 75 U/l. | |
| Om ALAT stiger upprepade gånger måste andra eventuella bakomliggande orsaker utredas. Behandlingsuppehåll. | |
| Se även «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 | |
| Oral- och dentalhälsan ska hållas god under hela medicineringen. | |
| Om antalet leukocyter är mindre än 3,0 x 109/l eller om antalet trombocyter är under 100 x 109/l, ska läkemedelsdosen minskas eller behandlingsuppehåll göras. | |
| * Alla nämnda uppföljningsprov behöver inte nödvändigtvis tas av varje patient, utan omfattningen bedöms individuellt. | |
| Rubrik | Bör beaktas |
|---|---|
| Dos | Startdosen är 2,5–5 mg/kg/dygn, antingen som kontinuerlig behandling eller, vid hudpsoriasis, som intermittenta kurer under 3 månader. |
| Biverkningar | Huvudvärk, förhöjt blodtryck, nedsatt njurfunktion: Behandling under längre tid än
2 år med en dygnsdos på över 5 mg/kg ökar risken för njurbiverkningar «Munuaishaittavaikutusten riskiä lisää yli 2 vuotta kestänyt hoito ja ≥ 5 mg/kg/vrk siklosporiiniannos.»A. Tandköttshyperplasi Ökad behåring Muskelkramper och darrningar |
| Interaktioner | Vanliga, ska alltid kontrolleras innan ny medicinering inleds |
| Kontraindikationer | Cancer under de senaste 10 åren (keratinocytcancer under de 5 föregående åren), hypertoni,
njursvikt, immunbristtillstånd, samtidig UV-ljusbehandling Se även tabell «Patienter med psoriasis och psoriasisartrit: systemisk läkemedelsbehandling under graviditet och amning ...»22 Graviditet och amning. |
| Användbar kombination | Vid hypomagnesemi, magnesiumtillskott 200–250 mg/dygn |
| Uppföljningsprov* | Kreatinin och blodtryck före behandling, efter behandling med 2 veckors intervall
under 2 månader och därefter med 2–3 månaders intervall Liten blodbild + trombocyter, ALAT, AFOS, kolesterol, triglycerider, magnesium och kalium efter 2–3 månader Serumkalium och magnesium med 6 månaders intervall Om kreatininhalten överstiger 30 % av utgångsvärdet måste dosen minskas och om ökningen överstiger 50 % ska medicineringen avslutas. Om blodtrycket stiger och dosreduktion inte hjälper, ska behandlingsuppehåll göras eller vid behov blodtrycksmedicinering inledas (i första hand kalciumblockerare) «Griffiths CE, Dubertret L, Ellis CN ym. Ciclospori...»160. Under graviditet kan ciklosporin endast användas om patienten följs intensivt (risk för förhöjt blodtryck och preeklampsi). Munnen och tänderna ska hållas vid god hälsa under hela medicineringen. Se även «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 |
| * Alla nämnda uppföljningsprov behöver inte nödvändigtvis tas av varje patient, utan omfattningen bedöms individuellt. | |
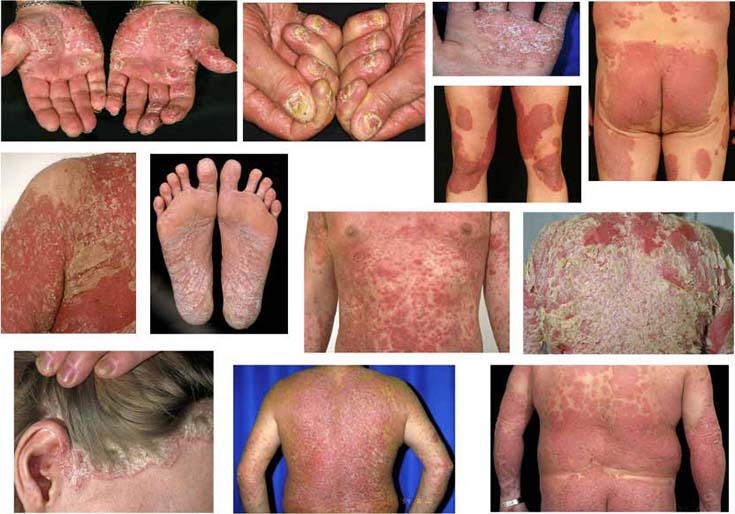
Esimerkkejä keskivaikeasta ja vaikeasta läiskäpsoriaasista ja erytrodermisestä psoriaasista sekä kämmen-, jalkapohja- ja hiuspohjan psoriaasista, joissa sisäinen lääkehoito saattaa olla aiheellinen.
© Raimo Suhonen
Sekundära systemiska läkemedel
Perorala läkemedel
- Apremilast (tabell «Detta bör beaktas vid apremilastbehandling...»6)
- Apremilast kan användas för behandling av svår psoriasis när de primära behandlingarna visat sig ineffektiva, kontraindicerade eller olämpliga.
- För att behandlingen ska ersättas krävs separat B-utlåtande.
- Vid behandling av plackpsoriasis har man med apremilast uppnått ett gott terapisvar
hos endast 29–33 % och ett utmärkt terapisvar hos 9–10 % av patienterna med 16 veckors
behandling «Apremilasti lienee turvallinen ja melko tehokas keskivaikean ja vaikean ihopsoriaasin induktiohoidossa.»B. Ett gott terapisvar verkar fortsätta under 102 veckors behandling hos cirka hälften
av patienterna «Reich K, Gooderham M, Bewley A ym. Safety and effi...»161.
- Apremilast verkar ha något sämre effekt än metotrexat och betydligt sämre effekt än de biologiska läkemedlen.
- Om minst PASI-75 inte uppnåtts inom 16 veckor ska behandlingen avbrytas.
- Hos 15–17 % av patienterna förekommer illamående eller diarré i början av behandlingen.
- Apremilastbehandlingen har inte varit förknippad med någon ökning av infektioner och ingen organtoxicitet har beskrivits. Under behandlingen behövs inte laboratorieuppföljning.
| Rubrik | Bör beaktas |
|---|---|
| Dos | Startdos under de första 6 dagarna: 10 mg x 1, därefter dag 1 10 mg x 2, dag 2 10
mg + 20 mg, dag 3 20 mg x 2, dag 4 20 mg + 30 mg och dag 5 30 mg x 2. Underhållsdosen är 30 mg genom munnen två gånger per dygn. |
| Biverkningar | Illamående och diarré under de första veckorna av behandlingen, viktminskning > 5 % |
| Interaktioner | Samtidig användning av starka CYP3A4-enzyminducerare (t.ex. rifampicin, fenobarbital, karbamazepin, fenytoin och äkta johannesört) rekommenderas inte. |
| Kontraindikationer | Gällande graviditet och amning, se tabell «Patienter med psoriasis och psoriasisartrit: systemisk läkemedelsbehandling under graviditet och amning ...»22. |
| Användbar kombination | Kan kombineras med metotrexat, men vid psoriasisartrit har inte kortvarig kombinationsbehandling ökat behandlingseffekten. Kombinationsbehandling har inte undersökts för behandling av hudpsoriasis. |
| Screeningundersökningar före behandlingen | Behövs inte enligt produktresumén |
| Uppföljningsprov | Ingen separat uppföljning av säkerhetsprov |
| Att beakta i vården | Vid svår njursvikt (GFR under 30 ml/mim/1,73 m2) halveras dosen. Om patienten är underviktig när behandlingen inleds ska vikten kontrolleras regelbundet. Förhöjd risk för suicid ska beaktas före och under behandlingen. Om patienten under behandlingen får ångest- eller depressionssymtom eller om de försvåras under behandlingen, ska behandlingen avbrytas. |
- Dimetylfumarat (tabell «Detta bör beaktas vid dimetylfumaratbehandling...»7):
- Dimetylfumarat kan användas för behandling av svår psoriasis när de primära behandlingarna
visat sig ineffektiva, kontraindicerade eller olämpliga.
- För att behandlingen ska ersättas krävs ett separat B-utlåtande.
- I en placebokontrollerad 16 veckor lång studie uppnådde endast 37,5 % av patienterna (placebo 15,3 %) «Dimethyl fumarate may increase the proportion of patients with moderate to severe psoriasis to achieve a clinically meaningful improvement at 16 weeks of tretament but the evidence is scarce. The number of adverse events may be higher than for placebo but the number of severe adverse events may be equal to placebo at 16 weeks of tretament.»D ett gott terapisvar (PASI-75), och 18,4 % (placebo 4,6 %) ett utmärkt svar (PASI-90) «Mrowietz U, Szepietowski JC, Loewe R ym. Efficacy ...»162.
- Det finns ingen tillförlitlig forskning om de långvariga behandlingsresultaten, men man antar att effekten bibehålls väl hos patienter som tål läkemedlet.
- Dimetylfumarat har ingen effekt på psoriasisartrit.
- Som biverkningar ger dimetylfumarat mycket allmänt diarré och andra symtom som hänför sig till mag-tarmkanalen samt rodnad i ansiktet och på kroppen, allmänt leukopeni, lymfopeni eller eosinofili. På grund av biverkningarna kan begränsning av dosökning eller behandlingsstopp bli aktuella.
- Multifokal leukoencefalopati orsakad av JC-viruset är en sällsynt biverkning, särskilt hos patienter med lymfopeni.
- Dimetylfumarat kan användas för behandling av svår psoriasis när de primära behandlingarna
visat sig ineffektiva, kontraindicerade eller olämpliga.
| Rubrik | Bör beaktas |
|---|---|
| Dos | Under den första veckan tas 30 mg dimetylfumarat en gång per dag (1 tablett på kvällen).
Under den andra veckan tas 30 mg dimetylfumarat två gånger dagligen (1 tablett på
morgonen och 1 tablett på kvällen). Under den tredje veckan tas dimetylfumarat 30
mg tre gånger dagligen (1 tablett på morgonen, 1 tablett mitt på dagen och 1 tablett
på kvällen). Från och med den fjärde veckan övergår man till en tablett dimetylfumarat
120 mg som tas på kvällen. Därefter höjs dosen enligt tolerans med en tablett dimetylfumarat
120 mg i veckan som tas vid en annan tidpunkt på dagen under de följande fem veckorna. Den högsta tillåtna dygnsdosen är 720 mg (3 x 2 dimetylfumarat 120 mg). När hudsymtomen har lättat, kan en gradvis dosreduktion eftersträvas. |
| Biverkningar | Vanliga: Rodnad i ansiktet och kroppen, symtom i mag-tarmkanalen (diarré, svullnad, illamående m.m.), leukopeni eller lymfopeni, eosinofili |
| Nyttig kombination | |
| Screeningundersökningar före behandlingen | Utredning av eventuell latent tuberkulos (se webbplats för Reumatologisk förening
«https://www.reumatologinenyhdistys.fi/app/uploads/2019/11/LTBI-ohje-SRY-p%C3%A4ivitys_15.11.2019.pdf»14) Tandläkarundersökning för konstaterande av eventuella infektionshärdar (vid behov t.ex. ortopantomografi) Fullständig blodbild (behandlingen får inte inledas om B-Leuk är under 3,0 eller B-Lymf är under 1,0 x 109) ALAT, AFOS, kreatinin HIV- och hepatitantikroppar (HBsAg, HBcAb, vid behov HBcAbM, HCVAb) vid behov Sänka, CRP, U-screening Kärnantikroppar vid behov |
| Uppföljningsundersökningar under behandlingen | Fullständig blodbild med minst 3 månaders intervall (se närmare anvisningar i produktresumén), ALAT, AFOS, kreatinin 3 månader efter behandlingsstart och därefter individuellt, till exempel med 3–12 månaders intervall. |
Biologiska läkemedel
- Beroende på det biologiska målet för läkemedlets verkan kan de biologiska läkemedlen
indelas i fem grupper:
- hämmare av tumörnekrosfaktor alfa (TNF-hämmare)
- interleukin (IL)-12/23-hämmare
- IL-17-hämmare
- IL-23-hämmare
- T-cellshämmare.
- De biologiska läkemedlen har i huvudsak undersökts inom ramen för prövningsprogram med patienter med svår psoriasis (urvalskriterium PASI > 12, i genomsnitt PASI 18–20), och därför är det oklart om resultaten kan tillämpas på patienter med lindrigare psoriasis.
Allmänna anvisningar för användning av biologiska läkemedel för behandling av hudpsoriasis och psoriasisartrit
- Innan ett biologiskt läkemedel tas i bruk ska en del tillstånd och sjukdomar uteslutas (se förteckningen nedan över kontraindikationer).
- Behandlingen inleds och övervakas av en specialist i hudsjukdomar eller reumatologi.
- Rätten till specialersättning förutsätter ett separat B-utlåtande att patienten har svår psoriasis eller psoriasisartrit, och att tillfredsställande terapirespons inte har uppnåtts med de primära systemiska behandlingarna eller att dessa inte kan användas.
- Vid val av läkemedel ska man med patienten gå genom vilka faktorer kan påverka behandlingsföljsamheten. Sådana faktorer är bland annat läkemedlets effekt och säkerhet, behandlingsprocessen och kostnaderna.
- Det finns en modifierad algoritm av en europeisk konsensusgrupp, vilken har uppdaterats så att den motsvarar resultaten av de senaste läkemedelsbehandlingarna. Denna algoritm rekommenderas som grund för målsättningen för behandlingen av hudpsoriasis, för uppföljning av behandlingseffekten och för att motivera förändringar i behandlingen. Se målorienterad behandlingsstrategi för biologisk behandling, bild «Målorienterad behandlingsstrategi för biologisk behandling för hudpsoriasis»48, «Mrowietz U, Kragballe K, Reich K ym. Definition of...»163.
- De gemensamma kontraindikationerna mot biologiska psoriasisläkemedel är
- graviditet (relativ kontraindikation) med undantag för certolizumab pegol
- amning (relativ kontraindikation)
- signifikanta aktiva infektioner (inklusive tandinfektioner) «Anttila VJ, Haapamäki J, Peltomaa R ym. [Interrupt...»148
- demyeliniserande sjukdom (gäller TNF-hämmare)
- aktiv malign sjukdom «Anttila VJ, Haapamäki J, Peltomaa R ym. [Interrupt...»148
- relativ kontraindikation: behandlad cancer
- gäller inte basalcellscancer eller skivepitelcellscancer med god prognos (diameter under 1 cm och väl differentierad)
- hjärtsvikt (NYHA III–IV) (gäller TNF-hämmare)
- överkänslighet mot preparatets beståndsdelar.
- Möjligheten att patienten kan ha latent tuberkulos måste uteslutas (aktivering av latent tuberkulos till tuberkulos under behandling av reumatisk sjukdom «https://www.reumatologinenyhdistys.fi/app/uploads/2019/11/LTBI-ohje-SRY-p%C3%A4ivitys_15.11.2019.pdf»14).
- Vid behov inleds profylaktisk skyddsmedicinering mot tuberkulos efter bedömning av infektions- eller lungläkare.
- Andra kroniska infektioner handläggs enligt klinisk bedömning (se läkemedelsspecifika tabeller).
- Patienter som behandlas med biologiska läkemedel ska kontakta den enhet som ansvarar
för vården eller ett separat vaccinationscenter, beroende på den lokala kapaciteten
- vid infektion
- Vid akut svår infektion görs behandlingsuppehåll.
- Se även «https://www.reumatologinenyhdistys.fi/ohjeet/»12.
- när vaccinationer planeras (generellt eller inför resa)
- Se anvisningar från Reumatologisk förening i Finland «https://www.reumatologinenyhdistys.fi/ohjeet/»12, Institutet för hälsa och välfärds vaccinationshandbok «https://www.thl.fi/fi/web/rokottaminen»15 och Reumahusets anvisningar «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumapotilaiden-rokotukset»16
- Levande vacciner är förbjudna (gäller bl.a. mässling, påssjuka, röda hund, vattkoppor och gula febern samt orala vacciner mot tyfoidfeber och polio). Se separat vaccinationsanvisning för barn på Reumatologisk förenings webbplats «https://www.reumatologinenyhdistys.fi/ohjeet/»12.
- Inaktiverade vacciner är tillåtna.
- Kontroll av giltighetstiden för vaccinationer som ingår i det normala vaccinationsprogrammet rekommenderas. Vaccinationer som saknas bör ges innan behandlingarna inleds (bl.a. vaccination mot stelkramp och difteri).
- Pneumokockvaccination rekommenderas för alla personer över 65 år och enligt den behandlande läkarens övervägande även för andra.
- Årlig influensavaccination rekommenderas.
- när kirurgiska ingrepp planeras
- I mån av möjlighet förläggs operationen till tidpunkten för nästa läkemedelsdos.
- Längden av behandlingsuppehållet varierar beroende på vilket läkemedel som används och ska kontrolleras från fall till fall «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeet-ja-leikkaus»17. Medicineringen kan i allmänhet inledas när stygnen avlägsnats och såret är snyggt.
- när graviditet planeras. Se tabell «Patienter med psoriasis och psoriasisartrit: systemisk läkemedelsbehandling under graviditet och amning ...»22, «Anttila VJ, Haapamäki J, Peltomaa R ym. [Interrupt...»148, «Götestam Skorpen C, Hoeltzenbein M, Tincani A ym. ...»164.
- vid infektion
- Terapisvaret bedöms första gången efter 12–16 veckors behandling och för alla mediciner
senast efter 24 veckor.
- Om tillräcklig respons inte uppnåtts övervägs intensifiering av behandlingen (bild «Målorienterad behandlingsstrategi för biologisk behandling för hudpsoriasis»48).
- De nämnda biologiska behandlingarna kan bytas ut mot varandra utan särskilt avbrott.
- Rekommendationerna för uppföljning av medicineringen presenteras i tabell «Detta bör beaktas vid biologisk läkemedelsbehandling...»8.
- Kombinationsbehandlingar har inte undersökts tillräckligt för hudpsoriasis.
- Att kombinera metotrexat med TNF-hämmare är vanligt vid psoriasisartrit och andra reumatiska sjukdomar. Hos en del patienter utvecklas neutraliserande antikroppar särskilt mot infliximab, adalimumab och golimumab, och då kan det vara till nytta att kombinera dem med metotrexat «Lecluse LL, Driessen RJ, Spuls PI ym. Extent and c...»165, «Hoffmann JH, Hartmann M, Enk AH ym. Autoantibodies...»166, «Kimball AB, Gordon KB, Fakharzadeh S ym. Long-term...»167. Antikropparna leder till att läkemedelshalterna minskar och ofta till att behandlingseffekten försämras, men inte till biverkningar (med undantag av infusionsreaktioner vid infliximabbehandling) «Hsu L, Snodgrass BT, Armstrong AW. Antidrug antibo...»168.
- Att kombinera metotrexat med IL-17- och IL-23-hämmare rekommenderas inte.
| Screeningprov före behandlingen | Fullständig blodbild, ALAT, kreatinin, sänka, CRP, U-screening Undersökning med tanke på eventuell latent tuberkulos: thorax-röntgen, Tb-INFg/IGRA-test HIV- och hepatitantikroppar (HbsAg, HBcAb, vid behov HBcAbM, HCVAb) Kärnantikroppar enligt övervägande Tandläkarundersökning för konstaterande av eventuella infektionshärdar (eventuellt ortopantomografi) Kontroll av vaccinationerna |
| Prov under behandlingen* | Fullständig blodbild, ALAT och kreatinin en månad efter inledd behandling och därefter enligt individuell bedömning, t.ex. med 3–12 månaders intervall |
| Prov för uppföljning av terapisvaret | Vid behandling av psoriasisartrit CRP och sänka i samband med läkarbesök eller enligt individuell bedömning |
| * Alla nämnda uppföljningsprov behöver inte nödvändigtvis tas av varje patient, utan behovet och omfattningen av laboratorietest bedöms individuellt. Under behandling med IL-17- och Il-23-hämmare behövs inga uppföljningsprov. | |
Användning av biologiska läkemedel vid hudpsoriasis
- Indikationer:
- svår plackpsoriasis (PASI, BSA eller DLQI över 10) hos vuxna som inte svarat på primära systemiska behandlingar och UV-ljusbehandlingar eller för vilka dessa behandlingar är kontraindicerade eller olämpliga (inklusive metotrexat eller ciklosporin på vanliga behandlingsdoser)
- Särskilda indikationer är
- svår och svårbehandlad erytrodermisk eller pustulös psoriasis
- psoriasis i särskilda hudområden (t.ex. handflator och fotsulor) som hotar leda till eller har lett till arbetsoförmåga eller betydande försämring av livskvaliteten.
- Vid behandling av psoriasis hos barn används adalimumab, etanercept och ustekinumab
(tabell «Biologiska läkemedel för behandling av hudpsoriasis hos barn...»9).
- Etanercept och ustekinumab kan vara effektiva för behandling av psoriasis hos barn «Etanersepti ja ustekinumabi saattavat olla tehokkaita lasten ihopsoriaasin hoidossa.»C.
- Då biologisk läkemedelsbehandling påbörjas, ges patienten grundlig handledning (se «Biologisen pistoslääkkeen hoidon ohjaus»10) och blanketten Biologisen lääkehoidon alkukartoitus (Inledande kartläggning av biologisk läkemedelsbehandling) «hoi50062e.pdf»4 gås igenom. Se även tabell «Detta bör beaktas vid biologisk läkemedelsbehandling...»8. Detta bör beaktas vid biologisk läkemedelsbehandling.
- Biosimilarer som beviljats försäljningstillstånd motsvarar referensläkemedlet vad gäller effekt och säkerhet. Se Fimeas anvisning «http://www.fimea.fi/laaketurvallisuus_ja_tieto/biosimilaarit/fimean-kanta-biosimilaarien-vaihtokelpoisuuteen»18.
| Läkemedel | Åldersgräns | Dosering |
|---|---|---|
| adalimumab | ≥ 4-år | 0,8 mg/kg (högst 40 mg) s.c. en gång i veckan 2 doser och därefter med 2 veckors intervall |
| etanercept | ≥ 6-år | 0,8 mg/kg (högst 50 mg) s.c. en gång i veckan |
| ustekinumab | ≥ 6-år | För personer som väger < 60 kg 0,75 mg/kg, 60–100 kg 45 mg och > 100 kg 90 mg s.c. vecka 0, 4 och därefter med 12 veckors intervall |
Biverkningar i samband med användning av biologiska läkemedel för psoriasis
- Ökad infektionsrisk:
- Användning av alla biologiska läkemedel, särskilt TNF-hämmare, är associerad med en
risk för infektioner. I fråga om psoriasisartrit ska också effekten av de reguljära
reumatiska läkemedlen och kortikosteroider beaktas «Germano V, Cattaruzza MS, Osborn J ym. Infection r...»169.
- Infektionsfebern kan utebli och symtomen kan vara lindrigare än vanligt.
- Det har visat sig att risken för allvarliga infektioner vid behandling av patienter
med ledgångsreumatism med TNF-hämmare är cirka 20 % större än för patienter som tar
traditionella syntetiska antireumatiska läkemedel «Galloway JB, Hyrich KL, Mercer LK ym. Anti-TNF the...»170. Resultatet kan dock inte tillämpas direkt på behandling av psoriasis «García-Doval I, Hernández MV, Vanaclocha F ym. Sho...»171.
- En metaanalys av kortvariga randomiserade placebokontrollerade läkemedelsprövningar visar ingen förhöjd risk för allvarliga infektioner «Yiu ZZN, Exton LS, Jabbar-Lopez Z ym. Risk of Seri...»172, men i en del av de långvariga registerstudierna har detta nog påvisats, särskilt för infliximab och adalimumab «Yiu ZZN, Exton LS, Jabbar-Lopez Z ym. Risk of Seri...»172, «Dávila-Seijo P, Dauden E, Descalzo MA ym. Infectio...»173, «Garcia-Doval I, Cohen AD, Cazzaniga S ym. Risk of ...»174, «Reich K, Mrowietz U, Radtke MA ym. Drug safety of ...»175, «Gniadecki R, Bang B, Bryld LE ym. Comparison of lo...»176
- Användning av ustekinumab är förenad med en lägre risk för allvarliga infektioner än användning av TNF-hämmare «Papp K, Gottlieb AB, Naldi L ym. Safety Surveillan...»177.
- Det finns inga rapporter om att användning av IL-23-hämmare skulle vara förknippad med en ökad risk för allvarliga infektioner «Crowley JJ, Warren RB, Cather JC. Safety of select...»178.
- Användning av IL-17-hämmare är förknippad med en ökad risk för jästinfektion i slemhinnorna, eventuellt med en ökad risk för urinvägsinfektion hos kvinnor «Sahuquillo-Torralba A, Carretero G, Rivera R ym. T...»179 och, beroende på preparat, med en varierande risk för exacerbation eller utbrott av inflammatoriska tarmsjukdomar.
- Användning av alla biologiska läkemedel, särskilt TNF-hämmare, är associerad med en
risk för infektioner. I fråga om psoriasisartrit ska också effekten av de reguljära
reumatiska läkemedlen och kortikosteroider beaktas «Germano V, Cattaruzza MS, Osborn J ym. Infection r...»169.
- Latent tuberkulos som aktiveras av TNF-hämmare framträder vanligen under det första
behandlingshalvåret.
- Med lämplig screening är risken liten.
- Hudcancer (basalcells- och skivepitelcellscancer):
- För TNF-hämmare är risken eventuellt något förhöjd «Mariette X, Matucci-Cerinic M, Pavelka K ym. Malig...»180, «van Lümig PP, Driessen RJ, Berends MA ym. Safety o...»181, «Raaschou P, Simard JF, Asker Hagelberg C ym. Rheum...»182. Risken kan också höjas av riklig UV-exponering och andra tidigare immunsuppressiva behandlingar.
- Övriga cancerformer:
- Svår psoriasis medför en lindrigt förhöjd risk för lymfom «Vaikeaan psoriaasiin näyttää liittyvän lievästi kohonnut lymfoomariski.»B. TNF-hämmare kan höja risken en aning, men detta har inte belagts vetenskapligt med säkerhet «Mariette X, Matucci-Cerinic M, Pavelka K ym. Malig...»180, «van Lümig PP, Driessen RJ, Berends MA ym. Safety o...»181.
- Risken för melanom kan öka något hos patienter på TNF-hämmare «Raaschou P, Simard JF, Holmqvist M ym. Rheumatoid ...»183, «Nyboe Andersen N, Pasternak B, Basit S ym. Associa...»184.
- Förekomsten av fasta tumörer har inte ökat.
Läkemedelspreparat
- En jämförelse av biologiska läkemedel som används vid hudpsoriasis finns i tabellerna «Jämförelse av biologiska läkemedel vid hudpsoriasis: TNF-hämmare och ustekinumab...»13 och «Jämförelse av biologiska läkemedel vid hudpsoriasis: IL-17- och IL-23-hämmare...»14.
- Adalimumab (tabell «TNF-hämmare: genomförande och biverkningar...»10):
- Adalimumab är ett effektivt läkemedel för induktionsbehandling av plackpsoriasis hos
vuxna.
- I kliniska läkemedelsprövningar uppnådde 53–80 % av patienterna med svår plackpsoriasis ett gott terapisvar vid 12–16 veckors behandling, men i klinikmaterial har också svagare responser beskrivits «Adalimumabilla saavutetaan hyvä hoitoteho läiskäpsoriaasin induktiohoidossa lumehoitoon verrattuna.»A.
- 45–50 % av patienterna fick utmärkt terapisvar (PASI-90) vid 16 veckors behandling och 17–24% av patienterna fick fullständigt terapisvar (PASI-100) «Adalimumabilla saavutetaan hyvä hoitoteho läiskäpsoriaasin induktiohoidossa lumehoitoon verrattuna.»A.
- Läkemedlet har oftast effekt också då psoriasisen är terapiresistent mot andra TNF-hämmare «Papoutsaki M, Chimenti MS, Costanzo A ym. Adalimum...»185, «Van Lümig PP, Lecluse LL, Driessen RJ ym. Switchin...»186, «Woolf RT, Smith CH, Robertson K ym. Switching to a...»187, «Strober BE, Poulin Y, Kerdel FA ym. Switching to a...»188, «Ortonne JP, Chimenti S, Reich K ym. Efficacy and s...»189.
- Om behandlingen avslutas eller om behandlingsuppehåll görs, leder det inte till någon
snabb försämring av hudpsoriasisen och därför kan behandlingen ges intermittent.
- Efter behandlingen återkommer sjukdomen långsamt under flera månaders tid «Papp K, Crowley J, Ortonne JP ym. Adalimumab for m...»190.
- Återupptagen behandling efter ett kort behandlingsuppehåll har samma effekt som tidigare, d.v.s. hos cirka 70 % av patienterna, men om relapsen har framskridit långt, kan behandlingseffekten bli sämre «Papp K, Crowley J, Ortonne JP ym. Adalimumab for m...»190.
- Uppehåll i behandlingen ökar risken för uppkomsten av antikroppar mot läkemedlet «Chiu HY, Wang TS, Chan CC ym. Risk Factor Analysis...»191.
- Under långtidsbehandling bibehålls terapisvaret relativt väl «Adalimumabilla 16 viikon induktiohoidossa saavutettu hoitovaste säilyy kohtalaisen hyvin pitkäaikaishoidossa, mutta osa potilaista tarvitsee ajoittain hoitoannoksen nostoa tai annosvälin tihentämistä tai yhdistelmähoitoa.»B, men en del patienter behöver en tillfällig doshöjning eller annan behandling (tabell
«Jämförelse av biologiska läkemedel vid hudpsoriasis: TNF-hämmare och ustekinumab...»13 Jämförelse av biologiska läkemedel vid hudpsoriasis).
- Den viktigaste orsaken till förlust av behandlingseffekt är neutraliserande antikroppar som uppkommer mot adalimumab. Detta kan förhindras eller reduceras genom samtidig användning av metotrexat «Hsu L, Snodgrass BT, Armstrong AW. Antidrug antibo...»168.
- Behandling med adalimumab kan kombineras med andra behandlingar, men forskningsdata kring ämnet har tills vidare varit knappt, förutom när det gäller metotrexat «Thaçi D, Ortonne JP, Chimenti S ym. A phase IIIb, ...»192, «Bagel J. Adalimumab plus narrowband ultraviolet B ...»193, «Wolf P, Hofer A, Weger W ym. 311 nm ultraviolet B-...»194, «Heiberg MS, Koldingsnes W, Mikkelsen K ym. The com...»195.
- Adalimumab är ett effektivt läkemedel för induktionsbehandling av plackpsoriasis hos
vuxna.
| Läkemedel* | Typisk dos vid hudpsoriasis | Typisk dos vid psoriasisartrit | Olägenheter |
|---|---|---|---|
| Adalimumab | Startdos 80 mg, därefter 40 mg varannan vecka. Kan höjas till 80 mg varannan vecka om behandlingseffekten försvagas | 40 mg varannan vecka s.c | Lindriga hudreaktioner vid injektionsställena, ökad infektionskänslighet och leukopeni |
| Etanercept | 50 mg två gånger i veckan under 3 månader och därefter 50 mg en gång i veckan | 50 mg en gång i veckan s.c | Lindriga hudreaktioner vid injektionsställena, ökad infektionskänslighet och leukopeni |
| Golimumab | - | 50 mg en gång i månaden s.c. För personer som väger över 100 kg 100 mg en gång i månaden | Lindriga hudreaktioner vid injektionsställena, ökad infektionskänslighet |
| Infliximab(1) | 5 mg/kg vecka 0, 2 och 6, därefter med 8 veckors intervall i.v. Beroende på den kliniska situationen kan infusionsintervallet och -dosen ändras | 3–5 mg/kg vecka 0, 2 och 6, därefter med 8 veckors intervall i.v. Beroende på den kliniska situationen kan infusionsintervallet och -dosen ändras | Infusionsreaktioner, anafylaxi, ökad infektionskänslighet och eventuell förhöjning av leverenzymvärdena |
| Certolizumab | Startdos 400 mg (2 injektioner) s.c. vecka 0, 2 och 4, därefter 200 mg med två veckors intervall. | Som vid hudpsoriasis | Lindriga hudreaktioner vid injektionsställena, ökad infektionskänslighet |
| * Metotrexat är en användbar kombination för alla behandlingar med TNF-hämmare. (1)Det finns också ett inflixamidpreparat som doseras s.c. Dess effekt på psoriasis och psoriasisartrit har inte påvisats i direkta studier. Det subkutana preparatets likvärdighet i jämförelse med i.v.-preparatet med doseringen 120 mg varannan vecka har påvisats hos patienter med inflammatorisk tarmsjukdom (farmakokinetik) och reumatoid artrit (klinisk effekt) i två RCT-studier «Schreiber S, Ben-Horin S, Leszczyszyn J ym. Random...»196, «Westhovens R, Wiland P, Zawadzki M ym. Efficacy, p...»197. |
|||
- Bimekizumab «IL-17-hämmare: genomförande och biverkningar ...»11:
- Bimekizumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Subcutaneous bimekizumab treatment at the dose of 320 mg monthly increases the proportion of patients with plaque psoriasis achieving the PASI90 and IGA 0/1 responses at week 16 when compared to placebo (PASI90 approximately 85–91 % vs. 1–5 % and IGA 0/1 84–93 % vs.»A.
- I två 16 veckors placebokontrollerade läkemedelsprövningar «Gordon KB, Foley P, Krueger JG ym. Bimekizumab eff...»198, «Reich K, Papp KA, Blauvelt A ym. Bimekizumab versu...»199 och i två 16 veckors läkemedelsprövningar med aktivt jämförelseläkemedel «Reich K, Warren RB, Lebwohl M ym. Bimekizumab vers...»200, «Warren RB, Blauvelt A, Bagel J ym. Bimekizumab ver...»201 uppnåddes gott terapisvar (PASI-75) hos 92–95 % (placebo 2,3–7,2 %), utmärkt (PASI-90) hos 85–91 % (placebo 1–5 %) och fullständigt (PASI-100) terapisvar hos 59–68 % (placebo 0–1 %) av patienterna.
- Det förefaller som om terapisvaret bibehålls väl under fortsatt behandling som sträcker
sig till 48–56 veckor med dosen 320 mg med 8 veckors intervall.
- PASI-90- och PASI-100-responsen var 82–86 % respektive 66–70 % «Reich K, Warren RB, Lebwohl M ym. Bimekizumab vers...»200, «Warren RB, Blauvelt A, Bagel J ym. Bimekizumab ver...»201.
- Om behandlingen avslutas eller avbryts, leder det inte till någon snabb försämring
av hudpsoriasisen och därför kan behandlingen vid behov också ges intermittent «Gordon KB, Foley P, Krueger JG ym. Bimekizumab eff...»198.
- Kliniska prövningar visar att sjukdomen återkommer cirka 8 månader efter avslutad behandling.
- Hos cirka 88 % av patienterna har behandlingen effekt när den återupptas efter ett uppehåll.
- Enligt produktresumén har man funnit att cirka 45 % av patienterna utvecklar läkemedelsantikroppar, varav en tredjedel är neutraliserande, men de har inte konstaterats påverka behandlingsresultaten eller associationen med biverkningar.
- Bimekizumab verkar vara säkert enligt en 60 veckors uppföljningsundersökning «Blauvelt A, Papp KA, Merola JF ym. Bimekizumab for...»202.
- De vanligaste biverkningarna är en ökning av förekomsten av övre luftvägsinfektioner och en ökad risk för candidainfektion i mun och svalg – något som är typiskt för IL-17-hämmare. En risk för dermatofytos föreligger också.
- Som kontraindikation betraktas kliniskt betydande aktiv inflammation och överkänslighet mot det verksamma ämnet. Bimekizumab rekommenderas inte för patienter med inflammatorisk tarmsjukdom. Om patienten utvecklar symtom och fynd på inflammatorisk tarmsjukdom eller om patienten redan har en inflammatorisk tarmsjukdom som förvärras, ska behandlingen med bimekizumab avslutas och lämplig behandling inledas.
- Bimekizumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Subcutaneous bimekizumab treatment at the dose of 320 mg monthly increases the proportion of patients with plaque psoriasis achieving the PASI90 and IGA 0/1 responses at week 16 when compared to placebo (PASI90 approximately 85–91 % vs. 1–5 % and IGA 0/1 84–93 % vs.»A.
- Brodalumab «IL-17-hämmare: genomförande och biverkningar ...»11:
- Brodalumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Brodalumab at dose of 210 mg, when compared to placebo, increases the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment. The safety profile of brodalumad may be equal to placebo after 12 weeks treatment.»B.
- I tre 12 veckors placebokontrollerade undersökningar uppnådde 83–86 % (placebo 2,7–8 %) av patienterna ett gott terapisvar (PASI-75), 70–73,3 % (placebo 0,1–3,2 %) ett utmärkt terapisvar (PASI-90) och 37–44 % (placebo 0,3–1 %) fullständigt terapisvar (PASI-100) «Papp KA, Reich K, Paul C ym. A prospective phase I...»203, «Lebwohl M, Strober B, Menter A ym. Phase 3 Studies...»204.
- Behandlingseffekten förefaller att bibehållas under fortsatt behandling i 52 veckor.
- Responsen PASI-75-/PASI-90-/PASI-100 hos patienter som fått en konstant dos på 210 mg enligt försäljningstillståndet var 80 %/73–75 %/53–56 % «Lebwohl M, Strober B, Menter A ym. Phase 3 Studies...»204.
- Antikroppar konstaterades vid testning hos 1,8–2,3 % av patienterna, men förekomsten av antikroppar påverkade inte behandlingsresultaten och var inte associerad med biverkningar.
- Enligt läkemedelsprövningar på 52 veckor förefaller brodalumab vara säkert. Vanliga biverkningar är ökad förekomst övre luftvägsinfektioner samt en ökad risk för jäst- och dermatofytinfektioner, vilket är typiskt för IL-17-hämmare. Crohns sjukdom betraktas som kontraindikation. I USA är användningen av läkemedlet förknippad med en varning för eventuellt förhöjd suicidbenägenhet och tillhörande uppföljning, men Europeiska läkemedelsmyndigheten har ingen sådan varning. Om patienten under behandlingen får ångest- eller depressionssymtom eller om de försvåras under behandlingen, ska behandlingen avbrytas.
- Brodalumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Brodalumab at dose of 210 mg, when compared to placebo, increases the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment. The safety profile of brodalumad may be equal to placebo after 12 weeks treatment.»B.
| Läkemedel | Dos vid hudpsoriasis | Dos vid psoriasisartrit | Olägenheter |
|---|---|---|---|
| Bimekizumab | 320 mg med 4 veckors intervall fram till vecka 16, därefter var 8:e vecka. | 160 mg var fjärde vecka. Vid samtidig medelsvår eller svår plackpsoriasis är den rekommenderade dosen densamma som vid behandling av plackpsoriasis. Efter 16 veckor ges medicineringen var 8:e vecka. Ifall behandlingsresponsen inte går att upprätthålla efter detta kan man överväga att återvända till dosen 160 mg var 4:e vecka. | Övre luftvägsinfektioner Jäst- och dermatofytosinfektioner Risk för uppkomst eller exacerbation av inflammatorisk tarmsjukdom |
| Brodalumab | 210 mg under veckorna 0, 1 och 2 och därefter varannan vecka | - | Lindriga hudreaktioner vid injektionsställena Övre luftvägsinfektioner Jäst- och dermatofytosinfektioner Leukopeni |
| Ixekizumab | Startdos 160 mg, därefter 80 mg med två veckors intervall fram till vecka 12, därefter 80 mg med 4 veckors intervall | Samma som vid hudpsoriasis | Lindriga hudreaktioner vid injektionsställena Övre luftvägsinfektioner Jäst- och dermatofytinfektioner |
| Sekukinumab | 300 mg under veckorna 0, 1, 2, 3 och 4, därefter 300 mg en gång i månaden | Samma dos som vid hudpsoriasis om psoriasisartrit är förknippad med svår hudpsoriasis eller om TNF-hämmare inte har gett ett tillräckligt terapisvar. I övriga fall samma behandlingsschema med engångsdoser på 150 mg | Övre luftvägsinfektioner Jäst- och dermatofytinfektioner |
- Etanercept «TNF-hämmare: genomförande och biverkningar...»10:
- Etanercept är ett effektivt läkemedel för induktionsbehandling av plackpsoriasis hos
vuxna.
- Beroende på dos uppnår 32–55 % av de vuxna patienterna ett gott terapisvar efter 12 veckors behandling och 56–71 % efter 24 veckors behandling «Hyvän hoitovasteen etanerseptilla saavuttaa annoksesta riippuen 12 viikon hoidossa vähintään kolmannes ja 24 viikon hoidossa vähintään puolet potilaista.»A.
- Läkemedlet lämpar sig särskilt väl för patienter som kan behöva avbrott i behandlingen och för patienter med aktiv psoriasisartrit.
- Om behandlingen inleds med 50 mg två gånger i veckan rekommenderas dosreduktion efter
12 veckor till 50 mg en gång i veckan.
- Effekten påverkas inte av dosreduktionen «Papp KA, Tyring S, Lahfa M ym. A global phase III ...»205.
- Terapisvaret visar sig långsammare än vid användning av monoklonala antikroppar.
- Om behandlingen avslutas eller avbryts leder detta inte till någon snabb försämring
av hudpsoriasis, och därför kan behandlingen kan också ges intermittent.
- Hos cirka 80 % av patienterna har behandlingen nästan samma effekt som tidigare när den återupptas efter ett avbrott «Gordon KB, Gottlieb AB, Leonardi CL ym. Clinical r...»206, «Moore A, Gordon KB, Kang S ym. A randomized, open-...»207, «Ortonne J, Griffiths C, Daudén Ey. Efficacy and sa...»208, «Ortonne JP, Taïeb A, Ormerod AD ym. Patients with ...»209.
- Sjukdomen återkommer (relaps, se tabell «Definitioner associerade med terapisvaret för patienter med hudpsoriasis , ...»1) cirka 3 månader efter att behandlingen avslutats «Gordon KB, Gottlieb AB, Leonardi CL ym. Clinical r...»206.
- Vid långtidsbehandling bibehålls terapisvaret relativt väl, men en del patienter behöver tidvis eller kontinuerligt en större behandlingsdos eller tilläggsbehandling «Etanerseptilla 24 viikon induktiohoidossa saavutettu hoitovaste säilyy kohtalaisen hyvin pitkäaikaishoidossa, mutta osa potilaista tarvitsee ajoittain tai jatkuvasti yhdistelmähoitoa tai hoitoannoksen nostoa.»B.
- Etanerceptbehandling kan kombineras med andra behandlingar, men hittills har antalet
publicerade forskningsrapporter om detta varit liten «Foley PA, Quirk C, Sullivan JR ym. Combining etane...»210.
- Om patienten vid inledningen av etanerceptbehandlingen sedan tidigare använder metotrexat utan tillräckligt terapisvar, får etanercept bättre effekt om metotrexatbehandlingen fortsätter parallellt med etanercept «Zachariae C, Mørk NJ, Reunala T ym. The combinatio...»211, «Gottlieb AB, Langley RG, Strober BE ym. A randomiz...»212.
- Etanercept är ett effektivt läkemedel för induktionsbehandling av plackpsoriasis hos
vuxna.
- Guselkumab «IL-12/23- och IL-23-hämmare: genomförande och biverkningar...»12:
- Guselkumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Guselkumab treatment when compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment.»B.
- I en 16 veckors placebokontrollerad läkemedelsprövning nådde 86,3–91,2 % (placebo 5,7–8,1%) av patienterna gott terapisvar (PASI-75), 70–73,3 % (placebo 2,4–2,9 %) utmärkt terapisvar (PASI-90) och 34,1–37,4 % (placebo 0,6–0,8 %) fullständigt terapisvar (PASI-100) «Blauvelt A, Papp KA, Griffiths CE ym. Efficacy and...»213, «Reich K, Armstrong AW, Foley P ym. Efficacy and sa...»214.
- Behandlingseffekten ser ut att förbli god vid fortsatt behandling under 48 veckor.
- Responsen PASI-75-/PASI-90-/PASI-100 hos personer som fått en konstant dos på 100 mg (såsom försäljningstillståndet föreskriver) var 87,8 %/76,3 %/47,4 % «Reich K, Armstrong AW, Foley P ym. Efficacy and sa...»214.
- Färre än 6 % av patienterna utvecklade antikroppar, 7 % var neutraliserande. Det förelåg inget samband med behandlingsresultat eller biverkningar.
- Enligt resultaten av undersökningar på 48 veckor verkar guselkumab vara säkert. Bland de vanliga biverkningarna fanns en ökad förekomst av övre luftvägsinfektioner.
- Guselkumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Guselkumab treatment when compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment.»B.
| Läkemedel | Dos vid hudpsoriasis | Dos vid psoriasisartrit | Olägenheter | Effektmål |
|---|---|---|---|---|
| Guselkumab | 100 mg under vecka 0 och 4 och därefter med 8 veckors intervall | Samma som vi hudpsoriasis. Vid svår psoriasisartrit kan underhållsdosen ges tätare: med 4 veckors intervall | Ökad benägenhet för övre luftvägsinfektioner | IL-23 |
| Risankizumab | 150 mg under vecka 0 och 4 och därefter med 12 veckors intervall | Samma som vi hudpsoriasis. | Ökad benägenhet för övre luftvägsinfektioner | IL-23 |
| Tildrakizumab | 100 mg under vecka 0 och 4 och därefter med 12 veckors intervall | - | Lindriga hudreaktioner på injektionsställena Ökad benägenhet för övre luftvägsinfektioner Leukopeni |
IL-23 |
| Ustekinumab | 45 mg (för personer som väger över 100 kg 90 mg) under vecka 0 och 4 och därefter med 12 veckors intervall | Samma som vid hudpsoriasis | Hudreaktioner vid injektionsställena Ökad benägenhet för övre luftvägsinfektioner |
IL-12/23 |
- Ixekizumab «IL-17-hämmare: genomförande och biverkningar ...»11:
- Ixekizumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Ixekizumab treatment at the dose of 80 mg, when compared to placebo, increases the proportion of patients with active skin psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment.»A.
- I 12 veckors placebokontrollerade läkemedelsprövningar uppnådde 87,3–89,7 % av patienterna gott terapisvar (PASI-75).
- Utmärkt (PASI-90) eller fullständigt (PASI-100) terapisvar uppnås inom 12 veckor av 68,7–70,9 %/ 35,5–40,5 % av patienterna, men det maximala terapisvaret uppnås först vecka 24/36.
- Behandlingseffekten verkar bibehållas väl under minst ett års uppföljning «Iksekitsumabin hoitoteho läiskäpsoriaasiin näyttää säilyvän hyvin vähintään 1 vuoden seurannassa.»C.
- Slutresultaten för dem som följt behandlingsschemat i försäljningstillståndet under hela perioden på 60 veckor var PASI-75: 83 %, PASI-90: 73 % och PASI-100: 55 %.
- Antikroppar mot ixekizumab uppkom hos 9 % av patienterna, men hos endast 1,7 % försvagade detta behandlingseffekten.
- Enligt undersökningsresultaten av 60 veckors behandling verkar ixekizumab säkert «Iksekitsumabin hoitoteho läiskäpsoriaasiin näyttää säilyvän hyvin vähintään 1 vuoden seurannassa.»C.
- Hudreaktioner vid injektionsstället är mycket vanliga (17 %).
- Övre luftvägsinfektioner förekommer oftare än vanligt. Antalet jästinfektioner i slemhinnorna ökar på samma sätt som för alla läkemedel som riktas mot IL-17.
- Ixekizumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Ixekizumab treatment at the dose of 80 mg, when compared to placebo, increases the proportion of patients with active skin psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment.»A.
- Infliximab «IL-17-hämmare: genomförande och biverkningar ...»11:
- Infliximabbehandling rekommenderas om psoriasisen är instabil, erytrodermisk eller pustulös.
- Infliximab är effektivt för induktionsbehandling av hudpsoriasis.
- Ett gott terapisvar uppnås hos cirka 80 % av patienterna som har kronisk plackpsoriasis «Infliksimabi on tehokas ja nopeavaikutteinen vaikean läiskäpsoriaasin induktiohoidossa.»A.
- Responsen är snabb: maximal respons uppnås inom 10 veckor.
- Infliximab bibehåller god behandlingseffekt i upp till ett halvt år och ganska väl i upp till ett år «Infliksimabin hyvä hoitoteho säilyy hyvin puoleen vuoteen asti ja melko hyvin vuoteen asti.»A.
- Avbrott i behandlingen rekommenderas inte, eftersom risken för anafylaxi ökar och behandlingseffekten försämras om behandlingen återupptas «Infliksimabihoitoa ei suositella tauotettavaksi, koska uudelleenaloituksiin näyttää liittyvän suurentunut anafylaksiariski sekä tehon heikkeneminen.»B. Då behandlingen återupptas rekommenderas långsammare infusion och eventuell premedicinering med 100–200 mg hydrokortison intravenöst eller 40 mg metylprednisolon intravenöst, 1 g paracetamol och antihistamin «Lecluse LL, Piskin G, Mekkes JR ym. Review and exp...»215.
- Risankizumab «IL-12/23- och IL-23-hämmare: genomförande och biverkningar...»12:
- Risankizumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Risankizumab treatment when compared to placebo, increases the proportion of patients moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 16 weeks of treatment. The safety profile of risankizumab seems to be equal to placebo after 16 weeks treatment.»B.
- I 16 veckors placebokontrollerade undersökningar uppnådde 74,8–75,3 % (placebo 2–4,9 %) av patienterna utmärkt terapisvar (PASI-90) och 35,9–50,7 % (placebo 0–2 %) av patienterna fullständigt terapisvar (PASI-100) «Gordon KB, Strober B, Lebwohl M ym. Efficacy and s...»216.
- Behandlingseffekten ser ut att förbli god vid fortsatt behandling under 52 veckor.
- Responsen PASI-75-/PASI-90-/PASI-100 hos personer som fått den konstanta dosen 150 mg som föreskrivs i försäljningstillståndet var 92 %/80,6–81,9 %/56,3–59,5 % «Gordon KB, Strober B, Lebwohl M ym. Efficacy and s...»216.
- Enligt undersökningsresultaten av 52 veckors behandling verkar risankizumab säkert. Vanliga biverkningar är ökad förekomst av övre luftvägsinfektioner.
- Risankizumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Risankizumab treatment when compared to placebo, increases the proportion of patients moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 16 weeks of treatment. The safety profile of risankizumab seems to be equal to placebo after 16 weeks treatment.»B.
- Sekukinumab «IL-17-hämmare: genomförande och biverkningar ...»11:
- Sekukinumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Sekukinumabi on tehokas läiskäpsoriaasin induktiohoidossa.»A.
- I 12 veckors placebokontrollerade undersökningar uppnådde 77,1–81,6 % av patienterna gott terapisvar (PASI-75) och den bästa responsen uppnåddes efter 16 veckor, då 86,1–86,7 % av patienterna fick gott terapisvar.
- Efter 16 veckor uppnådde 69,8–72,4 %/36,8–41,6 % av patienterna utmärkt (PASI-90) eller fullständigt (PASI-100) terapisvar.
- Behandlingseffekten verkar förbli god under minst ett års uppföljning «Sekukinumabin hoitoteho läiskäpsoriaasiin näyttää säilyvän hyvin vähintään 1 vuoden seurannassa.»C.
- Hos 81,6–84,3 % av dem som fått ett gott terapisvar vid vecka 12 bibehölls responsen till vecka 52.
- Sekukinumab verkar säkert enligt en undersökning på ett år. De vanligaste biverkningarna är övre luftvägsinfektioner, dessutom förekommer jästinfektioner i slemhinnorna oftare än i genomsnitt vilket är typiskt för IL-17-antikroppar.
- Sekukinumab är effektivt för induktionsbehandling av plackpsoriasis hos vuxna «Sekukinumabi on tehokas läiskäpsoriaasin induktiohoidossa.»A.
- Certolizumab pegol «TNF-hämmare: genomförande och biverkningar...»10:
- Certolizumab pegol är effektivt för induktionsbehandling av plackpsoriasis hos vuxna
«Certolizumab treatment, when compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 16 weeks of treatment. There may be more adverse events in certolizumab pegol treatment compared to placebo after 16 weeks of treatment.»B.
- I 16 veckors placebokontrollerade undersökningar uppnåddes gott terapisvar (PASI-75) med dosen 200 mg/400 mg hos 74,5 %/80,1 % (placebo 7,5 %) av patienterna och utmärkt terapisvar (PASI-90) hos 44,5 %/52,2 % (placebo 1,6 %) av patienterna «Blauvelt A, Reich K, Lebwohl M ym. Certolizumab pe...»217.
- Behandlingseffekten förefaller att bibehållas god vid fortsatt behandling under 48 veckor.
- Med dosen 200 mg/400 mg var PASI-75-responsen 70,7 %/83,6 %, PASI-90-responsen 50,0 %/61,6 % och PASI-100-responsen 28,5 %/34,5 % «Gottlieb AB, Blauvelt A, Thaçi D ym. Certolizumab ...»218.
- Antikroppsbildning mot läkemedlet har rapporterats hos 8–19 % av patienterna, av vilka en del hade neutraliserande antikroppar som minskade läkemedelshalterna och försvagade behandlingseffekten.
- Certolizumab pegol verkar enligt 48 veckors undersökningar vara säkert. Det finns långvarig erfarenhet av behandling av ledgångsreuma och ankyloserande spondylit. Också för behandling av psoriasisartrit har läkemedlet använts i flera år. De vanligaste biverkningarna av certolizumab pegol är ökad förekomst av övre luftvägsinfektioner. Läkemedlet omfattas av de allmänna begränsningarna och riskerna som gäller TNF-hämmare. Läkemedelsmolekylen avviker till sin struktur från alla andra biologiska psoriasisläkemedel och molekylen saknar antikropparnas Fc-del, och därför passerar läkemedlet inte aktivt genom moderkakan till fostercirkulationen.
- Certolizumab pegol är effektivt för induktionsbehandling av plackpsoriasis hos vuxna
«Certolizumab treatment, when compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 16 weeks of treatment. There may be more adverse events in certolizumab pegol treatment compared to placebo after 16 weeks of treatment.»B.
- Tildrakizumab «IL-12/23- och IL-23-hämmare: genomförande och biverkningar...»12:
- Tildrakizumab är effektiv induktionsbehandling för plackpsoriasis hos vuxna «Tildrakizumab, compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis who reach PGA0-1 at 12-16 weeks of treatment. It may be effective in terms of PASI90 and the safety profile may be comparable to placebo at 16 weeks of treatment.»B.
- Med en dos på 100 mg enligt försäljningstillståndet uppnåddes gott terapisvar (PASI-75) hos 62,3 % (placebo 5,6 %), utmärkt terapisvar (PASI-90) hos 35,9% (placebo 2 %) och ett fullständigt terapisvar (PASI-100%) hos 13,2 % (placebo 0,6 %) av patienterna «Papp KA, Reich K, Blauvelt A ym. Efficacy of tildr...»219.
- Effekten av behandlingen ser ut att öka när behandlingen fortsätter, enligt en studie
som sträckte sig till vecka 28.
- Responsen PASI-75/PASI-90/PASI-100 hos dem som fick kontinuerligt den i försäljningstillståndet föreskrivna dosen var 77,4 %/53,6 %/23,1 % «Papp KA, Reich K, Blauvelt A ym. Efficacy of tildr...»219.
- Inga långvariga behandlingsresultat har publicerats.
- På kort sikt verkar tildrakizumab säkert. En vanlig biverkning är en ökad benägenhet för övre luftvägsinfektioner.
- Tildrakizumab är effektiv induktionsbehandling för plackpsoriasis hos vuxna «Tildrakizumab, compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis who reach PGA0-1 at 12-16 weeks of treatment. It may be effective in terms of PASI90 and the safety profile may be comparable to placebo at 16 weeks of treatment.»B.
- Ustekinumab «IL-12/23- och IL-23-hämmare: genomförande och biverkningar...»12:
- Vid 12 veckors behandling enligt dos är terapisvaret gott hos 66–76 % av patienterna och utmärkt hos 37–52 % av patienterna med plackpsoriasis. 70–79 % av patienterna uppnår ett gott terapisvar och 45–56 % av patienterna ett utmärkt terapisvar med 28 veckors behandling «Ustekinumabin vaste ihopsoriaasissa on hyvä ja pitkäkestoinen.»A.
- Responsen är som bäst efter 28 veckor «Leonardi CL, Kimball AB, Papp KA ym. Efficacy and ...»220, «Papp KA, Langley RG, Lebwohl M ym. Efficacy and sa...»221.
- Den goda behandlingseffekten fortsätter under långvarig behandling: 61–79 % av patienterna har fortfarande PASI-75-respons efter 5 år «Ustekinumabin vaste ihopsoriaasissa on hyvä ja pitkäkestoinen.»A.
- Terapisvaret kan vara betydligt bättre hos patienter som är positiva för allelen HLA-C*06 «Talamonti M, Galluzzo M, Chimenti S ym. HLA-C*06 a...»222.
- Infektionsrisken förefaller vara mindre än för TNF-hämmarna «Gniadecki R, Bang B, Bryld LE ym. Comparison of lo...»176, «Leonardi CL, Kimball AB, Papp KA ym. Efficacy and ...»220, «Papp KA, Langley RG, Lebwohl M ym. Efficacy and sa...»221, «Gordon KB, Papp KA, Langley RG ym. Long-term safet...»223, «Warren RB, Smith CH, Yiu ZZN ym. Differential Drug...»224, «Zweegers J, van den Reek JM, van de Kerkhof PC ym....»225, «Menter A, Papp KA, Gooderham M ym. Drug survival o...»226, «Kalb RE, Fiorentino DF, Lebwohl MG ym. Risk of Ser...»227, «Carretero G, Ferrandiz C, Dauden E ym. Risk of adv...»228. Under 5 års uppföljning har inga väsentliga säkerhetsförändringar eller kumulerande biverkningar konstaterats «Lebwohl M, Leonardi C, Griffiths CE ym. Long-term ...»229, «Reich K, Papp KA, Griffiths CE ym. An update on th...»230, «Kimball AB, Papp KA, Wasfi Y ym. Long-term efficac...»231, «Langley RG, Lebwohl M, Krueger GG ym. Long-term ef...»232.
- Enligt flera års uppföljningsundersökningar fortsätter psoriasispatienterna längre på ustekinumab än på TNF-hämmare «Psoriaasipotilaiden hoidossa pysyminen biologisilla lääkkeillä rekisteritutkimuksissa ja muissa pitkän ajan seurantatutkimuksissa»11.
- Angående användning av biologiska läkemedel vid psoriasisartrit, se avsnittet Behandling av psoriasisartrit.
| Läkemedel | Adalimumab | Etanercept | Infliximab | Certolizumab pegol | Ustekinumab |
|---|---|---|---|---|---|
| Typ | human monoklonal antikropp (IgG1/κ) | fusionsprotein löslig receptor | chimerisk monoklonal antikropp (IgG1) | human monoklonal antikropp (IgG1/κ) | human monoklonal antikropp (IgG1/κ) |
| Effektmål | TNF-alfa | TNF-alfa, LT (TNF-beta) | TNF-alfa | TNF-alfa | p40 (IL-12/IL-23) |
| Halveringstid (median) | 14 dygn | 3 dygn | 9 dygn | 14 dygn | 21 dygn |
| Dos | startdos 80 mg, från och med följande vecka 40 mg varannan vecka Vid behov kan dosen höjas till 80 mg varannan vecka | 50 mg i veckan eller under de första 12 veckorna 50 mg två gånger i veckan och därefter en gång i veckan | 5 mg/kg i.v. vecka 0, 2 och 6 och därefter med 8 veckors intervall | startdos 400 mg vecka 0, 2 och 4 och därefter 200 mg varannan vecka Vid behov kan dosen höjas till 400 mg varannan vecka |
45 mg (för personer som väger över 100 kg 90 mg) under vecka 0 och 4 och därefter med 12 veckors intervall |
| Tid till terapisvar «Nast A, Sporbeck B, Rosumeck S ym. Which antipsori...»233 - 25 % PASI-75 |
ganska kort - 4,6 veckor |
lång - 6,6 veckor |
kort - 3,5 veckor |
ganska kort - 4,3 veckor |
ganska lång - 5,1 (4,6) veckor |
| Sannolikheten för terapisvar i slutet av induktionsfasen v. 8–24 vs. placebo RR (95 % KI) «Sbidian E, Chaimani A, Garcia-Doval I ym. Systemic...»236 | |||||
| PASI-75 PASI-90 |
10,05 (8,61–11,73) | 8,09 (7,22–9,06) | 18,02 (11,92–27,22) | 9,61 (7,78–11,88) | 11,04 (9,83–12,40) |
| Sannolikheten för terapisvar % (95 % KI) vid cirka ett års (44–60 veckor) behandling «Armstrong AW, Puig L, Joshi A ym. Comparison of Bi...»235. Siffrorna är inte nödvändigtvis jämförbara eftersom de har erhållits från olika undersökningar. | |||||
| PASI-75 | 67,1 (52,9–78,7) | 55,5 (50,1–60,9) | 58,3 (52,5–63,8) | 72,5 (65,9–78,2) | |
| PASI-90 | 46,2 (38,6–53,9) | 33,4 (28,5–38,7) | 40,1 (30,0–51,1) | 52,4 (47,1–57,7) | |
| Vårdkontinuitet* | ännu inte känt | ||||
| Efter 1 år | 69,0–79,0 % | 70,0–75,8 % | 58,0–68,8 % | 77,2–89,0 % | |
| Efter 2 år | 53,2–67,0 % | 51,0–60,8 % | 30,1–54,2 % | 68,5–82,0 % | |
| Efter 3 år | 41,9–59,0 % | 39,1–56,0 % | 22,6–45,5 % | 61,8–75,6 % | |
| * Vårdkontinuiteten i registerstudier. Se även tilläggsinformation «Psoriaasipotilaiden hoidossa pysyminen biologisilla lääkkeillä rekisteritutkimuksissa ja muissa pitkän ajan seurantatutkimuksissa»11 | |||||
| Läkemedel | Bimekizumab | Brodalumab | Ixekizumab | Sekukinumab | Guselkumab | Risankizumab | Tildrakizumab |
|---|---|---|---|---|---|---|---|
| Typ | humaniserad monoklonal antikropp (IgG1) | human monoklonal antikropp (IgG2) | humaniserad monoklonal antikropp (IgG4) | human monoklonal antikropp (IgG1/κ) | human monoklonal antikropp (IgG1/λ) | humaniserad monoklonal antikropp (IgG1) | humaniserad monoklonal antikropp (IgG1/κ) |
| Effektmål | IL-17A, AF, F | IL-17RA | IL-17A | IL-17A | IL-23 (P19) | IL-23 (P19) | IL-23 (P19) |
| Halveringstid (median) | 23 dygn | 23 dygn | 13 dygn | 27 dygn | 17 dygn | 28 dygn | 23 dygn |
| Dos | 320 mg med 4 veckors intervall till och med vecka 16, därefter med 8 veckors intervall | 210 mg under vecka 0, 1 och 2, därefter varannan vecka | startdos 160 mg, därefter 80 mg med två veckors intervall till och med vecka 12 och därefter 80 mg med 4 veckors intervall | 300 mg under vecka 0, 1, 2, 3 och 4, därefter 300 mg en gång i månaden | 100 mg under vecka 0 och 4, därefter med 8 veckors intervall | 150 mg under vecka 0 och 4, därefter 150 mg med 12 veckors intervall | 100 mg under vecka 0 och 4, därefter med 12 veckors intervall |
| Tid till terapisvar «Nast A, Sporbeck B, Rosumeck S ym. Which antipsori...»233, «Egeberg A, Andersen YMF, Halling-Overgaard AS ym. ...»234 | mycket snabbt | mycket snabbt | mycket snabbt | mycket snabbt | snabbt | snabbt | ganska långsamt |
| - 25 % PASI-75 | - | 2,1 veckor | 2,2 veckor | 3,0 veckor | 3,8 veckor | - | 5,6 veckor |
| - 25 % PASI-90 | - | 3,5 veckor | 4,1 veckor | 5,1 veckor | 6,2 veckor | 6,1 veckor | - |
| Sannolikheten för terapisvar i slutet av induktionsfasen v. 8–24 vs. placebo RR (95% KI) «Sbidian E, Chaimani A, Garcia-Doval I ym. Systemic...»236 | |||||||
| PASI-75 | 18,02 (11,92–27,22) | 12,20 (10,50–14,16) | 14,54 (12,59–16,79) | 12,71 (11,12–14,52) | 12,25 (10,22–14,68) | 13,44 (11,87–15,22) | 10,72 (8,78–13,08) |
| PASI-90 | 58,64 (3,72–923,86) | 23,55 (19,48–28,48) | 32,48 (27,13–38,87) | 25,79 (21,61–30,78) | 25,52 (21,25–30,64) | 28,76 (23,96–34,54) | 18,73 (14,21–24,69) |
| Sannolikheten för terapisvar % (95 % KI) vid cirka ett års (44–60 veckor) behandling «Armstrong AW, Puig L, Joshi A ym. Comparison of Bi...»235. Siffrorna är inte nödvändigtvis jämförbara eftersom de har erhållits från olika undersökningar. | |||||||
| PASI-75 | 80,0 (75,7–83,7) | 85,0 (79,2–89,4) | 88,6 (80,6–93,6) | 88,2 (84,6–91,1) | 90,1 (86,3–92,9) | ||
| PASI-90 | 74,0 (69,3–78,1) | 73,9 (69,9–77,5) | 71,3 (64,2–77,5) | 76,5 (72,1–80,5) | 79,4 (75,5–82,9) | ||
| Vårdkontinuiteten* Efter 1 år Efter 2 år Efter 3 år |
ännu inte känt | ännu inte känt | ännu inte känt | ännu inte känt | ännu inte känt | ännu inte känt | |
| * Vårdkontinuiteten i registerstudier. Se även tilläggsinformation «Psoriaasipotilaiden hoidossa pysyminen biologisilla lääkkeillä rekisteritutkimuksissa ja muissa pitkän ajan seurantatutkimuksissa»11 | |||||||
- Patientens associerade sjukdomar ska beaktas i val av systemiskt läkemedel. Se tabell «gvr00091b.pdf»5 som innehåller vägledande rekommendationer.
Psoriasisartrit
Diagnosen psoriasisartrit
- Diagnosen psoriasisartrit är i huvudsak klinisk. Vi rekommenderar användning av ICD-10-diagnoskoden M07.3*L40.5 då diagnosen psoriasisartrit är säker och diagnoskoden M13.8 vid misstanke om psoriasisartrit.
- Psoriasisartrit ska alltid misstänkas om artrit och hudpsoriasis förekommer samtidigt.
- Hos en liten del av patienterna uppkommer ledsymtomen först och därefter hudsymtomen.
- Om hudpsoriasis inte föreligger, underlättas diagnostiken av
- nagelförändringar typiska för psoriasis
- asymmetrisk artrit
- förekomst av korvfingrar och korvtår
- entesiter
- hudpsoriasis eller psoriasisartrit hos släkting i första ledet.
- Psoriasis hos patienter med artrit utesluter inte möjligheten att det är frågan om någon annan ledsjukdom.
- För klassificering av psoriasisartrit används klassificeringskriterierna CASPAR (Classification
Criteria for Psoriatic Arthritis), som lämpar sig särskilt väl för kliniska undersökningar
«CASPAR (Classification criteria for Psoriatic ARthritis) -kriteerit»12.
- CASPAR kan också användas som stöd för diagnostiken, om patienten har fastställd artrit, spondylartrit eller entesit.
- Vid psoriasisartrit kan följande symtom och fynd förekomma «Gladman DD, Farewell V, Buskila D ym. Reliability ...»237, «Oriente P, Biondi-Oriente C, Scarpa R. Psoriatic a...»238, «Cohen MR, Reda DJ, Clegg DO. Baseline relationship...»239, «Cantini F, Salvarani C, Olivieri I ym. Distal extr...»240
- ömhet i lederna och morgonstelhet
- ledinflammationer
- asymmetriska ledinflammationer i några leder
- inflammation i finger- och tåleder (bilderna «Varpaiden niveltulehdukset psoriartriitissa»50, «Varpaiden niveltulehdukset nivelpsoriaasissa»51, «Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa»52, «Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa»53, «Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa»54, «Sormien kärkijäsenten niveltulehdukset ja lievät kynsimuutokset nivelpsoriaasissa»55, «Sormien kärkinivelten tulehdukset ja kynsimuutokset»56 och «Sormien kärkinivelten tulehdukset ja kynsimuutokset»57)
- polyartrit som påminner om ledgångsreumatism
- inflammation som ofta är associerad med nagelförändringar
- inflammatorisk ryggsmärta (väcker patienten på morgonnatten, lindras genom rörelse
och kan förvärras i vila)
- Smärta kan vara ett tecken på spondylit och sakroilit.
- Till skillnad från klassisk ankyloserande spondylit kan sakroiliten vara unilateral eller saknas. Sjukdomen kan dessutom afficiera halskotpelaren redan tidigt.
- Vävnadsfaktorn HLAB27 är positiv betydligt mera sällan än vid ankyloserande spondylit «Coates LC, Baraliakos X, Blanco FJ ym. The Phenoty...»241.
- Den axiala sjukdomsformen av psoriasisartrit kan debutera i en senare ålder än ankyloserande spondylit «Chandran V. Psoriatic spondylitis or ankylosing sp...»242.
- entesiter (inflammation i fästena för muskelsenor eller ledband)
- Det typiska är inflammationer i synnerhet i akillessenans fästen samt plantar fasciit.
- daktyliter (enskilda korvliknande, svullna fingrar eller tår) (bilderna «Vaikea nivelpsoriaasin makkaramainen turvotus sormessa»58 och «Makkaramainen turvotus varpaassa nivelpsoriaasipotilaalla»59)
- sällan mutilerande inflammation
- unilateralt pittingödem i extremitet (bild «Käden pitting-turvotus vaikeaa nivelpsoriaasia sairastavalla potilaalla»60)
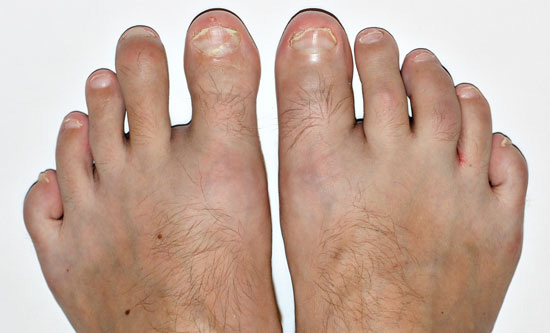
Varpaiden niveltulehdukset psoriartriitissa
© Riitta Luosujärvi
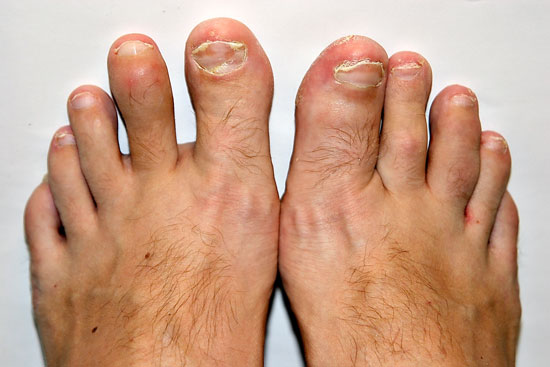
Varpaiden niveltulehdukset nivelpsoriaasissa
© Riitta Luosujärvi
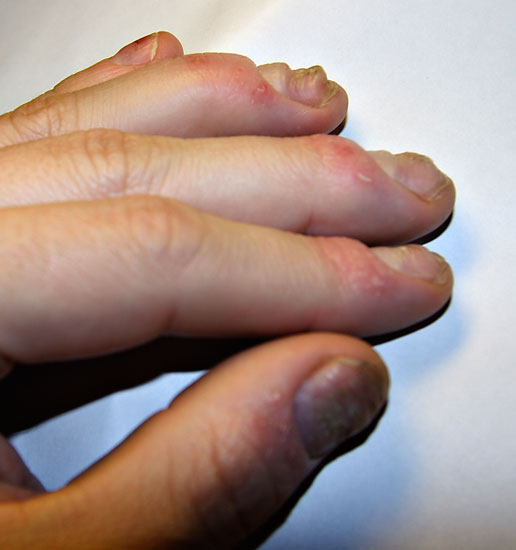
Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa.
Ledinflammationer i de yttersta fingerlederna och nagelförändringar vid ledpsoriasis.
© Riitta Luosujärvi
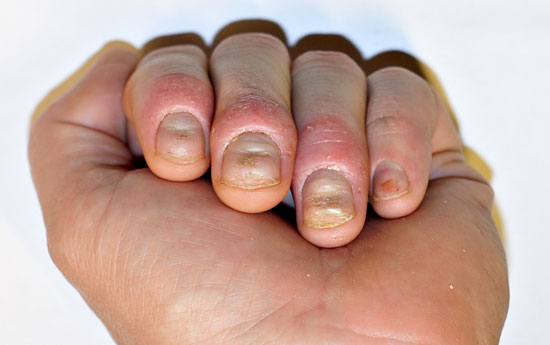
Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa
© Riitta Luosujärvi
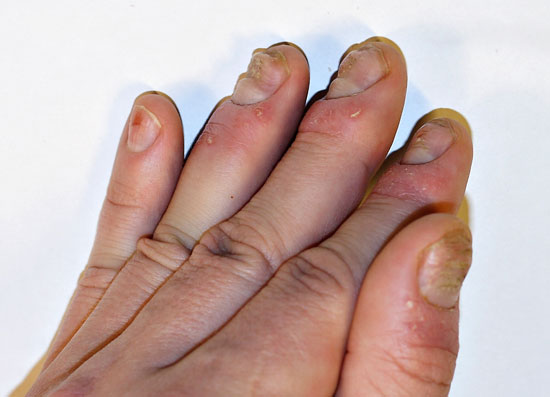
Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa
© Riitta Luosujärvi
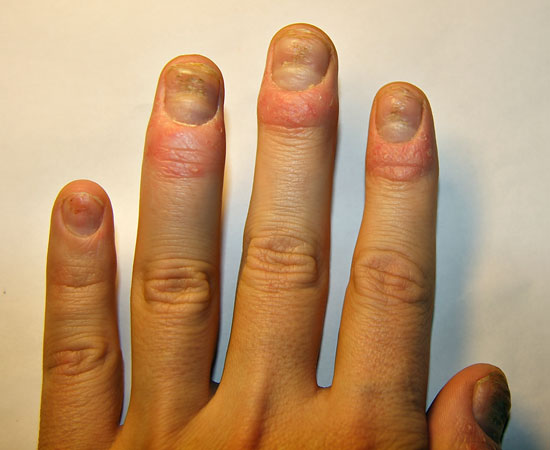
Sormien kärkijäsenten niveltulehdukset ja lievät kynsimuutokset nivelpsoriaasissa
© Riitta Luosujärvi
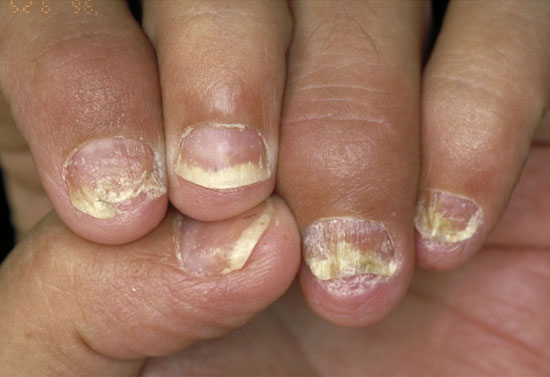
Sormien kärkinivelten tulehdukset ja kynsimuutokset
© Raimo Suhonen
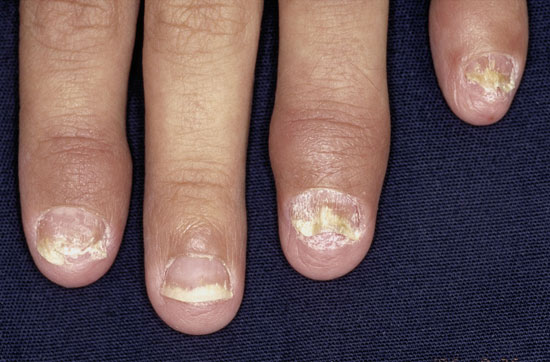
Sormien kärkinivelten tulehdukset ja kynsimuutokset
© Raimo Suhonen
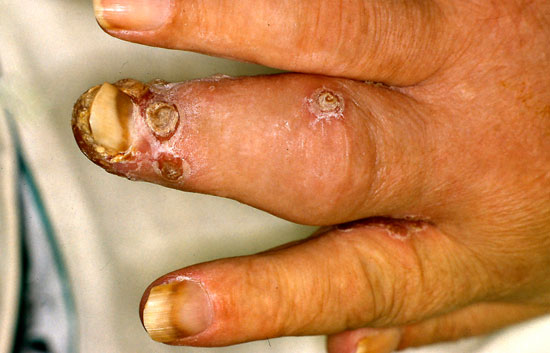
Vaikea nivelpsoriaasin makkaramainen turvotus sormessa
© Riitta Luosujärvi
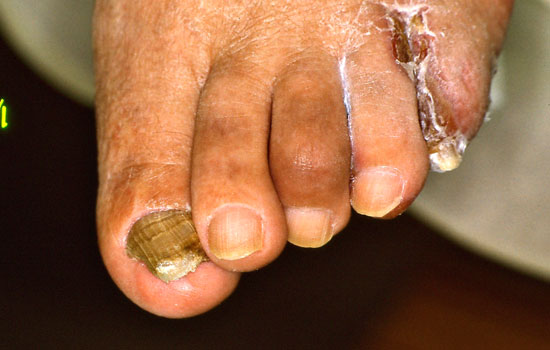
Makkaramainen turvotus varpaassa nivelpsoriaasipotilaalla
© Riitta Luosujärvi
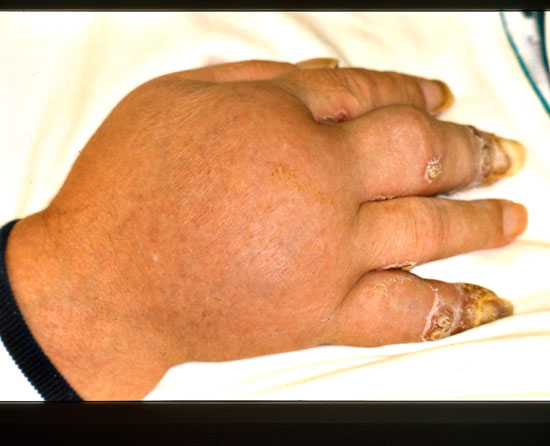
Käden pitting-turvotus vaikeaa nivelpsoriaasia sairastavalla potilaalla
© Riitta Luosujärvi
Laboratoriefynd och bilddiagnostiska fynd
- Laboratorieundersökningar gagnar inte diagnostiken av psoriasisartrit.
- Sänkan och CRP-halten kan vara normala eller förhöjda.
- Reumatoid faktor kan vanligen inte påvisas.
- Hos psoriasispatienterna är prevalensen av reumatoid faktor samma som bland den övriga befolkningen «Gladman DD, Shuckett R, Russell ML ym. Psoriatic a...»28.
- Antikroppar mot citrullinpeptid förekommer hos 6–13 % «Payet J, Goulvestre C, Bialé L ym. Anticyclic citr...»243.
- Nativröntgen:
- Nativröntgen används för diagnostik och uppföljning.
- De radiologiska förändringarna varierar och utvecklas under årens lopp. För mer information se «Nivelpsoriaasin tyypilliset radiologiset muutokset»13.
- De radiologiska förändringarna är ofta asymmetriska.
- Hos samma patient kan flera olika radiologiska förändringar ses samtidigt.
- Ultraljudsundersökning av lederna:
- Kräver förtrogenhet av den som utför undersökningen.
- Med ultraljudsundersökning kan man utöver artrit också se seninflammationer, daktyliter
och entesiter «Kane D. The role of ultrasound in the diagnosis an...»244, «Dubash SR, De Marco G, Wakefield RJ ym. Ultrasound...»245.
- Enligt OMERACT-arbetsgruppens definition från år 2018 gällande ultraljuddiagnostiserad entesit ska en sena vara förtjockad eller lågekogen nära insertionen i benet (< 2 mm från benets cortex). Dessutom behövs en positiv dopplersignal (vid aktiv inflammation) eller strukturell förändring i form av erosion, kortikal entesofyt eller senförkalkning «Balint PV, Terslev L, Aegerter P ym. Reliability o...»246.
- Resultatet av ultraljudsundersökning är inte som enda undersökning diagnostiskt för psoriasisartrit.
- Magnetröntgen:
- För att tolka bilderna krävs förtrogenhet med magnetröntgenundersökningar av stöd- och rörelseorganen.
- Magnetröntgen visar inflammationsförändringar i lederna tidigare än vanlig röntgen «Offidani A, Cellini A, Valeri G ym. Subclinical jo...»247. Beträffande entesiter möjliggör magnetröntgen undersökning av djupare strukturer än ultraljud. Dessutom gör den det möjligt att upptäcka ödem i benvävnaden i anslutning till insertiter.
- För yngre patienter (< 45 år) och för patienter med symtom en kort tid, rekommenderas i första hand magnetröntgen av SI-lederna och ryggraden «Mandl P, Navarro-Compán V, Terslev L ym. EULAR rec...»248.
- Strukturella förändringar orsakade av kronisk inflammation i åratal kan identifieras med nativröntgen.
- Magnetröntgen rekommenderas inte för uppföljning av ledförändringar.
- Vid diagnostik av psoriasis är datortomografi och nukleärmedicinska undersökningar sällan nödvändiga, men de används vid behov för att utesluta andra sjukdomar.
- Se mer information om bilddiagnostik vid psoriasisartrit «Kuvantaminen nivelpsoriaasissa»14.
Psoriasisartritfenotyper och bedömning av inflammationsaktiviteten
- Aktiviteten av psoriasisartrit ska bedömas som en helhet och alla fenotyper ska beaktas «Psoriasisartritfenotyper...»15, «Gossec L, Baraliakos X, Kerschbaumer A ym. EULAR r...»249, «Singh JA, Guyatt G, Ogdie A ym. Special Article: 2...»250, «Coates LC, Kavanaugh A, Mease PJ ym. Group for Res...»251.
- Faktorer som tyder på en sämre prognos indicerar en aktiv behandlingslinje «Faktorer associerade med dålig prognos...»16.
| Muskuloskeletala sjukdomsformer | Hudpsoriasis associerad med psoriasisartrit | Associerade sjukdomar |
|---|---|---|
Perifera artriter:
Axial sjukdom Entesiter Daktyliter |
Eksem Nagelförändringar |
I anknynting till spondylartropati
Andra associerade sjukdomar
|
|
Behandling av psoriasisartrit
- Behandlingen väljs alltid individuellt i samråd med patienten.
- För lyckad behandling krävs god behandlingsföljsamhet av patienten. Följsamheten påverkas i synnerhet av den förväntade effekten, av biverkningarna och av säkerheten hos den valda behandlingsformen. En del faktorer med anknytning till behandlingsprocessen påverkar också behandlingsföljsamheten, såsom läkemedlets administreringsväg, frågan huruvida läkemedlet ges på sjukhus eller om patienten doserar det självständigt och behandlingskostnaderna. Se även ytterligare information «Nivelpsoriaasia sairastavien potilaiden kokemuksia ja näkemyksiä»15.
Målsättningarna för behandlingen
- Målsättningen för behandlingen är att optimera patientens funktionsförmåga och livskvalitet och att förhindra bestående strukturella skador.
- Dessa mål nås lättare om sjukdomsaktiviteten är så låg som möjligt. På grund av sjukdomens heterogenitet är det svårt att både definiera och uppnå fullständig remission, särskilt om fullständig remission betyder fullständig smärtfrihet och lugn hud.
- Tills vidare fastställs låg sjukdomsaktivitet (minimal disease activity, MDA) som ett realistiskt behandlingsmål ("treat-to-target") av internationella behandlingsrekommendationer «Kriterier för låg sjukdomsaktivitet (minimal disease activity, MDA) ....»17.
- Fortfarande är forskningsresultaten knappa gällande nyttan av en behandlingsstrategi
som strävar efter låg sjukdomsaktivitet.
- Enligt undersökningen TICOPA (TIght Control of inflammation in early Psoriatic Arthritis) «Coates LC, Kavanaugh A, Mease PJ ym. Group for Res...»251, som var den första där man eftersträvade låg sjukdomsaktivitet, verkar en större del av patienterna uppnå ACR20- och ACR50-respons med en aktiv behandlingslinje än med traditionell behandling under ett års uppföljning. Vid fem års uppföljning observerades ingen skillnad mellan grupperna längre «Coates LC, Mahmood F, Freeston J ym. Long-term fol...»255.
| Ömma leder (av 68 leder) | ≤ 1 |
| Svullna leder (av 66 leder) | ≤ 1 |
| PASI eller BSA |
≤ 1 ≤ 3 |
| Graden av smärta enligt VAS (0–100 mm) | ≤ 15 |
| VAS för allmänt mående (0–100 mm) | ≤ 20 |
| HAQ | ≤ 0,5 |
| Ömma entesitpunkter (bilateralt enligt lokationspunkterna i Leeds Enthesitis Index) | ≤ 1 |
| MDA anses föreligga då minst 5/7 kriterier uppfylls. | |
| PASI = Psoriasis Area Severity Index (0–72), BSA = Body Surface Area, hur många procent av kroppen täcks av psoriasisutslag, handflateytan motsvarar cirka 1 %, VAS = Visual Analog Scale 0–100 mm, HAQ = Health Assessment Questionnaire | |
- I det kliniska arbetet är det naturligt att sträva efter så god funktionsförmåga, livskvalitet och låg sjukdomsaktivitet som möjligt med beaktande av sjukdomens alla tänkbara fenotyper, patientens läkemedelstolerans och hens associerade sjukdomar.
- Förutom psoriasisartrit ska de associerade sjukdomarna också behandlas aktivt.
- God vård förutsätter systematisk uppföljning av terapisvaret.
Uppföljning av terapisvaret
- Inom specialsjukvården bedöms aktiviteten för alla fenotyper då terapisvaret uppföljs:
- svullnad och ömhet i 66/68 leder
- infektionsvärdena
- patientens helhetsbedömning av sjukdomssituationen och smärtan (VAS 0–100 mm).
- DAPSA (Disease Activity in PSoriatic Arthrits) Score [DAPSA = TJC (tender joint count/antalet ömma leder) + SJC (swollen joint count/antalet svullna leder) + CRP-värdet + sjukdomsaktiviteten på VAS-skalan 0–10 cm + smärtan på VAS-skalan 0–10 cm].
- DAPSA:
- 0–4 = remission
- 5–14 = låg aktivitet
- 15–28 = måttlig aktivitet
- > 28 hög aktivitet.
- Vid axial sjukdom bedöms dessutom
- Ryggradsrörligheten (BASMI)
- BASDAI- och BASFI-enkäter
- Aktivitetsmätaren ASDAS (Ankylosing Spondylitis Disease Activity Score)
- Det finns olika mätare för daktyliter och entesiter. Leeds enthesitis index bedömer exempelvis ömhet på 6 lokationer (insertionerna vid akillessenan på båda sidorna, mediala femurkondylen och laterala humerusepikondyler) «Entesiittien arvioiminen nivelpriaasipotilailla (LEI)»61.
- Svaret på hudpsoriasisbehandlingen kan bedömas enligt en allmän bedömning av läkare eller utifrån en ändring i svårighetsgrad enligt PASI och/eller BSA.
- Bilddiagnostiska undersökningar används enligt klinisk prövning.
Leeds enthesitis indeksissä (LEI) arvioidaan arkuutta molemmin puolin akillesjänteen proksimaalisesta insertiosta, reisiluun sisänivelnastasta ja olkaluun ulkosivunastasta.
© Suomalainen Lääkäriseura Duodecim
Antiinflammatoriska smärtstillande läkemedel
- Smärta försämrar livskvaliteten och funktions- och arbetsförmågan hos patienter med psoriasisartrit. För mer information se «Nivelpsoriaasia sairastavien potilaiden kokemuksia ja näkemyksiä»15.
- Antiinflammatoriska smärtstillande läkemedel är den vanligaste symtomatiska medicineringen vid psoriasisartrit. Enligt klinisk erfarenhet får särskilt personer med axial sjukdom nytta av dem. Behandlingen är ofta långvarig.
- Vid all behandling med antiinflammatoriska smärtstillande läkemedel ska eventuella biverkningar beaktas. Om användning och biverkningar se God medicinsk praxis-rekommendationerna Nivelreuma «Nivelreuma»2 (på finska) och Kipu «Kipu»7 (på finska); Smärta «Smärta»8 (på svenska). Se även diagram Kipulääkkeen valinta (Val av smärtstillande läkemedel) «https://www.terveysportti.fi/xmedia/hoi/hoi50103/Kipulaakkeen_valinta.html»19 i God medicinsk praxis-rekommendationen Kipu; Smärta.
Traditionella syntetiska antireumatiska läkemedel (disease modifying antirheumatic drugs, csDMARD)
- Endast få adekvata behandlingsstudier har gjorts.
- I de äldre studierna har bedömningen av terapisvaret varierat. Antalet patienter i studierna har ofta varit litet och man har inte använt moderna kriterier för bedömning av terapisvar.
- Mer forskningsevidens om läkemedlens effekt behövs.
- Principerna för reumatisk läkemedelsbehandling har behandlats i God medicinsk praxis-rekommendationen om ledgångsreumatism (Nivelreuma «Nivelreuma»2 (på finska)) och på Reumatologisk förenings webbplats «https://www.reumatologinenyhdistys.fi/ohjeet/»12).
- Metotrexat «Detta bör beaktas vid metotrexatbehandling...»4:
- På basis av klinisk erfarenhet är metotrexat primärt och kan vara effektivt vid behandling
av psoriasisartrit; forskningsevidensen är dock fortfarande ringa «Metotreksaatti verrattuna lumeeseen saattaa nivelpsoriaasia sairastavilla lisätä hoitovasteen saavuttamista 6 kuukauden seurannassa (RR 1,76; 95 % luottamusväli 1,14–2,70).»C.
- Jämfört med placebo kan metotrexat eventuell förbättra terapisvaret hos psoriasisartritpatienter under 6 månaders uppföljning (RR 1,76 (95 % konfidensintervall 1,14–2,70)
- Metotrexat har effekt också vid behandling av hudpsoriasis (se avsnittet Behandling av hudpsoriasis, Primära systemiska läkemedel).
- Metotrexat har större biologisk tillgänglighet då det ges som subkutan injektion än oralt «Metotreksaatin hyötyosuus on parempi ihon alle tai lihakseen annosteltuna.»A.
- På basis av klinisk erfarenhet är metotrexat primärt och kan vara effektivt vid behandling
av psoriasisartrit; forskningsevidensen är dock fortfarande ringa «Metotreksaatti verrattuna lumeeseen saattaa nivelpsoriaasia sairastavilla lisätä hoitovasteen saavuttamista 6 kuukauden seurannassa (RR 1,76; 95 % luottamusväli 1,14–2,70).»C.
- Sulfasalazin «Detta bör ska beaktas vid sulfasalazinbehandling...»18:
- Sulfasalazin har svag effekt för behandling av psoriasisartrit «Sulfasalatsiini saattaa olla lumelääkettä tehokkaampi nivelpsoriaasin hoidossa, mutta tutkimusnäyttö siitä on vähäistä.»C, «Dressler C, Eisert L, Pham PA ym. Efficacy and saf...»257.
- Sulfasalazin kan användas ifall metotrexat är kontraindicerat (t.ex. pg.a. graviditet eller planering av graviditet) och sjukdomen är lindrig.
- Sulfasalazin saknar vanligtvis effekt på hudpsoriasis.
- Sulfasalazin har svag effekt för behandling av psoriasisartrit «Sulfasalatsiini saattaa olla lumelääkettä tehokkaampi nivelpsoriaasin hoidossa, mutta tutkimusnäyttö siitä on vähäistä.»C, «Dressler C, Eisert L, Pham PA ym. Efficacy and saf...»257.
- Leflunomid «Detta bör ska beaktas vid leflunomidbehandling...»19:
- I enskilda fall är leflunomid ett användbart läkemedel mot psoriasisartrit «Leflunomidi saattaa olla tehokas ja turvallinen hoitovaihtoehto nivelpsoriaasissa.»C.
- Forskningsevidensen om effekten på hudpsoriasis är dock ringa «Nash P, Thaçi D, Behrens F ym. Leflunomide improve...»258.
- Leflunomid är ett läkemedel med utdragen teratogen verkan.
- Kvinnor som planerar graviditet ska sluta använda leflunomid 2 år innan eller påskynda elimineringen av leflunomid med hjälp av kolestyramin eller medicinskt kol «Flint J, Panchal S, Hurrell A ym. BSR and BHPR gui...»259. Män behöver inte avbryta leflunomidbehandling då paret planerar graviditet «Brent RL. Teratogen update: reproductive risks of ...»260.
- Efter användning av läkemedel för att påskynda elimineringen av leflunomid ska ytterligare 2 bestämningar av leflunomidhalten i plasma göras.
- I enskilda fall är leflunomid ett användbart läkemedel mot psoriasisartrit «Leflunomidi saattaa olla tehokas ja turvallinen hoitovaihtoehto nivelpsoriaasissa.»C.
- Kortikosteroider:
- Kortikosteroidpreparat används vid behov lokalt som intraartikulära injektioner eller i små orala doser (prednison ≤ 7,5 mg/dag) i så korta kurer som möjligt.
- Lokala glukokortikoidinjektioner når bäst fram under ultraljudsstyrning.
- Om systemisk högdoskortikosteroidmedicinering avslutas plötsligt, kan hudpsoriasisen förvärras «Baker H, Ryan TJ. Generalized pustular psoriasis. ...»261, «Burns D, Breathnach S, Cox N ym. Rook´s Textbook o...»262.
- Gällande biverkningar, se God medicinsk praxis-rekommendationen Nivelreuma «Nivelreuma»2 (på finska).
| Rubrik | Bör beaktas |
|---|---|
| Dos | Startdos 500 mg × 2, under de påföljande veckorna ökas dosen till 1 g × 2, vid behov 1 g x 3/dygn |
| Biverkningar | Vanliga: Magbesvär, lindriga symtom i centrala nervsystemet, övergående oligospermi
och försämrad spermiemotilitet efter avslutad behandling Sällsynta: Svårt överkänslighetseksem och allvarliga förändringar i blodbilden |
| Interaktioner | – |
| Kontraindikationer | Allergi mot preparatet Om patienten har allergi mot sulfapreparat är det bäst att inleda exponeringen för sulfasalazin på sjukhus. Mycket höga kärnantikroppstitrar i blodet ökar risken för SLE. |
| Användbar kombination | Folsyratillskott 1–5 mg/dygn under graviditet «Flint J, Panchal S, Hurrell A ym. BSR and BHPR gui...»259 «https://www.terveyskyla.fi/reumatalo»20 |
| Uppföljningsprov* | Liten blodbild (fullständig blodbild), ALAT vecka 3, 6 och 12 och därefter med 3–6
månaders intervall Se även «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 |
| * Alla nämnda uppföljningsprov behöver inte nödvändigtvis tas av varje patient, utan omfattningen bedöms individuellt. | |
| Rubrik | Bör beaktas |
|---|---|
| Dos | 20 mg/dygn |
| Biverkningar | Högt blodtryck, huvudvärk Eksem, håravfall Diarré, illamående Förändringar i levervärdena, minskat antal blodkroppar |
| Interaktioner | Andra lever- och benmärgstoxiska läkemedel som används samtidigt |
| Kontraindikationer | Allergi mot läkemedlet i fråga, svår infektion, funktionsstörning i levern, svårt
bristtillstånd i immunsystemet, betydande funktionsstörning i benmärgen, medelsvår
eller svår funktionsstörning i njurarna Graviditet och amning (se tabell «Patienter med psoriasis och psoriasisartrit: systemisk läkemedelsbehandling under graviditet och amning ...»22) Samtidig användning av hepatotoxiska läkemedel mot reumatism (t.ex. metotrexat) rekommenderas inte, men de kan med särskild aktsamhet användas under uppföljning av specialistläkare. |
| Uppföljningsprov* | Liten blodbild (fullständig blodbild), ALAT och blodtryck vecka 3, 6 och 12 och därefter
med 3–6 månaders intervall Se även «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 |
| * Alla nämnda uppföljningsprov behöver inte nödvändigtvis tas av varje patient, utan omfattningen bedöms individuellt. | |
Allmänna principer för användning av biologiska läkemedel, JAK-hämmare och apremilast
- Allmänna anvisningar om användning av biologiska läkemedel finns i Allmänna anvisningar för användning av biologiska läkemedel vid behandling av hudpsoriasis och psoriasisartrit och tabell «Detta bör beaktas vid biologisk läkemedelsbehandling...»8 Detta bör beaktas vid biologisk läkemedelsbehandling.
- Av de biologiska läkemedlen används adalimumab, bimekizumab, etanercept, golimumab, guselkumab, ixekizumab, infliximab, risankizumab, sekukinumab, certolizumabpegol, ustekinumab och abatacept vid behandlingen av psoriasisartrit.
- Biosimilarer som beviljats försäljningstillstånd motsvarar referensläkemedlen till effekt och säkerhet. Se Fimeas anvisning «http://www.fimea.fi/laaketurvallisuus_ja_tieto/biosimilaarit/fimean-kanta-biosimilaarien-vaihtokelpoisuuteen»18.
- Användning av tillgängliga biosimilarpreparat rekommenderas med tanke på kostnadseffektiviteten. Se ställningstagande från Reumatologisk förening i Finland «https://www.reumatologinenyhdistys.fi/lausunnot/»21.
- Se jämförelse av kostnaderna för apremilast, JAK-hämmare och biologiska läkemedel (ACR50-respons), kostnader och terapisvar vid behandling av psoriasisartrit «https://www.terveysportti.fi/apps/laake/laakekustannus/hoi50062»22 (kräver åtkomsträttigheter) och mer information «The number needed to treat (NNT) and cost per responder for systemic therapies for psoriatic arthritis»16, «Hoitovasteen kustannukset Käypä hoito -suosituksissa: näin luen taulukoita (video)»17.
- Indikationen för biologiska läkemedel, JAK-hämmare och apremilast är psoriasisartrit
som behandlats med antireumatiska läkemedel, såsom metotrexat, utan tillräcklig effekt.
- När de traditionella syntetiska läkemedlen mot reumatism inte ger tillräckligt terapisvar eller är olämpliga, rekommenderas inledningsvis en TNF-hämmare eller IL-17-blockerare.
- Följande alternativ är IL-23-, IL-12/23- eller JAK-hämmare.
- Om inget av dessa alternativ är lämpliga, kommer apremilast eller abatacept i fråga.
- Klinisk erfarenhet har visat att responsen är god hos patienter med entesiter, daktyliter och spondylartropatier.
- Man har inte konstaterat någon kliniskt signifikant skillnad i effekt mellan de olika TNF-hämmarna «Biologisten lääkkeiden ja kohdennettujen synteettisten reumalääkkeiden vertailua nivelpsoriaasin hoidossa»18.
- Biologiska läkemedel har inte jämförts med traditionella syntetiska antireumatika i kliniska läkemedelsstudier.
- För bedömning av terapisvaret bör uppföljningstiden vara tillräckligt lång (3–6 månader)
och kliniskt betydande läkning av sjukdomen bör föreligga.
- I flera studier har endast ACR20 använts som det primära kriteriet för terapisvar, vilket följer läkemedelsmyndighetens rekommendation. Detta ska beaktas när resultaten granskas (se Clinical Development Programs for Drugs, Devices, and Biological Products for the Treatment of Rheumatoid Arthritis (RA) «https://www.fda.gov/regulatory-information/search-fda-guidance-documents/clinical-development-programs-drugs-devices-and-biological-products-treatment-rheumatoid-arthritis»23). ACR-klassificeringen beaktar inte hur daktyliter, entesiter eller spondyliter svarar på behandlingen.
- Enligt allmän klinisk praxis kan behandlingen fortsätta om ACR50-respons uppnås.
- Angående ACR-klassificering av terapisvar se «Arnett FC, Edworthy SM, Bloch DA ym. The American ...»269.
Sjukdomens fenotyp och val av behandling
- Vid valet av behandling ska sjukdomens fenotyp beaktas. Se tabell «Arbetsgruppens bedömning av läkemedlens effekt vid behandling av psoriasisartrit och
dess olika fenotyper. Vid valet av behandling ska också andra omständigheter beaktas,
såsom säkerhet och ekonomiska faktorer. Bearbetad från källorna , , , , , , , , .
, , ....»20.
- Vid svår hudpsoriasis är IL-17- eller IL-23-hämmare och dessutom IL-12/23-hämmare primära.
- Vid axial sjukdom rekommenderas i första hand TNF- och IL-17-hämmare. Som ett sekundärt alternativ kan JAK-hämmare övervägas.
- Det finns evidens att TNF-hämmarna, med undantag för etanercept, har effekt för behandlingen av irit «Brüner M, Dige A, Loft AG ym. Spondylitis-psoriasi...»301.
- Om patienten samtidigt har en inflammatorisk tarmsjukdom, är TNF-hämmare och IL12/23-hämmare de primära alternativen.
- Primärt rekommenderas det billigaste alternativet, såvida det inte finns medicinska skäl som kräver något annat.
- Se även Allmänna principer för användning av biologiska läkemedel, JAK-hämmare och apremilast.
| Hudpsoriasis | Perifer artrit | Entesit | Daktylit | Axial sjukdom | Uveit | Inflammatorisk tarmsjukdom | Radiologisk progression | |
|---|---|---|---|---|---|---|---|---|
| Metotrexat | ++ | + | - | - | - | + | + | - |
| Apremilast | + | + | ++ | ++ | ? | ? | - | - |
| JAK-hämmare | ++ | +++ | ++ | ++ | +++ | ? | ++ | ++ |
| TNF-hämmare | ++ | +++ | ++ | ++ | +++ | +++* | +++* | ++ |
| IL-23-hämmare | +++ | ++ | ++ | ++ | + | ? | + | + |
| IL-17-hämmare | +++ | +++ | ++ | ++ | +++ | + | - | ++ |
| Ustekinumab | ++ | ++ | ++ | ++ | ++ | ? | +++ | ++ |
| Abatacept | - | + | ? | ? | - | ? | - | + |
| + = kliniskt påvisad effekt ? = bristande eller motstridig information ? = rekommenderas inte * Andra TNF-hämmare än etanercept |
||||||||
Biologiska läkemedel
- Adalimumab «TNF-hämmare: genomförande och biverkningar...»10:
- Dosen injiceras subkutant med 2 veckors intervall.
- Adalimumab är effektivt för behandling av psoriasisartrit «Adalimumabi verrattuna lumeeseen lisää ACR20-vasteen saavuttaneiden osuutta (noin 60 % vs. noin 15–30 %) nivelpsoriaasipotilailla, joiden tauti on keskivaikea tai vaikea.»A, «Mease P, Hall S, FitzGerald O ym. Tofacitinib or A...»267.
- Vid vecka 24 hade 39 % uppnått ACR50-respons, medan motsvarande siffra för placebobehandling var 6 %.
- ACR70-respons uppnåddes av 30 % efter 48 veckors behandling «Gladman DD, Mease PJ, Ritchlin CT ym. Adalimumab f...»270.
- Antalet biverkningar har motsvarat placebobehandlingen.
- Golimumab (TNF-hämmare) «TNF-hämmare: genomförande och biverkningar...»10:
- Dosen injiceras subkutant med fyra veckors intervall.
- Golimumab förefaller effektivt för behandling av psoriasisartrit «Subkutaaninen golimumabi verrattuna lumeeseen ilmeisesti lisää ARC20-vasteen saavuttaneiden osuutta nivelpsoriaasia sairastavilla (noin 45–51 % riippuen annoksesta vs. noin 10 %) 14 viikon seurannassa.»B.
- ACR50-respons uppnåddes av 30–35 % av patienterna vid 24 veckors uppföljning «Mease PJ. Biologic Therapy for Psoriatic Arthritis...»271, «Ramiro S, Smolen JS, Landewé R ym. Pharmacological...»272.
- Generellt tolereras golimumab väl och man har inte funnit någon statistisk skillnad i biverkningar (inklusive allvarliga biverkningar) mellan dem som fått behandling med golimumab och dem som fått placebo.
- Vid två års uppföljning hade de vanligaste biverkningarna varit luftvägsinfektion och nasofaryngit. Under uppföljningsperioden hade 6 av 335 patienter insjuknat i en infektion som klassificerats som allvarlig «Kavanaugh A, van der Heijde D, McInnes IB ym. Goli...»273.
- Under fem års uppföljning uppnåddes ACR50-respons hos 43 % i placebogruppen, 48 % i gruppen som fick 50 mg golimumab och 51 % i gruppen som fick 100 mg golimumab «Kavanaugh A, McInnes IB, Mease P ym. Clinical effi...»274.
- Etanercept (TNF-hämmare) «TNF-hämmare: genomförande och biverkningar...»10:
- Dosen injiceras subkutant med en veckas intervall.
- Etanercept är effektivt för behandling av psoriasisartrit «Etanersepti verrattuna lumeeseen lisää ACR20-vasteen saavuttaneiden osuutta nivelpsoriaasia sairastavilla (noin 60 % vs. noin 15 %).»A.
- ACR50-respons har uppnåtts hos 44 % av de behandlade vid 48 veckors behandling «Mease PJ, Goffe BS, Metz J ym. Etanercept in the t...»275, «Mease PJ, Kivitz AJ, Burch FX ym. Etanercept treat...»276.
- Effekten har bibehållits både kliniskt och radiologiskt under två års uppföljning «Etanersepti verrattuna lumeeseen lisää ACR20-vasteen saavuttaneiden osuutta nivelpsoriaasia sairastavilla (noin 60 % vs. noin 15 %).»A.
- Antalet biverkningar har motsvarat placebobehandling.
- Infliximab (TNF-hämmare) «TNF-hämmare: genomförande och biverkningar...»10:
- infliximab är effektivt för behandling av psoriasisartrit «Intravenous infliximab with the dose of 5mg/kg increases the proportion of patients with active psoriatic arthritis achieving the ACR20* response at week 16-24 (54-65%), when compared to placebo (10-16%), and it is safe.»A.
- ACR50-respons uppnåddes efter 24 veckors behandling av cirka 40 % av patienterna. Motsvarande siffra för placebo var 4 % «Antoni C, Krueger GG, de Vlam K ym. Infliximab imp...»277.
- ACR70-respons uppnåddes efter 54 veckors behandling av 22 % av patienterna «Kavanaugh A, Krueger GG, Beutler A ym. Infliximab ...»278.
- Antalet biverkningar har motsvarat placebobehandlingen.
- Infliximab är effektivt även vid behandlingsresistent mutilerande psoriasisartrit «Feletar M, Brockbank JE, Schentag CT ym. Treatment...»279, «Kavanaugh A, Antoni CE, Gladman D ym. The Inflixim...»280.
- infliximab är effektivt för behandling av psoriasisartrit «Intravenous infliximab with the dose of 5mg/kg increases the proportion of patients with active psoriatic arthritis achieving the ACR20* response at week 16-24 (54-65%), when compared to placebo (10-16%), and it is safe.»A.
- Certolizumab pegol (TNF-hämmare) «TNF-hämmare: genomförande och biverkningar...»10:
- Dosen injiceras subkutant med två veckors intervall.
- Certolizumab pegol verkar ha effekt på ACR20-responsen och funktionsförmågan vid kortvarig
behandling av psoriasisartrit «Sertolitsumabipegoli verrattuna lumeeseen näyttää parantavan ACR20-vasteita (sen saavuttaa noin 56–64 % vs. noin 24 %) ja toimintakykyä nivelpsoriaasin hoidossa 24 viikon seurannassa.»B.
- Efter 24 veckor hade ACR50-respons uppnåtts av 44 % av dem som fick 200 mg certolizumab pegol (2 x/mån), hos 40 % av dem som fick 400 mg certolizumab pegol (1 x/mån) och hos cirka 13 % av dem som fick placebo «Mease PJ, Fleischmann R, Deodhar AA ym. Effect of ...»281.
- ACR70-respons uppnåddes hos 25 % efter 12 veckors behandling «Mease PJ. Biologic Therapy for Psoriatic Arthritis...»271, «Ramiro S, Smolen JS, Landewé R ym. Pharmacological...»282.
- Under kortvarig uppföljning har antalet biverkningar motsvarat antalet biverkningar vid placebobehandling.
- ACR-responsen kan bibehållas under flera års behandling «van der Heijde D, Deodhar A, FitzGerald O ym. 4-ye...»283.
- Cirka en femtedel av patienterna hade fått allvarliga biverkningar, oftast infektioner, under ettårsuppföljning.
- Certolizumab pegol passerar inte moderkakan och överförs inte till fostret och är därför det primära biologiska läkemedlet då patenten planerar graviditet.
- Guselkumab (IL-23-hämmare) «IL-12/23- och IL-23-hämmare: genomförande och biverkningar...»12:
- Läkemedlet ges till en början vid vecka 0 och 4 och därefter med 8 veckors intervall, men doseringen kan vid behov även ges med 4 veckors intervall.
- Guselkumab är effektivt för behandling av psoriasisartrit «Subcutaneous guselkumab treatment at the dose of 100 mg every 4 or 8 weeks, when compared to placebo, increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 24 (52–64 % vs. 18–33 %).»A.
- Med dosen 100 mg var 4:e eller 8:e vecka (s.c.) uppnås ACR50-respons hos drygt 30 % av patienterna efter 24 veckor; motsvarande siffra bland dem som får placebo är cirka 9–14 %.
- Biverkningarna är i huvudsak lindriga och antalet biverkningar verkar motsvara placebobehandlingen.
- Risankizumab (IL-23-hämmare) «IL-17-hämmare: genomförande och biverkningar ...»11
- Dosen injiceras subkutant vecka 0 och 4 i början av behandlingen och därefter med 12 veckors intervall vid etablerad användning..
- Risankizumab har effekt vid behandling av psoriasisartrit «Subcutaneous risankizumab treatment at the dose of 150 mg at weeks 0, 4 and 16 increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 16 (50–60%), when compared to placebo (25–35%), and it is safe.»A, «Kristensen LE, Keiserman M, Papp K, ym. Efficacy a...»284, «Östör A, Van den Bosch F, Papp K, ym. Efficacy and...»285, «Mease PJ, Kellner H, Morita A, ym. Long-Term Effic...»286.
- Vid vecka 24 hade 26–33 % uppnått ACR50-respons, medan motsvarande siffra för placebobehandling var 9–11 %.
- Vid vecka 24 hade 12–15 % uppnått ACR70-respons, medan motsvarande siffra för placebobehandling var 5–6 %.
- Biverkningarna är i huvudsak lindriga och antalet biverkningar verkar motsvara placebobehandling.
- • Risankizumab verkar säkert enligt undersökningar med 52 veckors uppföljning. En ökning i förekomsten av övre luftvägsinfektioner är en vanlig biverkning «Östör A, Van den Bosch F, Papp K, ym. Efficacy and...»287.
- Ustekinumab (IL-12/23-hämmare) «IL-12/23- och IL-23-hämmare: genomförande och biverkningar...»12:
- Dosen injiceras subkutant med 12 veckors intervall, sedan behandlingen etablerats. Behandlingen inleds med en injektion vecka 0 och 4.
- Ustekinumab verkar vara effektivt vid behandling av psoriasisartrit «Nivelpsoriaasipotilaista, joiden hoitona on ustekinumabi (annoksella 45 mg ja 90 mg 12 viikon välein), noin 40–50 % näyttää saavuttavan ACR20-vasteen viikkoon 24 mennessä, kun lumehoidossa noin 20 % saavuttaa sen.»B.
- Efter 24 veckors behandling uppnåddes ACR50-respons av 18–25 % av patienterna då dosen var 45 mg och av 23–28 % av patienterna då den var 90 mg. Motsvarande siffra för placebo var 7–9 %.
- Efter ett år uppnådde en tredjedel av patienterna ACR50-respons «McInnes IB, Kavanaugh A, Gottlieb AB ym. Efficacy ...»288.
- Effekten verkar kvarstå under uppföljning i 2 år «Kavanaugh A, Puig L, Gottlieb AB ym. Maintenance o...»289.
- Ustekinumab verkar vara särskilt effektivt för behandling av daktylit och entesiter «Kavanaugh A, Puig L, Gottlieb AB ym. Maintenance o...»289, «Araujo EG, Englbrecht M, Hoepken S ym. Effects of ...»290.
- Under 16 veckors uppföljning var antalet biverkningar lika i den grupp som fick verksamt läkemedel som i den som fick placebo. Säkerhetsprofilen för ustekinumab under långtidsuppföljning verkar vara god «Kavanaugh A, Puig L, Gottlieb AB ym. Maintenance o...»289, «Ruyssen-Witrand A, Perry R, Watkins C ym. Efficacy...»291
- Bimekizumab (IL-17-hämmare) «IL-17-hämmare: genomförande och biverkningar ...»11:
- Dosen injiceras subkutant med 4 veckors intervall.
- Bimekizumab har effekt vid behandling av psoriasisartrit. «Bimekizumab reduces symptoms of psoriatic arthritis and is safe to use. In the intervention group, 62-67% of participants achieved 20% reduction in symptom score (ACR20), compared to 16-20% in the control group.»A, «McInnes IB, Asahina A, Coates LC, ym. Bimekizumab ...»292, «Ritchlin CT, Kavanaugh A, Merola JF, ym. Bimekizum...»293, «Merola JF, Landewé R, McInnes IB, ym. Bimekizumab ...»294.
- Vid vecka 16 hade 43–44 % uppnått ACR50-respons, medan motsvarande siffra för placebobehandling var 7–10 %.
- Vid vecka 16 hade 24–27 % uppnått ACR70-respons, medan motsvarande siffra för placebobehandling var 1–4 %.
- Under 12–16 veckors uppföljning ökade de biverkningar som behandlingen orsakade jämfört med placebo, men biverkningarna var huvudsakligen icke-allvarliga infektioner.
- Bimekizumab verkar vara säkert enligt studier med 3 års uppföljning «Coates LC, McInnes IB, Merola JF, ym. Safety and E...»295.
- Ixekizumab (IL-17A-hämmare):
- Medicineringen inleds med dosen 160 mg subkutant och därefter ges 80 mg subkutant med 4 veckors intervall. Vid svår hudpsoriasis ges 80 mg vecka 2, 4, 6, 8, 10 och 12, varefter doseringen blir 80 mg med 4 veckors intervall.
- Ixekizumab är effektivt för behandling av psoriasisartrit «Ixekizumab treatment at the dose of 80 mg, when compared to placebo, increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 24 and probably already at week 12.»A.
- Under 24 veckors uppföljning uppnådde 35–45 % ACR50-respons i ixekizumabgruppen och 5–15 % i gruppen som fick placebo.
- Under 52 veckors uppföljning uppnådde 49,8 % av patienterna (n = 283) ACR50-respons «Smolen JS, Mease P, Tahir H ym. Multicentre, rando...»296.
- Under 24 veckors uppföljning var antalet biverkningar något högre i behandlingsgrupperna än i grupperna som fick placebo. Biverkningarna var i huvudsak lindriga.
- Enligt en direkt jämförelsestudie torde effekten av ixekizumab på ACR50-responsen vara densamma som av adalimumab «Smolen JS, Mease P, Tahir H ym. Multicentre, rando...»296.
- Sekukinumab (IL-17A-hämmare) «IL-17-hämmare: genomförande och biverkningar ...»11:
- Då behandlingen etablerats är dosen 150–300 mg subkutant med en månads intervall; under de första 4 veckorna sker injektionen med en veckas intervall.
- Sekukinumab förefaller effektivt för behandling av psoriasisartrit «Subcutaneous secukinumab treatment at the dose of 150-300 mg monthly increases the proportion of patients with psoriatic arthritis achieving the ACR20 response at week 24 when compared to placebo (approximately 42–63 % vs. 15–27 %), and it is safe.»A.
- ACR50-respons uppnåddes vid 24 veckors uppföljning hos 35 % av dem som fick 150 mg sekukinumab, hos 31% av dem som fick 75 mg och hos 7 % av dem som fick placebo «Mease PJ, McInnes IB, Kirkham B ym. Secukinumab In...»297.
- Vid uppföljning under 24 veckor var antalet allvarliga biverkningar i gruppen som fått 150 mg sekukinumab (329,7 patientår) 3,0 % och i gruppen som fick placebo (122,9 patientår) 3,6 % «Mease P, van der Heijde D, Landewé R ym. Secukinum...»298.
- Brodalumab (IL-17-hämmare) «IL-17-hämmare: genomförande och biverkningar ...»11:
- Jämfört med placebo förefaller det som om 210 mg brodalumab (s.c.) varannan vecka ökar andelen patienter med psoriasisartrit som uppnår ACR20-respons vid 24 veckors uppföljning «Subcutaneous brodalumab treatment at the dose of 210 mg every other week increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at weeks 16 and 24, when compared to placebo (47.9 % vs.»B.
- Cirka 20 % av patienterna på verksamt läkemedel uppnår ACR50-respons vid 16 veckors uppföljning; motsvarande siffra för patienterna på placebo är under 10 %.
- I USA, men inte enligt den europeiska läkemedelsmyndigheten EMA, förknippas användningen av läkemedlet med en varning för ökad suicidrisk och därmed med en uppmaning till uppföljning: Behandlingen ska avbrytas om patienten under behandling med brodalumab får ångest- eller depressionssymtom eller om dessa symtom förvärras.
- I maj 2021 var hudpsoriasis enda indikationen för brodalumab i Finland.
- Abatacept (T-cellshämmare)
- Läkemedlet ges subkutant med en veckas intervall.
- Abatacept förefaller effektivt för behandling av psoriasisartrit «Parenteral abatacept 125 mg per week treatment increases the ACR20 response at week 24 in patients with active psoriatic arthritis when compared to placebo.»B.
- Vid 24 veckors uppföljning hade cirka 20 % av patienterna som fått 125 mg abatacept per vecka och cirka 12 % «Mease PJ, Gottlieb AB, van der Heijde D ym. Effica...»299 av patienterna som fått placebo ACR50-respons.
- Vid 24 veckors uppföljning var antalet biverkningar lika i behandlingsgruppen som i gruppen som fick placebo.
- Abatacept är endast indicerat för psoriasisartrit. Effekten på de extraartikulära symtomen är anspråkslös.
- Det finns inga betydande skillnader mellan de biologiska läkemedlen när det gäller
effekten på daktylit och entesit.
- Enligt en metaanalys med 24 veckors uppföljning var RR för daktyliter 2,57 (95 % konfidensintervall 1,36–4,84) för TNF-hämmarna och 1,88 (1,33–2,65) för de nyare biologiska läkemedlen (ustekinumab, sekukinumab och ixekizumab) jämfört med placebo. Motsvarande siffror för entesiter var 1,93 (1,33–2,79) och 1,95 (1,60–2,38) «Mourad A, Gniadecki R. Treatment of Dactylitis and...»300.
JAK-hämmare
- JAK-hämmare tas dagligen i tablettform. Verkningsmekanismen bygger på att läkemedlet hämmar januskinaser och JAK-STAT-signaltransduktionen, vilket leder till försvagad effekt av flera cytokiner.
- Tofacitinib, se tabell «Dosering och uppföljning av apremilast och JAK-hämmare vid behandling av psoriasisartrit.
...»21.
- Tofacitinib verkar ha effekt vid behandling av psoriasisartrit «Tofacitinib treatment at the dose of 5 mg twice daily, when compared to placebo, seems to increase the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 12 (50–60 % vs. 25–30 %).»B.
- Med dosen 5 mg två gånger om dagen uppnådde cirka 30 % av patienterna ACR50-respons, medan motsvarande siffra för placebobehandling var cirka 10 % under en 12 veckors uppföljning «Nash P, Coates LC, Fleischmann R ym. Efficacy of T...»266.
- Effekten verkar bibehållas under 1 års uppföljning. I en öppen fortsatt studie uppnådde cirka 40 % ACR50-respons «Mease P, Hall S, FitzGerald O ym. Tofacitinib or A...»267.
- Biverkningarna är i huvudsak lindriga och till antal skiljdede sig inte från biverkningarna i placebogruppen. Uppföljningstiden var tre månader. Under 1 års uppföljning fick 7 % av dem som behandlats med tofacitinib en allvarlig biverkning (bl.a. allvarliga infektioner, herpes zoster) och 6 % avbröt behandlingen på grund av någon biverkning «Mease P, Hall S, FitzGerald O ym. Tofacitinib or A...»267.
- Tofacitinib verkar ha effekt vid behandling av psoriasisartrit «Tofacitinib treatment at the dose of 5 mg twice daily, when compared to placebo, seems to increase the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 12 (50–60 % vs. 25–30 %).»B.
- Upadacitinib, se tabell «Dosering och uppföljning av apremilast och JAK-hämmare vid behandling av psoriasisartrit.
...»21:
- Upadacitinib verkar ha effekt vid behandling av psoriasisartrit «Oral upadacitinib treatment at the dose of 15 mg daily increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 12, when compared to placebo (approximately 57–71 % vs. 24–36 %, depending on patient population).»A.
- I en studie med 12 veckors uppföljning uppnådde 37,5 % av patienterna som använde 15 mg upadacitinib en gång per dygn (n = 429) ACR50-respons; motsvarande siffra i gruppen som fick placebo var 13,2 % (n = 423).
- Vid 21 veckors uppföljning upplevde 67 % av patienterna i gruppen (n = 429) som använt 15 mg upadacitinib en gång per dag en biverkning; motsvarande siffra i placebogruppen var 60 % (n = 423).
- I en öppen fortsättningsstudie 24 veckor från inledning fortsatte de som fått upadacitinib med den tidigare dosen och de som hörde till placebogruppen randomiserades till två läkemedelsgrupper (15 eller 30 mg). «Mease PJ, Lertratanakul A, Papp KA ym. Upadacitini...»268. Vid vecka 56 hade 40,8 % av patienterna som fått 15 mg upadacitinib per dag (den ursprungliga interventionsgruppen) och 33,0 % av patienterna som hört till placebogruppen och gått över till 15 mg upadacitinib uppnått ACR50-respons.
- Vid 56 veckors uppföljning var förekomsten av allvarliga infektioner 2,6/100 patientår bland dem som fått upadacitinib 15 mg per dag och 6,1/100 patientår bland dem som fått 30 mg per dag.
- Upadacitinib verkar ha effekt vid behandling av psoriasisartrit «Oral upadacitinib treatment at the dose of 15 mg daily increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 12, when compared to placebo (approximately 57–71 % vs. 24–36 %, depending on patient population).»A.
- Användningen av JAK-hämmare hos patienter över 65 år medför en ökad risk för allvarliga infektioner, hjärtinfarkt och cancer. Enligt EMA:s rekommendation ska dessa preparat användas endast om det inte finns andra lämpliga behandlingsalternativ. «https://www.ema.europa.eu/en/medicines/human/referrals/janus-kinase-inhibitors-jaki»24.
Riktade syntetiska antireumatiska läkemedel (targeted synthetic disease-modifying antirheumatic drug, tsDMARD)
- Apremilast är en fosfodiesteras-4-hämmare. Dess verkningsmekanism bygger på hämning av cykliskt adenosinmonofosfat, vilket påverkar flera antiinflammatoriska cytokiner samtidigt. Läkemedlet tas dagligen i tablettform.
- Apremilast, se tabell «Dosering och uppföljning av apremilast och JAK-hämmare vid behandling av psoriasisartrit. ...»21.
- Apremilast kan övervägas vid psoriasisartrit hos vuxna när man inte kan använda annan
typ av antireumatika, d.v.s. sådana som hämmar den reumatiska sjukdomsprocessen (sDMARD
eller bDMARD) eller om de inte har haft effekt.
- Efter 16–24 veckors apremilastbehandling med standarddosering uppnådde cirka 40 %
av de läkemedelsbehandlade patienterna och cirka 20 % av patienterna som fått placebo
ACR20-respons «Apremilast treatment at the dose of 30 mg twice daily, when compared to placebo, may increase the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 16 to 24 from approximately 20% to 40%.»B.
- ACR50-respons uppnåddes hos mindre än 20 % av patienterna jämfört med 5–7 % i placebogruppen
- Effekten verkar bibehållas under 1–5 års uppföljning: Efter 5 år av fortsatt apremilastbehandling bibehölls ACR20-responsen hos 67 % av patienterna och ACR50-responsen hos 44 %, och inga långvariga biverkningar observerades «Kavanaugh A, Gladman DD, Edwards CJ ym. Long-term ...»263, «Nash P, Ohson K, Walsh J ym. Early and sustained e...»264, «Wells AF, Edwards CJ, Kivitz AJ ym. Apremilast mon...»265.
- 15–17 % av patienterna upplever illamående eller diarré i början av behandlingen.
- Apremilastbehandlingen har inte associerats med ökad förekomst av infektioner eller organtoxicitet.
- Ingen särskild laboratorieuppföljning behövs.
- Läkemedelsersättning förutsätter ett separat B-utlåtande.
- Efter 16–24 veckors apremilastbehandling med standarddosering uppnådde cirka 40 %
av de läkemedelsbehandlade patienterna och cirka 20 % av patienterna som fått placebo
ACR20-respons «Apremilast treatment at the dose of 30 mg twice daily, when compared to placebo, may increase the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 16 to 24 from approximately 20% to 40%.»B.
| Dos | Biverkningar | Uppföljning | Verkningsmekanism | Att beakta | |
|---|---|---|---|---|---|
| Apremilast | Gradvis titrering till dosen 30 mg x 2 | Mag-tarmkanalsymtom | Uppföljningsprov behövs inte | Fosfodiesteras-4-hämmare (PDE4) | |
| Tofacitinib | 5 mg x 2 | Övre luftvägsinfektioner Huvudvärk Ökad infektionsbenägenhet (särskilt herpes zoster) Neutro- och lymfopeni |
TVK och ALAT vecka 3, 6 och 12 efter start och i fortsättningen med 3–6 månaders
intervall. Lipider efter 3 månader. |
Januskinas 1/3-hämmare (JAK1/3) | Användningen hos patienter över 65 år medför en ökad risk för allvarliga infektioner, hjärtinfarkt och cancer. |
| Upadacitinib | 15 mg x 1 | Övre luftvägsinfektioner Illmående Ökad infektionsbenägenhet (särskilt herpes zoster) Neutropeni |
TVK och ALAT vecka 3, 6 och 12 efter start och i fortsättningen med 3–6 månaders
intervall. Lipider efter 3 månader. |
Januskinas 1-hämmare (JAK1) | Användningen hos patienter över 65 år medför en ökad risk för allvarliga infektioner, hjärtinfarkt och cancer. |
Kirurgisk behandling
- Behandlingen är densamma som vid ledgångsreumatism. Se God medicinsk praxis-rekommendationen Nivelreuma «Nivelreuma»2 (på finska).
Patientperspektiv på behandlingen av psoriasisartrit
- Psoriasisartrit och tillhörande symtom kan påverka såväl den fysiska och mentala som
den sociala livskvaliteten «Sumpton D, Kelly A, Tunnicliffe DJ ym. Patients' P...»252, «Coates LC, Orbai AM, Azevedo VF ym. Results of a g...»253. Mer information «Nivelpsoriaasia sairastavien potilaiden kokemuksia ja näkemyksiä»15.
- I en enkätundersökning (n = 1 286, 8 länder) uppgav nästan alla patienter med psoriasisartrit att de under de föregående 12 månaderna upplevt symtom i stöd- och rörelseorganen. De vanligaste symtomen var smärta, ömhet och svullnad i lederna «Coates LC, Orbai AM, Azevedo VF ym. Results of a g...»253.
- Utöver smärtorna påverkar tröttheten i hög grad arbets- och funktionsförmågan och de sociala relationerna.
- Behandlingsmål som är betydelsefulla för patienterna är «Garrido-Cumbrera M, Hillmann O, Mahapatra R ym. Im...»254
- smärtkontroll
- hantering av trötthet och upprätthållande av normal social, fysisk och mental funktionsförmåga
- upprätthållande av arbetsförmågan
- reducerad belastning av hudpsoriasisen.
Rehabilitering vid psoriasisartrit
- Syftet med såväl rehabiliteringen som behandlingen är att främja patientens funktions- och arbetsförmåga samt välbefinnande. Behandlingen och rehabiliteringen stöder varandra.
- I God medicinsk praxis-rekommendationen för ledgångsreumatism behandlas rehabilitering vid ledgångsreumatism. Samma principer gäller för rehabilitering vid psoriasisartrit. Se God medicinsk praxis-rekommendationen Nivelreuma avsnitt Nivelreuman hoito, Kuntoutus «Nivelreuma»2 (på finska).
- Se även Hälsobyns Rehabiliteringshus «https://www.terveyskyla.fi/kuntoutumistalo/sv»25.
Specialfall
Psoriasis och graviditet
- Psoriasis försämrar inte fertiliteten, och därför ska man alltid beakta möjligheten till graviditet då kvinnor i fertil ålder behandlas för psoriasis «Tauscher AE, Fleischer AB Jr, Phelps KC ym. Psoria...»310, «Hale EK, Pomeranz MK. Dermatologic agents during p...»311.
- Under graviditeten lindras hudpsoriasis hos 30–63 % av patienterna, men den förvärras
igen efter förlossningen «Murase JE, Chan KK, Garite TJ ym. Hormonal effect ...»312, «Raychaudhuri SP, Navare T, Gross J ym. Clinical co...»313, «Gudjonsson JE, Karason A, Runarsdottir EH ym. Dist...»314, «Yang YW, Chen CS, Chen YH ym. Psoriasis and pregna...»315.
- I bakgrunden finns skillnader i riskgenerna «Gudjonsson JE, Karason A, Runarsdottir EH ym. Dist...»314 och den dämpande effekten på immunsystemet som könshormonerna har «Tauscher AE, Fleischer AB Jr, Phelps KC ym. Psoria...»310, «Raychaudhuri SP, Navare T, Gross J ym. Clinical co...»313, «Mowad CM, Margolis DJ, Halpern AC ym. Hormonal inf...»316.
- Psoriasis kan också försvåras hos en liten del av patienterna under graviditeten.
- Psoriasisartriten håller sig ofta lugn under graviditet «Ursin K, Lydersen S, Skomsvoll JF ym. Psoriatic Ar...»317. Klinisk erfarenhet visar att symtomen på sakroilit kan dock aktiveras särskilt under andra och tredje trimestern och strax efter förlossningen.
- Svår psoriasis kan påverka graviditetsförloppet (prematuritet, kejsarsnitt, preeklampsi
och eklampsi) och slutresultatet (låg födelsevikt) «Yang YW, Chen CS, Chen YH ym. Psoriasis and pregna...»315, «Bobotsis R, Gulliver WP, Monaghan K ym. Psoriasis ...»318.
- Riskerna hänger uppenbarligen samman med själva sjukdomsprocessen, eftersom dessa risker inte kunde påvisas hos patienterna som behandlades med systemiska läkemedel under graviditeten «Yang YW, Chen CS, Chen YH ym. Psoriasis and pregna...»315.
- Det är önskvärt att sträva till att påverka patientens livsstils- och andra faktorer som ökar graviditetsriskerna «Bandoli G, Johnson DL, Jones KL ym. Potentially mo...»319.
- Vid behandling av psoriasis under graviditet, amning eller avlande av barn ska läkemedlens kontraindikationer beaktas «Patienter med psoriasis och psoriasisartrit: systemisk läkemedelsbehandling under graviditet och amning ...»22.
- Män behöver inte avbryta följande läkemedel då de används enligt reumatologiska doser och familjetillökning planeras: metotrexat, ciklosporin, leflunomid, apremilast, tofacitinib, upadacitinib eller biologiska läkemedel. Sulfasalazin kan försämra fertiliteten hos män, men effekten är övergående och försvinner vanligtvis inom 2 veckor till 2 månader efter att användningen av läkemedlet upphört. Se «https://www.terveyskyla.fi/reumatalo»20.
- För behandling av lindrig hudpsoriasis rekommenderas i första hand bassalvor och milda
eller medelstarka kortikosteroidsalvor «Bae YS, Van Voorhees AS, Hsu S ym. Review of treat...»320, «Chi CC, Kirtschig G, Aberer W ym. Evidence-based (...»321.
- Omfattande eller långvarig användning av starka eller mycket starka kortikosteroidsalvor rekommenderas inte, eftersom användningen av dem kan störa fostertillväxten och öka risken för låg födelsevikt «Chi CC, Wang SH, Wojnarowska F ym. Safety of topic...»322.
- För patienter som är gravida och som har omfattande hudpsoriasis är UVB-ljusbehandling
den primära behandlingen under graviditeten «Bae YS, Van Voorhees AS, Hsu S ym. Review of treat...»320. Vid behandling av svår hudpsoriasis kan man efter övervägande och under omsorgsfull
uppföljning använda ciklosporin och, i särskilda fall, TNF-hämmare «Götestam Skorpen C, Hoeltzenbein M, Tincani A ym. ...»164. För behandling av generaliserad pustulös psoriasis under graviditeten kan glukokortikoider
användas systemiskt (under II–III trimestern) «Bae YS, Van Voorhees AS, Hsu S ym. Review of treat...»320.
- I allmänhet rekommenderas att behandling med TNF-hämmare avslutas redan när graviditet planeras. Exponering under tidig graviditet ger dock inte orsak att överväga abort eller fosterdiagnostik på specialnivå.
- Certolizumab pegol är en säker TNF-hämmare under graviditet och kan vid behov användas under hela graviditeten och amningstiden.
- All annan behandling med TNF-hämmare ska i mån av möjlighet avslutas senast under 20–22:a graviditetsveckan (adalimumab, infliximab) eller 30–32:a graviditetsveckan (etanercept) «Götestam Skorpen C, Hoeltzenbein M, Tincani A ym. ...»164.
- Paracetamol kan användas som smärtstillande läkemedel under hela graviditeten vid lindrig psoriasisartrit, men regelbunden och långvarig användning bör undvikas om möjligt, och kortikosteroidinjektioner. Antiinflammatoriska smärtstillande läkemedel kan användas i begränsad utsträckning under I–III trimestern.
- Sulfasalazin är förstahandsvalet bland systemiska läkemedel vid behandling av lindrig psoriasisartrit under graviditet.
- Om behandlingen av moderns sjukdom kräver, kan biologisk medicinering övervägas, i första hand certolizumab pegol «Clowse ME, Förger F, Hwang C ym. Minimal to no tra...»323, «Mariette X, Förger F, Abraham B ym. Lack of placen...»324.
- Svår hudpsoriasis och psoriasisartrit som kräver systemisk medicinering behandlas alltid inom specialsjukvården.
- Patienter med psoriasisartrit som använder systemiska läkemedel ska remitteras för
konsultation till specialsjukvården redan före graviditeten.
- Kvinnor ska avbryta behandling med metotrexat 3 månader före graviditeten. Exponering
för metotrexat under tidig graviditet ökar risken för fostermissbildningar. Exponering
för metotrexat under organogenesen är en indikation för noggrann strukturell ultraljudsundersökning
utförd av specialist eller vid en fosterdiagnostisk enhet.
- Det är inte nödvändigt för män att avbryta leflunomid när graviditet planeras. Angående karenstider, se tabell «Patienter med psoriasis och psoriasisartrit: systemisk läkemedelsbehandling under graviditet och amning ...»22.
- Vid behov konsulteras Teratologiska informationstjänsten. Se «http://www.hus.fi/»26.
- Kvinnor ska avbryta behandling med metotrexat 3 månader före graviditeten. Exponering
för metotrexat under tidig graviditet ökar risken för fostermissbildningar. Exponering
för metotrexat under organogenesen är en indikation för noggrann strukturell ultraljudsundersökning
utförd av specialist eller vid en fosterdiagnostisk enhet.
| Behandling | Graviditet | Tilläggsinformation | Amning |
|---|---|---|---|
| Systemiska kortikosteroider | Tillåtet | Minsta möjliga dos, särskilt under första trimestern | Tillåtet |
| Paracetamol | Tillåtet | I mån av möjlighet ska regelbunden och långvarig användning undvikas | Tillåtet |
| Antiinflammatoriska smärtstillande läkemedel | |||
| icke-selektiva | Kan övervägas | Regelbunden användning bör i mån av möjlighet undvikas under första trimestern. Mot slutet av graviditeten ska läkemedlet inte alls användas upprepade gånger eller regelbundet. | Tillåtet |
| COX-2-hämmare selektiva | Förbjudet | Celekoxib tillåtet | |
| Primära systemiska läkemedel | |||
| Acitretin | Förbjudet | Teratogen, karenstid 3 år | Förbjudet |
| Leflunomid | Förbjudet | Kom ihåg: metod för eliminering av läkemedlet ur kroppen | Förbjudet |
| Metoxisalen | Rekommenderas inte | Otillräcklig information | Rekommenderas inte |
| Metotrexat | Förbjudet | Teratogen, karenstid 3 mån. | Förbjudet |
| Ciklosporin | Tillåtet | Tillåtet | |
| Sulfasalazin | Tillåtet | Folsyratillskott 0,4–1 mg/dygn rekommenderas under graviditet «Flint J, Panchal S, Hurrell A ym. BSR and BHPR gui...»259 | Tillåtet |
| Sekundära systemiska läkemedel | |||
| Adalimumab | Kan övervägas | Avslutas helst före graviditetsvecka 20 | Tillåtet |
| Abatacept | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Apremilast | Förbjudet | Förbjudet | |
| Bimekizumab | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Brodalumab | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Dimetylfumarat | Förbjudet | Förbjudet | |
| Etanercept | Kan övervägas | Avslutas helst före graviditetsvecka 30–32 | Tillåtet |
| Golimumab | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Guselkumab | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Ixekizumab | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Infliximab | Kan övervägas | Avslutas helst före graviditetsvecka 20 | Tillåtet |
| Risankizumab | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Sekukinumab | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Certolizumab pegol | Tillåtet | Passerar inte moderkakan och utsöndras inte i bröstmjölken | Tillåtet |
| Tildrakizumab | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Tofacitinib | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Upadacitinib | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Ustekinumab | Rekommenderas inte | Tillsvidare lite erfarenhet | Rekommenderas inte |
| Män behöver inte avbryta följande läkemedel då de används i reumatologiska doser och familjetillökning planeras: metotrexat, ciklosporin, leflunomid, apremilast, tofacitinib, upadacitinib eller biologiska läkemedel. Sulfasalazin kan försämra fertiliteten hos män, men effekten är övergående och försvinner vanligtvis inom 2 veckor till 2 månader efter att användningen av läkemedlet upphört «https://www.terveyskyla.fi/reumatalo»20. | |||
Behandling av hudpsoriasis hos barn
- En typisk form av psoriasis hos små barn är tunn, fjällande plackpsoriasis i ansiktet,
hårbottnen och blöjområdet (bilderna «Psoriaasi lapsen kasvoilla»62 och «Lapsen psoriaasi-ihottuma»63).
- Droppformad psoriasis (psoriasis guttata) är ganska sällsynt hos småbarn men vanligare hos tonåringar «Morris A, Rogers M, Fischer G ym. Childhood psoria...»326.
- Medelsvår eller svår hudpsoriasis försämrar barnpatienternas hälsorelaterade livskvalitet mer än diabetes och lika mycket som astma eller artrit «Varni JW, Globe DR, Gandra SR ym. Health-related q...»327.
- Under vårdrelationen måste behovet av barnpatientens och familjens psykosociala stöd
beaktas. För lokalbehandling av psoriasis hos barn ska följande beaktas:
- systemisk absorption (betydande särskilt vid behandling av blöjområde) «Siegfried EC. Neonatal skin and skin care. Dermato...»328, «Chiou YB, Blume-Peytavi U. Stratum corneum maturat...»329, «Lebwohl M, Ali S. Treatment of psoriasis. Part 1. ...»330
- förväntad lång sjukdomstid och den därmed ökade möjligheten till behandlingsrelaterade biverkningar.
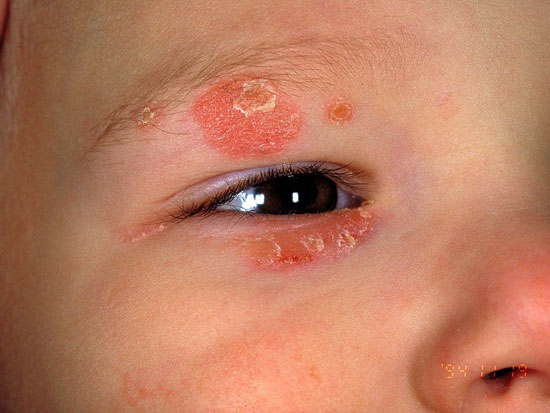
Psoriaasi lapsen kasvoilla
© Raimo Suhonen
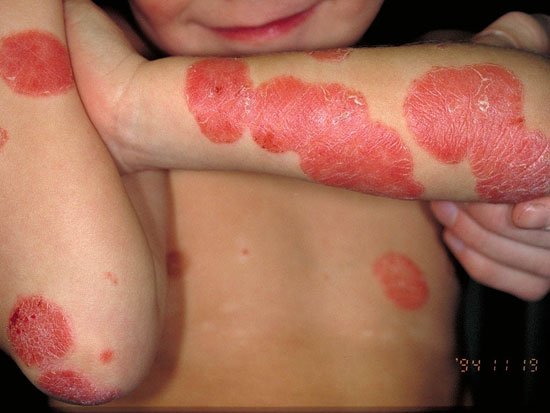
Lapsen psoriaasi-ihottuma
© Raimo Suhonen
Lokalbehandling
- Se även avsnittet Behandling av hudpsoriasis/Lokalbehandling.
- Keratolytika:
- Ex tempore-preparat som innehåller urea eller mjölksyra (3–5 % i fet bassalva) är användbara.
- Salicylsyrapreparat:
- När barn behandlas ska risken för salicylism beaktas. Se Konsultation i klinisk farmakologi nr 3208 om säkerhet vid användning av salicylatsalvor på barn «hoi50062c.pdf»6.
- För barn under skolåldern används preparaten endast på små hudområden (t.ex. i hårbottnen) och med en halt på högst 0,5 % «Sticherling M, Augustin M, Boehncke WH ym. Therapy...»331.
- Preparaten används inte på barn under 2 år. Se Konsultation i klinisk farmakologi nr 3208 om säkerhet vid användning av salicylatsalvor på barn «hoi50062c.pdf»6.
- Kortikosteroidsalvor:
- Användningen ska begränsas till behandling av akuta inflammatoriska faser.
- Kortikosteroidsalvor i grupp I–II (III) används (d.v.s. milda preparat gynnas).
- Upprepad användning av kortikosteroidsalvor ska undvikas «Kortikosteroidivoiteet psoriaasin hoidossa»4.
- D-vitaminderivat:
- Kalcipotriolsalva är relativt effektiv jämfört med placebo «Kalsipotrioli saattaa olla tehokas (PASI-alenema 60 %) lasten psoriaasin paikallishoidossa.»C.
- Efter flera veckors behandling (8–40 veckor) reduceras PASI-indexet med ca 60 %.
- Kalcipotriolsalva används på högst 30 % av hudytan.
- De rekommenderade doserna får inte överskridas.
- Mängden kalcipotriolsalva som används på barn över 12 år får inte överstiga 75 gram per vecka och på barn mellan 6 och 12 år 50 gram per vecka.
- På barn under 6 år används kalcipotriolsalva endast under specialistläkarkontroll.
- Tillgången begränsar användningen.
- Användningen av kalcitriolpreparat för behandling av personer under 18 år har inte undersökts på ett tillförlitligt sätt, men terapisvaret och säkerheten torde motsvara kalcipotriol «de Jager ME, de Jong EM, van de Kerkhof PC ym. Eff...»332.
- Kalcipotriolsalva är relativt effektiv jämfört med placebo «Kalsipotrioli saattaa olla tehokas (PASI-alenema 60 %) lasten psoriaasin paikallishoidossa.»C.
- Kalcineurinhämmare:
- Takrolimus i en halt på 0,1% verkar vara ett effektivt och säkert behandlingsalternativ för barnpatienter, särskilt för behandling av psoriasis i ansikte och hudveck «de Jager ME, de Jong EM, van de Kerkhof PC ym. Eff...»332. Takrolimuspreparat är inte FPA-ersatta när indikationen är psoriasis.
UV-fototerapi
- Effekten av ljusbehandling av psoriasis hos barn har inte utretts med kontrollerade prövningar, men terapisvaret och biverkningarna torde motsvara resultaten hos vuxna.
- Det finns inga tillförlitliga undersökningsresultat om långtidssäkerheten av ljusbehandling hos barn.
- Ljusbehandling (UVB-behandlingar eller SUP) kan efter övervägande användas under specialistövervakning «Jury CS, McHenry P, Burden AD ym. Narrowband ultra...»333, «Pasic A, Ceovic R, Lipozencic J ym. Phototherapy i...»334.
Systemiska och biologiska läkemedel
- Se tabell «Biologiska läkemedel för behandling av hudpsoriasis hos barn...»9.
- Behandlingen skräddarsys individuellt under specialistkontroll.
- Systembehandlingar, såsom acitretin eller metotrexat, kan i undantagsfall behövas för att behandla psoriasis hos barn. Vid behov genomförs behandlingen i samarbete med pediater.
- Av de biologiska läkemedlen kan barn vid behov använda adalimumab från 4 års ålder, etanercept från 6 års ålder och ustekinumab från 12 års ålder «Paller AS, Siegfried EC, Langley RG ym. Etanercept...»335, «Paller AS, Siegfried EC, Eichenfield LF ym. Long-t...»336, «Paller AS, Siegfried EC, Pariser DM ym. Long-term ...»337, «Landells I, Marano C, Hsu MC ym. Ustekinumab in ad...»338.
Psoriasisartrit hos barn
Kriterier och klassificering
- ILAR-kriterierna (International League of Associations for Rheumatology) för barnreuma uppfylls när artrit konstateras hos en patient under 16 års ålder, när den pågått i minst 6 veckor och när någon särskild orsak till artriten inte kan påvisas. Barnreuma delas enligt klassificeringskriterierna in i sex specifika subtyper samt en grupp som inte kan klassificeras «Petty RE, Southwood TR, Manners P ym. Internationa...»339.
- Psoriasisartrit hos barn är en av undertyperna av barnreuma. ILAR-kriterierna är följande:
- Patienten med barnreuma har psoriasisartrit då hen har antingen artrit och hudpsoriasis
eller artrit och 2 av följande:
- daktylit
- nagelförändringar förenliga med psoriasis
- psoriasis hos släkting i första ledet.
- Kriterier som exkluderar psoriasisartrit hos barn och som antyder annan specifik typ
av barnreuma, t.ex. entesitartrit eller seropositiv barnreuma eller barnreuma med
allmänna symtom, är bl.a.:
- RF+
- pojke som insjuknat efter 6 års ålder och är HLA-B27-positiv
- HLA-B27-associerad spondylartrit hos släkting i första ledet
- kriterierna för två subtyper uppfylls samtidigt.
- Patienten med barnreuma har psoriasisartrit då hen har antingen artrit och hudpsoriasis
eller artrit och 2 av följande:
- Ändringar till klassificeringskriterierna för barnreuma har föreslagits, emedan en
del av patienterna har drag av flera sjukdomstyper. När eksklusionskriterierna tillämpas
stringent blir inte mindre än 20–30 % av patienterna med barnreuma oklassificerade.
- Eksklusionskriteriernas inverkan på subtypen av barnreuma har undersökts i en kanadensisk studie med 162 barn med barnreuma. Av patienterna med barnreuma hade 67 % (57/85) en släkting i första ledet psoriasis och detta var orsaken till att diagnosen för dessa barn blev ospecificerad barnreumatism. Om psoriasis hos släktingar i första ledet inte beaktades som kriterium, klassificerades 14,3 % (11/77) av patienterna inte längre i kategorin psoriasisartrit.
- Psoriasisartrit hos barn har ansetts ha en mycket varierande sjukdomsbild och har
inte tidigare observerats skilja sig tydligt från andra barnreumatiska subtyper vad
gäller prognos och karakteristika såsom fenotyp, sjukdomsförlopp, förekomst av uveit,
terapisvar och prognos «Butbul Aviel Y, Tyrrell P, Schneider R ym. Juvenil...»340.
- I en nordisk studie var prognosen för psoriasisartrit hos barn dock sämre än för andra typer av barnreuma och sjukdomen var mer sällan i remission än andra typer. Tecken på dålig prognos var hudpsoriasis, daktylit, stort antal inflammatoriska leder och psoriasis hos en släkting i första ledet «Ekelund M, Aalto K, Fasth A ym. Psoriasis and asso...»341.
- Vid psoriasisartrit hos barn kan man urskilja två subgrupper enligt ålder. I båda dessa subtyper har patienterna många daktyliter, vilket skiljer dessa subtyper från andra barnreumatiska subtyper.
- Den form av psoriasisartrit hos barn som börjar i unga år påminner om de kärnantikroppspositiva subtyperna av barnreuma, medan den form som debuterar sent har drag av spondylartrit och påminner om psoriasisartrit hos vuxna typ spondylartropati.
- Enligt en studie var kategorierna oligoartrit och psoriasisartrit bland barnpatienter under 5 år som insjuknade i psoriasisartrit klart olika till sin sjukdomsbild trots en viss överlappning «Stoll ML, Nigrovic PA, Gotte AC ym. Clinical compa...»342.
- Det amerikanska pediatriska psoriasisartritmaterialet stödde tanken om två olika sjukdomsbilder bland barn under 4 år respektive barn över 4 år. Det var inte möjligt att diagnostisera alla fall av psoriasisartrit hos barn genom att tillämpa ILAR-kriterierna, där CASPAR-kriterierna för vuxna hade tillämpats. Detta beror främst på exklusionskriterierna som hänför sig till entesitartriterna hos barn «Zisman D, Gladman DD, Stoll ML ym. The Juvenile Ps...»343.
Särdrag
- Hos barn med psoriasisartrit kommer artriten ofta många år före hudutslaget. Bland 119 kanadensiska patienter kom utslaget före artriten hos 32 % av patienterna, 29 % av patienterna hade samtidiga manifestationer och hos 39 % kom artriten först och hudsymtomen flera år senare «Butbul Aviel Y, Tyrrell P, Schneider R ym. Juvenil...»340.
- Daktylit förekommer åtminstone hos 20–40 % av patienterna, om sjukdomen börjar före 6 års ålder «Stoll ML, Zurakowski D, Nigrovic LE ym. Patients w...»344.
- Vid psoriasisartrit hos barn kan man särskilja andra subtyper av barnreuma «Butbul Aviel Y, Tyrrell P, Schneider R ym. Juvenil...»340.
- Den vanligaste subtypen (55 %) var sjukdom som debuterade oligoartikulärt. Den avancerade och blev polyartrikulär hos en tredjedel av patienterna.
- Bland patienterna vars sjukdom kännetecknades av polyartrit (inklusive avancerad oligoartrit) (46 %) var sjukdomsförloppet svårare och prognosen sämre än för patienterna i andra subtyper. Hos barn konstaterades kontrakturer oftare och tiden till inaktiv sjukdom blev längre. Typiska drag för denna sjukdomstyp var symmetriska inflammationer i de små lederna och i handledslederna och behov av DMARD-behandling.
- 13 % av patienterna hade drag av barnreuma av entesittyp (bl.a. sakroilit).
Behandling
- Behandlingen av psoriasisartrit hos barn genomförs individuellt under övervakning
av specialist enligt samma principer som behandlingen av andra subtyper av barnreuma
«Kröger L, Vähäsalo P, Tynjälä P ym. [Medical treat...»345.
- Barnpatienter med psoriasisartrit har inte undersökts separat, utan dessa patienter kommer med i en del behandlingsstudier av barnreuma. För behandlingen av psoriasisartrit hos barn tillämpas resultaten som erhållits i barnreumastudier.
- Materialet är litet och målet är i allmänhet att utreda läkemedelssäkerheten.
- Vid bedömning av terapisvaret bör man använda kliniskt betydande läkningsresultat.
- Den viktigaste skillnaden i fråga om vaccinationer av barn jämfört med anvisningarna för vuxna är att man strävar efter att ge barnen åtminstone de levande primärvaccinerna (MPR och vid behov vattkoppsvaccin) innan behandling med metotrexat inleds.
- Metotrexat:
- Metotrexat är det primära läkemedlet för behandling av reuma hos barn,
- när terapisvaret vid behandling av psoriasisartrit typ oligoartrit enbart med intraartikulära injektioner och antiinflammatoriska smärtstillande läkemedel blir otillräckligt,
- oftast när det är fråga om psoriasisartrit typ polyartrit.
- Det finns inga separata undersökningar om behandling av psoriasisartrit med metotrexat hos barn. Metotrexat har dock visat sig vara effektivt både vid oral och subkutan administration, men biverkningarna ökar i takt med att dosen ökar «Ruperto N, Murray KJ, Gerloni V ym. A randomized t...»346.
- Se även tabell «Detta bör beaktas vid metotrexatbehandling...»4 Detta bör beaktas vid metotrexatbehandling.
- Metotrexat är det primära läkemedlet för behandling av reuma hos barn,
- Sulfasalazin:
- Det finns inga separata undersökningar om behandling av psoriasisartrit med sulfasalazin hos barn, men sulfasalazin är effektivt vid behandling av barnreuma «van Rossum MA, Fiselier TJ, Franssen MJ ym. Sulfas...»347.
- Leflunomid:
- Leflunomid kan vara nästan lika effektivt som metotrexat för behandling av barnreuma «Silverman E, Mouy R, Spiegel L ym. Leflunomide or ...»348.
- Hydroxiklorokin:
- Hydroxiklorokin används ibland vid barnreuma, främst för behandling av lindriga sjukdomsformer och i kombination med andra antireumatika.
- Kortikosteroider:
- Kortikosteroidpreparat andvänds vid behov lokalt för behandling av barnreuma i form av intraartikulära injektioner. Kortikosteroider används också oralt i små doser i svåra sjukdomsformer som överbryggande behandling vid introduktion av nya antireumatika, vid byte av läkemedel eller vid behandling av artrit i halskotpelaren.
- Biologiska läkemedel:
- Adalimumab, etanercept, golimumab, tocilizumab (IL-6-blockerare), sekukinumab (IL-17A-hämmare) och abatacept är officiellt indicerade för behandling av barnreuma (med undantag förgeneraliserad juvenil artrit) i Finland. Infliximab används också allmänt. «Tynjälä P, Vähäsalo P, Tarkiainen M ym. Aggressive...»349.
- Adalimumab:
- Adalimumab är effektivt för behandling av barnreuma, särskilt i kombination med metotrexat «Lovell DJ, Ruperto N, Goodman S ym. Adalimumab wit...»350.
- Randomiserade läkemedelprövningar med pediatriska patienter (som inkluderade icke-psoriasisartritpatienter) visade att säkerhetsprofilen för adalimumab i alla dessa indikationer var lika. Till exempel var svåra infektioner sällsynta och inga maligna sjukdomar förekom «Horneff G, Seyger MMB, Arikan D ym. Safety of Adal...»351.
- Etanercept:
- En öppen studie har publicerats omfattande 29 patienter med psoriasisartrit som ingick i datamaterialet med barnreumapatienter. Vid 2 års uppföljning hade 83 % uppnått ACRpedi70-respons och 24 % hade inaktiv sjukdom «Constantin T, Foeldvari I, Vojinovic J ym. Two-yea...»352.
- Effekt- och säkerhetsresultatet av etanercept bekräftades av en öppen 6 års uppföljningsstudie (CLIPPER) med 23 patienter med psoriasisartrit. Cirka 70 % av patienterna bibehöll ACRpedi70-responsen och cirka 25 % hade inaktiv sjukdom «Foeldvari I, Constantin T, Vojinovic J ym. Etanerc...»353.
- Effekt- och säkerhetsresultatet bekräftas också av en öppen registerstudie med 18 patienter «Otten MH, Prince FH, Ten Cate R ym. Tumour necrosi...»354 och 127 patienter «Windschall D, Müller T, Becker I ym. Safety and ef...»355.
- En jämförande studie av tre behandlingsstrategier visade att kombinationen metotrexat och etanercept har bättre effekt än DMARD-monoterapi (metotrexat eller sulfasalazin) eller överbryggande behandling med metotrexat och prednisolon. Undersökningen omfattade 94 patienter med barnreuma, varav 16 hade psoriasisartrit. Efter tre månaders behandling uppnåddes ACRpedi50 av 53 % av patienterna i gruppen som fått metotrexat och etanercept, av 31 % i gruppen som fått metotrexat och prednisolon och av 38 % i gruppen som fått metotrexat eller sulfasalazin (p=0,19). ACRpedi70 uppnåddes hos 47 %, 19 % och 25 % (p=0,04) «Hissink Muller PC, Brinkman DM, Schonenberg D ym. ...»356.
- I en annan behandlingsstrategistudie randomiserades 85 patienter med barnreuma typ polyartrit (inte psoriasisartrit, men en släkting i första ledet fick ha psoriasis) i två grupper: metotrexat s.c., prednison och etanercept eller metotrexat s.c., prednisonplacebo och etanerceptplacebo. Behandlingen inleddes senast inom 1 år efter diagnos. Vid sex månaders uppföljning konstaterades inaktiv sjukdom hos 40 % i kombinationsbehandlingsgruppen och hos 23 % i metotrexatgruppen (p = 0,088). Motsvarande siffror för 12 månader var 73 % och 58 % (p = 0,053) «Wallace CA, Giannini EH, Spalding SJ ym. Trial of ...»357.
- Golimumab:
- I en behandlingsstudie med barnreumapatienter med den polyartikulära sjuksdomsformen, där också lämpliga patienter med psoriasisartrit ingick, var golimumab effektivt, men 3 månader efter att medicineringen avslutats skilde sig antalet relapsfall inte längre mellan dem som fått verksamt ämne och dem som fått placebo. Golimumab ledde till att barnreuma typ polyartrit förbättrades, även om det primära målet inte uppnåddes i RCT-undersökningen. Läkemedlet tolererades väl av patienterna och några överraskande biverkningar förekom inte «Brunner HI, Ruperto N, Tzaribachev N ym. Subcutane...»358.
- Infliximab:
- För behandling av mycket tidig polyartikulär barnreuma var infliximab-metotrexatbehandling effektivare än en DMARD-kombination eller metotrexatmonoterapi «Tynjälä P, Vähäsalo P, Tarkiainen M ym. Aggressive...»349.
- Tocilizumab:
- Tocilizumab har visat sig vara effektivt för behandling av barnreuma med allmänna symtom och barnreuma typ polyartrit «De Benedetti F, Brunner HI, Ruperto N ym. Randomiz...»359, «Brunner HI, Ruperto N, Zuber Z ym. Efficacy and sa...»360.
- I en tvåårig kohortundersökning (56 barnreumapatienter i åldern 2–17 år med seropositiv eller seronegativ polyartrit eller avancerande oligoartrit, inga patienter med psoriasisartrit) ökade andelen patienter med låg sjukdomsaktivitet (JADAS10 ≤ 3,9) från 18 % till 58 % vid 1 års uppföljning och till 84 % vid 2 års uppföljning. Andelen patienter med inaktiv sjukdom (JADAS10 ≤ 0,7) ökade på motsvarande sätt från 2 % till 19 % och till 44 % och andelen patienter med kliniskt inaktiv sjukdom (Wallaces preliminära kriterier) ökade från 2 % till 28 % och till 46 %. Allvarliga biverkningar förekom som väntat: 12,9/100 patientår «Grönlund MM, Remes-Pakarinen T, Kröger L ym. Effic...»361.
- Abatacept
- I en öppen uppföljningsstudie som gällde patienter med barnreuma typ polyartrit (n = 190) påvisades att den uppnådda behandlingseffekten kvarstår i 7 år. Även de som fick placebo i början svarade på behandling med abatacept. Enligt intention-to- treat-analys uppnådde 27,4 % ACRpedi70-respons och hos 16,3 % var sjukdomen inaktiv «Lovell DJ, Ruperto N, Mouy R ym. Long-term safety,...»362.
- Sekukinumab
- IL-17A-hämmare med officiell indikation vid behandlingen av psoriasisartrit och entesitartrit hos barn.
- I en randomiserad kontrollerad studie deltog 86 patienter, av vilka 34 hade psoriasisartrit (och 52 hade barnreuma av entesittyp). I studiens öppna del fick de läkemedel i 12 veckor, varefter de randomiserades för att få sekukinumab eller placebo. Hos personer som fått sekukinumab tog det betydligt längre för sjukdomen att förvärras än hos personer som fått placebo (riskförhållande 0,28; 95 % konfidensintervall 0,13–0,63). Säkerhetsprofilen var densamma som i en studie där man undersökte psoriasisartrit och axial spondylartrit hos vuxna «Brunner HI, Foeldvari I, Alexeeva E, ym. Secukinum...»363.
- JAK-hämmare:
- Baricitinib
- Baricitinib har officiell indikation vid behandlingen av barnreuma i polyartritform samt vid psoriasisartrit och entesitartrit hos barn.
- Läkemedlet har undersökts i ett materialmed 220 barnreumapatienter av vilka 10 barn hade psoriasisartrit. I studien fick 219 patienter baricitinib under den 12 veckor långa öppna inledningsperioden. Av patienterna fick 163 (74 %) minst ACRpedi30-respons vid vecka 12. De randomiserades sedan dubbelblint för att få placebo (n = 81) eller baricitinib (n = 82) i 32 veckor. Tiden till försämring av sjukdomen var betydligt kortare för patienter som fått placebo än för personer som fått baricitinib (riskförhållande 0,241; 95 % konfidensintervall 0,128-0,453, p < 0,0001). Läkemedlets säkerhetsprofil motsvarade vuxenstudiernas säkerhetsprofil «Ramanan AV, Quartier P, Okamoto N, ym. Baricitinib...»364.
- Tofacitinib
- Tofasitinibilla on virallinen käyttöindikaatio polyartriittimuotoisessa lastenreumassa ja lasten nivelpsoriaasissa.
- Läkemedlet har visat sig vara effektivt i en randomiserad kontrollerad studie med 225 patienter. 20 patienter (9 %) hade psoriasisartrit. Deltagarna fick tofacitinib under den 18 veckor långa öppna inledningsperioden. 147 (65 %) fick samtidigt metotrexat. Av patienterna fick 142 (77 %) minst ACRpedi30-respons vid vecka 18. De randomiserades sedandubbelblint för att få placebo (n = 70) eller tofacitinib (n = 72) i 26 veckor. Sjukdomen hade förvärrats betydligt mer sällan hos personer som fått tofacitinib (29 %) än hos personer som fått placebo vid vecka 44 (53 %; riskförhållande 0,46; 95 % konfidensintervall 0,27-0,79; p = 0,0031) «Ruperto N, Brunner HI, Synoverska O, ym. Tofacitin...»365.
- Baricitinib
Ekonomisk information
- Se jämförelse av effekten (ACR50-respons), kostnaderna och kostnaderna för uppnått terapisvar för apremilast, JAK-hämmare och biologiska läkemedel vid behandling av psoriasisartrit «https://www.terveysportti.fi/apps/laake/laakekustannus/hoi50062»22 , mer information «The number needed to treat (NNT) and cost per responder for systemic therapies for psoriatic arthritis»16 och en video om hur man läser tabellen «Hoitovasteen kustannukset Käypä hoito -suosituksissa: näin luen taulukoita (video)»17.
Nivåstrukturering av vården
Diagnostik och nivåstrukturering av vården av hudpsoriasis
- För diagnostik och nivåstrukturering av vården av hudpsoriasis se diagram «Nivåstrukturering av vården vid hudpsoriasis»1.
- Inom primärvården behandlas följande patienter utan specialistkonsultation:
- psoriasis hos vuxna patienter,
- som kan kontrolleras med ändamålsenlig lokalbehandling
- som inte orsakar problem med arbetsförmågan
- som inte har ledsymtom.
- psoriasis hos vuxna patienter,
- Utredningen och behandlingen av andra sjukdomar och riskfaktorer ska påbörjas redan
före konsultationen inom specialsjukvården. Centrala är
- metabolt syndrom «Rutter MK, Kane K, Lunt M ym. Primary care-based s...»366, rökning och överkonsumtion av alkohol
- utredning och behandling av infektionshärdar (särskilt i munnen)
- depression och ångest.
- Patienten remitteras till specialsjukvården när
- det är fråga om snabbt expanderande, omfattande eller svår psoriasis
- det är fråga om hudpsoriasis hos barn eller misstanke om detta
- det är fråga om begränsad psoriasis som
- inte reagerar på lämplig lokalbehandling (för bekräftelse av diagnosen)
- orsakar problem med arbetsförmågan (t.ex. psoriasis i handflatan)
- orsakar oskälig subjektiv olägenhet (t.ex. psoriasis i ansiktet).
- det behövs mer information om handledning av patienten eller hens sjukdom
- det är fråga om överkonsumtion eller beroende av starka kortikosteroidsalvor.
- Efter specialistläkarkonsultation
- följs patienten upp inom primärvården såvida inte utslaget kräver UV-ljusbehandling eller systemisk medicinering.
Diagnostik och nivåstrukturering av vården vid psoriasisartrit
- Diagnosen psoriasisartrit och bedömningen av vårdbehovet görs av specialist förtrogen med psoriasisartrit.
- Inom primärvården behandlas följande patienter utan specialistkonsultation:
- psoriasisartrit med lindriga symtom.
- Behandlas med antiinflammatoriska smärtstillande läkemedel och intraartikulära kortikosteroidinjektioner.
- psoriasisartrit med lindriga symtom.
- Specialsjukvården ska konsulteras om det är fråga om
- artrit som blir långvarig eller svår och som inte svarar på antiinflammatoriska smärtstillande läkemedel och lokala kortikosteroidinjektioner (2–3 gånger)
- färsk polyartrit
- en sjukdomsform som påminner om ankyloserande spondylit
- psoriasisartrit hos barn eller misstanke om detta
- psoriasisartrit hos gravida kvinnor eller hos kvinnor som planerar graviditet.
- Efter konsultation med specialistläkare:
- När terapeutisk balans har uppnåtts kan behandlingen och uppföljningen av en vuxen
patient överföras till primärvården.
- Innan vårdansvaret överförs rekommenderas att specialistläkaren och den läkare inom primärvården som ansvarar för patienten samarbetar i form av mellanbedömningar (s.k. delat behandlingsansvar).
- Då terapisvaret försämras och då patientens symtom tilltar, konsulteras specialsjukvården.
- Uppföljningen av patienter som får biologisk läkemedelsbehandling och behandling med JAK-hämmare sker inom specialsjukvården.
- Regionala förfaranden för nivåstruktureringen av behandlingen (vårdkedjorna) kan avvika från denna rekommendation.
- När terapeutisk balans har uppnåtts kan behandlingen och uppföljningen av en vuxen
patient överföras till primärvården.
Arbetsgrupp tillsatt av Finska Läkarföreningen Duodecim, Finlands Dermatologförening och Reumatologisk Förening i Finland rf
För mer information om arbetsgruppsmedlemmar samt anmälan om intressekonflikter, se «Psoriaasi ja nivelpsoriaasi»1 (på finska)
Översättare: Lingsoft Language Services Oy
Granskning av översättningen: Robert Paul
Litteratur
Psoriasis och psoriasisartrit. God medicinsk praxis-rekommendation. Arbetsgrupp tillsatt av Finska Läkarföreningen Duodecim, Finlands Dermatologförening och Reumatologisk Förening i Finland rf. Helsingfors: Finska Läkarföreningen Duodecim, 2023 (hänvisning dd.mm.åååå). Tillgänglig på internet: www.kaypahoito.fi
Närmare anvisningar: «https://www.kaypahoito.fi/sv/god-medicinsk-praxis/nyttjanderattigheter/citering»27
Ansvarsbegränsning
God medicinsk praxis- och Avstå klokt-rekommendationerna är sammandrag gjorda av experter gällande diagnostik och behandling av bestämda sjukdomar. Rekommendationerna fungerar som stöd när läkare eller andra yrkesutbildade personer inom hälso- och sjukvården ska fatta behandlingsbeslut. De ersätter inte läkarens eller annan hälsovårdspersonals egen bedömning av vilken diagnostik, behandling och rehabilitering som är bäst för den enskilda patienten då behandlingsbeslut fattas.
Litteratur
- Mälkonen T, Suomela S. [What do we know about pathogenesis of psoriasis?]. Duodecim 2011;127:1579-89 «PMID: 21995128»PubMed
- Matikainen S, Jokiranta S, Eklund KK. [Role of cytokines and their blocking in immune-mediated inflammatory diseases]. Duodecim 2016;132:349-54 «PMID: 27017787»PubMed
- Global report on psoriasis. World Health Organization 2016. ISBN 978 92 4 156518 9. 2016
- Petty RE, Southwood TR, Manners P ym. International League of Associations for Rheumatology classification of juvenile idiopathic arthritis: second revision, Edmonton, 2001. J Rheumatol 2004;31:390-2 «PMID: 14760812»PubMed
- Felson DT, Anderson JJ, Boers M ym. American College of Rheumatology. Preliminary definition of improvement in rheumatoid arthritis. Arthritis Rheum 1995;38:727-35 «PMID: 7779114»PubMed
- Giannini EH, Ruperto N, Ravelli A ym. Preliminary definition of improvement in juvenile arthritis. Arthritis Rheum 1997;40:1202-9 «PMID: 9214419»PubMed
- Carlin CS, Feldman SR, Krueger JG ym. A 50% reduction in the Psoriasis Area and Severity Index (PASI 50) is a clinically significant endpoint in the assessment of psoriasis. J Am Acad Dermatol 2004;50:859-66 «PMID: 15153885»PubMed
- Gordon KB, Feldman SR, Koo JY ym. Definitions of measures of effect duration for psoriasis treatments. Arch Dermatol 2005;141:82-4 «PMID: 15655149»PubMed
- Parisi R, Symmons DP, Griffiths CE ym. Global epidemiology of psoriasis: a systematic review of incidence and prevalence. J Invest Dermatol 2013;133:377-85 «PMID: 23014338»PubMed
- Danielsen K, Olsen AO, Wilsgaard T ym. Is the prevalence of psoriasis increasing? A 30-year follow-up of a population-based cohort. Br J Dermatol 2013;168:1303-10 «PMID: 23374051»PubMed
- Svensson A, Ofenloch RF, Bruze M ym. Prevalence of skin disease in a population-based sample of adults from five European countries. Br J Dermatol 2018;178:1111-1118 «PMID: 29247509»PubMed
- Egeberg A, Andersen YMF, Thyssen JP. Prevalence and characteristics of psoriasis in Denmark: findings from the Danish skin cohort. BMJ Open 2019;9:e028116 «PMID: 30898836»PubMed
- Burden-Teh E, Thomas KS, Ratib S ym. The epidemiology of childhood psoriasis: a scoping review. Br J Dermatol 2016;174:1242-57 «PMID: 26928555»PubMed
- Tollefson MM, Crowson CS, McEvoy MT ym. Incidence of psoriasis in children: a population-based study. J Am Acad Dermatol 2010;62:979-87 «PMID: 19962785»PubMed
- Huerta C, Rivero E, Rodríguez LA. Incidence and risk factors for psoriasis in the general population. Arch Dermatol 2007;143:1559-65 «PMID: 18087008»PubMed
- Icen M, Crowson CS, McEvoy MT ym. Trends in incidence of adult-onset psoriasis over three decades: a population-based study. J Am Acad Dermatol 2009;60:394-401 «PMID: 19231638»PubMed
- Henseler T, Christophers E. Psoriasis of early and late onset: characterization of two types of psoriasis vulgaris. J Am Acad Dermatol 1985;13:450-6 «PMID: 4056119»PubMed
- Lønnberg AS, Skov L, Duffy DL ym. Genetic Factors Explain Variation in the Age at Onset of Psoriasis: A Population-based Twin Study. Acta Derm Venereol 2016;96:35-8 «PMID: 26073043»PubMed
- Vogel SA, Yentzer B, Davis SA ym. Trends in pediatric psoriasis outpatient health care delivery in the United States. Arch Dermatol 2012;148:66-71 «PMID: 21931013»PubMed
- Gelfand JM, Gladman DD, Mease PJ ym. Epidemiology of psoriatic arthritis in the population of the United States. J Am Acad Dermatol 2005;53:573 «PMID: 16198775»PubMed
- Madland TM, Apalset EM, Johannessen AE ym. Prevalence, disease manifestations, and treatment of psoriatic arthritis in Western Norway. J Rheumatol 2005;32:1918-22 «PMID: 16206347»PubMed
- Wilson FC, Icen M, Crowson CS ym. Time trends in epidemiology and characteristics of psoriatic arthritis over 3 decades: a population-based study. J Rheumatol 2009;36:361-7 «PMID: 19208565»PubMed
- Kaipiainen-Seppänen O. Incidence of psoriatic arthritis in Finland. Br J Rheumatol 1996;35:1289-91 «PMID: 9010058»PubMed
- Alamanos Y, Voulgari PV, Drosos AA. Incidence and prevalence of psoriatic arthritis: a systematic review. J Rheumatol 2008;35:1354-8 «PMID: 18464305»PubMed
- Wilson FC, Icen M, Crowson CS ym. Incidence and clinical predictors of psoriatic arthritis in patients with psoriasis: a population-based study. Arthritis Rheum 2009;61:233-9 «PMID: 19177544»PubMed
- Prey S, Paul C, Bronsard V ym. Assessment of risk of psoriatic arthritis in patients with plaque psoriasis: a systematic review of the literature. J Eur Acad Dermatol Venereol 2010;24 Suppl 2:31-5 «PMID: 20443998»PubMed
- Christophers E, Barker JN, Griffiths CE ym. The risk of psoriatic arthritis remains constant following initial diagnosis of psoriasis among patients seen in European dermatology clinics. J Eur Acad Dermatol Venereol 2010;24:548-54 «PMID: 19874432»PubMed
- Gladman DD, Shuckett R, Russell ML ym. Psoriatic arthritis (PSA)--an analysis of 220 patients. Q J Med 1987;62:127-41 «PMID: 3659255»PubMed
- Berntson L, Andersson Gäre B, Fasth A ym. Incidence of juvenile idiopathic arthritis in the Nordic countries. A population based study with special reference to the validity of the ILAR and EULAR criteria. J Rheumatol 2003;30:2275-82 «PMID: 14528529»PubMed
- Savolainen E, Kaipiainen-Seppänen O, Kröger L ym. Total incidence and distribution of inflammatory joint diseases in a defined population: results from the Kuopio 2000 arthritis survey. J Rheumatol 2003;30:2460-8 «PMID: 14677193»PubMed
- Virta R, Helenius H, Klaukka T. Lasten reuma yleistyy Suomessa. Suom Lääkäril 2008;63:2806-9
- Icen M, Crowson CS, McEvoy MT ym. Trends in incidence of adult-onset psoriasis over three decades: a population-based study. J Am Acad Dermatol 2009;60:394-401 «PMID: 19231638»PubMed
- Dand N, Mahil SK, Capon F ym. Psoriasis and Genetics. Acta Derm Venereol 2020;100:adv00030 «PMID: 31971603»PubMed
- Lomholt G. Psoriasis. Prevalence, Spontaneous Course, and Genetics; a Census Study on the Prevalence of Skin Diseases on the Faroe Islands. GEC Gad, Copenhagen 1963;
- Swanbeck G, Inerot A, Martinsson T ym. Genetic counselling in psoriasis: empirical data on psoriasis among first-degree relatives of 3095 psoriatic probands. Br J Dermatol 1997;137:939-42 «PMID: 9470911»PubMed
- Asumalahti K, Saarialho-Kere U, Kere J. [The pathogenesis of psoriasis--investigating the genetics of a multifactorial disease]. Duodecim 2003;119:1517-22 «PMID: 14535024»PubMed
- Andressen C, Henseler T. [Inheritance of psoriasis. Analysis of 2035 family histories]. Hautarzt 1982;33:214-7 «PMID: 7096085»PubMed
- Mallbris L, Larsson P, Bergqvist S ym. Psoriasis phenotype at disease onset: clinical characterization of 400 adult cases. J Invest Dermatol 2005;124:499-504 «PMID: 15737189»PubMed
- Harden JL, Krueger JG, Bowcock AM. The immunogenetics of Psoriasis: A comprehensive review. J Autoimmun 2015;64:66-73 «PMID: 26215033»PubMed
- Arakawa A, Siewert K, Stöhr J ym. Melanocyte antigen triggers autoimmunity in human psoriasis. J Exp Med 2015;212:2203-12 «PMID: 26621454»PubMed
- Lande R, Botti E, Jandus C ym. The antimicrobial peptide LL37 is a T-cell autoantigen in psoriasis. Nat Commun 2014;5:5621 «PMID: 25470744»PubMed
- Cheung KL, Jarrett R, Subramaniam S ym. Psoriatic T cells recognize neolipid antigens generated by mast cell phospholipase delivered by exosomes and presented by CD1a. J Exp Med 2016;213:2399-2412 «PMID: 27670592»PubMed
- Gudjonsson JE, Thorarinsson AM, Sigurgeirsson B ym. Streptococcal throat infections and exacerbation of chronic plaque psoriasis: a prospective study. Br J Dermatol 2003;149:530-4 «PMID: 14510985»PubMed
- Seville RH. Stress and psoriasis: the importance of insight and empathy in prognosis. J Am Acad Dermatol 1989;20:97-100 «PMID: 2643644»PubMed
- Naldi L, Peli L, Parazzini F ym. Family history of psoriasis, stressful life events, and recent infectious disease are risk factors for a first episode of acute guttate psoriasis: results of a case-control study. J Am Acad Dermatol 2001;44:433-8 «PMID: 11209111»PubMed
- Li WQ, Qureshi AA, Schernhammer ES ym. Rotating night-shift work and risk of psoriasis in US women. J Invest Dermatol 2013;133:565-7 «PMID: 22931920»PubMed
- Dominguez PL, Han J, Li T ym. Depression and the risk of psoriasis in US women. J Eur Acad Dermatol Venereol 2013;27:1163-7 «PMID: 23030685»PubMed
- Wu S, Li WQ, Han J ym. Hypercholesterolemia and risk of incident psoriasis and psoriatic arthritis in US women. Arthritis Rheumatol 2014;66:304-10 «PMID: 24504802»PubMed
- Naldi L, Chatenoud L, Linder D ym. Cigarette smoking, body mass index, and stressful life events as risk factors for psoriasis: results from an Italian case-control study. J Invest Dermatol 2005;125:61-7 «PMID: 15982303»PubMed
- Setty AR, Curhan G, Choi HK. Obesity, waist circumference, weight change, and the risk of psoriasis in women: Nurses' Health Study II. Arch Intern Med 2007;167:1670-5 «PMID: 17698691»PubMed
- Wolk K, Mallbris L, Larsson P ym. Excessive body weight and smoking associates with a high risk of onset of plaque psoriasis. Acta Derm Venereol 2009;89:492-7 «PMID: 19734975»PubMed
- Li W, Han J, Choi HK ym. Smoking and risk of incident psoriasis among women and men in the United States: a combined analysis. Am J Epidemiol 2012;175:402-13 «PMID: 22247049»PubMed
- Setty AR, Curhan G, Choi HK. Smoking and the risk of psoriasis in women: Nurses' Health Study II. Am J Med 2007;120:953-9 «PMID: 17976422»PubMed
- Poikolainen K, Reunala T, Karvonen J ym. Alcohol intake: a risk factor for psoriasis in young and middle aged men? BMJ 1990;300:780-3 «PMID: 1969757»PubMed
- Qureshi AA, Dominguez PL, Choi HK ym. Alcohol intake and risk of incident psoriasis in US women: a prospective study. Arch Dermatol 2010;146:1364-9 «PMID: 20713772»PubMed
- Ockenfels HM. [Trigger factors for psoriasis]. Hautarzt 2003;54:215-23 «PMID: 12634989»PubMed
- Poikolainen K, Reunala T, Karvonen J. Smoking, alcohol and life events related to psoriasis among women. Br J Dermatol 1994;130:473-7 «PMID: 8186112»PubMed
- Keller JJ, Wu CS, Lin HC. Increased risk of psoriasis following chronic rhinosinusitis without nasal polyps: a population-based matched-cohort study. Br J Dermatol 2013;168:289-94 «PMID: 23013326»PubMed
- Thorleifsdottir RH, Eysteinsdóttir JH, Olafsson JH ym. Throat Infections are Associated with Exacerbation in a Substantial Proportion of Patients with Chronic Plaque Psoriasis. Acta Derm Venereol 2016;96:788-91 «PMID: 26984718»PubMed
- Dika E, Varotti C, Bardazzi F ym. Drug-induced psoriasis: an evidence-based overview and the introduction of psoriatic drug eruption probability score. Cutan Ocul Toxicol 2006;25:1-11 «PMID: 16702050»PubMed
- Harrison MJ, Dixon WG, Watson KD ym. Rates of new-onset psoriasis in patients with rheumatoid arthritis receiving anti-tumour necrosis factor alpha therapy: results from the British Society for Rheumatology Biologics Register. Ann Rheum Dis 2009;68:209-15 «PMID: 18385277»PubMed
- Shmidt E, Wetter DA, Ferguson SB ym. Psoriasis and palmoplantar pustulosis associated with tumor necrosis factor-a inhibitors: the Mayo Clinic experience, 1998 to 2010. J Am Acad Dermatol 2012;67:e179-85 «PMID: 21752492»PubMed
- Guerra I, Algaba A, Pérez-Calle JL ym. Induction of psoriasis with anti-TNF agents in patients with inflammatory bowel disease: a report of 21 cases. J Crohns Colitis 2012;6:518-23 «PMID: 22398059»PubMed
- Brauchli YB, Jick SS, Curtin F ym. Association between beta-blockers, other antihypertensive drugs and psoriasis: population-based case-control study. Br J Dermatol 2008;158:1299-307 «PMID: 18410416»PubMed
- Karason A, Love TJ, Gudbjornsson B. A strong heritability of psoriatic arthritis over four generations--the Reykjavik Psoriatic Arthritis Study. Rheumatology (Oxford) 2009;48:1424-8 «PMID: 19741010»PubMed
- Green A, Shaddick G, Charlton R ym. Modifiable risk factors and the development of psoriatic arthritis in people with psoriasis. Br J Dermatol 2020;182:714-720 «PMID: 31209855»PubMed
- Eder L, Harvey P, Chandran V ym. Gaps in Diagnosis and Treatment of Cardiovascular Risk Factors in Patients with Psoriatic Disease: An International Multicenter Study. J Rheumatol 2018;45:378-384 «PMID: 29419462»PubMed
- Eder L, Shanmugarajah S, Thavaneswaran A ym. The association between smoking and the development of psoriatic arthritis among psoriasis patients. Ann Rheum Dis 2012;71:219-24 «PMID: 21953342»PubMed
- Pezzolo E, Naldi L. The relationship between smoking, psoriasis and psoriatic arthritis. Expert Rev Clin Immunol 2019;15:41-48 «PMID: 30380949»PubMed
- Zhao SS, Goodson NJ, Robertson S ym. Smoking in spondyloarthritis: unravelling the complexities. Rheumatology (Oxford) 2020;59:1472-1481 «PMID: 32236486»PubMed
- Tsuruta N, Imafuku S, Narisawa Y. Hyperuricemia is an independent risk factor for psoriatic arthritis in psoriatic patients. J Dermatol 2017;44:1349-1352 «PMID: 28691207»PubMed
- Neimann AL, Shin DB, Wang X ym. Prevalence of cardiovascular risk factors in patients with psoriasis. J Am Acad Dermatol 2006;55:829-35 «PMID: 17052489»PubMed
- Mallbris L, Ritchlin CT, Ståhle M. Metabolic disorders in patients with psoriasis and psoriatic arthritis. Curr Rheumatol Rep 2006;8:355-63 «PMID: 16973109»PubMed
- Husted JA, Thavaneswaran A, Chandran V ym. Cardiovascular and other comorbidities in patients with psoriatic arthritis: a comparison with patients with psoriasis. Arthritis Care Res (Hoboken) 2011;63:1729-35 «PMID: 21905258»PubMed
- McAleer MA, Mason DL, Cunningham S ym. Alcohol misuse in patients with psoriasis: identification and relationship to disease severity and psychological distress. Br J Dermatol 2011;164:1256-61 «PMID: 21457207»PubMed
- Mehta NN, Azfar RS, Shin DB ym. Patients with severe psoriasis are at increased risk of cardiovascular mortality: cohort study using the General Practice Research Database. Eur Heart J 2010;31:1000-6 «PMID: 20037179»PubMed
- Gelfand JM, Troxel AB, Lewis JD ym. The risk of mortality in patients with psoriasis: results from a population-based study. Arch Dermatol 2007;143:1493-9 «PMID: 18086997»PubMed
- Abuabara K, Azfar RS, Shin DB ym. Cause-specific mortality in patients with severe psoriasis: a population-based cohort study in the U.K. Br J Dermatol 2010;163:586-92 «PMID: 20633008»PubMed
- Cohen AD, Dreiher J, Birkenfeld S. Psoriasis associated with ulcerative colitis and Crohn's disease. J Eur Acad Dermatol Venereol 2009;23:561-5 «PMID: 19207663»PubMed
- Ludvigsson JF, Lindelöf B, Zingone F ym. Psoriasis in a nationwide cohort study of patients with celiac disease. J Invest Dermatol 2011;131:2010-6 «PMID: 21654830»PubMed
- Rehal B, Modjtahedi BS, Morse LS ym. Ocular psoriasis. J Am Acad Dermatol 2011;65:1202-12 «PMID: 21550135»PubMed
- Boffetta P, Gridley G, Lindelöf B. Cancer risk in a population-based cohort of patients hospitalized for psoriasis in Sweden. J Invest Dermatol 2001;117:1531-7 «PMID: 11886519»PubMed
- Brauchli YB, Jick SS, Miret M ym. Psoriasis and risk of incident cancer: an inception cohort study with a nested case-control analysis. J Invest Dermatol 2009;129:2604-12 «PMID: 19440219»PubMed
- Chen YJ, Wu CY, Chen TJ ym. The risk of cancer in patients with psoriasis: a population-based cohort study in Taiwan. J Am Acad Dermatol 2011;65:84-91 «PMID: 21458106»PubMed
- Schmitt J, Ford DE. Psoriasis is independently associated with psychiatric morbidity and adverse cardiovascular risk factors, but not with cardiovascular events in a population-based sample. J Eur Acad Dermatol Venereol 2010;24:885-92 «PMID: 20015170»PubMed
- Kurd SK, Troxel AB, Crits-Christoph P ym. The risk of depression, anxiety, and suicidality in patients with psoriasis: a population-based cohort study. Arch Dermatol 2010;146:891-5 «PMID: 20713823»PubMed
- De Lorenzis E, Natalello G, Bruno D ym. Psoriatic arthritis and depressive symptoms: does systemic inflammation play a role? Clin Rheumatol 2021;40:1893-1902 «PMID: 33009969»PubMed
- Augustin M, Radtke MA, Glaeske G ym. Epidemiology and Comorbidity in Children with Psoriasis and Atopic Eczema. Dermatology 2015;231:35-40 «PMID: 25966818»PubMed
- Finlay AY, Coles EC. The effect of severe psoriasis on the quality of life of 369 patients. Br J Dermatol 1995;132:236-44 «PMID: 7888360»PubMed
- Rapp SR, Feldman SR, Exum ML ym. Psoriasis causes as much disability as other major medical diseases. J Am Acad Dermatol 1999;41:401-7 «PMID: 10459113»PubMed
- Burden AD, Hilton Boon M, Leman J ym. Diagnosis and management of psoriasis and psoriatic arthritis in adults: summary of SIGN guidance. BMJ 2010;341:c5623 «PMID: 21036815»PubMed
- Ahlehoff O, Gislason GH, Charlot M ym. Psoriasis is associated with clinically significant cardiovascular risk: a Danish nationwide cohort study. J Intern Med 2011;270:147-57 «PMID: 21114692»PubMed
- Gelfand JM, Troxel AB, Lewis JD ym. The risk of mortality in patients with psoriasis: results from a population-based study. Arch Dermatol 2007;143:1493-9 «PMID: 18086997»PubMed
- Daudén E, Puig L, Ferrándiz C ym. Consensus document on the evaluation and treatment of moderate-to-severe psoriasis: Psoriasis Group of the Spanish Academy of Dermatology and Venereology. J Eur Acad Dermatol Venereol 2016;30 Suppl 2:1-18 «PMID: 26812550»PubMed
- Strober B, Ryan C, van de Kerkhof P ym. Recategorization of psoriasis severity: Delphi consensus from the International Psoriasis Council. J Am Acad Dermatol 2020;82:117-122 «PMID: 31425723»PubMed
- Lodén M. Role of topical emollients and moisturizers in the treatment of dry skin barrier disorders. Am J Clin Dermatol 2003;4:771-88 «PMID: 14572299»PubMed
- Lebwohl M. The role of salicylic acid in the treatment of psoriasis. Int J Dermatol 1999;38:16-24 «PMID: 10065604»PubMed
- Fetil E, Ozka S, Soyal MC ym. Effects of topical petrolatum and salicylic acid on the erythemogenicity of UVB. Eur J Dermatol 2002;12:154-6 «PMID: 11872412»PubMed
- Lebwohl M, Martinez J, Weber P ym. Effects of topical preparations on the erythemogenicity of UVB: implications for psoriasis phototherapy. J Am Acad Dermatol 1995;32:469-71 «PMID: 7868718»PubMed
- Surber C, Itin PH, Bircher AJ ym. Topical corticosteroids. J Am Acad Dermatol 1995;32:1025-30 «PMID: 7751447»PubMed
- Mason J, Mason AR, Cork MJ. Topical preparations for the treatment of psoriasis: a systematic review. Br J Dermatol 2002;146:351-64 «PMID: 11952534»PubMed
- Haapasaari KM, Risteli J, Oikarinen A. Recovery of human skin collagen synthesis after short-term topical corticosteroid treatment and comparison between young and old subjects. Br J Dermatol 1996;135:65-9 «PMID: 8776361»PubMed
- Murdoch D, Clissold SP. Calcipotriol. A review of its pharmacological properties and therapeutic use in psoriasis vulgaris. Drugs 1992;43:415-29 «PMID: 1374321»PubMed
- Liu X, Liu Y, Xu M ym. Zinc finger protein A20 is involved in the antipsoriatic effect of calcipotriol. Br J Dermatol 2016;175:314-24 «PMID: 26875609»PubMed
- Germán B, Wei R, Hener P ym. Disrupting the IL-36 and IL-23/IL-17 loop underlies the efficacy of calcipotriol and corticosteroid therapy for psoriasis. JCI Insight 2019;4: «PMID: 30674716»PubMed
- Barnes L, Altmeyer P, Fôrstrôm L ym. Long-term treatment of psoriasis with calcipotriol scalp solution and cream. Eur J Dermatol 2000;10:199-204 «PMID: 10725818»PubMed
- Ramsay CA, Berth-Jones J, Brundin G ym. Long-term use of topical calcipotriol in chronic plaque psoriasis. Dermatology 1994;189:260-4 «PMID: 7949479»PubMed
- Bruner CR, Feldman SR, Ventrapragada M ym. A systematic review of adverse effects associated with topical treatments for psoriasis. Dermatol Online J 2003;9:2 «PMID: 12639460»PubMed
- Carboni I, de Felice C, Bergamin A ym. Topical use of calcitriol 3 microg/g ointment in the treatment of mild-to-moderate psoriasis: results from an open-label study. J Eur Acad Dermatol Venereol 2005;19 Suppl 3:11-3 «PMID: 16274406»PubMed
- Ortonne JP, Humbert P, Nicolas JF ym. Intra-individual comparison of the cutaneous safety and efficacy of calcitriol 3 microg g(-1) ointment and calcipotriol 50 microg g(-1) ointment on chronic plaque psoriasis localized in facial, hairline, retroauricular or flexural areas. Br J Dermatol 2003;148:326-33 «PMID: 12588387»PubMed
- Bourke JF, Iqbal SJ, Hutchinson PE. Vitamin D analogues in psoriasis: effects on systemic calcium homeostasis. Br J Dermatol 1996;135:347-54 «PMID: 8949424»PubMed
- Berth-Jones J, Bourke JF, Iqbal SJ ym. Urine calcium excretion during treatment of psoriasis with topical calcipotriol. Br J Dermatol 1993;129:411-4 «PMID: 8217755»PubMed
- Koo J, Tyring S, Werschler WP ym. Superior efficacy of calcipotriene and betamethasone dipropionate aerosol foam versus ointment in patients with psoriasis vulgaris--A randomized phase II study. J Dermatolog Treat 2016;27:120-7 «PMID: 26444907»PubMed
- Paul C, Stein Gold L, Cambazard F ym. Calcipotriol plus betamethasone dipropionate aerosol foam provides superior efficacy vs. gel in patients with psoriasis vulgaris: randomized, controlled PSO-ABLE study. J Eur Acad Dermatol Venereol 2017;31:119-126 «PMID: 27531752»PubMed
- Zonneveld IM, Rubins A, Jablonska S ym. Topical tacrolimus is not effective in chronic plaque psoriasis. A pilot study. Arch Dermatol 1998;134:1101-2 «PMID: 9762021»PubMed
- Harth W, Caffier PP, Mayelzadeh B ym. Topical tacrolimus treatment for chronic dermatitis of the ear. Eur J Dermatol 2007;17:405-11 «PMID: 17673384»PubMed
- Crowley JJ, Weinberg JM, Wu JJ ym. Treatment of nail psoriasis: best practice recommendations from the Medical Board of the National Psoriasis Foundation. JAMA Dermatol 2015;151:87-94 «PMID: 25471223»PubMed
- Gümüsel M, Özdemir M, Mevlitoglu I ym. Evaluation of the efficacy of methotrexate and cyclosporine therapies on psoriatic nails: a one-blind, randomized study. J Eur Acad Dermatol Venereol 2011;25:1080-4 «PMID: 21118309»PubMed
- Jiaravuthisan MM, Sasseville D, Vender RB ym. Psoriasis of the nail: anatomy, pathology, clinical presentation, and a review of the literature on therapy. J Am Acad Dermatol 2007;57:1-27 «PMID: 17572277»PubMed
- Tosti A, Ricotti C, Romanelli P ym. Evaluation of the efficacy of acitretin therapy for nail psoriasis. Arch Dermatol 2009;145:269-71 «PMID: 19289755»PubMed
- Yones SS, Palmer RA, Garibaldinos TT ym. Randomized double-blind trial of the treatment of chronic plaque psoriasis: efficacy of psoralen-UV-A therapy vs narrowband UV-B therapy. Arch Dermatol 2006;142:836-42 «PMID: 16847198»PubMed
- Hearn RM, Kerr AC, Rahim KF ym. Incidence of skin cancers in 3867 patients treated with narrow-band ultraviolet B phototherapy. Br J Dermatol 2008;159:931-5 «PMID: 18834483»PubMed
- Ibbotson SH, Bilsland D, Cox NH ym. An update and guidance on narrowband ultraviolet B phototherapy: a British Photodermatology Group Workshop Report. Br J Dermatol 2004;151:283-97 «PMID: 15327535»PubMed
- Diffey BL. Factors affecting the choice of a ceiling on the number of exposures with TL01 ultraviolet B phototherapy. Br J Dermatol 2003;149:428-30 «PMID: 12932263»PubMed
- Koek MB, Buskens E, van Weelden H ym. Home versus outpatient ultraviolet B phototherapy for mild to severe psoriasis: pragmatic multicentre randomised controlled non-inferiority trial (PLUTO study). BMJ 2009;338:b1542 «PMID: 19423623»PubMed
- Koek MB, Sigurdsson V, van Weelden H ym. Cost effectiveness of home ultraviolet B phototherapy for psoriasis: economic evaluation of a randomised controlled trial (PLUTO study). BMJ 2010;340:c1490 «PMID: 20406865»PubMed
- Koek MB, Buskens E, Bruijnzeel-Koomen CA ym. Home ultraviolet B phototherapy for psoriasis: discrepancy between literature, guidelines, general opinions and actual use. Results of a literature review, a web search, and a questionnaire among dermatologists. Br J Dermatol 2006;154:701-11 «PMID: 16536814»PubMed
- Koek MB, Buskens E, Steegmans PH ym. UVB phototherapy in an outpatient setting or at home: a pragmatic randomised single-blind trial designed to settle the discussion. The PLUTO study. BMC Med Res Methodol 2006;6:39 «PMID: 16882343»PubMed
- Voss A, Leverkus M, Bröcker EB ym. Topical psoralen photochemotherapy with lethal outcome. Arch Dermatol 2001;137:383 «PMID: 11255360»PubMed
- Hannuksela-Svahn A, Pukkala E, Koulu L ym. Cancer incidence among Finnish psoriasis patients treated with 8-methoxypsoralen bath PUVA. J Am Acad Dermatol 1999;40:694-6 «PMID: 10321595»PubMed
- Stern RS, Liebman EJ, Väkevä L. Oral psoralen and ultraviolet-A light (PUVA) treatment of psoriasis and persistent risk of nonmelanoma skin cancer. PUVA Follow-up Study. J Natl Cancer Inst 1998;90:1278-84 «PMID: 9731734»PubMed
- Stern RS, PUVA Follow up Study.. The risk of melanoma in association with long-term exposure to PUVA. J Am Acad Dermatol 2001;44:755-61 «PMID: 11312420»PubMed
- Griffiths CE, Clark CM, Chalmers RJ ym. A systematic review of treatments for severe psoriasis. Health Technol Assess 2000;4:1-125 «PMID: 11207450»PubMed
- Stern RS, Lunder EJ. Risk of squamous cell carcinoma and methoxsalen (psoralen) and UV-A radiation (PUVA). A meta-analysis. Arch Dermatol 1998;134:1582-5 «PMID: 9875197»PubMed
- Lebwohl M, Menter A, Koo J ym. Combination therapy to treat moderate to severe psoriasis. J Am Acad Dermatol 2004;50:416-30 «PMID: 14988684»PubMed
- Sugie N, Fujii N, Danno K. Cyclosporin-A suppresses p53-dependent repair DNA synthesis and apoptosis following ultraviolet-B irradiation. Photodermatol Photoimmunol Photomed 2002;18:163-8 «PMID: 12390669»PubMed
- Paul CF, Ho VC, McGeown C ym. Risk of malignancies in psoriasis patients treated with cyclosporine: a 5 y cohort study. J Invest Dermatol 2003;120:211-6 «PMID: 12542524»PubMed
- Marcil I, Stern RS. Squamous-cell cancer of the skin in patients given PUVA and ciclosporin: nested cohort crossover study. Lancet 2001;358:1042-5 «PMID: 11589933»PubMed
- Murphy GM. Skin cancer in patients with psoriasis-many intertwined risk factors. Br J Dermatol 1999;141:1001-2 «PMID: 10606842»PubMed
- Snellman E. E. Heliotherapy of psoriasis (thesis). Publications of the Social Insurance Institution, Finland, ML 124 1993;
- Puig L. PASI90 response: the new standard in therapeutic efficacy for psoriasis. J Eur Acad Dermatol Venereol 2015;29:645-8 «PMID: 25370811»PubMed
- Strober B, Papp KA, Lebwohl M ym. Clinical meaningfulness of complete skin clearance in psoriasis. J Am Acad Dermatol 2016;75:77-82.e7 «PMID: 27206759»PubMed
- Elewski BE, Puig L, Mordin M ym. Psoriasis patients with psoriasis Area and Severity Index (PASI) 90 response achieve greater health-related quality-of-life improvements than those with PASI 75-89 response: results from two phase 3 studies of secukinumab. J Dermatolog Treat 2017;28:492-499 «PMID: 28266243»PubMed
- Sbidian E, Maza A, Montaudié H ym. Efficacy and safety of oral retinoids in different psoriasis subtypes: a systematic literature review. J Eur Acad Dermatol Venereol 2011;25 Suppl 2:28-33 «PMID: 21388456»PubMed
- Gollnick H, Bauer R, Brindley C ym. Acitretin versus etretinate in psoriasis. Clinical and pharmacokinetic results of a German multicenter study. J Am Acad Dermatol 1988;19:458-68 «PMID: 2971692»PubMed
- Ruzicka T, Sommerburg C, Braun-Falco O ym. Efficiency of acitretin in combination with UV-B in the treatment of severe psoriasis. Arch Dermatol 1990;126:482-6 «PMID: 2138875»PubMed
- Warren RB, Weatherhead SC, Smith CH ym. British Association of Dermatologists' guidelines for the safe and effective prescribing of methotrexate for skin disease 2016. Br J Dermatol 2016;175:23-44 «PMID: 27484275»PubMed
- Anttila VJ, Haapamäki J, Peltomaa R ym. [Interruption of biological drugs in patients affected with inflammatory diseases]. Duodecim 2016;132:369-76 «PMID: 27017789»PubMed
- Ryan C, Amor KT, Menter A. The use of cyclosporine in dermatology: part II. J Am Acad Dermatol 2010;63:949-72; quiz 973-4 «PMID: 21093660»PubMed
- Koo J, Lebwohl M. Duration of remission of psoriasis therapies. J Am Acad Dermatol 1999;41:51-9 «PMID: 10411411»PubMed
- Berbis P, Geiger JM, Vaisse C ym. Benefit of progressively increasing doses during the initial treatment with acitretin in psoriasis. Dermatologica 1989;178:88-92 «PMID: 2522405»PubMed
- Murray HE, Anhalt AW, Lessard R ym. A 12-month treatment of severe psoriasis with acitretin: results of a Canadian open multicenter study. J Am Acad Dermatol 1991;24:598-602 «PMID: 1827800»PubMed
- Roenigk HH Jr, Callen JP, Guzzo CA ym. Effects of acitretin on the liver. J Am Acad Dermatol 1999;41:584-8 «PMID: 10495381»PubMed
- Kuitunen T, Malmström J, Palva E ym. Pancytopenia induced by low-dose methotrexate. A study of the cases reported to the Finnish Adverse Drug Reaction Register From 1991 to 1999. Scand J Rheumatol 2005;34:238-41 «PMID: 16134732»PubMed
- Lim AY, Gaffney K, Scott DG. Methotrexate-induced pancytopenia: serious and under-reported? Our experience of 25 cases in 5 years. Rheumatology (Oxford) 2005;44:1051-5 «PMID: 15901903»PubMed
- Whiting-O'Keefe QE, Fye KH, Sack KD. Methotrexate and histologic hepatic abnormalities: a meta-analysis. Am J Med 1991;90:711-6 «PMID: 1828327»PubMed
- Barker J, Horn EJ, Lebwohl M ym. Assessment and management of methotrexate hepatotoxicity in psoriasis patients: report from a consensus conference to evaluate current practice and identify key questions toward optimizing methotrexate use in the clinic. J Eur Acad Dermatol Venereol 2011;25:758-64 «PMID: 21198946»PubMed
- Kent PD, Luthra HS, Michet C Jr. Risk factors for methotrexate-induced abnormal laboratory monitoring results in patients with rheumatoid arthritis. J Rheumatol 2004;31:1727-31 «PMID: 15338491»PubMed
- Alarcón GS, Kremer JM, Macaluso M ym. Risk factors for methotrexate-induced lung injury in patients with rheumatoid arthritis. A multicenter, case-control study. Methotrexate-Lung Study Group. Ann Intern Med 1997;127:356-64 «PMID: 9273826»PubMed
- Griffiths CE, Dubertret L, Ellis CN ym. Ciclosporin in psoriasis clinical practice: an international consensus statement. Br J Dermatol 2004;150 Suppl 67:11-23 «PMID: 15115441»PubMed
- Reich K, Gooderham M, Bewley A ym. Safety and efficacy of apremilast through 104 weeks in patients with moderate to severe psoriasis who continued on apremilast or switched from etanercept treatment: findings from the LIBERATE study. J Eur Acad Dermatol Venereol 2018;32:397-402 «PMID: 29220542»PubMed
- Mrowietz U, Szepietowski JC, Loewe R ym. Efficacy and safety of LAS41008 (dimethyl fumarate) in adults with moderate-to-severe chronic plaque psoriasis: a randomized, double-blind, Fumaderm® - and placebo-controlled trial (BRIDGE). Br J Dermatol 2017;176:615-623 «PMID: 27515097»PubMed
- Mrowietz U, Kragballe K, Reich K ym. Definition of treatment goals for moderate to severe psoriasis: a European consensus. Arch Dermatol Res 2011;303:1-10 «PMID: 20857129»PubMed
- Götestam Skorpen C, Hoeltzenbein M, Tincani A ym. The EULAR points to consider for use of antirheumatic drugs before pregnancy, and during pregnancy and lactation. Ann Rheum Dis 2016;75:795-810 «PMID: 26888948»PubMed
- Lecluse LL, Driessen RJ, Spuls PI ym. Extent and clinical consequences of antibody formation against adalimumab in patients with plaque psoriasis. Arch Dermatol 2010;146:127-32 «PMID: 20157022»PubMed
- Hoffmann JH, Hartmann M, Enk AH ym. Autoantibodies in psoriasis as predictors for loss of response and anti-infliximab antibody induction. Br J Dermatol 2011;165:1355-8 «PMID: 21801160»PubMed
- Kimball AB, Gordon KB, Fakharzadeh S ym. Long-term efficacy of ustekinumab in patients with moderate-to-severe psoriasis: results from the PHOENIX 1 trial through up to 3 years. Br J Dermatol 2012;166:861-72 «PMID: 22356258»PubMed
- Hsu L, Snodgrass BT, Armstrong AW. Antidrug antibodies in psoriasis: a systematic review. Br J Dermatol 2014;170:261-73 «PMID: 24117166»PubMed
- Germano V, Cattaruzza MS, Osborn J ym. Infection risk in rheumatoid arthritis and spondyloarthropathy patients under treatment with DMARDs, corticosteroids and TNF-a antagonists. J Transl Med 2014;12:77 «PMID: 24655394»PubMed
- Galloway JB, Hyrich KL, Mercer LK ym. Anti-TNF therapy is associated with an increased risk of serious infections in patients with rheumatoid arthritis especially in the first 6 months of treatment: updated results from the British Society for Rheumatology Biologics Register with special emphasis on risks in the elderly. Rheumatology (Oxford) 2011;50:124-31 «PMID: 20675706»PubMed
- García-Doval I, Hernández MV, Vanaclocha F ym. Should tumour necrosis factor antagonist safety information be applied from patients with rheumatoid arthritis to psoriasis? Rates of serious adverse events in the prospective rheumatoid arthritis BIOBADASER and psoriasis BIOBADADERM cohorts. Br J Dermatol 2017;176:643-649 «PMID: 27258623»PubMed
- Yiu ZZN, Exton LS, Jabbar-Lopez Z ym. Risk of Serious Infections in Patients with Psoriasis on Biologic Therapies: A Systematic Review and Meta-Analysis. J Invest Dermatol 2016;136:1584-1591 «PMID: 27085754»PubMed
- Dávila-Seijo P, Dauden E, Descalzo MA ym. Infections in Moderate to Severe Psoriasis Patients Treated with Biological Drugs Compared to Classic Systemic Drugs: Findings from the BIOBADADERM Registry. J Invest Dermatol 2017;137:313-321 «PMID: 27677836»PubMed
- Garcia-Doval I, Cohen AD, Cazzaniga S ym. Risk of serious infections, cutaneous bacterial infections, and granulomatous infections in patients with psoriasis treated with anti-tumor necrosis factor agents versus classic therapies: Prospective meta-analysis of Psonet registries. J Am Acad Dermatol 2017;76:299-308.e16 «PMID: 27693008»PubMed
- Reich K, Mrowietz U, Radtke MA ym. Drug safety of systemic treatments for psoriasis: results from The German Psoriasis Registry PsoBest. Arch Dermatol Res 2015;307:875-83 «PMID: 26358263»PubMed
- Gniadecki R, Bang B, Bryld LE ym. Comparison of long-term drug survival and safety of biologic agents in patients with psoriasis vulgaris. Br J Dermatol 2015;172:244-52 «PMID: 25132294»PubMed
- Papp K, Gottlieb AB, Naldi L ym. Safety Surveillance for Ustekinumab and Other Psoriasis Treatments From the Psoriasis Longitudinal Assessment and Registry (PSOLAR). J Drugs Dermatol 2015;14:706-14 «PMID: 26151787»PubMed
- Crowley JJ, Warren RB, Cather JC. Safety of selective IL-23p19 inhibitors for the treatment of psoriasis. J Eur Acad Dermatol Venereol 2019;33:1676-1684 «PMID: 31054215»PubMed
- Sahuquillo-Torralba A, Carretero G, Rivera R ym. The risk of urinary tract infections in patients with psoriasis on systemic medications in Biobadaderm Registry: A prospective cohort study. J Am Acad Dermatol 2020;82:738-741 «PMID: 31306726»PubMed
- Mariette X, Matucci-Cerinic M, Pavelka K ym. Malignancies associated with tumour necrosis factor inhibitors in registries and prospective observational studies: a systematic review and meta-analysis. Ann Rheum Dis 2011;70:1895-904 «PMID: 21885875»PubMed
- van Lümig PP, Driessen RJ, Berends MA ym. Safety of treatment with biologics for psoriasis in daily practice: 5-year data. J Eur Acad Dermatol Venereol 2012;26:283-91 «PMID: 21435026»PubMed
- Raaschou P, Simard JF, Asker Hagelberg C ym. Rheumatoid arthritis, anti-tumour necrosis factor treatment, and risk of squamous cell and basal cell skin cancer: cohort study based on nationwide prospectively recorded data from Sweden. BMJ 2016;352:i262 «PMID: 26823527»PubMed
- Raaschou P, Simard JF, Holmqvist M ym. Rheumatoid arthritis, anti-tumour necrosis factor therapy, and risk of malignant melanoma: nationwide population based prospective cohort study from Sweden. BMJ 2013;346:f1939 «PMID: 23568792»PubMed
- Nyboe Andersen N, Pasternak B, Basit S ym. Association between tumor necrosis factor-a antagonists and risk of cancer in patients with inflammatory bowel disease. JAMA 2014;311:2406-13 «PMID: 24938563»PubMed
- Papoutsaki M, Chimenti MS, Costanzo A ym. Adalimumab for severe psoriasis and psoriatic arthritis: an open-label study in 30 patients previously treated with other biologics. J Am Acad Dermatol 2007;57:269-75 «PMID: 17574299»PubMed
- Van Lümig PP, Lecluse LL, Driessen RJ ym. Switching from etanercept to adalimumab is effective and safe: results in 30 patients with psoriasis with primary failure, secondary failure or intolerance to etanercept. Br J Dermatol 2010;163:838-46 «PMID: 20649798»PubMed
- Woolf RT, Smith CH, Robertson K ym. Switching to adalimumab in patients with moderate to severe psoriasis who have failed on etanercept: a retrospective case cohort study. Br J Dermatol 2010;163:889-92 «PMID: 20854408»PubMed
- Strober BE, Poulin Y, Kerdel FA ym. Switching to adalimumab for psoriasis patients with a suboptimal response to etanercept, methotrexate, or phototherapy: efficacy and safety results from an open-label study. J Am Acad Dermatol 2011;64:671-81 «PMID: 21414495»PubMed
- Ortonne JP, Chimenti S, Reich K ym. Efficacy and safety of adalimumab in patients with psoriasis previously treated with anti-tumour necrosis factor agents: subanalysis of BELIEVE. J Eur Acad Dermatol Venereol 2011;25:1012-20 «PMID: 21214631»PubMed
- Papp K, Crowley J, Ortonne JP ym. Adalimumab for moderate to severe chronic plaque psoriasis: efficacy and safety of retreatment and disease recurrence following withdrawal from therapy. Br J Dermatol 2011;164:434-41 «PMID: 21083543»PubMed
- Chiu HY, Wang TS, Chan CC ym. Risk Factor Analysis for the Immunogenicity of Adalimumab Associated with Decreased Clinical Response in Chinese Patients with Psoriasis. Acta Derm Venereol 2015;95:711-6 «PMID: 25673333»PubMed
- Thaçi D, Ortonne JP, Chimenti S ym. A phase IIIb, multicentre, randomized, double-blind, vehicle-controlled study of the efficacy and safety of adalimumab with and without calcipotriol/betamethasone topical treatment in patients with moderate to severe psoriasis: the BELIEVE study. Br J Dermatol 2010;163:402-11 «PMID: 20377585»PubMed
- Bagel J. Adalimumab plus narrowband ultraviolet B light phototherapy for the treatment of moderate to severe psoriasis. J Drugs Dermatol 2011;10:366-71 «PMID: 21455546»PubMed
- Wolf P, Hofer A, Weger W ym. 311 nm ultraviolet B-accelerated response of psoriatic lesions in adalimumab-treated patients. Photodermatol Photoimmunol Photomed 2011;27:186-9 «PMID: 21729166»PubMed
- Heiberg MS, Koldingsnes W, Mikkelsen K ym. The comparative one-year performance of anti-tumor necrosis factor alpha drugs in patients with rheumatoid arthritis, psoriatic arthritis, and ankylosing spondylitis: results from a longitudinal, observational, multicenter study. Arthritis Rheum 2008;59:234-40 «PMID: 18240258»PubMed
- Schreiber S, Ben-Horin S, Leszczyszyn J ym. Randomized Controlled Trial: Subcutaneous vs Intravenous Infliximab CT-P13 Maintenance in Inflammatory Bowel Disease. Gastroenterology 2021;160:2340-53 «PMID: 33676969»PubMed
- Westhovens R, Wiland P, Zawadzki M ym. Efficacy, pharmacokinetics and safety of subcutaneous versus intravenous CT-P13 in rheumatoid arthritis: a randomized phase I/III trial. Rheumatology (Oxford) 2021;60:2277-87 «PMID: 33230526»PubMed
- Gordon KB, Foley P, Krueger JG ym. Bimekizumab efficacy and safety in moderate to severe plaque psoriasis (BE READY): a multicentre, double-blind, placebo-controlled, randomised withdrawal phase 3 trial. Lancet 2021;397:475-486 «PMID: 33549192»PubMed
- Reich K, Papp KA, Blauvelt A ym. Bimekizumab versus ustekinumab for the treatment of moderate to severe plaque psoriasis (BE VIVID): efficacy and safety from a 52-week, multicentre, double-blind, active comparator and placebo controlled phase 3 trial. Lancet 2021;397:487-498 «PMID: 33549193»PubMed
- Reich K, Warren RB, Lebwohl M ym. Bimekizumab versus Secukinumab in Plaque Psoriasis. N Engl J Med 2021;385:142-152 «PMID: 33891380»PubMed
- Warren RB, Blauvelt A, Bagel J ym. Bimekizumab versus Adalimumab in Plaque Psoriasis. N Engl J Med 2021;385:130-141 «PMID: 33891379»PubMed
- Blauvelt A, Papp KA, Merola JF ym. Bimekizumab for patients with moderate to severe plaque psoriasis: 60-week results from BE ABLE 2, a randomized, double-blinded, placebo-controlled, phase 2b extension study. J Am Acad Dermatol 2020;83:1367-1374 «PMID: 32473974»PubMed
- Papp KA, Reich K, Paul C ym. A prospective phase III, randomized, double-blind, placebo-controlled study of brodalumab in patients with moderate-to-severe plaque psoriasis. Br J Dermatol 2016;175:273-86 «PMID: 26914406»PubMed
- Lebwohl M, Strober B, Menter A ym. Phase 3 Studies Comparing Brodalumab with Ustekinumab in Psoriasis. N Engl J Med 2015;373:1318-28 «PMID: 26422722»PubMed
- Papp KA, Tyring S, Lahfa M ym. A global phase III randomized controlled trial of etanercept in psoriasis: safety, efficacy, and effect of dose reduction. Br J Dermatol 2005;152:1304-12 «PMID: 15948997»PubMed
- Gordon KB, Gottlieb AB, Leonardi CL ym. Clinical response in psoriasis patients discontinued from and then reinitiated on etanercept therapy. J Dermatolog Treat 2006;17:9-17 «PMID: 16467018»PubMed
- Moore A, Gordon KB, Kang S ym. A randomized, open-label trial of continuous versus interrupted etanercept therapy in the treatment of psoriasis. J Am Acad Dermatol 2007;56:598-603 «PMID: 17113190»PubMed
- Ortonne J, Griffiths C, Daudén Ey. Efficacy and safety of continuous versus paused etanercept treatment in patients with moderate-to-severe psoriasis over 54 weeks: the CRYSTEL study. Expert Rev Dermatol 2008;3:657-65
- Ortonne JP, Taïeb A, Ormerod AD ym. Patients with moderate-to-severe psoriasis recapture clinical response during re-treatment with etanercept. Br J Dermatol 2009;161:1190-5 «PMID: 19566665»PubMed
- Foley PA, Quirk C, Sullivan JR ym. Combining etanercept with traditional agents in the treatment of psoriasis: a review of the clinical evidence. J Eur Acad Dermatol Venereol 2010;24:1135-43 «PMID: 20337816»PubMed
- Zachariae C, Mørk NJ, Reunala T ym. The combination of etanercept and methotrexate increases the effectiveness of treatment in active psoriasis despite inadequate effect of methotrexate therapy. Acta Derm Venereol 2008;88:495-501 «PMID: 18779890»PubMed
- Gottlieb AB, Langley RG, Strober BE ym. A randomized, double-blind, placebo-controlled study to evaluate the addition of methotrexate to etanercept in patients with moderate to severe plaque psoriasis. Br J Dermatol 2012;167:649-57 «PMID: 22533447»PubMed
- Blauvelt A, Papp KA, Griffiths CE ym. Efficacy and safety of guselkumab, an anti-interleukin-23 monoclonal antibody, compared with adalimumab for the continuous treatment of patients with moderate to severe psoriasis: Results from the phase III, double-blinded, placebo- and active comparator-controlled VOYAGE 1 trial. J Am Acad Dermatol 2017;76:405-417 «PMID: 28057360»PubMed
- Reich K, Armstrong AW, Foley P ym. Efficacy and safety of guselkumab, an anti-interleukin-23 monoclonal antibody, compared with adalimumab for the treatment of patients with moderate to severe psoriasis with randomized withdrawal and retreatment: Results from the phase III, double-blind, placebo- and active comparator-controlled VOYAGE 2 trial. J Am Acad Dermatol 2017;76:418-431 «PMID: 28057361»PubMed
- Lecluse LL, Piskin G, Mekkes JR ym. Review and expert opinion on prevention and treatment of infliximab-related infusion reactions. Br J Dermatol 2008;159:527-36 «PMID: 18627374»PubMed
- Gordon KB, Strober B, Lebwohl M ym. Efficacy and safety of risankizumab in moderate-to-severe plaque psoriasis (UltIMMa-1 and UltIMMa-2): results from two double-blind, randomised, placebo-controlled and ustekinumab-controlled phase 3 trials. Lancet 2018;392:650-661 «PMID: 30097359»PubMed
- Blauvelt A, Reich K, Lebwohl M ym. Certolizumab pegol for the treatment of patients with moderate-to-severe chronic plaque psoriasis: pooled analysis of week 16 data from three randomized controlled trials. J Eur Acad Dermatol Venereol 2019;33:546-552 «PMID: 30242918»PubMed
- Gottlieb AB, Blauvelt A, Thaçi D ym. Certolizumab pegol for the treatment of chronic plaque psoriasis: Results through 48 weeks from 2 phase 3, multicenter, randomized, double-blinded, placebo-controlled studies (CIMPASI-1 and CIMPASI-2). J Am Acad Dermatol 2018;79:302-314.e6 «PMID: 29660421»PubMed
- Papp KA, Reich K, Blauvelt A ym. Efficacy of tildrakizumab for moderate-to-severe plaque psoriasis: pooled analysis of three randomized controlled trials at weeks 12 and 28. J Eur Acad Dermatol Venereol 2019;33:1098-1106 «PMID: 30838709»PubMed
- Leonardi CL, Kimball AB, Papp KA ym. Efficacy and safety of ustekinumab, a human interleukin-12/23 monoclonal antibody, in patients with psoriasis: 76-week results from a randomised, double-blind, placebo-controlled trial (PHOENIX 1). Lancet 2008;371:1665-74 «PMID: 18486739»PubMed
- Papp KA, Langley RG, Lebwohl M ym. Efficacy and safety of ustekinumab, a human interleukin-12/23 monoclonal antibody, in patients with psoriasis: 52-week results from a randomised, double-blind, placebo-controlled trial (PHOENIX 2). Lancet 2008;371:1675-84 «PMID: 18486740»PubMed
- Talamonti M, Galluzzo M, Chimenti S ym. HLA-C*06 and response to ustekinumab in Caucasian patients with psoriasis: Outcome and long-term follow-up. J Am Acad Dermatol 2016;74:374-5 «PMID: 26775778»PubMed
- Gordon KB, Papp KA, Langley RG ym. Long-term safety experience of ustekinumab in patients with moderate to severe psoriasis (Part II of II): results from analyses of infections and malignancy from pooled phase II and III clinical trials. J Am Acad Dermatol 2012;66:742-51 «PMID: 21978572»PubMed
- Warren RB, Smith CH, Yiu ZZN ym. Differential Drug Survival of Biologic Therapies for the Treatment of Psoriasis: A Prospective Observational Cohort Study from the British Association of Dermatologists Biologic Interventions Register (BADBIR). J Invest Dermatol 2015;135:2632-2640 «PMID: 26053050»PubMed
- Zweegers J, van den Reek JM, van de Kerkhof PC ym. Body mass index predicts discontinuation due to ineffectiveness and female sex predicts discontinuation due to side-effects in patients with psoriasis treated with adalimumab, etanercept or ustekinumab in daily practice: a prospective, comparative, long-term drug-survival study from the BioCAPTURE registry. Br J Dermatol 2016;175:340-7 «PMID: 26989852»PubMed
- Menter A, Papp KA, Gooderham M ym. Drug survival of biologic therapy in a large, disease-based registry of patients with psoriasis: results from the Psoriasis Longitudinal Assessment and Registry (PSOLAR). J Eur Acad Dermatol Venereol 2016;30:1148-58 «PMID: 27027388»PubMed
- Kalb RE, Fiorentino DF, Lebwohl MG ym. Risk of Serious Infection With Biologic and Systemic Treatment of Psoriasis: Results From the Psoriasis Longitudinal Assessment and Registry (PSOLAR). JAMA Dermatol 2015;151:961-9 «PMID: 25970800»PubMed
- Carretero G, Ferrandiz C, Dauden E ym. Risk of adverse events in psoriasis patients receiving classic systemic drugs and biologics in a 5-year observational study of clinical practice: 2008-2013 results of the Biobadaderm registry. J Eur Acad Dermatol Venereol 2015;29:156-63 «PMID: 24684267»PubMed
- Lebwohl M, Leonardi C, Griffiths CE ym. Long-term safety experience of ustekinumab in patients with moderate-to-severe psoriasis (Part I of II): results from analyses of general safety parameters from pooled Phase 2 and 3 clinical trials. J Am Acad Dermatol 2012;66:731-41 «PMID: 21930328»PubMed
- Reich K, Papp KA, Griffiths CE ym. An update on the long-term safety experience of ustekinumab: results from the psoriasis clinical development program with up to four years of follow-up. J Drugs Dermatol 2012;11:300-12 «PMID: 22395580»PubMed
- Kimball AB, Papp KA, Wasfi Y ym. Long-term efficacy of ustekinumab in patients with moderate-to-severe psoriasis treated for up to 5 years in the PHOENIX 1 study. J Eur Acad Dermatol Venereol 2013;27:1535-45 «PMID: 23279003»PubMed
- Langley RG, Lebwohl M, Krueger GG ym. Long-term efficacy and safety of ustekinumab, with and without dosing adjustment, in patients with moderate-to-severe psoriasis: results from the PHOENIX 2 study through 5 years of follow-up. Br J Dermatol 2015;172:1371-83 «PMID: 25307931»PubMed
- Nast A, Sporbeck B, Rosumeck S ym. Which antipsoriatic drug has the fastest onset of action? Systematic review on the rapidity of the onset of action. J Invest Dermatol 2013;133:1963-70 «PMID: 23426133»PubMed
- Egeberg A, Andersen YMF, Halling-Overgaard AS ym. Systematic review on rapidity of onset of action for interleukin-17 and interleukin-23 inhibitors for psoriasis. J Eur Acad Dermatol Venereol 2020;34:39-46 «PMID: 31465593»PubMed
- Armstrong AW, Puig L, Joshi A ym. Comparison of Biologics and Oral Treatments for Plaque Psoriasis: A Meta-analysis. JAMA Dermatol 2020;156:258-269 «PMID: 32022825»PubMed
- Sbidian E, Chaimani A, Garcia-Doval I ym. Systemic pharmacological treatments for chronic plaque psoriasis: a network meta-analysis. Cochrane Database Syst Rev 2021;4:CD011535 «PMID: 33871055»PubMed
- Gladman DD, Farewell V, Buskila D ym. Reliability of measurements of active and damaged joints in psoriatic arthritis. J Rheumatol 1990;17:62-4 «PMID: 2313676»PubMed
- Oriente P, Biondi-Oriente C, Scarpa R. Psoriatic arthritis. Clinical manifestations. Baillieres Clin Rheumatol 1994;8:277-94 «PMID: 8076388»PubMed
- Cohen MR, Reda DJ, Clegg DO. Baseline relationships between psoriasis and psoriatic arthritis: analysis of 221 patients with active psoriatic arthritis. Department of Veterans Affairs Cooperative Study Group on Seronegative Spondyloarthropathies. J Rheumatol 1999;26:1752-6 «PMID: 10451073»PubMed
- Cantini F, Salvarani C, Olivieri I ym. Distal extremity swelling with pitting edema in psoriatic arthritis: a case-control study. Clin Exp Rheumatol 2001;19:291-6 «PMID: 11407082»PubMed
- Coates LC, Baraliakos X, Blanco FJ ym. The Phenotype of Axial Spondyloarthritis: Is It Dependent on HLA-B27 Status? Arthritis Care Res (Hoboken) 2021;73:856-860 «PMID: 32100954»PubMed
- Chandran V. Psoriatic spondylitis or ankylosing spondylitis with psoriasis: same or different? Curr Opin Rheumatol 2019;31:329-334 «PMID: 31135567»PubMed
- Payet J, Goulvestre C, Bialé L ym. Anticyclic citrullinated peptide antibodies in rheumatoid and nonrheumatoid rheumatic disorders: experience with 1162 patients. J Rheumatol 2014;41:2395-402 «PMID: 25274898»PubMed
- Kane D. The role of ultrasound in the diagnosis and management of psoriatic arthritis. Curr Rheumatol Rep 2005;7:319-24 «PMID: 16045836»PubMed
- Dubash SR, De Marco G, Wakefield RJ ym. Ultrasound Imaging in Psoriatic Arthritis: What Have We Learnt in the Last Five Years? Front Med (Lausanne) 2020;7:487 «PMID: 32984374»PubMed
- Balint PV, Terslev L, Aegerter P ym. Reliability of a consensus-based ultrasound definition and scoring for enthesitis in spondyloarthritis and psoriatic arthritis: an OMERACT US initiative. Ann Rheum Dis 2018;77:1730-1735 «PMID: 30076154»PubMed
- Offidani A, Cellini A, Valeri G ym. Subclinical joint involvement in psoriasis: magnetic resonance imaging and X-ray findings. Acta Derm Venereol 1998;78:463-5 «PMID: 9833050»PubMed
- Mandl P, Navarro-Compán V, Terslev L ym. EULAR recommendations for the use of imaging in the diagnosis and management of spondyloarthritis in clinical practice. Ann Rheum Dis 2015;74:1327-39 «PMID: 25837448»PubMed
- Gossec L, Baraliakos X, Kerschbaumer A ym. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2019 update. Ann Rheum Dis 2020;79:700-712 «PMID: 32434812»PubMed
- Singh JA, Guyatt G, Ogdie A ym. Special Article: 2018 American College of Rheumatology/National Psoriasis Foundation Guideline for the Treatment of Psoriatic Arthritis. Arthritis Care Res (Hoboken) 2019;71:2-29 «PMID: 30499259»PubMed
- Coates LC, Kavanaugh A, Mease PJ ym. Group for Research and Assessment of Psoriasis and Psoriatic Arthritis 2015 Treatment Recommendations for Psoriatic Arthritis. Arthritis Rheumatol 2016;68:1060-71 «PMID: 26749174»PubMed
- Sumpton D, Kelly A, Tunnicliffe DJ ym. Patients' Perspectives and Experience of Psoriasis and Psoriatic Arthritis: A Systematic Review and Thematic Synthesis of Qualitative Studies. Arthritis Care Res (Hoboken) 2020;72:711-722 «PMID: 30927508»PubMed
- Coates LC, Orbai AM, Azevedo VF ym. Results of a global, patient-based survey assessing the impact of psoriatic arthritis discussed in the context of the Psoriatic Arthritis Impact of Disease (PsAID) questionnaire. Health Qual Life Outcomes 2020;18:173 «PMID: 32513190»PubMed
- Garrido-Cumbrera M, Hillmann O, Mahapatra R ym. Improving the Management of Psoriatic Arthritis and Axial Spondyloarthritis: Roundtable Discussions with Healthcare Professionals and Patients. Rheumatol Ther 2017;4:219-231 «PMID: 28600789»PubMed
- Coates LC, Mahmood F, Freeston J ym. Long-term follow-up of patients in the TIght COntrol of inflammation in early Psoriatic Arthritis (TICOPA) trial. Rheumatology (Oxford) 2020;59:807-810 «PMID: 31504996»PubMed
- Coates LC, Fransen J, Helliwell PS. Defining minimal disease activity in psoriatic arthritis: a proposed objective target for treatment. Ann Rheum Dis 2010;69:48-53 «PMID: 19147615»PubMed
- Dressler C, Eisert L, Pham PA ym. Efficacy and safety of systemic treatments in psoriatic arthritis: a systematic review, meta-analysis and GRADE evaluation. J Eur Acad Dermatol Venereol 2019;33:1249-1260 «PMID: 30735612»PubMed
- Nash P, Thaçi D, Behrens F ym. Leflunomide improves psoriasis in patients with psoriatic arthritis: an in-depth analysis of data from the TOPAS study. Dermatology 2006;212:238-49 «PMID: 16549920»PubMed
- Flint J, Panchal S, Hurrell A ym. BSR and BHPR guideline on prescribing drugs in pregnancy and breastfeeding-Part I: standard and biologic disease modifying anti-rheumatic drugs and corticosteroids. Rheumatology (Oxford) 2016;55:1693-7 «PMID: 26750124»PubMed
- Brent RL. Teratogen update: reproductive risks of leflunomide (Arava); a pyrimidine synthesis inhibitor: counseling women taking leflunomide before or during pregnancy and men taking leflunomide who are contemplating fathering a child. Teratology 2001;63:106-12 «PMID: 11241434»PubMed
- Baker H, Ryan TJ. Generalized pustular psoriasis. A clinical and epidemiological study of 104 cases. Br J Dermatol 1968;80:771-93 «PMID: 4236712»PubMed
- Burns D, Breathnach S, Cox N ym. Rook´s Textbook of Dermatology. Blackwell Publishing 2004;
- Kavanaugh A, Gladman DD, Edwards CJ ym. Long-term experience with apremilast in patients with psoriatic arthritis: 5-year results from a PALACE 1-3 pooled analysis. Arthritis Res Ther 2019;21:118 «PMID: 31077258»PubMed
- Nash P, Ohson K, Walsh J ym. Early and sustained efficacy with apremilast monotherapy in biological-naïve patients with psoriatic arthritis: a phase IIIB, randomised controlled trial (ACTIVE). Ann Rheum Dis 2018;77:690-698 «PMID: 29343507»PubMed
- Wells AF, Edwards CJ, Kivitz AJ ym. Apremilast monotherapy in DMARD-naive psoriatic arthritis patients: results of the randomized, placebo-controlled PALACE 4 trial. Rheumatology (Oxford) 2018;57:1253-1263 «PMID: 29635379»PubMed
- Nash P, Coates LC, Fleischmann R ym. Efficacy of Tofacitinib for the Treatment of Psoriatic Arthritis: Pooled Analysis of Two Phase 3 Studies. Rheumatol Ther 2018;5:567-582 «PMID: 30414064»PubMed
- Mease P, Hall S, FitzGerald O ym. Tofacitinib or Adalimumab versus Placebo for Psoriatic Arthritis. N Engl J Med 2017;377:1537-1550 «PMID: 29045212»PubMed
- Mease PJ, Lertratanakul A, Papp KA ym. Upadacitinib in Patients with Psoriatic Arthritis and Inadequate Response to Biologics: 56-Week Data from the Randomized Controlled Phase 3 SELECT-PsA 2 Study. Rheumatol Ther 2021;8:903-919 «PMID: 33913086»PubMed
- Arnett FC, Edworthy SM, Bloch DA ym. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis. Arthritis Rheum 1988;31:315-24 «PMID: 3358796»PubMed
- Gladman DD, Mease PJ, Ritchlin CT ym. Adalimumab for long-term treatment of psoriatic arthritis: forty-eight week data from the adalimumab effectiveness in psoriatic arthritis trial. Arthritis Rheum 2007;56:476-88 «PMID: 17265483»PubMed
- Mease PJ. Biologic Therapy for Psoriatic Arthritis. Rheum Dis Clin North Am 2015;41:723-38 «PMID: 26476229»PubMed
- Ramiro S, Smolen JS, Landewé R ym. Pharmacological treatment of psoriatic arthritis: a systematic literature review for the 2015 update of the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis 2016;75:490-8 «PMID: 26660203»PubMed
- Kavanaugh A, van der Heijde D, McInnes IB ym. Golimumab in psoriatic arthritis: one-year clinical efficacy, radiographic, and safety results from a phase III, randomized, placebo-controlled trial. Arthritis Rheum 2012;64:2504-17 «PMID: 22378566»PubMed
- Kavanaugh A, McInnes IB, Mease P ym. Clinical efficacy, radiographic and safety findings through 5 years of subcutaneous golimumab treatment in patients with active psoriatic arthritis: results from a long-term extension of a randomised, placebo-controlled trial (the GO-REVEAL study). Ann Rheum Dis 2014;73:1689-94 «PMID: 24748630»PubMed
- Mease PJ, Goffe BS, Metz J ym. Etanercept in the treatment of psoriatic arthritis and psoriasis: a randomised trial. Lancet 2000;356:385-90 «PMID: 10972371»PubMed
- Mease PJ, Kivitz AJ, Burch FX ym. Etanercept treatment of psoriatic arthritis: safety, efficacy, and effect on disease progression. Arthritis Rheum 2004;50:2264-72 «PMID: 15248226»PubMed
- Antoni C, Krueger GG, de Vlam K ym. Infliximab improves signs and symptoms of psoriatic arthritis: results of the IMPACT 2 trial. Ann Rheum Dis 2005;64:1150-7 «PMID: 15677701»PubMed
- Kavanaugh A, Krueger GG, Beutler A ym. Infliximab maintains a high degree of clinical response in patients with active psoriatic arthritis through 1 year of treatment: results from the IMPACT 2 trial. Ann Rheum Dis 2007;66:498-505 «PMID: 17114188»PubMed
- Feletar M, Brockbank JE, Schentag CT ym. Treatment of refractory psoriatic arthritis with infliximab: a 12 month observational study of 16 patients. Ann Rheum Dis 2004;63:156-61 «PMID: 14722204»PubMed
- Kavanaugh A, Antoni CE, Gladman D ym. The Infliximab Multinational Psoriatic Arthritis Controlled Trial (IMPACT): results of radiographic analyses after 1 year. Ann Rheum Dis 2006;65:1038-43 «PMID: 16439444»PubMed
- Mease PJ, Fleischmann R, Deodhar AA ym. Effect of certolizumab pegol on signs and symptoms in patients with psoriatic arthritis: 24-week results of a Phase 3 double-blind randomised placebo-controlled study (RAPID-PsA). Ann Rheum Dis 2014;73:48-55 «PMID: 23942868»PubMed
- Ramiro S, Smolen JS, Landewé R ym. Pharmacological treatment of psoriatic arthritis: a systematic literature review for the 2015 update of the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis 2016;75:490-8 «PMID: 26660203»PubMed
- van der Heijde D, Deodhar A, FitzGerald O ym. 4-year results from the RAPID-PsA phase 3 randomised placebo-controlled trial of certolizumab pegol in psoriatic arthritis. RMD Open 2018;4:e000582 «PMID: 29556416»PubMed
- Kristensen LE, Keiserman M, Papp K, ym. Efficacy and safety of risankizumab for active psoriatic arthritis: 24-week results from the randomised, double-blind, phase 3 KEEPsAKE 1 trial. Ann Rheum Dis 2022;81(2):225-231 «PMID: 34911706»PubMed
- Östör A, Van den Bosch F, Papp K, ym. Efficacy and safety of risankizumab for active psoriatic arthritis: 24-week results from the randomised, double-blind, phase 3 KEEPsAKE 2 trial. Ann Rheum Dis 2022;81(3):351-358 «PMID: 34815219»PubMed
- Mease PJ, Kellner H, Morita A, ym. Long-Term Efficacy and Safety of Risankizumab in Patients with Active Psoriatic Arthritis: Results from a 76-Week Phase 2 Randomized Trial. Rheumatol Ther 2022;9(5):1361-1375 «PMID: 35931879»PubMed
- Östör A, Van den Bosch F, Papp K, ym. Efficacy and safety of risankizumab for active psoriatic arthritis: 52-week results from the KEEPsAKE 2 study. Rheumatology (Oxford) 2023;62(6):2122-2129 «PMID: 36282537»PubMed
- McInnes IB, Kavanaugh A, Gottlieb AB ym. Efficacy and safety of ustekinumab in patients with active psoriatic arthritis: 1 year results of the phase 3, multicentre, double-blind, placebo-controlled PSUMMIT 1 trial. Lancet 2013;382:780-9 «PMID: 23769296»PubMed
- Kavanaugh A, Puig L, Gottlieb AB ym. Maintenance of Clinical Efficacy and Radiographic Benefit Through Two Years of Ustekinumab Therapy in Patients With Active Psoriatic Arthritis: Results From a Randomized, Placebo-Controlled Phase III Trial. Arthritis Care Res (Hoboken) 2015;67:1739-49 «PMID: 26097039»PubMed
- Araujo EG, Englbrecht M, Hoepken S ym. Effects of ustekinumab versus tumor necrosis factor inhibition on enthesitis: Results from the enthesial clearance in psoriatic arthritis (ECLIPSA) study. Semin Arthritis Rheum 2019;48:632-637 «PMID: 30037432»PubMed
- Ruyssen-Witrand A, Perry R, Watkins C ym. Efficacy and safety of biologics in psoriatic arthritis: a systematic literature review and network meta-analysis. RMD Open 2020;6: «PMID: 32094304»PubMed
- McInnes IB, Asahina A, Coates LC, ym. Bimekizumab in patients with psoriatic arthritis, naive to biologic treatment: a randomised, double-blind, placebo-controlled, phase 3 trial (BE OPTIMAL). Lancet 2023;401(10370):25-37 «PMID: 36493791»PubMed
- Ritchlin CT, Kavanaugh A, Merola JF, ym. Bimekizumab in patients with active psoriatic arthritis: results from a 48-week, randomised, double-blind, placebo-controlled, dose-ranging phase 2b trial. Lancet 2020;395(10222):427-440 «PMID: 32035552»PubMed
- Merola JF, Landewé R, McInnes IB, ym. Bimekizumab in patients with active psoriatic arthritis and previous inadequate response or intolerance to tumour necrosis factor-α inhibitors: a randomised, double-blind, placebo-controlled, phase 3 trial (BE COMPLETE). Lancet 2023;401(10370):38-48 «PMID: 36495881»PubMed
- Coates LC, McInnes IB, Merola JF, ym. Safety and Efficacy of Bimekizumab in Patients With Active Psoriatic Arthritis: Three-Year Results From a Phase IIb Randomized Controlled Trial and Its Open-Label Extension Study. Arthritis Rheumatol 2022;74(12):1959-1970 «PMID: 35829656»PubMed
- Smolen JS, Mease P, Tahir H ym. Multicentre, randomised, open-label, parallel-group study evaluating the efficacy and safety of ixekizumab versus adalimumab in patients with psoriatic arthritis naïve to biological disease-modifying antirheumatic drug: final results by week 52. Ann Rheum Dis 2020;79:1310-1319 «PMID: 32660977»PubMed
- Mease PJ, McInnes IB, Kirkham B ym. Secukinumab Inhibition of Interleukin-17A in Patients with Psoriatic Arthritis. N Engl J Med 2015;373:1329-39 «PMID: 26422723»PubMed
- Mease P, van der Heijde D, Landewé R ym. Secukinumab improves active psoriatic arthritis symptoms and inhibits radiographic progression: primary results from the randomised, double-blind, phase III FUTURE 5 study. Ann Rheum Dis 2018;77:890-897 «PMID: 29550766»PubMed
- Mease PJ, Gottlieb AB, van der Heijde D ym. Efficacy and safety of abatacept, a T-cell modulator, in a randomised, double-blind, placebo-controlled, phase III study in psoriatic arthritis. Ann Rheum Dis 2017;76:1550-1558 «PMID: 28473423»PubMed
- Mourad A, Gniadecki R. Treatment of Dactylitis and Enthesitis in Psoriatic Arthritis with Biologic Agents: A Systematic Review and Metaanalysis. J Rheumatol 2020;47:59-65 «PMID: 30824641»PubMed
- Brüner M, Dige A, Loft AG ym. Spondylitis-psoriasis-enthesitis-enterocolitis-dactylitis-uveitis-peripheral synovitis (SPEED-UP) treatment. Autoimmun Rev 2021;20:102731 «PMID: 33326852»PubMed
- Noviani M, Feletar M, Nash P ym. Choosing the right treatment for patients with psoriatic arthritis. Ther Adv Musculoskelet Dis 2020;12:1759720X20962623 «PMID: 33133245»PubMed
- Mease P, Gottlieb A, McInnes I, Rahman P, Ch'ng Suyin S, Kollmeier A, et al. Low rates of radiographic progression with 2 years of Guselkumab: results from a phase-3/ randomized/double-blind/ placebo-controlled study of biologic-naïve active PsA patients. International journal of rheumatic diseases. 2023;26:113-4
- Mease PJ, Helliwell PS, Gladman DD, ym. Efficacy of guselkumab on axial involvement in patients with active psoriatic arthritis and sacroiliitis: a post-hoc analysis of the phase 3 DISCOVER-1 and DISCOVER-2 studies. Lancet Rheumatol 2021;3(10):e715-e723 «PMID: 38287608»PubMed
- Brown MA, Rudwaleit M, van Gaalen FA, ym. Low uveitis rates in patients with axial spondyloarthritis treated with bimekizumab: pooled results from phase 2b/3 trials. Ann Rheum Dis 2024;(): «PMID: 38977276»PubMed
- McInnes IB, Anderson JK, Magrey M, ym. Trial of Upadacitinib and Adalimumab for Psoriatic Arthritis. N Engl J Med 2021;384(13):1227-1239 «PMID: 33789011»PubMed
- Dai Q, Zhang Y, Liu Q, ym. Efficacy and safety of tofacitinib for chronic plaque psoriasis and psoriatic arthritis: a systematic review and meta-analysis of randomized controlled trials. Clin Rheumatol 2024;43(5):1605-1613 «PMID: 38517652»PubMed
- Gossec L, Kerschbaumer A, Ferreira RJO, ym. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2023 update. Ann Rheum Dis 2024;83(6):706-719 «PMID: 38499325»PubMed
- Kerschbaumer A, Smolen JS, Ferreira RJO, ym. Efficacy and safety of pharmacological treatment of psoriatic arthritis: a systematic literature research informing the 2023 update of the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis 2024;83(6):760-774 «PMID: 38503473»PubMed
- Tauscher AE, Fleischer AB Jr, Phelps KC ym. Psoriasis and pregnancy. J Cutan Med Surg 2002;6:561-70 «PMID: 12362257»PubMed
- Hale EK, Pomeranz MK. Dermatologic agents during pregnancy and lactation: an update and clinical review. Int J Dermatol 2002;41:197-203 «PMID: 12031026»PubMed
- Murase JE, Chan KK, Garite TJ ym. Hormonal effect on psoriasis in pregnancy and post partum. Arch Dermatol 2005;141:601-6 «PMID: 15897382»PubMed
- Raychaudhuri SP, Navare T, Gross J ym. Clinical course of psoriasis during pregnancy. Int J Dermatol 2003;42:518-20 «PMID: 12839599»PubMed
- Gudjonsson JE, Karason A, Runarsdottir EH ym. Distinct clinical differences between HLA-Cw*0602 positive and negative psoriasis patients--an analysis of 1019 HLA-C- and HLA-B-typed patients. J Invest Dermatol 2006;126:740-5 «PMID: 16439971»PubMed
- Yang YW, Chen CS, Chen YH ym. Psoriasis and pregnancy outcomes: a nationwide population-based study. J Am Acad Dermatol 2011;64:71-7 «PMID: 20970879»PubMed
- Mowad CM, Margolis DJ, Halpern AC ym. Hormonal influences on women with psoriasis. Cutis 1998;61:257-60 «PMID: 9608337»PubMed
- Ursin K, Lydersen S, Skomsvoll JF ym. Psoriatic Arthritis Disease Activity During and After Pregnancy: A Prospective Multicenter Study. Arthritis Care Res (Hoboken) 2019;71:1092-1100 «PMID: 30192071»PubMed
- Bobotsis R, Gulliver WP, Monaghan K ym. Psoriasis and adverse pregnancy outcomes: a systematic review of observational studies. Br J Dermatol 2016;175:464-72 «PMID: 26991866»PubMed
- Bandoli G, Johnson DL, Jones KL ym. Potentially modifiable risk factors for adverse pregnancy outcomes in women with psoriasis. Br J Dermatol 2010;163:334-9 «PMID: 20545678»PubMed
- Bae YS, Van Voorhees AS, Hsu S ym. Review of treatment options for psoriasis in pregnant or lactating women: from the Medical Board of the National Psoriasis Foundation. J Am Acad Dermatol 2012;67:459-77 «PMID: 22018758»PubMed
- Chi CC, Kirtschig G, Aberer W ym. Evidence-based (S3) guideline on topical corticosteroids in pregnancy. Br J Dermatol 2011;165:943-52 «PMID: 21729030»PubMed
- Chi CC, Wang SH, Wojnarowska F ym. Safety of topical corticosteroids in pregnancy. Cochrane Database Syst Rev 2015;:CD007346 «PMID: 26497573»PubMed
- Clowse ME, Förger F, Hwang C ym. Minimal to no transfer of certolizumab pegol into breast milk: results from CRADLE, a prospective, postmarketing, multicentre, pharmacokinetic study. Ann Rheum Dis 2017;76:1890-1896 «PMID: 28814432»PubMed
- Mariette X, Förger F, Abraham B ym. Lack of placental transfer of certolizumab pegol during pregnancy: results from CRIB, a prospective, postmarketing, pharmacokinetic study. Ann Rheum Dis 2018;77:228-233 «PMID: 29030361»PubMed
- Sihvonen S, Pertovaara M. Reumasairaudet raskauden aikana. Duodecim 2019;135:257-64
- Morris A, Rogers M, Fischer G ym. Childhood psoriasis: a clinical review of 1262 cases. Pediatr Dermatol 2001;18:188-98 «PMID: 11437997»PubMed
- Varni JW, Globe DR, Gandra SR ym. Health-related quality of life of pediatric patients with moderate to severe plaque psoriasis: comparisons to four common chronic diseases. Eur J Pediatr 2012;171:485-92 «PMID: 21960290»PubMed
- Siegfried EC. Neonatal skin and skin care. Dermatol Clin 1998;16:437-46 «PMID: 9704203»PubMed
- Chiou YB, Blume-Peytavi U. Stratum corneum maturation. A review of neonatal skin function. Skin Pharmacol Physiol 2004;17:57-66 «PMID: 14976382»PubMed
- Lebwohl M, Ali S. Treatment of psoriasis. Part 1. Topical therapy and phototherapy. J Am Acad Dermatol 2001;45:487-98; quiz 499-502 «PMID: 11568737»PubMed
- Sticherling M, Augustin M, Boehncke WH ym. Therapy of psoriasis in childhood and adolescence - a German expert consensus. J Dtsch Dermatol Ges 2011;9:815-23 «PMID: 21585653»PubMed
- de Jager ME, de Jong EM, van de Kerkhof PC ym. Efficacy and safety of treatments for childhood psoriasis: a systematic literature review. J Am Acad Dermatol 2010;62:1013-30 «PMID: 19900732»PubMed
- Jury CS, McHenry P, Burden AD ym. Narrowband ultraviolet B (UVB) phototherapy in children. Clin Exp Dermatol 2006;31:196-9 «PMID: 16487089»PubMed
- Pasic A, Ceovic R, Lipozencic J ym. Phototherapy in pediatric patients. Pediatr Dermatol 2003;20:71-7 «PMID: 12558852»PubMed
- Paller AS, Siegfried EC, Langley RG ym. Etanercept treatment for children and adolescents with plaque psoriasis. N Engl J Med 2008;358:241-51 «PMID: 18199863»PubMed
- Paller AS, Siegfried EC, Eichenfield LF ym. Long-term etanercept in pediatric patients with plaque psoriasis. J Am Acad Dermatol 2010;63:762-8 «PMID: 20605256»PubMed
- Paller AS, Siegfried EC, Pariser DM ym. Long-term safety and efficacy of etanercept in children and adolescents with plaque psoriasis. J Am Acad Dermatol 2016;74:280-7.e1-3 «PMID: 26775775»PubMed
- Landells I, Marano C, Hsu MC ym. Ustekinumab in adolescent patients age 12 to 17 years with moderate-to-severe plaque psoriasis: results of the randomized phase 3 CADMUS study. J Am Acad Dermatol 2015;73:594-603 «PMID: 26259989»PubMed
- Petty RE, Southwood TR, Manners P ym. International League of Associations for Rheumatology classification of juvenile idiopathic arthritis: second revision, Edmonton, 2001. J Rheumatol 2004;31:390-2 «PMID: 14760812»PubMed
- Butbul Aviel Y, Tyrrell P, Schneider R ym. Juvenile Psoriatic Arthritis (JPsA): juvenile arthritis with psoriasis? Pediatr Rheumatol Online J 2013;11:11 «PMID: 23497068»PubMed
- Ekelund M, Aalto K, Fasth A ym. Psoriasis and associated variables in classification and outcome of juvenile idiopathic arthritis - an eight-year follow-up study. Pediatr Rheumatol Online J 2017;15:13 «PMID: 28222745»PubMed
- Stoll ML, Nigrovic PA, Gotte AC ym. Clinical comparison of early-onset psoriatic and non-psoriatic oligoarticular juvenile idiopathic arthritis. Clin Exp Rheumatol 2011;29:582-8 «PMID: 21385553»PubMed
- Zisman D, Gladman DD, Stoll ML ym. The Juvenile Psoriatic Arthritis Cohort in the CARRA Registry: Clinical Characteristics, Classification, and Outcomes. J Rheumatol 2017;44:342-351 «PMID: 28148698»PubMed
- Stoll ML, Zurakowski D, Nigrovic LE ym. Patients with juvenile psoriatic arthritis comprise two distinct populations. Arthritis Rheum 2006;54:3564-72 «PMID: 17075862»PubMed
- Kröger L, Vähäsalo P, Tynjälä P ym. [Medical treatment of juvenile idiopathic arthritis]. Duodecim 2012;128:477-86 «PMID: 22486063»PubMed
- Ruperto N, Murray KJ, Gerloni V ym. A randomized trial of parenteral methotrexate comparing an intermediate dose with a higher dose in children with juvenile idiopathic arthritis who failed to respond to standard doses of methotrexate. Arthritis Rheum 2004;50:2191-201 «PMID: 15248217»PubMed
- van Rossum MA, Fiselier TJ, Franssen MJ ym. Sulfasalazine in the treatment of juvenile chronic arthritis: a randomized, double-blind, placebo-controlled, multicenter study. Dutch Juvenile Chronic Arthritis Study Group. Arthritis Rheum 1998;41:808-16 «PMID: 9588731»PubMed
- Silverman E, Mouy R, Spiegel L ym. Leflunomide or methotrexate for juvenile rheumatoid arthritis. N Engl J Med 2005;352:1655-66 «PMID: 15843668»PubMed
- Tynjälä P, Vähäsalo P, Tarkiainen M ym. Aggressive combination drug therapy in very early polyarticular juvenile idiopathic arthritis (ACUTE-JIA): a multicentre randomised open-label clinical trial. Ann Rheum Dis 2011;70:1605-12 «PMID: 21623000»PubMed
- Lovell DJ, Ruperto N, Goodman S ym. Adalimumab with or without methotrexate in juvenile rheumatoid arthritis. N Engl J Med 2008;359:810-20 «PMID: 18716298»PubMed
- Horneff G, Seyger MMB, Arikan D ym. Safety of Adalimumab in Pediatric Patients with Polyarticular Juvenile Idiopathic Arthritis, Enthesitis-Related Arthritis, Psoriasis, and Crohn's Disease. J Pediatr 2018;201:166-175.e3 «PMID: 30054164»PubMed
- Constantin T, Foeldvari I, Vojinovic J ym. Two-year Efficacy and Safety of Etanercept in Pediatric Patients with Extended Oligoarthritis, Enthesitis-related Arthritis, or Psoriatic Arthritis. J Rheumatol 2016;43:816-24 «PMID: 26932344»PubMed
- Foeldvari I, Constantin T, Vojinovic J ym. Etanercept treatment for extended oligoarticular juvenile idiopathic arthritis, enthesitis-related arthritis, or psoriatic arthritis: 6-year efficacy and safety data from an open-label trial. Arthritis Res Ther 2019;21:125 «PMID: 31122296»PubMed
- Otten MH, Prince FH, Ten Cate R ym. Tumour necrosis factor (TNF)-blocking agents in juvenile psoriatic arthritis: are they effective? Ann Rheum Dis 2011;70:337-40 «PMID: 21068101»PubMed
- Windschall D, Müller T, Becker I ym. Safety and efficacy of etanercept in children with the JIA categories extended oligoarthritis, enthesitis-related arthritis and psoriasis arthritis. Clin Rheumatol 2015;34:61-9 «PMID: 25034081»PubMed
- Hissink Muller PC, Brinkman DM, Schonenberg D ym. A comparison of three treatment strategies in recent onset non-systemic Juvenile Idiopathic Arthritis: initial 3-months results of the BeSt for Kids-study. Pediatr Rheumatol Online J 2017;15:11 «PMID: 28166785»PubMed
- Wallace CA, Giannini EH, Spalding SJ ym. Trial of early aggressive therapy in polyarticular juvenile idiopathic arthritis. Arthritis Rheum 2012;64:2012-21 «PMID: 22183975»PubMed
- Brunner HI, Ruperto N, Tzaribachev N ym. Subcutaneous golimumab for children with active polyarticular-course juvenile idiopathic arthritis: results of a multicentre, double-blind, randomised-withdrawal trial. Ann Rheum Dis 2018;77:21-29 «PMID: 28507219»PubMed
- De Benedetti F, Brunner HI, Ruperto N ym. Randomized trial of tocilizumab in systemic juvenile idiopathic arthritis. N Engl J Med 2012;367:2385-95 «PMID: 23252525»PubMed
- Brunner HI, Ruperto N, Zuber Z ym. Efficacy and safety of tocilizumab in patients with polyarticular-course juvenile idiopathic arthritis: results from a phase 3, randomised, double-blind withdrawal trial. Ann Rheum Dis 2015;74:1110-7 «PMID: 24834925»PubMed
- Grönlund MM, Remes-Pakarinen T, Kröger L ym. Efficacy and safety of tocilizumab in a real-life observational cohort of patients with polyarticular juvenile idiopathic arthritis. Rheumatology (Oxford) 2020;59:732-741 «PMID: 31359057»PubMed
- Lovell DJ, Ruperto N, Mouy R ym. Long-term safety, efficacy, and quality of life in patients with juvenile idiopathic arthritis treated with intravenous abatacept for up to seven years. Arthritis Rheumatol 2015;67:2759-70 «PMID: 26097215»PubMed
- Brunner HI, Foeldvari I, Alexeeva E, ym. Secukinumab in enthesitis-related arthritis and juvenile psoriatic arthritis: a randomised, double-blind, placebo-controlled, treatment withdrawal, phase 3 trial. Ann Rheum Dis 2023;82(1):154-160 «PMID: 35961761»PubMed
- Ramanan AV, Quartier P, Okamoto N, ym. Baricitinib in juvenile idiopathic arthritis: an international, phase 3, randomised, double-blind, placebo-controlled, withdrawal, efficacy, and safety trial. Lancet 2023;402(10401):555-570 «PMID: 37423231»PubMed
- Ruperto N, Brunner HI, Synoverska O, ym. Tofacitinib in juvenile idiopathic arthritis: a double-blind, placebo-controlled, withdrawal phase 3 randomised trial. Lancet 2021;398(10315):1984-1996 «PMID: 34767764»PubMed
- Rutter MK, Kane K, Lunt M ym. Primary care-based screening for cardiovascular risk factors in patients with psoriasis. Br J Dermatol 2016;175:348-56 «PMID: 26990294»PubMed

