Psoriaasi ja nivelpsoriaasi
Miten viitata Käypä hoito -suositukseen? «K1»1
Keskeinen sisältö
- Psoriaasi on ihon ja nivelten monimuotoinen, krooninen ja usein suvuittain esiintyvä immunologinen tulehdustauti.
- Iho- ja niveloireet ovat valtaosalla potilaista lieviä. Jo lieväkin iho- tai nivelpsoriaasi saattaa kuitenkin heikentää potilaan elämänlaatua. Elämänlaatua heikentävät etenkin näkyvillä alueilla esiintyvä tai laaja-alainen ihopsoriaasi ja vaikea nivelpsoriaasi.
- Psoriaasin oireita voidaan hoitaa monella tavalla, vaikkei tautia voida parantaa. Hoidon tavoitteena on minimoida oireet ja parantaa elämänlaatua sekä säilyttää potilaan työ- ja toimintakyky.
- Psoriaasiin liittyvä valtimotautien ja diabeteksen riski on huomioitava aina hoitoa suunniteltaessa. Jo lapsilla voidaan todeta liitännäissairauksia. Potilasta kannustetaan terveisiin elämäntapoihin. Mahdollinen ahdistuneisuus ja masennus tulee huomioida ja hoitaa jo varhain.
- Hoito valitaan aina yksilöllisesti (ks. Ihopsoriaasin hoidon porrastus «Ihopsoriaasin hoidon porrastus»1). Nivelpsoriaasin hoidon valinnassa otetaan huomioon sairauden aktiivisuus ja sen ilmenemismuodot.
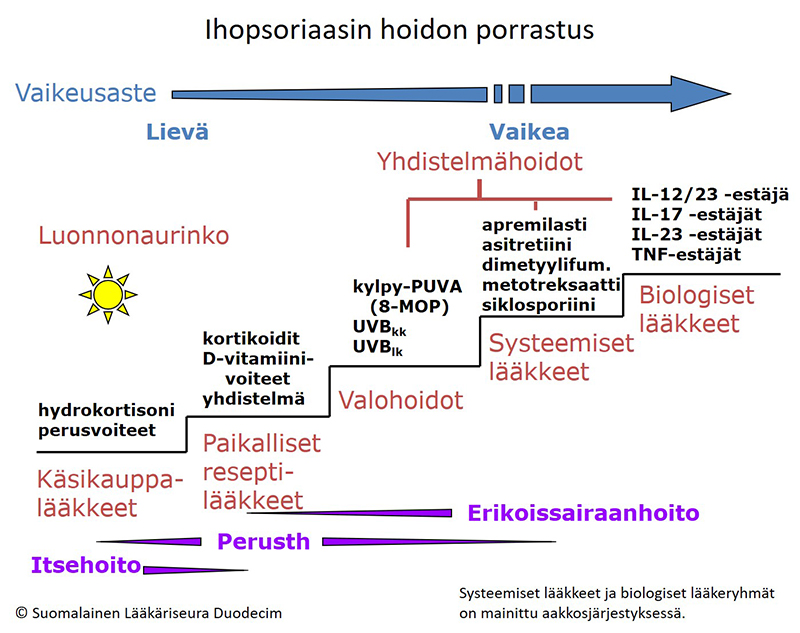
Ihopsoriaasin hoidon porrastus.
Kuva: Tapio Rantanen
© Suomalainen Lääkäriseura Duodecim
Tiivistelmä ja potilasversio
- Suosituksen tiivistelmä «Psoriaasi ja nivelpsoriaasi»1
- Suosituksen yleiskielinen potilasversio suomeksi «Psoriaasi (iho- ja nivelpsoriaasi) hallintaan säännöllisellä hoidolla»2 ja ruotsiksi «Psoriasis (hudpsoriasis och psoriasisartrit) under kontroll med regelbunden behandling»3
Tavoite
- Suosituksen tavoitteena on
- yhdenmukaistaa näytön pohjalta iho- ja nivelpsoriaasin diagnostiikkaa ja hoitoja
- antaa suositus hoidon porrastuksesta perus- ja erikoissairaanhoitoon.
Kohderyhmä
- Suositus on tarkoitettu kaikille terveydenhuollon ammattihenkilöille, jotka työssään hoitavat psoriaasipotilaita.
Rajaus
- Suosituksessa ei käsitellä pustulosis palmoplantarista.
- Lasten niveltaudin osalta haut ovat koskeneet nivelpsoriaasia. Hakuja ei ole tehty kattavasti lastenreuman osalta.
- Suosituksen päivityksessä (julkaistu 8.10.2024) päivitettiin suosituksen nivelpsoriaasiosa.
Määritelmät
- Psoriaasi on krooninen, monimuotoinen, immuunivälitteinen tulehdussairaus, jonka tavallisimmat ilmenemismuodot ovat iho- ja nivelpsoriaasi «Mälkonen T, Suomela S. [What do we know about path...»1, «Matikainen S, Jokiranta S, Eklund KK. [Role of cyt...»2, «Global report on psoriasis. World Health Organizat...»3, «https://www.duodecimlehti.fi/lehti/2011/15/duo99684»1.
- Lapsilla nivelpsoriaasi kuuluu ILAR (International League Against Rheumatism) -luokittelussa
lastenreumadiagnoosin alle «Petty RE, Southwood TR, Manners P ym. Internationa...»4. Määritelmän mukaan lasten nivelpsoriaasi on tuntemattomasta syystä alle 16-vuotiaana
alkanut, pitkäaikainen, vähintään 6 viikkoa kestänyt niveltulehdustauti, johon diagnostisten
kriteerien mukaan liittyy psoriaasi-ihottuma tai sen puuttuessa vähintään 2 kriteeriä
seuraavista täyttyy:
- kynsimuutokset
- daktyliitti
- 1. asteen sukulaisen psoriaasi.
Käytetyt lyhenteet
- ACR (American College of Rheumatology) -kriteerit = kriteeristö nivelreuman aktiivisuuden arvioimiseksi. Kriteeristöä käytetään myös nivelpsoriaasin lääkehoidon tehon arvioimisessa «Felson DT, Anderson JJ, Boers M ym. American Colle...»5.
- BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) = taudin aktiivisuutta mittaava työkalu spondyloartropatioissa ( «https://www.reumatologinenyhdistys.fi/laakerekisteri-lomakkeet/»2).
- BASFI (Bath Ankylosing Spondylitis Functional Index) = toimintakykyä mittaava työkalu spondylartropatioissa ( «https://www.reumatologinenyhdistys.fi/laakerekisteri-lomakkeet/»2 ).
- BSA (Body Surface Area) = ihottuman peitossa oleva ihoalue (%).
- DLQI (Dermatology Life Quality Index) = ihotaudeissa elämänlaadun mittarina käytetty kysymyssarja (kyselyn ohjeet «hoi50062b.pdf»1) ja kyselyn internetlinkki ( «https://www.cardiff.ac.uk/medicine/resources/quality-of-life-questionnaires/dermatology-life-quality-index»3 ).
- HAQ (Health Assessment Questionnaire) = reumatologian alueella käytetty toimintakykymittari ( «https://www.reumatologinenyhdistys.fi/laakerekisteri-lomakkeet/»2 ) (ks. Käypä hoito -suositus Nivelreuma «Nivelreuma»4).
- JADAS10-indeksi (Juvenile Arthritis Disease Activity Score) = lastenreuman taudin aktiivisuuden mittari.
- PASI (Psoriasis Area and Severity Index) = ihopsoriaasin vaikeusasteen määrityksessä käytettävä työkalu, joka huomio ihottuman laajuuden (prosenttiosuutena) pään, vartalon ja ylä- ja alaraajojen alueilta erikseen arvioituna sekä läiskien punoituksen, paksuuden ja hilseilyn (ks. kohta Ihopsoriaasin vaikeusaste «A1»2) (PASI-laskin «hoi50062d.xls»2). Ks. myös taulukko «Ihopsoriaasin hoitovasteeseen liittyviä määritelmiä , ...»1.
- PsA (Psoriatic Arthritis) = nivelpsoriaasi.
- PsARC (Psoriatic Arthritis Response Criteria) = nivelpsoriaasin aktiivisuuden mittari.
- ACR Pedi -vaste = American College of Rheumatologyn suositus lastenreuman aktiivisuuden muutoksen arvioimiseksi «Giannini EH, Ruperto N, Ravelli A ym. Preliminary ...»6.
| Lyhenne | Määritelmä | |
|---|---|---|
| Riittämätön hoitovaste | < PASI-50 | PASI pienentynyt vähemmän kuin 50 % lähtötilanteesta |
| Kohtalainen hoitovaste | PASI-50 | PASI pienentynyt vähintään 50 % lähtötilanteesta |
| Hyvä hoitovaste | PASI-75 | PASI pienentynyt vähintään 75 % lähtötilanteesta, vastaa PASI-arvoa ≤ 4 |
| Erinomainen hoitovaste | PASI-90 | PASI pienentynyt vähintään 90 % lähtötilanteesta, vastaa PASI-arvoa ≤ 2 |
| Täydellinen hoitovaste | PASI-100 | PASI pienentynyt 100 % lähtötilanteesta = iho on oireeton |
| Relapsi | PASIn pienenemästä vähintään 50 % tullut takaisin | |
| Relapsiaika | Aika hoidon päättymisestä relapsiin | |
| Hoitovasteen kestoaika | Aika PASI-50-vasteen saavuttamisesta sen menettämiseen | |
| Rebound | PASI+125 | Vähintään 25 %:n pahenema lähtötilanteeseen verrattuna |
Esiintyvyys
- Ihopsoriaasia sairastaa Euroopassa ja Pohjois-Amerikassa 1,5–3 % «Global report on psoriasis. World Health Organizat...»3, «Parisi R, Symmons DP, Griffiths CE ym. Global epid...»9 väestöstä. Väestökyselyistä on julkaistu suurempia esiintyvyyslukuja «Danielsen K, Olsen AO, Wilsgaard T ym. Is the prev...»10, «Svensson A, Ofenloch RF, Bruze M ym. Prevalence of...»11 «Egeberg A, Andersen YMF, Thyssen JP. Prevalence an...»12.
- Alle 18-vuotiailla esiintyvyys on ennen puberteettia 0,1–0,5 % ja puberteetin jälkeen 0,6–1,3 % «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13.
- Ihopsoriaasin ilmaantuvuus oli 1990-luvulla Yhdysvaltojen valkoisessa väestössä ja Euroopassa 100–140 uutta tapausta 100000 asukasta kohden vuodessa. Vuosittainen ilmaantuvuus alle 18-vuotiailla oli 63/100 000 «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13, «Tollefson MM, Crowson CS, McEvoy MT ym. Incidence ...»14, «Huerta C, Rivero E, Rodríguez LA. Incidence and ri...»15, «Icen M, Crowson CS, McEvoy MT ym. Trends in incide...»16.
- Psoriaasi voi ilmaantua missä iässä tahansa.
- Ilmaantumisiässä on kaksi huippua: ensimmäinen nuoruusiässä ja toinen 50–60 vuoden iässä, mikä johtuu pääasiassa geneettisistä alttiustekijöistä «Henseler T, Christophers E. Psoriasis of early and...»17, «Lønnberg AS, Skov L, Duffy DL ym. Genetic Factors ...»18.
- Kolmasosalla potilaista taudin ensimmäiset oireet alkavat alle 20-vuotiaana «Tollefson MM, Crowson CS, McEvoy MT ym. Incidence ...»14, «Vogel SA, Yentzer B, Davis SA ym. Trends in pediat...»19.
- Nivelpsoriaasia sairastaa 0,16–0,25 % valikoimattomasta väestöstä «Gelfand JM, Gladman DD, Mease PJ ym. Epidemiology ...»20, «Madland TM, Apalset EM, Johannessen AE ym. Prevale...»21, «Wilson FC, Icen M, Crowson CS ym. Time trends in e...»22. Uusia tapauksia ilmaantuu vuosittain 6–10/100 000 «Kaipiainen-Seppänen O. Incidence of psoriatic arth...»23, «Alamanos Y, Voulgari PV, Drosos AA. Incidence and ...»24, «Wilson FC, Icen M, Crowson CS ym. Incidence and cl...»25.
- Psoriaasipotilaan riski sairastua nivelpsoriaasiin kasvaa tasaisesti sairausvuosien
mukaan.
- Väestöpohjaisessa tutkimuksessa 2,4 %:lla psoriaatikoista oli taudin ilmaantuessa myös nivelpsoriaasi, ja 20 vuoden seurannassa se kehittyi lisäksi 5,1 %:lle «Wilson FC, Icen M, Crowson CS ym. Time trends in e...»22.
- Vaikeaa ihopsoriaasia sairastavilla nivelpsoriaasin riski on huomattavasti suurempi, ja se kasvaa biologista lääkehoitoa vaativissa psoriaasitapauksissa 20–35 %:iin «Prey S, Paul C, Bronsard V ym. Assessment of risk ...»26, «Christophers E, Barker JN, Griffiths CE ym. The ri...»27.
- Pienellä osalla niveloireet edeltävät iho-oireita «Gladman DD, Shuckett R, Russell ML ym. Psoriatic a...»28.
- Niveloireita on raportoitu esiintyvän 0,7–10,5 %:lla lapsipsoriaatikoista «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13.
- Naiset ja miehet sairastuvat nivelpsoriaasiin yhtä usein, mutta spondylartropatiatautityyppi on miehillä yleisempi «Kaipiainen-Seppänen O. Incidence of psoriatic arth...»23. Lastenreuman ilmaantuvuus on eri maissa ja tutkimuksissa ollut 1,6–23 «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13 ja suomalaisessa aineistossa 21–23/100 000 «Berntson L, Andersson Gäre B, Fasth A ym. Incidenc...»29, «Savolainen E, Kaipiainen-Seppänen O, Kröger L ym. ...»30, «Virta R, Helenius H, Klaukka T. Lasten reuma yleis...»31. Näistä lasten nivelpsoriaasin osuus on noin 6 % «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13. Lasten nivelpsoriaasin ilmaantuvuudeksi on saatu 0,3–0,5/100 000 «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13. Lapsilla tautia on raportoitu esiintyvän enemmän tytöillä kuin pojilla «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13.
- Sekä iho- että nivelpsoriaasin ilmaantuvuus on kasvanut 30 vuoden seurannassa «Tollefson MM, Crowson CS, McEvoy MT ym. Incidence ...»14, «Huerta C, Rivero E, Rodríguez LA. Incidence and ri...»15, «Wilson FC, Icen M, Crowson CS ym. Incidence and cl...»25, «Icen M, Crowson CS, McEvoy MT ym. Trends in incide...»32, «Dand N, Mahil SK, Capon F ym. Psoriasis and Geneti...»33.
Riskitekijät
- Psoriaasin taustalla on geneettisiä alttiustekijöitä «Dand N, Mahil SK, Capon F ym. Psoriasis and Geneti...»33.
- Jos molemmat vanhemmat sairastavat psoriaasia, sairastumisen riski on 41–65 % «Lomholt G. Psoriasis. Prevalence, Spontaneous Cour...»34, «Swanbeck G, Inerot A, Martinsson T ym. Genetic cou...»35, «Mallbris L, Larsson P, Bergqvist S ym. Psoriasis p...»38.
- Jos toinen vanhempi sairastaa psoriaasia, sairastumisen riski on 14–28 % «Swanbeck G, Inerot A, Martinsson T ym. Genetic cou...»35, «Asumalahti K, Saarialho-Kere U, Kere J. [The patho...»36, «Andressen C, Henseler T. [Inheritance of psoriasis...»37.
- Nivelpsoriaasipotilaista noin 30 %:lla psoriaasia esiintyy lähisuvussa «Mallbris L, Larsson P, Bergqvist S ym. Psoriasis p...»38.
- Useita alttiusgeenejä on paikannettu eri kromosomeihin, ja niiden toiminnallinen yhteys biologisiin mekanismeihin on alkanut hahmottua «Mälkonen T, Suomela S. [What do we know about path...»1, «Dand N, Mahil SK, Capon F ym. Psoriasis and Geneti...»33, «Harden JL, Krueger JG, Bowcock AM. The immunogenet...»39. Käsitys psoriaasista autoimmuunitautina on saanut vahvistusta kolmen autoantigeenin löytymisestä «Arakawa A, Siewert K, Stöhr J ym. Melanocyte antig...»40, «Lande R, Botti E, Jandus C ym. The antimicrobial p...»41, «Cheung KL, Jarrett R, Subramaniam S ym. Psoriatic ...»42. Ks. lisätietoa aiheesta «Psoriaasin alttiusgeenejä»1.
- Tunnetuin laukaiseva tekijä pisarapsoriaasissa on Streptococcus pyogenes -bakteerin aiheuttama nielutulehdus «Mallbris L, Larsson P, Bergqvist S ym. Psoriasis p...»38, «Gudjonsson JE, Thorarinsson AM, Sigurgeirsson B ym...»43.
- Stressi «Mallbris L, Larsson P, Bergqvist S ym. Psoriasis p...»38, «Seville RH. Stress and psoriasis: the importance o...»44, «Naldi L, Peli L, Parazzini F ym. Family history of...»45, «Li WQ, Qureshi AA, Schernhammer ES ym. Rotating ni...»46, masennus «Dominguez PL, Han J, Li T ym. Depression and the r...»47, ylipaino «Huerta C, Rivero E, Rodríguez LA. Incidence and ri...»15, «Wu S, Li WQ, Han J ym. Hypercholesterolemia and ri...»48, «Naldi L, Chatenoud L, Linder D ym. Cigarette smoki...»49, «Setty AR, Curhan G, Choi HK. Obesity, waist circum...»50, «Wolk K, Mallbris L, Larsson P ym. Excessive body w...»51, tupakointi «Huerta C, Rivero E, Rodríguez LA. Incidence and ri...»15, «Naldi L, Chatenoud L, Linder D ym. Cigarette smoki...»49, «Wolk K, Mallbris L, Larsson P ym. Excessive body w...»51, «Li W, Han J, Choi HK ym. Smoking and risk of incid...»52, «Setty AR, Curhan G, Choi HK. Smoking and the risk ...»53 ja runsas alkoholin käyttö «Poikolainen K, Reunala T, Karvonen J ym. Alcohol i...»54, «Qureshi AA, Dominguez PL, Choi HK ym. Alcohol inta...»55 suurentavat läiskäpsoriaasin ilmaantumisen riskiä ja pahentavat sen oireita «Ockenfels HM. [Trigger factors for psoriasis]. Hau...»56, «Poikolainen K, Reunala T, Karvonen J. Smoking, alc...»57.
- Lisäksi psoriaasia saattavat laukaista tai pahentaa erilaiset infektiot «Keller JJ, Wu CS, Lin HC. Increased risk of psoria...»58 (esim. nielun streptokokki-infektiot «Thorleifsdottir RH, Eysteinsdóttir JH, Olafsson JH...»59, parodontiitti ja muut hammastulehdukset sekä HIV), traumat (Köbnerin ilmiö) ja eräät
lääkkeet «Dika E, Varotti C, Bardazzi F ym. Drug-induced pso...»60.
- Kliinisen kokemuksen mukaan psoriaasia pahentavat muun muassa litium, klorokiini ja terbinafiini.
- Interferonit alfa ja gamma sekä imikimodi vaikuttavat immuunijärjestelmään psoriaasia pahentavasti.
- Psoriaasi tai pustulosis palmoplantaris voi ilmaantua tuumorinekroositekijä alfan estäjien käytön yhteydessä muissa käyttöaiheissa «Harrison MJ, Dixon WG, Watson KD ym. Rates of new-...»61, «Shmidt E, Wetter DA, Ferguson SB ym. Psoriasis and...»62, «Guerra I, Algaba A, Pérez-Calle JL ym. Induction o...»63.
- Beetasalpaajat ja ACE:n estäjät eivät näytä vaikuttavan psoriaasin kulkuun «Brauchli YB, Jick SS, Curtin F ym. Association bet...»64.
- Nivelpsoriaasin kehittymisen tärkeimpiä riski- ja ennustetekijöitä ovat nivelpsoriaasin esiintyminen suvussa «Karason A, Love TJ, Gudbjornsson B. A strong herit...»65 sekä psoriaasin esiintyminen kynsissä ja useilla eri ihoalueilla «Wilson FC, Icen M, Crowson CS ym. Incidence and cl...»25. Ylipaino suurentaa psoriaasipotilaiden riskiä sairastua nivelpsoriaasiin, kun taas laihtuminen pienentää riskiä lineaarisesti 10 vuoden seurannassa «Green A, Shaddick G, Charlton R ym. Modifiable ris...»66, «Eder L, Harvey P, Chandran V ym. Gaps in Diagnosis...»67. Tutkimustulokset tupakoinnin vaikutuksesta nivelpsoriaasin riskitekijänä ovat ristiriitaisia «Li W, Han J, Choi HK ym. Smoking and risk of incid...»52, «Eder L, Shanmugarajah S, Thavaneswaran A ym. The a...»68. Aksiaalista spondyloartropatiaa sairastavilla tupakointi suurentaa nivelpsoriaasiin sairastumisen riskiä «Pezzolo E, Naldi L. The relationship between smoki...»69, «Zhao SS, Goodson NJ, Robertson S ym. Smoking in sp...»70, «Tsuruta N, Imafuku S, Narisawa Y. Hyperuricemia is...»71.
Liitännäissairaudet
- Vaikeaa ihopsoriaasia ja nivelpsoriaasia sairastavilla esiintyy muuta väestöä useammin sydän- ja verisuonitauteja, sydän- ja aivoinfarkteja «Vaikeaa ihopsoriaasia sairastavilla on muuta väestöä useammin sydän- ja verisuonisairauksia.»A sekä niiden vaaratekijöitä «Neimann AL, Shin DB, Wang X ym. Prevalence of card...»72, «Mallbris L, Ritchlin CT, Ståhle M. Metabolic disor...»73, «Husted JA, Thavaneswaran A, Chandran V ym. Cardiov...»74, kuten ylipainoa, verenpainetautia, aikuisiän diabetesta, rasvamaksaa, veren suurentuneita rasva-arvoja, tupakointia «Naldi L, Chatenoud L, Linder D ym. Cigarette smoki...»49, «Li W, Han J, Choi HK ym. Smoking and risk of incid...»52, «Poikolainen K, Reunala T, Karvonen J. Smoking, alc...»57 ja alkoholin liikakäyttöä «Poikolainen K, Reunala T, Karvonen J ym. Alcohol i...»54, «McAleer MA, Mason DL, Cunningham S ym. Alcohol mis...»75. Vaikeaan psoriaasiin liittyvä elimistön krooninen yleistulehdus on itsenäinen sepelvaltimotaudin riskitekijä «Mehta NN, Azfar RS, Shin DB ym. Patients with seve...»76. Sepelvaltimotauti on tärkein vaikeaan psoriaasiin liittyvän ylikuolleisuuden aiheuttaja «Gelfand JM, Troxel AB, Lewis JD ym. The risk of mo...»77, «Abuabara K, Azfar RS, Shin DB ym. Cause-specific m...»78. Metabolista oireyhtymää sairastavilla veren uraattiarvo on usein suurentunut.
- Iho- ja nivelpsoriaasia sairastavilla on jonkin verran muuta väestöä useammin tulehduksellisia suolistosairauksia (Crohnin tautia ja haavaista paksusuolitulehdusta) «Cohen AD, Dreiher J, Birkenfeld S. Psoriasis assoc...»79 sekä keliakiaa «Ludvigsson JF, Lindelöf B, Zingone F ym. Psoriasis...»80. Kuivasilmäisyyttä ja anteriorista uveiittia voi esiintyä etenkin nivelpsoriaasia sairastavilla «Rehal B, Modjtahedi BS, Morse LS ym. Ocular psoria...»81.
- Vaikeaan psoriaasiin liittyy lievästi suurentunut lymfooman «Vaikeaan psoriaasiin näyttää liittyvän lievästi kohonnut lymfoomariski.»B ja ihon keratinosyyttisyöpien riski «Vaikeaan psoriaasiin liittyy lievästi kohonnut ihon okasolusyövän riski, jonka tärkein riskitekijä on metoksaleeni-tabletti-PUVA-hoito.»A sekä elintapoihin liittyviä suurentuneita syöpäriskejä «Boffetta P, Gridley G, Lindelöf B. Cancer risk in ...»82, «Brauchli YB, Jick SS, Miret M ym. Psoriasis and ri...»83, «Chen YJ, Wu CY, Chen TJ ym. The risk of cancer in ...»84.
- Masennuksen, ahdistuksen ja itsemurhan vaara on tavallista suurempi etenkin vaikeaa psoriaasia sairastavilla ja nuorilla psoriaatikoilla «Schmitt J, Ford DE. Psoriasis is independently ass...»85, «Kurd SK, Troxel AB, Crits-Christoph P ym. The risk...»86. Masennusoireet ovat yleisempiä myös nivelpsoriaasipotilailla, joilla on kynsimuutoksia, merkittävä toimintakyvyn heikkenemä (HAQ > 0,5) ja suuri IL-6 pitoisuus «De Lorenzis E, Natalello G, Bruno D ym. Psoriatic ...»87. On esitetty, että systeemisellä inflammaatiolla olisi yhteys mielialan säätelyyn nivelpsoriaasipotilailla.
- Liitännäissairauksia on myös lapsipsoriaatikoilla. Yleisimpiä ovat uveiitti, kohonnut verenpaine, lihavuus, hyperlipidemia ja masennus «Burden-Teh E, Thomas KS, Ratib S ym. The epidemiol...»13, «Augustin M, Radtke MA, Glaeske G ym. Epidemiology ...»88.
- Liitännäissairaudet on huomioitava potilaan seurannassa ja kokonaisvaltaisessa hoidossa. Potilasta kannustetaan terveisiin elämäntapoihin: normaalipainoisuuteen, säännölliseen liikuntaan, tupakoimattomuuteen ja korkeintaan kohtuulliseen alkoholinkäyttöön.
- Työryhmä suosittelee, että iho- tai nivelpsoriaasia sairastavan potilaan sydän- ja verisuonisairauksien kokonaisriski arvioidaan säännöllisin väliajoin, ks. Käypä hoito -suositukset Dyslipidemiat «Dyslipidemiat»5, Kohonnut verenpaine «Kohonnut verenpaine»6, Tyypin 2 diabetes «Tyypin 2 diabetes»7 ja Lihavuus (lapset, nuoret ja aikuiset) «Lihavuus (lapset, nuoret ja aikuiset)»8.
Iho- ja nivelpsoriaasin hoidon tavoitteet
- Hoidon tavoitteena ovat oireiden minimointi, elämänlaadun parantaminen ja potilaan
työ- ja toimintakyvyn säilyttäminen. Parantavaa hoitoa ei ole.
- Nivelpsoriaasissa pyritään tulehdusreaktion sammuttamiseen ja rakenteellisten vaurioiden estämiseen.
- Hoitomuoto valitaan aina yksilöllisesti.
- Potilaalle on hyvä selittää, mitä kullakin hoidolla voidaan saavuttaa.
- Osa potilaista hyötyy moniammatillisesta hoidosta.
- Hoitomuodon valintaan vaikuttavat
- ihottuman vaikeusaste ja nivelpsoriaasin aktiivisuus ja ilmenemismuodot (ks. kohdat Ihopsoriaasin vaikeusaste «A1»2, Nivelpsoriaasin aktiivisuuden arviointi «A12»3 ja Taulukko «Nivelpsoriaasin ilmenemismuotoja ...»15 Nivelpsoriaasin ilmenemismuotoja)
- potilaan mahdollisuus ja kyky sitoutua hoidon toteuttamiseen
- potilaskohtaiset vasta-aiheet
- potilaan kokemukset aiemmista hoidoista
- potilaan muut sairaudet.
- Riittävä tieto sairaudesta ja sen hoidoista sekä hoitojen vaikutuksista ja käytännön
toteutuksesta lisännee potilaan valmiuksia sopeutua sairauteensa.
- Ks. lisätietoa sairaudesta Ihotautitalosta «https://www.terveyskyla.fi/ihotautitalo/ihotaudit/psoriaasi»4 ja Reumatalosta «https://www.terveyskyla.fi/reumatalo/tietoa/selk%C3%A4rankareumat/nivelpsoriaasi»5.
- Kirjalliset potilasohjeet ovat saatavilla Terveyskirjastosta «http://www.terveyskirjasto.fi/»6 ja Psoriasisliiton internetsivuilta «http://www.psoriasisliitto.fi»7.
- Sopeutumisvalmennuskursseista on tietoa Psoriasisliiton internetsivuilla «http://www.psoriasisliitto.fi»7.
Ihopsoriaasi
Diagnoosi
- Diagnoosi tehdään kliinisen kuvan perusteella.
- Ihokoepalasta on joskus hyötyä erotusdiagnostiikassa.
- Ihokoepala otetaan keskeltä hoitamatonta läiskää (ks. Lääkärin käsikirjan artikkeli: Ihokoepalan oton aiheet ja tekniikka «Ihokoepalan oton aiheet ja tekniikka»1 (vaatii käyttöoikeuden)).
Taudinkuva ja erotusdiagnostiikka
- Ihopsoriaasin taudinkuvaa ja erotusdiagnostiikkaa kuvataan taulukossa «Ihopsoriaasin taudinkuva, erotusdiagnostiikka ja hoito...»2.
- Psoriaasia esiintyy kaikilla ihoalueilla ja kynsissä.
- Ihottuman laajuus vaihtelee muutamasta pienestä läiskästä lähes koko ihon peittävään ihottumaan.
- Psoriaasiin saattaa liittyä kutinaa ja ihon arkuutta.
- Tyypillistä ihottumalle on rauhallisten ja oireisten kausien vaihtelu.
- Psoriaasi voi ilmaantua ihon vauriokohtiin (Köbnerin ilmiö).
Vaikeusaste
- Vaikeusasteen arvioinnissa on huomioitava muun muassa
- objektiivisesti todettavissa olevien iho-oireiden laajuus ja voimakkuus
- subjektiivisten oireiden, kuten kutinan ja kivun, voimakkuus
- taudin vaikutus potilaan elämään ja elämänlaatuun «Finlay AY, Coles EC. The effect of severe psoriasi...»89, «Rapp SR, Feldman SR, Exum ML ym. Psoriasis causes ...»90
- aikaisempien hoitojen vaikuttavuus
- niveloireet.
- Objektiivisten iho-oireiden tavallisesti käytettyjä mittareita, jotka sopivat vain
läiskäpsoriaasin mittaamiseen, ovat muun muassa
- psoriaasin prosenttiosuus ihon pinta-alasta (body surface area, BSA)
- Apukeinona voidaan käyttää likiarvoa 1 % = käden jäljen (kämmen ja sormet) pinta-ala «Burden AD, Hilton Boon M, Leman J ym. Diagnosis an...»91, «Ahlehoff O, Gislason GH, Charlot M ym. Psoriasis i...»92, «Gelfand JM, Troxel AB, Lewis JD ym. The risk of mo...»93, «Daudén E, Puig L, Ferrándiz C ym. Consensus docume...»94.
- PASI (psoriasis area and severity index).
- Pään, vartalon, ylä- ja alaraajojen alueilta arvioidaan erikseen ihottuman prosenttiosuus sekä läiskien punoitus, paksuus ja hilseily, jotka laskentataulukkoon sijoitettuina antavat lukuarvon asteikolla 0–72 (PASI-laskin «hoi50062d.xls»2).
- psoriaasin prosenttiosuus ihon pinta-alasta (body surface area, BSA)
- Psoriaasiin ja muihin ihosairauksiin liittyvän elämänlaadun mittarina on käytetty eniten Dermatology Life Quality Index (DLQI) -nimistä kymmenen kysymyksen sarjaa, joka antaa lukuarvon asteikolla 0–30 (kyselyn ohjeet «hoi50062b.pdf»1, suomenkielinen kysely «https://www.cardiff.ac.uk/medicine/resources/quality-of-life-questionnaires/dermatology-life-quality-index»3).
- Ihopsoriaasi jaetaan nykyisin useissa suosituksissa «Strober B, Ryan C, van de Kerkhof P ym. Recategori...»95, lääkkeiden korvattavuuskriteereissä ja valtaosassa väestöpohjaisia epidemiologisia
tutkimuksia kahteen vaikeusasteryhmään:
- lievään psoriaasiin
- Ihopsoriaasia pidetään lievänä, kun se on suppea-alainen ja hallittavissa pelkillä paikallishoidoilla.
- vaikeaan psoriaasiin.
- Ihopsoriaasia pidetään vaikeana, kun ihottuman prosenttiosuus koko ihon pinta-alasta (BSA) on yli 10 % tai PASI on yli 10 tai DLQI on suurempi kuin 10.
- Vaikeaksi luetaan myös pinta-alaltaan suppeampi (tai PASI alle 10) psoriaasi, jos se oireilee voimakkaana tai märkärakkulaisena erityisillä alueilla, esimerkiksi kämmenissä, jalkapohjissa, kasvoissa tai genitaaleissa.
- Psoriaasi ei ole hallittavissa toteutetuilla paikallishoidoilla.
- lievään psoriaasiin
Hoito
- Ks. hoitoalgoritmi (kaavio «Ihopsoriaasin hoitomuodon valinta»2) ja taulukko «Ihopsoriaasin taudinkuva, erotusdiagnostiikka ja hoito...»2.
- Suppea-alaista ihopsoriaasia ei tarvitse hoitaa, ellei se haittaa potilasta.
| Päätyypit | Erotusdiagnostiikka | Hoito |
|---|---|---|
| Pisarapsoriaasi (psoriasis guttata) | ||
Kuvat «Pisarapsoriaasi eli psoriasis guttata»3, «Pisarapsoriaasi eli psoriasis guttata»4, «Pisarapsoriaasi eli psoriasis guttata»5, «Pisarapsoriaasi eli psoriasis guttata»6 ja «Pisarapsoriaasi eli psoriasis guttata»7
|
Kuvakollaasi pisarapsoriaasin erotusdiagnostiikasta «Esimerkkejä pisarapsoriaasin erotusdiagnostiikasta huomioitavista ihottumista»8
|
|
| Läiskäpsoriaasi (psoriasis vulgaris) | ||
Kuvat «Läiskäpsoriaasi eli psoriasis vulgaris»9, «Läiskäpsoriaasi eli psoriasis vulgaris»10, «Läiskäpsoriaasi eli psoriasis vulgaris»11, «Läiskäpsoriaasi eli psoriasis vulgaris»12, «Läiskäpsoriaasi eli psoriasis vulgaris»13, «Läiskäpsoriaasi eli psoriasis vulgaris»14, «Läiskäpsoriaasi eli psoriasis vulgaris»15 ja «Läiskäpsoriaasi eli psoriasis vulgaris»16
|
Kuvakollaasi läiskäpsoriaasin erotusdiagnostiikasta «Läiskäpsoriaasin erotusdiagnostiikassa huomioitavia ihottumia»17
|
Lievä:
|
| Erityisalueiden psoriaasi | ||
| Taivepsoriaasi (psoriasis inversa, kuvat «Taivepsoriaasi eli psoriasis in versa»18 ja «Taivepsoriaasi kainalossa eli psoriasis in versa»19) | Kuvakollaasi taivepsoriaasin erotusdiagnostiikasta «Taivepsoriaasin erotusdiagnostiikassa huomioitavia ihottumia»20
|
|
| Päänahan psoriaasi (psoriasis capitis, kuvat «Päänahan psoriaasi»21, «Päänahan psoriaasi»22, «Päänahan psoriaasi»23, «Päänahan psoriaasi»24, «Päänahan psoriaasi»25) | Kuvakollaasi päänahan psoriaasin erotusdiagnostiikasta «Päänahan psoriaasin erotusdiagnostiikassa huomioitavia ihottumia»26
|
|
| Kasvopsoriaasi (kuva «Otsan psoriaasi»27) | Kuvakollaasi kasvopsoriaasin erotusdiagnostiikasta «Kasvopsoriaasin erotusdiagnostiikassa huomioitavia ihottumia»28
|
|
| Kämmenten ja jalkapohjien psoriaasi (kuvat «Jalkapohjien psoriaasi»29, «Jalkapohjien psoriaasi»30, «Jalkapohjien psoriaasi»31, «Kämmenten psoriaasi»32, «Kämmenten psoriaasi»33, «Kämmenten psoriaasi»34, «Kämmenten psoriaasi»35, «Kämmenten psoriaasi»36) | Kuvakollaasi kämmen- ja jalkapsoriaasin erotusdiagnostiikasta «Kämmen- ja jalkapohjapsoriaasin erotusdiagnostiikassa huomioitavia ihottumia»37
|
|
| Sukupuolielinten psoriaasi (kuva «Genitaalialueen psoriaasi»38) | Erotusdiagnostiikka:
|
|
| Märkärakkulainen psoriaasi (psoriasis pustulosa) | ||
Yleistynyt muoto
|
|
|
Paikallinen muoto
|
|
|
| Koko ihon psoriaasi (psoriasis erythrodermica) | ||
Kuva «Erytroderminen psoriaasi»40
|
|
|
| Psoriaasin kynsimuutokset | ||
| Kuvat «Psoriaasin kynsimuutoksia»41, «Psoriaasin kynsimuutoksia»42, «Psoriaasin kynsimuutoksia»43, «Psoriaasin kynsimuutoksia»44 |
|
|
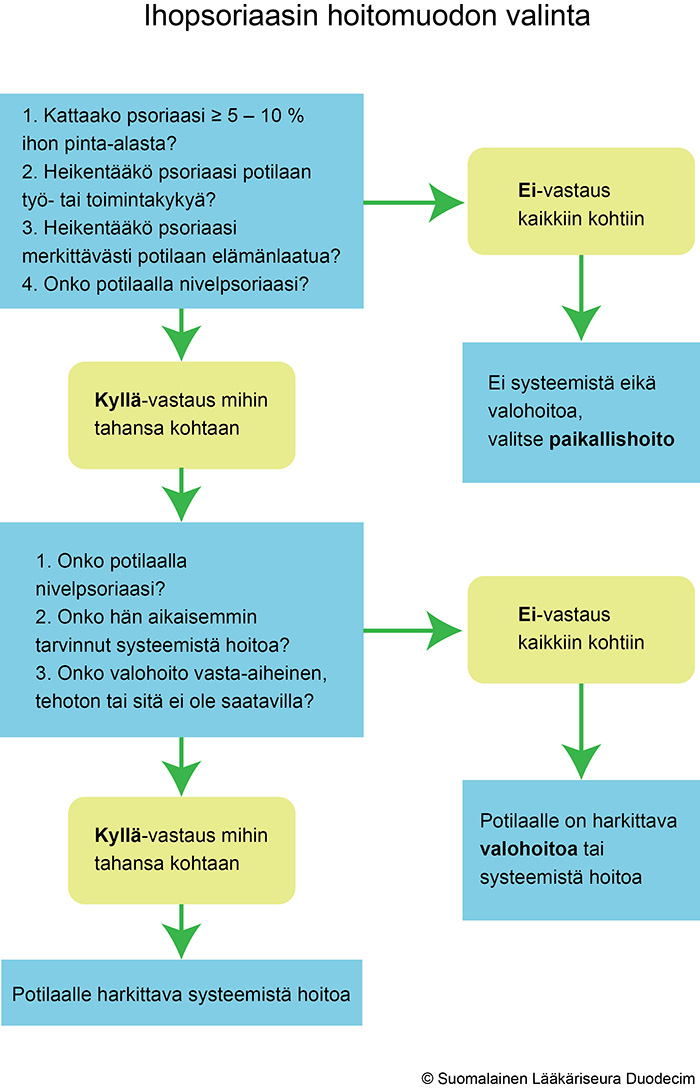
Ihopsoriaasin hoitomuodon valinta
© Suomalainen Lääkäriseura Duodecim
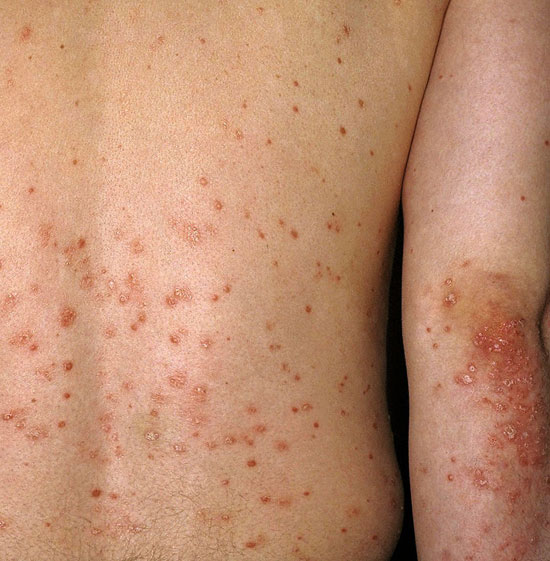
Pisarapsoriaasi eli psoriasis guttata.
© Raimo Suhonen
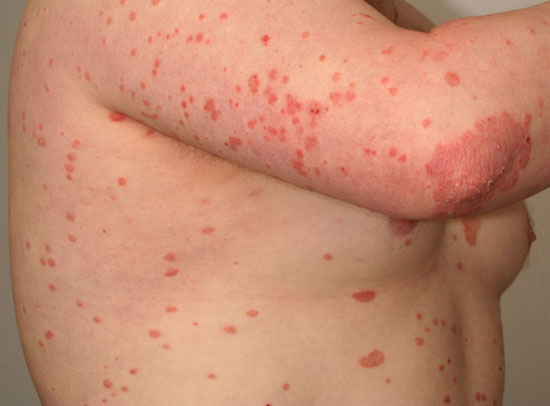
Pisarapsoriaasi eli psoriasis guttata
© Raimo Suhonen
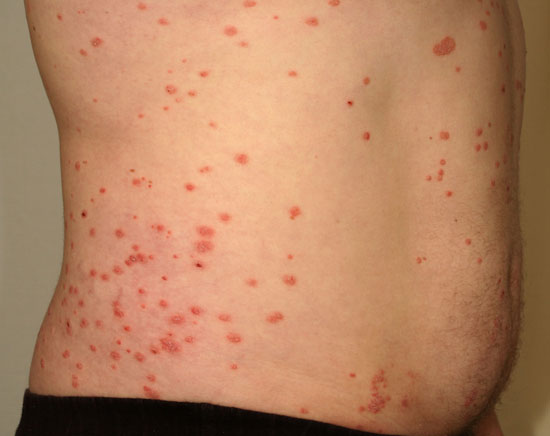
Pisarapsoriaasi eli psoriasis guttata
© Raimo Suhonen
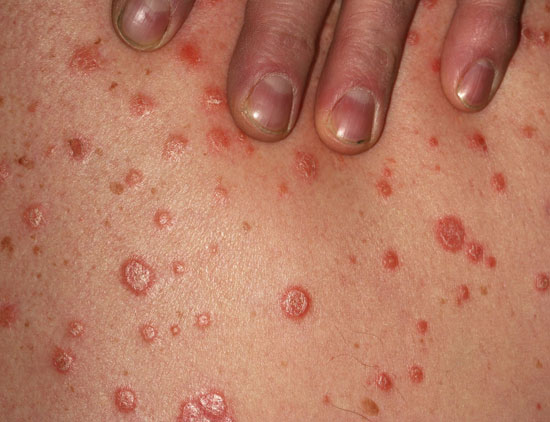
Pisarapsoriaasi eli psoriasis guttata
© Raimo Suhonen
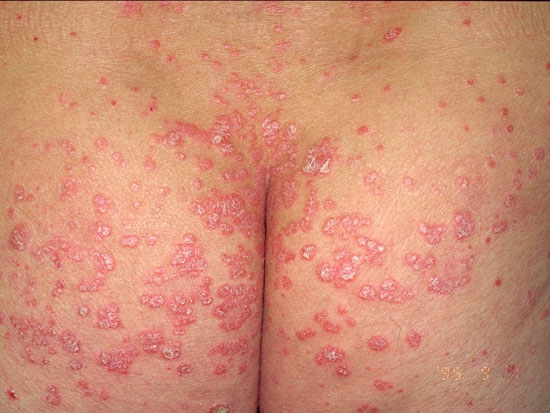
Pisarapsoriaasi eli psoriasis guttata
© Raimo Suhonen
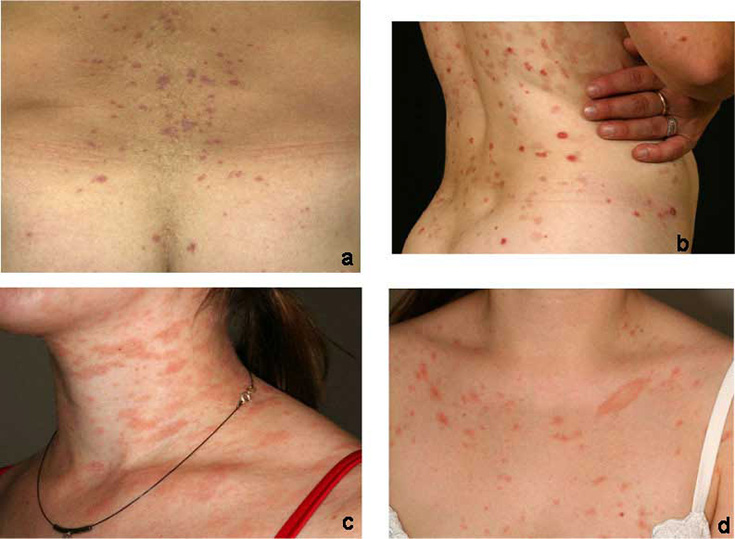
Esimerkkejä pisarapsoriaasin erotusdiagnostiikasta huomioitavista ihottumista: a= lichen planus eli punajäkälä (a), pityriasis lichenoides chronica (b), pityriasis rosea (c) ja pityriasis rosea (d).
© Raimo Suhonen
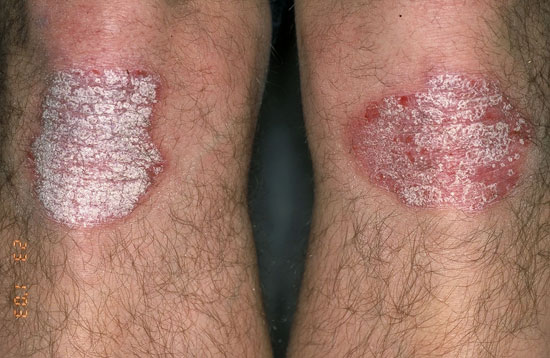
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
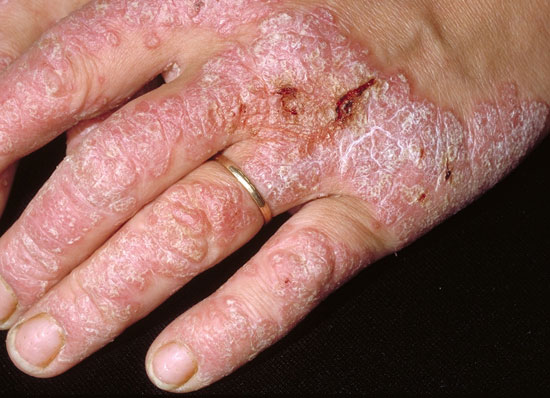
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
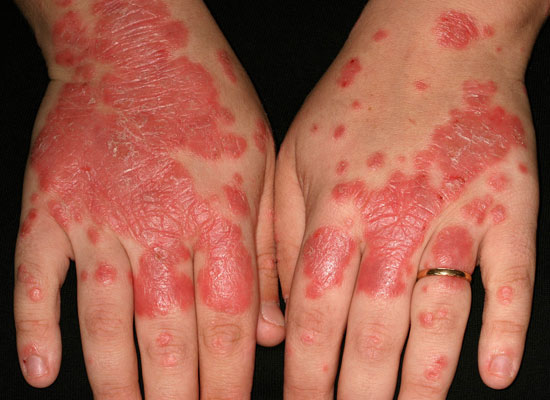
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
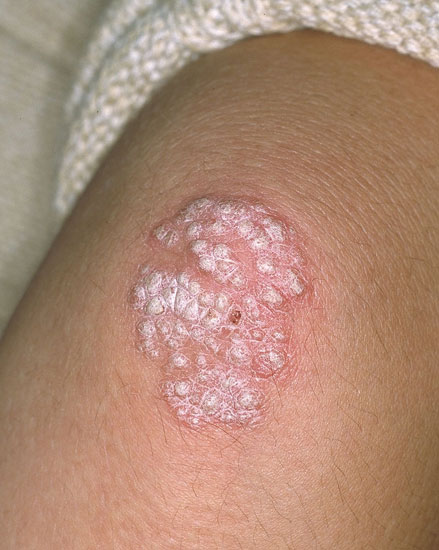
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
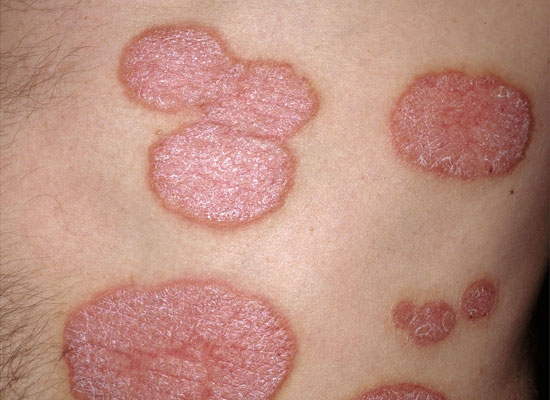
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
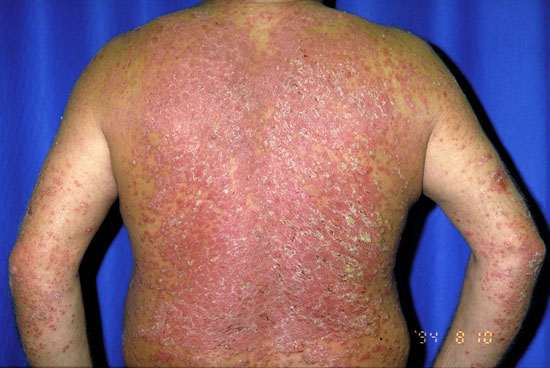
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
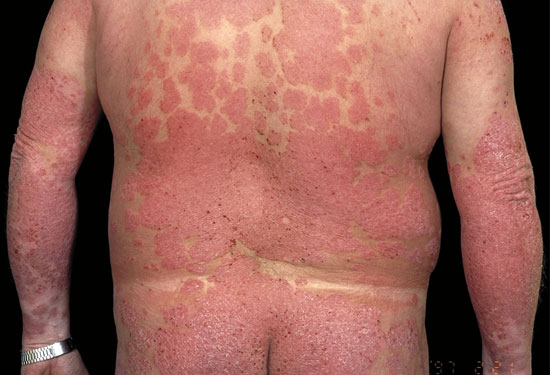
Läiskäpsoriaasi eli psoriasis vulgaris
© Raimo Suhonen
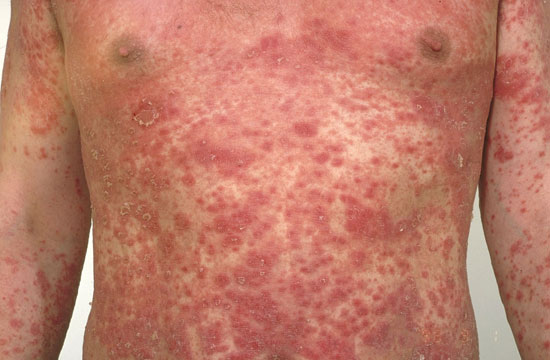
Laaja-alainen, lähes erytroderminen läiskäpsoriaasi, jossa myös pustulaarisen psoriaasin piirteitä.
© Raimo Suhonen
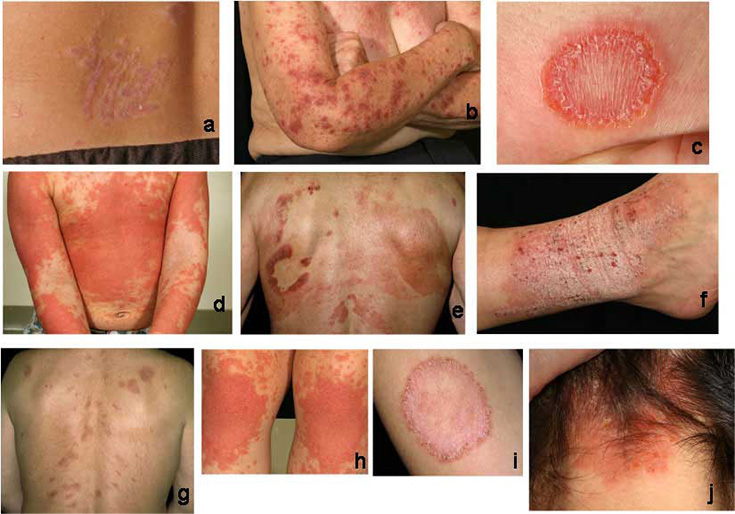
Läiskäpsoriaasin erotusdiagnostiikassa huomioitavia ihottumia: läiskäekseema (eczema nummulare) (b, c), neurodermatiitti (f, j), silsa (tinea) (i), punajäkälä (lichen planus) (a, g), ihon T-solulymfooma (Mycosis fungoides) (e), pityriasis rubra pilaris (d, h).
© Raimo Suhonen
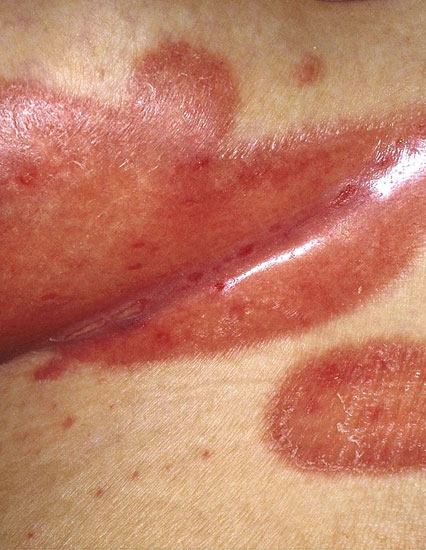
Taivepsoriaasi eli psoriasis in versa
© Raimo Suhonen
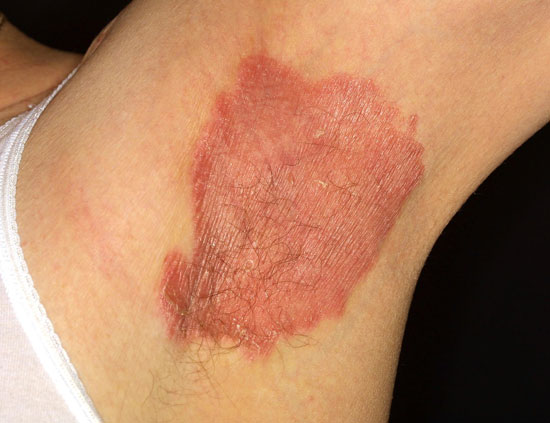
Taivepsoriaasi kainalossa eli psoriasis in versa
© Raimo Suhonen
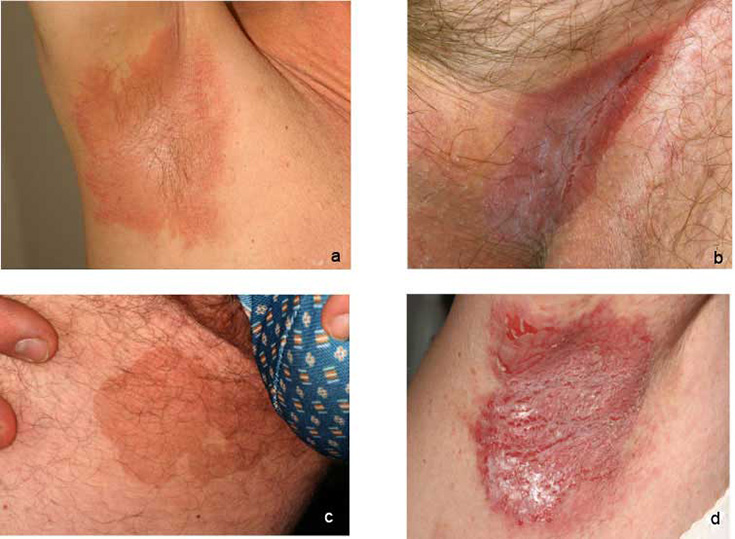
Taivepsoriaasin erotusdiagnostiikassa huomioitavia ihottumia ovat mm. hiivan aiheuttama intertrigo, seborroinen ekseema (a, b), bakteeri-infektion aiheuttama taivealueiden ihottuma (erytrasma) (c) ja Mb Hailey-Hailey (Benign chronic familial pemphigus) (d).
© Raimo Suhonen
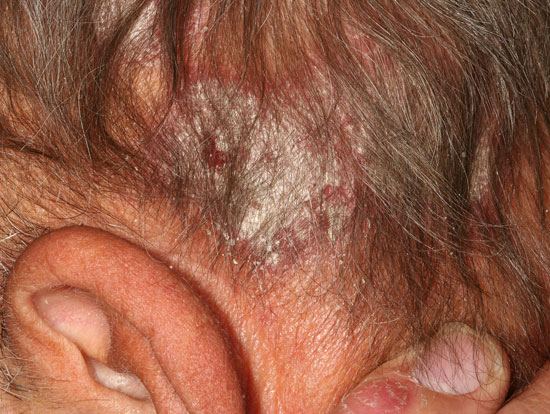
Päänahan psoriaasi
©: Raimo Suhonen

Päänahan psoriaasi
© Raimo Suhonen
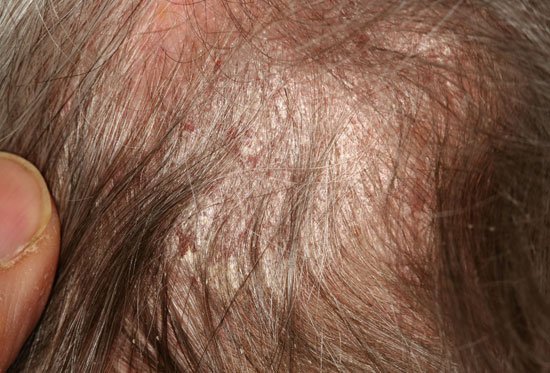
Päänahan psoriaasi
© Raimo Suhonen
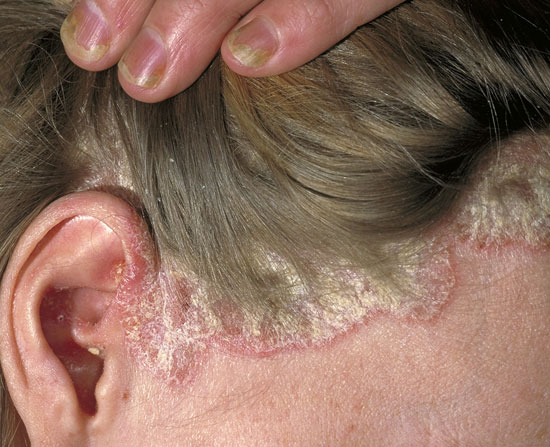
Päänahan psoriaasi
© Raimo Suhonen
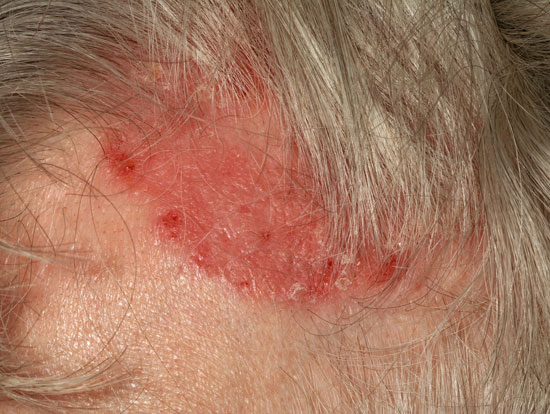
Päänahan psoriaasi
© Raimo Suhonen
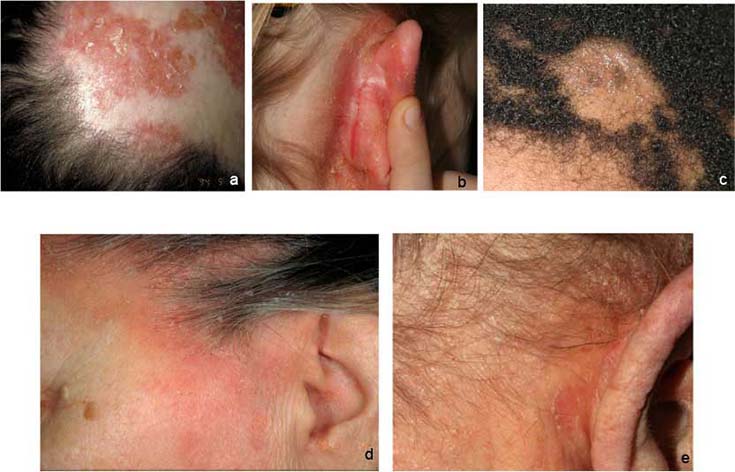
Päänahan psoriaasin erotusdiagnostiikassa huomioitavia ihottumia ovat mm. seborroinen ekseema (b, d, e), silsa (tinea) (c) ja punahukka (DLE) (a).
© Raimo Suhonen
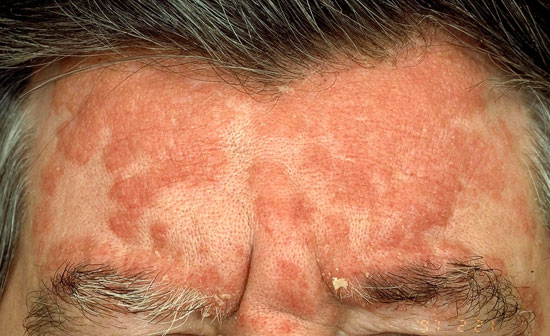
Otsan psoriaasi
© Raimo Suhonen
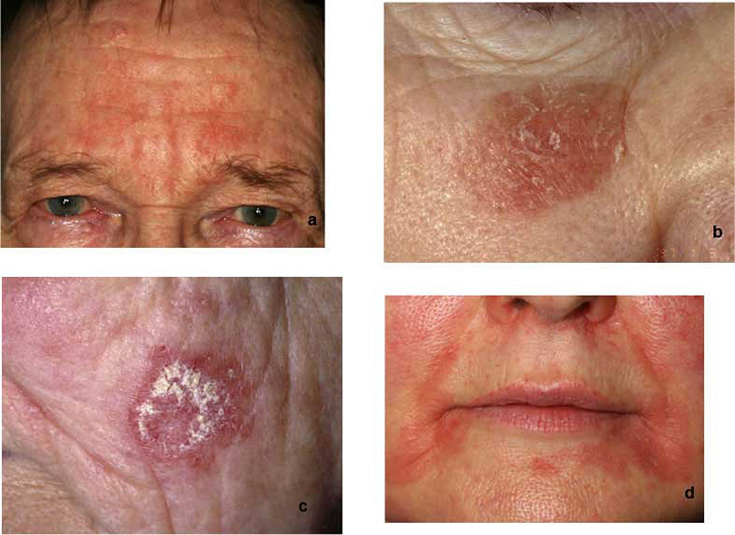
Kasvopsoriaasin erotusdiagnostiikassa huomioitavia ihottumia ovat esim. taliköhnä (seborroinen ekseema) (a, d), punahukka (DLE) (c) ja joskus myös aktiini keratoosi (b).
© Raimo Suhonen
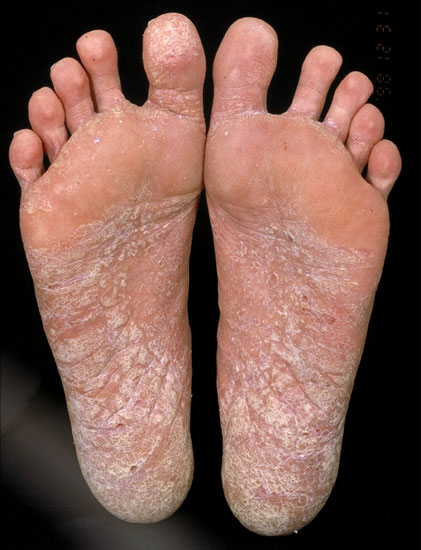
Jalkapohjien psoriaasi
© Raimo Suhonen
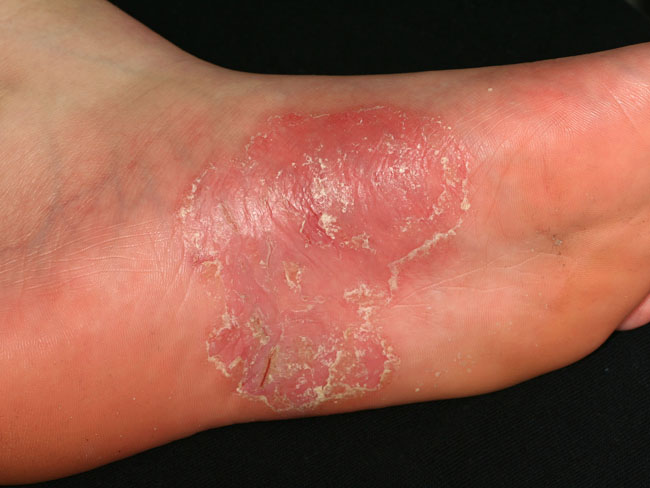
Jalkapohjien psoriaasi
© Raimo Suhonen
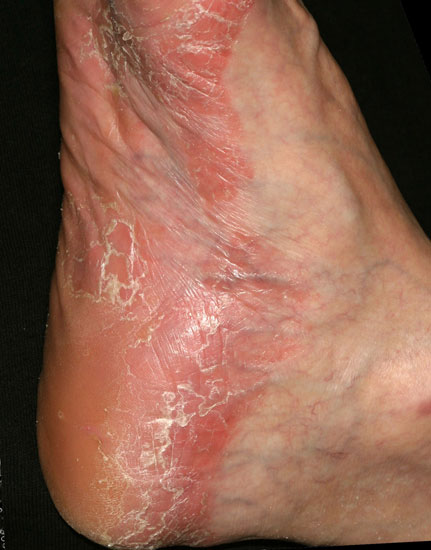
Jalkapohjien psoriaasi
© Raimo Suhonen
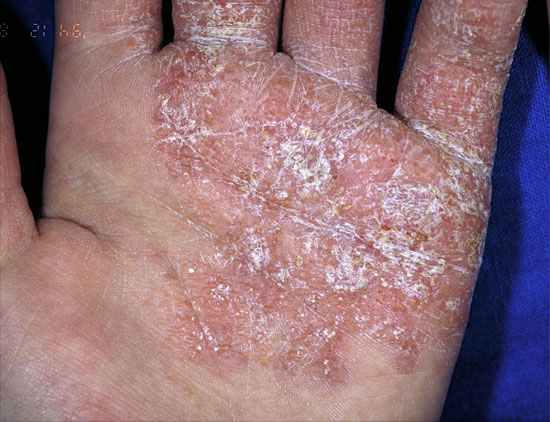
Kämmenten psoriaasi
© Raimo Suhonen
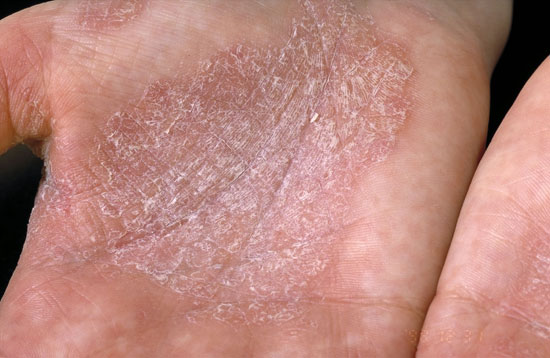
Kämmenten psoriaasi
© Raimo Suhonen
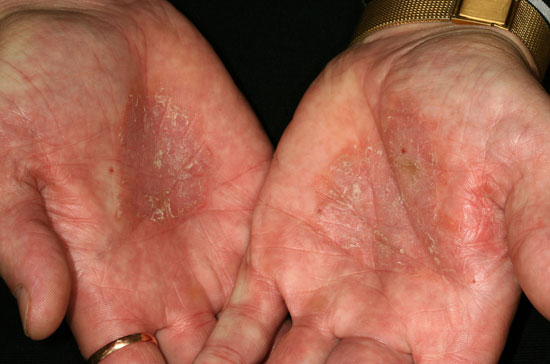
Kämmenten psoriaasi
© Raimo Suhonen
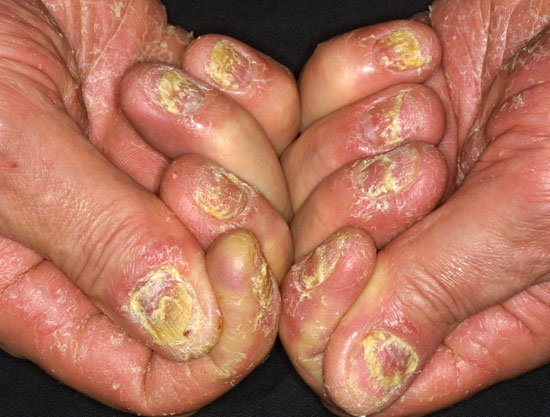
Kämmenten psoriaasi
© Raimo Suhonen
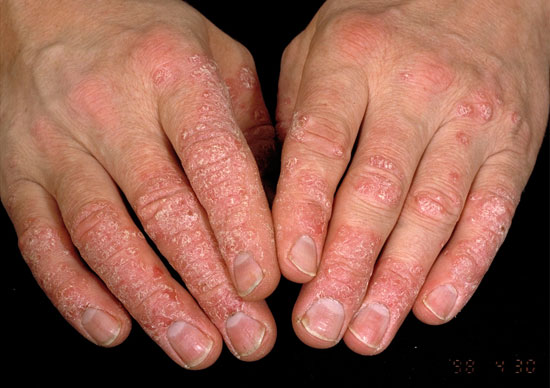
Kämmenten psoriaasi
© Raimo Suhonen
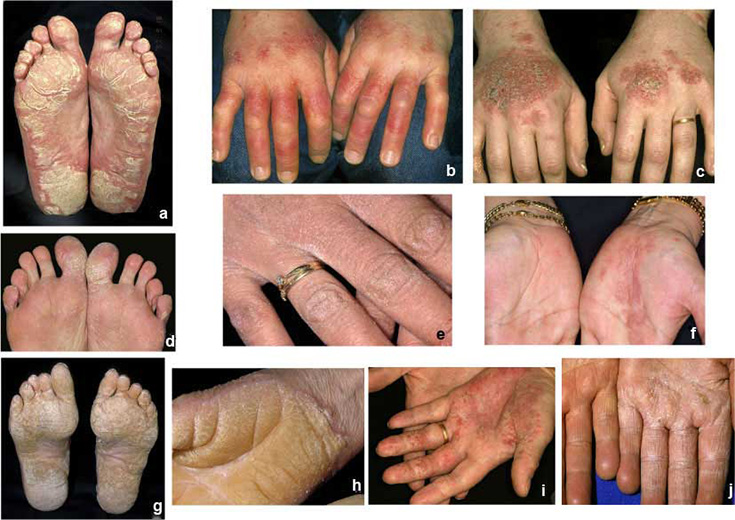
Kämmen- ja jalkapohjapsoriaasin erotusdiagnostiikassa huomioitavia ihottumia ovat muun muassa ekseemat, kuten atoopikon krooninen käsi- ja jalkaihottuma (kuva a), läiskäekseema (kuvat c ja i) tai toksinen ekseema (kuva e), silsa (tinea) (kuvat d ja j), hyperkeratoosit (keratodermat) (kuvat g ja h), punajäkälä (lichen planus) (kuva f) tai kosketusallergiat (kuva b).
© Raimo Suhonen
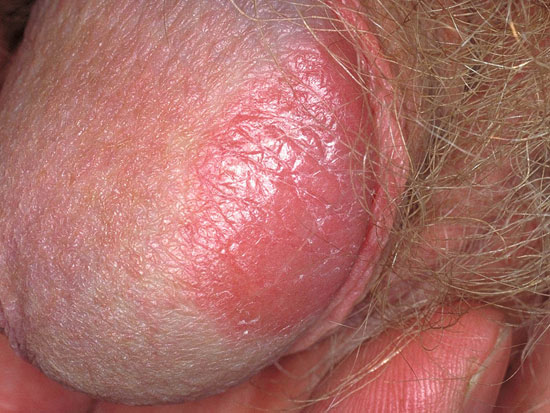
Genitaalialueen psoriaasi
© Raimo Suhonen
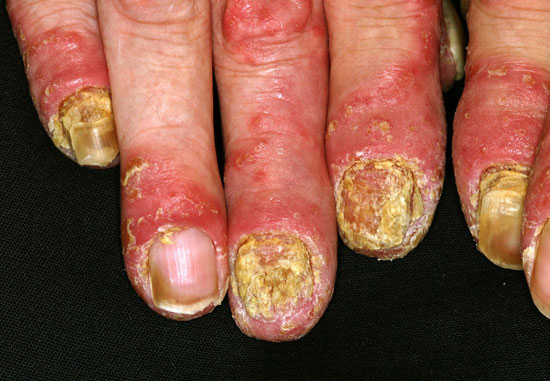
Sormien pustuloiva psoriaasi eli Acrodermatitis continua Hallopeau
© Raimo Suhonen
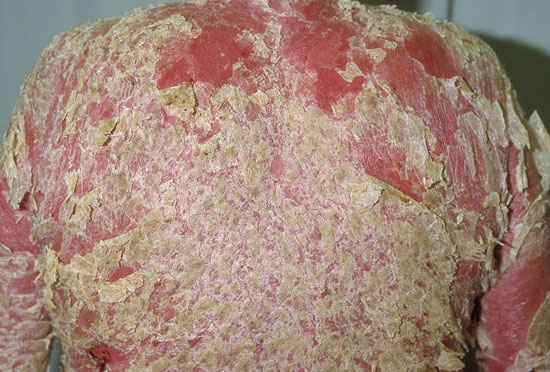
Erytroderminen psoriaasi
©: Raimo Suhonen
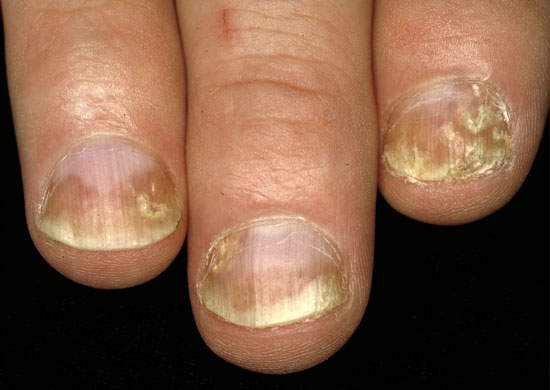
Psoriaasin kynsimuutoksia
© Raimo Suhonen
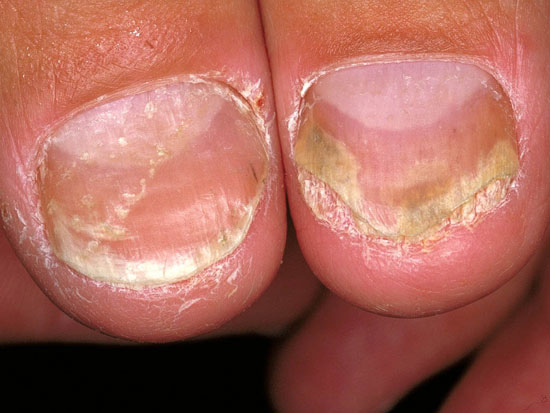
Psoriaasin kynsimuutoksia
© Raimo Suhonen
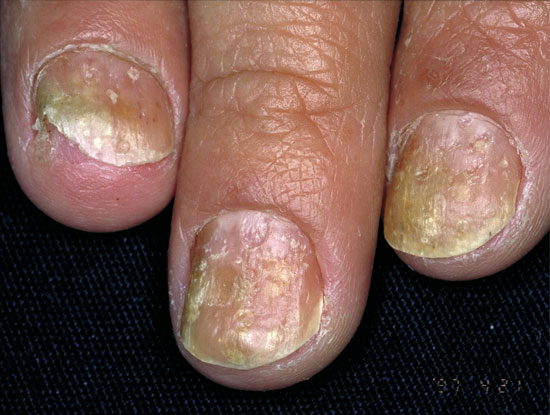
Psoriaasin kynsimuutoksia
© Raimo Suhonen
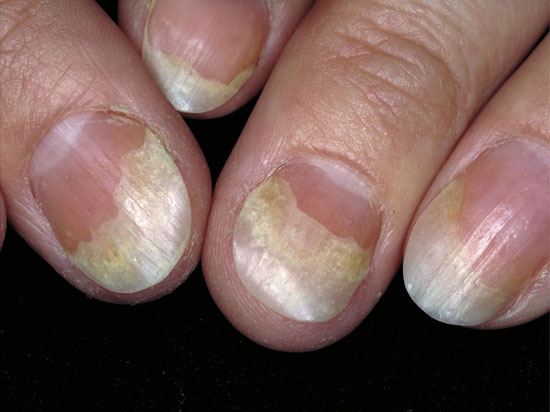
Psoriaasin kynsimuutoksia
© Raimo Suhonen
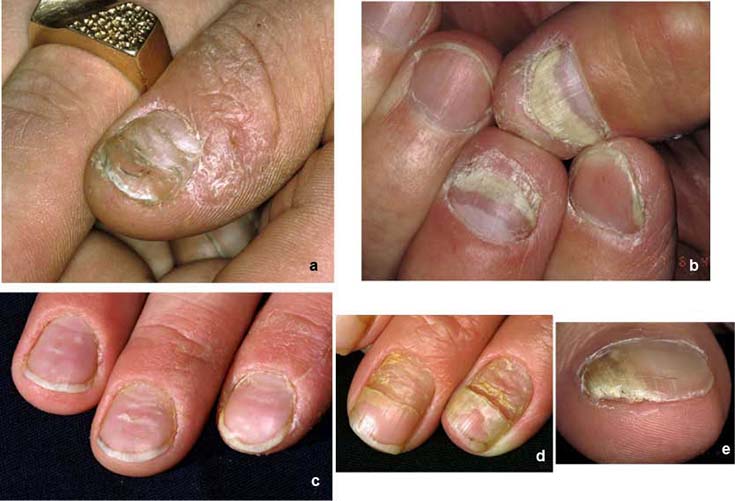
Kynsipsoriaasin erotusdiagnostiikassa huomioitavia kynsimuutoksia ovat mm. käsiekseemojen aiheuttamat kynsimuutokset (a, c, d) ja kynsisilsa (tinea) (b, e).
© Raimo Suhonen
Paikallishoito
- Valtaosalle potilaista riittää paikallishoito.
- Lisäksi paikallishoitoa käytetään muiden hoitojen tukena laaja-alaisessa psoriaasissa.
- Lääkevoiteiden annosmäärät riippuvat hoidettavan ihoalueen laajuudesta «Lääkevoiteiden kulutus ihotautien hoidossa»2.
Perusvoiteet
- Perusvoiteen säännöllinen siveleminen puhtaalle iholle vähentää ihottuman kuivuutta, kutinaa ja hilseen määrää mutta tuskin yksinään poistaa ihottumaa «Lodén M. Role of topical emollients and moisturize...»96.
Salisyylihappovoide
- Salisyylihappovoidetta käytetään paksuhilseisen psoriaasin kuorimiseen «Salisyylihappopitoinen voide psoriaasi-ihottuman hilseen pehmittämiseksi»3.
- Paksu hilsekerros estää lääkevoiteiden imeytymistä ja hidastaa valohoidon tehoa.
- Voide voi ärsyttää etenkin tervettä ihoa.
- Voide imeytyy ihon läpi.
- Laaja-alaisen psoriaasin (yli 20 % ihon pinta-alasta) hoitoon voide ei sovi «Lebwohl M. The role of salicylic acid in the treat...»97.
- Voidetta ei tule käyttää välittömästi ennen valohoitoa «Fetil E, Ozka S, Soyal MC ym. Effects of topical p...»98, «Lebwohl M, Martinez J, Weber P ym. Effects of topi...»99.
- Salisyylihappovoide absorboi UV-säteitä.
Kortikosteroidivoiteet
- Kortikosteroidivoiteet soveltuvat useimpien psoriaasityyppien hoitoon, mutta niitä ei pidä käyttää yli 10 % ihon pinta-alasta kattavan psoriaasin pääasiallisena hoitona.
- Vaikutus on anti-inflammatorinen «Surber C, Itin PH, Bircher AJ ym. Topical corticos...»100.
- Valmiste ja voidepohja valitaan psoriaasin tyypin ja ihoalueen mukaan:
- ohuelle taivealueelle ja kasvoihin luokan I–II valmiste
- paksuihin plakkimaisiin läiskiin luokan III–IV valmiste «Mason J, Mason AR, Cork MJ. Topical preparations f...»101.
- Voiteet annostellaan 1–2 kertaa vuorokaudessa, paitsi luokan IV valmisteet vain kerran
vuorokaudessa.
- Enimmäisannos on 30–50 g viikossa.
- Hoitoaika:
- Ohuen ihon alueilla (kasvot, taipeet) hoitoaika on yhtäjaksoisesti 1–2 viikkoa.
- Paksumman ihon alueilla (vartalo, raajojen ojentajapuolet, kämmenet, jalkapohjat) hoitoaika on 3–4 viikkoa.
- Erityisesti ryhmän IV kortikosteroidit lopetetaan asteittain.
- Hoitoa voidaan jatkaa kuureina tai ylläpitohoitona 2 päivänä viikossa.
- Ohuilla ihoalueilla siirrytään nopeasti hoitovaihtoehtoihin, joissa ei ole kortikosteroideja. Ks. Erityisalueiden hoidot «A3»4.
- Kortikosteroidivoiteet eivät sovellu pitkäaikaiseen päivittäiseen käyttöön «Kortikosteroidivoiteet psoriaasin hoidossa»4.
- Mahdollisena haittavaikutuksena on korjaantumaton ihoatrofia.
- Ihon kollageenin puoliintumisaika on pitkä, joten atrofia ilmaantuu viiveellä.
- Lyhytkin kortikosteroidivoidehoito vähentää kollageenin tuotantoa ihossa jopa usean viikon ajaksi. Kollageenisynteesin korjaantumisaikaa ei tunneta luotettavasti «Haapasaari KM, Risteli J, Oikarinen A. Recovery of...»102, «Murdoch D, Clissold SP. Calcipotriol. A review of ...»103.
- Mahdollisena haittavaikutuksena on korjaantumaton ihoatrofia.
- Kortikosteroidivoiteet voivat aiheuttaa lisämunuaislamaa, mikä on huomioitava erityisesti silloin, kun hoidetaan laaja-alaista ihottumaa tai vanhuksia ja lapsia tai kun käytetään vahvoja tai erityisen vahvoja kortikosteroideja.
- Oireeton aika käytön jälkeen on usein vain joitakin viikkoja.
D-vitamiinijohdokset (kalsipotrioli ja kalsitrioli)
- D-vitamiinijohdokset vähentävät interleukiini 36:n ja transkriptiotekijä NF-κB:n aktivoitumista sekä edistävät solujen erilaistumista ja apoptoosia ihon okasolukerroksessa «Murdoch D, Clissold SP. Calcipotriol. A review of ...»103, «Liu X, Liu Y, Xu M ym. Zinc finger protein A20 is ...»104, «Germán B, Wei R, Hener P ym. Disrupting the IL-36 ...»105.
- Paras hoitotapa on annostella D-vitamiinijohdokset kahdesti päivässä, kunnes psoriaasiläiskät
ovat parantuneet.
- Hyvään hoitotulokseen pääsy voi kestää jopa 6 viikkoa.
- Hoitotuloksen pysyvyydestä ei ole luotettavaa tutkimusnäyttöä.
- D-vitamiinijohdokset sopivat pitkäaikaiskäyttöön «Barnes L, Altmeyer P, Fôrstrôm L ym. Long-term tre...»106, «Ramsay CA, Berth-Jones J, Brundin G ym. Long-term ...»107.
- Paikallinen ihoärsytys on tavallisin haittavaikutus, ja se voi rajoittaa D-vitamiinijohdosten käyttöä herkillä ihoalueilla (taivealueet ja kasvot) «Bruner CR, Feldman SR, Ventrapragada M ym. A syste...»108, «Carboni I, de Felice C, Bergamin A ym. Topical use...»109, «Ortonne JP, Humbert P, Nicolas JF ym. Intra-indivi...»110.
- Liika-annostus saattaa aiheuttaa hyperkalsemiaa.
- Ohjeen mukaisia annoksia (kalsipotriolia enintään 100 g viikossa ja kalsitriolia 30 g/vrk) käytettäessä ei ole odotettavissa kalsiumaineenvaihdunnan häiriöitä «Bourke JF, Iqbal SJ, Hutchinson PE. Vitamin D anal...»111.
- Suositettua annosta ei tule ylittää ilman tarkkaa laboratorioseurantaa (fP-Pi, P-Ca, dU-Ca, P-AFOS) «Berth-Jones J, Bourke JF, Iqbal SJ ym. Urine calci...»112.
Kortikosteroidin ja kalsipotriolin yhdistelmä
- Yhdistelmä on tehokkaampi kuin kalsipotrioli tai beetametasonidipropionaatti ainoana
hoitona «Kalsipotrioli-beetametasonidipropionaattiyhdistelmävoide on kuukauden hoitokuurina tehokkaampi kuin vaikuttavat aineet käytettynä erikseen.»A.
- Yhdistelmä on saatavilla geeli-, vaahto- ja voidemuodossa, joista vaahto on tehokkain «Koo J, Tyring S, Werschler WP ym. Superior efficac...»113, «Paul C, Stein Gold L, Cambazard F ym. Calcipotriol...»114.
- Annostelu kerran vuorokaudessa, enintään 15 g kerralla.
- 4 viikon käytön jälkeen siirrytään asteittain paikallishoitoon ilman kortikosteroidivoidetta tai ylläpitohoitoon 1–2 päivänä viikossa.
- Kalsipotriolia ja beetametasonidipropionaattia sisältävissä yhdistelmävalmisteissa
on mukana vahva kortikosteroidi.
- Atrofiaa aiheuttavien ominaisuuksien vuoksi käyttöön pätevät samat säännöt kuin muihin vahvoihin kortikosteroidivoiteisiin «Kalsipotrioli-beetametasonidipropionaattivoiteen atrofogeeniset ominaisuudet vastannevat beetametasonidipropionaattia. Pitkäaikaiskäytön turvallisuutta ei ole pystytty osoittamaan.»C (ks. kohta Kortikosteroidivoiteet «A4»5).
Ditranoli eli antraliini
- Nykyään ditranolia käytetään sairaalapoliklinikoissa harvoin, koska se on värjäävää ja tahraavaa.
- Ditranoli saattaa olla yhtä tehokas kuin kalsipotrioli psoriaasin hoidossa «Ditranoli ja kalsipotrioli ovat todennäköisesti yhtä tehokkaita psoriaasin paikallishoitoja poliklinikan avohoito-osastolla käytettynä vähintään 12 viikon pituisessa hoidossa. Molemmat hoidot vaikuttavat positiivisesti psoriaatikon elämänlaatuun.»C erityisesti paksuläiskäisessä psorissa.
- Ks. lisätietoa aiheesta «Ditranoli psoriaasin hoidossa»5.
Erityisalueiden psoriaasin hoito
Hiuspohjan psoriaasin hoito
- Hiuspohjan psoriaasiin käytetään jaksoittain valmisteita, joissa on ryhmän III–IV kortikosteroidia yksinään tai yhdistelmänä salisyylihapon tai kalsipotriolin kanssa.
- Päänahan paksun hilseen irrottamiseen käytetään 5–10-prosenttista salisyylihappoa vesiliukoisessa voidepohjassa tai öljyssä «Salisyylihappopitoinen voide psoriaasi-ihottuman hilseen pehmittämiseksi»3.
- Hilseshampoota voidaan käyttää jaksoittain Malassezia-sienen pitämiseksi poissa.
Muiden erityisalueiden psoriaasin paikallishoito
- Kasvot ja hiusraja:
- ryhmän I–II paikalliskortikosteroidit 1–2 viikon hoitojaksoina
- kalsitriolivoide
- Ihoärsytystä vähentää vuorottelu kortikosteroidien kanssa.
- paikalliset kalsineuriinin salpaajat (takrolimuusi, pimekrolimuusi), jotka näyttävät
olevan tehokkaita «Paikalliset kalsineuriinin estäjät näyttävät tehoavan kasvojen ja taivealueiden psoriaasiin.»B
- Psoriaasin hoito ei kuitenkaan ole kalsineuriinin salpaajien virallinen käyttöaihe.
- Yleisiä haittavaikutuksia etenkin hoidon alussa ovat hoitoalueen ärsytys, kuumoitus ja kutina.
- Vartalon plakkipsoriaasiin kalsineuriinin salpaajat eivät näytä tehoavan «Zonneveld IM, Rubins A, Jablonska S ym. Topical ta...»115.
- Korvakäytävien hilsettä voidaan pehmittää ja poistaa ihoöljyllä ja korvahuuhteluin «Harth W, Caffier PP, Mayelzadeh B ym. Topical tacr...»116. Takrolimuusivoidetta ja kortikosteroidivoiteita voidaan käyttää jaksoittain, mutta tieteellinen näyttö asiasta puuttuu.
- Taive- ja genitaalialueiden hilseetön psoriaasi:
- Taivealueet hautuvat helposti rikki.
- Mietoon tai keskivahvaan kortikosteroidivoiteeseen voidaan liittää antimikrobinen aine tai antimykootti «Rikkipitoinen ex tempore -valmiste taivepsoriaasin hoitoon»6.
- Kalsineuriinin salpaajat tehoavat taivealueiden psoriaasiin «Paikalliset kalsineuriinin estäjät näyttävät tehoavan kasvojen ja taivealueiden psoriaasiin.»B.
- Kynsien psoriaasimuutoksiin ei ole tehokasta paikallishoitoa «Crowley JJ, Weinberg JM, Wu JJ ym. Treatment of na...»117.
- Alkavaan onykolyysiin ja kynsipedin liikasarveistumiin voi kokeilla vahvoja kortikosteroidivoiteita.
- Kynsimuutokset voivat vähentyä systeemisten lääkehoitojen yhteydessä «Gümüsel M, Özdemir M, Mevlitoglu I ym. Evaluation ...»118, «Jiaravuthisan MM, Sasseville D, Vender RB ym. Psor...»119, «Tosti A, Ricotti C, Romanelli P ym. Evaluation of ...»120. Pelkkiä kynsimuutoksia hoidetaan systeemisillä lääkkeellä kuitenkin vain harvinaisissa erityistapauksissa (esim. työkyvyn ylläpito).
- Kynsisieni kannattaa sulkea pois sieniviljelyllä myös psoriaatikolta.
- Potilas voi hyötyä terveydenhuollon ammattikoulutuksen saaneen jalkojenhoitajan tai jalkaterapeutin hoidosta.
UV-valohoidot
- Määritelmät:
- Fototerapia: ultraviolettisäteitä (UV-säteitä) käytetään hoidoksi sellaisenaan (UVB-hoidot ja SUP-hoito).
- Fotokemoterapia (PUVA-hoidot): potilaan iho herkistetään ennen valotusta UVA-säteille systeemisesti tai ulkoisesti käytettävällä psoraleenilääkkeellä.
- Käyttöaiheet:
- UV-valohoidon käyttöaiheita ovat pisara- ja läiskäpsoriaasi (kuva «Esimerkkejä keskivaikeasta pisara- ja läiskäpsoriaasista»46).
- Vasta-aiheet:
- Ehdottomia vasta-aiheita ei ole.
- Suhteellisia vasta-aiheita ovat
- pustulaarinen ja erytroderminen psoriaasi
- valoherkkyys (valoihottumat, punahukka)
- aiempi ihosyöpä tai sille altistavat tekijät (mm. siklosporiini).
- Käyttöä rajoittavat
- hoidon sitovuus
- hoidon saatavuus ja matkat hoitoon
- mahdollisesti suurentunut ihosyöpäriski.
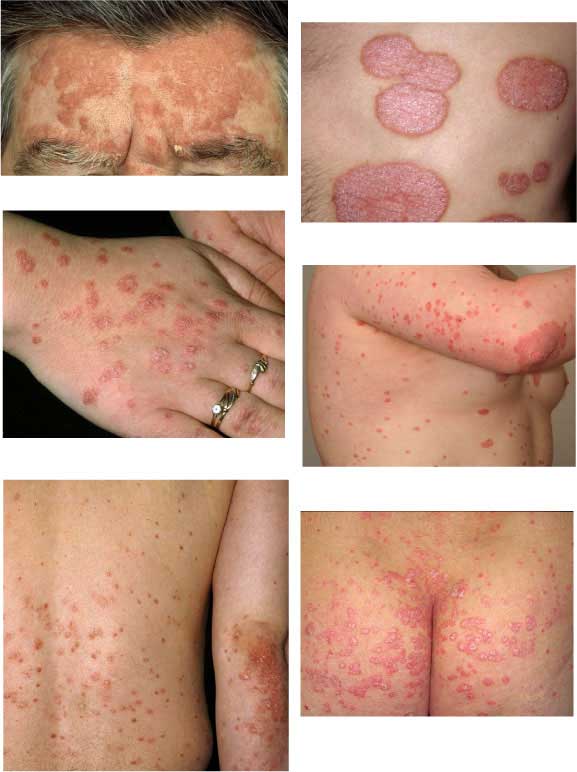
Esimerkkejä keskivaikeasta pisara- ja läiskäpsoriaasista. Näissä valohoidot ovat usein hyvä hoitovalinta.
© Raimo Suhonen
Valohoitolaitteet ja laadunhallinta
- Laitteen säteilijän UV-spektrin mukaan laitteet luokitellaan UVB-, UVA- ja SUP-laitteisiin (kaavio «Eri valohoitolamppujen emittoiman UV-säteilyn aallonpituusspektrit»47).
- Valohoitoja antavien laitosten tulee noudattaa viranomaisten antamia ohjeita. Ks. Fimean «http://www.fimea.fi/documents/160140/753095/19694_julkaisut_4_2005_UV_julkaisu_verkko_v2-rd.pdf.pdf»8 sivusto . Valvira valvoo terveydenhuollon laitteiden käytön turvallisuutta.
- Ihosairauksien UV-valohoitoja voivat antaa vain terveydenhuollon ammattihenkilöt,
jotka ovat perehtyneet valohoitoihin.
- Itsehoidosta ei ole säädöksiä.
- Potilaan saamaa kumulatiivista UV-annosta tulee seurata.
- Jokaisen hoitojakson kumulatiivinen UV-annos kirjataan sairauskertomukseen.
- Myös potilaan elinikäinen UV-rasitus kirjataan jaoteltuna PUVA-hoitoihin, UVB-hoitoihin ja luonnon UV-altistukseen (ilmastohoidot).
- Suositeltava yläraja vuosittaisille hoidoille on 2 jaksoa.
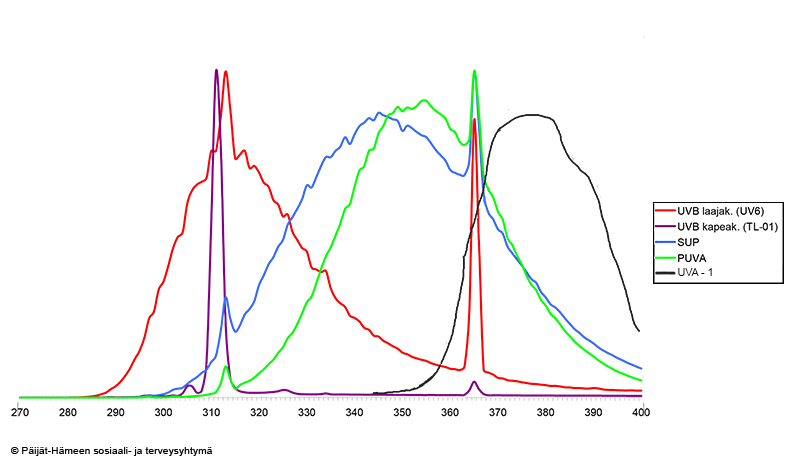
Eri valohoitolamppujen emittoiman UV-säteilyn aallonpituusspektrit
© Tapio Rantanen
UVB-hoidot
- Kapeakaistainen UVB-hoito (loisteputkityyppi TL/01, aallonpituusalue 311 ± 2 nm):
- Aikuispotilaiden ensisijainen UV-valohoito:
- Vaikea ihottuma paranee oireettomaksi noin 70 %:lla potilaista 20–30 hoitokerralla «Keskivaikea psoriaasi-ihottuma ilmeisesti paranee oireettomaksi kapeakaistaisella UVB-hoidolla noin 70 %:lla potilaista.»B.
- Luotettavia tutkimuksia tehosta verrattuna metoksaleeni-kylpy-PUVAan ei ole.
- UV-säteille herkistävät lääkkeet eivät yleensä aiheuta ongelmia kapeakaistaisessa UVB-hoidossa, sillä systeemisten lääkkeiden valoherkistymä kohdistuu UVA-aallonpituuteen.
- Hoidon toteutuksesta on lisätietoa tausta-aineistossa «Psoriaasin valohoitojen toteutus»7.
- Suomen Ihotautilääkäriyhdistyksen valojaos on laatinut suomalaisille ihotyypeille sovelletut ohjeelliset annoskaaviot (kapeakaista-UVB, annosteluohje «hoi50062a.pdf»3).
- Suositeltavin antotaajuus on 3 kertaa viikossa «Kapeakaistaisen UVB-hoidon suositeltava antotiheys lienee kolme kertaa viikossa.»C.
- Remissioaika hoidon jälkeen:
- Eri tutkimusten mukaan 6 kuukauden kuluttua hoidon loppumisesta 12–35 % potilaista on vielä remissiossa «Yones SS, Palmer RA, Garibaldinos TT ym. Randomize...»121.
- Mahdollinen akuutti haittavaikutus on punekynnyksen ylittävästä annoksesta johtuva ihon punoitus (UV-eryteema).
- Ihosyöpäriskiä suurentavasta vaikutuksesta ei ole tietoa «Hearn RM, Kerr AC, Rahim KF ym. Incidence of skin ...»122.
- Teoreettisen mallinnuksen perusteella 450 hoitokertaa kapeakaistaista UVB-hoitoa saattaisi sopia hoitokertojen ylärajaksi «Ibbotson SH, Bilsland D, Cox NH ym. An update and ...»123, «Diffey BL. Factors affecting the choice of a ceili...»124. Konsensusta asiasta ei kuitenkaan ole.
- Kapeakaistainen UVB-hoito saattaa soveltua myös kotihoitoon, jos sopiva laite tulee markkinoille «Koek MB, Buskens E, van Weelden H ym. Home versus ...»125, «Koek MB, Sigurdsson V, van Weelden H ym. Cost effe...»126.
- UVB-hoidosta on potilasohje: «Psoriaasin UV311-hoito»8.
- Aikuispotilaiden ensisijainen UV-valohoito:
- Laajakaistainen UVB-hoito (TL/12, yli 275 nm; UV6, yli 285 nm):
- Terveydenhuollonyksiköissä laajakaistainen UVB-hoito on väistyvä hoito, mutta kotikäytössä
se on mahdollinen.
- Osa psoriasisyhdistyksistä vuokraa hoitomääräyksen saaneille kotiin UVB-valohoitolaitteita «https://psori.fi/tietoa-psoriasiksesta/psoriasiksen-hoito/hoitovaihtoehdot/»9.
- Psoriasisliitto edellyttää ensimmäisellä hoitojaksolla ihotautilääkärin lähetettä.
- Kotihoidossa on noudatettava erityistä harkintaa «Koek MB, Buskens E, Bruijnzeel-Koomen CA ym. Home ...»127, «Koek MB, Buskens E, Steegmans PH ym. UVB photother...»128.
- Terveydenhuollonyksiköissä laajakaistainen UVB-hoito on väistyvä hoito, mutta kotikäytössä
se on mahdollinen.
SUP-hoito (selektiivinen ultraviolettivalohoito)
- Teho psoriaasiin on vähäinen, koska UVB-säteilyn osuus on pieni.
PUVA-hoidot
- Ulkoiseen herkistykseen perustuvat PUVA-hoidot:
- Suomessa on käytössä 8-metoksipsoraleeni (8-MOP) -kylpy-PUVA. Myös voide-PUVA on mahdollinen, kun ihottuma on rajallisilla alueilla esimerkiksi kämmenissä tai jalkapohjissa.
- Jaksottaisella PUVA-hoidolla potilas voi pärjätä useita vuosia.
- Kylpy-PUVA-hoito ei ole riskitöntä, ja se edellyttää henkilökunnalta erityistä perehtyneisyyttä «Voss A, Leverkus M, Bröcker EB ym. Topical psorale...»129.
- Pitkäaikaishoidon vaikutuksia ei tunneta tarkoin «Hannuksela-Svahn A, Pukkala E, Koulu L ym. Cancer ...»130.
- Ks. lisätietoa hoidon aloituksesta «Psoriaasin valohoitojen toteutus»7.
- Systeemiseen herkistykseen perustuvat PUVA-hoidot:
- Suomessa systeemiseen herkistykseen perustuvia PUVA-hoitoja käytetään psoriaasiin vain erityistilanteissa.
- Käytettävä psoraleeni on 8-metoksipsoraleeni (8-MOP). Pitkäaikainen hoito suurentaa
pysyvästi ihosyöpien, erityisesti okasolusyövän, riskiä «Vaikeaan psoriaasiin liittyy lievästi kohonnut ihon okasolusyövän riski, jonka tärkein riskitekijä on metoksaleeni-tabletti-PUVA-hoito.»A.
- Riski on elinikäinen, joten hoitoa saaneiden iho on tarkastettava säännöllisesti «Stern RS, Liebman EJ, Väkevä L. Oral psoralen and ...»131, «Stern RS, PUVA Follow up Study.. The risk of melan...»132.
- Fotokarsinogeneesiriskin vuoksi PUVA-hoitojen enimmäismääräksi suositellaan 200–250:tä hoitokertaa tai kumulatiivista UVA-annosta 1000 J/cm² «Griffiths CE, Clark CM, Chalmers RJ ym. A systemat...»133, «Stern RS, Lunder EJ. Risk of squamous cell carcino...»134.
Yhdistelmähoidot UV-valohoidon yhteydessä
- Kortikosteroidivoiteet:
- Kortikosteroidivoiteiden käyttö lopetetaan asteittain valohoidon yhteydessä.
- UV-valohoito aloitetaan usein kortikosteroidivoiteiden tauottamiseksi.
- Kortikosteroidivoiteen yhdistäminen UVB-hoitoihin ei näytä parantavan hoitotulosta tai pienentävän tarvittavaa UV-säteilyannosta «Griffiths CE, Clark CM, Chalmers RJ ym. A systemat...»133, «Stern RS, Lunder EJ. Risk of squamous cell carcino...»134.
- Remissioaika saattaa olla yhdistelmähoidon jälkeen lyhempi kuin pelkän UVB-hoidon «Griffiths CE, Clark CM, Chalmers RJ ym. A systemat...»133, «Lebwohl M, Menter A, Koo J ym. Combination therapy...»135.
- Kortikosteroidivoiteiden käyttö lopetetaan asteittain valohoidon yhteydessä.
- Systeeminen retinoidi (yleensä asitretiini):
- Yhdistelmä saattaa nopeuttaa ihottuman paranemista «Asitretiinin ja UVB-valon yhdistelmähoito näyttää olevan tehokkaampi kuin pelkkä UVB-valohoito.»B ja pienentää tarvittavaa UV-säteilyannosta.
- Retinoidihoidolla saattaa olla paljon valohoitoja saaneilla potilailla suotuisa okasolusyövän riskiä pienentävä vaikutus, joka häviää lääkityksen lopettamisen jälkeen «Asitretiini saattaa vähentää ihon okasolusyövän riskiä hoidon aikana.»C.
- Metotreksaatti:
- Yhdistelmä tulee kyseeseen erityistilanteissa.
- Siklosporiini:
- Siklosporiinihoitoa ei suurentuneen fotokarsinogeneesiriskin vuoksi tule yhdistää UV-valohoitoihin «Sugie N, Fujii N, Danno K. Cyclosporin-A suppresse...»136.
- Paljon UV-valohoitoja saaneille ei suositella siklosporiinihoitoa «Paul CF, Ho VC, McGeown C ym. Risk of malignancies...»137, «Marcil I, Stern RS. Squamous-cell cancer of the sk...»138, «Murphy GM. Skin cancer in patients with psoriasis-...»139.
- Biologiset lääkkeet, apremilasti ja dimetyylifumaraatti:
- Työryhmän käsityksen mukaan yhdistelmä tulee kyseeseen erityistilanteissa, mutta tutkimusnäyttö asiasta on vähäistä.
Ilmastohoito
- Ilmastohoito vastaa teholtaan UVB-valohoitoa «Snellman E. E. Heliotherapy of psoriasis (thesis)....»140.
- Noin puolella potilaista ihottuma palautuu entiselleen puolen vuoden kuluessa 4 viikon ilmastohoitomatkan päättymisestä «Snellman E. E. Heliotherapy of psoriasis (thesis)....»140.
- Hoidon vasta-aiheena on siklosporiinihoito.
- Ks. auringonotto-ohje «Auringonotto-ohje ihopsoriaasipotilaalle»9.
Systeeminen lääkehoito
- Ihopsoriaasin systeemisen hoidon aloittaa ja sitä seuraa ihotautien erikoislääkäri.
- Hyvään hoitotapaan kuuluu systeemisen lääkehoidon turvallisuuden «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10 ja tehon seuranta, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11.
- Ohjeistettu verikoeseuranta voidaan toteuttaa perusterveydenhuollossa.
- Ohjeet koskevat aikuispotilaita.
- Suomen Reumatologisen Yhdistyksen internetsivuille «https://www.reumatologinenyhdistys.fi/ohjeet/»12 on koottu ohjeita infektioalttiuden arvioinnista, rokotuksista, hepatiitti B -viruksesta ja latentista tuberkuloosista.
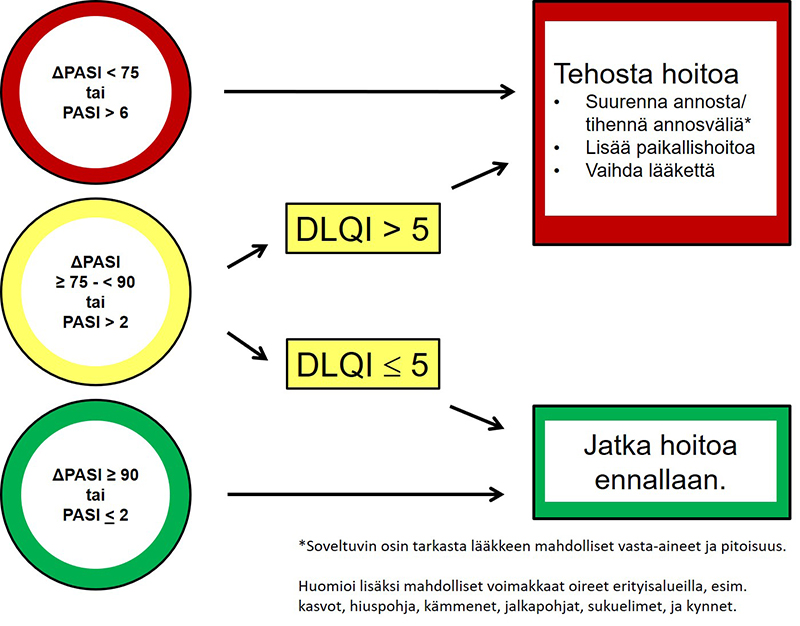
- Hoidon tavoitteena on mahdollisimman vähäoireinen tila. Mittareina käytetään yleisimmin PASI-paranemista (ΔPASI) tai absoluuttista PASIa ja elämänlaatumittaria DLQI, joilla hoitopäätöksiä voidaan perustella (ks. kuva «Biologisen hoidon tavoitelähtöinen ihopsoriaasin hoitostrategia»48).
- Biologisen hoidon tavoitteena on vähintään PASI-75-vaste (hyvä hoitovaste) mutta mielellään PASI-90-vaste (erinomainen hoitovaste). PASI-90-vasteen saavuttaneilla potilailla on merkittävästi parempi elämänlaatu kuin PASI-75-vasteen saavuttaneilla «Puig L. PASI90 response: the new standard in thera...»141, «Strober B, Papp KA, Lebwohl M ym. Clinical meaning...»142, «Elewski BE, Puig L, Mordin M ym. Psoriasis patient...»143.
- Sairausvakuutuskorvattavuus jakaa systeemiset psoriaasilääkkeet ensisijaisiin ja toissijaisiin:
- Ensisijaisia ja ilman erillistä lausuntoa peruskorvattavia ovat perinteiset lääkkeet
asitretiini, metotreksaatti ja siklosporiini.
- Erytrodermisen psoriaasin hoidossa nämä voidaan lausunnon perusteella korvata ylemmän erityiskorvattavuuden (100 %) mukaan.
- Toissijaisia ovat kaikki muut. Niihin voidaan myöntää lausunnon perusteella rajoitettu peruskorvattavuus. Sen edellytyksenä on vaikea psoriaasi, jonka hoidossa ensisijainen lääke ei ole tehonnut tai sitä ei ole voitu vasta-aiheen tai haittojen vuoksi käyttää.
- Ensisijaisia ja ilman erillistä lausuntoa peruskorvattavia ovat perinteiset lääkkeet
asitretiini, metotreksaatti ja siklosporiini.
Ensisijaiset systeemiset lääkkeet
- Käyttöaiheet (kuva «Esimerkkejä keskivaikeasta ja vaikeasta läiskäpsoriaasista ja erytrodermisestä psoriaasista sekä kämmen-, jalkapohja- ja hiuspohjan psoriaasista»49):
- vaikea läiskäpsoriaasi
- erytroderminen tai pustulaarinen psoriaasi
- paikallishoitoon reagoimaton kämmen- tai jalkapohjapsoriaasi
- vaikea hiuspohjan psoriaasi
- Hoitovasteen arvioinnista ks. taulukko «Ihopsoriaasin hoitovasteeseen liittyviä määritelmiä , ...»1.
- Asitretiini «Sbidian E, Maza A, Montaudié H ym. Efficacy and sa...»144 (taulukko «Asitretiinilääkityksessä huomioon otettavia asioita ...»3):
- Asitretiinia käytetään vaikean läiskäpsoriaasin, kämmenten ja jalkapohjien paksuhilseisen
psoriaasin sekä yleistyneen pustulaarisen psoriaasin hoidossa.
- Nivelpsoriaasiin asitretiini ei tehoa.
- Hyvä hoitovaste voidaan saavuttaa 22–25 %:lla läiskäpsoriaasia sairastavista potilaista 8 viikossa 10–50 mg:n annoksella «Gollnick H, Bauer R, Brindley C ym. Acitretin vers...»145, mutta näyttö tehosta lumelääkkeeseen verrattuna on vähäinen «Tutkimusnäyttö asitretiinin tehosta näyttää olevan vähäinen.»C.
- Läiskäpsoriaasissa asitretiinihoito voidaan yhdistää UV-valohoitoon.
- Kliininen kokemus tukee PUVA-yhdistelmähoidon paremmuutta pelkkään asitretiiniin nähden, mutta tutkimusnäyttöä tehon lisääntymisestä PUVA-hoitoon yhdistettäessä ei ole «Griffiths CE, Clark CM, Chalmers RJ ym. A systemat...»133.
- Yhdistelmähoito UVB-valon kanssa lisää tehoa pelkkään UV-valoon verrattuna. Hyvä hoitovaste voidaan saavuttaa 60 %:lla potilaista 8 viikon aikana «Ruzicka T, Sommerburg C, Braun-Falco O ym. Efficie...»146.
- Asitretiini ei heikennä immuunivastetta.
- Okasolusyövän ilmaantuvuus saattaa vähentyä hoidon aikana «Asitretiini saattaa vähentää ihon okasolusyövän riskiä hoidon aikana.»C.
- Asitretiini sopii pitkäaikaishoitoon, ja hoito voidaan tauottaa.
- Teratogeenisuuden vuoksi käyttöä pyritään välttämään fertiili-ikäisillä naisilla.
- Asitretiinia käytetään vaikean läiskäpsoriaasin, kämmenten ja jalkapohjien paksuhilseisen
psoriaasin sekä yleistyneen pustulaarisen psoriaasin hoidossa.
- Metotreksaatti (taulukko «Metotreksaattilääkityksessä huomioon otettavia asioita ...»4):
- Metotreksaattia käytetään vaikeassa psoriaasissa «Warren RB, Weatherhead SC, Smith CH ym. British As...»147.
- Jos potilaalla on myös nivelpsoriaasi, metotreksaattihoito on ensisijainen hoito.
- Läiskäpsoriaasissa metotreksaatti on tehokas «Metotreksaatti on tehokas hoito läiskäpsoriaasissa.»A.
- Hyvä hoitovaste saavutetaan noin 40–60 %:lla potilaista 15–20 mg:n viikkoannoksella 12 viikon hoidon aikana.
- Metotreksaattihoito vaikuttaa immuunivasteeseen.
- Metotreksaatti sopii pitkäaikaishoitoon, ja hoito voidaan tauottaa.
- Lääkityksen toteuttaminen vaatii poikkeuksellisen annostelunsa ja lääkitykseen liittyvien haittavaikutusten vuoksi erityistä huolellisuutta. Ks. «http://www.nrls.npsa.nhs.uk/resources/type/alerts/?entryid45=59800&q=0%C2%ACmethotrexate%C2%AC»13.
- Metotreksaatin hyötyosuus on parempi, kun sitä käytetään ihonalaisena pistoksena tai lihakseen annosteltuna «Metotreksaatin hyötyosuus on parempi ihon alle tai lihakseen annosteltuna.»A.
- Äkillisessä vakavassa infektiotilanteessa lääkitys tauotetaan «Anttila VJ, Haapamäki J, Peltomaa R ym. [Interrupt...»148.
- Vuosittaista kausi-influenssarokotusta suositellaan.
- Pneumokokkirokotusta suositellaan kaikille yli 65-vuotiaille. Muille ryhmille sitä suositellaan lääkärin harkinnan mukaan.
- Metotreksaattia ei tarvitse tauottaa ennen rokotuksia «https://www.reumatologinenyhdistys.fi/ohjeet/»12. Ks. ohjeet lasten osalta «https://www.reumatologinenyhdistys.fi/ohjeet/»12.
- Siklosporiini (taulukko «Siklosporiinilääkityksessä huomioon otettavia asioita ...»5):
- Siklosporiinia voidaan käyttää erityistapauksissa vaikeassa psoriaasissa, kun tarvitaan nopeaa vastetta tai muut ensisijaiset hoidot ovat sopimattomia.
- Läiskäpsoriaasissa siklosporiini on tehokas «Siklosporiini on tehokas hoito läiskäpsoriaasissa.»A.
- Hyvä hoitovaste voidaan saavuttaa 50–70 %:lla potilaista 3 mg/kg:n vuorokausiannoksella 8–16 viikon aikana.
- Siklosporiini heikentää immuunivastetta.
- Etenkin sellaisilla potilailla, joita on aiemmin hoidettu tabletti-PUVAlla, siklosporiini suurentaa ihon okasolusyövän riskiä «Siklosporiini näyttää lisäävän ihon okasolusyövän riskiä psoriaasipotilailla.»B.
- Pitkäaikaishoitoa (yli 2 vuotta) pyritään välttämään munuaishaittavaikutusten vuoksi «Ryan C, Amor KT, Menter A. The use of cyclosporine...»149, «Munuaishaittavaikutusten riskiä lisää yli 2 vuotta kestänyt hoito ja ≥ 5 mg/kg/vrk siklosporiiniannos.»A.
- Lääkitys voidaan tarvittaessa tauottaa.
- Äkillisissä infektioissa lääkitys tauotetaan.
- Ihopsoriaasi uusiutuu kaikkien systeemisten lääkkeiden käytön lopettamisen jälkeen yleensä parin kuukauden kuluessa «Koo J, Lebwohl M. Duration of remission of psorias...»150.
- Systeemisten lääkkeiden seurantakokeet luetellaan taulukoissa «Asitretiinilääkityksessä huomioon otettavia asioita ...»3, «Metotreksaattilääkityksessä huomioon otettavia asioita ...»4 ja «Siklosporiinilääkityksessä huomioon otettavia asioita ...»5.
- Systeemihoitoja, kuten asiteretiini- tai metotreksaattihoitoja, voidaan joskus poikkeuksellisesti tarvita lapsen psoriaasin hoidossa. Tarvittaessa hoito toteutetaan yhteistyössä lastenlääkärin kanssa.
| Aihe | Huomioon otettavia asioita |
|---|---|
| *Kaikkia mainittuja seurantakokeita ei välttämättä tarvitse ottaa jokaiselta potilaalta, vaan niiden laajuus arvioidaan yksilöllisesti. | |
| Annos | Aloitusannos 10–25 mg/vrk Annosta suurennetaan tarvittaessa 2–4 viikon välein enintään määrään 50 mg/vrk «Sbidian E, Maza A, Montaudié H ym. Efficacy and sa...»144, «Gollnick H, Bauer R, Brindley C ym. Acitretin vers...»145, «Berbis P, Geiger JM, Vaisse C ym. Benefit of progr...»151. |
| Haittavaikutukset | Sikiövauriot lääkityksen aikana ja 3 vuoden ajan käytön jälkeen Ihon ja limakalvojen kuivuminen Hiustenlähdön mahdollinen lisääntyminen Triglyseridien, kolesterolin ja maksan toimintakokeiden arvojen mahdollinen suureneminen «Gollnick H, Bauer R, Brindley C ym. Acitretin vers...»145, «Murray HE, Anhalt AW, Lessard R ym. A 12-month tre...»152, «Roenigk HH Jr, Callen JP, Guzzo CA ym. Effects of ...»153 Hyperostoosista ei ole näyttöä. |
| Yhteisvaikutukset | A-vitamiini ja sen johdokset, tetrasykliini, metotreksaatti ja fenytoiini |
| Vasta-aiheet | Raskaus ja imetys (ks. taulukko «Systeeminen lääkehoito raskauden ja imetyksen aikana iho- ja nivelpsoriaasia sairastavilla
...»22) Naisten, jotka saattavat tulla raskaaksi, ei tule käyttää alkoholia hoidon aikana eikä 2 kuukauteen hoidon päättymisestä, koska mahdollisesti muodostuva etretinaatti suurentaa sikiövaurion vaaraa. Maksan tai munuaisten vakava vajaatoiminta |
| Hyödyllinen yhdistelmä | UV-valohoidot «Asitretiinin ja UVB-valon yhdistelmähoito näyttää olevan tehokkaampi kuin pelkkä UVB-valohoito.»B |
| Seurantakokeet ennen hoitoa ja hoidon aikana* | Triglyseridit, ALAT (ja kolesteroli) ja kreatiniini ennen hoitoa, kuukauden kuluttua
hoidon alusta ja sen jälkeen 3–6 kuukauden välein Fertiili-ikäisillä raskauden sulkeminen pois ennen hoitoa Jos triglyseridiarvo on suurempi kuin 4 mmol/l tai ALAT-arvo suurempi kuin 2 x viitearvo, annosta on pienennettävä tai lääkitys lopetettava. Ks. myös «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 |
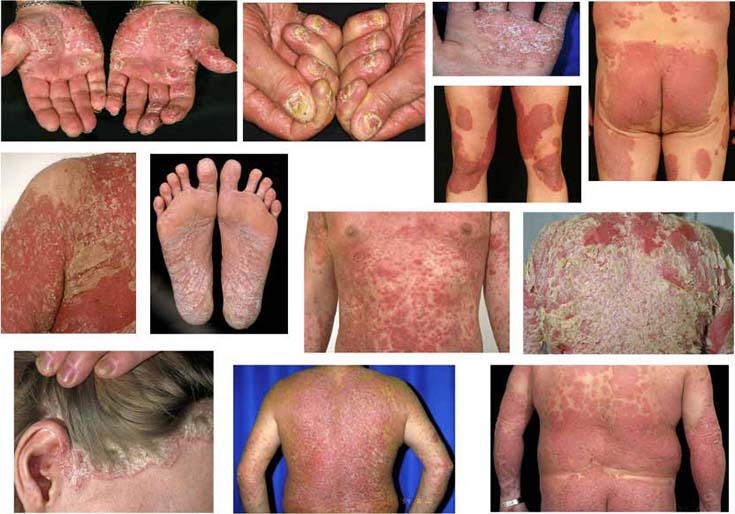
Esimerkkejä keskivaikeasta ja vaikeasta läiskäpsoriaasista ja erytrodermisestä psoriaasista sekä kämmen-, jalkapohja- ja hiuspohjan psoriaasista, joissa sisäinen lääkehoito saattaa olla aiheellinen.
© Raimo Suhonen
| Aihe | Huomioon otettavia asioita |
|---|---|
| *Kaikkia mainittuja seurantakokeita ei välttämättä tarvitse ottaa jokaiselta potilaalta, vaan niiden laajuus arvioidaan yksilöllisesti. | |
| Annos | Tabletteina tai ihonalaisesti 7,5–25 mg kerran viikossa. Aloitusannos on 10–15 mg suun kautta annosteltuna tai ihonalaisena pistoksena. Annosta
suurennetaan vasteen perusteella 2–4 viikon välein tarvittaessa 25 mg:aan saakka.
Jos lääke on tehoton suun kautta annosteltuna, siirrytään käyttämään ihonalaisia pistoksia. Ihonalainen annostelu vähentää maha-suolikanavan haittavaikutuksia ja saattaa parantaa tehoa. Vanhuksille käytetään varovaista annostusta. Lapsilla lääkitys aloitetaan yleensä suoraan ylläpitoannoksella. Lääkityksen toteuttaminen vaatii erityistä huolellisuutta poikkeuksellisen annostelun ja haittavaikutusten vuoksi. |
| Haittavaikutukset | Pahoinvointi ja ripuli Luuytimen heikentynyt toiminta (sytopenia)
|
| Stomatiitti Maksan rasvoittuminen, maksan toksiset soluvauriot ja fibroosi:
|
|
| Interstitiaalinen keuhkoreaktio Korkea ikä, hypoalbuminemia ja munuaisten toiminnan heikentyminen lisäävät haittavaikutuksia «Puig L. PASI90 response: the new standard in thera...»141, «Kent PD, Luthra HS, Michet C Jr. Risk factors for ...»158, «Alarcón GS, Kremer JM, Macaluso M ym. Risk factors...»159. |
|
| Yhteisvaikutukset | Trimetopriimi, probenesidi ja retinoidit Tulehduskipulääke ja protonipumpun estäjä tulisi ottaa eri aikaan vuorokaudesta kuin metotreksaatti (muuten käyttö sallittu). |
| Vasta-aiheet | Munuaisten, maksan tai luuytimen vajaatoiminta Merkittävä keuhkofibroosi ja merkittävästi heikentynyt keuhkojen toiminta Alkoholin liikakäyttö Raskaus ja imetys (ks. taulukko «Systeeminen lääkehoito raskauden ja imetyksen aikana iho- ja nivelpsoriaasia sairastavilla ...»22) |
| Hyödyllinen yhdistelmä | Foolihappolisä 5 mg viikossa tai 1 mg/vrk vähentää metotreksaatin aiheuttamaa maksatoksisuutta ja maha-suolikanavan oireita vähentämättä kuitenkaan lääkityksen tehoa «Foolihapposubstituutio 5 mg/vko tai 1 mg/vrk saattaa vähentää metotreksaatin aiheuttamaa maksatoksisuutta ja gastrointestinaalioireita vähentämättä kuitenkaan metotreksaatin tehoa.»C. |
| Seurantakokeet* | B-PVK+TKD, ALAT ennen hoitoa, sen jälkeen 3, 6 ja 12 viikon kohdalla ja sen jälkeen
3–6 kuukauden välein Krea 6 kuukauden välein Harkinnanvaraisesti annoksen suurentamisen yhteydessä. |
| Aikuisilla keuhkojen röntgenkuvaus ennen hoidon aloitusta, ellei sitä ole tehty edeltäneen vuoden aikana. | |
| Jos ALAT suurentunut > 2–2,5 x viitearvon ylärajan verran, tauotetaan metotreksaatti ja ALAT-seurantakoe aikuisilla 2 ja lapsilla 1 viikon kuluttua. Potilaan alkoholin ja muiden lääkkeiden käyttöön sekä painoindeksiin (rasvamaksan mahdollisuus) kiinnitettävä huomiota. Lääkityksen voi aloittaa uudelleen, kun ALAT on aikuisilla takaisin lähtöarvossa ja lapsilla < 75 U/l. | |
| Jos ALAT suurenee toistuvasti, on selvitettävä muut mahdolliset taustalla piilevät syyt. Lääke tulee tällöin tauottaa. | |
| Ks. myös «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 | |
| Suun ja hampaiden hyvästä terveydestä on huolehdittava koko lääkityksen ajan. | |
| Jos leukosyyttimäärä on alle 3,0 x 109/l tai trombosyyttimäärä alle 100 x 109/l, lääkeannosta pienennetään tai lääkitys tauotetaan. | |
| Aihe | Huomioon otettavia asioita |
|---|---|
| *Kaikkia mainittuja seurantakokeita ei välttämättä tarvitse ottaa jokaiselta potilaalta, vaan niiden laajuus arvioidaan yksilöllisesti. | |
| Annos | Aloitusannos on 2,5–5 mg/kg/vrk joko yhtäjaksoisena hoitona tai ihopsoriaasissa myös toistuvina alle 3 kuukauden kuureina. |
| Haittavaikutukset | Päänsärky, kohonnut verenpaine, munuaisten huonontunut toiminta: munuaishaittavaikutusten
riskiä suurentavat yli 2 vuotta kestänyt hoito ja yli 5 mg/kg:n vuorokausiannos «Munuaishaittavaikutusten riskiä lisää yli 2 vuotta kestänyt hoito ja ≥ 5 mg/kg/vrk siklosporiiniannos.»A. Ienhyperplasia Karvoituksen lisääntyminen Lihaskrampit ja vapina |
| Yhteisvaikutukset | Tavallisia, aina tarkistettava ennen uuden lääkityksen aloitusta |
| Vasta-aiheet | Syöpä 10 edellisen vuoden aikana (keratinosyytti-ihosyöpä 5 edellisen vuoden aikana),
epätasapainoinen verenpainetauti, munuaisten vajaatoiminta, immuunipuutostila, samanaikainen
UV-valohoito Lisäksi ks. taulukko «Systeeminen lääkehoito raskauden ja imetyksen aikana iho- ja nivelpsoriaasia sairastavilla ...»22 Raskaus ja imetys. |
| Hyödyllinen yhdistelmä | Hypomagnesemiassa magnesiumlisä 200–250 mg/vrk |
| Seurantakokeet* | Kreatiniini ja verenpaine ennen hoitoa, hoidon alettua 2 viikon välein 2 kuukauden
ajan ja sen jälkeen 2–3 kuukauden välein PVK+t, ALAT, AFOS, kolesteroli, triglyseridit, magnesium ja kalium 2–3 kuukauden kohdalla Seerumin kalium ja magnesium 6 kuukauden välein Jos kreatiniinipitoisuus suurenee yli 30 % lähtöarvosta, annosta on pienennettävä, ja jos suurenema on yli 50 %, lääkitys on lopetettava. Jos verenpaine kohoaa eikä annoksen pienentäminen auta, lääkkeen käyttö tauotetaan tai tarvittaessa aloitetaan verenpainelääkitys (ensisijaisesti kalsiumin salpaaja) «Griffiths CE, Dubertret L, Ellis CN ym. Ciclospori...»160. Raskauden aikana siklosporiinia voidaan käyttää vain, jos potilasta seurataan tiiviisti (verenpaineen nousun ja pre-eklampsian riski). Suun ja hampaiden hyvästä terveydestä on huolehdittava koko lääkityksen ajan. Ks. myös «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 |
Toissijaiset systeemiset lääkkeet
Peroraaliset lääkkeet
- Apremilasti (taulukko «Apremilastilääkityksessä huomioon otettavia asioita ...»6):
- Apremilastia voidaan käyttää vaikean psoriaasin hoidossa, kun ensisijaiset hoidot ovat olleet tehottomia, vasta-aiheisia tai sopimattomia.
- Hoidon korvattavuus vaatii erillisen svB-lausunnon.
- Läiskäpsoriaasin hoidossa apremilastilla on saavutettu hyvä hoitovaste vain 29–33
%:lla ja erinomainen hoitovaste 9–10 %:lla potilaista 16 viikon hoidolla «Apremilasti lienee turvallinen ja melko tehokas keskivaikean ja vaikean ihopsoriaasin induktiohoidossa.»B. Hyvä hoitovaste näyttää jatkuvan 102 viikon hoidon aikana noin puolella potilaista
«Reich K, Gooderham M, Bewley A ym. Safety and effi...»161.
- Apremilastin teho vaikuttaa jonkin verran huonommalta kuin metotreksaatin ja merkittävästi huonommalta kuin biologisten lääkkeiden teho.
- Ellei hoidossa ole saavutettu vähintään PASI-75-vastetta 16 viikon kohdalla, hoito tulee keskeyttää.
- 15–17 %:lla potilaista esiintyy hoidon alussa pahoinvointia tai ripulia.
- Apremilastihoitoon ei ole liittynyt infektioiden lisääntymistä, eikä sillä ole kuvattu elintoksisuutta. Hoidon aikana ei ole tarvetta laboratoriokoeseurannalle.
| Aihe | Huomioon otettavia asioita |
|---|---|
| Annos | Aloitusannos on ensimmäisten 6 päivän aikana:10 mg x 1, sen jälkeen 1. päivänä 10
mg x 2, 2. päivänä 10 mg + 20 mg, 3. päivänä 20 mg x 2, 4. päivänä 20 mg + 30 mg ja
5. päivänä 30 mg x 2. Ylläpitoannos on 30 mg p.o. kahdesti vuorokaudessa. |
| Haittavaikutukset | Pahoinvointi ja ripuli hoidon alkuviikkoina, > 5 %:n painon lasku |
| Yhteisvaikutukset | Voimakkaiden CYP3A4-entsyymin indusoijien (esim. rifampisiini, fenobarbitaali, karbamatsepiini, fenytoiini ja mäkikuisma) samanaikaista käyttöä apremilastin kanssa ei suositella. |
| Vasta-aiheet | Raskaudesta ja imetyksestä ks. taulukko «Systeeminen lääkehoito raskauden ja imetyksen aikana iho- ja nivelpsoriaasia sairastavilla ...»22. |
| Hyödyllinen yhdistelmä | Voidaan yhdistää metotreksaattiin, mutta nivelpsoriaasissa yhdistelmähoito ei ole lyhytaikaisessa hoidossa lisännyt hoitotehoa Yhdistelmähoitoa ei ole tutkittu ihopsoriaasissa. |
| Seulontatutkimukset ennen hoitoa | Valmisteyhteenvedon mukaan ei tarvita |
| Seurantakokeet | Ei erillistä turvakoeseurantaa |
| Hoidossa huomioitavaa | Vaikeassa munuaisten vajaatoiminnassa (GFR alle 30 ml/mim/1,73 m2) annos puolitetaan. Jos potilas on alipainoinen hoitoa aloitettaessa, hänen painoaan pitää tarkkailla säännöllisesti. Itsemurhariskin suurenemisen mahdollisuus on huomioitava ennen hoitoa ja sen aikana. Jos potilaalla ilmenee hoidon aikana ahdistus- tai masennusoireita tai ne pahenevat hoidon aikana, hoito tulee keskeyttää. |
- Dimetyylifumaraatti (taulukko «Dimetyylifumaraattilääkityksessä huomioon otettavia asioita...»7):
- Dimetyylifumaraattia voidaan käyttää vaikean psoriaasin hoidossa, kun ensisijaiset
hoidot ovat olleet tehottomia, vasta-aiheisia tai sopimattomia.
- Hoidon korvattavuus vaatii erillisen SvB-lausunnon.
- Hyvän hoitovasteen (PASI-75) saavutti lumekontrolloidussa 16 viikon tutkimuksessa vain 37,5 % potilaista (lume 15,3 %) «Dimethyl fumarate may increase the proportion of patients with moderate to severe psoriasis to achieve a clinically meaningful improvement at 16 weeks of tretament but the evidence is scarce. The number of adverse events may be higher than for placebo but the number of severe adverse events may be equal to placebo at 16 weeks of tretament.»D, erinomaisen vasteen (PASI-90) 18,4 % (lume 4,6 %) «Mrowietz U, Szepietowski JC, Loewe R ym. Efficacy ...»162.
- Pitkäaikaisista hoitotuloksista ei ole luotettavaa tutkimustietoa, mutta tehon oletetaan säilyvän hyvin lääkettä sietävillä potilailla.
- Dimetyylifumaraatti ei vaikuta nivelpsoriaasiin.
- Haittavaikutuksina esiintyy hyvin yleisesti ripulia ja muita maha-suolikanavan oireita sekä kasvojen ja vartalon punoitusta, yleisesti myös leuko- tai lymfopeniaa tai eosinofiliaa. Haittojen vuoksi lääkeannoksen nostoa saatetaan joutua rajoittamaan tai hoito keskeytyy.
- Harvinaisena haittana etenkin lymfopeenisillä potilailla on tavattu JC-viruksen aiheuttamaa multifokaalista leukoenkefalopatiaa.
- Dimetyylifumaraattia voidaan käyttää vaikean psoriaasin hoidossa, kun ensisijaiset
hoidot ovat olleet tehottomia, vasta-aiheisia tai sopimattomia.
| Aihe | Huomioon otettavia asioita |
|---|---|
| Annos | Ensimmäisen viikon aikana otetaan dimetyylifumaraattia 30 mg kerran päivässä (1 tabletti
iltaisin). Toisen viikon aikana otetaan dimetyylifumaraattia 30 mg kahdesti päivässä
(1 tabletti aamulla ja 1 tabletti illalla). Kolmannella viikolla otetaan dimetyylifumaraattia
30 mg kolmesti päivässä (1 tabletti aamulla, 1 tabletti keskipäivällä ja 1 tabletti
illalla). Neljännestä viikosta eteenpäin siirrytään yhteen iltaisin otettavaan dimetyylifumaraatti
120 mg -tablettiin. Tämän jälkeen annosta suurennetaan sietokyvyn mukaan yhdellä eri
aikaan päivästä otettavalla dimetyylifumaraatti 120 mg -tabletilla viikossa seuraavien
viiden viikon ajan. Suurin sallittu vuorokausiannos on 720 mg (3 x 2 dimetyylifumaraatti 120 mg -tablettia). Iho-oireiden parannuttua voidaan annosta pyrkiä asteittain alentamaan. |
| Haittavaikutukset | Tavalliset: kasvojen ja vartalon ihon punoitus, maha-suolikanavan oireet (ripuli, turvotus, pahoinvointi ym.), leuko- tai lymfopenia, eosinofilia |
| Hyödyllinen yhdistelmä | |
| Seulontatutkimukset ennen hoitoa | Latentin tuberkuloosin tutkiminen (ks. Reumatologisen yhdistyksen sivustot «https://www.reumatologinenyhdistys.fi/app/uploads/2019/11/LTBI-ohje-SRY-p%C3%A4ivitys_15.11.2019.pdf»14) Hammaslääkärin tarkastus mahdollisten infektiopesäkkeiden toteamiseksi (harkinnan mukaan esim. ortopantomografia) TVK (hoitoa ei saa aloittaa, jos B-Leuk alle 3,0 tai B-Lymf alle 1,0 x 109 ) ALAT, AFOS, kreatiniini HIV- ja hepatiittivasta-aineet (HBsAg, HBcAb, tarvittaessa HBcAbM, HCVAb) harkinnan mukaan Lasko, CRP, U-seula Tuma-vasta-aineet harkinnan mukaan |
| Seurantakokeet hoidon aikana | TVK vähintään 3 kuukauden välein (ks. tarkemmat ohjeet valmisteyhteenvedosta) ALAT, AFOS, kreatiniini 3 kuukauden kuluttua ja sen jälkeen yksilöllisesti esimerkiksi 3–12 kuukauden välein. |
Biologiset lääkkeet
- Vaikutuskohteen mukaan voidaan jakaa viiteen ryhmään:
- tuumorinekroositekijä-alfan estäjiin (TNF:n estäjät)
- interleukiini (IL) -12/23:n estäjiin
- IL-17:n estäjiin
- IL-23:n estäjiin
- T-solujen estäjiin.
- Biologisten lääkkeiden tutkimusohjelmat on tehty pääosin vaikeaa psoriaasia sairastavilla (sisäänottokriteeri PASI > 12, keskimäärin PASI 18–20), joten tulosten soveltuvuus lievempää psoriaasia sairastaviin on epäselvää.
Yleisohjeet biologisten lääkkeiden käytöstä iho- ja nivelpsoriaasin hoidossa
- Ennen biologisen lääkkeen aloitusta tulee sulkea pois tietyt tilat ja sairaudet (ks. alempaa tässä kappaleessa lista hoidon vasta-aiheista).
- Hoidon aloittaa ja sitä valvoo ihotautien tai reumatologian erikoislääkäri.
- Erityiskorvausoikeus edellyttää erillistä SvB-lausuntoa vaikeasta psoriaasista tai nivelpsoriaasista, jonka hoidossa ensisijaisilla systeemisillä hoidoilla ei ole saavutettu tyydyttävää vastetta tai niitä ei voida käyttää.
- Lääkkeen valintaa tehtäessä, potilaan kanssa tulee keskustella tekijöistä, jotka saattavat vaikuttaa hoitoon sitoutumiseen. Tällaisia ovat muun muassa teho, turvallisuus, hoitoprosessiin liittyvät asiat ja kustannukset.
- Ihopsoriaasin hoidon tavoiteasettelun, hoitotehon seurannan ja muutosten perustelun pohjaksi suositellaan modifioitua eurooppalaisen konsensusryhmän algoritmia, joka on päivitetty vastaamaan uusimpien lääkehoitojen tuloksia. Ks. biologisen hoidon tavoitelähtöinen hoitostrategia kuva «Biologisen hoidon tavoitelähtöinen ihopsoriaasin hoitostrategia»48, «Mrowietz U, Kragballe K, Reich K ym. Definition of...»163.
- Biologisille psoriaasilääkkeille aloittamisen yhteisiä vasta-aiheita ovat
- raskaus (suhteellinen) sertolitsumabipegolia lukuun ottamatta
- imetys (suhteellinen)
- aktiiviset merkittävät infektiot (hammasinfektiot mukaan luettuina) «Anttila VJ, Haapamäki J, Peltomaa R ym. [Interrupt...»148
- demyelinisoiva sairaus (koskee TNF:n estäjiä)
- aktiivinen pahanlaatuinen tauti «Anttila VJ, Haapamäki J, Peltomaa R ym. [Interrupt...»148
- suhteellinen vasta-aihe: hoidettu syöpä
- ei koske tyvisolusyöpää eikä hyväennusteista okasolusyöpää (läpimitaltaan alle 1 cm:n kokoinen ja hyvin erilaistunut)
- sydämen vajaatoiminta (NYHA III–IV) (koskee TNF:n estäjiä)
- yliherkkyys valmisteen ainesosille.
- Latentin tuberkuloosin mahdollisuus on suljettava pois (latentin tuberkuloosin aktivoituminen tuberkuloosiksi reumataudin hoidon aikana «https://www.reumatologinenyhdistys.fi/app/uploads/2019/11/LTBI-ohje-SRY-p%C3%A4ivitys_15.11.2019.pdf»14).
- Tarvittaessa harkinnan mukaan lääkitys aloitetaan tuberkuloosin estolääkityksen suojassa infektio- tai keuhkolääkärin arvion jälkeen.
- Muiden kroonisten infektioiden osalta toimitaan harkinnan mukaan (ks. tarkemmin lääkekohtaiset taulukot).
- Hoitoa saavien potilaiden on otettava yhteyttä hoidosta vastaavaan yksikköön tai erillisiin
rokotuskeskuksiin paikallisen kapasiteetin mukaan
- infektiotilanteissa
- Akuutin vaikean infektion ajaksi hoito tauotetaan.
- Ks. myös «https://www.reumatologinenyhdistys.fi/ohjeet/»12
- rokotuksia (yleensä tai matkailua varten) suunniteltaessa
- Ks. Reumatologisen yhdistyksen ohjeet «https://www.reumatologinenyhdistys.fi/ohjeet/»12, Kansanterveyslaitoksen rokotuskäsikirja «https://www.thl.fi/fi/web/rokottaminen»15 ja Reumatalon ohjeet «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumapotilaiden-rokotukset»16
- Kiellettyjä ovat elävät rokotteet (esim. tuhkarokko, sikotauti, vihurirokko, vesirokko, keltakuume, suun kautta otettavat lavantauti- ja poliorokotteet). Ks. erikseen rokotusohje lapsille Reumatologisen yhdistyksen sivuilta «https://www.reumatologinenyhdistys.fi/ohjeet/»12.
- Inaktivoidut rokotteet ovat sallittuja.
- Normaalissa rokotusohjelmassa olevien rokotusten voimassaolon tarkistusta ja puuttuvien rokotusten antamista suositellaan ennen hoitojen aloitusta (mm. jäykkäkouristus- ja kurkkumätärokotukset).
- Pneumokokkirokotusta suositellaan kaikille yli 65-vuotiaille ja hoitavan lääkärin harkinnan mukaan mahdollisesti myös muille.
- Vuosittaista influenssarokotetta suositellaan.
- kirurgisia toimenpiteitä suunniteltaessa
- Mahdollisuuksien mukaan leikkaus pyritään ajoittamaan ajankohtaan, jolloin seuraava lääkeannos annettaisiin.
- Tauon pituus vaihtelee lääkeaineen mukaan ja on tarkastettava tilannekohtaisesti «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/reumal%C3%A4%C3%A4kkeet-ja-leikkaus»17. Lääkityksen voi yleensä aloittaa, kun ompeleet on poistettu ja haava on siisti.
- raskautta suunniteltaessa. Ks. taulukko «Systeeminen lääkehoito raskauden ja imetyksen aikana iho- ja nivelpsoriaasia sairastavilla ...»22, «Anttila VJ, Haapamäki J, Peltomaa R ym. [Interrupt...»148, «Götestam Skorpen C, Hoeltzenbein M, Tincani A ym. ...»164.
- infektiotilanteissa
- Hoitovaste arvioidaan ensimmäisen kerran 12–16 viikon hoidon jälkeen ja lääkkeittäin
viimeistään 24 viikon kohdalla.
- Ellei riittävää vastetta ole saavutettu, hoidon tehostamista on harkittava (kuva «Biologisen hoidon tavoitelähtöinen ihopsoriaasin hoitostrategia»48).
- Mainitut biologiset hoidot voidaan vaihtaa toiseen ilman erityisiä taukoja.
- Suositukset lääkityksen seurannasta esitetään taulukossa «Biologisessa lääkehoidossa huomioon otettavia asioita ...»8 Biologisessa lääkehoidossa huomioon otettavia asioita.
- Yhdistelmähoitoja ei ole riittävästi tutkittu ihopsoriaasissa.
- Metotreksaatin yhdistäminen TNF:n estäjiin on tavallista nivelpsoriaasissa ja muissa reumataudeissa. Osalle potilaista kehittyy neutraloivia vasta-aineita erityisesti infliksimabia, adalimumabia ja golimumabia kohtaan, joten niiden yhdistäminen metotreksaattiin voi tässä mielessä olla hyödyllistä «Lecluse LL, Driessen RJ, Spuls PI ym. Extent and c...»165, «Hoffmann JH, Hartmann M, Enk AH ym. Autoantibodies...»166, «Kimball AB, Gordon KB, Fakharzadeh S ym. Long-term...»167. Vasta-aineet johtavat lääkepitoisuuksien pienenemiseen ja usein hoitotehon heikkenemiseen mutteivät haittoihin (lukuun ottamatta infuusioreaktioita infliksimabihoidossa) «Hsu L, Snodgrass BT, Armstrong AW. Antidrug antibo...»168.
- IL-17:n ja IL-23:n estäjien oheen ei suositella metotreksaattia.
| *Kaikkia mainittuja seurantakokeita ei välttämättä tarvitse ottaa jokaiselta potilaalta, vaan niiden tarve ja laajuus arvioidaan yksilöllisesti. IL17:n ja IL23:n estäjähoidon aikana ei tarvita lääkehoidon seurantakokeita. | |
| Seulontakokeet ennen hoitoa | TVK, ALAT, kreatiniini, lasko, CRP, U-seula Latentin tuberkuloosin tutkiminen: thorax-röntgen, Tb-INFg/IGRA testi HIV- ja hepatiittivasta-aineet (HbsAg, HBcAb, tarvittaessa HBcAbM, HCVAb) Tuma-vasta-aineet harkinnan mukaan Hammaslääkärin tarkastus mahdollisten infektiopesäkkeiden toteamiseksi (harkinnan mukaan ortopantomografia) Rokotusten tarkistaminen |
| Seurantakokeet hoidon aikana* | TVK, ALAT ja kreatiniini kuukauden kuluttua aloituksesta ja sen jälkeen yksilöllisesti esimerkiksi 3–12 kuukauden välein |
| Hoitovasteen seurantakokeet | Nivelpsoriaasia hoidettaessa CRP ja lasko lääkärinvastaanoton yhteydessä tai harkinnan mukaan |
Biologisten lääkkeiden käyttö ihopsoriaasissa
- Käyttöaiheet:
- vaikea läiskäpsoriaasi (PASI, BSA tai DLQI on suurempi kuin 10) aikuisilla, joilla ei ole ilmaantunut vastetta ensisijaisiin systeemisiin hoitoihin ja UV-valohoitoihin tai joille nämä hoidot ovat vasta-aiheisia tai sopimattomia (mukaan luettuna metotreksaatti tai siklosporiini yleisesti käytetyillä hoitoannoksilla)
- Erityisiä käyttöaiheita ovat
- vaikea ja vaikeahoitoinen erytroderminen tai pustuloiva psoriaasi
- erityisalueiden (esim. kämmenet ja jalkapohjat) psoriaasi, joka uhkaa johtaa tai on johtanut työkyvyttömyyteen tai elämänlaadun huomattavaan heikkenemiseen.
- Lasten psoriaasin hoidossa käytetään adalimumabia, etanerseptiä ja ustekinumabia (taulukko
«Lasten ihopsoriaasin hoitoon käytettäviä biologisia lääkkeitä ...»9).
- Etanersepti ja ustekinumabi saattavat olla tehokkaita lasten psoriaasin hoidossa «Etanersepti ja ustekinumabi saattavat olla tehokkaita lasten ihopsoriaasin hoidossa.»C.
- Biologisen lääkehoidon aloituksen yhteydessä annetaan huolellinen ohjaus (ks. «Biologisen pistoslääkkeen hoidon ohjaus»10) ja käydään läpi Biologisen lääkehoidon alkukartoitus -lomake «hoi50062e.pdf»4. Ks. myös Taulukko «Biologisessa lääkehoidossa huomioon otettavia asioita ...»8 Biologisessa lääkehoidossa huomioon otettavia asioita.
- Myyntiluvan saaneet biosimilaarit vastaavat teholtaan ja turvallisuudeltaan viitevalmisteita. Ks. Fimean ohjeisto «http://www.fimea.fi/laaketurvallisuus_ja_tieto/biosimilaarit/fimean-kanta-biosimilaarien-vaihtokelpoisuuteen»18.
| Lääke | Ikäraja | Annostus |
|---|---|---|
| adalimumabi | ≥ 4-vuotiaille | 0,8 mg/kg (enintään 40 mg) s.c. kerran viikossa 2 annosta ja sen jälkeen 2 viikon välein |
| etanersepti | ≥ 6-vuotiaille | 0,8 mg/kg (enintään 50 mg) s.c. kerran viikossa |
| ustekinumabi | ≥ 6-vuotiaille | < 60 kg painaville 0,75 mg/kg, 60–100 kg painaville 45 mg ja > 100 kg painaville 90 mg s.c. viikolla 0, 4 ja sen jälkeen 12 viikon välein |
Psoriaasin biologisiin hoitoihin liittyviä haittoja
- Infektioriskin suureneminen:
- Infektioriski liittyy kaikkiin biologisiin lääkkeisiin, erityisesti TNF:n estäjiin.
Nivelpsoriaasin tapauksessa varsinaisten reumalääkkeiden ja kortikosteroidin vaikutus
tulee ottaa huomioon «Germano V, Cattaruzza MS, Osborn J ym. Infection r...»169.
- Kuume voi puuttua, ja oireet voivat olla tavallista lievempiä.
- On osoitettu, että vakavien infektioiden riski on TNF:n estäjähoidossa nivelreumapotilailla
noin 20 % suurempi kuin perinteisiä synteettisiä reumalääkkeitä käyttävillä potilailla
«Galloway JB, Hyrich KL, Mercer LK ym. Anti-TNF the...»170. Tulos ei ole kuitenkaan ole suoraan sovellettavissa psoriaasin hoitoon «García-Doval I, Hernández MV, Vanaclocha F ym. Sho...»171.
- Lyhytkestoisten satunnaistettujen lumekontrolloitujen tutkimusten meta-analyysi ei osoita suurentunutta riskiä «Yiu ZZN, Exton LS, Jabbar-Lopez Z ym. Risk of Seri...»172, mutta osassa pitkäaikaisia rekisteritutkimuksia se on osoitettu etenkin infliksimabin ja adalimumabin osalta «Yiu ZZN, Exton LS, Jabbar-Lopez Z ym. Risk of Seri...»172, «Dávila-Seijo P, Dauden E, Descalzo MA ym. Infectio...»173, «Garcia-Doval I, Cohen AD, Cazzaniga S ym. Risk of ...»174, «Reich K, Mrowietz U, Radtke MA ym. Drug safety of ...»175, «Gniadecki R, Bang B, Bryld LE ym. Comparison of lo...»176
- Ustekinumabilla vakavien infektioiden riski on pienempi kuin TNF:n estäjillä «Papp K, Gottlieb AB, Naldi L ym. Safety Surveillan...»177.
- IL-23:n estäjiin ei ole kuvattu liittyvän suurentunutta vakavien infektioiden riskiä «Crowley JJ, Warren RB, Cather JC. Safety of select...»178.
- IL-17:n estäjiin liittyy suurentunut limakalvojen hiivainfektion riski, mahdollisesti suurentunut virtsatieinfektioriski naisilla «Sahuquillo-Torralba A, Carretero G, Rivera R ym. T...»179 ja valmisteittain vaihtelevasti suurentunut inflammatorisen suolistosairauden pahenemisen tai ilmaantumisen riski.
- Infektioriski liittyy kaikkiin biologisiin lääkkeisiin, erityisesti TNF:n estäjiin.
Nivelpsoriaasin tapauksessa varsinaisten reumalääkkeiden ja kortikosteroidin vaikutus
tulee ottaa huomioon «Germano V, Cattaruzza MS, Osborn J ym. Infection r...»169.
- Latentin tuberkuloosin aktivoituminen TNF:n estäjillä ilmaantuu tavallisesti ensimmäisen
puolen vuoden aikana.
- Kun käytetään asianmukaista seulontaa, riski on pieni.
- Ihon tyvi- ja okasolusyövät:
- TNF:n estäjillä riski on mahdollisesti hieman suurentunut «Mariette X, Matucci-Cerinic M, Pavelka K ym. Malig...»180, «van Lümig PP, Driessen RJ, Berends MA ym. Safety o...»181, «Raaschou P, Simard JF, Asker Hagelberg C ym. Rheum...»182. Riskiä voivat suurentaa myös runsas UV-altistus ja muut aiemmat immunosuppressiiviset hoidot.
- Muut syövät:
- Vaikeaan psoriaasiin liittyy lievästi suurentunut lymfoomariski «Vaikeaan psoriaasiin näyttää liittyvän lievästi kohonnut lymfoomariski.»B. TNF:n estäjähoito saattaa hieman suurentaa riskiä, mutta varmaa tutkimusnäyttöä asiasta ei ole «Mariette X, Matucci-Cerinic M, Pavelka K ym. Malig...»180, «van Lümig PP, Driessen RJ, Berends MA ym. Safety o...»181.
- Melanoomariski saattaa hieman suurentua TNF:n estäjähoidossa «Raaschou P, Simard JF, Holmqvist M ym. Rheumatoid ...»183, «Nyboe Andersen N, Pasternak B, Basit S ym. Associa...»184.
- Kiinteiden kasvainten esiintyvyys ei ole lisääntynyt.
Lääkevalmisteet
- Ihopsoriaasissa käytettyjen biologisten lääkkeiden vertailu on taulukoissa «Ihopsoriaasin biologisten lääkkeiden vertailu: TNF:n estäjät ja ustekinumabi ...»13 ja «Ihopsoriaasin biologisten lääkkeiden vertailu: IL-17:n ja IL-23:n estäjät ...»14.
- Adalimumabi (taulukko «TNF:n estäjähoidon toteutus ja haittavaikutukset ...»10):
- Adalimumabi on tehokas lääke läiskäpsoriaasin induktiohoidossa aikuisilla.
- Hyvän hoitovasteen saavutti kliinisissä lääketutkimuksissa 12–16 viikon hoidossa 53–80 % vaikeaa läiskäpsoriaasia sairastavista, joskin klinikka-aineistoissa on kuvattu myös heikompia vasteita «Adalimumabilla saavutetaan hyvä hoitoteho läiskäpsoriaasin induktiohoidossa lumehoitoon verrattuna.»A.
- Erinomaisen (PASI-90) hoitovasteen 16 viikon hoidossa saavutti 45–50 % ja täydellisen (PASI-100) vasteen 17–24 % potilaista «Adalimumabilla saavutetaan hyvä hoitoteho läiskäpsoriaasin induktiohoidossa lumehoitoon verrattuna.»A.
- Lääke tehoaa useimmiten myös muille TNF:n estäjille resistentteihin tapauksiin «Papoutsaki M, Chimenti MS, Costanzo A ym. Adalimum...»185, «Van Lümig PP, Lecluse LL, Driessen RJ ym. Switchin...»186, «Woolf RT, Smith CH, Robertson K ym. Switching to a...»187, «Strober BE, Poulin Y, Kerdel FA ym. Switching to a...»188, «Ortonne JP, Chimenti S, Reich K ym. Efficacy and s...»189.
- Hoidon lopetus tai tauotus ei johda ihopsoriaasin nopeaan pahenemiseen, joten hoito
voidaan tarvittaessa tauottaa.
- Hoidon päätyttyä tauti uusiutuu hitaasti usean kuukauden aikana «Papp K, Crowley J, Ortonne JP ym. Adalimumab for m...»190.
- Hoidon uudelleenaloitus lyhyen tauon jälkeen tehoaa aikaisempaan tapaan noin 70 %:ssa tapauksista, mutta jos relapsi on edennyt pitkälle, hoitoteho saattaa jäädä heikommaksi «Papp K, Crowley J, Ortonne JP ym. Adalimumab for m...»190.
- Hoidon tauotus on kuitenkin lääkkeeseen kohdistuvien vasta-aineiden muodostuksen riskitekijä «Chiu HY, Wang TS, Chan CC ym. Risk Factor Analysis...»191.
- Pitkäaikaishoidossa hoitovaste säilyy kohtalaisen hyvin «Adalimumabilla 16 viikon induktiohoidossa saavutettu hoitovaste säilyy kohtalaisen hyvin pitkäaikaishoidossa, mutta osa potilaista tarvitsee ajoittain hoitoannoksen nostoa tai annosvälin tihentämistä tai yhdistelmähoitoa.»B, mutta osa potilaista saattaa tarvita tilapäistä annosnostoa tai lisäksi muuta hoitoa
(taulukko «Ihopsoriaasin biologisten lääkkeiden vertailu: TNF:n estäjät ja ustekinumabi ...»13 Ihopsoriaasin biologisten lääkkeiden vertailu).
- Hoitotehon menetyksen tärkein syy on adalimumabiin kohdistuvien neutraloivien vasta-aineiden muodostus, jota voidaan estää tai vähentää käyttämällä lisäksi metotreksaattia «Hsu L, Snodgrass BT, Armstrong AW. Antidrug antibo...»168.
- Adalimumabihoitoon voidaan yhdistää muita hoitoja, mutta tutkimustietoa aiheesta on metotreksaattia lukuun ottamatta toistaiseksi julkaistu vain vähän «Thaçi D, Ortonne JP, Chimenti S ym. A phase IIIb, ...»192, «Bagel J. Adalimumab plus narrowband ultraviolet B ...»193, «Wolf P, Hofer A, Weger W ym. 311 nm ultraviolet B-...»194, «Heiberg MS, Koldingsnes W, Mikkelsen K ym. The com...»195.
- Adalimumabi on tehokas lääke läiskäpsoriaasin induktiohoidossa aikuisilla.
| Lääke* | Tyypillinen annos ihopsoriaasissa | Tyypillinen annos nivelpsoriaasissa | Haitat |
|---|---|---|---|
| *Metotreksaatti on kaikkien TNF:n estäjähoitojen kanssa hyödyllinen yhdistelmä. (1) Infliksimabista on olemassa myös s.c. annosteltava valmiste. Sen tehoa psoriaasin ja nivelpsoriaasin hoidossa ei ole osoitettu suorissa tutkimuksissa. S.c. valmisteen yhdenvertaisuus i.v. valmisteen kanssa annoksella 120 mg kahden viikon välein on osoitettu tulehduksellista suolistotautia sairastavilla (farmakokinetiikka) ja reumaa sairastavilla (kliininen teho) kahdessa RCT-tutkimuksessa «Schreiber S, Ben-Horin S, Leszczyszyn J ym. Random...»196, «Westhovens R, Wiland P, Zawadzki M ym. Efficacy, p...»197. |
|||
| Adalimumabi | Aloitusannos 80 mg, minkä jälkeen 40 mg joka toinen viikko. Hoitovaikutuksen heikennettyä voidaan nostaa tasolle 80 mg joka toinen viikko | 40 mg joka toinen viikko s.c | Pistoskohtien lievät ihoreaktiot, lisääntynyt infektioalttius ja leukopenia |
| Etanersepti | 50 mg kahdesti viikossa 3 kuukauden ajan ja sen jälkeen 50 mg kerran viikossa | 50 mg kerran viikossa s.c | Pistoskohtien lievät ihoreaktiot, lisääntynyt infektioalttius ja leukopenia |
| Golimumabi | - | 50 mg kerran kuukaudessa s.c. Yli 100 kg painaville 100 mg kerran kuukaudessa | Pistoskohtien lievät ihoreaktiot, lisääntynyt infektioalttius |
| Infliksimabi (1) | 5 mg/kg viikoilla 0, 2 ja 6, minkä jälkeen 8 viikon välein i.v. Kliinisen tilanteen mukaan infuusioväliä ja -annosta voidaan muuttaa | 3–5 mg/kg viikoilla 0, 2 ja 6, minkä jälkeen 8 viikon välein i.v. Kliinisen tilanteen mukaan infuusioväliä ja -annosta voidaan muuttaa | Infuusioreaktiot, anafylaksia, lisääntynyt infektioalttius ja mahdollinen maksaentsyymiarvojen suureneminen |
| Sertolitsumabi | Aloitusannos 400 mg (2 injektiota) s.c. viikoilla 0, 2 ja 4, minkä jälkeen 200 mg kahden viikon välein. | Kuten ihopsoriaasissa | Pistoskohtien lievät ihoreaktiot, lisääntynyt infektioalttius |
- Bimekitsumabi (taulukko «IL-17:n estäjähoidon toteutus ja haittavaikutukset ...»11):
- Bimekitsumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Subcutaneous bimekizumab treatment at the dose of 320 mg monthly increases the proportion of patients with plaque psoriasis achieving the PASI90 and IGA 0/1 responses at week 16 when compared to placebo (PASI90 approximately 85–91 % vs. 1–5 % and IGA 0/1 84–93 % vs.»A.
- Hyvän hoitovasteen (PASI-75) saavutti kahdessa 16 viikon lumekontrolloidussa «Gordon KB, Foley P, Krueger JG ym. Bimekizumab eff...»198, «Reich K, Papp KA, Blauvelt A ym. Bimekizumab versu...»199 ja kahdessa 16 viikon aktiivisella vertailuvalmisteella kontrolloidussa tutkimuksessa «Reich K, Warren RB, Lebwohl M ym. Bimekizumab vers...»200, «Warren RB, Blauvelt A, Bagel J ym. Bimekizumab ver...»201 92–95 % (lume 2,3–7,2 %) potilaista, erinomaisen (PASI-90) 85–91 % (lume 1–5 %) ja täydellisen (PASI-100) vasteen 59–68 % (lume 0–1 %) potilaista.
- Hoitovaste näyttää säilyvän hyvin 48–56 viikkoon ulottuneessa jatkohoidossa annoksella
320 mg 8 viikon välein.
- PASI-90- ja PASI-100-vasteet olivat 82–86 % ja 66–70 % «Reich K, Warren RB, Lebwohl M ym. Bimekizumab vers...»200, «Warren RB, Blauvelt A, Bagel J ym. Bimekizumab ver...»201.
- Hoidon lopetus tai tauotus ei johda ihopsoriaasin nopeaan pahenemiseen, joten hoito
voidaan myös tarvittaessa tauottaa «Gordon KB, Foley P, Krueger JG ym. Bimekizumab eff...»198.
- Tauti uusiutuu kliinisten tutkimusten mukaan noin 8 kuukauden kuluttua hoidon lopettamisesta.
- Hoidon uudelleenaloitus tauon jälkeen tehoaa noin 88 %:lla potilaista.
- Valmisteyhteenvedon mukaan noin 45 %:lle potilaista on kuvattu kehittyvän lääkevasta-aineita, joista kolmasosa on neutraloivia, mutta niillä ei ole todettu olevan vaikutusta hoitotuloksiin eikä yhteyttä haittatapahtumiin.
- Bimekitsumabi vaikuttaa 60 viikon seurannan perusteella turvalliselta «Blauvelt A, Papp KA, Merola JF ym. Bimekizumab for...»202.
- Tavallisimpia haittoja ovat lisääntyneet ylähengitystieinfektiot sekä IL-17:n estäjille tyypillinen suurentunut suun ja nielun kandidainfektion riski sekä silsainfektion riski.
- Vasta-aiheena pidetään kliinisesti merkittävää aktiivista infektiota ja yliherkkyyttä vaikuttavalle aineelle. Bimekitsumabia ei suositella potilaille, joilla on tulehduksellinen suolistosairaus. Jos potilaalle kehittyy tulehduksellisen suolistosairauden oireita ja löydöksiä tai hänen jo ennestään sairastamansa tulehduksellinen suolistosairaus pahenee, tulee lopettaa bimekitsumabihoito ja aloittaa asianmukainen hoito.
- Bimekitsumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Subcutaneous bimekizumab treatment at the dose of 320 mg monthly increases the proportion of patients with plaque psoriasis achieving the PASI90 and IGA 0/1 responses at week 16 when compared to placebo (PASI90 approximately 85–91 % vs. 1–5 % and IGA 0/1 84–93 % vs.»A.
- Brodalumabi (taulukko «IL-17:n estäjähoidon toteutus ja haittavaikutukset ...»11):
- Brodalumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Brodalumab at dose of 210 mg, when compared to placebo, increases the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment. The safety profile of brodalumad may be equal to placebo after 12 weeks treatment.»B.
- Hyvän hoitovasteen (PASI-75) saavutti kolmessa 12 viikon lumekontrolloidussa tutkimuksessa 83–86 % (lume 2,7–8 %) potilaista, erinomaisen (PASI-90) 70–73,3 % (lume 0,1–3,2 %) ja täydellisen (PASI-100) vasteen 37–44 % (lume 0,3–1 %) potilaista «Papp KA, Reich K, Paul C ym. A prospective phase I...»203, «Lebwohl M, Strober B, Menter A ym. Phase 3 Studies...»204.
- Hoitoteho näyttää säilyvän hyvin 52 viikkoon ulottuneessa jatkohoidossa.
- Myyntiluvan mukaista 210 mg:n annosta koko ajan saaneiden PASI-75-/PASI-90-/PASI-100-vasteet olivat 80 %/73–75 %/53–56 % «Lebwohl M, Strober B, Menter A ym. Phase 3 Studies...»204.
- Vasta-aineita todettiin 1,8–2,3 %:lla potilaista, mutta niillä ei ollut vaikutusta hoitotuloksiin eikä yhteyttä haittatapahtumiin.
- Brodalumabi vaikuttaa 52 viikon tutkimusten perusteella turvalliselta. Tavallisia haittoja ovat lisääntyneet ylähengitystieinfektiot sekä IL-17:n estäjille tyypillinen suurentunut hiiva- ja silsainfektioriski. Crohnin tautia pidetään vasta-aiheena. Yhdysvalloissa lääkkeen käyttöön liittyy varoitus mahdollisesti suurentuneesta itsemurha-alttiudesta ja siihen liittyvä seuranta, mutta Euroopan lääkevirasto ei tällaista esitä. Jos potilaalla ilmenee hoidon aikana ahdistus- tai masennusoireita tai ne pahenevat hoidon aikana, hoito tulee keskeyttää.
- Brodalumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Brodalumab at dose of 210 mg, when compared to placebo, increases the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment. The safety profile of brodalumad may be equal to placebo after 12 weeks treatment.»B.
| Lääke | Annos ihopsoriaasissa | Annos nivelpsoriaasissa | Haitat |
|---|---|---|---|
| Bimekitsumabi | 320 mg 4 viikon välein viikolle 16 saakka, minkä jälkeen joka 8. viikko. | 160 mg joka 4. viikko. Jos on samanaikainen keskivaikea tai vaikea läiskäpsoriaasi, suositeltu annos on sama kuin läiskäpsoriaasin hoidossa. 16 viikon jälkeen joka 8. viikko tai jos riittävää hoitovastetta ei pystytä ylläpitämään, voidaan harkita siirtymistä annokseen 160 mg joka 4. viikko. | Ylähengitystieinfektiot Hiiva- ja silsainfektiot Inflammatorisen suolistosairauden pahenemisen tai ilmaantumisen riski |
| Brodalumabi | 210 mg viikoilla 0, 1 ja 2 ja sen jälkeen joka toinen viikko | - | Pistoskohtien lievät ihoreaktiot Ylähengitystieinfektiot Hiiva- ja silsainfektiot Leukopenia |
| Iksekitsumabi | Aloitusannos 160 mg, minkä jälkeen 80 mg kahden viikon välein viikolle 12 saakka, minkä jälkeen 80 mg 4 viikon välein | Sama kuin ihopsoriaasissa | Pistoskohtien lievät ihoreaktiot Ylähengitystieinfektiot Hiiva- ja silsainfektiot |
| Sekukinumabi | 300 mg viikoilla 0, 1, 2, 3 ja 4, minkä jälkeen 300 mg kerran kuukaudessa | Sama annostus kuin ihopsoriaasissa, jos nivelpsoriaasiin liittyy vaikea ihopsoriaasi tai jos TNF:n estäjillä ei ole saavutettu riittävää hoitovastetta. Muissa tapauksissa sama hoitokaavio 150 mg:n kerta-annoksin. | Ylähengitystieinfektiot Hiiva- ja silsainfektiot |
- Etanersepti (taulukko «TNF:n estäjähoidon toteutus ja haittavaikutukset ...»10):
- Etanersepti on tehokas lääke läiskäpsoriaasin induktiohoidossa aikuisilla.
- Hyvän hoitovasteen saavuttaa annoksen mukaan 12 viikon hoidossa 32–55 % ja 24 viikon hoidossa 56–71 % aikuispotilaista «Hyvän hoitovasteen etanerseptilla saavuttaa annoksesta riippuen 12 viikon hoidossa vähintään kolmannes ja 24 viikon hoidossa vähintään puolet potilaista.»A.
- Lääke soveltuu erityisesti potilaille, jotka saattavat tarvita hoidon tauottamista, ja potilaille, joilla on aktiivinen nivelpsoriaasi.
- Kun hoito aloitetaan annoksella 50 mg kahdesti viikossa, suositellaan, että 12 viikon
kuluttua annosta pienennetään yhteen kerran viikossa otettavaan 50 mg:n annokseen.
- Teho ei kärsi annoksen pienentämisestä «Papp KA, Tyring S, Lahfa M ym. A global phase III ...»205.
- Hoitovaste ilmenee hitaammin kuin monoklonaalisia vasta-aineita käytettäessä.
- Hoidon lopetus tai tauotus ei johda ihopsoriaasin nopeaan pahenemiseen, joten hoito
voidaan myös tarvittaessa tauottaa.
- Hoidon uudelleenaloitus tauon jälkeen tehoaa lähes aikaisemman tavoin noin 80 %:lla «Gordon KB, Gottlieb AB, Leonardi CL ym. Clinical r...»206, «Moore A, Gordon KB, Kang S ym. A randomized, open-...»207, «Ortonne J, Griffiths C, Daudén Ey. Efficacy and sa...»208, «Ortonne JP, Taïeb A, Ormerod AD ym. Patients with ...»209.
- Tauti uusiutuu (relapsista ks. taulukko «Ihopsoriaasin hoitovasteeseen liittyviä määritelmiä , ...»1) hoidon päättymisen jälkeen noin 3 kuukauden kuluttua «Gordon KB, Gottlieb AB, Leonardi CL ym. Clinical r...»206.
- Pitkäaikaishoidossa hoitovaste säilyy kohtalaisen hyvin, mutta osa potilaista tarvitsee ajoittain tai jatkuvasti suurempaa hoitoannosta tai lisäksi muuta hoitoa «Etanerseptilla 24 viikon induktiohoidossa saavutettu hoitovaste säilyy kohtalaisen hyvin pitkäaikaishoidossa, mutta osa potilaista tarvitsee ajoittain tai jatkuvasti yhdistelmähoitoa tai hoitoannoksen nostoa.»B.
- Etanerseptihoitoon voidaan yhdistää muita hoitoja, mutta tutkimustietoa aiheesta on
toistaiseksi julkaistu vain vähän «Foley PA, Quirk C, Sullivan JR ym. Combining etane...»210.
- Jos potilaalla on etanerseptihoitoa aloitettaessa ennestään käytössään metotreksaatti ilman riittävää hoitovastetta, etanerseptilla saadaan parempi teho jatkamalla metotreksaattihoitoa sen rinnalla «Zachariae C, Mørk NJ, Reunala T ym. The combinatio...»211, «Gottlieb AB, Langley RG, Strober BE ym. A randomiz...»212.
- Etanersepti on tehokas lääke läiskäpsoriaasin induktiohoidossa aikuisilla.
- Guselkumabi (taulukko «IL-12/23:n ja IL-23:n estäjähoidon toteutus ja haittavaikutukset ...»12):
- Guselkumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Guselkumab treatment when compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment.»B.
- Hyvän hoitovasteen (PASI-75) saavutti 16 viikon lumekontrolloiduissa tutkimuksissa 86,3–91,2 % (lume 5,7–8,1 %) potilaista, erinomaisen (PASI-90) 70–73,3 % (lume 2,4–2,9 %) ja täydellisen (PASI-100) vasteen 34,1–37,4 % (lume 0,6–0,8 %) potilaista «Blauvelt A, Papp KA, Griffiths CE ym. Efficacy and...»213, «Reich K, Armstrong AW, Foley P ym. Efficacy and sa...»214.
- Hoitoteho näyttää säilyvän hyvin 48 viikkoon ulottuneessa jatkohoidossa.
- Myyntiluvan mukaista 100 mg:n annosta koko ajan saaneiden PASI-75-/PASI-90-/PASI-100-vasteet olivat 87,8 %/76,3 %/47,4 % «Reich K, Armstrong AW, Foley P ym. Efficacy and sa...»214.
- Vasta-aineita todettiin alle 6 %:lla potilaista, joista 7 % oli neutraloivia, mutta niillä ei havaittu yhteyttä hoitotuloksiin eikä haittatapahtumiin.
- Guselkumabi vaikuttaa 48 viikon tutkimusten perusteella turvalliselta. Tavallisia haittoja ovat lisääntyneet ylähengitystieinfektiot.
- Guselkumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Guselkumab treatment when compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment.»B.
| Lääke | Annos ihopsoriaasissa | Annos nivelpsoriaasissa | Haitat | Vaikutuskohde |
|---|---|---|---|---|
| Guselkumabi | 100 mg viikoilla 0 ja 4 ja sen jälkeen 8 viikon välein | Sama kuin ihopsoriaasissa. Vaikeassa nivelpsoriaasissa ylläpitoannosta voidaan tihentää 4 viikon välein annettavaksi | Lisääntynyt alttius ylähengitystieinfektioille | IL-23 |
| Risankitsumabi | 150 mg viikoilla 0 ja 4 ja sen jälkeen 12 viikon välein | Sama kuin ihopsoriaasissa | Lisääntynyt alttius ylähengitystieinfektioille | IL-23 |
| Tildrakitsumabi | 100 mg viikoilla 0 ja 4 ja sen jälkeen 12 viikon välein Jos potilaalla on suuri tautikuorma tai potilaan paino on yli 90 kg, lääkäri saattaa arvioida 200 mg:n annoksen tehokkaammaksi. |
- | Pistokohtien lievät ihoreaktiot Lisääntynyt alttius ylähengitystieinfektioille Leukopenia |
IL-23 |
| Ustekinumabi | 45 mg (yli 100 kg painaville 90 mg) viikoilla 0 ja 4 ja sen jälkeen 12 viikon välein | Sama kuin ihopsoriaasissa | Pistokohtien ihoreaktiot Lisääntynyt alttius ylähengitystieinfektioille |
IL-12/23 |
- Iksekitsumabi (taulukko «IL-17:n estäjähoidon toteutus ja haittavaikutukset ...»11):
- Iksekitsumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Ixekizumab treatment at the dose of 80 mg, when compared to placebo, increases the proportion of patients with active skin psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment.»A.
- Hyvän hoitovasteen (PASI-75) saavutti 12 viikon lumekontrolloiduissa tutkimuksissa 87,3–89,7 % potilaista.
- Erinomaisen (PASI-90) tai täydellisen (PASI-100) vasteen saavuttaa 12 viikossa 68,7–70,9 %/35,5–40,5 % potilaista, mutta enimmäisvasteet saavutetaan vasta viikoilla 24/36.
- Hoitoteho näyttää säilyvän hyvin vähintään vuoden seurannassa «Iksekitsumabin hoitoteho läiskäpsoriaasiin näyttää säilyvän hyvin vähintään 1 vuoden seurannassa.»C.
- Myyntiluvan mukaista hoitokaaviota koko 60 viikon ajan seuranneiden lopputulokset olivat PASI-75: 83 %, PASI-90: 73 % ja PASI-100: 55 %.
- Vasta-aineita iksekitsumabia kohtaan on havaittu 9 %:lla potilaista, mutta vain 1,7 %:lla ne olivat hoitotehoa heikentäviä.
- Iksekitsumabi vaikuttaa 60 viikon tutkimusten perusteella turvalliselta «Iksekitsumabin hoitoteho läiskäpsoriaasiin näyttää säilyvän hyvin vähintään 1 vuoden seurannassa.»C.
- Pistoskohdan ihoreaktiot ovat varsin yleisiä (17 %).
- Ylähengitystieinfektioita esiintyy tavallista useammin. Limakalvojen hiivainfektioiden määrä on kaikkien IL-17-väylään kohdistuvien lääkkeiden tapaan lisääntynyt.
- Iksekitsumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Ixekizumab treatment at the dose of 80 mg, when compared to placebo, increases the proportion of patients with active skin psoriasis to achieve a clinically meaningful improvement at 12 weeks of treatment.»A.
- Infliksimabi (taulukko «IL-17:n estäjähoidon toteutus ja haittavaikutukset ...»11):
- Infliksimabihoito on suositeltavin hoito, jos psoriaasi on epästabiili, erytroderminen tai pustuloiva.
- Ihopsoriaasin induktiohoidossa infliksimabi on tehokas.
- Hyvä hoitovaste saavutetaan noin 80 %:lla kroonista läiskäpsoriaasia sairastavista «Infliksimabi on tehokas ja nopeavaikutteinen vaikean läiskäpsoriaasin induktiohoidossa.»A.
- Vaste on nopea: enimmäisvaste saavutetaan 10 viikossa.
- Infliksimabin hyvä hoitoteho säilyy hyvin puoleen vuoteen asti ja melko hyvin vuoteen asti «Infliksimabin hyvä hoitoteho säilyy hyvin puoleen vuoteen asti ja melko hyvin vuoteen asti.»A.
- Hoitoa ei suositella tauotettavaksi, koska uudelleenaloitukset suurentavat anafylaksiariskiä ja heikentävät hoidon tehoa «Infliksimabihoitoa ei suositella tauotettavaksi, koska uudelleenaloituksiin näyttää liittyvän suurentunut anafylaksiariski sekä tehon heikkeneminen.»B. Uudelleenaloituksen yhteydessä suositellaan hitaampaa infuusiota ja mahdollisesti esilääkitykseksi 100–200 mg hydrokortisonia suonensisäisesti tai 40 mg metyyliprednisolonia suonensisäisesti, 1 g parasetamolia ja antihistamiinia «Lecluse LL, Piskin G, Mekkes JR ym. Review and exp...»215.
- Risankitsumabi (taulukko «IL-12/23:n ja IL-23:n estäjähoidon toteutus ja haittavaikutukset ...»12):
- Risankitsumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Risankizumab treatment when compared to placebo, increases the proportion of patients moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 16 weeks of treatment. The safety profile of risankizumab seems to be equal to placebo after 16 weeks treatment.»B.
- Erinomaisen hoitovasteen (PASI-90) saavutti 16 viikon lumekontrolloiduissa tutkimuksissa 74,8–75,3 % (lume 2–4,9 %) potilaista ja täydellisen (PASI-100) vasteen 35,9–50,7 % (lume 0–2 %) potilaista «Gordon KB, Strober B, Lebwohl M ym. Efficacy and s...»216.
- Hoitoteho näyttää säilyvän hyvin 52 viikkoon ulottuneessa jatkohoidossa.
- Myyntiluvan mukaista 150 mg:n annosta koko ajan saaneiden PASI-75-/PASI-90-/PASI-100-vasteet olivat 92 %/80,6–81,9 %/56,3–59,5 % «Gordon KB, Strober B, Lebwohl M ym. Efficacy and s...»216.
- Risankitsumabi vaikuttaa 52 viikon tutkimusten perusteella turvalliselta. Tavallisia haittoja ovat lisääntyneet ylähengitystieinfektiot.
- Risankitsumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Risankizumab treatment when compared to placebo, increases the proportion of patients moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 16 weeks of treatment. The safety profile of risankizumab seems to be equal to placebo after 16 weeks treatment.»B.
- Sekukinumabi (taulukko «IL-17:n estäjähoidon toteutus ja haittavaikutukset ...»11):
- Sekukinumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Sekukinumabi on tehokas läiskäpsoriaasin induktiohoidossa.»A.
- Hyvän hoitovasteen (PASI-75) saavutti 12 viikon lumekontrolloiduissa tutkimuksissa 77,1–81,6 % ja parhaimmillaan 16 viikon kohdalla 86,1–86,7 % potilaista.
- Erinomaisen (PASI-90) tai täydellisen (PASI-100) vasteen saavutti 16 viikon kohdalla 69,8–72,4 %/36,8–41,6 % potilaista.
- Hoitoteho näyttää säilyvän hyvin vähintään vuoden seurannassa «Sekukinumabin hoitoteho läiskäpsoriaasiin näyttää säilyvän hyvin vähintään 1 vuoden seurannassa.»C.
- Viikolla 12 hyvän hoitovasteen saaneista 81,6–84,3 %:lla vaste säilyi viikolle 52.
- Sekukinumabi vaikuttaa turvalliselta vuoden kestäneessä tutkimuksessa. Yleisimpiä haittatapahtumia ovat ylähengitystieinfektiot, joiden lisäksi IL-17-vasta-aineille tyypillisesti limakalvojen hiivainfektioita esiintyy tavallista yleisemmin.
- Sekukinumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Sekukinumabi on tehokas läiskäpsoriaasin induktiohoidossa.»A.
- Sertolitsumabipegoli (taulukko «TNF:n estäjähoidon toteutus ja haittavaikutukset ...»10):
- Sertolitsumabipegoli on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Certolizumab treatment, when compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 16 weeks of treatment. There may be more adverse events in certolizumab pegol treatment compared to placebo after 16 weeks of treatment.»B.
- Hyvän hoitovasteen (PASI-75) saavutti 16 viikon lumekontrolloiduissa tutkimuksissa 200 mg/400 mg:n annoksella 74,5 %/80,1 % potilaista (lume 7,5 %) ja erinomaisen (PASI-90) vasteen 44,5 %/52,2 % potilaista (lume 1,6 %) «Blauvelt A, Reich K, Lebwohl M ym. Certolizumab pe...»217.
- Hoitoteho näyttää säilyvän hyvin 48 viikkoon ulottuneessa jatkohoidossa.
- Annoksella 200 mg/400 mg PASI-75-vaste oli 70,7 %/83,6 %, PASI-90-vaste 50,0 %/61,6 % ja PASI-100-vaste 28,5 %/34,5 % «Gottlieb AB, Blauvelt A, Thaçi D ym. Certolizumab ...»218.
- Lääkkeelle on kuvattu muodostuneen vasta-aineita 8–19 %:lla potilaista, joista osalla ne olivat neutraloivia, lääkepitoisuuksia pienentäviä ja hoitovaikutusta heikentäviä.
- Sertolitsumabipegoli vaikuttaa 48 viikon tutkimusten perusteella turvalliselta. Pitkäaikaista käyttökokemusta on nivel- ja selkärankareuman hoidosta. Myös nivelpsoriaasin hoidossa sitä on käytetty useamman vuoden ajan. Sertolitsumabipegolin tavallisia haittoja ovat lisääntyneet ylähengitystieinfektiot, ja sitä koskevat TNF:n estäjien yleiset rajoitteet ja riskit. Lääkemolekyyli poikkeaa rakenteeltaan kaikista muista biologisista psoriaasilääkkeistä siten, ettei se sisällä lainkaan vasta-aineiden Fc-osaa, eikä sitä siten aktiivisesti kuljeteta istukan läpi sikiön verenkiertoon.
- Sertolitsumabipegoli on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Certolizumab treatment, when compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis to achieve a clinically meaningful improvement at 16 weeks of treatment. There may be more adverse events in certolizumab pegol treatment compared to placebo after 16 weeks of treatment.»B.
- Tildrakitsumabi ((taulukko «IL-12/23:n ja IL-23:n estäjähoidon toteutus ja haittavaikutukset ...»12):
- Tildrakitsumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Tildrakizumab, compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis who reach PGA0-1 at 12-16 weeks of treatment. It may be effective in terms of PASI90 and the safety profile may be comparable to placebo at 16 weeks of treatment.»B.
- Hyvän hoitovasteen (PASI-75) myyntiluvan mukaisella 100 mg:n annoksella saavutti kolmessa yhteenlasketussa 12 viikon lumekontrolloidussa tutkimuksessa 62,3 % potilaista (lume 5,6 %), erinomaisen (PASI-90) 35,9 % (lume 2 %) ja täydellisen (PASI-100) vasteen 13,2 % (lume 0,6 %) potilaista «Papp KA, Reich K, Blauvelt A ym. Efficacy of tildr...»219.
- Hoidon teho näyttää lisääntyvän hoidon jatkuessa viikkoon 28 ulottuneessa tutkimuksessa.
- Myyntiluvan mukaista annosta koko ajan saaneiden PASI-75-/PASI-90-/PASI-100-vasteet olivat 77,4 %/53,6 %/23,1 % «Papp KA, Reich K, Blauvelt A ym. Efficacy of tildr...»219.
- Pitkäaikaisia hoitotuloksia ei ole julkaistu.
- Lyhyellä aikavälillä tildrakitsumabi vaikuttaa turvalliselta. Tavallinen haitta on lisääntynyt ylähengitystieinfektiotaipumus.
- Tildrakitsumabi on tehokas läiskäpsoriaasin induktiohoidossa aikuisilla «Tildrakizumab, compared to placebo, seems to increase the proportion of patients with moderate to severe plaque psoriasis who reach PGA0-1 at 12-16 weeks of treatment. It may be effective in terms of PASI90 and the safety profile may be comparable to placebo at 16 weeks of treatment.»B.
- Ustekinumabi (taulukko «IL-12/23:n ja IL-23:n estäjähoidon toteutus ja haittavaikutukset ...»12):
- Hoitovaste on läiskäpsoriaasissa 12 viikon hoidossa annoksen mukaan hyvä 66–76 %:lla potilaista ja erinomainen 37–52 %:lla potilaista. Hyvän hoitovasteen saavuttaa 70–79 % potilaista 28 viikon hoidossa ja erinomaisen hoitovasteen 45–56 % potilaista «Ustekinumabin vaste ihopsoriaasissa on hyvä ja pitkäkestoinen.»A.
- Vaste on parhaimmillaan 28 viikon kohdalla «Leonardi CL, Kimball AB, Papp KA ym. Efficacy and ...»220, «Papp KA, Langley RG, Lebwohl M ym. Efficacy and sa...»221.
- Hyvä hoitoteho jatkuu pitkäaikaisessa hoidossa: PASI-75-vasteessa on 5 vuoden kohdalla edelleen 61–79 % potilaista «Ustekinumabin vaste ihopsoriaasissa on hyvä ja pitkäkestoinen.»A.
- Hoitovaste saattaa olla merkittävästi parempi HLA-C*06-alleelipositiivisilla «Talamonti M, Galluzzo M, Chimenti S ym. HLA-C*06 a...»222.
- Infektioriski vaikuttaa pienemmältä kuin TNF:n estäjillä «Gniadecki R, Bang B, Bryld LE ym. Comparison of lo...»176, «Leonardi CL, Kimball AB, Papp KA ym. Efficacy and ...»220, «Papp KA, Langley RG, Lebwohl M ym. Efficacy and sa...»221, «Gordon KB, Papp KA, Langley RG ym. Long-term safet...»223, «Warren RB, Smith CH, Yiu ZZN ym. Differential Drug...»224, «Zweegers J, van den Reek JM, van de Kerkhof PC ym....»225, «Menter A, Papp KA, Gooderham M ym. Drug survival o...»226, «Kalb RE, Fiorentino DF, Lebwohl MG ym. Risk of Ser...»227, «Carretero G, Ferrandiz C, Dauden E ym. Risk of adv...»228. Turvallisuudessa ei 5 vuoden seurannassa ole todettu oleellisia muutoksia eikä kumuloituvia haittoja «Lebwohl M, Leonardi C, Griffiths CE ym. Long-term ...»229, «Reich K, Papp KA, Griffiths CE ym. An update on th...»230, «Kimball AB, Papp KA, Wasfi Y ym. Long-term efficac...»231, «Langley RG, Lebwohl M, Krueger GG ym. Long-term ef...»232.
- Usean vuoden seurantatutkimuksissa psoriaasipotilaat pysyvät pidempään ustekinumabihoidossa kuin TNF:n estäjähoidossa «Psoriaasipotilaiden hoidossa pysyminen biologisilla lääkkeillä rekisteritutkimuksissa ja muissa pitkän ajan seurantatutkimuksissa»11.
- Biologisten lääkkeiden käytöstä nivelpsoriaasissa ks. kohta Nivelpsoriaasin hoito «A6»6.
| Lääke | Adalimumabi | Etanersepti | Infliksimabi | Sertolitsumabipegoli | Ustekinumabi |
|---|---|---|---|---|---|
| *Hoidon jatkuvuus rekisteritutkimuksissa. Ks. myös lisätietoa «Psoriaasipotilaiden hoidossa pysyminen biologisilla lääkkeillä rekisteritutkimuksissa ja muissa pitkän ajan seurantatutkimuksissa»11 | |||||
| Tyyppi | humaani monoklonaalinen vasta-aine (IgG1/κ) | fuusioproteiini liukoinen reseptori | kimeerinen monoklonaalinen vasta-aine (IgG1) | humaani monoklonaalinen vasta-aine (IgG1/κ) | humaani monoklonaalinen vasta-aine (IgG1/κ) |
| Vaikutuskohde | TNF-alfa | TNF-alfa, LT (TNF-beeta) | TNF-alfa | TNF-alfa | p40 (IL-12/IL-23) |
| Puoliintumisaika (mediaani) | 14 vrk | 3 vrk | 9 vrk | 14 vrk | 21 vrk |
| Annos | alkuannos 80 mg, seuraavalta viikolta alkaen 40 mg joka toinen viikko Tarvittaessa annos voidaan nostaa tasolle 80 mg joka toinen viikko | 50 mg viikossa tai ensimmäiset 12 viikkoa 50 mg kahdesti viikossa ja sen jälkeen kerran viikossa | 5 mg/kg i.v. viikoilla 0, 2 ja 6 ja sen jälkeen 8 viikon välein | alkuannos 400 mg viikoilla 0, 2, ja 4 ja sen jälkeen 200 mg joka toinen viikko Tarvittaessa annos voidaan nostaa tasolle 400 mg joka toinen viikko |
45 mg (yli 100 kg painaville 90 mg) viikoilla 0 ja 4 ja sen jälkeen 12 viikon välein |
| Hoitovasteen alkamisaika «Nast A, Sporbeck B, Rosumeck S ym. Which antipsori...»233 - 25 % PASI-75 |
melko nopea 4,6 viikkoa |
hidas 6,6 viikkoa |
nopea 3,5 viikkoa |
melko nopea 4,3 viikkoa |
melko hidas 5,1 (4,6) viikkoa |
| Hoitovasteen todennäköisyys induktiovaiheen lopussa vk 8–24 vs. lume RR (95 % LV) «Sbidian E, Chaimani A, Garcia-Doval I ym. Systemic...»236. | |||||
| PASI-75 PASI-90 |
10,05 (8,61–11,73) | 8,09 (7,22–9,06) | 18,02 (11,92–27,22) | 9,61 (7,78–11,88) | 11,04 (9,83–12,40) |
| Hoitovasteen todennäköisyys % (95 % LV)) noin vuoden (44–60 viikkoa) hoidossa «Armstrong AW, Puig L, Joshi A ym. Comparison of Bi...»235. Luvut eivät ole välttämättä vertailukelpoisia, koska ne on saatu eri tutkimuksista. | |||||
| PASI-75 | 67,1 (52,9–78,7) | 55,5 (50,1–60,9) | 58,3 (52,5–63,8) | 72,5 (65,9–78,2) | |
| PASI-90 | 46,2 (38,6–53,9) | 33,4 (28,5–38,7) | 40,1 (30,0–51,1) | 52,4 (47,1–57,7) | |
| Hoidon jatkuvuus* | ei vielä tiedossa | ||||
| 1 vuoden jälkeen | 69,0–79,0 % | 70,0–75,8 % | 58,0–68,8 % | 77,2–89,0 % | |
| 2 vuoden jälkeen | 53,2–67,0 % | 51,0–60,8 % | 30,1–54,2 % | 68,5–82,0 % | |
| 3 vuoden jälkeen | 41,9–59,0 % | 39,1–56,0 % | 22,6–45,5 % | 61,8–75,6 % | |
| Lääke | Bimekitsumabi | Brodalumabi | Iksekitsumabi | Sekukinumabi | Guselkumabi | Risankitsumabi | Tildrakitsumabi |
|---|---|---|---|---|---|---|---|
| *Hoidon jatkuvuus rekisteritutkimuksissa. Ks. myös lisätietoa «Psoriaasipotilaiden hoidossa pysyminen biologisilla lääkkeillä rekisteritutkimuksissa ja muissa pitkän ajan seurantatutkimuksissa»11 | |||||||
| Tyyppi | humanisoitu monoklonaalinen vasta-aine (IgG1) |
humaani monoklonaalinen vasta-aine (IgG2) |
humanisoitu monoklonaalinen vasta-aine (IgG4) |
humaani monoklonaalinen vasta-aine (IgG1/κ) |
humaani monoklonaalinen vasta-aine (IgG1/λ) |
humanisoitu monoklonaalinen vasta-aine (IgG1) |
humanisoitu monoklonaalinen vasta-aine (IgG1/κ) |
| Vaikutuskohde | IL-17A, AF, F | IL-17RA | IL-17A | IL-17A | IL-23(p19) | IL-23(p19) | IL-23(p19) |
| Puoliintumisaika (mediaani) | 23 vrk | 23 vrk | 13 vrk | 27 vrk | 17 vrk | 28 vrk | 23 vrk |
| Annos | 320 mg 4 viikon välein viikolle 16 saakka, minkä jälkeen 8 viikon välein |
210 mg viikoilla 0, 1 ja 2, minkä jälkeen joka toinen viikko |
alkuannos 160 mg, minkä jälkeen 80 mg kahden viikon välein 12 viikkoon saakka ja sen jälkeen 80 mg 4 viikon välein |
300 mg viikoilla 0, 1, 2, 3 ja 4, minkä jälkeen 300 mg kerran kuukaudessa |
100 mg viikoilla 0 ja 4, minkä jälkeen 8 viikon välein |
150 mg viikoilla 0 ja 4, minkä jälkeen 150 mg 12 viikon välein |
100 mg viikoilla 0, ja 4, minkä jälkeen 12 viikon välein Jos potilaalla on suuri tautikuorma tai potilaan paino on yli 90 kg, lääkäri saattaa arvioida 200 mg:n annoksen tehokkaammaksi. |
| Hoitovasteen alkamisaika «Nast A, Sporbeck B, Rosumeck S ym. Which antipsori...»233, «Egeberg A, Andersen YMF, Halling-Overgaard AS ym. ...»234 | erittäin nopea | erittäin nopea | erittäin nopea | erittäin nopea | nopea | nopea | melko hidas |
| - 25 % PASI-75 | - | 2,1 viikkoa | 2,2 viikkoa | 3,0 viikkoa | 3,8 viikkoa | - | 5,6 viikkoa |
| - 25 % PASI-90 | - | 3,5 viikkoa | 4,1 viikkoa | 5,1 viikkoa | 6,2 viikkoa | 6,1 viikkoa | - |
| Hoitovasteen todennäköisyys induktiovaiheen lopussa vk 8–24 vs. lume RR (95 % LV) «Sbidian E, Chaimani A, Garcia-Doval I ym. Systemic...»236. | |||||||
| PASI-75 | 18,02 (11,92–27,22) |
12,20 (10,50–14,16) |
14,54 (12,59–16,79) |
12,71 (11,12–14,52) |
12,25 (10,22–14,68) |
13,44 (11,87–15,22) |
10,72 (8,78–13,08) |
| PASI-90 | 58,64 (3,72–923,86) |
23,55 (19,48–28,48) |
32,48 (27,13–38,87) |
25,79 (21,61–30,78) |
25,52 (21,25–30,64) |
28,76 (23,96–34,54) |
18,73 (14,21–24,69) |
| Hoitovasteen todennäköisyys % (95 % LV) noin vuoden (44–60 viikkoa) hoidossa «Armstrong AW, Puig L, Joshi A ym. Comparison of Bi...»235. Luvut eivät ole välttämättä vertailukelpoisia, koska ne on saatu eri tutkimuksista. | |||||||
| PASI-75 | 80,0 (75,7–83,7) |
85,0 (79,2–89,4) |
88,6 (80,6–93,6) |
88,2 (84,6–91,1) |
90,1 (86,3–92,9) |
||
| PASI-90 | 74,0 (69,3–78,1) |
73,9 (69,9–77,5) |
71,3 (64,2–77,5) |
76,5 (72,1–80,5) |
79,4 (75,5–82,9) | ||
| Hoidon jatkuvuus* 1 vuoden jälkeen 2 vuoden jälkeen 3 vuoden jälkeen |
ei vielä tiedossa |
ei vielä tiedossa |
ei vielä tiedossa |
ei vielä tiedossa |
ei vielä tiedossa |
ei vielä tiedossa |
|
- Potilaan liitännäissairaudet on huomioitava systeemisen lääkkeen valinnassa. Ks. taulukko «hoi50062f.pdf»5, johon on koottu suuntaa antavia suosituksia.
Nivelpsoriaasi
Nivelpsoriaasin diagnoosi
- Nivelpsoriaasin diagnoosi on pääasiassa kliininen. Suosittelemme käyttämään ICD-10-diagnoosikoodia M07.3*L40.5, kun diagnoosi on varma, ja diagnoosikoodia M13.8, kun kyseessä on epäily.
- Nivelpsoriaasia tulee epäillä aina, jos niveltulehdus ja ihopsoriaasi esiintyvät samanaikaisesti.
- Pienellä osalla potilaista iho-oireet ilmaantuvat niveloireiden jälkeen.
- Ihopsoriaasin puuttuessa diagnostiikassa antavat vihjeitä
- psoriaasille ominaiset kynsimuutokset
- niveltulehduksen epäsymmetrisyys
- makkarasormien ja -varpaiden esiintyminen
- entesiitit
- ensimmäisen asteen sukulaisella esiintyvä iho- tai nivelpsoriaasi.
- Psoriaasi niveltulehduspotilaalla ei sulje pois muiden nivelsairauksien mahdollisuutta.
- Nivelpsoriaasin luokitteluun käytetään niin sanottua CASPAR (Classification Criteria
for Psoriatic Arthritis) -luokittelukriteeristöä, joka soveltuu erityisesti kliinisiin
tutkimuksiin «CASPAR (Classification criteria for Psoriatic ARthritis) -kriteerit»12.
- Sitä voi käyttää myös diagnostiikan apuna, jos potilaalla on varma artriitti, spodylartriitti tai entesiitti.
- Nivelpsoriaasissa oireena ja löydöksinä voi esiintyä «Gladman DD, Farewell V, Buskila D ym. Reliability ...»237, «Oriente P, Biondi-Oriente C, Scarpa R. Psoriatic a...»238, «Cohen MR, Reda DJ, Clegg DO. Baseline relationship...»239, «Cantini F, Salvarani C, Olivieri I ym. Distal extr...»240
- nivelten arkuutta ja aamujäykkyyttä
- niveltulehduksia
- muutaman nivelen epäsymmetrisiä niveltulehduksia
- sormien ja varpaiden kärkinivelten tulehdusta (kuvat «Varpaiden niveltulehdukset psoriartriitissa»50, «Varpaiden niveltulehdukset nivelpsoriaasissa»51, «Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa»52, «Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa»53, «Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa»54, «Sormien kärkijäsenten niveltulehdukset ja lievät kynsimuutokset nivelpsoriaasissa»55, «Sormien kärkinivelten tulehdukset ja kynsimuutokset»56 ja «Sormien kärkinivelten tulehdukset ja kynsimuutokset»57)
- nivelreuman kaltaista moniniveltulehdusta
- Tulehdus liittyy usein kynsimuutoksiin.
- tulehduksellista selkäkipua (herättää aamuyöstä, helpottuu liikkumisella ja voi pahentua
levossa)
- Kipu voi olla merkki spondyliitistä ja sakroiliitistä.
- Klassisesta selkärankareumasta poikkeavasti sakroiliitti voi olla toispuoleinen tai puuttua. Lisäksi sairaus voi affisioida kaularankaa jo varhain.
- HLAB27-kudostekijä on positiivinen selvästi harvemmin kuin selkärankareumassa «Coates LC, Baraliakos X, Blanco FJ ym. The Phenoty...»241.
- Nivelpsoriaasin aksiaalinen tautimuoto voi alkaa myöhemmällä iällä kuin selkärankareuma «Chandran V. Psoriatic spondylitis or ankylosing sp...»242.
- entesiittejä (lihasjänteiden tai nivelsiteiden kiinnittymiskohtien tulehdusta)
- Tyypillisiä ovat erityisesti akillesjänteen kiinnityskohdan tulehdukset ja jalkapohjan plantaarifaskiitti.
- daktyliitteja (makkaramaisesti turvonneet yksittäiset sormet tai varpaat) (kuvat «Vaikea nivelpsoriaasin makkaramainen turvotus sormessa»58 ja «Makkaramainen turvotus varpaassa nivelpsoriaasipotilaalla»59)
- harvoin mutiloivaa (luita syövyttävää) tulehdusta
- toispuoleista raajan pitting-turvotusta (kuva «Käden pitting-turvotus vaikeaa nivelpsoriaasia sairastavalla potilaalla»60).
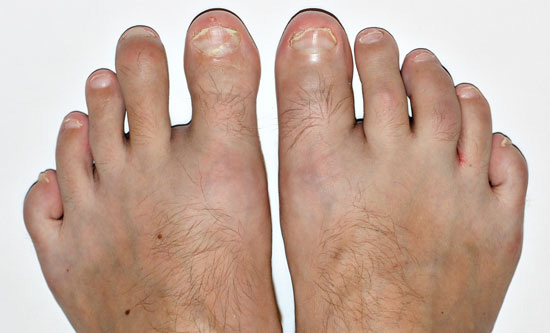
Varpaiden niveltulehdukset psoriartriitissa
© Riitta Luosujärvi
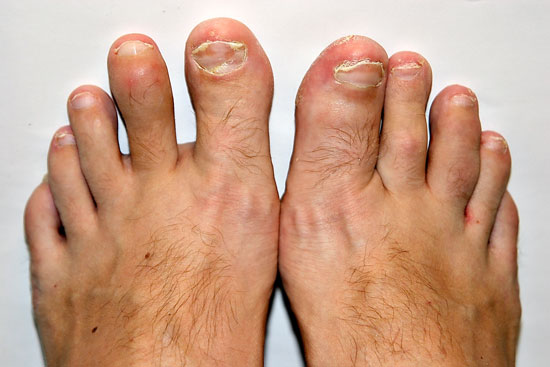
Varpaiden niveltulehdukset nivelpsoriaasissa
© Riitta Luosujärvi
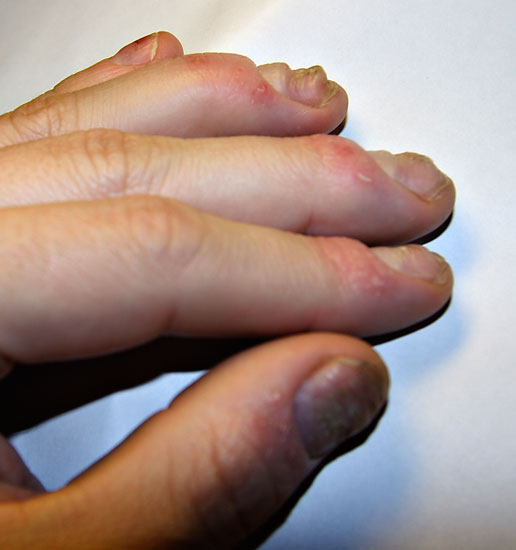
Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa.
Ledinflammationer i de yttersta fingerlederna och nagelförändringar vid ledpsoriasis.
© Riitta Luosujärvi
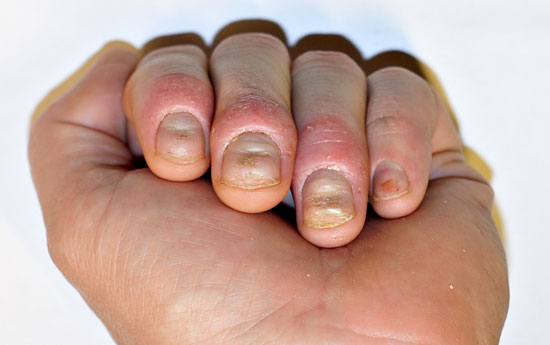
Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa
© Riitta Luosujärvi
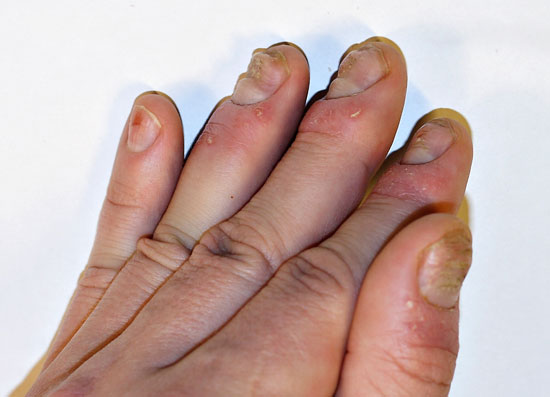
Sormien kärkijäsenten niveltulehdukset ja kynsimuutokset nivelpsoriaasissa
© Riitta Luosujärvi
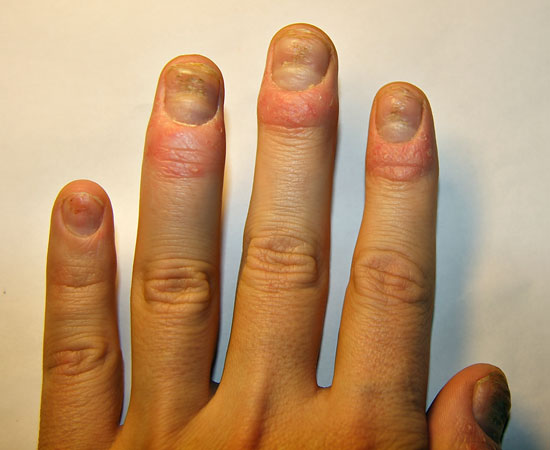
Sormien kärkijäsenten niveltulehdukset ja lievät kynsimuutokset nivelpsoriaasissa
© Riitta Luosujärvi
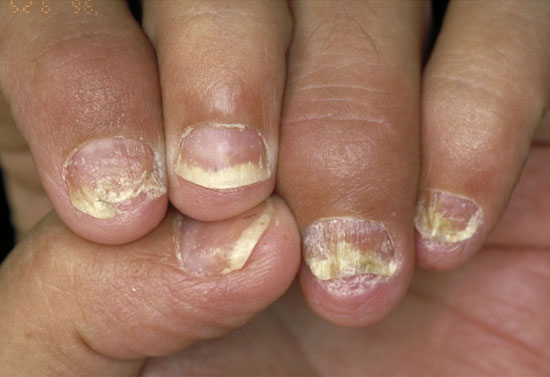
Sormien kärkinivelten tulehdukset ja kynsimuutokset
© Raimo Suhonen
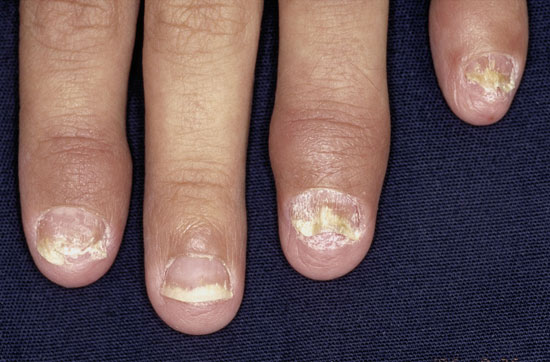
Sormien kärkinivelten tulehdukset ja kynsimuutokset
© Raimo Suhonen
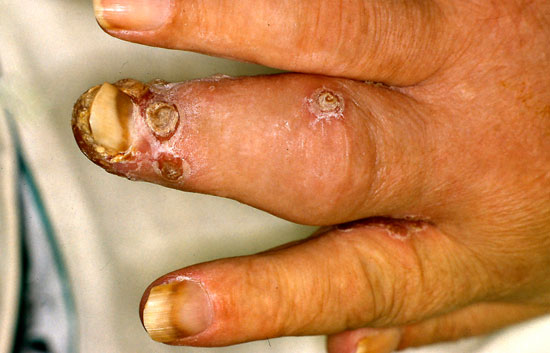
Vaikea nivelpsoriaasin makkaramainen turvotus sormessa
© Riitta Luosujärvi
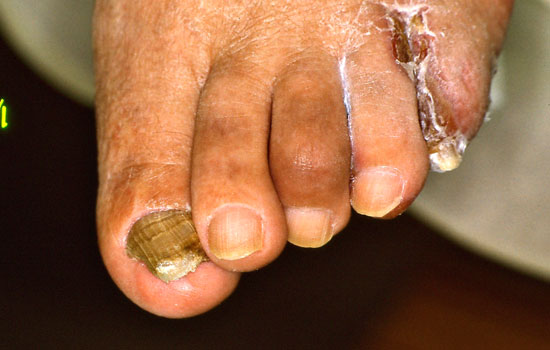
Makkaramainen turvotus varpaassa nivelpsoriaasipotilaalla
© Riitta Luosujärvi
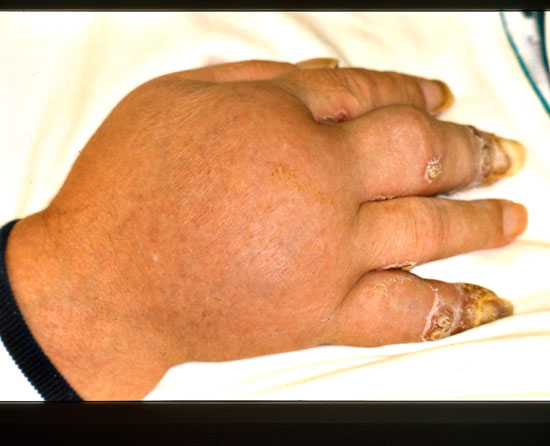
Käden pitting-turvotus vaikeaa nivelpsoriaasia sairastavalla potilaalla
© Riitta Luosujärvi
Laboratorio- ja kuvantamislöydökset
- Laboratoriotutkimuksista ei ole hyötyä nivelpsoriaasin diagnostiikassa.
- Lasko ja CRP-pitoisuus voivat olla normaaleja tai suurentuneita.
- Potilailla ei yleensä esiinny veressä reumatekijää.
- Psoriaatikoilla esiintyy reumatekijää kuten muullakin väestöllä «Gladman DD, Shuckett R, Russell ML ym. Psoriatic a...»28.
- Sitrulliinipeptidivasta-aineita esiintyy 6–13 %:lla «Payet J, Goulvestre C, Bialé L ym. Anticyclic citr...»243.
- Natiiviröntgenkuvaus:
- Natiiviröntgenkuvausta käytetään diagnostiikassa ja hoidon seurannassa.
- Radiologiset muutokset ovat monimuotoisia, ja ne kehittyvät vuosien kuluessa. Ks. lisätietoa aiheesta «Nivelpsoriaasin tyypilliset radiologiset muutokset»13.
- Radiologiset muutokset esiintyvät usein epäsymmetrisesti.
- Samalla potilaalla voidaan todeta useita erilaisia radiologisia muutoksia samanaikaisesti.
- Nivelten ultraäänitutkimus:
- Tekijältä vaaditaan perehtyneisyyttä.
- Ultraäänitutkimuksella voidaan osoittaa niveltulehduksen lisäksi jännetulehdus, daktyliitti
ja entesiitti «Kane D. The role of ultrasound in the diagnosis an...»244, «Dubash SR, De Marco G, Wakefield RJ ym. Ultrasound...»245.
- OMERACT-työryhmän määritelmä ultraäänellä todettavalle entesiitille vuodelta 2018 edellyttää, että jänne todetaan paksuuntuneeksi tai vähäkaikuiseksi lähellä insertiota luuhun (< 2 mm luun korteksista). Lisäksi tarvitaan positiivinen doppler-signaali (aktiivisessa tulehduksessa) tai rakenteellisena muutoksena korteksin eroosio tai entesofyytti tai jänteen kalsifikaatio «Balint PV, Terslev L, Aegerter P ym. Reliability o...»246.
- Ultraäänitutkimus ei ole yksinään diagnostinen nivelpsoriaasissa.
- Magneettikuvantaminen:
- Tulkitsijalta vaaditaan tuki- ja liikuntaelinten magneettikuvaukseen perehtyneisyyttä.
- Magneettikuvantaminen osoittaa nivelten tulehdusmuutokset aikaisemmin kuin tavanomainen röntgenkuva «Offidani A, Cellini A, Valeri G ym. Subclinical jo...»247. Entesiittien kuvantamisessa magneettikuvaus mahdollistaa syvemmällä olevien kohteiden tutkimisen kuin ultraääni. Lisäksi se mahdollistaa jänneinsertiittiin liittyvän luuödeemin havaitsemisen.
- Nuorilla tutkittavilla (< 45 vuotta) ja potilailla, joiden oireet ovat kestäneet vain lyhyen aikaa, SI-nivelten ja rangan kuvantamiseen suositellaan ensisijaisesti magneettikuvausta «Mandl P, Navarro-Compán V, Terslev L ym. EULAR rec...»248.
- Vuosia kestäneen tulehduksen aiheuttamia rakenteellisia muutoksia voidaan havaita natiiviröntgentutkimuksella.
- Magneettikuvausta ei suositella nivelmuutosten etenemisen seurantaan.
- Nivelpsoriaasin diagnostiikassa tietokonetomografia ja isotooppitutkimukset ovat harvoin tarpeen, mutta niitä käytetään tarpeen mukaan muiden sairauksien sulkemiseen pois.
- Ks. lisätietoa kuvantamisesta nivelpsoriaasissa «Kuvantaminen nivelpsoriaasissa»14.
Nivelpsoriaasin ilmenemismuodot ja aktiivisuuden arviointi
- Nivelpsoriaasin aktiivisuus tulee arvioida kokonaisuutena ja kaikki sen ilmenemismuodot tulee huomioida «Nivelpsoriaasin ilmenemismuotoja ...»15, «Gossec L, Baraliakos X, Kerschbaumer A ym. EULAR r...»249, «Singh JA, Guyatt G, Ogdie A ym. Special Article: 2...»250, «Coates LC, Kavanaugh A, Mease PJ ym. Group for Res...»251.
- Huonon ennusteen tekijät ovat aihe aktiiviseen hoitolinjaan «Huonon ennusteen tekijöitä...»16.
| Muskuloskeletaaliset tautimuodot | Ihopsoriaasi liittyneenä nivelpsoriin | Liitännäissairaudet |
|---|---|---|
Perifeeriset artriitit
Aksiaalinen tauti Entesiitit Daktyliitit |
Ihottuma Kynsimuutokset |
Spondyloartropatian ilmentymät
Muut liitännäissairaudet
|
|
Nivelpsoriaasin hoito
- Hoito valitaan aina yksilöllisesti yhdessä potilaan kanssa.
- Onnistunut hoito vaatii potilaalta sitoutumista. Hoitoon sitoutumiseen vaikuttavat erityisesti valitun hoitomuodon odotettu teho ja sen haitat sekä turvallisuus. Myös hoitoprosessiin liittyvät tekijät, kuten se, mikä on lääkkeen antoreitti ja annetaanko lääke sairaalassa vai annosteleeko potilas sen itsenäisesti, ja hoidosta aiheutuvat kustannukset vaikuttavat hoitoon sitoutumiseen. Ks. myös lisätietoa «Nivelpsoriaasia sairastavien potilaiden kokemuksia ja näkemyksiä»15.
Hoidon tavoitteet
- Hoidon tavoitteena ovat potilaan toimintakyvyn ja elämänlaadun optimointi ja pysyvien rakenteellisten vaurioiden estäminen.
- Taudin mahdollisimman vähäinen aktiivisuus edistää näiden tavoitteiden saavuttamista. Sairauden heterogeenisuuden vuoksi täydellinen remissio on vaikea sekä määritellä että saavuttaa, varsinkin jos katsotaan, että siihen kuuluvat täydellinen kivuttomuus ja rauhallinen ihotilanne.
- Toistaiseksi kansainvälisissä hoitosuosituksissa realistiseksi hoitotavoitteeksi ("treat-to-target") määritetäänkin taudin vähäinen aktiivisuus (minimal disease activity, MDA), «Taudin vähäisen aktiivisuuden (Minimal disease activity, MDA) kriteerit ....»17.
- Tutkimusnäyttö taudin vähäiseen aktiivisuuteen pyrkivän hoitostrategian hyödyistä
on vielä vähäistä.
- Ensimmäisen taudin vähäiseen aktiivisuuteen pyrkineen TICOPA (TIght Control of inflammation in early Psoriatic Arthritis) -tutkimuksen «Coates LC, Kavanaugh A, Mease PJ ym. Group for Res...»251 mukaan vuoden seurannassa aktiivisella hoitolinjalla suurempi osa potilaista näyttää saavuttavan ACR20- ja ACR50-vasteet kuin perinteisellä hoidolla. Viiden vuoden seurannassa ryhmien välillä ei havaittu eroa «Coates LC, Mahmood F, Freeston J ym. Long-term fol...»255.
| PASI = Psoriasis Area Severity Index (0–72), BSA = Body Surface Area, kuinka monta prosenttia vartalosta psoriaasi-ihottuman peitossa, kämmenen alue vastaa noin 1 %:a, VAS = Visual Analog Scale 0–100 mm, HAQ = Health Assessment Questionnaire | |
| Arat nivelet (68:sta nivelestä) | ≤ 1 |
| Turvonneet nivelet (66:sta nivelestä) | ≤ 1 |
| PASI tai BSA |
≤ 1 ≤ 3 |
| Potilaan Kipu-VAS (0–100 mm) | ≤ 15 |
| Potilaan Yleisvointi-VAS (0–100 mm) | ≤ 20 |
| HAQ | ≤ 0,5 |
| Arat entesiittipisteet (Leeds Enthesitis Indexin kohdista bilateraalisesti) | ≤ 1 |
| Potilaan katsotaan saavuttavan MDA:n, jos hän täyttää vähintään 5/7 kriteeriä. | |
- Kliinisessä työssä on luontevaa pyrkiä mahdollisimman hyvään toimintakykyyn, elämänlaatuun ja taudin vähäiseen aktiivisuuteen siten, että huomioidaan kaikki taudin ilmenemismuodot ja lääkityksen siedettävyys sekä liitännäissairaudet.
- Nivelpsoriaasin hoidon ohella liitännäissairauksia tulee hoitaa aktiivisesti.
- Hyvä hoito edellyttää systemaattista hoitovasteen seurantaa.
Hoitovasteen seuranta
- Erikoissairaanhoidossa hoitovasteen seurannassa arvioidaan kaikkien ilmenemismuotojen
aktiivisuus:
- 66/68 nivelen turvotus ja arkuus
- tulehdusarvot
- potilaan kokonaisarvio sairauden tilasta ja kivusta (VAS 0–100 mm).
- DAPSA (Disease Activity in PSoriatic Arthrits) Score (DAPSA = TJC (tender joint count) + SJC (swollen joint count) + CRP + sairauden aktiivisuus VAS-asteikolla 0–10 cm + kipu VAS-asteikolla 0–10 cm).
- DAPSA:
- 0–4 = remissio
- 5–14 = vähäinen aktiivisuus
- 15–28 = kohtuullinen aktiivisuus
- > 28 suuri aktiivisuus.
- Aksiaalisessa sairaudessa arvioidaan lisäksi
- rangan liikkuvuusmittaukset (BASMI)
- BASDAI- ja BASFI-kyselyt
- ASDAS (Ankylosing Spondylitis Disease Activity Score) -aktiivisuusmittari.
- Daktyliittien ja entesiittien esiintymiseen on erilaisia mittareita. Esimerkiksi Leeds enthesitis indeksissä arvioidaan 6 paikan (molemmin puolin akillesjänteen insertiot, reisiluun sisänivelnastat ja olkaluun ulkosivunastat) arkuutta «Entesiittien arvioiminen nivelpriaasipotilailla (LEI)»61.
- Ihopsoriaasin hoitovastetta voidaan arvioida lääkärin yleisarvion tai vaikeusastemittarin (PASI, BSA) muutoksen perusteella.
- Kuvantamistutkimuksia käytetään kliinisen harkinnan mukaan.
Leeds enthesitis indeksissä (LEI) arvioidaan arkuutta molemmin puolin akillesjänteen proksimaalisesta insertiosta, reisiluun sisänivelnastasta ja olkaluun ulkosivunastasta.
© Suomalainen Lääkäriseura Duodecim
Tulehduskipulääkkeet
- Kipu heikentää nivelpsoriaasipotilaan elämänlaatua ja toiminta- ja työkykyä. Ks. lisätietoa aiheesta «Nivelpsoriaasia sairastavien potilaiden kokemuksia ja näkemyksiä»15.
- Tulehduskipulääkkeet ovat tavallisin oireenmukainen lääkitys nivelpsoriaasissa. Kliinisen kokemuksen mukaan niistä hyötyvät erityisesti aksiaalista tautimuotoa sairastavat. Usein hoito on pitkäaikaista.
- Kaikessa tulehduskipulääkehoidossa tulee huomioida hoitoon mahdollisesti liittyvät haittavaikutukset. Käytöstä ja haittavaikutuksista ks. Käypä hoito -suositukset Nivelreuma «Nivelreuma»4 ja Kipu «Kipu»9. Ks. myös Käypä hoito -suosituksen Kipu kaavio Kipulääkkeen valinta «https://www.terveysportti.fi/xmedia/hoi/hoi50103/Kipulaakkeen_valinta.html»19.
Perinteiset synteettiset reumalääkkeet (disease modifying antirheumatic drugs, csDMARD)
- Kelvollisia hoitotutkimuksia on tehty vähän.
- Vanhoissa tutkimuksissa hoitovasteen arviointi on vaihdellut. Tutkimusten potilasmäärät ovat olleet usein pieniä, eikä niissä ole käytetty nykyisiä hoitovasteen arvioinnin kriteereitä.
- Lääkkeiden tehosta tarvitaan lisää tutkimusnäyttöä.
- Reumalääkehoidon toteuttamisen periaatteita on käsitelty Käypä hoito -suosituksessa Nivelreuma «Nivelreuma»4 ja Reumatologisen yhdistyksen internetsivuilla «https://www.reumatologinenyhdistys.fi/ohjeet/»12, kohta Ohjeita).
- Metotreksaatti «Metotreksaattilääkityksessä huomioon otettavia asioita ...»4:
- Kliinisen kokemuksen perusteella metotreksaatti on ensisijainen ja sillä saattaa olla
tehoa nivelpsoriaasin hoidossa, vaikka tutkimusnäyttö asiasta on edelleen vähäinen
«Metotreksaatti verrattuna lumeeseen saattaa nivelpsoriaasia sairastavilla lisätä hoitovasteen saavuttamista 6 kuukauden seurannassa (RR 1,76; 95 % luottamusväli 1,14–2,70).»C.
- Metotreksaatti saattaa lumeeseen verrattuna lisätä hoitovasteen saavuttamista nivelpsoriaasia sairastavilla 6 kuukauden seurannassa (RR 1,76 (95 % luottamusväli 1,14–2,70))
- Metotreksaatti tehoaa myös ihopsoriaasiin (ks. kohta Ihopsoriaasin hoito, Ensisijaiset systeemiset lääkkeet «A8»7).
- Metotreksaatin hyötyosuus on parempi ihonalaisena pistoksena «Metotreksaatin hyötyosuus on parempi ihon alle tai lihakseen annosteltuna.»A.
- Kliinisen kokemuksen perusteella metotreksaatti on ensisijainen ja sillä saattaa olla
tehoa nivelpsoriaasin hoidossa, vaikka tutkimusnäyttö asiasta on edelleen vähäinen
«Metotreksaatti verrattuna lumeeseen saattaa nivelpsoriaasia sairastavilla lisätä hoitovasteen saavuttamista 6 kuukauden seurannassa (RR 1,76; 95 % luottamusväli 1,14–2,70).»C.
- Sulfasalatsiini «Sulfasalatsiinilääkityksessä huomioon otettavia asioita ...»18:
- Nivelpsoriaasin hoidossa sulfasalatsiini on heikkotehoinen «Sulfasalatsiini saattaa olla lumelääkettä tehokkaampi nivelpsoriaasin hoidossa, mutta tutkimusnäyttö siitä on vähäistä.»C, «Dressler C, Eisert L, Pham PA ym. Efficacy and saf...»257.
- Sulfasalatsiinia voidaan käyttää, jos metotreksaatti on vasta-aiheinen (esim. raskaus tai sen suunnittelu) ja sairaus on lieväoireinen.
- Ihopsoriaasiin sulfasalatsiini ei yleensä tehoa.
- Nivelpsoriaasin hoidossa sulfasalatsiini on heikkotehoinen «Sulfasalatsiini saattaa olla lumelääkettä tehokkaampi nivelpsoriaasin hoidossa, mutta tutkimusnäyttö siitä on vähäistä.»C, «Dressler C, Eisert L, Pham PA ym. Efficacy and saf...»257.
- Leflunomidi «Leflunomidilääkityksessä huomioon otettavia asioita ...»19:
- Yksittäistapauksissa leflunomidi on käyttökelpoinen lääke nivelpsoriaasiin «Leflunomidi saattaa olla tehokas ja turvallinen hoitovaihtoehto nivelpsoriaasissa.»C.
- Tutkimusnäyttö tehosta ihopsoriaasiin on kuitenkin vähäinen «Nash P, Thaçi D, Behrens F ym. Leflunomide improve...»258.
- Leflunomidi on pitkävaikutteisesti teratogeeninen lääke.
- Raskautta suunnittelevien naisten tulee lopettaa leflunomidin käyttö 2 vuotta aikaisemmin tai toteuttaa leflunomidin nopeutettu poisto kolestyramiinin tai lääkehiilen avulla «Flint J, Panchal S, Hurrell A ym. BSR and BHPR gui...»259. Miesten ei yhdessä kumppaninsa kanssa raskautta suunnitellessa ole välttämätöntä tauottaa leflunomidia «Brent RL. Teratogen update: reproductive risks of ...»260.
- Poistolääkityksen jälkeen tulee vielä tehdä 2 pitoisuuden määritystä plasmasta.
- Yksittäistapauksissa leflunomidi on käyttökelpoinen lääke nivelpsoriaasiin «Leflunomidi saattaa olla tehokas ja turvallinen hoitovaihtoehto nivelpsoriaasissa.»C.
- Kortikosteroidit:
- Kortikosteroidivalmisteita käytetään tarvittaessa paikallisesti niveliin ruiskutettuna tai pieninä annoksina (prednisoni ≤ 7,5 mg/päivä) suun kautta mahdollisimman lyhyinä kuureina.
- Ultraääniohjauksessa glukokortikoidipaikallishoidot ohjautuvat oikeaan kohteeseen.
- Suuriannoksisen systeemisen kortikosteroidilääkityksen äkillinen lopettaminen saattaa pahentaa ihopsoriaasia «Baker H, Ryan TJ. Generalized pustular psoriasis. ...»261, «Burns D, Breathnach S, Cox N ym. Rook´s Textbook o...»262.
- Hoidon haittavaikutuksista ks. Käypä hoito -suositus Nivelreuma «Nivelreuma»4.
| Aihe | Huomioon otettavia asioita |
|---|---|
| * Kaikkia mainittuja seurantakokeita ei välttämättä tarvitse ottaa jokaiselta potilaalta, vaan niiden laajuus arvioidaan yksilöllisesti. | |
| Annos | Aloitusannos 500 mg × 2, seuraavien viikkojen kuluessa tasolle 1 g × 2, tarvittaessa 1 g x 3/vrk |
| Haittavaikutukset | Tavalliset: vatsavaivat, lievät keskushermostoperäiset oireet, hoidon loputtua ohimenevä
oligospermia ja siittiöiden liikkuvuuden heikkeneminen Harvinaiset: vaikea yliherkkyysihottuma ja vakavat verenkuvamuutokset |
| Yhteisvaikutukset | – |
| Vasta-aiheet | Allergia valmistetta kohtaan Sulfa-allergiatapauksissa kannattaa tehdä altistus sairaalaoloissa. Voimakkaasti suurentuneet veren tumavasta-aineet suurentavat SLE-tyyppisen taudin puhkeamisen riskiä. |
| Hyödyllinen yhdistelmä | Foolihappolisä 1–5 mg/vrk raskauden aikana «Flint J, Panchal S, Hurrell A ym. BSR and BHPR gui...»259 «https://www.terveyskyla.fi/reumatalo»20 |
| Seurantakokeet* | PVK (TVK), ALAT viikoilla 3, 6 ja 12 ja jatkossa 3–6 kuukauden välein Ks. myös «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 |
| Aihe | Huomioon otettavia asioita |
|---|---|
| * Kaikkia mainittuja seurantakokeita ei välttämättä tarvitse ottaa jokaiselta potilaalta, vaan niiden laajuus arvioidaan yksilöllisesti. | |
| Annos | 20 mg/vrk |
| Haittavaikutukset | Verenpaineen nousu, päänsärky Ihottumat, hiustenlähtö Ripuli, pahoinvointi Maksa-arvojen muutokset, verisolujen väheneminen |
| Yhteisvaikutukset | Muut samanaikaisesti käytettävät maksa- ja luuydintoksiset lääkkeet |
| Vasta-aiheet | Allergia kyseiselle lääkkeelle, vaikea infektio, maksan toimintahäiriö, vaikea immuunijärjestelmän
puutostila, merkittävä luuytimen toimintahäiriö, keskivaikea tai vaikea munuaisten
toimintahäiriö Raskaus ja imetys (ks. taulukko «Systeeminen lääkehoito raskauden ja imetyksen aikana iho- ja nivelpsoriaasia sairastavilla ...»22) Hepatotoksisten reumalääkkeiden (esim. metotreksaatti) samanaikaista käyttöä ei suositella, mutta niitä voidaan erityistä huolellisuutta noudattaen käyttää erikoislääkärin seurannassa. |
| Seurantakokeet* | PVK (TVK), ALAT ja verenpaine viikoilla 3, 6, ja 12 ja jatkossa 3–6 kuukauden välein
Ks. myös «http://www.terveysportti.fi/xmedia/shp/shp01174/turvakokeet_ja_tulkinta.html»10, «https://www.terveyskyla.fi/reumatalo/l%C3%A4%C3%A4ke-ja-toimenpideohjeet/l%C3%A4%C3%A4kehoidon-seurantakokeet»11 |
Yleisperiaatteet biologisten lääkkeiden, JAK:n estäjien ja apremilastin käytöstä
- Yleisohjeet biologisten lääkkeiden käytöstä ovat kohdassa Yleisohjeet biologisten lääkkeiden käytöstä iho- ja nivelpsoriaasin hoidossa ja taulukossa Biologisessa lääkehoidossa huomioon otettavaa «Biologisessa lääkehoidossa huomioon otettavia asioita ...»8.
- Biologisista lääkkeistä nivelpsoriaasin hoidossa käytetään adalimumabia, bimekitsumabia, etanerseptia, golimumabia, guselkumabia, iksekitsumabia, infliksimabia, risankitsumabia, sekukinumabia, sertolitsumabipegolia, ustekinumabia ja abataseptia.
- Myyntiluvan saaneet biosimilaarit vastaavat teholtaan ja turvallisuudeltaan viitevalmisteita. ks. Fimean ohjeisto «http://www.fimea.fi/laaketurvallisuus_ja_tieto/biosimilaarit/fimean-kanta-biosimilaarien-vaihtokelpoisuuteen»18.
- Saatavilla olevien biosimilaarivalmisteiden käyttö on kustannusvaikuttavuuden näkökulmasta suositeltavaa. Ks. Suomen Reumatologisen Yhdistyksen kannanotto «https://www.reumatologinenyhdistys.fi/lausunnot/»21.
- Ks. apremilastin, JAK-estäjien ja biologisten lääkkeiden vaikuttavuuden (ACR50-vaste), kustannusten ja hoitovasteen kustannusten vertailu nivelpsoriaasin hoidossa «https://www.terveysportti.fi/apps/laake/laakekustannus/hoi50062»22 (vaatii käyttöoikeuden), lisätietoa «The number needed to treat (NNT) and cost per responder for systemic therapies for psoriatic arthritis»16 ja opasvideo taulukon lukemisesta «Hoitovasteen kustannukset Käypä hoito -suosituksissa: näin luen taulukoita (video)»17.
- Biologisten lääkkeiden, JAK:n estäjien ja apremilastin käyttöaiheena on nivelpsoriaasi,
jonka hoidossa ei ole ilmaantunut riittävää vastetta varsinaisiin reumalääkkeisiin,
kuten metotreksaattiin.
- Kun perinteisillä synteettisillä reumalääkkeillä ei saada riittävää hoitovastetta tai ne eivät sovi, suositellaan aloitettavaksi TNF:n estäjä tai IL-17:n salpaaja.
- Seuraavina vaihtoehtoina ovat IL-23:n estäjä, IL-12/23:n estäjä tai JAK:n estäjä.
- Jos mikään edellä kuvatuista vaihtoehdoista ei sovellu, kyseeseen tulevat apremilasti tai abatasepti.
- Kliinisen kokemuksen mukaan vaste on hyvä entesiiteissä, daktyliiteissä ja spondyloartropatioissa.
- TNF:n estäjien välillä ei ole todettu kliinisesti merkittävää eroa tehossa «Biologisten lääkkeiden ja kohdennettujen synteettisten reumalääkkeiden vertailua nivelpsoriaasin hoidossa»18.
- Biologisia lääkkeitä ei ole tutkimuksissa verrattu perinteisiin synteettisiin reumalääkkeisiin.
- Hoitovasteen arvioinnissa tulisi käyttää riittävän pitkää seuranta-aikaa (3–6 kuukautta)
ja kliinisesti merkittävää paranemistulosta.
- Useissa tutkimuksissa hoitovasteen ensisijaiseksi kriteeriksi on lääkeviranomaisen suosituksesta asetettu vain ACR20, mikä tulee huomioida tuloksia tarkasteltaessa (ks. Clinical Development Programs for Drugs, Devices, and Biological Products for the Treatment of Rheumatoid Arthritis (RA) «https://www.fda.gov/regulatory-information/search-fda-guidance-documents/clinical-development-programs-drugs-devices-and-biological-products-treatment-rheumatoid-arthritis»23). ACR-luokitus ei kuitenkaan huomioi daktyliittien, entesiittien tai spondyliittien vastetta hoitoon.
- Yleisen käytännön mukaan kliinisessä työssä hoitoa voidaan jatkaa, jos ACR50-vaste
saavutetaan.
- ACR-hoitovasteluokituksesta ks. «Arnett FC, Edworthy SM, Bloch DA ym. The American ...»269.
Taudin ilmenemismuoto ja hoidon valinta
- Hoidon valinnassa tulee ottaa huomioon taudin ilmenemismuodot. Ks. taulukko «Työryhmän arvio lääkkeiden tehosta nivelpsoriaasin hoidossa taudin eri ilmenemismuodoissa.
Hoidon valinnassa tulee ottaa huomioon myös muita seikkoja, kuten turvallisuus ja
taloudelliset seikat. Mukailtu lähteistä , , , , , , , , , , , ....»20
- Jos ihopsoriaasi on vaikea, IL-17:n tai IL-23:n estäjät ja lisäksi IL-12/23:n estäjä ovat ensisijaisia.
- Aksiaalisessa tautimuodossa suositellaan ensisijaisesti TNF:n ja IL-17:n estäjän käyttöä. Toissijaisena vaihtoehtona voidaan harkita JAK:n estäjiä.
- TNF:n estäjillä, lukuun ottamatta etanerseptiä, on näyttöä iriitin hoidossa «Brüner M, Dige A, Loft AG ym. Spondylitis-psoriasi...»301.
- Jos potilaalla on samanaikainen tulehduksellinen suolistosairaus, TNF:n estäjät ja IL12/23:n estäjät ovat ensisijaisia vaihtoehtoja.
- Elleivät lääketieteelliset syyt muuta edellytä, suositellaan ensisijaisesti valitsemaan hinnaltaan edullisin vaihtoehto.
- Ks. myös Yleisperiaatteet biologisten lääkkeiden, JAK:n estäjien ja apremilastin käytöstä «A11»8
| Ihopsoriaasi | Perifeerinen artriitti | Entesiitti | Daktyliitti | Aksiaalinen sairaus | Uveiitti | Tulehduksellinen suolistosairaus | Radiologinen progressio | |
|---|---|---|---|---|---|---|---|---|
| + = kliininen näyttö tehosta ? = liian vähän tai ristiriitaista tietoa – = ei suositella i*Muilla TNF:n estäjillä kuin etanerseptillä |
||||||||
| Metotreksaatti | ++ | + | - | - | - | + | + | - |
| Apremilasti | + | + | ++ | ++ | ? | ? | - | - |
| JAK:n estäjät | ++ | +++ | ++ | ++ | +++ | ? | ++ | ++ |
| TNF:n estäjät | ++ | +++ | ++ | ++ | +++ | +++* | +++* | ++ |
| IL-23:n estäjät | +++ | ++ | ++ | ++ | + | ? | + | + |
| IL-17:n estäjät | +++ | +++ | ++ | ++ | +++ | + | - | ++ |
| Ustekinumabi | ++ | ++ | ++ | ++ | ++ | ? | +++ | ++ |
| Abatasepti | - | + | ? | ? | - | ? | - | + |
Biologiset lääkkeet
- Adalimumabi (TNF:n estäjä) «TNF:n estäjähoidon toteutus ja haittavaikutukset ...»10:
- Annos pistetään ihon alle 2 viikon välein.
- Nivelpsoriaasissa adalimumabilla on tehoa «Adalimumabi verrattuna lumeeseen lisää ACR20-vasteen saavuttaneiden osuutta (noin 60 % vs. noin 15–30 %) nivelpsoriaasipotilailla, joiden tauti on keskivaikea tai vaikea.»A, «Mease P, Hall S, FitzGerald O ym. Tofacitinib or A...»267.
- Viikolla 24 ACR50-vasteen saavutti 39 %, kun lumehoidossa vastaava luku oli 6 %.
- ACR70-vaste on saavutettu 30 %:lla hoidetuista 48 viikon hoidon jälkeen «Gladman DD, Mease PJ, Ritchlin CT ym. Adalimumab f...»270.
- Haittatapahtumien määrä on vastannut lumehoitoa.
- Golimumabi (TNF:n estäjä) «TNF:n estäjähoidon toteutus ja haittavaikutukset ...»10:
- Annos pistetään ihon alle neljän viikon välein.
- Golimumabilla näyttää olevan tehoa nivelpsoriaasin hoidossa «Subkutaaninen golimumabi verrattuna lumeeseen ilmeisesti lisää ARC20-vasteen saavuttaneiden osuutta nivelpsoriaasia sairastavilla (noin 45–51 % riippuen annoksesta vs. noin 10 %) 14 viikon seurannassa.»B.
- ACR50-vasteen saavuttaa 24 viikon seurannassa 30–35 % potilaista «Mease PJ. Biologic Therapy for Psoriatic Arthritis...»271, «Ramiro S, Smolen JS, Landewé R ym. Pharmacological...»272.
- Yleisesti golimumabi on hyvin siedetty eikä tilastollista eroa haittavaikutusten osalta (vakavat haittavaikutukset mukaan luettuina) todettu hoito- ja lumeryhmien välillä.
- Kahden vuoden seurannassa yleisimmät haittavaikutukset olivat ylähengitystieinfektio ja nasofaryngiitti. Seuranta-aikana 6 potilasta 335:stä sai vakavaksi luokitellun infektion «Kavanaugh A, van der Heijde D, McInnes IB ym. Goli...»273.
- Viiden vuoden seurannassa ACR50-vasteen saavutti lumeryhmässä 43 %, 50 mg golimumabia saaneiden ryhmässä 48 % ja 100 mg golimumabia saaneiden ryhmässä 51 % «Kavanaugh A, McInnes IB, Mease P ym. Clinical effi...»274.
- Etanersepti (TNF:n estäjä) «TNF:n estäjähoidon toteutus ja haittavaikutukset ...»10:
- Annos pistetään ihon alle viikon välein.
- Nivelpsoriaasissa etanerseptilla on tehoa «Etanersepti verrattuna lumeeseen lisää ACR20-vasteen saavuttaneiden osuutta nivelpsoriaasia sairastavilla (noin 60 % vs. noin 15 %).»A.
- ACR50-vaste on saavutettu 44 %:lla hoidetuista 48 viikon seurannassa «Mease PJ, Goffe BS, Metz J ym. Etanercept in the t...»275, «Mease PJ, Kivitz AJ, Burch FX ym. Etanercept treat...»276.
- Kahden vuoden seurannassa teho on säilynyt sekä kliinisesti että radiologisesti «Etanersepti verrattuna lumeeseen lisää ACR20-vasteen saavuttaneiden osuutta nivelpsoriaasia sairastavilla (noin 60 % vs. noin 15 %).»A.
- Haittatapahtumien määrä on vastannut lumehoitoa.
- Infliksimabi (TNF:n estäjä) «TNF:n estäjähoidon toteutus ja haittavaikutukset ...»10:
- Nivelpsoriaasissa infliksimabilla on tehoa «Intravenous infliximab with the dose of 5mg/kg increases the proportion of patients with active psoriatic arthritis achieving the ACR20* response at week 16-24 (54-65%), when compared to placebo (10-16%), and it is safe.»A.
- ACR50-vasteen saavutti 24 viikon seurannassa noin 40 % potilaista, kun lumehoidossa vastaava luku oli 4 % «Antoni C, Krueger GG, de Vlam K ym. Infliximab imp...»277.
- ACR70-vasteen saavutti 54 viikon hoidon jälkeen 22 % «Kavanaugh A, Krueger GG, Beutler A ym. Infliximab ...»278.
- Haittatapahtumien määrä on vastannut lumehoitoa.
- Infliksimabi on tehokas myös hoitoresistenssissä mutiloivassa nivelpsoriaasissa «Feletar M, Brockbank JE, Schentag CT ym. Treatment...»279, «Kavanaugh A, Antoni CE, Gladman D ym. The Inflixim...»280.
- Nivelpsoriaasissa infliksimabilla on tehoa «Intravenous infliximab with the dose of 5mg/kg increases the proportion of patients with active psoriatic arthritis achieving the ACR20* response at week 16-24 (54-65%), when compared to placebo (10-16%), and it is safe.»A.
- Sertolitsumabipegoli (TNF:n estäjä) «TNF:n estäjähoidon toteutus ja haittavaikutukset ...»10:
- Annos pistetään ihon alle kahden viikon välein.
- Sertolitsumabipegolilla on ilmeisesti tehoa ACR20-vasteisiin ja toimintakykyyn nivelpsoriaasin
lyhytkestoisessa hoidossa «Sertolitsumabipegoli verrattuna lumeeseen näyttää parantavan ACR20-vasteita (sen saavuttaa noin 56–64 % vs. noin 24 %) ja toimintakykyä nivelpsoriaasin hoidossa 24 viikon seurannassa.»B.
- ACR50-vasteen saavutti viikon 24 kohdalla 200 mg sertolitsumabipegolia (2 x/kk) saaneiden ryhmässä 44 % potilaista, 400 mg (1 x/kk) sertolitsumabipegolia saaneiden ryhmässä 40 % ja lumeryhmässä noin 13 % «Mease PJ, Fleischmann R, Deodhar AA ym. Effect of ...»281.
- ACR70-vasteen saavutti 12 viikon hoidon jälkeen 25 % «Mease PJ. Biologic Therapy for Psoriatic Arthritis...»271, «Ramiro S, Smolen JS, Landewé R ym. Pharmacological...»282.
- Lyhytaikaisessa seurannassa haittatapahtumien määrä on vastannut lumehoitoa.
- ACR-vaste saattaa säilyä myös useita vuosia kestävässä hoidossa «van der Heijde D, Deodhar A, FitzGerald O ym. 4-ye...»283.
- Vuoden seurannassa vakavia haittatapahtumia, useimmiten infektioita, esiintyi noin viidenneksellä.
- Sertolitsumabipegoli ei siirry istukan läpi sikiöön. Se on ensisijainen biologinen lääke raskautta suunnittelevalle potilaalle.
- Guselkumabi (IL-23:n estäjä) «IL-12/23:n ja IL-23:n estäjähoidon toteutus ja haittavaikutukset ...»12:
- Lääke annetaan aluksi viikoilla 0 ja 4 ja siitä eteenpäin 8 viikon välein, mutta annostelua voidaan tarvittaessa tihentää myös 4:n viikon välein annettavaksi.
- Guselkumabilla on tehoa nivelpsoriaasin hoidossa «Subcutaneous guselkumab treatment at the dose of 100 mg every 4 or 8 weeks, when compared to placebo, increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 24 (52–64 % vs. 18–33 %).»A.
- Annoksella 100 mg joka 4 tai 8 viikko (s.c.) 24 viikon jälkeen ACR50-vasteen saavuttaa hieman yli 30 % potilaista, kun lumehoidossa vastaava luku on vaihdellut välillä 9–14 %.
- Haittatapahtumat ovat pääosin lieviä, ja niiden määrä näyttää vastaavan lumehoitoa.
- Risankitsumabi (IL-23:n estäjä) «IL-17:n estäjähoidon toteutus ja haittavaikutukset ...»11:
- Annos pistetään ihon alle hoidon aluksi viikoilla 0 ja 4 ja sen jälkeen vakiintuneessa käytössä 12 viikon välein.
- Risankitsumabilla on tehoa nivelpsoriaasin hoidossa «Subcutaneous risankizumab treatment at the dose of 150 mg at weeks 0, 4 and 16 increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 16 (50–60%), when compared to placebo (25–35%), and it is safe.»A, «Kristensen LE, Keiserman M, Papp K, ym. Efficacy a...»284, «Östör A, Van den Bosch F, Papp K, ym. Efficacy and...»285, «Mease PJ, Kellner H, Morita A, ym. Long-Term Effic...»286.
- Viikolla 24 ACR50-vasteen saavutti 26–33 %, kun lumehoidossa vastaava luku oli 9–11 %.
- Viikolla 24 ACR70-vasteen saavutti 12–15 %, kun lumehoidossa vastaava luku oli 5–6 %.
- Haittatapahtumat ovat pääosin lieviä, ja niiden määrä näyttää vastaavan lumehoitoa.
- Risankitsumabi vaikuttaa 52 viikon tutkimusten perusteella turvalliselta. Tavallisia haittoja ovat lisääntyneet ylähengitystieinfektiot «Östör A, Van den Bosch F, Papp K, ym. Efficacy and...»287.
- Ustekinumabi (IL-12/23:n estäjä) «IL-12/23:n ja IL-23:n estäjähoidon toteutus ja haittavaikutukset ...»12:
- Annos pistetään ihon alle vakiintuneessa käytössä 12 viikon välein ja hoidon aluksi viikoilla 0 ja 4.
- Ustekinumabilla näyttää olevan tehoa nivelpsoriaasin hoidossa «Nivelpsoriaasipotilaista, joiden hoitona on ustekinumabi (annoksella 45 mg ja 90 mg 12 viikon välein), noin 40–50 % näyttää saavuttavan ACR20-vasteen viikkoon 24 mennessä, kun lumehoidossa noin 20 % saavuttaa sen.»B.
- 24 viikon hoidon jälkeen 18–25 % potilaista saavutti ACR50-vasteen 45 mg annoksella ja 23–28 % potilaista 90 mg annoksella, kun lumeryhmässä vastaava luku oli 7–9 %.
- Vuoden kohdalla ACR50-vasteen saavutti kolmannes potilaista «McInnes IB, Kavanaugh A, Gottlieb AB ym. Efficacy ...»288.
- Teho näyttää säilyvän 2 vuoden seurannassa «Kavanaugh A, Puig L, Gottlieb AB ym. Maintenance o...»289.
- Erityisen tehokas ustekinumabi näyttää olevan daktyliittien ja entesiittien suhteen «Kavanaugh A, Puig L, Gottlieb AB ym. Maintenance o...»289, «Araujo EG, Englbrecht M, Hoepken S ym. Effects of ...»290
- 16 viikon seurannassa haittatapahtumien määrä oli samanlainen hoito- ja lumeryhmissä. Pitkäaikaisseurannassa ustekinumabin turvallisuusprofiili vaikuttaa hyvältä «Kavanaugh A, Puig L, Gottlieb AB ym. Maintenance o...»289, «Ruyssen-Witrand A, Perry R, Watkins C ym. Efficacy...»291
- Bimekitsumabi (IL-17:n estäjä) «IL-17:n estäjähoidon toteutus ja haittavaikutukset ...»11:
- Annos pistetään ihon alle 4 viikon välein.
- Bimekitsumabilla on tehoa nivelpsoriaasin hoidossa «Bimekizumab reduces symptoms of psoriatic arthritis and is safe to use. In the intervention group, 62-67% of participants achieved 20% reduction in symptom score (ACR20), compared to 16-20% in the control group.»A, «McInnes IB, Asahina A, Coates LC, ym. Bimekizumab ...»292, «Ritchlin CT, Kavanaugh A, Merola JF, ym. Bimekizum...»293, «Merola JF, Landewé R, McInnes IB, ym. Bimekizumab ...»294.
- Viikolla 16 ACR50-vasteen saavutti 43–44 %, kun lumehoidossa vastaava luku oli 7–10 %.
- Viikolla 16 ACR70-vasteen saavutti 24–27 %, kun lumehoidossa vastaava luku oli 1–4 %.
- 12–16 viikon seurannassa hoidosta aiheutuneet haittatapahtumat lisääntyivät lumeeseen verrattuna, mutta ne olivat pääosin ei-vakavia infektioita.
- Bimekitsumabi vaikuttaa 3 vuoden seurannan perusteella turvalliselta «Coates LC, McInnes IB, Merola JF, ym. Safety and E...»295.
- Iksekitsumabi (IL-17A:n estäjä):
- Lääkitys aloitetaan annoksella 160 mg ihon alle, minkä jälkeen jatketaan annoksella 80 mg ihon alle 4:n viikon välein. Jos ihon psoriaasi on vaikea, pistetään 80 mg:n annos viikoilla 2, 4, 6, 8, 10 ja 12. Sen jälkeen jatketaan annoksella 80 mg 4:n viikon välein.
- Iksekitsumabilla on tehoa nivelpsoriaasin hoidossa «Ixekizumab treatment at the dose of 80 mg, when compared to placebo, increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 24 and probably already at week 12.»A.
- 24 viikon seurannassa ACR50-vasteen saavutti iksekitsumabiryhmässä 35–45 % ja lumeryhmässä 5–15 %.
- 52 viikon seurannassa 49,8 % potilaista (n = 283) saavutti ACR50-vasteen «Smolen JS, Mease P, Tahir H ym. Multicentre, rando...»296.
- 24 viikon seurannassa haittatapahtumien määrä oli hieman suurempi hoito- kuin lumeryhmissä. Haittatapahtumat olivat pääosin lieviä.
- Suorassa vertailututkimuksessa iksekitsumabin teho ACR50-vasteeseen saattaa olla yhtäläinen adalimumabin kanssa «Smolen JS, Mease P, Tahir H ym. Multicentre, rando...»296.
- Sekukinumabi (IL-17A:n estäjä) «IL-17:n estäjähoidon toteutus ja haittavaikutukset ...»11:
- Vakiintuneessa käytössä 150–300 mg:n annos pistetään ihon alle kuukauden välein ja hoidon ensimmäisten 4 viikon aikana viikon välein.
- Sekukinumabilla näyttää olevan tehoa nivelpsoriaasin hoidossa «Subcutaneous secukinumab treatment at the dose of 150-300 mg monthly increases the proportion of patients with psoriatic arthritis achieving the ACR20 response at week 24 when compared to placebo (approximately 42–63 % vs. 15–27 %), and it is safe.»A.
- ACR50-vasteen saavutti 24 viikon seurannassa 35 % sekukinumabia 150 mg käyttäneistä, 31 % 75 mg käyttäneistä ja 7 % lumelääkeryhmästä «Mease PJ, McInnes IB, Kirkham B ym. Secukinumab In...»297.
- 24 viikon seurannassa vakavien haittatapahtumien määrä 150 mg sekukinumabia käyttäneiden potilaiden ryhmässä (329,7 potilasvuotta) oli 3,0 % ja lumeryhmässä (122,9 potilasvuotta) 3,6 % «Mease P, van der Heijde D, Landewé R ym. Secukinum...»298.
- Brodalumabi (IL-17:n estäjä) «IL-17:n estäjähoidon toteutus ja haittavaikutukset ...»11:
- 210 mg brodalumabia (s.c.) joka toinen viikko näyttää lumeeseen verrattuna lisäävän niiden nivelpsoriaasipotilaiden osuutta, jotka saavuttavat ACR20-vasteen viikon 24 seurannassa «Subcutaneous brodalumab treatment at the dose of 210 mg every other week increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at weeks 16 and 24, when compared to placebo (47.9 % vs.»B.
- Noin 20 % potilaista saavuttaa ACR50-vasteen 16 viikon seurannassa, kun vastaava luku lumehoidossa on alle 10 %.
- Yhdysvalloissa lääkkeen käyttöön liittyy varoitus ja seuranta mahdollisesti suurentuneen itsemurha-alttiuden osalta, mutta Euroopan lääkevirasto ei tällaista esitä. Jos potilaalla ilmenee hoidon aikana ahdistus- tai masennusoireita tai ne pahenevat hoidon aikana, hoito tulee keskeyttää.
- Brodalumabilla oli Suomessa toukokuussa 2021 käyttöaihe vain ihopsoriaasiin.
- Abatasepti (T-solujen estäjä)
- Lääke annetaan viikon välein ihon alle.
- Abataseptillä näyttää olevan tehoa nivelpsoriaasin hoidossa «Parenteral abatacept 125 mg per week treatment increases the ACR20 response at week 24 in patients with active psoriatic arthritis when compared to placebo.»B.
- 24 viikon seurannassa noin 20 % abataseptiä 125 mg viikossa käyttäneistä ja lumeryhmässä noin 12 % «Mease PJ, Gottlieb AB, van der Heijde D ym. Effica...»299 potilaista saavutti ACR50-vasteen.
- 24 viikon seurannassa haittatapahtumien määrä oli samanlainen hoito- ja lumeryhmissä.
- Abataseptillä on indikaatio ainoastaan nivelpsoriaasiin. Teho nivelten ulkopuolisiin oireisiin on vaatimaton.
- Biologisten lääkkeiden välillä ei ole merkittäviä eroja daktyliitin ja entesiitin
paranemisessa.
- Meta-analyysissä 24 viikon seurannassa RR oli daktyliittien osalta TNF:n estäjillä 2,57 (95 % luottamusväli 1,36–4,84) ja uusilla biologisilla lääkkeillä (ustekinumabi, sekukinumabi ja iksekitsumabi) 1,88 (1,33–2,65) lumeeseen verrattuna. Vastaavat luvut entesiiteillä olivat 1,93 (1,33–2,79) ja 1,95 (1,60–2,38) «Mourad A, Gniadecki R. Treatment of Dactylitis and...»300.
JAK:n estäjät
- JAK:n estäjät ovat tablettimuotoisia lääkkeitä, joita otetaan päivittäin. Vaikutusmekanismi perustuu januskinaasien ja JAK-STAT-signalointireitin estämiseen, mikä johtaa useiden sytokiinien vaikutuksen vähenemiseen.
- Tofasitinibi, ks. taulukko «Apremilastin ja JAK:n estäjien annostus ja seuranta nivelpsoriaasissa ...»21.
- Tofasitinibilla näyttää olevan tehoa nivelpsoriaasin hoidossa «Tofacitinib treatment at the dose of 5 mg twice daily, when compared to placebo, seems to increase the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 12 (50–60 % vs. 25–30 %).»B.
- Annoksella 5 mg kahdesti päivässä ACR50-vasteen näytti saavuttavan noin 30 % potilaista, kun lumehoidossa vastaava luku oli 12 viikon seurannassa noin 10 % «Nash P, Coates LC, Fleischmann R ym. Efficacy of T...»266.
- Teho näyttää säilyvän 1 vuoden seurannassa. Avoimessa jatkotutkimuksessa noin 40 % saavutti ACR50-vasteen «Mease P, Hall S, FitzGerald O ym. Tofacitinib or A...»267.
- Haittatapahtumat ovat pääosin lieviä, eikä niiden määrä eronnut lumeryhmästä 3 kuukauden seurannassa. Vuoden seurannassa 7 % tofasitinibilla hoidetuista sai vakavan haittatapahtuman (mm. vakavat infektiot, herpes zoster) ja 6 % keskeytti hoidon haittatapahtuman vuoksi «Mease P, Hall S, FitzGerald O ym. Tofacitinib or A...»267.
- Tofasitinibilla näyttää olevan tehoa nivelpsoriaasin hoidossa «Tofacitinib treatment at the dose of 5 mg twice daily, when compared to placebo, seems to increase the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 12 (50–60 % vs. 25–30 %).»B.
- Upadasitinibi, ks. taulukko «Apremilastin ja JAK:n estäjien annostus ja seuranta nivelpsoriaasissa ...»21:
- Upadasitinibilla näyttää olevan tehoa nivelpsoriaasin hoidossa «Oral upadacitinib treatment at the dose of 15 mg daily increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 12, when compared to placebo (approximately 57–71 % vs. 24–36 %, depending on patient population).»A.
- 12 viikon seurannassa upadasitinibia annoksella 15 mg kerran päivässä käyttäneistä potilaista (n = 429) 37,5 % saavutti ACR50-vasteen, kun lumeryhmässä (n = 423) saman vasteen saavutti 13,2 %.
- 21 viikon seurannassa upadasitinibia annoksella 15 mg kerran päivässä käyttäneiden potilaiden ryhmässä (n = 429) 67 % potilaista sai haittatapahtuman, kun lumeryhmässä (n = 423) haittatapahtuman sai noin 60 % potilaista.
- Avoimessa jatkotutkimuksessa viikon 24 jälkeen upadasitinibia saaneet jatkoivat aikaisempaa annosta ja lumeryhmään kuuluneet satunnaistettiin lääkeryhmiin (15 tai 30 mg) «Mease PJ, Lertratanakul A, Papp KA ym. Upadacitini...»268. Viikolla 56 ACR50-vasteen saavutti upadasitinibia annoksella 15 mg päivässä saaneista potilaista 40,8 % ja lumeryhmään kuuluneista ja 15 mg upadasitinibia saaneiden ryhmään siirtyneistä 33,0 %.
- 56 viikon seurannassa vakavia infektioita todettiin upadasitinibia 15 mg päivässä saaneilla 2,6/100 potilasvuotta ja 30 mg päivässä saaneilla 6,1/100 potilasvuotta.
- Upadasitinibilla näyttää olevan tehoa nivelpsoriaasin hoidossa «Oral upadacitinib treatment at the dose of 15 mg daily increases the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 12, when compared to placebo (approximately 57–71 % vs. 24–36 %, depending on patient population).»A.
- JAK:n estäjien käyttöön yli 65-vuotiailla potilailla liittyy vakavien infektioiden, sydäninfarktin ja syövän suurentunut riski. EMA:n suosituksen mukaan näitä valmisteita tulisi käyttää vain, jos muita sopivia hoitovaihtoehtoja ei ole «https://www.ema.europa.eu/en/medicines/human/referrals/janus-kinase-inhibitors-jaki»24.
Kohdennetut synteettiset reumalääkkeet (targeted synthetic disease-modifying antirheumatic drug, tsDMARD)
- Apremilasti on fosfodiesteraasi 4:n estäjä. Sen vaikutusmekanismi perustuu syklisen adenosiinimonofosfaatin estoon, jonka kautta vaikutus kohdistuu yhtä aikaa useisiin anti-inflammatorisiin sytokiineihin. Tablettimuotoinen lääkitys otetaan päivittäin.
- Apremilasti, ks. taulukko «Apremilastin ja JAK:n estäjien annostus ja seuranta nivelpsoriaasissa ...»21.
- Apremilastia voidaan harkita aikuisilla nivelpsoriaasissa silloin, kun ei voida käyttää
toisentyyppistä, tautiprosessia hidastaviin reumalääkkeisiin kuuluvaa lääkettä (sDMARD-
tai bDMARD-lääkettä) tai ne eivät ole tehonneet.
- Apremilastihoidolla on saavutettu annostuksen mukaan 16–24 viikon tutkimuksissa ACR20-vasteita
noin 40 %:lla potilaista, kun lumepotilaista vasteen saavutti noin 20 % «Apremilast treatment at the dose of 30 mg twice daily, when compared to placebo, may increase the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 16 to 24 from approximately 20% to 40%.»B.
- ACR50-vasteen saavutti alle 20 % potilaista, kun vastaava luku oli lumeryhmässä 5–7 %
- 1–5 vuoden seurannassa vaikutus näyttää säilyvän: 5 vuoden kohdalla 67 % apremilastia jatkavista potilaista säilytti ACR20- ja 44 % ACR50-vasteen, eikä pitkäaikaishaittoja havaittu «Kavanaugh A, Gladman DD, Edwards CJ ym. Long-term ...»263, «Nash P, Ohson K, Walsh J ym. Early and sustained e...»264, «Wells AF, Edwards CJ, Kivitz AJ ym. Apremilast mon...»265.
- 15–17 %:lla potilaista esiintyy hoidon alussa pahoinvointia tai ripulia.
- Apremilastihoitoon ei ole liittynyt infektioiden lisääntymistä, eikä sillä ole kuvattu elintoksisuutta.
- Erillistä laboratoriokoeseurantaa ei tarvita.
- Hoidon korvattavuus vaatii erillisen SvB-lausunnon.
- Apremilastihoidolla on saavutettu annostuksen mukaan 16–24 viikon tutkimuksissa ACR20-vasteita
noin 40 %:lla potilaista, kun lumepotilaista vasteen saavutti noin 20 % «Apremilast treatment at the dose of 30 mg twice daily, when compared to placebo, may increase the proportion of patients with active psoriatic arthritis achieving the ACR20 response at week 16 to 24 from approximately 20% to 40%.»B.
| Annos | Haitat | Seuranta | Vaikutuskohta | Huomioitavaa | |
|---|---|---|---|---|---|
| Apremilasti | Annoksen titraus asteittain 30 mg x 2 | Maha-suolikanavan oireet | Seurantakokeita ei tarvita | fosfodiesteraasi 4:n estäjä (PDE4) | |
| Tofasitinibi | 5 mg x 2 | Ylähengitystieinfektiot Päänsärky Lisääntynyt infektioalttius (erityisesti herpes zoster) Neutro- ja lymfopenia |
TVK, ALAT viikoilla 3, 6 ja 12 aloituksesta ja jatkossa 3–6 kuukauden välein, 3 kuukauden kohdalla lipidit |
Janus-kinaasi 1/3:n estäjä (JAK1/3) | Käyttöön yli 65-vuotiailla potilailla liittyy vakavien infektioiden, sydäninfarktin ja syövän suurentunut riski. |
| Upadasitinibi | 15 mg x 1 | Ylähengitystieinfektiot Pahoinvointi Lisääntynyt infektioalttius (erityisesti herpes zoster) Neutropenia |
TVK, ALAT viikoilla 3, 6 ja 12 aloituksesta ja jatkossa 3–6 kuukauden välein, 3 kuukauden kohdalla lipidit |
Janus-kinaasi 1 estäjä (JAK1) | Käyttöön yli 65-vuotiailla potilailla liittyy vakavien infektioiden, sydäninfarktin ja syövän suurentunut riski. |
Kirurginen hoito
- Hoito on samanlaista kuin nivelreumassa. Ks. Käypä hoito -suositus Nivelreuma «Nivelreuma»4).
Potilasnäkökulmia nivelpsoriaasin hoitoon
- Nivelpsoriaasi ja sen oireet voivat vaikuttaa niin fyysiseen, psyykkiseen kuin sosiaaliseenkin
elämänlaatuun «Sumpton D, Kelly A, Tunnicliffe DJ ym. Patients' P...»252, «Coates LC, Orbai AM, Azevedo VF ym. Results of a g...»253. Ks. lisätietoa «Nivelpsoriaasia sairastavien potilaiden kokemuksia ja näkemyksiä»15.
- Kyselytutkimuksen (n = 1 286, 8 maasta) mukaan lähes kaikki nivelpsoriaasipotilaat ilmoittivat kokeneensa edeltäneiden 12 kuukauden aikana tuki- ja liikuntaelimistön oireita. Yleisimpiä olivat nivelten kipu, arkuus ja turvotus «Coates LC, Orbai AM, Azevedo VF ym. Results of a g...»253.
- Kipujen lisäksi väsymys vaikuttaa voimakkaasti työ- ja toimintakykyyn ja sosiaalisiin suhteisiin.
- Potilaille merkityksellisiä hoidon tavoitteita ovat «Garrido-Cumbrera M, Hillmann O, Mahapatra R ym. Im...»254
- kipujen hallinta
- väsymyksen hallinta ja tavanomaisen sosiaalisen, fyysisen ja psyykkisen toimintakyvyn ylläpitäminen
- työkyvyn ylläpitäminen
- ihopsoriaasin aiheuttaman taakan vähentäminen.
Nivelpsoriaasin kuntoutus
- Kuntoutuksen tavoitteena on hoidon tavoin edistää potilaan toiminta- ja työkykyä sekä hyvinvointia. Hoito ja kuntoutus tukevat toisiaan.
- Nivelreuman Käypä hoito -suosituksessa on käsitelty nivelreuman kuntoutusta. Samat periaatteet pätevät nivelpsoriaasin kuntoutukseen. Ks. Käypä hoito -suositus Nivelreuma, kappale: Nivelreuman hoito, Kuntoutus «Nivelreuma»4.
- Ks. Myös Terveyskylän Kuntoutumistalo «https://www.terveyskyla.fi/kuntoutumistalo»25.
Erityistapaukset
Psoriaasi ja raskaus
- Psoriaasi ei heikennä fertiliteettiä, joten hedelmällisessä iässä olevien naisten psoriaasin hoidossa tulee aina ottaa huomioon raskauden mahdollisuus «Tauscher AE, Fleischer AB Jr, Phelps KC ym. Psoria...»310, «Hale EK, Pomeranz MK. Dermatologic agents during p...»311.
- Raskauden aikana 30–63 %:lla potilaista ihopsoriaasi lievittyy, minkä jälkeen se taas
synnytyksen jälkeen vaikeutuu «Murase JE, Chan KK, Garite TJ ym. Hormonal effect ...»312, «Raychaudhuri SP, Navare T, Gross J ym. Clinical co...»313, «Gudjonsson JE, Karason A, Runarsdottir EH ym. Dist...»314, «Yang YW, Chen CS, Chen YH ym. Psoriasis and pregna...»315.
- Taustalla on alttiusgeeneihin liittyviä eroja «Gudjonsson JE, Karason A, Runarsdottir EH ym. Dist...»314 ja sukupuolihormonien immuunijärjestelmää vaimentava vaikutus «Tauscher AE, Fleischer AB Jr, Phelps KC ym. Psoria...»310, «Raychaudhuri SP, Navare T, Gross J ym. Clinical co...»313, «Mowad CM, Margolis DJ, Halpern AC ym. Hormonal inf...»316.
- Psoriaasi voi pienellä osalla potilaista myös vaikeutua raskauden aikana.
- Nivelpsoriaasi pysyy raskauden aikana usein rauhallisena «Ursin K, Lydersen S, Skomsvoll JF ym. Psoriatic Ar...»317. Kliinisen kokemuksen mukaan sakroiliitin oireet saattavat aktivoitua varsinkin II ja III kolmanneksen aikana ja pian synnytyksen jälkeen.
- Vaikea psoriaasi saattaa vaikuttaa raskauden kulkuun (ennenaikainen synnytys, keisarileikkaus,
pre-eklampsia ja eklampsia) ja lopputulokseen (pieni syntymäpaino) «Yang YW, Chen CS, Chen YH ym. Psoriasis and pregna...»315, «Bobotsis R, Gulliver WP, Monaghan K ym. Psoriasis ...»318.
- Riskit liittyvät ilmeisesti tautiprosessiin, koska niillä potilailla, joita hoidettiin raskauden aikana systeemisillä lääkkeillä, näitä riskejä ei ollut osoitettavissa «Yang YW, Chen CS, Chen YH ym. Psoriasis and pregna...»315.
- Raskausriskejä suurentaviin elintapa- ym. tekijöihin pitää pyrkiä vaikuttamaan «Bandoli G, Johnson DL, Jones KL ym. Potentially mo...»319.
- Psoriaasin hoidossa raskauden, imetyksen tai lapsen siittämisen aikana on huomioitava lääkkeiden vasta-aiheet «Systeeminen lääkehoito raskauden ja imetyksen aikana iho- ja nivelpsoriaasia sairastavilla ...»22.
- Miesten ei tarvitse tauottaa (reumatologisilla annoksilla käytettävää) metotreksaattia, siklosporiinia, leflunomidia, apremilastia, tofasitinibiä, upadasitinibiä tai biologisia lääkkeitä perheenlisäystä suunniteltaessa. Sulfasalatsiini voi heikentää miesten hedelmällisyyttä, mutta vaikutus on ohimenevä ja häviää tyypillisesti 2 viikon–2 kuukauden kuluessa lääkkeen käytön lopettamisesta. Ks. «https://www.terveyskyla.fi/reumatalo»20.
- Lievän ihopsoriaasin hoitoon suositellaan ensisijaisesti perusvoiteita ja mietoja
tai keskivahvoja kortikosteroidivoiteita «Bae YS, Van Voorhees AS, Hsu S ym. Review of treat...»320, «Chi CC, Kirtschig G, Aberer W ym. Evidence-based (...»321.
- Vahvojen tai erittäin vahvojen kortikosteroidivoiteiden laaja-alaista tai pitkäaikaista käyttöä ei suositella, koska niiden käyttö saattaa haitata sikiön kasvua ja suurentaa pienen syntymäpainon riskiä «Chi CC, Wang SH, Wojnarowska F ym. Safety of topic...»322.
- Laaja-alaisessa ihopsoriaasissa ensisijainen hoito raskauden aikana on UVB-valohoito
«Bae YS, Van Voorhees AS, Hsu S ym. Review of treat...»320. Vaikean ihopsoriaasin hoidossa voidaan harkitusti ja tarkkaan seuraten käyttää siklosporiinia
ja erityistapauksissa TNF:n estäjiä «Götestam Skorpen C, Hoeltzenbein M, Tincani A ym. ...»164 sekä raskausajan yleistyneen pustuloivan psoriaasin hoidossa systeemistä kortikosteroidia
(II–III kolmanneksen aikana) «Bae YS, Van Voorhees AS, Hsu S ym. Review of treat...»320.
- Yleensä suositellaan, että TNF:n estäjähoito lopetettaisiin jo raskautta suunniteltaessa. Altistuminen alkuraskauden aikana ei kuitenkaan ole aihe keskeytysharkintaan eikä erityistason sikiödiagnostiikkaan.
- Sertolitsumabipegoli on turvallinen TNF:n estäjä raskauden aikana, ja sitä voidaan tarvittaessa käyttää läpi koko raskaus- ja imetysajan.
- Muu TNF:n estäjähoito suositellaan mahdollisuuksien mukaan lopetettavan viimeistään raskausviikolla 20–22 (adalimumabi, infliksimabi) tai 30–32 (etanersepti) «Götestam Skorpen C, Hoeltzenbein M, Tincani A ym. ...»164.
- Lievän nivelpsoriaasin hoidossa voidaan käyttää parasetamolia kipulääkkeenä koko raskauden ajan, kuitenkin mahdollisuuksien mukaan välttäen säännöllistä ja pitkäaikaista käyttöä, ja kortikosteroidipistoksia. Tulehduskipulääkkeitä voi käyttää rajallisesti I–II kolmanneksen aikana.
- Lieväoireisen nivelpsoriaasin ensisijainen systeeminen lääke raskauden aikana on sulfasalatsiini.
- Kun äidin taudin hoito sitä edellyttää, voidaan harkita biologista lääkitystä, ensisijaisesti sertolitsumabipegolia «Clowse ME, Förger F, Hwang C ym. Minimal to no tra...»323, «Mariette X, Förger F, Abraham B ym. Lack of placen...»324.
- Vaikea, systeemistä lääkitystä vaativa ihopsoriaasi ja nivelpsoriaasi hoidetaan aina erikoissairaanhoidossa.
- Erikoissairaanhoidon konsultaatioon tulee lähettää jo ennen raskautta ne nivelpsoriaasipotilaat,
jotka käyttävät systeemisiä lääkkeitä.
- Naisten tulee tauottaa metotreksaattihoito 3 kuukautta ennen raskautta. Alkuraskauden
aikainen altistuminen metotreksaatille suurentaa epämuodostumariskiä. Altistuminen
organogeneesivaiheessa on aihe tarkkaan erikoislääkärin tai sikiötutkimusyksikön suorittamaan
rakenneultraäänitutkimukseen.
- Miesten ei ole välttämätöntä tauottaa leflunomidia raskautta suunniteltaessa. Varoajoista ks. taulukko «Systeeminen lääkehoito raskauden ja imetyksen aikana iho- ja nivelpsoriaasia sairastavilla ...»22.
- Tarvittaessa konsultoidaan Teratologista tietopalvelua. Ks. «http://www.hus.fi/»26.
- Naisten tulee tauottaa metotreksaattihoito 3 kuukautta ennen raskautta. Alkuraskauden
aikainen altistuminen metotreksaatille suurentaa epämuodostumariskiä. Altistuminen
organogeneesivaiheessa on aihe tarkkaan erikoislääkärin tai sikiötutkimusyksikön suorittamaan
rakenneultraäänitutkimukseen.
| Hoito | Raskaus | Lisätietoa | Imetys |
|---|---|---|---|
| Miesten ei tarvitse tauottaa (reumatologisilla annoksilla käytettävää) metotreksaattia, siklosporiinia, leflunomidia, apremilastia, tofasitinibiä, upadasitinibiä tai biologisia lääkkeitä perheenlisäystä suunniteltaessa. Sulfasalatsiini voi heikentää miesten hedelmällisyyttä, mutta vaikutus on ohimenevä ja häviää tyypillisesti 2 viikon–2 kuukauden kuluessa lääkkeen käytön lopettamisesta «https://www.terveyskyla.fi/reumatalo»20 | |||
| Systeemiset kortikosteroidit | Sallittu | Pienin mahdollinen annos erityisesti I kolmanneksen aikana | Sallittu |
| Parasetamoli | Sallittu | Mahdollisuuksien mukaan välttäen säännöllistä ja pitkäaikaista käyttöä | Sallittu |
| Tulehduskipulääkkeet | |||
| epäselektiiviset | Harkittavissa | Säännöllistä käyttöä on mahdollisuuksien mukaan syytä välttää I raskauskolmanneksen aikana. Loppuraskauden aikana lääkettä ei tule käyttää toistuvasti tai säännöllisesti edes lyhyesti. | Sallittu |
| COX-2:n estäjät selektiiviset | Kielletty | Selekoksibi sallittu | |
| Ensisijaiset systeemiset lääkkeet | |||
| Asitretiini | Kielletty | Teratogeeninen, varoaika 3 v | Kielletty |
| Leflunomidi | Kielletty | Huom. poistamismenetelmä | Kielletty |
| Metoksisaleeni | Ei suositella | Riittämättömästi tietoa | Ei suositella |
| Metotreksaatti | Kielletty | Teratogeeninen, varoaika 3 kk | Kielletty |
| Siklosporiini | Sallittu | Sallittu | |
| Sulfasalatsiini | Sallittu | Foolihappolisä 0,4–1 mg/vrk raskauden aikana suositeltava «Flint J, Panchal S, Hurrell A ym. BSR and BHPR gui...»259 | Sallittu |
| Toissijaiset systeemiset lääkkeet | |||
| Adalimumabi | Harkittavissa | Pyrittävä lopettamaan raskausviikkoon 20 mennessä | Sallittu |
| Abatasepti | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Apremilasti | Kielletty | Kielletty | |
| Bimekitsumabi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Brodalumabi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Dimetyylifumaratti | Kielletty | Kielletty | |
| Etanersepti | Harkittavissa | Pyrittävä lopettamaan raskausviikkoon 30–32 mennessä | Sallittu |
| Golimumabi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Guselkumabi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Iksekitsumabi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Infliksimabi | Harkittavissa | Pyrittävä lopettamaan raskausviikkoon 20 mennessä | Sallittu |
| Risankitsumabi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Sekukinumabi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Sertolitsumabipegoli | Sallittu | Ei läpäise istukkaa eikä mene rintamaitoon | Sallittu |
| Tildrakitsumabi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Tofasitinibi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Upadasitinibi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
| Ustekinumabi | Ei suositella | Toistaiseksi vähän kokemusta | Ei suositella |
Lasten ihopsoriaasin hoito
- Tyypillinen pienten lasten psoriaasin muoto on ohuthilseinen läiskäpsoriaasi kasvoissa,
hiuspohjassa ja vaippa-alueella (kuvat «Psoriaasi lapsen kasvoilla»62 ja «Lapsen psoriaasi-ihottuma»63).
- Pisarapsoriaasi (psoriasis guttata) on pikkulapsilla melko harvinainen mutta teini-ikäisillä yleisempi «Morris A, Rogers M, Fischer G ym. Childhood psoria...»326.
- Keskivaikea tai vaikea ihopsoriaasi heikentää lapsipotilaiden terveyteen liittyvää elämänlaatua enemmän kuin diabetes ja yhtä paljon kuin astma tai niveltulehdus «Varni JW, Globe DR, Gandra SR ym. Health-related q...»327.
- Hoidossa on muistettava lapsipotilaan ja hänen perheensä psykososiaalinen tuki. Lasten
psoriaasin paikallishoidossa on huomioitava
- systeemisen imeytymisen mahdollisuus (merkittävä etenkin vaippa-aluetta hoidettaessa) «Siegfried EC. Neonatal skin and skin care. Dermato...»328, «Chiou YB, Blume-Peytavi U. Stratum corneum maturat...»329, «Lebwohl M, Ali S. Treatment of psoriasis. Part 1. ...»330
- odotettavissa oleva pitkä sairastamisaika ja sen myötä mahdollisesti ilmenevät hoitojen haitat.
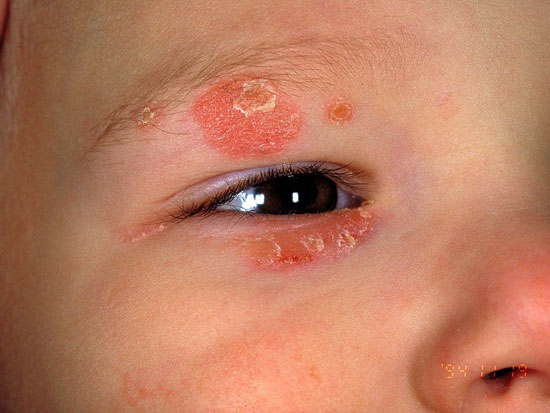
Psoriaasi lapsen kasvoilla
© Raimo Suhonen
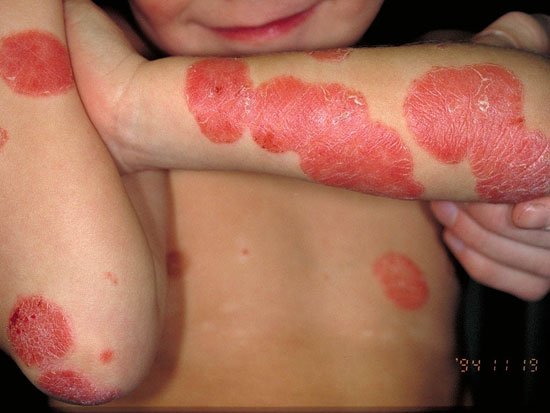
Lapsen psoriaasi-ihottuma
© Raimo Suhonen
Paikallishoito
- Ks. myös kohta Ihopsoriaasin hoito/Paikallishoito «A7»9.
- Keratolyytit:
- Ureaa tai maitohappoa (3–5 % rasvaisessa perusvoidepohjassa) sisältävät ex tempore -valmisteet ovat käyttökelpoisia.
- Salisyylihappovalmisteet:
- Lasten hoidossa on huomioitava salisylismiriski. Ks. Kliinisen farmakologian konsultaatio nro 3208 Salisylaattivoiteiden käytön turvallisuus lapsilla «hoi50062c.pdf»6.
- Alle kouluikäisillä valmisteita käytetään vain pienille ihoalueille (esim. hiuspohjaan) ja korkeintaan 0,5 %:n vahvuisina «Sticherling M, Augustin M, Boehncke WH ym. Therapy...»331.
- Alle 2-vuotiailla valmisteita ei käytetä. Ks. Kliinisen farmakologian konsultaatio nro 3208 Salisylaattivoiteiden käytön turvallisuus lapsilla «hoi50062c.pdf»6.
- Kortikosteroidivoiteet:
- Käyttö tulee rajata vain akuutin tulehduksellisen vaiheen hoitoon.
- Kortikosteroidivoiteita käytetään ryhmän I–II (III) kortikosteroidivoiteita (mietoja valmisteita suosien).
- Kortikosteroidivoiteiden toistuvaa käyttöä tulee karttaa «Kortikosteroidivoiteet psoriaasin hoidossa»4.
- D-vitamiinijohdokset:
- Kalsipotriolivoide on lumevoiteeseen verrattuna melko tehokas «Kalsipotrioli saattaa olla tehokas (PASI-alenema 60 %) lasten psoriaasin paikallishoidossa.»C.
- Usean viikon hoidolla (8–40 viikkoa) PASI-pienenemä on noin 60 %.
- Kalsipotriolivoidetta käytetään enintään 30 %:lla ihon pinta-alasta.
- Suositeltuja annoksia ei tule ylittää.
- Kalsipotriolivoiteen käyttömäärä yli 12-vuotiailla lapsilla ei saa ylittää 75:tä grammaa eikä 6–12-vuotiailla 50:tä grammaa viikossa.
- Alle 6-vuotiailla kalsipotriolivoidetta käytetään vain erikoislääkärin seurannassa.
- Saatavuus rajoittaa käyttöä.
- Kalsitriolivalmisteen käyttöä alle 18-vuotiaiden hoidossa ei ole tutkittu luotettavasti, mutta sen hoitovaste ja turvallisuus todennäköisesti vastaavat kalsipotriolia «de Jager ME, de Jong EM, van de Kerkhof PC ym. Eff...»332.
- Kalsipotriolivoide on lumevoiteeseen verrattuna melko tehokas «Kalsipotrioli saattaa olla tehokas (PASI-alenema 60 %) lasten psoriaasin paikallishoidossa.»C.
- Kalsineuriinin salpaajat:
- Takrolimuusi 0,1 %:n vahvuisena näyttää olevan tehokas ja turvallinen hoitovaihtoehto lapsipotilailla varsinkin kasvo- ja taivealueiden psoriaasin hoidossa «de Jager ME, de Jong EM, van de Kerkhof PC ym. Eff...»332. Takrolimuusivalmisteista ei saa sairausvakuuskorvausta, kun käyttöaiheena on psoriaasi.
UV-valohoito
- Tehoa lasten psoriaasin hoidossa ei ole selvitetty kontrolloiduin tutkimuksin, mutta hoitovaste ja haitat todennäköisesti vastaavat aikuisilla saatuja tuloksia.
- Lasten valohoidon pitkäaikaisturvallisuudesta ei ole luotettavaa tutkimusnäyttöä.
- Valohoitoa (UVB-hoidot tai SUP) voidaan käyttää harkitusti erikoislääkärin valvonnassa «Jury CS, McHenry P, Burden AD ym. Narrowband ultra...»333, «Pasic A, Ceovic R, Lipozencic J ym. Phototherapy i...»334.
Systeemiset ja biologiset lääkkeet
- Ks. taulukko «Lasten ihopsoriaasin hoitoon käytettäviä biologisia lääkkeitä ...»9.
- Hoito räätälöidään yksilöllisesti erikoislääkärin valvonnassa.
- Systeemihoitoja, kuten asitretiinia tai metotreksaattia, saatetaan poikkeustapauksissa tarvita lapsen psoriaasin hoidossa. Tarvittaessa hoito toteutetaan yhteistyössä lastenlääkärin kanssa.
- Biologisista lääkkeistä lapsilla voidaan tarvittaessa käyttää adalimumabia 4 vuoden iästä, etanerseptiä 6 vuoden iästä ja ustekinumabia 12 vuoden iästä alkaen «Paller AS, Siegfried EC, Langley RG ym. Etanercept...»335, «Paller AS, Siegfried EC, Eichenfield LF ym. Long-t...»336, «Paller AS, Siegfried EC, Pariser DM ym. Long-term ...»337, «Landells I, Marano C, Hsu MC ym. Ustekinumab in ad...»338.
Lasten nivelpsoriaasi
Kriteerit ja luokittelu
- Lastenreuman ILAR (International League of Associations for Rheumatology) -kriteerit täyttyvät, kun niveltulehdus on todettu alle 16 vuoden iässä, se on kestänyt vähintään 6 viikkoa eikä sille ole osoitettavissa erityistä syytä. Lastenreuma jaetaan luokittelukriteerien mukaisesti kuuteen spesifiseen alatyyppiin ja luokittelemattomaan ryhmään «Petty RE, Southwood TR, Manners P ym. Internationa...»339.
- Lasten nivelpsoriaasi on yksi lastenreuman alatyypeistä. Voimassa olevat ILAR-kriteerit
ovat seuraavat:
- Lastenreumapotilaalla on artriitti ja ihopsoriaasi tai artriitti ja 2 seuraavista:
- daktyliitti
- psoriasikseen sopivat kynsimuutokset
- 1. asteen sukulaisen psoriaasi.
- Poissulkukriteerejä ovat muuhun spesifiseen lastenreumatyyppiin, kuten lasten entesiittiartriittiin,
tai yleisoireiseen tai seropositiiviseen lastenreumaan, viittaavat kriteerit:
- RF+
- poika, joka on sairastunut yli 6 vuoden Iässä ja HLA-B27+
- 1. asteen sukulaisen HLA-B27+:aan liittyvä (spondyloartriitti) sairaus
- kahden alatyypin kriteerien täyttyminen.
- Lastenreumapotilaalla on artriitti ja ihopsoriaasi tai artriitti ja 2 seuraavista:
- Lastenreuman luokittelukriteereitä on ehdotettu muokattavaksi, koska osalla potilaista
on piirteitä useista tautityypeistä ja poissulkukriteerejä huolellisesti käytettäessä
jopa 20–30 % lastenreumapotilaista jäisi luokittelematta.
- Poissulkukriteerien vaikutusta lastenreuman alatyyppiin on tutkittu kanadalaisessa 162 lastenreumapotilaan aineistossa. Lastenreumapotilaan ensimmäisen asteen sukulaisten psoriaasi oli 67 %:lla (57/85) syynä potilaiden joutumiselle määrittämättömään lastenreumaluokkaan. Jos ensimmäisen asteen sukulaisten psoriaasi jätettiin kriteerinä huomiotta, 14,3 %:ia (11/77) potilaista ei enää luokiteltu lasten nivelpsoriaasiluokkaan.
- Lasten nivelpsoriaasia on pidetty taudinkuvaltaan hyvin monimuotoisena, eikä sen ole
aiemmin havaittu eroavan ennusteeltaan ja piirteiltään (ilmiasu, taudinkulku, uveiitin
esiintyminen, hoitovaste ja ennuste) selvästi muista lastenreuman alatyypeistä «Butbul Aviel Y, Tyrrell P, Schneider R ym. Juvenil...»340.
- Pohjoismaisessa tutkimuksessa lasten nivelpsoriaasin ennuste oli kuitenkin muihin lastenreumatyyppeihin verrattuna huonompi ja sairaus oli harvemmin remissiossa kuin muissa tyypeissä. Huonon ennusteen merkkejä olivat ihopsoriaasi, daktyliitti, suurempi tulehtuneiden nivelten määrä ja 1. asteen sukulaisen psoriaasi «Ekelund M, Aalto K, Fasth A ym. Psoriasis and asso...»341.
- Lasten nivelpsoriaasissa on erotettavissa kaksi iänmukaista alaryhmää, joista molemmissa on paljon daktyliitteja, mikä erottaa ne muista lastenreuman alatyypeistä.
- Varhain alkava tautimuoto muistuttaa tumavasta-ainepositiivisia lastenreuman alatyyppejä, kun taas myöhään alkavassa tautimuodossa on spondyloartriitin piirteitä ja se muistuttaa aikuisten spondyloartropatiaryhmän nivelpsoriaasia.
- Yhden tutkimuksen mukaan alle 5-vuotiaiden nivelpsoriaasiin sairastuneiden ryhmässä oligoartriitin ja nivelpsoriaasin kategoriat olivat taudinkuvaltaan selvästi erilliset, vaikka niillä olikin päällekkäisyyttä «Stoll ML, Nigrovic PA, Gotte AC ym. Clinical compa...»342.
- Amerikkalainen lasten nivelpsoriaasiaineisto vahvisti ajatusta kahdesta erilaisesta taudinkuvasta alle ja yli 4-vuotiailla. ILAR-kriteerien mukaisesti määriteltynä ei voitu diagnosoida kaikkia sellaisia lasten nivelpsoriaasitapauksia, jotka diagnosoitiin aikuisten CASPAR-kriteereillä. Tämä johtuu lähinnä lasten entesiittiartriittiin liittyvistä poissulkukriteereistä «Zisman D, Gladman DD, Stoll ML ym. The Juvenile Ps...»343.
Erityispiirteitä
- Lasten nivelpsoriaasissa niveltulehdus edeltää psoriaasin ihoilmentymää usein monien vuosien ajan. Kanadalaisessa 119 potilaan aineistossa psoriaasi-ihottuma edelsi niveltulehdusta 32 %:lla potilaista, 29 %:lla manifestaatiot todettiin samanaikaisesti ja 39 %:lla iho-oireet ilmaantuivat vuosia myöhemmin «Butbul Aviel Y, Tyrrell P, Schneider R ym. Juvenil...»340.
- Daktyliittia esiintyy 20–40 %:lla tai jopa useammalla, jos sairaus alkaa ennen 6 vuoden ikää «Stoll ML, Zurakowski D, Nigrovic LE ym. Patients w...»344.
- Lasten nivelpsoriaasissa voidaan erottaa lastenreuman muita eri alatyyppejä «Butbul Aviel Y, Tyrrell P, Schneider R ym. Juvenil...»340.
- Yleisin (55 %) alatyyppi oli oligoartrikulaarisena alkava tauti. Se laajeni polyartrikulaariseksi kolmasosassa tapauksista.
- Polyartriittimuotoisen taudinkulun tyypissä (laajentunut oligoartritti mukaan luettuna) (46 %) taudinkulku oli vaikeampi ja ennuste huonompi kuin muissa alaryhmissä. Lapsilla todettiin useammin kontraktuuria ja tarvittiin pidempi aika saavuttaa inaktiivinen tauti. Tälle tautityypille tyypillisiä ilmentymiä olivat symmetriset pienten nivelten tulehdukset, ranneniveltulehdukset ja DMARD-hoidon tarve.
- Entesiittityyppisen lastenreuman piirteet (mm. sakroiliitti ja' lonkkanivelen tulehdus) oli 13 %:lla potilaista.
Hoito
- Lasten nivelpsoriaasin hoito toteutetaan yksilöllisesti erikoislääkärin valvonnassa
samoin periaattein kuin muidenkin lastenreuman alatyyppien hoito «Kröger L, Vähäsalo P, Tynjälä P ym. [Medical treat...»345.
- Nivelpsoriaasia sairastavia lapsia ei ole tutkittu erikseen, vaan heitä on mukana joissakin lastenreuman hoitotutkimuksissa. Lasten nivelpsoriaasin hoidossa sovelletaan lastenreuman tutkimuksissa saatuja tuloksia.
- Aineistot ovat pieniä, ja tavoitteena on yleensä tutkia lääkkeen turvallisuutta.
- Hoitovasteen arvioinnissa tulisi käyttää kliinisesti merkittävää paranemistulosta.
- Lasten rokotuksista tärkein ero aikuisten ohjeistoon verrattuna on se, että lapsille pyritään antamaan ainakin elävät primaarirokotteet (MPR ja tarvittaessa vesirokkorokote) ennen metotreksaatin aloitusta.
- Metotreksaatti:
- Metotreksaatti on lastenreuman hoidon ensisijainen lääke,
- kun oligoartriittimuotoisessa taudissa pelkillä nivelten sisäisillä pistoksilla ja tulehduskipulääkkeillä ei saada riittävää hoitovastetta,
- useimmiten kun kyse on polyartriittimuotoisesta taudista.
- Metotreksaatista ei ole erikseen tutkimusnäyttöä lasten nivelpsoriaasissa. Se on osoitettu tehokkaaksi sekä suun kautta että ihonalaisesti annosteltuna, mutta sen haitat lisääntyvät annoksen suurentamisen myötä «Ruperto N, Murray KJ, Gerloni V ym. A randomized t...»346.
- Ks. myös taulukko «Metotreksaattilääkityksessä huomioon otettavia asioita ...»4 Metotreksaattilääkityksessä huomioon otettavia asioita.
- Metotreksaatti on lastenreuman hoidon ensisijainen lääke,
- Sulfasalatsiini:
- Sulfasalatsiinista ei ole erikseen tutkimusnäyttöä lasten nivelpsoriaasissa, mutta se on tehokas lastenreuman hoidossa «van Rossum MA, Fiselier TJ, Franssen MJ ym. Sulfas...»347.
- Leflunomidi:
- Lastenreumassa leflunomidi saattaa olla lähes yhtä tehokas kuin metotreksaatti «Silverman E, Mouy R, Spiegel L ym. Leflunomide or ...»348.
- Hydroksiklorokiini:
- Hydroksiklorokiinia käytetään joskus lastenreumassa lähinnä lievissä tautimuodoissa ja yhdistelmähoitona muiden reumalääkkeiden kanssa.
- Kortikosteroidit:
- Lastenreumassa kortikosteroidivalmisteita käytetään tarvittaessa paikallisesti niveliin pistettyinä ja suun kautta pieninä annoksina vaikeissa tautimuodoissa siltahoitona lääkkeiden aloituksissa ja vaihdoissa tai kaularanka-artriitin hoidossa.
- Biologiset lääkkeet:
- Lapsilla Suomessa virallinen käyttöaihe muissa kuin yleisoireisessa lastenreuman tautityypissä on adalimumabilla, etanerseptilla, golimumabilla, tosilitsumabilla (IL-6:n salpaaja), sekukinumabilla (IL-17A:n estäjä) ja abataseptillä. Yleisesti käytetään myös infliksimabia «Tynjälä P, Vähäsalo P, Tarkiainen M ym. Aggressive...»349.
- Adalimumabi:
- Adalimumabi on tehokas lastenreuman hoidossa erityisesti metotreksaattiin yhdistettynä «Lovell DJ, Ruperto N, Goodman S ym. Adalimumab wit...»350.
- Lapsilla tehdyt satunnaistetut tutkimukset (ei-nivelpsoriaasipotilaita mukana) yhteen koottuina osoittivat, että adalimumabin turvallisuusprofiili näissä kaikissa käyttöaiheissa oli samantyyppinen. Esimerkiksi vaikeat infektiot olivat harvinaisia, eikä pahanlaatuisuuksia ilmaantunut «Horneff G, Seyger MMB, Arikan D ym. Safety of Adal...»351.
- Etanersepti:
- Lastenreuma-aineistossa on tehty avoin tutkimus, jossa oli mukana 29 nivelpsoriaasipotilasta. Heistä 2 vuoden seurannassa 83 % saavutti ACRpedi70-vasteen ja 24 % inaktiivisen taudin «Constantin T, Foeldvari I, Vojinovic J ym. Two-yea...»352.
- Teho- ja turvallisuustulosta vahvistaa avoin saman etanerseptitutkimuksen (CLIPPER) 6 vuoden seurantatutkimus, jossa oli mukana vielä 23 nivelpsoriaasipotilasta. Heistä noin 70 % säilytti ACRpedi70-vasteen ja noin 25 % inaktiivisen taudin vasteen «Foeldvari I, Constantin T, Vojinovic J ym. Etanerc...»353.
- Teho- ja turvallisuustulosta vahvistavat myös avoin 18 potilaan «Otten MH, Prince FH, Ten Cate R ym. Tumour necrosi...»354 ja 127 potilaan rekisteritutkimus «Windschall D, Müller T, Becker I ym. Safety and ef...»355.
- Kolmen hoitostrategian vertailututkimus osoitti, että metotreksaatin ja etanerseptin yhdistelmän teho on parempi kuin DMARD-monoterapian (metotreksaatti tai sulfasalatsiini) tai metotreksaatti ja prednisoloni -siltahoidon. Tutkimuksessa oli 94 lastenreumapotilasta, joista 16:lla oli lasten nivelpsoriaasi. Kolmen kuukauden hoidon jälkeen ACRpedi50:n saavutti 53 % metotreksaattia ja etanerseptiä saaneiden ryhmästä, 31 % metotreksaattia ja prednisolonia saaneiden ryhmästä ja 38 % metotreksaattia tai sulfasalatsiinia saaneiden ryhmästä (p=0,19). ACRpedi70:n saavutti vastaavasti 47 %, 19 % ja 25 %, (p = 0,04) «Hissink Muller PC, Brinkman DM, Schonenberg D ym. ...»356.
- Toisessa hoitostrategiatutkimuksessa satunnaistettiin 85 polyartriittimuotoista lastenreumaa sairastavaa lasta (ei nivelpsoriaasia, mutta 1. asteen sukulaisella sai olla psoriaasi) kahteen ryhmään: metotreksaatti s.c., prednisoni ja etanersepti tai metotreksaatti s.c., prednisoni-lumelääke ja etanersepti-lumelääke. Hoito aloitettiin alle 1 vuoden kuluessa diagnoosista. Kuuden kuukauden seurannassa inaktiivinen tauti todettiin yhdistelmähoitoryhmässä 40 %:lla ja metotreksaattiryhmässä 23 %:lla (p = 0,088). Vastaavat luvut 12 kuukauden kohdalla olivat 73 % ja 58 % (p = 0,053) «Wallace CA, Giannini EH, Spalding SJ ym. Trial of ...»357.
- Golimumabi:
- Polyartikulaarisen lastenreuman hoitotutkimuksessa, jossa mukana sai olla soveltuvia nivelpsoriaasipotilaita, lääke oli tehokas mutta lääkityksen lopetuksessa 3 kuukauden kohdalla sen relapsitapauksien määrä ei eronnut lumeesta. Golimumabi johti polyartriittityyppisen lastenreuman paranemiseen, vaikkei primääristä tavoitetta RCT-tutkimuksessa saavutettukaan. Lääke on lapsilla hyvin siedetty, eikä yllättäviä haittoja ole ilmennyt «Brunner HI, Ruperto N, Tzaribachev N ym. Subcutane...»358.
- Infliksimabi:
- Hyvin varhaisen polyartikulaarisen lastenreuman hoidossa infliksimabi-metotreksaattihoito oli tehokkaampi kuin DMARD-yhdistelmä tai pelkkä metotreksaatti «Tynjälä P, Vähäsalo P, Tarkiainen M ym. Aggressive...»349.
- Tosilitsumabi:
- Tosilitsumabi on osoitettu tehokkaaksi yleisoireisen ja polyartriittimuotoisen lastenreuman hoidossa «De Benedetti F, Brunner HI, Ruperto N ym. Randomiz...»359, «Brunner HI, Ruperto N, Zuber Z ym. Efficacy and sa...»360.
- Kahden vuoden kohorttitutkimuksessa (56 iältään 2–17-vuotiasta lastenreumapotilasta, joilla oli seropositiivinen tai -negatiivinen polyartriitti tai laajeneva oligoartriitti, ei nivelpsoriaasipotilaita) vähäisen aktiivisuuden taudin osuus potilaista (JADAS10 ≤ 3,9) lisääntyi 18 %:sta 58 %:iin 1 vuoden seurannassa ja 84 %:iin 2 vuoden seurannassa, inaktiivisen taudin osuus (JADAS10 ≤ 0,7) vastaavasti 2 %:sta 19 %:iin ja 44 %:iin ja kliinisesti inaktiivisen taudin osuus (Wallacen preliminääriset kriteerit) 2 %:sta 28 %:iin ja 46 %:iin . Vakavia haittoja esiintyi odotetusti: 12,9/100 potilasvuotta «Grönlund MM, Remes-Pakarinen T, Kröger L ym. Effic...»361.
- Abatasepti
- Avoimessa polyartriittimuotoista lastenreumaa (n = 190) sairastavien 7 vuoden seurantatutkimuksessa osoitettiin, että saavutettu hoitoteho säilyy. Myös aluksi lumetta saaneet saivat hoitovastetta. Hoitoaieanalyysissä ACRpedi70-vasteen saavutti 27,4 % ja inaktiivisen taudin osuus oli 16,3 % «Lovell DJ, Ruperto N, Mouy R ym. Long-term safety,...»362.
- Sekukinumabi
- IL-17A:n estäjä, jolla on virallinen käyttöindikaatio lasten nivelpsoriaasissa sekä entesiittiartriitissa.
- Satunnaistetussa kontrolloidussa tutkimuksessa oli 86 potilasta, joista 34:llä oli nivelpsoriaasi (ja 52:lla entesiittityyppinen lastenreuma). Tutkimuksen avoimessa osassa he saivat lääkettä 12 viikon ajan, minkä jälkeen heidät satunnaistettiin saamaan sekukinumabia tai lumetta. Sekukinumabia saaneilla kului merkitsevästi pidempi aika taudin pahenemiseen kuin lumetta saaneilla (riskisuhde 0,28; 95 % luottamusväli 0,13–0,63). Turvallisuusprofiili oli samansuuntainen kuin tutkimuksessa, jossa tutkittiin aikuisten nivelpsoriaasia ja aksiaalista spondylartriittia «Brunner HI, Foeldvari I, Alexeeva E, ym. Secukinum...»363.
- JAK-estäjät:
- Barisitinibi
- Barisitinibilla on virallinen käyttöindikaatio polyartriittimuotoisessa lastenreumassa sekä lasten nivelpsoriaasissa ja entesiittiartriitissa.
- Lääkettä on tutkittu 220 lastenreumapotilaan aineistossa, jossa oli mukana 10 lasten nivelpsoriaasia sairastavaa. Tutkimuksessa 219 potilasta sai baritsitinibia avoimessa 12 viikon aloitusjaksossa. Potilaista 163 (74 %) sai vähintään ACRpedi30-vasteen viikolla 12. Heidät jaettiin sitten satunnaisesti ja kaksoissokkoutetusti saamaan lumetta (n = 81) tai barisitinibia (n = 82) 32 viikon ajan. Aika taudin pahenemiseen oli merkitsevästi lyhyempi lumetta saaneilla potilailla kuin baritsitinibia saaneilla (riskisuhde 0,241; 95 % luottamusväli 0,128–0,453, p < 0,0001). Lääkkeen turvallisuusprofiili oli vastaava kuin aikuistutkimuksissa «Ramanan AV, Quartier P, Okamoto N, ym. Baricitinib...»364.
- Tofasitinibi
- Tofasitinibilla on virallinen käyttöindikaatio polyartriittimuotoisessa lastenreumassa ja lasten nivelpsoriaasissa.
- Lääke on osoitettu tehokkaaksi 225 potilaan satunnaistetussa kontrolloidussa tutkimuksessa. Potilaista 20:llä (9 %) oli nivelpsoriaasi. Tutkittavat saivat tofasitinibia avoimessa 18 viikon aloitusjaksossa. 147 (65 %) sai samanaikaisesti metotreksaattia. Potilaista 142 (77 %) sai vähintään ACRpedi30-vasteen viikolla 18. Heidät jaettiin sitten satunnaisesti ja kaksoissokkoutetusti saamaan lumetta (n = 70) tai tofasitinibia (n = 72) 26 viikon ajan. Tauti oli pahentunut viikolla 44 merkittävästi harvemmin tofasitinibia saaneilla (29 %) kuin lumetta saaneilla (53 %; riskisuhde 0,46; 95 % luottamusväli 0,27–0,79; p = 0,0031) «Ruperto N, Brunner HI, Synoverska O, ym. Tofacitin...»365.
- Barisitinibi
Taloudellista tietoa
- Ks. apremilastin, JAK-estäjien ja biologisten lääkkeiden vaikuttavuuden (ACR50-vaste), kustannusten ja hoitovasteen kustannusten vertailu nivelpsoriaasin hoidossa «https://www.terveysportti.fi/apps/laake/laakekustannus/hoi50062»22 (vaatii käyttöoikeuden), lisätietoa «The number needed to treat (NNT) and cost per responder for systemic therapies for psoriatic arthritis»16 ja opasvideo taulukon lukemisesta «Hoitovasteen kustannukset Käypä hoito -suosituksissa: näin luen taulukoita (video)»17.
Hoidon porrastus
Ihopsoriaasin diagnostiikan ja hoidon porrastus
- Ihopsoriaasin diagnostiikan ja hoidon porrastuksesta ks. kaavio «Ihopsoriaasin hoidon porrastus»1.
- Perusterveydenhuollossa hoidetaan ilman erikoislääkärin konsultaatiota
- aikuispotilaan psoriaasi,
- joka on hallittavissa asianmukaisella paikallishoidolla
- joka ei aiheuta työkykyongelmia
- johon ei liity niveloireita.
- aikuispotilaan psoriaasi,
- Muiden sairauksien ja riskitekijöiden selvitys ja hoito tulee aloittaa jo ennen erikoissairaanhoidon
konsultaatiota. Keskeisiä ovat
- metabolinen oireyhtymä «Rutter MK, Kane K, Lunt M ym. Primary care-based s...»366, tupakointi ja alkoholin liikakäyttö
- infektiopesäkkeiden selvitys ja hoito (erityisesti suun alue)
- masennus ja ahdistuneisuus.
- Potilas lähetetään erikoissairaanhoitoon, kun
- kyseessä on nopeasti laajeneva, laaja-alainen tai vaikea psoriaasi
- kyseessä on lasten ihopsoriaasi tai sen epäily
- kyseessä on pienialainen psoriaasi, joka
- ei reagoi asianmukaiseen paikallishoitoon (diagnoosin tarkistus)
- aiheuttaa työkykyongelman (esim. kämmenpsoriaasi)
- aiheuttaa kohtuutonta subjektiivista haittaa (esim. kasvopsoriaasi).
- tarvitaan hoidonohjausta tai sairautta koskevia lisätietoja
- kyseessä on vahvojen kortikosteroidivoiteiden liikakäyttö tai riippuvuus niistä.
- Erikoislääkärikonsultaation jälkeen
- potilasta seurataan perusterveydenhuollossa, jos ihottuma ei vaadi UV-valohoitoa tai systeemilääkitystä.
Nivelpsoriaasin diagnostiikan ja hoidon porrastus
- Nivelpsoriaasin diagnoosin ja hoidontarpeenarvion tekee nivelpsoriaasiin perehtynyt erikoislääkäri.
- Perusterveydenhuollossa hoidetaan ilman erikoislääkärin konsultaatiota
- lieväoireinen nivelpsoriaasi.
- Hoitona käytetään tulehduskipulääkkeitä ja kortikosteroidipistoksia niveliin.
- lieväoireinen nivelpsoriaasi.
- Erikoissairaanhoitoa tulee konsultoida, jos kyseessä on
- niveltulehdus, joka pitkittyy tai vaikeutuu, eikä tulehduskipulääkkeillä ja paikallisilla kortikosteroidipistoksilla (2–3 kertaa) saada vastetta
- tuore moniniveltulehdus
- selkärankareumaa muistuttava tautimuoto
- lasten nivelpsoriaasi tai epäily sellaisesta.
- raskaana olevan tai raskautta harkitsevan naisen nivelpsoriaasi.
- Erikoislääkärikonsultaation jälkeen:
- Kun hoitotasapaino on saavutettu, aikuispotilaan hoito ja seuranta voidaan siirtää
perusterveydenhuoltoon.
- Ennen hoitovastuun siirtymistä on suositeltavaa, että erikoislääkäri ja potilaasta vastaava perusterveydenhuollon lääkäri tekevät yhteistyötä väliarviointien avulla (ns. jaettu hoitovastuu).
- Hoitovasteen heiketessä, kun potilaan oireet lisääntyvät, konsultoidaan erikoissairaanhoitoa.
- Biologista lääkehoitoa ja JAK:n estäjähoitoa saavien potilaiden seuranta jatkuu erikoissairaanhoidossa.
- Alueelliset hoidonporrastusmenettelyt (hoitoketjut) voivat poiketa tästä suosituksesta.
- Kun hoitotasapaino on saavutettu, aikuispotilaan hoito ja seuranta voidaan siirtää
perusterveydenhuoltoon.
Suomalaisen Lääkäriseuran Duodecimin, Suomen Ihotautilääkäriyhdistyksen ja Suomen Reumatologinen Yhdistys ry:n asettama työryhmä
Psoriaasi ja nivelpsoriaasi -suosituksen historiatiedot «Psoriaasi ja nivelpsoriaasi, Käypä hoito -suosituksen historiatiedot»19
16.3.2026 julkaistusta kohdennetusta päivityksestä vastasivat:
Raija Sipilä, LT, terveydenhuollon erikoislääkäri, päätoimittaja; Suomalainen Lääkäriseura Duodecim, Käypä hoito
Tarja Mälkönen, LT, ihotautien ja allergologian erikoislääkäri; HUS Iho- ja allergiasairaala, Helsinki
Edellinen kohdennettu päivitys ihopsoriaasin osalta on julkaistu 22.12.2021 ja nivelpsoriaasin osalta 27.2.2025.
Suosituksesta vastaava työryhmä:
Työryhmän puheenjohtaja
Raija Sipilä, LT, terveydenhuollon erikoislääkäri, päätoimittaja; Suomalainen Lääkäriseura Duodecim, Käypä hoito
Kokoavat kirjoittajat
Tarja Mälkönen, LT, ihotautien ja allergologian erikoislääkäri; HUS Iho- ja allergiasairaala, Helsinki
Kati Mykkänen, reumatologian erikoislääkäri; HUS Meilahden sairaala
Tapio Rantanen, LL, iho- ja sukupuolitautien erikoislääkäri; Tampere
Työryhmän jäsenet
Päivi Ekman, LT, reumatologian erikoislääkäri, ylilääkäri; Satasairaala, Rauma
Anna Hannuksela-Svahn, LT, iho- ja sukupuolitautien erikoislääkäri; HUS Iho- ja allergiasairaala, Helsinki
Johanna Höök-Nikanne, LT, dosentti, ihotautien ja allergologian erikoislääkäri, ylilääkäri; HUS Lohjan sairaala
Leena Koulu, LKT, dosentti, iho- ja sukupuolitautien ja allergologian erikoislääkäri, hallinnollinen osastonylilääkäri; TYKS Ihoklinikka
Krista Nuotio, LT, neurologian erikoislääkäri, lääkärikouluttajan erityispätevyys, Käypä hoito -toimittaja; Suomalainen Lääkäriseura Duodecim
Vappu Rantalaiho, LT, dosentti sisätautien ja reumatologian erikoislääkäri, reumatologian tenure track professori, vs. ylilääkäri; Tampereen yliopisto ja Pirkanmaan Sairaanhoitopiiri
Erna Snellman, professori emer., iho- ja sukupuolitautien erikoislääkäri; Tampereen yliopisto
Heikki Valleala, LT, dosentti, sisätautien ja reumatologian erikoislääkäri; HUS, Reumaklinikka
Paula Vähäsalo, LT, dosentti, lastentautien erikoislääkäri, lastenreumatologi; Oulun yliopisto, kliinisen lääketieteen tutkimusyksikkö ja OYS Lasten ja nuorten klinikka
Asiantuntija
Bianca Arrhenius, LT, yleislääketieteen erikoislääkäri, Käypä hoito -toimittaja; Suomalainen Lääkäriseura Duodecim, ammatinharjoittaja; Lääkärikeskus Aava
Sidonnaisuudet
Sidonnaisuusilmoitukset on tarkistettu 8.10.2024 julkaistun kohdennetun päivityksen yhteydessä niiden kirjoittajien osalta, jotka ovat osallistuneet nivelpsoriaasia koskevan suositusosan päivityksen laatimiseen.
Päivi Ekman: Sivutoimet: lääkäri, hallituksen jäsen; MP-lääkärit Oy, Rauma, yksityisvastaanotto; Lääkärikeskus Kanalinhelmi, Rauma ja Lääkärikeskus Karhulinna, Pori. Korvaukset seminaari- ja kongressikuluista: Astra-Zeneca, Medac, Novartis, Pfizer, UCB. Luento-, koulutus- ja asiantuntijapalkkiot: Janssen-Cilag, Orion, UCB.
Anna Hannuksela-Svahn: Ei sidonnaisuuksia.
Johanna Höök-Nikanne: Sivutoimet: Pikkujätti Myyrmäki ja Ihosairaala Kamppi yksityislääkäri. Luento-, koulutus- ja asiantuntijapalkkiot: UCB-pharma Advisory board, Sanofi Advisory Board. Korvaukset koulutus- ja kongressikuluista: Novartis, Sanofi, Abbvie, Janssen Cilag, Leo Pharma. Muut sidonnaisuudet: Janssen-Cilag-lääketutkimus.
Leena Koulu: Sivutoimet: Mehiläinen, Turku, ihotautilääkärin vastaanotto. Luento-, koulutus- ja asiantuntijapalkkiot: AbbVie, UCB Pharma, Janssen, Novartis, Eli Lilly, Leo Pharma, Sanofi. Korvaukset koulutus- ja kongressikuluista: Sanofi. Luottamustoimet: Valvira, asiantuntija. Muut sidonnaisuudet: Pfizer, kliininen lääkeainetutkimus on alkamassa.
Kati Mykkänen: Sivutoimet: Lääkärikeskus Fenix. Luento-, koulutus- ja asiantuntijapalkkiot: Suomen reumaliitto, Duodecim, Janssen Cilag, Novartis. Korvaukset seminaari- ja kongressikuluista: Amgen. Tutkimusrahoitus: Paulon Säätiö, Medicinska Understödsföreningen Liv och Hälsa, Reumatautien tutkimussäätiö, HUS. Luottamustoimet: EULAR ( European League Against Rheumatism) Quality of Care - toimikunta.
Tarja Mälkönen: Sivutoimet: Terveystalo ja Ihosairaala Oy, yksityisvastaanotto. Luento-, koulutus- ja asiantuntijapalkkiot: Abbvie, Amgen, Janssen, Medac, Novartis, Sanofi Genzyme. Korvaukset koulutus- ja kongressikuluista: Abbvie, Janssen, Sanofi Genzyme. Luottamustoimet: Psoriasisliitto, asiantuntijalääkäri; EuroGuiDerm Psoriasis Guideline-projekti (eurooppalainen hoitosuositus), asiantuntija.
Krista Nuotio: Sivutoimet: Yksityisvastaanotto, Terveystalo. Luottamustoimet: Helsingin lääkäripäivien ohjelmatyöryhmä, jäsenyys.
Vappu Rantalaiho: Koulutus, konsultointi ja asiantuntijatoiminta: Novartis, Viatris, Abbvie, BMS, Johnson&Johnson, Lilly. Luottamustoimet: Suomen Reumatologinen Yhdistys, hallitus; Suomen Reumatologinen Yhdistys, tiedevaliokunta; Reumasairauksien valtakunnallisen koordinaatiokeskuksen ohjausryhmän sihteeri; Scandinavian Journal of Rheumatology editorial board, jäsen; Scandinavian Rheumatology Research Foundation jäsen.
Tapio Rantanen: Sivutoimet: Pirkanmaan Syöpäyhdistys ry, Tampere, 22.10.2018–28.2.2019, väliaikainen ylilääkäri, terveydenhuollon palveluista vastaava johtaja. Tutkimusrahoitus: Pirkanmaan Syöpäyhdistys ry. Luento-, koulutus- ja asiantuntijapalkkiot: AbbVie, Janssen-Cilag, Leo Pharma, Lilly, Novartis, UCB. Korvaukset koulutus- ja kongressikuluista: AbbVie, Celgene, Galderma, Janssen-Cilag, Lilly, Novartis, Sanofi. Luottamustoimet: Psoriasisliitto ry, asiantuntijalääkäri.
Raija Sipilä: Sivutoimet: yleislääkäri; Terveystalo (3/2024 asti). Tutkimus ja kehitystyö: Potilaat mukaan Käypä hoito -suositusten laatimiseen -hanke, työnantajalle rahoitus, rahoittajana STEA (2019–2022) PROSHADE, työnantajalle rahoitus, rahoittajana STN 10/2020–. Koulutustoiminta: Medimerc (Turun yliopisto). Luottamustoimet: GIN Nordic ohjausryhmän jäsen 2019–4/2023, GIN Nordic ohjausryhmän puheenjohtaja 5/2023–, Kela sosiaalilääketieteen neuvottelukunta 2/2019–, Lääkärintietokannat neuvottelukunnan jäsen 2010–2021 HUS Hyte-asiantuntijaryhmä 4/21– Scandinavian GRADE, ohjausryhmän jäsen 5/2024–, Palko, asiantuntija 7/2024–.
Erna Snellman: Sivutoimet: Terveystalo Pori ja Mehiläinen Lahti, yksityisvastaanotto, TAYS, tutkija 2019–. Korvaukset seminaari- ja kongressikuluista: Sanofi Ihotautien maailmankongressi 2019.
Heikki Valleala: Sivutoimet: yksitysivastaanotto; Mehiläinen, Töölö ja Pihlajalinna, Tavastia. Luento-, koulutus- ja asiantuntijapalkkiot: Abbvie, Pfizer, UCB, Novartis, BMS. Korvaukset seminaari- ja kongressikuluista: Abbvie, Janssen-Cilag, Pfizer, Pfizer, Novartis, BMS. Muut sidonnaisuudet: Kliinisiin lääketutkimuksiin osallistuminen: Abbvie, Pfizer, BMS.
Paula Vähäsalo: Sivutoimet: konsultoiva lastenreumatologi; Vaasan keskussairaala, lasten yksikkö, asiantuntija; THL, Tulehduksellisten reumasairauksien laaturekisteri, toimittaja; Reumasairaudet -oppikirja Duodecim. Kansainvälisessä työryhmässä, jonka tavoitteena on yhtenäistää lääkärin arvioiman lastenreuman taudinaktiivisuuden kriteerejä. Koulutus, konsultointi ja asiantuntijatoiminta: Novartis, UCB. Korvaukset seminaari- ja kongressikuluista: Novartis, Pfizer, Orion. Luottamustoimet: Suomen lastenlääkäriyhdistyksen lastenreumatologian alajaoksen puheenjohtaja; Suomen reumatologisen yhdistyksen tiedevaliokunta.
Kirjallisuusviite
Psoriaasi (iho ja nivelet). Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Ihotautilääkäriyhdistyksen asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2026 (viitattu pp.kk.vvvv). Saatavilla internetissä: www.kaypahoito.fi
Tarkemmat viittausohjeet: «http://www.kaypahoito.fi/web/kh/viittaaminen»27
Vastuun rajaus
Käypä hoito -suositukset ja Vältä viisaasti -suositukset ovat asiantuntijoiden laatimia yhteenvetoja yksittäisten sairauksien diagnostiikan ja hoidon vaikuttavuudesta. Suositukset toimivat lääkärin tai muun terveydenhuollon ammattilaisen päätöksenteon tukena hoitopäätöksiä tehtäessä. Ne eivät korvaa lääkärin tai muun terveydenhuollon ammattilaisen omaa arviota yksittäisen potilaan parhaasta mahdollisesta diagnostiikasta, hoidosta ja kuntoutuksesta hoitopäätöksiä tehtäessä.
Tiedonhakukäytäntö
Systemaattinen kirjallisuushaku on hoitosuosituksen perusta. Lue lisää artikkelista khk00007
Kirjallisuutta
- Mälkonen T, Suomela S. [What do we know about pathogenesis of psoriasis?]. Duodecim 2011;127:1579-89 «PMID: 21995128»PubMed
- Matikainen S, Jokiranta S, Eklund KK. [Role of cytokines and their blocking in immune-mediated inflammatory diseases]. Duodecim 2016;132:349-54 «PMID: 27017787»PubMed
- Global report on psoriasis. World Health Organization 2016. ISBN 978 92 4 156518 9. 2016
- Petty RE, Southwood TR, Manners P ym. International League of Associations for Rheumatology classification of juvenile idiopathic arthritis: second revision, Edmonton, 2001. J Rheumatol 2004;31:390-2 «PMID: 14760812»PubMed
- Felson DT, Anderson JJ, Boers M ym. American College of Rheumatology. Preliminary definition of improvement in rheumatoid arthritis. Arthritis Rheum 1995;38:727-35 «PMID: 7779114»PubMed
- Giannini EH, Ruperto N, Ravelli A ym. Preliminary definition of improvement in juvenile arthritis. Arthritis Rheum 1997;40:1202-9 «PMID: 9214419»PubMed
- Carlin CS, Feldman SR, Krueger JG ym. A 50% reduction in the Psoriasis Area and Severity Index (PASI 50) is a clinically significant endpoint in the assessment of psoriasis. J Am Acad Dermatol 2004;50:859-66 «PMID: 15153885»PubMed
- Gordon KB, Feldman SR, Koo JY ym. Definitions of measures of effect duration for psoriasis treatments. Arch Dermatol 2005;141:82-4 «PMID: 15655149»PubMed
- Parisi R, Symmons DP, Griffiths CE ym. Global epidemiology of psoriasis: a systematic review of incidence and prevalence. J Invest Dermatol 2013;133:377-85 «PMID: 23014338»PubMed
- Danielsen K, Olsen AO, Wilsgaard T ym. Is the prevalence of psoriasis increasing? A 30-year follow-up of a population-based cohort. Br J Dermatol 2013;168:1303-10 «PMID: 23374051»PubMed
- Svensson A, Ofenloch RF, Bruze M ym. Prevalence of skin disease in a population-based sample of adults from five European countries. Br J Dermatol 2018;178:1111-1118 «PMID: 29247509»PubMed
- Egeberg A, Andersen YMF, Thyssen JP. Prevalence and characteristics of psoriasis in Denmark: findings from the Danish skin cohort. BMJ Open 2019;9:e028116 «PMID: 30898836»PubMed
- Burden-Teh E, Thomas KS, Ratib S ym. The epidemiology of childhood psoriasis: a scoping review. Br J Dermatol 2016;174:1242-57 «PMID: 26928555»PubMed
- Tollefson MM, Crowson CS, McEvoy MT ym. Incidence of psoriasis in children: a population-based study. J Am Acad Dermatol 2010;62:979-87 «PMID: 19962785»PubMed
- Huerta C, Rivero E, Rodríguez LA. Incidence and risk factors for psoriasis in the general population. Arch Dermatol 2007;143:1559-65 «PMID: 18087008»PubMed
- Icen M, Crowson CS, McEvoy MT ym. Trends in incidence of adult-onset psoriasis over three decades: a population-based study. J Am Acad Dermatol 2009;60:394-401 «PMID: 19231638»PubMed
- Henseler T, Christophers E. Psoriasis of early and late onset: characterization of two types of psoriasis vulgaris. J Am Acad Dermatol 1985;13:450-6 «PMID: 4056119»PubMed
- Lønnberg AS, Skov L, Duffy DL ym. Genetic Factors Explain Variation in the Age at Onset of Psoriasis: A Population-based Twin Study. Acta Derm Venereol 2016;96:35-8 «PMID: 26073043»PubMed
- Vogel SA, Yentzer B, Davis SA ym. Trends in pediatric psoriasis outpatient health care delivery in the United States. Arch Dermatol 2012;148:66-71 «PMID: 21931013»PubMed
- Gelfand JM, Gladman DD, Mease PJ ym. Epidemiology of psoriatic arthritis in the population of the United States. J Am Acad Dermatol 2005;53:573 «PMID: 16198775»PubMed
- Madland TM, Apalset EM, Johannessen AE ym. Prevalence, disease manifestations, and treatment of psoriatic arthritis in Western Norway. J Rheumatol 2005;32:1918-22 «PMID: 16206347»PubMed
- Wilson FC, Icen M, Crowson CS ym. Time trends in epidemiology and characteristics of psoriatic arthritis over 3 decades: a population-based study. J Rheumatol 2009;36:361-7 «PMID: 19208565»PubMed
- Kaipiainen-Seppänen O. Incidence of psoriatic arthritis in Finland. Br J Rheumatol 1996;35:1289-91 «PMID: 9010058»PubMed
- Alamanos Y, Voulgari PV, Drosos AA. Incidence and prevalence of psoriatic arthritis: a systematic review. J Rheumatol 2008;35:1354-8 «PMID: 18464305»PubMed
- Wilson FC, Icen M, Crowson CS ym. Incidence and clinical predictors of psoriatic arthritis in patients with psoriasis: a population-based study. Arthritis Rheum 2009;61:233-9 «PMID: 19177544»PubMed
- Prey S, Paul C, Bronsard V ym. Assessment of risk of psoriatic arthritis in patients with plaque psoriasis: a systematic review of the literature. J Eur Acad Dermatol Venereol 2010;24 Suppl 2:31-5 «PMID: 20443998»PubMed
- Christophers E, Barker JN, Griffiths CE ym. The risk of psoriatic arthritis remains constant following initial diagnosis of psoriasis among patients seen in European dermatology clinics. J Eur Acad Dermatol Venereol 2010;24:548-54 «PMID: 19874432»PubMed
- Gladman DD, Shuckett R, Russell ML ym. Psoriatic arthritis (PSA)--an analysis of 220 patients. Q J Med 1987;62:127-41 «PMID: 3659255»PubMed
- Berntson L, Andersson Gäre B, Fasth A ym. Incidence of juvenile idiopathic arthritis in the Nordic countries. A population based study with special reference to the validity of the ILAR and EULAR criteria. J Rheumatol 2003;30:2275-82 «PMID: 14528529»PubMed
- Savolainen E, Kaipiainen-Seppänen O, Kröger L ym. Total incidence and distribution of inflammatory joint diseases in a defined population: results from the Kuopio 2000 arthritis survey. J Rheumatol 2003;30:2460-8 «PMID: 14677193»PubMed
- Virta R, Helenius H, Klaukka T. Lasten reuma yleistyy Suomessa. Suom Lääkäril 2008;63:2806-9
- Icen M, Crowson CS, McEvoy MT ym. Trends in incidence of adult-onset psoriasis over three decades: a population-based study. J Am Acad Dermatol 2009;60:394-401 «PMID: 19231638»PubMed
- Dand N, Mahil SK, Capon F ym. Psoriasis and Genetics. Acta Derm Venereol 2020;100:adv00030 «PMID: 31971603»PubMed
- Lomholt G. Psoriasis. Prevalence, Spontaneous Course, and Genetics; a Census Study on the Prevalence of Skin Diseases on the Faroe Islands. GEC Gad, Copenhagen 1963;
- Swanbeck G, Inerot A, Martinsson T ym. Genetic counselling in psoriasis: empirical data on psoriasis among first-degree relatives of 3095 psoriatic probands. Br J Dermatol 1997;137:939-42 «PMID: 9470911»PubMed
- Asumalahti K, Saarialho-Kere U, Kere J. [The pathogenesis of psoriasis--investigating the genetics of a multifactorial disease]. Duodecim 2003;119:1517-22 «PMID: 14535024»PubMed
- Andressen C, Henseler T. [Inheritance of psoriasis. Analysis of 2035 family histories]. Hautarzt 1982;33:214-7 «PMID: 7096085»PubMed
- Mallbris L, Larsson P, Bergqvist S ym. Psoriasis phenotype at disease onset: clinical characterization of 400 adult cases. J Invest Dermatol 2005;124:499-504 «PMID: 15737189»PubMed
- Harden JL, Krueger JG, Bowcock AM. The immunogenetics of Psoriasis: A comprehensive review. J Autoimmun 2015;64:66-73 «PMID: 26215033»PubMed
- Arakawa A, Siewert K, Stöhr J ym. Melanocyte antigen triggers autoimmunity in human psoriasis. J Exp Med 2015;212:2203-12 «PMID: 26621454»PubMed
- Lande R, Botti E, Jandus C ym. The antimicrobial peptide LL37 is a T-cell autoantigen in psoriasis. Nat Commun 2014;5:5621 «PMID: 25470744»PubMed
- Cheung KL, Jarrett R, Subramaniam S ym. Psoriatic T cells recognize neolipid antigens generated by mast cell phospholipase delivered by exosomes and presented by CD1a. J Exp Med 2016;213:2399-2412 «PMID: 27670592»PubMed
- Gudjonsson JE, Thorarinsson AM, Sigurgeirsson B ym. Streptococcal throat infections and exacerbation of chronic plaque psoriasis: a prospective study. Br J Dermatol 2003;149:530-4 «PMID: 14510985»PubMed
- Seville RH. Stress and psoriasis: the importance of insight and empathy in prognosis. J Am Acad Dermatol 1989;20:97-100 «PMID: 2643644»PubMed
- Naldi L, Peli L, Parazzini F ym. Family history of psoriasis, stressful life events, and recent infectious disease are risk factors for a first episode of acute guttate psoriasis: results of a case-control study. J Am Acad Dermatol 2001;44:433-8 «PMID: 11209111»PubMed
- Li WQ, Qureshi AA, Schernhammer ES ym. Rotating night-shift work and risk of psoriasis in US women. J Invest Dermatol 2013;133:565-7 «PMID: 22931920»PubMed
- Dominguez PL, Han J, Li T ym. Depression and the risk of psoriasis in US women. J Eur Acad Dermatol Venereol 2013;27:1163-7 «PMID: 23030685»PubMed
- Wu S, Li WQ, Han J ym. Hypercholesterolemia and risk of incident psoriasis and psoriatic arthritis in US women. Arthritis Rheumatol 2014;66:304-10 «PMID: 24504802»PubMed
- Naldi L, Chatenoud L, Linder D ym. Cigarette smoking, body mass index, and stressful life events as risk factors for psoriasis: results from an Italian case-control study. J Invest Dermatol 2005;125:61-7 «PMID: 15982303»PubMed
- Setty AR, Curhan G, Choi HK. Obesity, waist circumference, weight change, and the risk of psoriasis in women: Nurses' Health Study II. Arch Intern Med 2007;167:1670-5 «PMID: 17698691»PubMed
- Wolk K, Mallbris L, Larsson P ym. Excessive body weight and smoking associates with a high risk of onset of plaque psoriasis. Acta Derm Venereol 2009;89:492-7 «PMID: 19734975»PubMed
- Li W, Han J, Choi HK ym. Smoking and risk of incident psoriasis among women and men in the United States: a combined analysis. Am J Epidemiol 2012;175:402-13 «PMID: 22247049»PubMed
- Setty AR, Curhan G, Choi HK. Smoking and the risk of psoriasis in women: Nurses' Health Study II. Am J Med 2007;120:953-9 «PMID: 17976422»PubMed
- Poikolainen K, Reunala T, Karvonen J ym. Alcohol intake: a risk factor for psoriasis in young and middle aged men? BMJ 1990;300:780-3 «PMID: 1969757»PubMed
- Qureshi AA, Dominguez PL, Choi HK ym. Alcohol intake and risk of incident psoriasis in US women: a prospective study. Arch Dermatol 2010;146:1364-9 «PMID: 20713772»PubMed
- Ockenfels HM. [Trigger factors for psoriasis]. Hautarzt 2003;54:215-23 «PMID: 12634989»PubMed
- Poikolainen K, Reunala T, Karvonen J. Smoking, alcohol and life events related to psoriasis among women. Br J Dermatol 1994;130:473-7 «PMID: 8186112»PubMed
- Keller JJ, Wu CS, Lin HC. Increased risk of psoriasis following chronic rhinosinusitis without nasal polyps: a population-based matched-cohort study. Br J Dermatol 2013;168:289-94 «PMID: 23013326»PubMed
- Thorleifsdottir RH, Eysteinsdóttir JH, Olafsson JH ym. Throat Infections are Associated with Exacerbation in a Substantial Proportion of Patients with Chronic Plaque Psoriasis. Acta Derm Venereol 2016;96:788-91 «PMID: 26984718»PubMed
- Dika E, Varotti C, Bardazzi F ym. Drug-induced psoriasis: an evidence-based overview and the introduction of psoriatic drug eruption probability score. Cutan Ocul Toxicol 2006;25:1-11 «PMID: 16702050»PubMed
- Harrison MJ, Dixon WG, Watson KD ym. Rates of new-onset psoriasis in patients with rheumatoid arthritis receiving anti-tumour necrosis factor alpha therapy: results from the British Society for Rheumatology Biologics Register. Ann Rheum Dis 2009;68:209-15 «PMID: 18385277»PubMed
- Shmidt E, Wetter DA, Ferguson SB ym. Psoriasis and palmoplantar pustulosis associated with tumor necrosis factor-a inhibitors: the Mayo Clinic experience, 1998 to 2010. J Am Acad Dermatol 2012;67:e179-85 «PMID: 21752492»PubMed
- Guerra I, Algaba A, Pérez-Calle JL ym. Induction of psoriasis with anti-TNF agents in patients with inflammatory bowel disease: a report of 21 cases. J Crohns Colitis 2012;6:518-23 «PMID: 22398059»PubMed
- Brauchli YB, Jick SS, Curtin F ym. Association between beta-blockers, other antihypertensive drugs and psoriasis: population-based case-control study. Br J Dermatol 2008;158:1299-307 «PMID: 18410416»PubMed
- Karason A, Love TJ, Gudbjornsson B. A strong heritability of psoriatic arthritis over four generations--the Reykjavik Psoriatic Arthritis Study. Rheumatology (Oxford) 2009;48:1424-8 «PMID: 19741010»PubMed
- Green A, Shaddick G, Charlton R ym. Modifiable risk factors and the development of psoriatic arthritis in people with psoriasis. Br J Dermatol 2020;182:714-720 «PMID: 31209855»PubMed
- Eder L, Harvey P, Chandran V ym. Gaps in Diagnosis and Treatment of Cardiovascular Risk Factors in Patients with Psoriatic Disease: An International Multicenter Study. J Rheumatol 2018;45:378-384 «PMID: 29419462»PubMed
- Eder L, Shanmugarajah S, Thavaneswaran A ym. The association between smoking and the development of psoriatic arthritis among psoriasis patients. Ann Rheum Dis 2012;71:219-24 «PMID: 21953342»PubMed
- Pezzolo E, Naldi L. The relationship between smoking, psoriasis and psoriatic arthritis. Expert Rev Clin Immunol 2019;15:41-48 «PMID: 30380949»PubMed
- Zhao SS, Goodson NJ, Robertson S ym. Smoking in spondyloarthritis: unravelling the complexities. Rheumatology (Oxford) 2020;59:1472-1481 «PMID: 32236486»PubMed
- Tsuruta N, Imafuku S, Narisawa Y. Hyperuricemia is an independent risk factor for psoriatic arthritis in psoriatic patients. J Dermatol 2017;44:1349-1352 «PMID: 28691207»PubMed
- Neimann AL, Shin DB, Wang X ym. Prevalence of cardiovascular risk factors in patients with psoriasis. J Am Acad Dermatol 2006;55:829-35 «PMID: 17052489»PubMed
- Mallbris L, Ritchlin CT, Ståhle M. Metabolic disorders in patients with psoriasis and psoriatic arthritis. Curr Rheumatol Rep 2006;8:355-63 «PMID: 16973109»PubMed
- Husted JA, Thavaneswaran A, Chandran V ym. Cardiovascular and other comorbidities in patients with psoriatic arthritis: a comparison with patients with psoriasis. Arthritis Care Res (Hoboken) 2011;63:1729-35 «PMID: 21905258»PubMed
- McAleer MA, Mason DL, Cunningham S ym. Alcohol misuse in patients with psoriasis: identification and relationship to disease severity and psychological distress. Br J Dermatol 2011;164:1256-61 «PMID: 21457207»PubMed
- Mehta NN, Azfar RS, Shin DB ym. Patients with severe psoriasis are at increased risk of cardiovascular mortality: cohort study using the General Practice Research Database. Eur Heart J 2010;31:1000-6 «PMID: 20037179»PubMed
- Gelfand JM, Troxel AB, Lewis JD ym. The risk of mortality in patients with psoriasis: results from a population-based study. Arch Dermatol 2007;143:1493-9 «PMID: 18086997»PubMed
- Abuabara K, Azfar RS, Shin DB ym. Cause-specific mortality in patients with severe psoriasis: a population-based cohort study in the U.K. Br J Dermatol 2010;163:586-92 «PMID: 20633008»PubMed
- Cohen AD, Dreiher J, Birkenfeld S. Psoriasis associated with ulcerative colitis and Crohn's disease. J Eur Acad Dermatol Venereol 2009;23:561-5 «PMID: 19207663»PubMed
- Ludvigsson JF, Lindelöf B, Zingone F ym. Psoriasis in a nationwide cohort study of patients with celiac disease. J Invest Dermatol 2011;131:2010-6 «PMID: 21654830»PubMed
- Rehal B, Modjtahedi BS, Morse LS ym. Ocular psoriasis. J Am Acad Dermatol 2011;65:1202-12 «PMID: 21550135»PubMed
- Boffetta P, Gridley G, Lindelöf B. Cancer risk in a population-based cohort of patients hospitalized for psoriasis in Sweden. J Invest Dermatol 2001;117:1531-7 «PMID: 11886519»PubMed
- Brauchli YB, Jick SS, Miret M ym. Psoriasis and risk of incident cancer: an inception cohort study with a nested case-control analysis. J Invest Dermatol 2009;129:2604-12 «PMID: 19440219»PubMed
- Chen YJ, Wu CY, Chen TJ ym. The risk of cancer in patients with psoriasis: a population-based cohort study in Taiwan. J Am Acad Dermatol 2011;65:84-91 «PMID: 21458106»PubMed
- Schmitt J, Ford DE. Psoriasis is independently associated with psychiatric morbidity and adverse cardiovascular risk factors, but not with cardiovascular events in a population-based sample. J Eur Acad Dermatol Venereol 2010;24:885-92 «PMID: 20015170»PubMed
- Kurd SK, Troxel AB, Crits-Christoph P ym. The risk of depression, anxiety, and suicidality in patients with psoriasis: a population-based cohort study. Arch Dermatol 2010;146:891-5 «PMID: 20713823»PubMed
- De Lorenzis E, Natalello G, Bruno D ym. Psoriatic arthritis and depressive symptoms: does systemic inflammation play a role? Clin Rheumatol 2021;40:1893-1902 «PMID: 33009969»PubMed
- Augustin M, Radtke MA, Glaeske G ym. Epidemiology and Comorbidity in Children with Psoriasis and Atopic Eczema. Dermatology 2015;231:35-40 «PMID: 25966818»PubMed
- Finlay AY, Coles EC. The effect of severe psoriasis on the quality of life of 369 patients. Br J Dermatol 1995;132:236-44 «PMID: 7888360»PubMed
- Rapp SR, Feldman SR, Exum ML ym. Psoriasis causes as much disability as other major medical diseases. J Am Acad Dermatol 1999;41:401-7 «PMID: 10459113»PubMed
- Burden AD, Hilton Boon M, Leman J ym. Diagnosis and management of psoriasis and psoriatic arthritis in adults: summary of SIGN guidance. BMJ 2010;341:c5623 «PMID: 21036815»PubMed
- Ahlehoff O, Gislason GH, Charlot M ym. Psoriasis is associated with clinically significant cardiovascular risk: a Danish nationwide cohort study. J Intern Med 2011;270:147-57 «PMID: 21114692»PubMed
- Gelfand JM, Troxel AB, Lewis JD ym. The risk of mortality in patients with psoriasis: results from a population-based study. Arch Dermatol 2007;143:1493-9 «PMID: 18086997»PubMed
- Daudén E, Puig L, Ferrándiz C ym. Consensus document on the evaluation and treatment of moderate-to-severe psoriasis: Psoriasis Group of the Spanish Academy of Dermatology and Venereology. J Eur Acad Dermatol Venereol 2016;30 Suppl 2:1-18 «PMID: 26812550»PubMed
- Strober B, Ryan C, van de Kerkhof P ym. Recategorization of psoriasis severity: Delphi consensus from the International Psoriasis Council. J Am Acad Dermatol 2020;82:117-122 «PMID: 31425723»PubMed
- Lodén M. Role of topical emollients and moisturizers in the treatment of dry skin barrier disorders. Am J Clin Dermatol 2003;4:771-88 «PMID: 14572299»PubMed
- Lebwohl M. The role of salicylic acid in the treatment of psoriasis. Int J Dermatol 1999;38:16-24 «PMID: 10065604»PubMed
- Fetil E, Ozka S, Soyal MC ym. Effects of topical petrolatum and salicylic acid on the erythemogenicity of UVB. Eur J Dermatol 2002;12:154-6 «PMID: 11872412»PubMed
- Lebwohl M, Martinez J, Weber P ym. Effects of topical preparations on the erythemogenicity of UVB: implications for psoriasis phototherapy. J Am Acad Dermatol 1995;32:469-71 «PMID: 7868718»PubMed
- Surber C, Itin PH, Bircher AJ ym. Topical corticosteroids. J Am Acad Dermatol 1995;32:1025-30 «PMID: 7751447»PubMed
- Mason J, Mason AR, Cork MJ. Topical preparations for the treatment of psoriasis: a systematic review. Br J Dermatol 2002;146:351-64 «PMID: 11952534»PubMed
- Haapasaari KM, Risteli J, Oikarinen A. Recovery of human skin collagen synthesis after short-term topical corticosteroid treatment and comparison between young and old subjects. Br J Dermatol 1996;135:65-9 «PMID: 8776361»PubMed
- Murdoch D, Clissold SP. Calcipotriol. A review of its pharmacological properties and therapeutic use in psoriasis vulgaris. Drugs 1992;43:415-29 «PMID: 1374321»PubMed
- Liu X, Liu Y, Xu M ym. Zinc finger protein A20 is involved in the antipsoriatic effect of calcipotriol. Br J Dermatol 2016;175:314-24 «PMID: 26875609»PubMed
- Germán B, Wei R, Hener P ym. Disrupting the IL-36 and IL-23/IL-17 loop underlies the efficacy of calcipotriol and corticosteroid therapy for psoriasis. JCI Insight 2019;4: «PMID: 30674716»PubMed
- Barnes L, Altmeyer P, Fôrstrôm L ym. Long-term treatment of psoriasis with calcipotriol scalp solution and cream. Eur J Dermatol 2000;10:199-204 «PMID: 10725818»PubMed
- Ramsay CA, Berth-Jones J, Brundin G ym. Long-term use of topical calcipotriol in chronic plaque psoriasis. Dermatology 1994;189:260-4 «PMID: 7949479»PubMed
- Bruner CR, Feldman SR, Ventrapragada M ym. A systematic review of adverse effects associated with topical treatments for psoriasis. Dermatol Online J 2003;9:2 «PMID: 12639460»PubMed
- Carboni I, de Felice C, Bergamin A ym. Topical use of calcitriol 3 microg/g ointment in the treatment of mild-to-moderate psoriasis: results from an open-label study. J Eur Acad Dermatol Venereol 2005;19 Suppl 3:11-3 «PMID: 16274406»PubMed
- Ortonne JP, Humbert P, Nicolas JF ym. Intra-individual comparison of the cutaneous safety and efficacy of calcitriol 3 microg g(-1) ointment and calcipotriol 50 microg g(-1) ointment on chronic plaque psoriasis localized in facial, hairline, retroauricular or flexural areas. Br J Dermatol 2003;148:326-33 «PMID: 12588387»PubMed
- Bourke JF, Iqbal SJ, Hutchinson PE. Vitamin D analogues in psoriasis: effects on systemic calcium homeostasis. Br J Dermatol 1996;135:347-54 «PMID: 8949424»PubMed
- Berth-Jones J, Bourke JF, Iqbal SJ ym. Urine calcium excretion during treatment of psoriasis with topical calcipotriol. Br J Dermatol 1993;129:411-4 «PMID: 8217755»PubMed
- Koo J, Tyring S, Werschler WP ym. Superior efficacy of calcipotriene and betamethasone dipropionate aerosol foam versus ointment in patients with psoriasis vulgaris--A randomized phase II study. J Dermatolog Treat 2016;27:120-7 «PMID: 26444907»PubMed
- Paul C, Stein Gold L, Cambazard F ym. Calcipotriol plus betamethasone dipropionate aerosol foam provides superior efficacy vs. gel in patients with psoriasis vulgaris: randomized, controlled PSO-ABLE study. J Eur Acad Dermatol Venereol 2017;31:119-126 «PMID: 27531752»PubMed
- Zonneveld IM, Rubins A, Jablonska S ym. Topical tacrolimus is not effective in chronic plaque psoriasis. A pilot study. Arch Dermatol 1998;134:1101-2 «PMID: 9762021»PubMed
- Harth W, Caffier PP, Mayelzadeh B ym. Topical tacrolimus treatment for chronic dermatitis of the ear. Eur J Dermatol 2007;17:405-11 «PMID: 17673384»PubMed
- Crowley JJ, Weinberg JM, Wu JJ ym. Treatment of nail psoriasis: best practice recommendations from the Medical Board of the National Psoriasis Foundation. JAMA Dermatol 2015;151:87-94 «PMID: 25471223»PubMed
- Gümüsel M, Özdemir M, Mevlitoglu I ym. Evaluation of the efficacy of methotrexate and cyclosporine therapies on psoriatic nails: a one-blind, randomized study. J Eur Acad Dermatol Venereol 2011;25:1080-4 «PMID: 21118309»PubMed
- Jiaravuthisan MM, Sasseville D, Vender RB ym. Psoriasis of the nail: anatomy, pathology, clinical presentation, and a review of the literature on therapy. J Am Acad Dermatol 2007;57:1-27 «PMID: 17572277»PubMed
- Tosti A, Ricotti C, Romanelli P ym. Evaluation of the efficacy of acitretin therapy for nail psoriasis. Arch Dermatol 2009;145:269-71 «PMID: 19289755»PubMed
- Yones SS, Palmer RA, Garibaldinos TT ym. Randomized double-blind trial of the treatment of chronic plaque psoriasis: efficacy of psoralen-UV-A therapy vs narrowband UV-B therapy. Arch Dermatol 2006;142:836-42 «PMID: 16847198»PubMed
- Hearn RM, Kerr AC, Rahim KF ym. Incidence of skin cancers in 3867 patients treated with narrow-band ultraviolet B phototherapy. Br J Dermatol 2008;159:931-5 «PMID: 18834483»PubMed
- Ibbotson SH, Bilsland D, Cox NH ym. An update and guidance on narrowband ultraviolet B phototherapy: a British Photodermatology Group Workshop Report. Br J Dermatol 2004;151:283-97 «PMID: 15327535»PubMed
- Diffey BL. Factors affecting the choice of a ceiling on the number of exposures with TL01 ultraviolet B phototherapy. Br J Dermatol 2003;149:428-30 «PMID: 12932263»PubMed
- Koek MB, Buskens E, van Weelden H ym. Home versus outpatient ultraviolet B phototherapy for mild to severe psoriasis: pragmatic multicentre randomised controlled non-inferiority trial (PLUTO study). BMJ 2009;338:b1542 «PMID: 19423623»PubMed
- Koek MB, Sigurdsson V, van Weelden H ym. Cost effectiveness of home ultraviolet B phototherapy for psoriasis: economic evaluation of a randomised controlled trial (PLUTO study). BMJ 2010;340:c1490 «PMID: 20406865»PubMed
- Koek MB, Buskens E, Bruijnzeel-Koomen CA ym. Home ultraviolet B phototherapy for psoriasis: discrepancy between literature, guidelines, general opinions and actual use. Results of a literature review, a web search, and a questionnaire among dermatologists. Br J Dermatol 2006;154:701-11 «PMID: 16536814»PubMed
- Koek MB, Buskens E, Steegmans PH ym. UVB phototherapy in an outpatient setting or at home: a pragmatic randomised single-blind trial designed to settle the discussion. The PLUTO study. BMC Med Res Methodol 2006;6:39 «PMID: 16882343»PubMed
- Voss A, Leverkus M, Bröcker EB ym. Topical psoralen photochemotherapy with lethal outcome. Arch Dermatol 2001;137:383 «PMID: 11255360»PubMed
- Hannuksela-Svahn A, Pukkala E, Koulu L ym. Cancer incidence among Finnish psoriasis patients treated with 8-methoxypsoralen bath PUVA. J Am Acad Dermatol 1999;40:694-6 «PMID: 10321595»PubMed
- Stern RS, Liebman EJ, Väkevä L. Oral psoralen and ultraviolet-A light (PUVA) treatment of psoriasis and persistent risk of nonmelanoma skin cancer. PUVA Follow-up Study. J Natl Cancer Inst 1998;90:1278-84 «PMID: 9731734»PubMed
- Stern RS, PUVA Follow up Study.. The risk of melanoma in association with long-term exposure to PUVA. J Am Acad Dermatol 2001;44:755-61 «PMID: 11312420»PubMed
- Griffiths CE, Clark CM, Chalmers RJ ym. A systematic review of treatments for severe psoriasis. Health Technol Assess 2000;4:1-125 «PMID: 11207450»PubMed
- Stern RS, Lunder EJ. Risk of squamous cell carcinoma and methoxsalen (psoralen) and UV-A radiation (PUVA). A meta-analysis. Arch Dermatol 1998;134:1582-5 «PMID: 9875197»PubMed
- Lebwohl M, Menter A, Koo J ym. Combination therapy to treat moderate to severe psoriasis. J Am Acad Dermatol 2004;50:416-30 «PMID: 14988684»PubMed
- Sugie N, Fujii N, Danno K. Cyclosporin-A suppresses p53-dependent repair DNA synthesis and apoptosis following ultraviolet-B irradiation. Photodermatol Photoimmunol Photomed 2002;18:163-8 «PMID: 12390669»PubMed
- Paul CF, Ho VC, McGeown C ym. Risk of malignancies in psoriasis patients treated with cyclosporine: a 5 y cohort study. J Invest Dermatol 2003;120:211-6 «PMID: 12542524»PubMed
- Marcil I, Stern RS. Squamous-cell cancer of the skin in patients given PUVA and ciclosporin: nested cohort crossover study. Lancet 2001;358:1042-5 «PMID: 11589933»PubMed
- Murphy GM. Skin cancer in patients with psoriasis-many intertwined risk factors. Br J Dermatol 1999;141:1001-2 «PMID: 10606842»PubMed
- Snellman E. E. Heliotherapy of psoriasis (thesis). Publications of the Social Insurance Institution, Finland, ML 124 1993;
- Puig L. PASI90 response: the new standard in therapeutic efficacy for psoriasis. J Eur Acad Dermatol Venereol 2015;29:645-8 «PMID: 25370811»PubMed
- Strober B, Papp KA, Lebwohl M ym. Clinical meaningfulness of complete skin clearance in psoriasis. J Am Acad Dermatol 2016;75:77-82.e7 «PMID: 27206759»PubMed
- Elewski BE, Puig L, Mordin M ym. Psoriasis patients with psoriasis Area and Severity Index (PASI) 90 response achieve greater health-related quality-of-life improvements than those with PASI 75-89 response: results from two phase 3 studies of secukinumab. J Dermatolog Treat 2017;28:492-499 «PMID: 28266243»PubMed
- Sbidian E, Maza A, Montaudié H ym. Efficacy and safety of oral retinoids in different psoriasis subtypes: a systematic literature review. J Eur Acad Dermatol Venereol 2011;25 Suppl 2:28-33 «PMID: 21388456»PubMed
- Gollnick H, Bauer R, Brindley C ym. Acitretin versus etretinate in psoriasis. Clinical and pharmacokinetic results of a German multicenter study. J Am Acad Dermatol 1988;19:458-68 «PMID: 2971692»PubMed
- Ruzicka T, Sommerburg C, Braun-Falco O ym. Efficiency of acitretin in combination with UV-B in the treatment of severe psoriasis. Arch Dermatol 1990;126:482-6 «PMID: 2138875»PubMed
- Warren RB, Weatherhead SC, Smith CH ym. British Association of Dermatologists' guidelines for the safe and effective prescribing of methotrexate for skin disease 2016. Br J Dermatol 2016;175:23-44 «PMID: 27484275»PubMed
- Anttila VJ, Haapamäki J, Peltomaa R ym. [Interruption of biological drugs in patients affected with inflammatory diseases]. Duodecim 2016;132:369-76 «PMID: 27017789»PubMed
- Ryan C, Amor KT, Menter A. The use of cyclosporine in dermatology: part II. J Am Acad Dermatol 2010;63:949-72; quiz 973-4 «PMID: 21093660»PubMed
- Koo J, Lebwohl M. Duration of remission of psoriasis therapies. J Am Acad Dermatol 1999;41:51-9 «PMID: 10411411»PubMed
- Berbis P, Geiger JM, Vaisse C ym. Benefit of progressively increasing doses during the initial treatment with acitretin in psoriasis. Dermatologica 1989;178:88-92 «PMID: 2522405»PubMed
- Murray HE, Anhalt AW, Lessard R ym. A 12-month treatment of severe psoriasis with acitretin: results of a Canadian open multicenter study. J Am Acad Dermatol 1991;24:598-602 «PMID: 1827800»PubMed
- Roenigk HH Jr, Callen JP, Guzzo CA ym. Effects of acitretin on the liver. J Am Acad Dermatol 1999;41:584-8 «PMID: 10495381»PubMed
- Kuitunen T, Malmström J, Palva E ym. Pancytopenia induced by low-dose methotrexate. A study of the cases reported to the Finnish Adverse Drug Reaction Register From 1991 to 1999. Scand J Rheumatol 2005;34:238-41 «PMID: 16134732»PubMed
- Lim AY, Gaffney K, Scott DG. Methotrexate-induced pancytopenia: serious and under-reported? Our experience of 25 cases in 5 years. Rheumatology (Oxford) 2005;44:1051-5 «PMID: 15901903»PubMed
- Whiting-O'Keefe QE, Fye KH, Sack KD. Methotrexate and histologic hepatic abnormalities: a meta-analysis. Am J Med 1991;90:711-6 «PMID: 1828327»PubMed
- Barker J, Horn EJ, Lebwohl M ym. Assessment and management of methotrexate hepatotoxicity in psoriasis patients: report from a consensus conference to evaluate current practice and identify key questions toward optimizing methotrexate use in the clinic. J Eur Acad Dermatol Venereol 2011;25:758-64 «PMID: 21198946»PubMed
- Kent PD, Luthra HS, Michet C Jr. Risk factors for methotrexate-induced abnormal laboratory monitoring results in patients with rheumatoid arthritis. J Rheumatol 2004;31:1727-31 «PMID: 15338491»PubMed
- Alarcón GS, Kremer JM, Macaluso M ym. Risk factors for methotrexate-induced lung injury in patients with rheumatoid arthritis. A multicenter, case-control study. Methotrexate-Lung Study Group. Ann Intern Med 1997;127:356-64 «PMID: 9273826»PubMed
- Griffiths CE, Dubertret L, Ellis CN ym. Ciclosporin in psoriasis clinical practice: an international consensus statement. Br J Dermatol 2004;150 Suppl 67:11-23 «PMID: 15115441»PubMed
- Reich K, Gooderham M, Bewley A ym. Safety and efficacy of apremilast through 104 weeks in patients with moderate to severe psoriasis who continued on apremilast or switched from etanercept treatment: findings from the LIBERATE study. J Eur Acad Dermatol Venereol 2018;32:397-402 «PMID: 29220542»PubMed
- Mrowietz U, Szepietowski JC, Loewe R ym. Efficacy and safety of LAS41008 (dimethyl fumarate) in adults with moderate-to-severe chronic plaque psoriasis: a randomized, double-blind, Fumaderm® - and placebo-controlled trial (BRIDGE). Br J Dermatol 2017;176:615-623 «PMID: 27515097»PubMed
- Mrowietz U, Kragballe K, Reich K ym. Definition of treatment goals for moderate to severe psoriasis: a European consensus. Arch Dermatol Res 2011;303:1-10 «PMID: 20857129»PubMed
- Götestam Skorpen C, Hoeltzenbein M, Tincani A ym. The EULAR points to consider for use of antirheumatic drugs before pregnancy, and during pregnancy and lactation. Ann Rheum Dis 2016;75:795-810 «PMID: 26888948»PubMed
- Lecluse LL, Driessen RJ, Spuls PI ym. Extent and clinical consequences of antibody formation against adalimumab in patients with plaque psoriasis. Arch Dermatol 2010;146:127-32 «PMID: 20157022»PubMed
- Hoffmann JH, Hartmann M, Enk AH ym. Autoantibodies in psoriasis as predictors for loss of response and anti-infliximab antibody induction. Br J Dermatol 2011;165:1355-8 «PMID: 21801160»PubMed
- Kimball AB, Gordon KB, Fakharzadeh S ym. Long-term efficacy of ustekinumab in patients with moderate-to-severe psoriasis: results from the PHOENIX 1 trial through up to 3 years. Br J Dermatol 2012;166:861-72 «PMID: 22356258»PubMed
- Hsu L, Snodgrass BT, Armstrong AW. Antidrug antibodies in psoriasis: a systematic review. Br J Dermatol 2014;170:261-73 «PMID: 24117166»PubMed
- Germano V, Cattaruzza MS, Osborn J ym. Infection risk in rheumatoid arthritis and spondyloarthropathy patients under treatment with DMARDs, corticosteroids and TNF-a antagonists. J Transl Med 2014;12:77 «PMID: 24655394»PubMed
- Galloway JB, Hyrich KL, Mercer LK ym. Anti-TNF therapy is associated with an increased risk of serious infections in patients with rheumatoid arthritis especially in the first 6 months of treatment: updated results from the British Society for Rheumatology Biologics Register with special emphasis on risks in the elderly. Rheumatology (Oxford) 2011;50:124-31 «PMID: 20675706»PubMed
- García-Doval I, Hernández MV, Vanaclocha F ym. Should tumour necrosis factor antagonist safety information be applied from patients with rheumatoid arthritis to psoriasis? Rates of serious adverse events in the prospective rheumatoid arthritis BIOBADASER and psoriasis BIOBADADERM cohorts. Br J Dermatol 2017;176:643-649 «PMID: 27258623»PubMed
- Yiu ZZN, Exton LS, Jabbar-Lopez Z ym. Risk of Serious Infections in Patients with Psoriasis on Biologic Therapies: A Systematic Review and Meta-Analysis. J Invest Dermatol 2016;136:1584-1591 «PMID: 27085754»PubMed
- Dávila-Seijo P, Dauden E, Descalzo MA ym. Infections in Moderate to Severe Psoriasis Patients Treated with Biological Drugs Compared to Classic Systemic Drugs: Findings from the BIOBADADERM Registry. J Invest Dermatol 2017;137:313-321 «PMID: 27677836»PubMed
- Garcia-Doval I, Cohen AD, Cazzaniga S ym. Risk of serious infections, cutaneous bacterial infections, and granulomatous infections in patients with psoriasis treated with anti-tumor necrosis factor agents versus classic therapies: Prospective meta-analysis of Psonet registries. J Am Acad Dermatol 2017;76:299-308.e16 «PMID: 27693008»PubMed
- Reich K, Mrowietz U, Radtke MA ym. Drug safety of systemic treatments for psoriasis: results from The German Psoriasis Registry PsoBest. Arch Dermatol Res 2015;307:875-83 «PMID: 26358263»PubMed
- Gniadecki R, Bang B, Bryld LE ym. Comparison of long-term drug survival and safety of biologic agents in patients with psoriasis vulgaris. Br J Dermatol 2015;172:244-52 «PMID: 25132294»PubMed
- Papp K, Gottlieb AB, Naldi L ym. Safety Surveillance for Ustekinumab and Other Psoriasis Treatments From the Psoriasis Longitudinal Assessment and Registry (PSOLAR). J Drugs Dermatol 2015;14:706-14 «PMID: 26151787»PubMed
- Crowley JJ, Warren RB, Cather JC. Safety of selective IL-23p19 inhibitors for the treatment of psoriasis. J Eur Acad Dermatol Venereol 2019;33:1676-1684 «PMID: 31054215»PubMed
- Sahuquillo-Torralba A, Carretero G, Rivera R ym. The risk of urinary tract infections in patients with psoriasis on systemic medications in Biobadaderm Registry: A prospective cohort study. J Am Acad Dermatol 2020;82:738-741 «PMID: 31306726»PubMed
- Mariette X, Matucci-Cerinic M, Pavelka K ym. Malignancies associated with tumour necrosis factor inhibitors in registries and prospective observational studies: a systematic review and meta-analysis. Ann Rheum Dis 2011;70:1895-904 «PMID: 21885875»PubMed
- van Lümig PP, Driessen RJ, Berends MA ym. Safety of treatment with biologics for psoriasis in daily practice: 5-year data. J Eur Acad Dermatol Venereol 2012;26:283-91 «PMID: 21435026»PubMed
- Raaschou P, Simard JF, Asker Hagelberg C ym. Rheumatoid arthritis, anti-tumour necrosis factor treatment, and risk of squamous cell and basal cell skin cancer: cohort study based on nationwide prospectively recorded data from Sweden. BMJ 2016;352:i262 «PMID: 26823527»PubMed
- Raaschou P, Simard JF, Holmqvist M ym. Rheumatoid arthritis, anti-tumour necrosis factor therapy, and risk of malignant melanoma: nationwide population based prospective cohort study from Sweden. BMJ 2013;346:f1939 «PMID: 23568792»PubMed
- Nyboe Andersen N, Pasternak B, Basit S ym. Association between tumor necrosis factor-a antagonists and risk of cancer in patients with inflammatory bowel disease. JAMA 2014;311:2406-13 «PMID: 24938563»PubMed
- Papoutsaki M, Chimenti MS, Costanzo A ym. Adalimumab for severe psoriasis and psoriatic arthritis: an open-label study in 30 patients previously treated with other biologics. J Am Acad Dermatol 2007;57:269-75 «PMID: 17574299»PubMed
- Van Lümig PP, Lecluse LL, Driessen RJ ym. Switching from etanercept to adalimumab is effective and safe: results in 30 patients with psoriasis with primary failure, secondary failure or intolerance to etanercept. Br J Dermatol 2010;163:838-46 «PMID: 20649798»PubMed
- Woolf RT, Smith CH, Robertson K ym. Switching to adalimumab in patients with moderate to severe psoriasis who have failed on etanercept: a retrospective case cohort study. Br J Dermatol 2010;163:889-92 «PMID: 20854408»PubMed
- Strober BE, Poulin Y, Kerdel FA ym. Switching to adalimumab for psoriasis patients with a suboptimal response to etanercept, methotrexate, or phototherapy: efficacy and safety results from an open-label study. J Am Acad Dermatol 2011;64:671-81 «PMID: 21414495»PubMed
- Ortonne JP, Chimenti S, Reich K ym. Efficacy and safety of adalimumab in patients with psoriasis previously treated with anti-tumour necrosis factor agents: subanalysis of BELIEVE. J Eur Acad Dermatol Venereol 2011;25:1012-20 «PMID: 21214631»PubMed
- Papp K, Crowley J, Ortonne JP ym. Adalimumab for moderate to severe chronic plaque psoriasis: efficacy and safety of retreatment and disease recurrence following withdrawal from therapy. Br J Dermatol 2011;164:434-41 «PMID: 21083543»PubMed
- Chiu HY, Wang TS, Chan CC ym. Risk Factor Analysis for the Immunogenicity of Adalimumab Associated with Decreased Clinical Response in Chinese Patients with Psoriasis. Acta Derm Venereol 2015;95:711-6 «PMID: 25673333»PubMed
- Thaçi D, Ortonne JP, Chimenti S ym. A phase IIIb, multicentre, randomized, double-blind, vehicle-controlled study of the efficacy and safety of adalimumab with and without calcipotriol/betamethasone topical treatment in patients with moderate to severe psoriasis: the BELIEVE study. Br J Dermatol 2010;163:402-11 «PMID: 20377585»PubMed
- Bagel J. Adalimumab plus narrowband ultraviolet B light phototherapy for the treatment of moderate to severe psoriasis. J Drugs Dermatol 2011;10:366-71 «PMID: 21455546»PubMed
- Wolf P, Hofer A, Weger W ym. 311 nm ultraviolet B-accelerated response of psoriatic lesions in adalimumab-treated patients. Photodermatol Photoimmunol Photomed 2011;27:186-9 «PMID: 21729166»PubMed
- Heiberg MS, Koldingsnes W, Mikkelsen K ym. The comparative one-year performance of anti-tumor necrosis factor alpha drugs in patients with rheumatoid arthritis, psoriatic arthritis, and ankylosing spondylitis: results from a longitudinal, observational, multicenter study. Arthritis Rheum 2008;59:234-40 «PMID: 18240258»PubMed
- Schreiber S, Ben-Horin S, Leszczyszyn J ym. Randomized Controlled Trial: Subcutaneous vs Intravenous Infliximab CT-P13 Maintenance in Inflammatory Bowel Disease. Gastroenterology 2021;160:2340-53 «PMID: 33676969»PubMed
- Westhovens R, Wiland P, Zawadzki M ym. Efficacy, pharmacokinetics and safety of subcutaneous versus intravenous CT-P13 in rheumatoid arthritis: a randomized phase I/III trial. Rheumatology (Oxford) 2021;60:2277-87 «PMID: 33230526»PubMed
- Gordon KB, Foley P, Krueger JG ym. Bimekizumab efficacy and safety in moderate to severe plaque psoriasis (BE READY): a multicentre, double-blind, placebo-controlled, randomised withdrawal phase 3 trial. Lancet 2021;397:475-486 «PMID: 33549192»PubMed
- Reich K, Papp KA, Blauvelt A ym. Bimekizumab versus ustekinumab for the treatment of moderate to severe plaque psoriasis (BE VIVID): efficacy and safety from a 52-week, multicentre, double-blind, active comparator and placebo controlled phase 3 trial. Lancet 2021;397:487-498 «PMID: 33549193»PubMed
- Reich K, Warren RB, Lebwohl M ym. Bimekizumab versus Secukinumab in Plaque Psoriasis. N Engl J Med 2021;385:142-152 «PMID: 33891380»PubMed
- Warren RB, Blauvelt A, Bagel J ym. Bimekizumab versus Adalimumab in Plaque Psoriasis. N Engl J Med 2021;385:130-141 «PMID: 33891379»PubMed
- Blauvelt A, Papp KA, Merola JF ym. Bimekizumab for patients with moderate to severe plaque psoriasis: 60-week results from BE ABLE 2, a randomized, double-blinded, placebo-controlled, phase 2b extension study. J Am Acad Dermatol 2020;83:1367-1374 «PMID: 32473974»PubMed
- Papp KA, Reich K, Paul C ym. A prospective phase III, randomized, double-blind, placebo-controlled study of brodalumab in patients with moderate-to-severe plaque psoriasis. Br J Dermatol 2016;175:273-86 «PMID: 26914406»PubMed
- Lebwohl M, Strober B, Menter A ym. Phase 3 Studies Comparing Brodalumab with Ustekinumab in Psoriasis. N Engl J Med 2015;373:1318-28 «PMID: 26422722»PubMed
- Papp KA, Tyring S, Lahfa M ym. A global phase III randomized controlled trial of etanercept in psoriasis: safety, efficacy, and effect of dose reduction. Br J Dermatol 2005;152:1304-12 «PMID: 15948997»PubMed
- Gordon KB, Gottlieb AB, Leonardi CL ym. Clinical response in psoriasis patients discontinued from and then reinitiated on etanercept therapy. J Dermatolog Treat 2006;17:9-17 «PMID: 16467018»PubMed
- Moore A, Gordon KB, Kang S ym. A randomized, open-label trial of continuous versus interrupted etanercept therapy in the treatment of psoriasis. J Am Acad Dermatol 2007;56:598-603 «PMID: 17113190»PubMed
- Ortonne J, Griffiths C, Daudén Ey. Efficacy and safety of continuous versus paused etanercept treatment in patients with moderate-to-severe psoriasis over 54 weeks: the CRYSTEL study. Expert Rev Dermatol 2008;3:657-65
- Ortonne JP, Taïeb A, Ormerod AD ym. Patients with moderate-to-severe psoriasis recapture clinical response during re-treatment with etanercept. Br J Dermatol 2009;161:1190-5 «PMID: 19566665»PubMed
- Foley PA, Quirk C, Sullivan JR ym. Combining etanercept with traditional agents in the treatment of psoriasis: a review of the clinical evidence. J Eur Acad Dermatol Venereol 2010;24:1135-43 «PMID: 20337816»PubMed
- Zachariae C, Mørk NJ, Reunala T ym. The combination of etanercept and methotrexate increases the effectiveness of treatment in active psoriasis despite inadequate effect of methotrexate therapy. Acta Derm Venereol 2008;88:495-501 «PMID: 18779890»PubMed
- Gottlieb AB, Langley RG, Strober BE ym. A randomized, double-blind, placebo-controlled study to evaluate the addition of methotrexate to etanercept in patients with moderate to severe plaque psoriasis. Br J Dermatol 2012;167:649-57 «PMID: 22533447»PubMed
- Blauvelt A, Papp KA, Griffiths CE ym. Efficacy and safety of guselkumab, an anti-interleukin-23 monoclonal antibody, compared with adalimumab for the continuous treatment of patients with moderate to severe psoriasis: Results from the phase III, double-blinded, placebo- and active comparator-controlled VOYAGE 1 trial. J Am Acad Dermatol 2017;76:405-417 «PMID: 28057360»PubMed
- Reich K, Armstrong AW, Foley P ym. Efficacy and safety of guselkumab, an anti-interleukin-23 monoclonal antibody, compared with adalimumab for the treatment of patients with moderate to severe psoriasis with randomized withdrawal and retreatment: Results from the phase III, double-blind, placebo- and active comparator-controlled VOYAGE 2 trial. J Am Acad Dermatol 2017;76:418-431 «PMID: 28057361»PubMed
- Lecluse LL, Piskin G, Mekkes JR ym. Review and expert opinion on prevention and treatment of infliximab-related infusion reactions. Br J Dermatol 2008;159:527-36 «PMID: 18627374»PubMed
- Gordon KB, Strober B, Lebwohl M ym. Efficacy and safety of risankizumab in moderate-to-severe plaque psoriasis (UltIMMa-1 and UltIMMa-2): results from two double-blind, randomised, placebo-controlled and ustekinumab-controlled phase 3 trials. Lancet 2018;392:650-661 «PMID: 30097359»PubMed
- Blauvelt A, Reich K, Lebwohl M ym. Certolizumab pegol for the treatment of patients with moderate-to-severe chronic plaque psoriasis: pooled analysis of week 16 data from three randomized controlled trials. J Eur Acad Dermatol Venereol 2019;33:546-552 «PMID: 30242918»PubMed
- Gottlieb AB, Blauvelt A, Thaçi D ym. Certolizumab pegol for the treatment of chronic plaque psoriasis: Results through 48 weeks from 2 phase 3, multicenter, randomized, double-blinded, placebo-controlled studies (CIMPASI-1 and CIMPASI-2). J Am Acad Dermatol 2018;79:302-314.e6 «PMID: 29660421»PubMed
- Papp KA, Reich K, Blauvelt A ym. Efficacy of tildrakizumab for moderate-to-severe plaque psoriasis: pooled analysis of three randomized controlled trials at weeks 12 and 28. J Eur Acad Dermatol Venereol 2019;33:1098-1106 «PMID: 30838709»PubMed
- Leonardi CL, Kimball AB, Papp KA ym. Efficacy and safety of ustekinumab, a human interleukin-12/23 monoclonal antibody, in patients with psoriasis: 76-week results from a randomised, double-blind, placebo-controlled trial (PHOENIX 1). Lancet 2008;371:1665-74 «PMID: 18486739»PubMed
- Papp KA, Langley RG, Lebwohl M ym. Efficacy and safety of ustekinumab, a human interleukin-12/23 monoclonal antibody, in patients with psoriasis: 52-week results from a randomised, double-blind, placebo-controlled trial (PHOENIX 2). Lancet 2008;371:1675-84 «PMID: 18486740»PubMed
- Talamonti M, Galluzzo M, Chimenti S ym. HLA-C*06 and response to ustekinumab in Caucasian patients with psoriasis: Outcome and long-term follow-up. J Am Acad Dermatol 2016;74:374-5 «PMID: 26775778»PubMed
- Gordon KB, Papp KA, Langley RG ym. Long-term safety experience of ustekinumab in patients with moderate to severe psoriasis (Part II of II): results from analyses of infections and malignancy from pooled phase II and III clinical trials. J Am Acad Dermatol 2012;66:742-51 «PMID: 21978572»PubMed
- Warren RB, Smith CH, Yiu ZZN ym. Differential Drug Survival of Biologic Therapies for the Treatment of Psoriasis: A Prospective Observational Cohort Study from the British Association of Dermatologists Biologic Interventions Register (BADBIR). J Invest Dermatol 2015;135:2632-2640 «PMID: 26053050»PubMed
- Zweegers J, van den Reek JM, van de Kerkhof PC ym. Body mass index predicts discontinuation due to ineffectiveness and female sex predicts discontinuation due to side-effects in patients with psoriasis treated with adalimumab, etanercept or ustekinumab in daily practice: a prospective, comparative, long-term drug-survival study from the BioCAPTURE registry. Br J Dermatol 2016;175:340-7 «PMID: 26989852»PubMed
- Menter A, Papp KA, Gooderham M ym. Drug survival of biologic therapy in a large, disease-based registry of patients with psoriasis: results from the Psoriasis Longitudinal Assessment and Registry (PSOLAR). J Eur Acad Dermatol Venereol 2016;30:1148-58 «PMID: 27027388»PubMed
- Kalb RE, Fiorentino DF, Lebwohl MG ym. Risk of Serious Infection With Biologic and Systemic Treatment of Psoriasis: Results From the Psoriasis Longitudinal Assessment and Registry (PSOLAR). JAMA Dermatol 2015;151:961-9 «PMID: 25970800»PubMed
- Carretero G, Ferrandiz C, Dauden E ym. Risk of adverse events in psoriasis patients receiving classic systemic drugs and biologics in a 5-year observational study of clinical practice: 2008-2013 results of the Biobadaderm registry. J Eur Acad Dermatol Venereol 2015;29:156-63 «PMID: 24684267»PubMed
- Lebwohl M, Leonardi C, Griffiths CE ym. Long-term safety experience of ustekinumab in patients with moderate-to-severe psoriasis (Part I of II): results from analyses of general safety parameters from pooled Phase 2 and 3 clinical trials. J Am Acad Dermatol 2012;66:731-41 «PMID: 21930328»PubMed
- Reich K, Papp KA, Griffiths CE ym. An update on the long-term safety experience of ustekinumab: results from the psoriasis clinical development program with up to four years of follow-up. J Drugs Dermatol 2012;11:300-12 «PMID: 22395580»PubMed
- Kimball AB, Papp KA, Wasfi Y ym. Long-term efficacy of ustekinumab in patients with moderate-to-severe psoriasis treated for up to 5 years in the PHOENIX 1 study. J Eur Acad Dermatol Venereol 2013;27:1535-45 «PMID: 23279003»PubMed
- Langley RG, Lebwohl M, Krueger GG ym. Long-term efficacy and safety of ustekinumab, with and without dosing adjustment, in patients with moderate-to-severe psoriasis: results from the PHOENIX 2 study through 5 years of follow-up. Br J Dermatol 2015;172:1371-83 «PMID: 25307931»PubMed
- Nast A, Sporbeck B, Rosumeck S ym. Which antipsoriatic drug has the fastest onset of action? Systematic review on the rapidity of the onset of action. J Invest Dermatol 2013;133:1963-70 «PMID: 23426133»PubMed
- Egeberg A, Andersen YMF, Halling-Overgaard AS ym. Systematic review on rapidity of onset of action for interleukin-17 and interleukin-23 inhibitors for psoriasis. J Eur Acad Dermatol Venereol 2020;34:39-46 «PMID: 31465593»PubMed
- Armstrong AW, Puig L, Joshi A ym. Comparison of Biologics and Oral Treatments for Plaque Psoriasis: A Meta-analysis. JAMA Dermatol 2020;156:258-269 «PMID: 32022825»PubMed
- Sbidian E, Chaimani A, Garcia-Doval I ym. Systemic pharmacological treatments for chronic plaque psoriasis: a network meta-analysis. Cochrane Database Syst Rev 2021;4:CD011535 «PMID: 33871055»PubMed
- Gladman DD, Farewell V, Buskila D ym. Reliability of measurements of active and damaged joints in psoriatic arthritis. J Rheumatol 1990;17:62-4 «PMID: 2313676»PubMed
- Oriente P, Biondi-Oriente C, Scarpa R. Psoriatic arthritis. Clinical manifestations. Baillieres Clin Rheumatol 1994;8:277-94 «PMID: 8076388»PubMed
- Cohen MR, Reda DJ, Clegg DO. Baseline relationships between psoriasis and psoriatic arthritis: analysis of 221 patients with active psoriatic arthritis. Department of Veterans Affairs Cooperative Study Group on Seronegative Spondyloarthropathies. J Rheumatol 1999;26:1752-6 «PMID: 10451073»PubMed
- Cantini F, Salvarani C, Olivieri I ym. Distal extremity swelling with pitting edema in psoriatic arthritis: a case-control study. Clin Exp Rheumatol 2001;19:291-6 «PMID: 11407082»PubMed
- Coates LC, Baraliakos X, Blanco FJ ym. The Phenotype of Axial Spondyloarthritis: Is It Dependent on HLA-B27 Status? Arthritis Care Res (Hoboken) 2021;73:856-860 «PMID: 32100954»PubMed
- Chandran V. Psoriatic spondylitis or ankylosing spondylitis with psoriasis: same or different? Curr Opin Rheumatol 2019;31:329-334 «PMID: 31135567»PubMed
- Payet J, Goulvestre C, Bialé L ym. Anticyclic citrullinated peptide antibodies in rheumatoid and nonrheumatoid rheumatic disorders: experience with 1162 patients. J Rheumatol 2014;41:2395-402 «PMID: 25274898»PubMed
- Kane D. The role of ultrasound in the diagnosis and management of psoriatic arthritis. Curr Rheumatol Rep 2005;7:319-24 «PMID: 16045836»PubMed
- Dubash SR, De Marco G, Wakefield RJ ym. Ultrasound Imaging in Psoriatic Arthritis: What Have We Learnt in the Last Five Years? Front Med (Lausanne) 2020;7:487 «PMID: 32984374»PubMed
- Balint PV, Terslev L, Aegerter P ym. Reliability of a consensus-based ultrasound definition and scoring for enthesitis in spondyloarthritis and psoriatic arthritis: an OMERACT US initiative. Ann Rheum Dis 2018;77:1730-1735 «PMID: 30076154»PubMed
- Offidani A, Cellini A, Valeri G ym. Subclinical joint involvement in psoriasis: magnetic resonance imaging and X-ray findings. Acta Derm Venereol 1998;78:463-5 «PMID: 9833050»PubMed
- Mandl P, Navarro-Compán V, Terslev L ym. EULAR recommendations for the use of imaging in the diagnosis and management of spondyloarthritis in clinical practice. Ann Rheum Dis 2015;74:1327-39 «PMID: 25837448»PubMed
- Gossec L, Baraliakos X, Kerschbaumer A ym. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2019 update. Ann Rheum Dis 2020;79:700-712 «PMID: 32434812»PubMed
- Singh JA, Guyatt G, Ogdie A ym. Special Article: 2018 American College of Rheumatology/National Psoriasis Foundation Guideline for the Treatment of Psoriatic Arthritis. Arthritis Care Res (Hoboken) 2019;71:2-29 «PMID: 30499259»PubMed
- Coates LC, Kavanaugh A, Mease PJ ym. Group for Research and Assessment of Psoriasis and Psoriatic Arthritis 2015 Treatment Recommendations for Psoriatic Arthritis. Arthritis Rheumatol 2016;68:1060-71 «PMID: 26749174»PubMed
- Sumpton D, Kelly A, Tunnicliffe DJ ym. Patients' Perspectives and Experience of Psoriasis and Psoriatic Arthritis: A Systematic Review and Thematic Synthesis of Qualitative Studies. Arthritis Care Res (Hoboken) 2020;72:711-722 «PMID: 30927508»PubMed
- Coates LC, Orbai AM, Azevedo VF ym. Results of a global, patient-based survey assessing the impact of psoriatic arthritis discussed in the context of the Psoriatic Arthritis Impact of Disease (PsAID) questionnaire. Health Qual Life Outcomes 2020;18:173 «PMID: 32513190»PubMed
- Garrido-Cumbrera M, Hillmann O, Mahapatra R ym. Improving the Management of Psoriatic Arthritis and Axial Spondyloarthritis: Roundtable Discussions with Healthcare Professionals and Patients. Rheumatol Ther 2017;4:219-231 «PMID: 28600789»PubMed
- Coates LC, Mahmood F, Freeston J ym. Long-term follow-up of patients in the TIght COntrol of inflammation in early Psoriatic Arthritis (TICOPA) trial. Rheumatology (Oxford) 2020;59:807-810 «PMID: 31504996»PubMed
- Coates LC, Fransen J, Helliwell PS. Defining minimal disease activity in psoriatic arthritis: a proposed objective target for treatment. Ann Rheum Dis 2010;69:48-53 «PMID: 19147615»PubMed
- Dressler C, Eisert L, Pham PA ym. Efficacy and safety of systemic treatments in psoriatic arthritis: a systematic review, meta-analysis and GRADE evaluation. J Eur Acad Dermatol Venereol 2019;33:1249-1260 «PMID: 30735612»PubMed
- Nash P, Thaçi D, Behrens F ym. Leflunomide improves psoriasis in patients with psoriatic arthritis: an in-depth analysis of data from the TOPAS study. Dermatology 2006;212:238-49 «PMID: 16549920»PubMed
- Flint J, Panchal S, Hurrell A ym. BSR and BHPR guideline on prescribing drugs in pregnancy and breastfeeding-Part I: standard and biologic disease modifying anti-rheumatic drugs and corticosteroids. Rheumatology (Oxford) 2016;55:1693-7 «PMID: 26750124»PubMed
- Brent RL. Teratogen update: reproductive risks of leflunomide (Arava); a pyrimidine synthesis inhibitor: counseling women taking leflunomide before or during pregnancy and men taking leflunomide who are contemplating fathering a child. Teratology 2001;63:106-12 «PMID: 11241434»PubMed
- Baker H, Ryan TJ. Generalized pustular psoriasis. A clinical and epidemiological study of 104 cases. Br J Dermatol 1968;80:771-93 «PMID: 4236712»PubMed
- Burns D, Breathnach S, Cox N ym. Rook´s Textbook of Dermatology. Blackwell Publishing 2004;
- Kavanaugh A, Gladman DD, Edwards CJ ym. Long-term experience with apremilast in patients with psoriatic arthritis: 5-year results from a PALACE 1-3 pooled analysis. Arthritis Res Ther 2019;21:118 «PMID: 31077258»PubMed
- Nash P, Ohson K, Walsh J ym. Early and sustained efficacy with apremilast monotherapy in biological-naïve patients with psoriatic arthritis: a phase IIIB, randomised controlled trial (ACTIVE). Ann Rheum Dis 2018;77:690-698 «PMID: 29343507»PubMed
- Wells AF, Edwards CJ, Kivitz AJ ym. Apremilast monotherapy in DMARD-naive psoriatic arthritis patients: results of the randomized, placebo-controlled PALACE 4 trial. Rheumatology (Oxford) 2018;57:1253-1263 «PMID: 29635379»PubMed
- Nash P, Coates LC, Fleischmann R ym. Efficacy of Tofacitinib for the Treatment of Psoriatic Arthritis: Pooled Analysis of Two Phase 3 Studies. Rheumatol Ther 2018;5:567-582 «PMID: 30414064»PubMed
- Mease P, Hall S, FitzGerald O ym. Tofacitinib or Adalimumab versus Placebo for Psoriatic Arthritis. N Engl J Med 2017;377:1537-1550 «PMID: 29045212»PubMed
- Mease PJ, Lertratanakul A, Papp KA ym. Upadacitinib in Patients with Psoriatic Arthritis and Inadequate Response to Biologics: 56-Week Data from the Randomized Controlled Phase 3 SELECT-PsA 2 Study. Rheumatol Ther 2021;8:903-919 «PMID: 33913086»PubMed
- Arnett FC, Edworthy SM, Bloch DA ym. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis. Arthritis Rheum 1988;31:315-24 «PMID: 3358796»PubMed
- Gladman DD, Mease PJ, Ritchlin CT ym. Adalimumab for long-term treatment of psoriatic arthritis: forty-eight week data from the adalimumab effectiveness in psoriatic arthritis trial. Arthritis Rheum 2007;56:476-88 «PMID: 17265483»PubMed
- Mease PJ. Biologic Therapy for Psoriatic Arthritis. Rheum Dis Clin North Am 2015;41:723-38 «PMID: 26476229»PubMed
- Ramiro S, Smolen JS, Landewé R ym. Pharmacological treatment of psoriatic arthritis: a systematic literature review for the 2015 update of the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis 2016;75:490-8 «PMID: 26660203»PubMed
- Kavanaugh A, van der Heijde D, McInnes IB ym. Golimumab in psoriatic arthritis: one-year clinical efficacy, radiographic, and safety results from a phase III, randomized, placebo-controlled trial. Arthritis Rheum 2012;64:2504-17 «PMID: 22378566»PubMed
- Kavanaugh A, McInnes IB, Mease P ym. Clinical efficacy, radiographic and safety findings through 5 years of subcutaneous golimumab treatment in patients with active psoriatic arthritis: results from a long-term extension of a randomised, placebo-controlled trial (the GO-REVEAL study). Ann Rheum Dis 2014;73:1689-94 «PMID: 24748630»PubMed
- Mease PJ, Goffe BS, Metz J ym. Etanercept in the treatment of psoriatic arthritis and psoriasis: a randomised trial. Lancet 2000;356:385-90 «PMID: 10972371»PubMed
- Mease PJ, Kivitz AJ, Burch FX ym. Etanercept treatment of psoriatic arthritis: safety, efficacy, and effect on disease progression. Arthritis Rheum 2004;50:2264-72 «PMID: 15248226»PubMed
- Antoni C, Krueger GG, de Vlam K ym. Infliximab improves signs and symptoms of psoriatic arthritis: results of the IMPACT 2 trial. Ann Rheum Dis 2005;64:1150-7 «PMID: 15677701»PubMed
- Kavanaugh A, Krueger GG, Beutler A ym. Infliximab maintains a high degree of clinical response in patients with active psoriatic arthritis through 1 year of treatment: results from the IMPACT 2 trial. Ann Rheum Dis 2007;66:498-505 «PMID: 17114188»PubMed
- Feletar M, Brockbank JE, Schentag CT ym. Treatment of refractory psoriatic arthritis with infliximab: a 12 month observational study of 16 patients. Ann Rheum Dis 2004;63:156-61 «PMID: 14722204»PubMed
- Kavanaugh A, Antoni CE, Gladman D ym. The Infliximab Multinational Psoriatic Arthritis Controlled Trial (IMPACT): results of radiographic analyses after 1 year. Ann Rheum Dis 2006;65:1038-43 «PMID: 16439444»PubMed
- Mease PJ, Fleischmann R, Deodhar AA ym. Effect of certolizumab pegol on signs and symptoms in patients with psoriatic arthritis: 24-week results of a Phase 3 double-blind randomised placebo-controlled study (RAPID-PsA). Ann Rheum Dis 2014;73:48-55 «PMID: 23942868»PubMed
- Ramiro S, Smolen JS, Landewé R ym. Pharmacological treatment of psoriatic arthritis: a systematic literature review for the 2015 update of the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis 2016;75:490-8 «PMID: 26660203»PubMed
- van der Heijde D, Deodhar A, FitzGerald O ym. 4-year results from the RAPID-PsA phase 3 randomised placebo-controlled trial of certolizumab pegol in psoriatic arthritis. RMD Open 2018;4:e000582 «PMID: 29556416»PubMed
- Kristensen LE, Keiserman M, Papp K, ym. Efficacy and safety of risankizumab for active psoriatic arthritis: 24-week results from the randomised, double-blind, phase 3 KEEPsAKE 1 trial. Ann Rheum Dis 2022;81(2):225-231 «PMID: 34911706»PubMed
- Östör A, Van den Bosch F, Papp K, ym. Efficacy and safety of risankizumab for active psoriatic arthritis: 24-week results from the randomised, double-blind, phase 3 KEEPsAKE 2 trial. Ann Rheum Dis 2022;81(3):351-358 «PMID: 34815219»PubMed
- Mease PJ, Kellner H, Morita A, ym. Long-Term Efficacy and Safety of Risankizumab in Patients with Active Psoriatic Arthritis: Results from a 76-Week Phase 2 Randomized Trial. Rheumatol Ther 2022;9(5):1361-1375 «PMID: 35931879»PubMed
- Östör A, Van den Bosch F, Papp K, ym. Efficacy and safety of risankizumab for active psoriatic arthritis: 52-week results from the KEEPsAKE 2 study. Rheumatology (Oxford) 2023;62(6):2122-2129 «PMID: 36282537»PubMed
- McInnes IB, Kavanaugh A, Gottlieb AB ym. Efficacy and safety of ustekinumab in patients with active psoriatic arthritis: 1 year results of the phase 3, multicentre, double-blind, placebo-controlled PSUMMIT 1 trial. Lancet 2013;382:780-9 «PMID: 23769296»PubMed
- Kavanaugh A, Puig L, Gottlieb AB ym. Maintenance of Clinical Efficacy and Radiographic Benefit Through Two Years of Ustekinumab Therapy in Patients With Active Psoriatic Arthritis: Results From a Randomized, Placebo-Controlled Phase III Trial. Arthritis Care Res (Hoboken) 2015;67:1739-49 «PMID: 26097039»PubMed
- Araujo EG, Englbrecht M, Hoepken S ym. Effects of ustekinumab versus tumor necrosis factor inhibition on enthesitis: Results from the enthesial clearance in psoriatic arthritis (ECLIPSA) study. Semin Arthritis Rheum 2019;48:632-637 «PMID: 30037432»PubMed
- Ruyssen-Witrand A, Perry R, Watkins C ym. Efficacy and safety of biologics in psoriatic arthritis: a systematic literature review and network meta-analysis. RMD Open 2020;6: «PMID: 32094304»PubMed
- McInnes IB, Asahina A, Coates LC, ym. Bimekizumab in patients with psoriatic arthritis, naive to biologic treatment: a randomised, double-blind, placebo-controlled, phase 3 trial (BE OPTIMAL). Lancet 2023;401(10370):25-37 «PMID: 36493791»PubMed
- Ritchlin CT, Kavanaugh A, Merola JF, ym. Bimekizumab in patients with active psoriatic arthritis: results from a 48-week, randomised, double-blind, placebo-controlled, dose-ranging phase 2b trial. Lancet 2020;395(10222):427-440 «PMID: 32035552»PubMed
- Merola JF, Landewé R, McInnes IB, ym. Bimekizumab in patients with active psoriatic arthritis and previous inadequate response or intolerance to tumour necrosis factor-α inhibitors: a randomised, double-blind, placebo-controlled, phase 3 trial (BE COMPLETE). Lancet 2023;401(10370):38-48 «PMID: 36495881»PubMed
- Coates LC, McInnes IB, Merola JF, ym. Safety and Efficacy of Bimekizumab in Patients With Active Psoriatic Arthritis: Three-Year Results From a Phase IIb Randomized Controlled Trial and Its Open-Label Extension Study. Arthritis Rheumatol 2022;74(12):1959-1970 «PMID: 35829656»PubMed
- Smolen JS, Mease P, Tahir H ym. Multicentre, randomised, open-label, parallel-group study evaluating the efficacy and safety of ixekizumab versus adalimumab in patients with psoriatic arthritis naïve to biological disease-modifying antirheumatic drug: final results by week 52. Ann Rheum Dis 2020;79:1310-1319 «PMID: 32660977»PubMed
- Mease PJ, McInnes IB, Kirkham B ym. Secukinumab Inhibition of Interleukin-17A in Patients with Psoriatic Arthritis. N Engl J Med 2015;373:1329-39 «PMID: 26422723»PubMed
- Mease P, van der Heijde D, Landewé R ym. Secukinumab improves active psoriatic arthritis symptoms and inhibits radiographic progression: primary results from the randomised, double-blind, phase III FUTURE 5 study. Ann Rheum Dis 2018;77:890-897 «PMID: 29550766»PubMed
- Mease PJ, Gottlieb AB, van der Heijde D ym. Efficacy and safety of abatacept, a T-cell modulator, in a randomised, double-blind, placebo-controlled, phase III study in psoriatic arthritis. Ann Rheum Dis 2017;76:1550-1558 «PMID: 28473423»PubMed
- Mourad A, Gniadecki R. Treatment of Dactylitis and Enthesitis in Psoriatic Arthritis with Biologic Agents: A Systematic Review and Metaanalysis. J Rheumatol 2020;47:59-65 «PMID: 30824641»PubMed
- Brüner M, Dige A, Loft AG ym. Spondylitis-psoriasis-enthesitis-enterocolitis-dactylitis-uveitis-peripheral synovitis (SPEED-UP) treatment. Autoimmun Rev 2021;20:102731 «PMID: 33326852»PubMed
- Noviani M, Feletar M, Nash P ym. Choosing the right treatment for patients with psoriatic arthritis. Ther Adv Musculoskelet Dis 2020;12:1759720X20962623 «PMID: 33133245»PubMed
- Mease P, Gottlieb A, McInnes I, Rahman P, Ch'ng Suyin S, Kollmeier A, et al. Low rates of radiographic progression with 2 years of Guselkumab: results from a phase-3/ randomized/double-blind/ placebo-controlled study of biologic-naïve active PsA patients. International journal of rheumatic diseases. 2023;26:113-4
- Mease PJ, Helliwell PS, Gladman DD, ym. Efficacy of guselkumab on axial involvement in patients with active psoriatic arthritis and sacroiliitis: a post-hoc analysis of the phase 3 DISCOVER-1 and DISCOVER-2 studies. Lancet Rheumatol 2021;3(10):e715-e723 «PMID: 38287608»PubMed
- Brown MA, Rudwaleit M, van Gaalen FA, ym. Low uveitis rates in patients with axial spondyloarthritis treated with bimekizumab: pooled results from phase 2b/3 trials. Ann Rheum Dis 2024;(): «PMID: 38977276»PubMed
- McInnes IB, Anderson JK, Magrey M, ym. Trial of Upadacitinib and Adalimumab for Psoriatic Arthritis. N Engl J Med 2021;384(13):1227-1239 «PMID: 33789011»PubMed
- Dai Q, Zhang Y, Liu Q, ym. Efficacy and safety of tofacitinib for chronic plaque psoriasis and psoriatic arthritis: a systematic review and meta-analysis of randomized controlled trials. Clin Rheumatol 2024;43(5):1605-1613 «PMID: 38517652»PubMed
- Gossec L, Kerschbaumer A, Ferreira RJO, ym. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2023 update. Ann Rheum Dis 2024;83(6):706-719 «PMID: 38499325»PubMed
- Kerschbaumer A, Smolen JS, Ferreira RJO, ym. Efficacy and safety of pharmacological treatment of psoriatic arthritis: a systematic literature research informing the 2023 update of the EULAR recommendations for the management of psoriatic arthritis. Ann Rheum Dis 2024;83(6):760-774 «PMID: 38503473»PubMed
- Tauscher AE, Fleischer AB Jr, Phelps KC ym. Psoriasis and pregnancy. J Cutan Med Surg 2002;6:561-70 «PMID: 12362257»PubMed
- Hale EK, Pomeranz MK. Dermatologic agents during pregnancy and lactation: an update and clinical review. Int J Dermatol 2002;41:197-203 «PMID: 12031026»PubMed
- Murase JE, Chan KK, Garite TJ ym. Hormonal effect on psoriasis in pregnancy and post partum. Arch Dermatol 2005;141:601-6 «PMID: 15897382»PubMed
- Raychaudhuri SP, Navare T, Gross J ym. Clinical course of psoriasis during pregnancy. Int J Dermatol 2003;42:518-20 «PMID: 12839599»PubMed
- Gudjonsson JE, Karason A, Runarsdottir EH ym. Distinct clinical differences between HLA-Cw*0602 positive and negative psoriasis patients--an analysis of 1019 HLA-C- and HLA-B-typed patients. J Invest Dermatol 2006;126:740-5 «PMID: 16439971»PubMed
- Yang YW, Chen CS, Chen YH ym. Psoriasis and pregnancy outcomes: a nationwide population-based study. J Am Acad Dermatol 2011;64:71-7 «PMID: 20970879»PubMed
- Mowad CM, Margolis DJ, Halpern AC ym. Hormonal influences on women with psoriasis. Cutis 1998;61:257-60 «PMID: 9608337»PubMed
- Ursin K, Lydersen S, Skomsvoll JF ym. Psoriatic Arthritis Disease Activity During and After Pregnancy: A Prospective Multicenter Study. Arthritis Care Res (Hoboken) 2019;71:1092-1100 «PMID: 30192071»PubMed
- Bobotsis R, Gulliver WP, Monaghan K ym. Psoriasis and adverse pregnancy outcomes: a systematic review of observational studies. Br J Dermatol 2016;175:464-72 «PMID: 26991866»PubMed
- Bandoli G, Johnson DL, Jones KL ym. Potentially modifiable risk factors for adverse pregnancy outcomes in women with psoriasis. Br J Dermatol 2010;163:334-9 «PMID: 20545678»PubMed
- Bae YS, Van Voorhees AS, Hsu S ym. Review of treatment options for psoriasis in pregnant or lactating women: from the Medical Board of the National Psoriasis Foundation. J Am Acad Dermatol 2012;67:459-77 «PMID: 22018758»PubMed
- Chi CC, Kirtschig G, Aberer W ym. Evidence-based (S3) guideline on topical corticosteroids in pregnancy. Br J Dermatol 2011;165:943-52 «PMID: 21729030»PubMed
- Chi CC, Wang SH, Wojnarowska F ym. Safety of topical corticosteroids in pregnancy. Cochrane Database Syst Rev 2015;:CD007346 «PMID: 26497573»PubMed
- Clowse ME, Förger F, Hwang C ym. Minimal to no transfer of certolizumab pegol into breast milk: results from CRADLE, a prospective, postmarketing, multicentre, pharmacokinetic study. Ann Rheum Dis 2017;76:1890-1896 «PMID: 28814432»PubMed
- Mariette X, Förger F, Abraham B ym. Lack of placental transfer of certolizumab pegol during pregnancy: results from CRIB, a prospective, postmarketing, pharmacokinetic study. Ann Rheum Dis 2018;77:228-233 «PMID: 29030361»PubMed
- Sihvonen S, Pertovaara M. Reumasairaudet raskauden aikana. Duodecim 2019;135:257-64
- Morris A, Rogers M, Fischer G ym. Childhood psoriasis: a clinical review of 1262 cases. Pediatr Dermatol 2001;18:188-98 «PMID: 11437997»PubMed
- Varni JW, Globe DR, Gandra SR ym. Health-related quality of life of pediatric patients with moderate to severe plaque psoriasis: comparisons to four common chronic diseases. Eur J Pediatr 2012;171:485-92 «PMID: 21960290»PubMed
- Siegfried EC. Neonatal skin and skin care. Dermatol Clin 1998;16:437-46 «PMID: 9704203»PubMed
- Chiou YB, Blume-Peytavi U. Stratum corneum maturation. A review of neonatal skin function. Skin Pharmacol Physiol 2004;17:57-66 «PMID: 14976382»PubMed
- Lebwohl M, Ali S. Treatment of psoriasis. Part 1. Topical therapy and phototherapy. J Am Acad Dermatol 2001;45:487-98; quiz 499-502 «PMID: 11568737»PubMed
- Sticherling M, Augustin M, Boehncke WH ym. Therapy of psoriasis in childhood and adolescence - a German expert consensus. J Dtsch Dermatol Ges 2011;9:815-23 «PMID: 21585653»PubMed
- de Jager ME, de Jong EM, van de Kerkhof PC ym. Efficacy and safety of treatments for childhood psoriasis: a systematic literature review. J Am Acad Dermatol 2010;62:1013-30 «PMID: 19900732»PubMed
- Jury CS, McHenry P, Burden AD ym. Narrowband ultraviolet B (UVB) phototherapy in children. Clin Exp Dermatol 2006;31:196-9 «PMID: 16487089»PubMed
- Pasic A, Ceovic R, Lipozencic J ym. Phototherapy in pediatric patients. Pediatr Dermatol 2003;20:71-7 «PMID: 12558852»PubMed
- Paller AS, Siegfried EC, Langley RG ym. Etanercept treatment for children and adolescents with plaque psoriasis. N Engl J Med 2008;358:241-51 «PMID: 18199863»PubMed
- Paller AS, Siegfried EC, Eichenfield LF ym. Long-term etanercept in pediatric patients with plaque psoriasis. J Am Acad Dermatol 2010;63:762-8 «PMID: 20605256»PubMed
- Paller AS, Siegfried EC, Pariser DM ym. Long-term safety and efficacy of etanercept in children and adolescents with plaque psoriasis. J Am Acad Dermatol 2016;74:280-7.e1-3 «PMID: 26775775»PubMed
- Landells I, Marano C, Hsu MC ym. Ustekinumab in adolescent patients age 12 to 17 years with moderate-to-severe plaque psoriasis: results of the randomized phase 3 CADMUS study. J Am Acad Dermatol 2015;73:594-603 «PMID: 26259989»PubMed
- Petty RE, Southwood TR, Manners P ym. International League of Associations for Rheumatology classification of juvenile idiopathic arthritis: second revision, Edmonton, 2001. J Rheumatol 2004;31:390-2 «PMID: 14760812»PubMed
- Butbul Aviel Y, Tyrrell P, Schneider R ym. Juvenile Psoriatic Arthritis (JPsA): juvenile arthritis with psoriasis? Pediatr Rheumatol Online J 2013;11:11 «PMID: 23497068»PubMed
- Ekelund M, Aalto K, Fasth A ym. Psoriasis and associated variables in classification and outcome of juvenile idiopathic arthritis - an eight-year follow-up study. Pediatr Rheumatol Online J 2017;15:13 «PMID: 28222745»PubMed
- Stoll ML, Nigrovic PA, Gotte AC ym. Clinical comparison of early-onset psoriatic and non-psoriatic oligoarticular juvenile idiopathic arthritis. Clin Exp Rheumatol 2011;29:582-8 «PMID: 21385553»PubMed
- Zisman D, Gladman DD, Stoll ML ym. The Juvenile Psoriatic Arthritis Cohort in the CARRA Registry: Clinical Characteristics, Classification, and Outcomes. J Rheumatol 2017;44:342-351 «PMID: 28148698»PubMed
- Stoll ML, Zurakowski D, Nigrovic LE ym. Patients with juvenile psoriatic arthritis comprise two distinct populations. Arthritis Rheum 2006;54:3564-72 «PMID: 17075862»PubMed
- Kröger L, Vähäsalo P, Tynjälä P ym. [Medical treatment of juvenile idiopathic arthritis]. Duodecim 2012;128:477-86 «PMID: 22486063»PubMed
- Ruperto N, Murray KJ, Gerloni V ym. A randomized trial of parenteral methotrexate comparing an intermediate dose with a higher dose in children with juvenile idiopathic arthritis who failed to respond to standard doses of methotrexate. Arthritis Rheum 2004;50:2191-201 «PMID: 15248217»PubMed
- van Rossum MA, Fiselier TJ, Franssen MJ ym. Sulfasalazine in the treatment of juvenile chronic arthritis: a randomized, double-blind, placebo-controlled, multicenter study. Dutch Juvenile Chronic Arthritis Study Group. Arthritis Rheum 1998;41:808-16 «PMID: 9588731»PubMed
- Silverman E, Mouy R, Spiegel L ym. Leflunomide or methotrexate for juvenile rheumatoid arthritis. N Engl J Med 2005;352:1655-66 «PMID: 15843668»PubMed
- Tynjälä P, Vähäsalo P, Tarkiainen M ym. Aggressive combination drug therapy in very early polyarticular juvenile idiopathic arthritis (ACUTE-JIA): a multicentre randomised open-label clinical trial. Ann Rheum Dis 2011;70:1605-12 «PMID: 21623000»PubMed
- Lovell DJ, Ruperto N, Goodman S ym. Adalimumab with or without methotrexate in juvenile rheumatoid arthritis. N Engl J Med 2008;359:810-20 «PMID: 18716298»PubMed
- Horneff G, Seyger MMB, Arikan D ym. Safety of Adalimumab in Pediatric Patients with Polyarticular Juvenile Idiopathic Arthritis, Enthesitis-Related Arthritis, Psoriasis, and Crohn's Disease. J Pediatr 2018;201:166-175.e3 «PMID: 30054164»PubMed
- Constantin T, Foeldvari I, Vojinovic J ym. Two-year Efficacy and Safety of Etanercept in Pediatric Patients with Extended Oligoarthritis, Enthesitis-related Arthritis, or Psoriatic Arthritis. J Rheumatol 2016;43:816-24 «PMID: 26932344»PubMed
- Foeldvari I, Constantin T, Vojinovic J ym. Etanercept treatment for extended oligoarticular juvenile idiopathic arthritis, enthesitis-related arthritis, or psoriatic arthritis: 6-year efficacy and safety data from an open-label trial. Arthritis Res Ther 2019;21:125 «PMID: 31122296»PubMed
- Otten MH, Prince FH, Ten Cate R ym. Tumour necrosis factor (TNF)-blocking agents in juvenile psoriatic arthritis: are they effective? Ann Rheum Dis 2011;70:337-40 «PMID: 21068101»PubMed
- Windschall D, Müller T, Becker I ym. Safety and efficacy of etanercept in children with the JIA categories extended oligoarthritis, enthesitis-related arthritis and psoriasis arthritis. Clin Rheumatol 2015;34:61-9 «PMID: 25034081»PubMed
- Hissink Muller PC, Brinkman DM, Schonenberg D ym. A comparison of three treatment strategies in recent onset non-systemic Juvenile Idiopathic Arthritis: initial 3-months results of the BeSt for Kids-study. Pediatr Rheumatol Online J 2017;15:11 «PMID: 28166785»PubMed
- Wallace CA, Giannini EH, Spalding SJ ym. Trial of early aggressive therapy in polyarticular juvenile idiopathic arthritis. Arthritis Rheum 2012;64:2012-21 «PMID: 22183975»PubMed
- Brunner HI, Ruperto N, Tzaribachev N ym. Subcutaneous golimumab for children with active polyarticular-course juvenile idiopathic arthritis: results of a multicentre, double-blind, randomised-withdrawal trial. Ann Rheum Dis 2018;77:21-29 «PMID: 28507219»PubMed
- De Benedetti F, Brunner HI, Ruperto N ym. Randomized trial of tocilizumab in systemic juvenile idiopathic arthritis. N Engl J Med 2012;367:2385-95 «PMID: 23252525»PubMed
- Brunner HI, Ruperto N, Zuber Z ym. Efficacy and safety of tocilizumab in patients with polyarticular-course juvenile idiopathic arthritis: results from a phase 3, randomised, double-blind withdrawal trial. Ann Rheum Dis 2015;74:1110-7 «PMID: 24834925»PubMed
- Grönlund MM, Remes-Pakarinen T, Kröger L ym. Efficacy and safety of tocilizumab in a real-life observational cohort of patients with polyarticular juvenile idiopathic arthritis. Rheumatology (Oxford) 2020;59:732-741 «PMID: 31359057»PubMed
- Lovell DJ, Ruperto N, Mouy R ym. Long-term safety, efficacy, and quality of life in patients with juvenile idiopathic arthritis treated with intravenous abatacept for up to seven years. Arthritis Rheumatol 2015;67:2759-70 «PMID: 26097215»PubMed
- Brunner HI, Foeldvari I, Alexeeva E, ym. Secukinumab in enthesitis-related arthritis and juvenile psoriatic arthritis: a randomised, double-blind, placebo-controlled, treatment withdrawal, phase 3 trial. Ann Rheum Dis 2023;82(1):154-160 «PMID: 35961761»PubMed
- Ramanan AV, Quartier P, Okamoto N, ym. Baricitinib in juvenile idiopathic arthritis: an international, phase 3, randomised, double-blind, placebo-controlled, withdrawal, efficacy, and safety trial. Lancet 2023;402(10401):555-570 «PMID: 37423231»PubMed
- Ruperto N, Brunner HI, Synoverska O, ym. Tofacitinib in juvenile idiopathic arthritis: a double-blind, placebo-controlled, withdrawal phase 3 randomised trial. Lancet 2021;398(10315):1984-1996 «PMID: 34767764»PubMed
- Rutter MK, Kane K, Lunt M ym. Primary care-based screening for cardiovascular risk factors in patients with psoriasis. Br J Dermatol 2016;175:348-56 «PMID: 26990294»PubMed