Atopiskt eksem
Hur kan man hänvisa till God medicinsk praxis-rekommendationen? «K1»1
Den här svenskspråkiga God medicinsk praxis-rekommendationen har översatts från den finska God medicinsk praxis-rekommendationen (Käypä hoito -suositus Atooppinen ekseema «Atooppinen ekseema»1). Om det finns skillnader i texterna gäller den uppdaterade finskspråkiga versionen.
Huvudsakligen finns evidenssammandragen och bakgrundsmaterialen samt internetlänkarna på finska.
Centrala rekommendationer
- Atopiskt eksem är en kronisk, kliande, inflammatorisk hudsjukdom. Typiskt för sjukdomen är försämringsskov som är svåra att förutse. Personer med atopiskt eksem upplever ofta också hudsmärta och beröringsömhet.
- Vid atopiskt eksem fungerar hudens skyddsbarriär sämre än i frisk hud.
- Vid atopiskt eksem kan man urskilja flera fenotyper enligt de bakomliggande genetiska faktorerna, till exempel patientens etniska bakgrund och inflammationsmekanismerna. Sjukdomens kliniska bild och inflammationssvar förändras med åldern.
- Diagnosen är klinisk och därför behövs laboratorie- eller allergiundersökningar i
allmänhet inte.
- En del barn under ett år med måttligt eller svårt eksem kan ha födoämnesallergi i bakgrunden. I andra patientgrupper behöver man i allmänhet inte leta efter födoämnesallergi.
- Det finns inga obestridliga metoder för att förebygga atopiskt eksem.
- Hos de flesta är sjukdomen lindrig och prognosen god. Svårt atopiskt eksem försämrar livskvaliteten och arbets- och funktionsförmågan.
- Målet med behandlingen är långvarig symtomkontroll: att minimera symtomen, minska
antalet skov och lindra svårighetsgraden samt förbättra patientens livskvalitet och
arbets- och funktionsförmåga.
- Validerade mätare kan användas för att bedöma eksemets svårighetsgrad och mäta sjukdomens inverkan på livskvaliteten. I synnerhet inom den specialiserade sjukvården rekommenderas att sjukdomens svårighetsgrad och effekter beskrivs med hjälp av mätare även i uppföljningen av vårdresponsen.
- Det atopiska eksemets svårighetsgrad påverkar valet av behandling; en adekvat behandling
av eksemet lindrar klådan bäst. Se behandlingsalgoritmen «Behandlingsalgoritm vid atopiskt eksem»1.
- Bassalvor används för att behandla torr hud vid atopiskt eksem. Inflammation i huden
behandlas med läkemedelssalvor och vid behov med systemisk läkemedelsbehandling eller
UV-behandling.
- De flesta patienter klarar sig med bassalva och en periodisk användning av lokala kortikosteroider.
- Om man inte får tillräcklig respons med en korrekt användning av lokala kortikosteroider används lokala kalcineurinhämmare som långtidsbehandling eller UV-behandling.
- Vid eksem som återkommer lätt rekommenderas underhållsbehandling med kortikosteroidsalva eller takrolimussalva två gånger i veckan.
- Beakta åldersgränserna och styrkan på olika kortikosteroidsalvor när du vårdar barn.
- Vid svår sjukdom behövs ofta långvarig systemisk läkemedelsbehandling som kan genomföras
med traditionella immunsuppressiva läkemedel, biologiska läkemedel eller januskinashämmare
(JAK).
- Läkemedelskostnaderna för responsen från biologiska läkemedel och JAK-hämmare presenteras i tabellen, se «https://www.terveysportti.fi/apps/laake/laakekustannus/hoi50077»1.
- Bassalvor används för att behandla torr hud vid atopiskt eksem. Inflammation i huden
behandlas med läkemedelssalvor och vid behov med systemisk läkemedelsbehandling eller
UV-behandling.
- En förutsättning för att behandlingen av atopiskt eksem ska lyckas är att patienterna
och föräldrarna till barnpatienter har tillräcklig information om atopiskt eksem och
dess behandling.
- Anvisningar om atopiskt eksem för föräldrar «Ohje vanhemmille atooppisesta ekseemasta»1
- Regelbunden användning av bassalvor, undvikande av faktorer som irriterar huden och
användning av läkemedelssalvor under aktivt eksem är hörnstenar i egenvården.
- Handledd egenvård av atopiskt eksem hos vuxna «hoi50077c.pdf»1
- Handledd egenvård av atopiskt eksem hos barn «hoi50077d.pdf»2
- Videor: Lokalbehandling av atopiskt eksem hos vuxna «Atooppinen ekseema -suosituksen videot (aikuiset)»2 och barn «Atooppinen ekseema -suosituksen videot (lapset)»3
- På grund av associerade sjukdomar till atopiskt eksem och den mångformiga sjukdomsbördan kan det behövas multiprofessionellt grepp om vården.
- Specialistkonsultation behövs om sjukdomen är omfattande eller svårbehandlad.
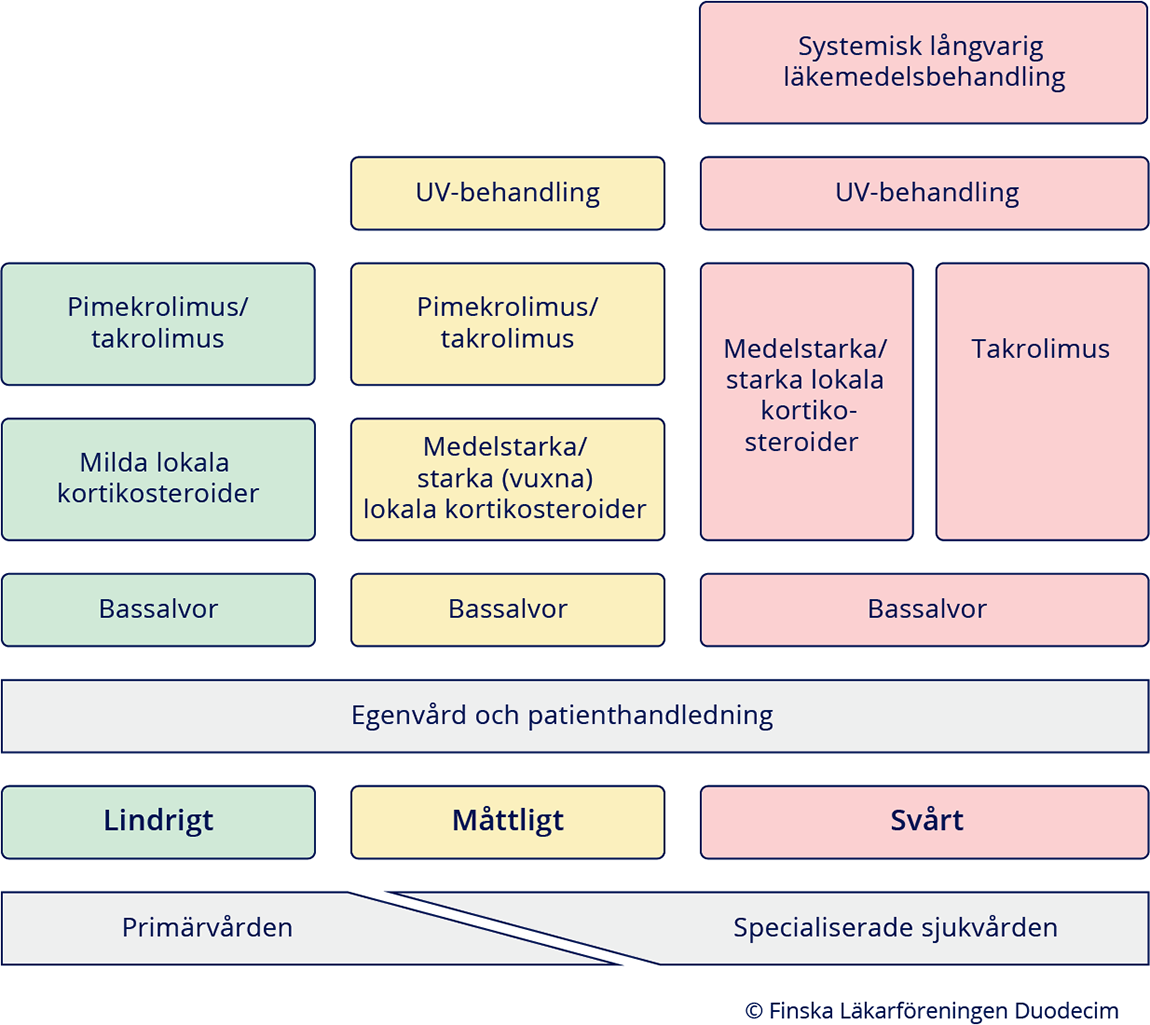
I behandlingen används bassalvor, kortikosteroidsalvor av olika styrka, kalcineurinhämmare och UV-behandling enligt eksemets svårighetsgrad. Vid svårt eksem kan invärtes läkemedelsbehandling behövas.
© Finska Läkarföreningen Duodecim
Rekommendationens syfte
- Syftet med rekommendationen är att skapa enhetlig praxis för diagnostik och behandling av atopiskt eksem samt att förtydliga nivåstruktureringen av diagnostiken och behandlingen. Målet är att behandlingen av atopiskt eksem ska grunda sig på forskningsevidens, vara jämlik och genomföras framgångsrikt.
Målgrupp
- Målgruppen för rekommendationen är yrkesutbildade personer inom hälso- och sjukvården som vårdar personer med atopiskt eksem.
Definition
- Atopiskt eksem (atopiska utslag, atopisk dermatit, böjveckseksem, "mjölkskorv") är en kronisk och kliande inflammatorisk hudsjukdom som kännetecknas av svårförutsägbara försämringsskov.
- Hos personer med atopiskt eksem är huden i allmänhet torr, även om eksem inte alltid kan observeras. Huden kan då kallas atopisk hud.
- Cirka 20–30 procent av personer med atopiskt eksem har inte atopisk allergibenägenhet, dvs. IgE-förmedlade allergier eller känslighet för de vanligaste allergenerna «Tokura Y, Hayano S. Subtypes of atopic dermatitis:...»1, «Johansson EK, Bergström A, Kull I ym. Prevalence a...»2.
Prevalens och prognos
- Prevalensen av atopiskt eksem hos barn är 10–20 procent «Williams H, Stewart A, von Mutius E ym. Is eczema ...»3. I en internationell, standardiserad studie av förekomsten av allergiska sjukdomar hade 24 procent av 13–14-åriga barn någon gång haft atopiskt eksem, 17 procent hade haft eksem under det senaste året och 0,9 procent hade haft svårt eksem under det senaste året «Williams H, Stewart A, von Mutius E ym. Is eczema ...»3. I en europeisk födelsekohortstudie, där även finländska barn deltog, var prevalensen av atopiskt eksem 27 procent vid 4 års ålder «Roduit C, Frei R, Loss G ym. Development of atopic...»4. Atopiskt eksem som bryter ut i barndomen börjar ge symtom hos hälften av patienterna under det första levnadsåret och hos 85 procent före det femte levnadsåret «Vakharia PP, Silverberg JI. Adult-Onset Atopic Der...»5.
- Av vuxna har 25–30 procent någon gång under sitt liv haft atopiskt eksem och cirka hälften av dem hade haft eksem under det föregående året «Vartiainen E, Petäys T, Haahtela T ym. Allergic di...»6, «von Hertzen L, Mäkelä MJ, Petäys T ym. Growing dis...»7, «Mortz CG, Andersen KE, Dellgren C ym. Atopic derma...»8. Hos vuxna är prevalensen av atopiskt eksem i olika studier 2–10 procent «Silverberg JI, Hanifin JM. Adult eczema prevalence...»9, «Barbarot S, Auziere S, Gadkari A ym. Epidemiology ...»10. I ett finländskt födelsekohortmaterial konstaterades atopiskt eksem vid studietidpunkten hos 4,8 procent av medelålders vuxna «Sinikumpu SP, Huilaja L, Jokelainen J ym. High pre...»11. Var fjärde vuxen patient med atopiskt eksem uppgav att eksemet börjat först i vuxen ålder «Lee HH, Patel KR, Singam V ym. A systematic review...»12.
- Av de personer som har atopiskt eksem bedöms cirka 10 procent ha en svår sjukdomsform. Hos barn är en svår sjukdomsform mer sällsynt «Langan SM, Irvine AD, Weidinger S. Atopic dermatit...»13, «Barbarot S, Auziere S, Gadkari A ym. Epidemiology ...»10.
- Atopiskt eksem har blivit vanligare under de senaste årtiondena på samma sätt som andra sjukdomar förknippade med atopiskt eksem (astma, allergisk snuva) och IgE-förmedlad allergi. I en finländsk studie bland beväringar tiodubblades prevalensen av atopiskt eksem under 1966–1987 och 2020 konstaterades att prevalensen ytterligare ökat något «Reijula J, Latvala J, Mäkelä M ym. Long-term trend...»14.
- Man har antagit att sjukdomsförloppet hos en stor del av barnpatienterna skulle följa den så kallade atopiska marschen, dvs. förekomsten av symtom i följande ordning: eksem, födoämnesallergier, astma och luftvägsallergier. I ljuset av nya omfattande kohortstudier följer symtomen den atopiska marschen endast hos en liten del av patienterna. Enligt befolkningsstudier fördubblar eller tredubblar atopiskt eksem i barndomen risken för att insjukna i astma och allergisk snuva «Dharmage SC, Lowe AJ, Matheson MC ym. Atopic derma...»15, «Haider S, Fontanella S, Ullah A ym. Evolution of E...»16.
- Hos en stor del av barnen läker eller lindras atopiskt eksem under årens lopp men kan förvärras på nytt i ungdomen eller vuxen ålder «IIlli S, von Mutius E, Lau S ym. The natural cours...»17, «Williams HC, Strachan DP. The natural history of c...»18.
- Läs mer om det atopiska eksemets naturliga förlopp «Atooppisen ekseeman luonnollinen kulku»4.
Etiologi och patogenes
- Bakgrunden till atopiskt eksem är den aktivering av inflammationsceller som orsakas av arvsmassan, en bristande funktion av hudens skyddsbarriär och immunologiska reaktioner, både i huden och systemiskt, vilket leder till torr hud, klåda och inflammation. Vid atopiskt eksem pågår flera processer som förstärker varandra.
- Enligt befolknings- och tvillingstudier är atopiskt eksem delvis ärftligt «Bieber T. Atopic dermatitis. N Engl J Med 2008;358...»19. Förekomsten av atopiskt eksem i den närmaste släkten är den viktigaste identifierade riskfaktorn «Langan SM, Irvine AD, Weidinger S. Atopic dermatit...»13. I en tysk studie konstaterades att atopiskt eksem hos modern eller fadern ungefär tredubblar barnets risk att insjukna i atopiskt eksem «Apfelbacher CJ, Diepgen TL, Schmitt J. Determinan...»20. Om båda föräldrarna har atopiskt eksem kan risken vara upp till fem gånger större.
- Kandidater för predispositionsgener för atopiskt eksem har i associationsstudier som omfattar hela arvsmassan hittats i generna hos proteiner som bygger upp och bearbetar hudens skyddsbarriär och i generna som styr immunförsvarets funktion «Sliz E, Huilaja L, Pasanen A ym. Uniting biobank r...»21.
- Filaggrinet i epidermis hornlager är ett av de viktigaste proteinerna i hudens skyddsbarriär. Mutationer av filaggringenen som leder till bristfällig funktion av hudbarriären är den mest kända enskilda genetiska faktorn som utsätter för atopiskt eksem. Dessa mutationer finns hos 20–40 procent av patienterna med atopiskt eksem «Palmer CN, Irvine AD, Terron-Kwiatkowski A ym. Com...»22. Endast 5,6 procent av de finländska patienter med atopiskt eksem, som vårdades inom den specialiserade sjukvården, konstaterades i ett europeiskt patientmaterial ha de vanligaste filaggrinmutationerna «Luukkonen TM, Kiiski V, Ahola M ym. The Value of F...»23.
- I huden hos en person med atopiskt eksem avviker keratinskiktets fettsyrasammansättning från lipidsammansättningen i frisk hud «van Smeden J, Bouwstra JA. Stratum Corneum Lipids:...»24, «Joo KM, Hwang JH, Bae S ym. Relationship of cerami...»25.
- En frisk hud har ett surt pH-värde på 4–6, men atopisk hud är alkalisk. Den atopiska hudens knappa svettning och avvikande fettsyrasammansättning höjer pH-värdet «Geoghegan JA, Irvine AD, Foster TJ: Staphylococcu...»26.
- Bakteriestammen (mikrobiom) hos atopisk hud är inte så mångformig som hos frisk hud «Atooppista ekseemaa sairastavilla on suurella osalla Staphylococcus aureus -bakteeri sekä ekseema-alueilla että terveeltä näyttävällä iholla. Atooppisessa ekseemassa bakteerikannan monimuotoisuus on vähäisempi kuin terveellä iholla.»A. Detta leder till att en stor del av patienterna med atopiskt eksem har en överrepresentation av bakterien Staphylococcus aureus både i eksemområden och på hud som ser frisk ut.
- Skyddsbarriären i epidermis är bristfällig i atopisk hud både i eksemområdet och på hud som ser frisk ut. Utöver de genetiska faktorerna försvagas skyddsbarriären av den mekaniska skada som orsakas av att man skrapar huden och av toxiner och proteaser från bakterien Staphylococcus aureus som koloniserar den atopiska huden. Mikrober, toxiska stimuli och allergener kan tränga in i huden och aktivera inflammatoriska celler. Typiska inflammationsmediatorer vid atopiskt eksem (IL-4, IL-13 och IL-31) förhindrar en ytterligare uppkomst av filaggrin och andra proteiner i skyddsbarriären «Langan SM, Irvine AD, Weidinger S. Atopic dermatit...»13, «Geoghegan JA, Irvine AD, Foster TJ: Staphylococcu...»26.
- Atopiskt eksem är alltid kliande. Alla hudlager har sensoriska nervceller som kan förmedla en signal om klåda till hjärnan och därmed utlösa en skrapreaktion. En person med atopiskt eksem har visat sig ha sensoriska nervceller i huden tätare än normalt. De viktigaste faktorerna som utlöser kroniskt atopiskt eksem (pruritogener) verkar vara inflammationscytokiner av typ 2, såsom IL-4, IL-13 och IL-31. I hudens sensoriska nervändor har man hittat bland annat receptorer för dessa cytokiner. En del av nervcellerna som förmedlar klåda aktiveras när histamin frigörs från mastcellerna «Legat FJ. Itch in Atopic Dermatitis - What Is New?...»27.
- Sensoriska nerver som förmedlar klåda och smärta i huden överlappar delvis varandra. Klåda och smärtkänningar har ofta samband med varandra i atopiskt eksem, men hos en del patienter kan hudsmärta också vara ett självständigt symtom. Mekaniska hudirriterande faktorer som skadar hudens skyddsbarriär och frigör inflammationsmediatorer från huden kan åstadkomma strukturella förändringar i hudens nervceller som leder till ökad känslighet. När symtomen blir mer kroniska sker en sensibilisering för både klåda och smärta även i det centrala nervsystemet «Ständer S, Simpson EL, Guttman-Yassky E ym. Clinic...»28.
- Se bilden Patogenesen av atopiskt eksem i huvuddrag «Atooppisen ekseeman patogeneesi pääpiirteissään»2.
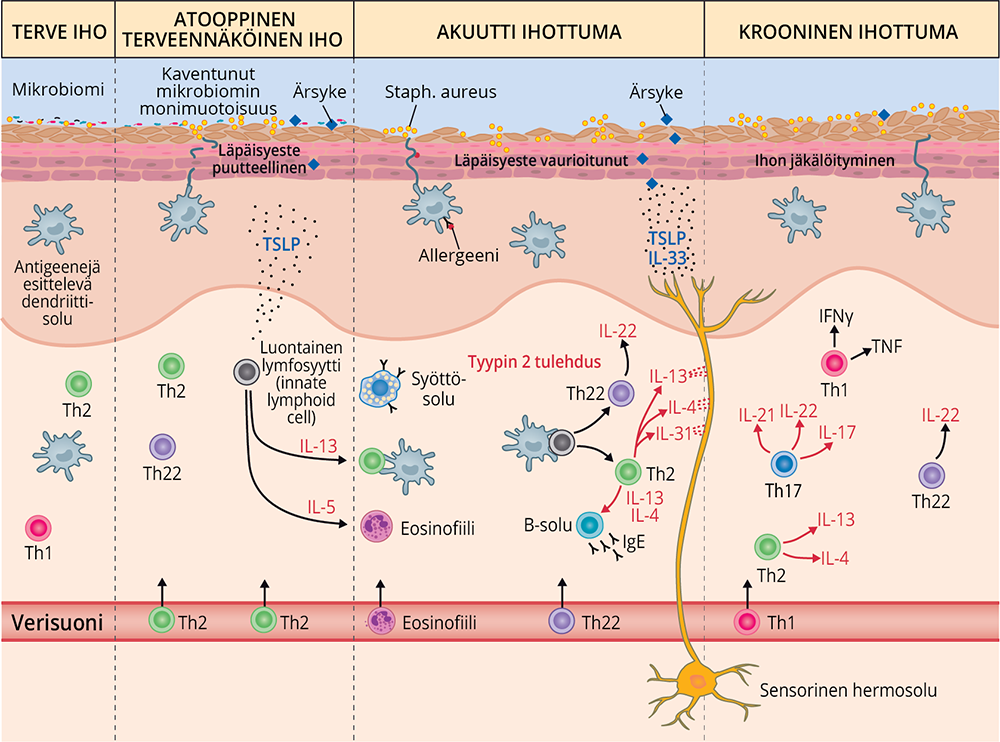
Atooppisen ekseeman patogeneesi pääpiirteissään
IFNγ = gamma-interferoni, IgE = immunoglobuliini E, IL = interleukiini, Th = auttaja-T-solu, TNF = tuumorinekroositekijä, TSLP = thymic stromal lymphopoietin.
Terve iho muodostaa fyysisen, kemiallisen ja biologisen läpäisyesteen haitallisille tekijöille (ärsykkeille, kuten bakteerit, kemikaalit ja allergeenit). Monimuotoinen ihon mikrobiomi tukee terveen immuunipuolustuksen kehittymistä aktivoimalla esimerkiksi antimikrobiaalisia mekanismeja, jotka estävät taudinaiheuttajien kasvua iholla.
Atoopikon terveennäköiselläkin iholla läpäisyeste on heikko, ihon mikrobiomin monimuotoisuus on kaventunut ja antimikrobiaalisten peptidien tuotanto vähentynyt. TSLP (thymic stromal lymphopoietin) on epiteelisolujen tuottama alarmiini (hälytysaine), joka säätelee tyypin 2 tulehdusvasteen aktivoitumista. Akuutissa ihottumavaiheessa antigeenejä esittelevät dendriittisolut, kuten Langerhansin solut ja dendriittisolut, joihin on kiinnittynyt IgE-vasta-aineita, aktivoivat tyypin 2 tulehdussoluja tuottamaan sytokiineja IL-4, IL-13 ja IL-31. Nämä toimivat kutinaa laukaisevina välittäjäaineina. Kehittyy noidankehä, jossa tyypin 2 tulehdus vaurioittaa lisää ihon läpäisyestettä ja epiteelisolut tuottavat lisää alarmiineja, kuten TSLP ja IL-33, jotka voimistavat kutinaa entisestään.
Kroonisessa atooppisessa ekseemassa Th1- ja erityisesti lapsilla ja aasialaista taustaa olevilla potilailla Th17-tulehdussolut aktivoituvat.
Kuva muokattu lähteestä: Langan SM, Irvine AD & Weidinger S. Atopic dermatitis. Lancet 2020;396:345-60
Aiheesta lisää:
Fyhrquist N. Ihon mikrobiomi ja atooppiset taudit. Duodecim 2021;137:2553-9
Beck LA, Cork MJ, Amagai M, De Benedetto A, Kabashima K, Hamilton JD, Rossi AB. Type 2 Inflammation Contributes to Skin Barrier Dysfunction in Atopic Dermatitis. JID Innovations 2022;2:100131
Prevention
- Atopiskt eksem kan inte förebyggas effektivt.
- Exklusiv amning som varar i över 4 månader kan inte minska risken för atopiskt eksem. Den allmänt rekommenderade helamningen i 4–6 månader lämpar sig också för familjer med allergirisk «Greer FR, Sicherer SH, Burks AW ym. The Effects of...»29.
- Om bröstmjölken inte räcker till används i allmänhet vanlig komjölksbaserad ersättning. Det finns inte tillräckliga bevis för att användningen av delvis eller långt uppspjälkad ersättningsmjölk i en allergiriskfamilj under de första 4 månaderna, om mängden bröstmjölk är otillräcklig, skulle minska risken för atopiskt eksem «Boyle RJ, Ierodiakonou D, Khan T ym. Hydrolysed fo...»30, «Osborn DA, Sinn JK, Jones LJ. Infant formulas cont...»31.
- Annan kost:
- Mammans undvikande kost under graviditeten eller amningen verkar inte minska barnets risk att insjukna i atopiskt eksem och den kan ha en skadlig inverkan på mammans eller fostrets näring «Foisy M, Boyle RJ, Chalmers JR ym. Overview of Rev...»32, «Netting MJ, Middleton PF, Makrides M. Does materna...»33. Se God medicinsk praxis-rekommendationen Födoämnesallergi (barn) «Matallergi (barn)»2.
- För att förebygga atopiskt eksem rekommenderas inte att man fördröjer inledandet av fast föda «Greer FR, Sicherer SH, Burks AW ym. The Effects of...»29. Det finns inga bevis på att en förflyttning av inledningen av fast föda från 4 månaders ålder till 6 månaders ålder eller senare skulle minska incidensen av atopiskt eksem «Zutavern A, Brockow I, Schaaf B ym. Timing of soli...»34, «Williams HC, Chalmers J. Prevention of Atopic Derm...»35.
- Att lägga till mat som allmänt orsakar allergi (jordnöt, ägg) i kosten från 4 månaders ålder ökar inte risken för atopiskt eksem, men kan förhindra ägg- och jordnötsallergi «Obbagy JE, English LK, Wong YP ym. Complementary f...»36. Se God medicinsk praxis-rekommendationen Födoämnesallergi (barn) «Matallergi (barn)»2.
- Probiotika och prebiotika
- Probiotika är levande mikrobpreparat som enligt WHO:s definition främjar hälsan om det används tillräckligt «Pfefferle PI, Prescott SL, Kopp M. Microbial influ...»37. Prebiotika är icke nedbrytbara kosttillskott som enligt WHO:s definition har en gynnsam effekt genom att selektivt stimulera vissa bakteriers (probiotika) tillväxt eller aktivitet i tarmen och är därmed hälsofrämjande «Kuitunen M. Probiotics and prebiotics in preventin...»38.
- Vissa probiotiska preparat minskar incidensen av atopiskt eksem i familjer med risk
för allergi «Jotkut probiootit vähentävät atooppisen ekseeman ilmaantuvuutta lapsilla ainakin 2 vuoden ikään asti, kun allergian riskiperheissä äiti aloittaa probiootin käytön vähintään 4 viikkoa ennen laskettua aikaa ja käyttöä jatketaan lapsella 6 kuukauden ajan.»A. Kunskapen om vilken probiotikastam eller kombination av probiotikastammar som ska
användas, behandlingens längd eller en lämplig dos är fortfarande bristfällig.
- Man känner till att inledande av Lactobacillus rhamnosus GG (LGG) för mamman i en allergiriskfamilj minst 4 veckor före beräknad tid och administrering till barnet i 6 månader minskar incidensen av atopiskt eksem fram till 2 års ålder «Li L, Han Z, Niu X ym. Probiotic Supplementation f...»39.
- Prebiotika (t.ex. galakto- eller frukto-oligosackarid) kan ha en minskande effekt på atopiskt eksem, men det finns fortfarande knappt med forskningsdata i frågan och tills vidare kan man inte ge någon rekommendation om användningen av dem «Osborn DA, Sinn JK. Prebiotics in infants for prev...»40, «Sestito S, D'Auria E, Baldassarre ME ym. The Role ...»41.
- En avvikelse i hudens skyddsbarriär har en betydande inverkan på patogenesen av atopiskt eksem. Bassalvor utgör en central del av behandlingen av atopiskt eksem, men deras effekt vid förebyggandet av atopiskt eksem har inte kunnat påvisas på ett tillförlitligt sätt. Forskningsdata i systematiska litteraturöversikter och metaanalyser är motstridiga «Kelleher MM, Cro S, Cornelius V ym. Skin care inte...»42, «Liang J, Hu F, Tang H ym. Systematic review and ne...»43. I tidigare mindre studier har man påvisat att risken för atopiskt eksem minskar jämfört med kontrollspädbarn, när huden hos ett spädbarn i en familj med hög allergirisk smörjdes regelbundet in med bassalva efter födseln åtminstone en gång per dygn i 6–7 månader «Simpson EL, Chalmers JR, Hanifin JM ym. Emollient ...»44, «Horimukai K, Morita K, Narita M ym. Application of...»45. I senare mer omfattande studier har resultatet inte kunnat verifieras «Kelleher MM, Cro S, Cornelius V ym. Skin care inte...»42, «Liang J, Hu F, Tang H ym. Systematic review and ne...»43, «Skjerven HO, Rehbinder EM, Vettukattil R ym. Skin ...»46, «Chalmers JR, Haines RH, Bradshaw LE ym. Daily emol...»47.
Diagnostik, symtom och fynd
- Diagnosen atopiskt eksem är klinisk.
- För diagnosen räcker det vanligen att patienten har följande fynd «Brenninkmeijer EE, Schram ME, Leeflang MM ym. Diag...»48, «Champion RH ym. (toim.) Textbook of Dermatology, 6...»49:
- kliande och kroniskt eller kontinuerligt återkommande eksem i typiska hudområden (bild «Ihottuman tyyppialueet»3)
- rodnad, knottror (papler), fjällning, skrapmärken och hudsår i eksemområdet. I den akuta fasen kan också små vätskeblåsor (vesikler) och vätskning framträda på huden. När sjukdomen blir kronisk förtjockas eksemområdet (likenifikation) till följd av skrapning.
- Mer detaljerade diagnostiska kriterier är följande:
- Atopiskt eksem är alltid kliande – eksem utan klåda är inte atopiskt eksem.
- Utöver klåda ska patienten ha minst tre av fem av följande symtom och fynd «Williams HC, Burney PG, Pembroke AC ym. The U.K. W...»50:
- eksem i ett typiskt område vid undersökningstidpunkten (bild «Ihottuman tyyppialueet»3)
- eksem i ett typiskt område tidigare
- torr hud
- eksemet har börjat före det andra levnadsåret
- allergisk snuva eller astma (kriteriet för barn under 4 år är en atopisk sjukdom hos en familjemedlem).
- Atopiskt eksem är ofta också förknippat med hudsmärta, enligt olika studier förekommer det hos upp till 43–92 procent av patienterna. Smärtan är oftast brännande eller framträder som ömhet eller beröringskänslighet i huden. Smärtsymtomet korrelerar med eksemets svårighetsgrad «Ständer S, Simpson EL, Guttman-Yassky E ym. Clinic...»28, «Li JX, Dong RJ, Zeng YP. Characteristics, mechanis...»51.
- På sommaren lindras ofta symtomen på atopiskt eksem.
- Atopiskt eksem kan i kliniskt arbete klassificeras enligt följande:
- Lindrigt atopiskt eksem: patienten har torra hudområden, tillfälligt förekommande klåda och rodnad på små hudområden (bild «Leikki-ikäisen lievä atooppinen ekseema»4). Lokalt verkande läkemedelsbehandling behövs tidvis.
- Måttligt atopiskt eksem: patienten har torra hudområden, ofta förekommande klåda och rodnad samt eventuellt sårig och förtjockad hud (se bilden «Atooppinen ekseema nuoren miehen ranteessa»5). Lokalt verkande läkemedelsbehandling behövs ständigt i perioder eller som underhållsbehandling.
- Svårt atopiskt eksem: torr hud, konstant klåda och utbredd rodnad. Dessutom förekommer hudskador, betydande förtjockning av huden, blödning, vätskning, skorvbildning och pigmenteringsstörningar (bilderna «Kouluikäisen vaikea atooppinen ekseema kaulassa ja ylävartalossa»6 och «Kouluikäisen vaikea atooppinen ekseema yläraajoissa»7). Svårt atopiskt eksem kan vara erytrodermiskt (eksem på hela huden). Långvarig systemisk medicinering behövs eller övervägs.
- Validerade mätare kan användas för en klinisk bedömning av eksemets svårighetsgrad «Thomas KS, Apfelbacher CA, Chalmers JR ym. Recomme...»52. Särskilt inom den specialiserade sjukvården rekommenderas användning av mätare som beskriver sjukdomens svårighetsgrad. Läs mer om mätarna för bedömning av atopiskt eksem «Atooppisen ekseeman arvioinnissa käytettäviä mittareita»5 och punkten Verktyg för bedömning av symtom, svårighetsgrad och vårdrespons vid atopiskt eksem «A1»2.
- Det verkar som om man vid atopiskt eksem kan urskilja flera fenotyper enligt de bakomliggande
genetiska faktorerna och inflammationsmekanismerna.
- Den kliniska bilden av atopiskt eksem förändras med åldern särskilt i fråga om eksemområdenas läge. Även inflammationssvaret förändras från Th2-, Th22- och Th17-prevelens av atopiskt eksem i barndomen till Th2-, Th22- och Th1-prevalens «Czarnowicki T, He H, Krueger JG ym. Atopic dermati...»53.
- Hos en del vuxna (cirka 80 %) har IgE-halten i serum ökat hos personer med atopiskt eksem. Dessa personer har i allmänhet en ärftlig benägenhet för atopi och mutationer i filaggringenen är vanliga. Hos cirka 20 procent av patienterna är IgE-halten i serum normal. Dessa patienter är ofta kvinnor och deras eksem har inte börjat förrän i vuxen ålder «Czarnowicki T, He H, Krueger JG ym. Atopic dermati...»53, «Tokura Y, Hayano S. Subtypes of atopic dermatitis:...»54.
- Vid sjukdomsförlopp hos barn kan man identifiera olika fenotyper från en sjukdomsbild som bryter ut tidigt och snabbt blir symtomfri till en kronisk sjukdom som fortsätter i vuxen ålder. Riskfaktorerna och prognosen varierar beroende på genetiska faktorer och miljöfaktorer. Konsensus om olika undertyper finns dock inte «Langan SM, Irvine AD, Weidinger S. Atopic dermatit...»13, «Paternoster L, Savenije OEM, Heron J ym. Identific...»55, «Roduit C, Frei R, Depner M ym. Phenotypes of Atopi...»56.
- Atopiskt eksem och mekanismerna på molekylnivå samt immunologin bakom eksemet varierar enligt patienternas etniska bakgrund «Czarnowicki T, He H, Krueger JG ym. Atopic dermati...»53.
- Tills vidare finns det inga genetiska markörer eller biomarkörer som lämpar sig för klinisk användning vid diagnostik av atopiskt eksem eller för bedömning av dess svårighetsgrad eller prognos. Eftersom responsen på olika behandlingar kan variera enligt eksemets fenotyp och de bakomliggande mekanismerna, är det framtida målet en mer individuell behandling «Renert-Yuval Y, Thyssen JP, Bissonnette R ym. Biom...»57.
- Särdrag «Akdis CA, Akdis M, Bieber T ym. Diagnosis and trea...»58:
- I spädbarnsåldern börjar eksem ofta med fjällbildning på huvudet och sprider sig till bålen och extremiteterna. Blöjområdet är vanligen fritt från eksem. Eksemet kan utsöndra sårvätska och påminner då om impetigo eller omvandlas till erytrodermi (kraftig rodnad och inflammation i hela huden) (bilderna «Vauvaikäisen lievä atooppinen ekseema»8 och «Vauvan vaikea atooppinen ekseema»9). Atopiskt eksem kan förekomma som förtjockade små fläckar, varvid det kallas nummulärt atopiskt eksem «Nummulaarinen ekseema»10.
- Typiska områden för atopiskt eksem hos småbarn från två års ålder är hals, nacke, armbågs- och knäveck, handleder, bakfåra och vrister. Andra typiska områden är ögonområdet, bakom öronen, i örsnibbarna och runt munnen. Det är också vanligt med torr läppinflammation. Eksem kan förekomma på bålen och på extensorsidan av extremiteterna (bilderna «Leikki-ikäisen lievä atooppinen ekseema»4 och «Leikki-ikäisen keskivaikea atooppinen ekseema»11).
- I skolåldern framträder eksemet ofta i knä- och armvecken. Eksem påträffas också i samband med så kallat ridbyxområde på baken och låren samt i händerna, fötterna, nacken och ansiktet. Andra vanliga specialformer är atopisk vinterfot, dermatitis palmaris sicca i händerna och neurodermatit i nacken. I puberteten sprider sig eksemet ofta till axlarna, bröstet och ryggen (bilderna «Atooppinen ekseema pojan jalkapohjan alueella (ns. talvijalka)»12, «Kouluikäisen vaikea atooppinen ekseema kaulassa ja ylävartalossa»6 och «Kouluikäisen vaikea atooppinen ekseema yläraajoissa»7).
- Typiska områden med atopiskt eksem i vuxen ålder är förutom armbågs- och knäveck även ansikte, hals och överkropp. Vuxna har atopiskt eksem ofta i händerna (bilderna «Atooppinen ekseema nuoren naisen kyynärtaipeissa»13, «Atooppinen ekseema polvitaipeessa»14, «Atooppinen ekseema silmäluomissa»15, «Atooppinen ekseema nuoren naisen kaulan alueella»16, «Atooppinen ekseema kaulan alueella»17, «Vaikea atooppinen ekseema niskan alueella»18, «Laaja-alainen atooppinen ekseema (erytrodermia)»19, «Atooppinen ekseema nuoren miehen ranteessa»5, «Atooppinen ekseema nuoren aikuisen kädessä»20, «Atooppinen ekseema ranteissa»21, «Vaikea atooppinen ekseema alaraajoissa»22).
- Atopiskt eksem ger ofta också symtom på ögonlock och som blefarokonjunktivit.
- Hos mörkhyade patienter syns mindre rodnad på huden än hos ljushyade, vilket kan leda till en underskattning av eksemets svårighetsgrad. Att skilja rodnaden från postinflammatorisk hyperpigmentering kan vara utmanande och försvåra uppföljningen av sjukdomen. EASI-mätaren lämpar sig dock väl även för mörkhyade «Zhao CY, Hao EY, Oh DD ym. A comparison study of c...»59, «Vauvaikäisen tummaihoisen lapsen atooppinen ekseema»23, «Leikki-ikäisen tummaihoisen atooppinen ekseema»24, «Nuoren tummaihoisen atooppinen ekseema»25, «Tummaihoisen atooppinen ekseema»26.
- I differentialdiagnostiken ska man särskilt beakta följande:
- hormonkvisslor, seborroiskt eksem, iktyos, psoriasis, hudceliaki, keratosis pilaris, skabb, acrodermatitis enteropathica och immunbristsyndrom hos spädbarn och barn
- andra eksem (seborroiskt eksem, nummulärt eksem, infektionseksem, asteatotiskt eksem), psoriasis, skabb, hudceliaki, immunbristsyndrom, parapsoriasis och hudlymfom hos vuxna
- allergiskt kontakteksem och irritationskontakteksem hos personer i alla åldrar
- i den akuta fasen impetigo och erysipelas.
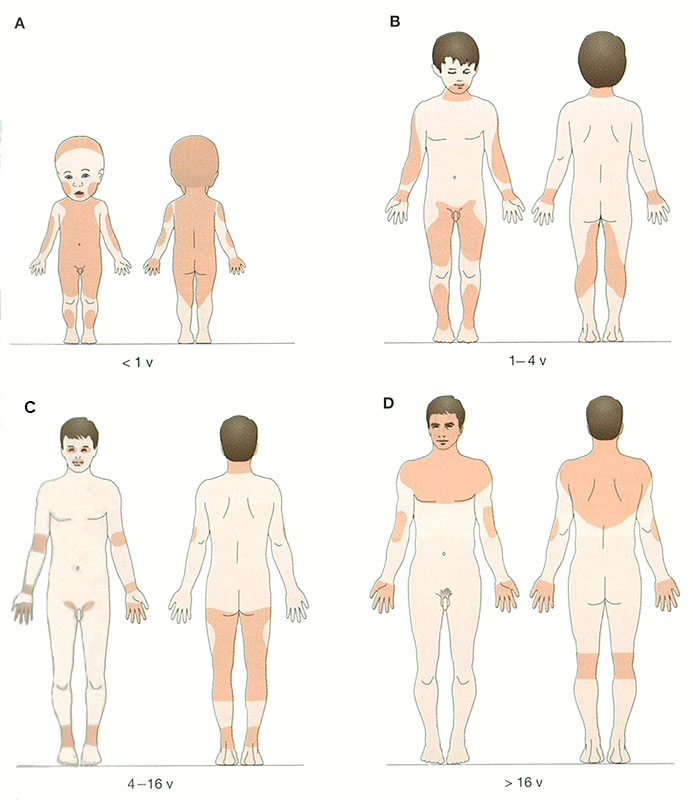
Ihottuman tyyppialueet. Atooppisen ekseeman tyypilliset ihoalueet eri ikäkausina.
Lähde: Hannuksela M, Alanko K. Atooppinen ekseema. Kirjassa: Hannuksela M, Karvonen J, Reunala T, Suhonen R (toim.). Ihotaudit. Kustannus Oy Duodecim 2003, s. 79
Lupa käyttöön saatu Kustannus Oy Duodecim/Hannele Pirttimaa 21.8.2008
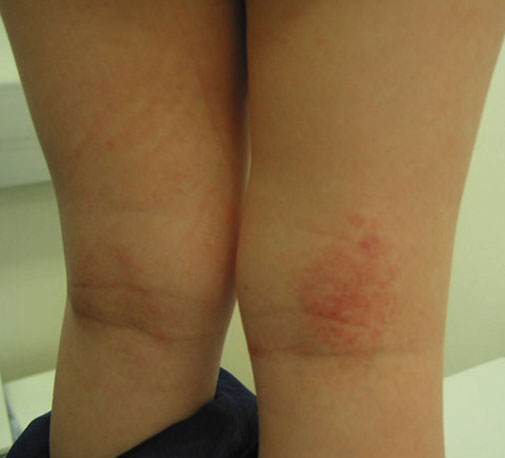
Leikki-ikäisen lievä atooppinen ekseema.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Mika Mäkelä
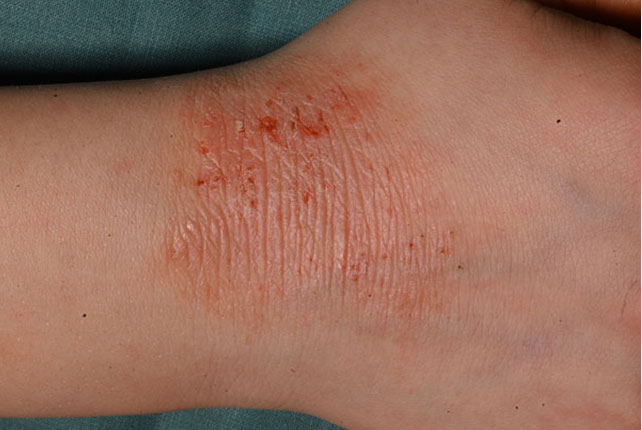
Atooppinen ekseema nuoren miehen ranteessa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
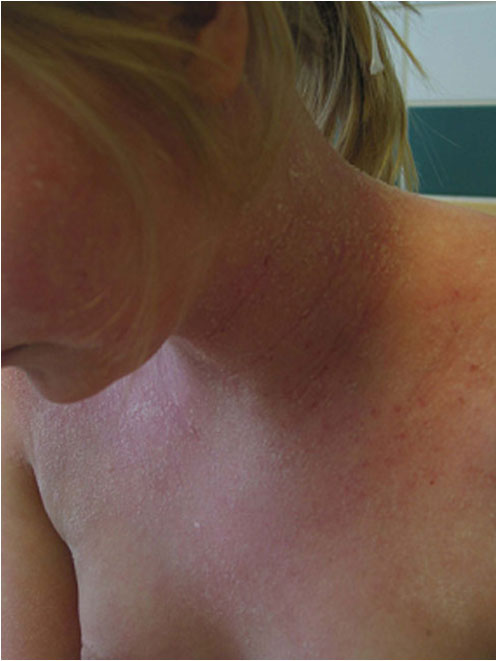
Kouluikäisen vaikea atooppinen ekseema kaulassa ja ylävartalossa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Anna Pelkonen
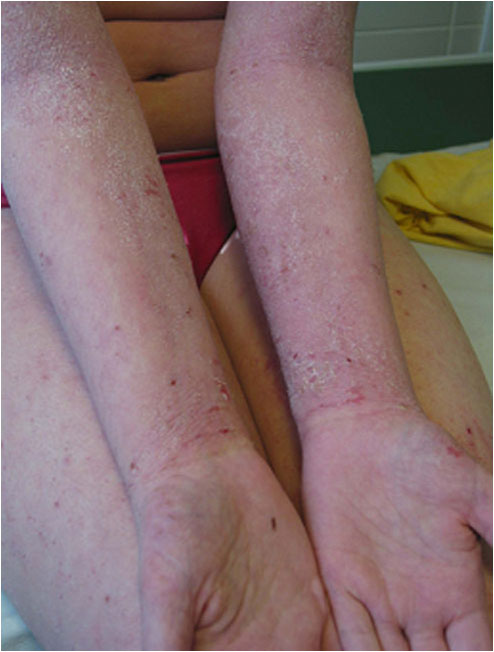
Kouluikäisen vaikea atooppinen ekseema yläraajoissa.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Anna Pelkonen.
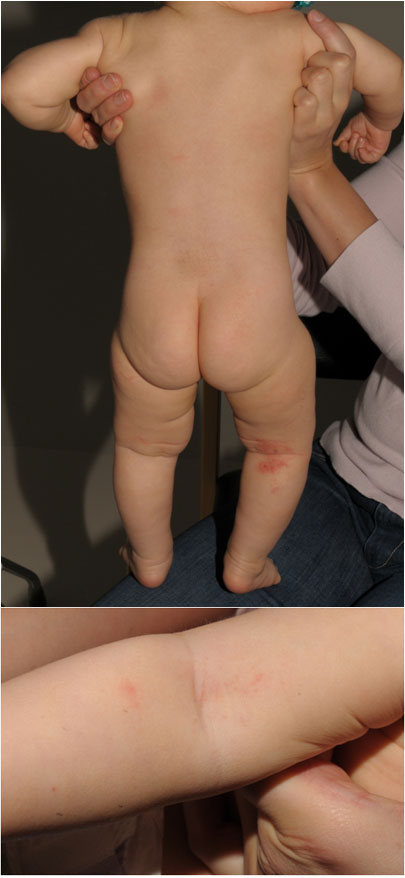
Vauvaikäisen lievä atooppinen ekseema
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Anna Pelkonen
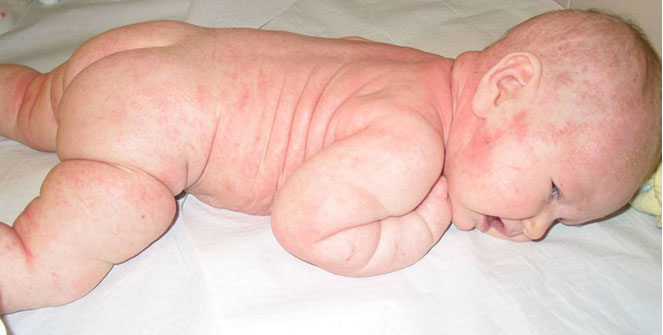
Vauvan vaikea atooppinen ekseema
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Mika Mäkelä .
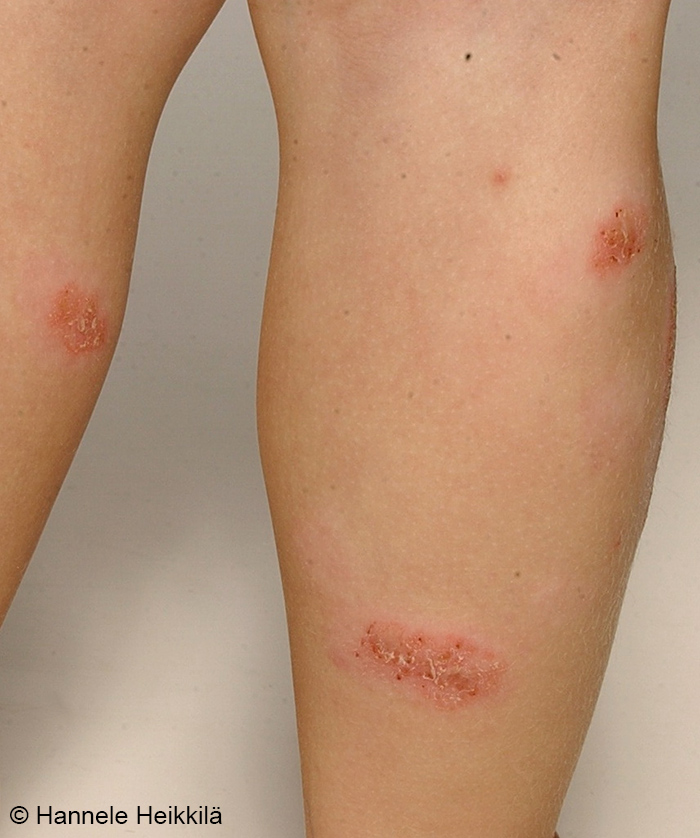
Nummulaarinen ekseema.
© Hannele Heikkilä
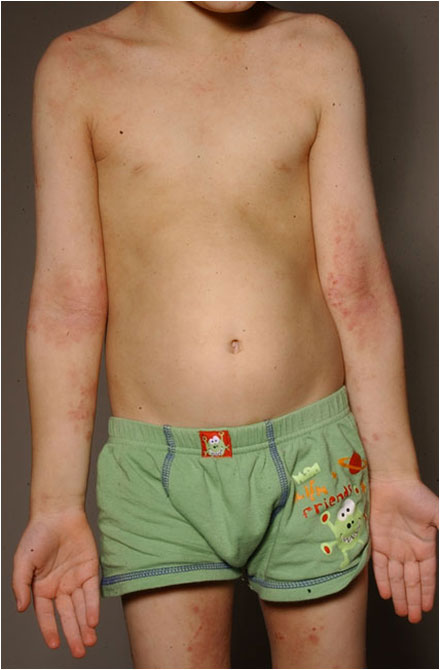
Leikki-ikäisen keskivaikea atooppinen ekseema.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Anna Pelkonen
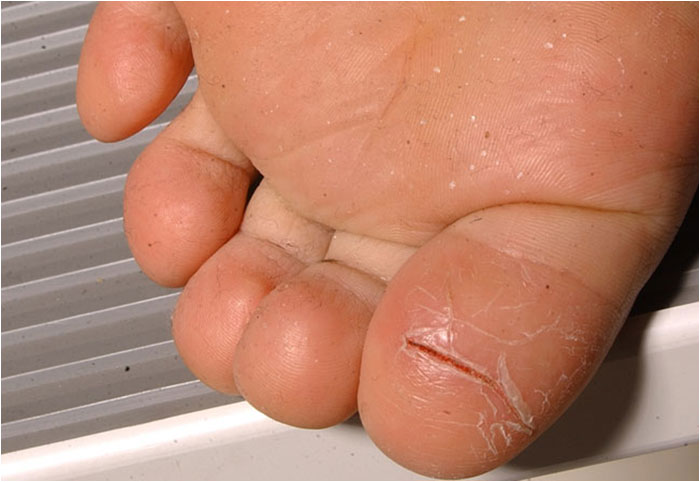
Atooppinen ekseema pojan jalkapohjan alueella (ns. talvijalka)
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
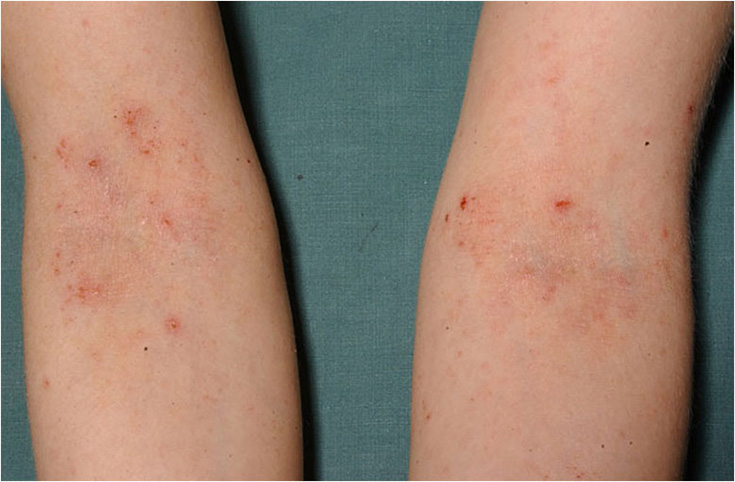
Atooppinen ekseema nuoren naisen kyynärtaipeissa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
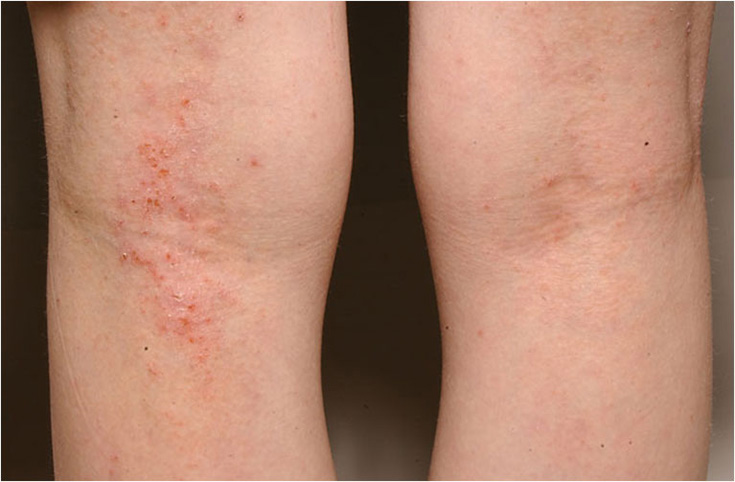
Atooppinen ekseema polvitaipeessa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
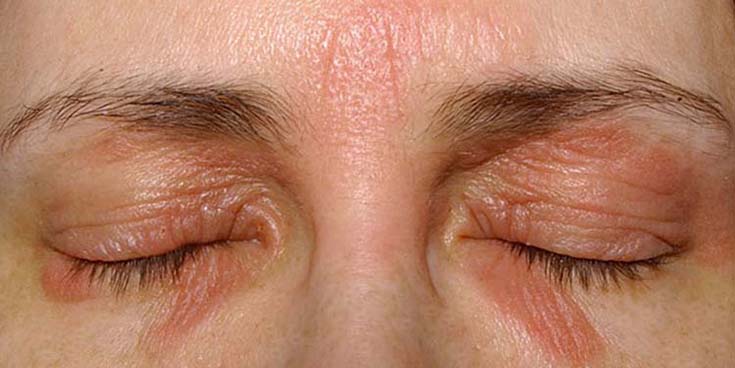
Atooppinen ekseema silmäluomissa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
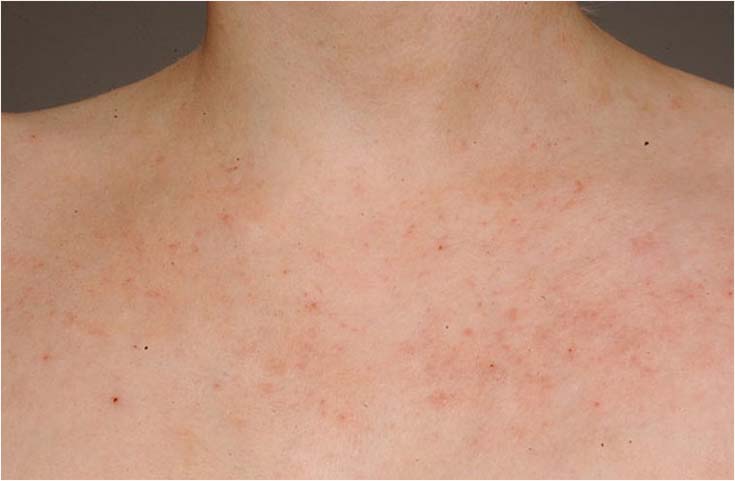
Atooppinen ekseema nuoren naisen kaulan alueella
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
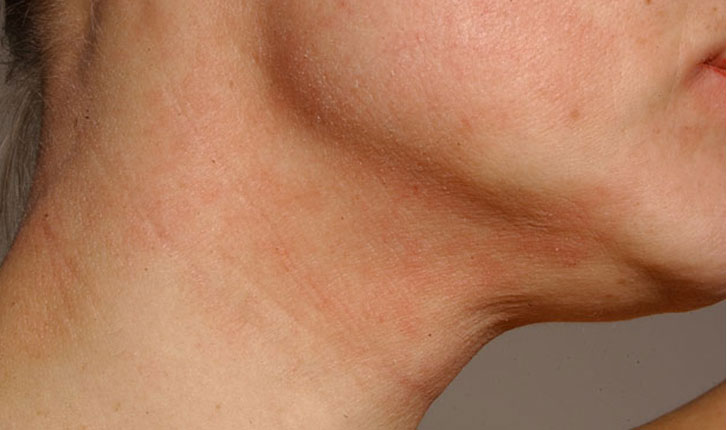
Atooppinen ekseema kaulan alueella
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
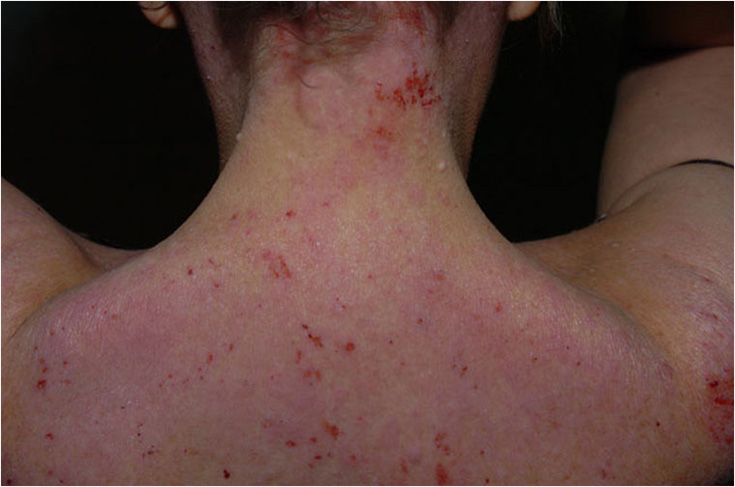
Vaikea atooppinen ekseema niskan alueella. Pitkään kestänyt, voimakkaasti kutiseva ja rikki raavittu atooppinen ekseema niskan ja yläselän alueella.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
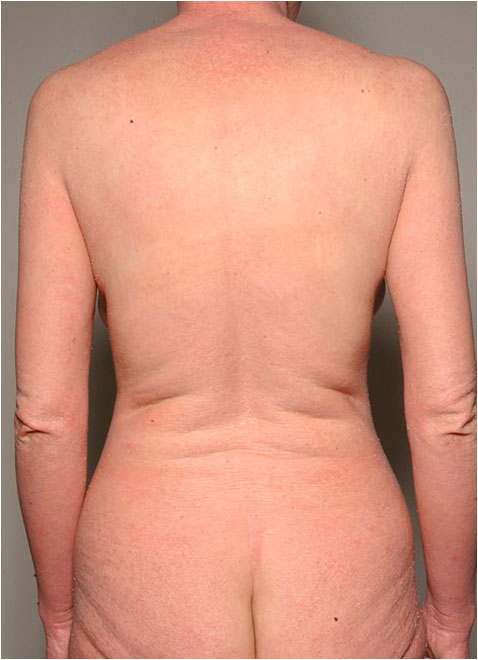
Laaja-alainen atooppinen ekseema (erytrodermia)
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
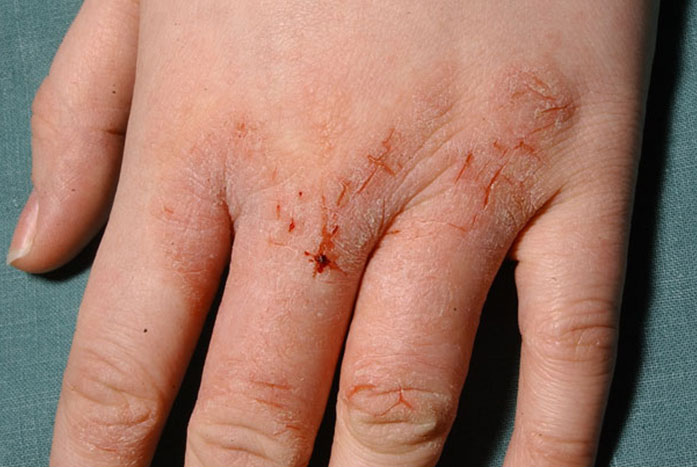
Atooppinen ekseema nuoren aikuisen kädessä
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
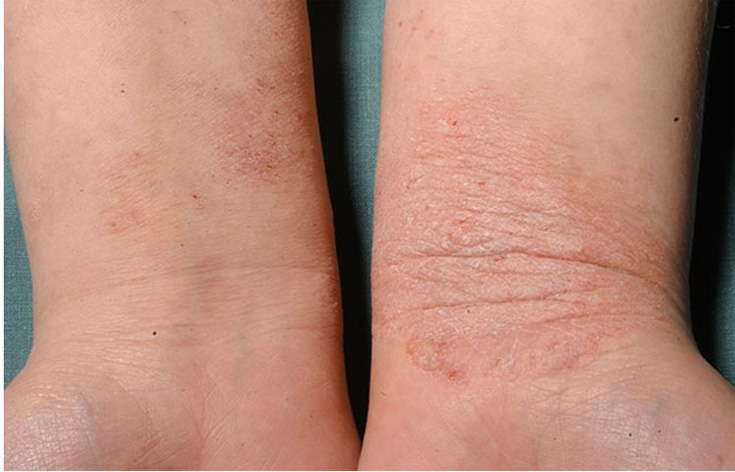
Atooppinen ekseema ranteissa
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
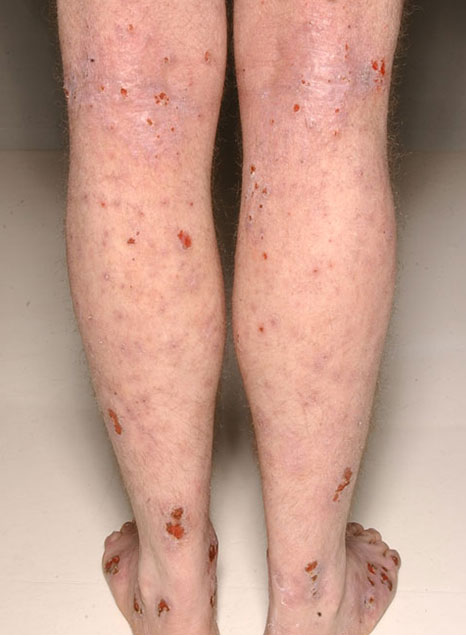
Vaikea atooppinen ekseema alaraajoissa. Pitkään kestänyt, hyvin kutiseva, jäkälöitynyt ja rikki raavittu atooppinen ekseema.
Lähde: HYKS:n iho- ja allergiasairaala
Kuva: Hannele Heikkilä
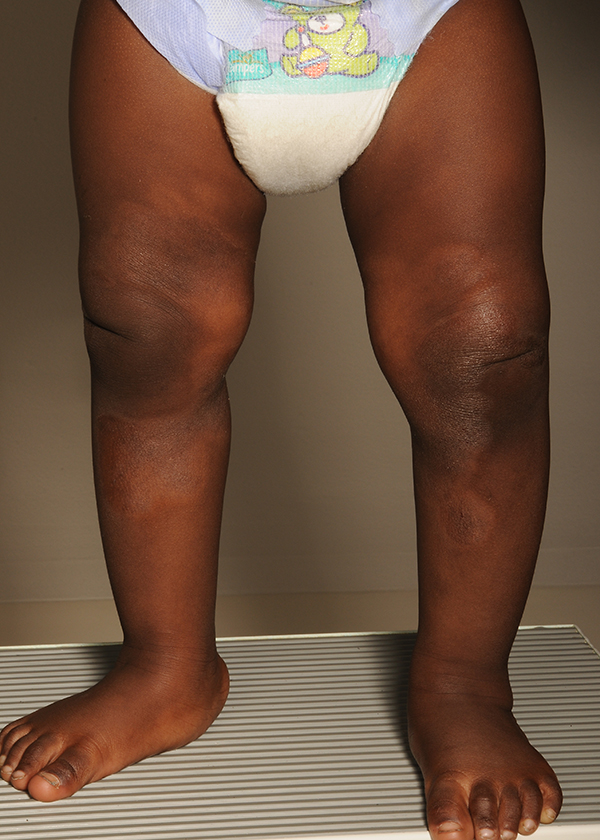
Vauvaikäisen tummaihoisen lapsen atooppinen ekseema. Tummaihoisilla ihotulehdus aiheuttaa yleisesti ihon hypo- ja hyperpigmentaatiota.
Lähde: HYKS:n iho- ja allergiasairaala
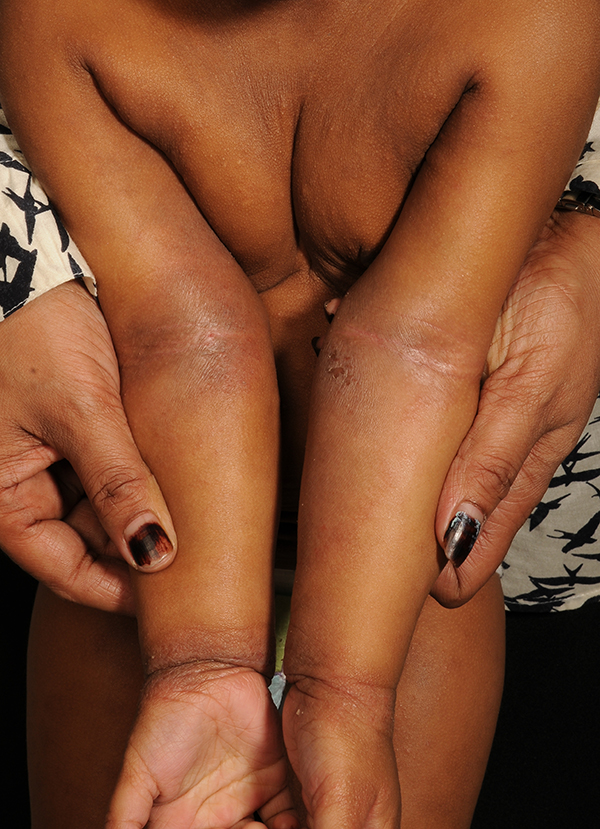
Leikki-ikäisen tummaihoisen atooppinen ekseema. Kyynärtaipeiden ja ranteiden tyypillinen atooppinen ekseema.
Lähde: HYKS:n iho- ja allergiasairaala
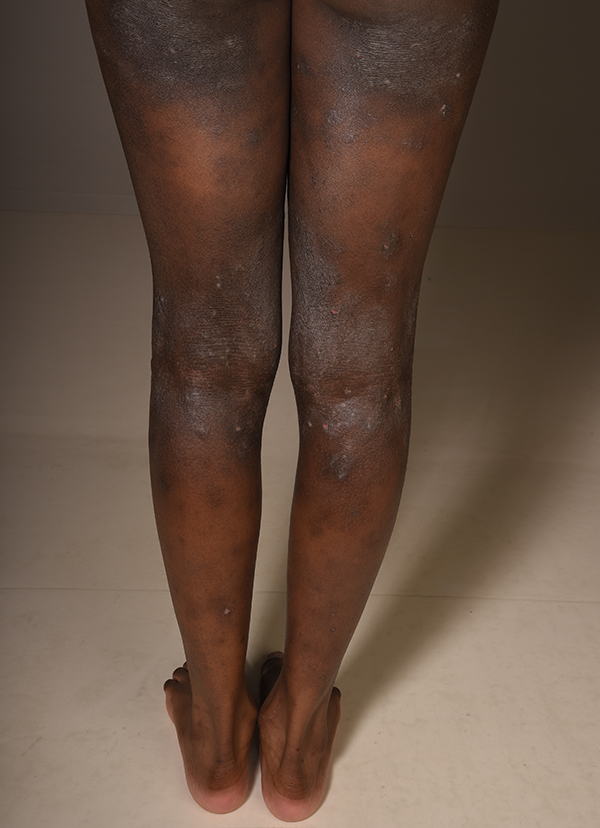
Nuoren tummaihoisen atooppinen ekseema. Voimakkaasta ihotulehduksesta huolimatta iholla ei näy punoitusta vaan väritys on harmahtava vaaleasta hilseilystä johtuen.
Lähde: HYKS:n iho- ja allergiasairaala
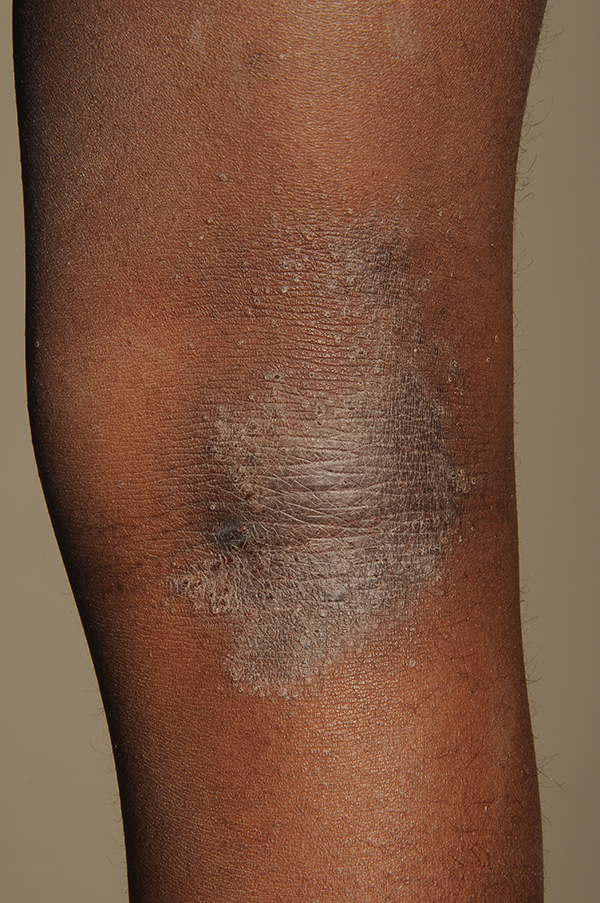
Tummaihoisen atooppinen ekseema. Polvitaipeen kuvassa näkyy tummaihoisilla yleisemmät papulaiset muutokset ja korostuneet ihon follikkeliaukot.
Lähde: HYKS:n iho- ja allergiasairaala
Allergiutredningar hos vuxna
- I allmänhet behövs inga allergiutredningar.
- Allergiutredningar kan användas för att utreda faktorer som förvärrar svårbehandlat eksem.
- Om respons mot atopiskt eksem inte fås genom normal lokalbehandling, kan det vara fråga om utveckling av kontaktallergi till exempel mot beståndsdelar i kosmetika eller lokalbehandlingar. Då är det motiverat med epikutantest.
- En vuxen behöver i allmänhet inte eliminera födoämnen från kosten.
- Korsallergier mot födoämnen i samband med pollenallergier kan förvärra atopiskt eksem hos unga och vuxna, men mängden tillförlitliga studier är liten «Siitepölyallergioihin liittyvät ristiallergiat ruoka-aineille saattavat pahentaa yli 12-vuotiaiden atooppista ekseemaa, mutta luotettavan tutkimuksen määrä on vähäinen.»C. Om personer med pollenallergi exponeras för pollen kan det förvärra särskilt atopiskt eksem i ansiktet «Werfel T, Heratizadeh A, Niebuhr M ym. Exacerbatio...»60.
- Det finns ingen tillförlitlig forskningsevidens på kvalsterallergins negativa effekt på atopiskt eksem «Nankervis H, Pynn EV, Boyle RJ ym. House dust mite...»61.
Allergiutredningar hos barn
- En del barn under ett år som lider av måttligt eller svårt (bild «Vauvan vaikea atooppinen ekseema»9) atopiskt eksem kan ha födoämnesallergi i bakgrunden, vanligtvis mot komjölk eller
ägg, och allergiutredningar är då motiverade.
- Hos större barn är allergiutredningar på grund av eksem sällan nödvändiga.
- Se även Avstå klokt-rekommendationen om utredning av födoämnesallergi hos barn med atopiskt eksem «Ruoka-allergiaselvitykset atooppista ekseemaa sairastavilla lapsilla»6. Inled inte utredningar av födoämnesallergi hos barn med lindrigt atopiskt eksem. Inled inte rutinmässigt utredningar hos spädbarn med måttligt atopiskt eksem.
- Födoämnesallergier hos barn behandlas separat i God medicinsk praxis-rekommendationen Födoämnesallergi (barn) «Matallergi (barn)»2.
- Mer information om födoämnesallergier vid atopiskt eksem hos barn finns i tilläggsmaterialet «Lisätietoa ruoka-allergioista lasten atooppisessa ekseemassa»7.
Faktorer som försämrar atopiskt eksem
- Hos patienter med atopiskt eksem är huden känslig för irritation och klådan ökar till följd av olika mekaniska, fysikaliska och kemiska faktorer. En del irriterande faktorer är kända på basis av studier, men största delen av observationerna grundar sig på klinisk erfarenhet.
- Svettning, psykiska faktorer (se avsnittet Livskvalitet och psykiska faktorer «A12»3), torr inomhusluft, vintertid, luftföroreningar, grova kläder, för lätta eller feta salvor samt andra kosmetika- eller hygienprodukter som används på huden kan förvärra eksemet genom irritationsmekanismen. Andra försämrande faktorer kan vara bakterie- och virusinfektioner eller allmänna infektioner i huden «Ring J, Alomar A, Bieber T ym. Guidelines for trea...»62.
- Födoämnes-, pollen- och djurepitelallergi samt kontaktallergier kan också ibland förvärra eller upprätthålla atopiskt eksem (se avsnittet Allergiutredningar hos vuxna «A2»4 och God medicinsk praxis-rekommendationen Födoämnesallergi (barn) «Matallergi (barn)»2), «Werfel T, Heratizadeh A, Niebuhr M ym. Exacerbatio...»60.
- Se bilden Atopisk ond cirkel «Atooppinen noidankehä»27.
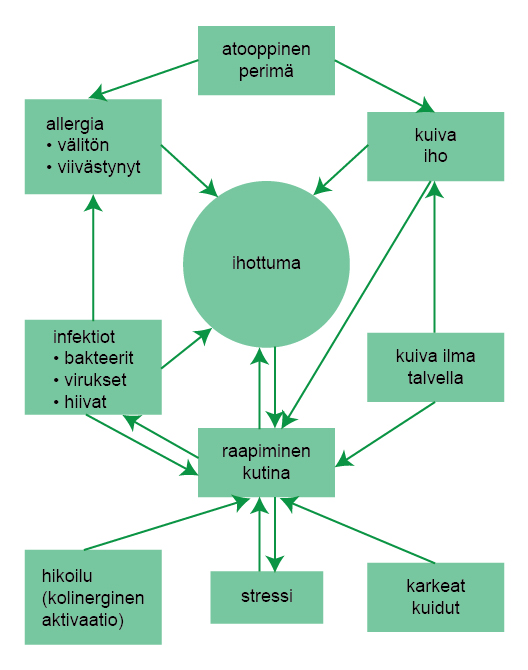
Atooppinen noidankehä
Lähde: Hannuksela M, Lauerma A. Atooppinen ekseema. Kirjassa: Hannuksela M, Peltonen S, Reunala T, Suhonen R (toim.). Ihotaudit. 2., uudistettu painos. Kustannus Oy Duodecim 2011, s. 55
Lupa käyttöön saatu Kustannus Oy Duodecim / Hannele Pirttimaa 21.3.2016
Associerade sjukdomar till atopiskt eksem
- I den övergripande behandlingen av atopiskt eksem är det viktigt att beakta patientens eventuella associerade sjukdomar, i synnerhet atopiska sjukdomar. Behandlingen av atopiskt eksem planeras individuellt. Om patienten har andra immunologiska sjukdomar kan man om möjligt välja en sådan medicinering för behandling av atopiskt eksem som också har effekt på dessa.
- Cirka en fjärdedel av vuxna med atopiskt eksem har astma. Det tydligaste sambandet
föreligger mellan svårt atopiskt eksem och astma «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63.
- Vuxna med atopiskt eksem har tre gånger större sannolikhet för en astmadiagnos än den övriga befolkningen.
- Atopiskt eksem hos vuxna verkar också ha samband med allergisk snuva och födoämnesallergier. Kopplingen till födoämnesallergier är starkast hos personer med svårt atopiskt eksem (RR 8,5; 95 % konfidensintervall, 5,4–11,5). Födoämnesallergiernas betydelse i symtomhelheten för atopiskt eksem hos vuxna är dock liten «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63.
- Kontaktallergi är inte vanligare hos personer med atopiskt eksem än hos den övriga befolkningen «Hamann CR, Hamann D, Egeberg A ym. Association bet...»64.
- Risken för hudinfektioner, särskilt stafylokocker och infektioner orsakade av viruset
herpes simplex, är klart högre hos personer med atopiskt eksem «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63.
- I atopisk hud kan virusinfektioner spridas i stor omfattning på grund av skadad hud, skrapning och avvikande cellmedierat immunförsvar. Sådana virusinfektioner är bland annat eczema herpeticum (generaliserad herpes simplex i huden) «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63 och mollusker. Läs mer om virusinfektioner i huden vid atopiskt eksem «Lisätietoa ihon virusinfektioista atooppisessa ekseemassa»8.
- Effektiv behandling av atopiskt eksem minskar förekomsten av hudinfektioner «Wang V, Boguniewicz J, Boguniewicz M ym. The infec...»65.
- Risken för hudlymfom är något högre hos personer med atopiskt eksem. Svårt atopiskt eksem verkar vara en betydande riskfaktor «Legendre L, Barnetche T, Mazereeuw-Hautier J ym. R...»66. För mer information se «Syöpä- ja lymfoomariski kalsineuriinin estäjien paikallisen käytön yhteydessä»9.
- Personer med atopiskt eksem har oftare än den övriga befolkningen ögonsjukdomar, såsom inflammation i ögonlockskanten (blefarit), horn- och bindhinneinflammation, keratokonus, glaukom, grå starr, näthinneavlossning och herpes simplex-infektion «Hsu JI, Pflugfelder SC, Kim SJ. Ocular complicatio...»67.
- Hos personer med atopiskt eksem förekommer det mer autoimmuna sjukdomar än hos den övriga befolkningen, såsom fläckvist håravfall (alopecia) och kronisk urtikaria «Andersen YM, Egeberg A, Gislason GH ym. Autoimmune...»68, «Narla S, Silverberg JI. Association between atopic...»69, «Ivert LU, Wahlgren CF, Lindelöf B ym. Association ...»70, «Kauppi S, Jokelainen J, Timonen M ym. Atopic Derma...»71.
- Barn och vuxna med atopiskt eksem löper ökad risk att insjukna i depression eller
ångestsyndrom «Rønnstad ATM, Halling-Overgaard AS, Hamann CR ym. ...»72, «Silverberg JI, Gelfand JM, Margolis DJ ym. Symptom...»73, «Kern C, Wan J, LeWinn KZ ym. Association of Atopic...»74.
- I en systematisk översikt och metaanalys baserad på 36 originalpublikationer konstaterades att en av sex personer med atopiskt eksem hade klinisk depression och var fjärde hade depressionssymtom «Patel KR, Immaneni S, Singam V ym. Association bet...»75. I en finländsk nationell registerstudie hade 10,4 procent av vuxna med atopiskt eksem fått diagnosen depression «Kauppi S, Jokelainen J, Timonen M ym. Adult Patien...»76. Det finns ingen tydlig bild av sambandet mellan svårighetsgraden av atopiskt eksem och depression.
- Orsaken till sambandet mellan atopiskt eksem och depression eller ångest är oklar. En förklaring till detta kan vara den psykosociala börda som orsakas av atopiskt eksem, klåda som leder till sömnstörningar, allmän försämring av livskvaliteten till följd av sjukdomen eller en kombination av dessa. I kliniska läkemedelsprövningar har också depressions- och ångestsymtomen kunnat lindras utöver en förbättring av de fysiska symtomen och fynden vid måttligt eller svårt atopiskt eksem «de Bruin-Weller M, Thaçi D, Smith CH ym. Dupilumab...»77, «Simpson EL, Wollenberg A, Bissonnette R ym. Patien...»78.
- Barn som har eller har haft atopiskt eksem verkar oftare än andra barn ha uppmärksamhetsstörningar
med hyperaktivitet.
- I en metaanalys baserad på sex originalpublikationer konstaterades hos barn och unga som haft atopiskt eksem en cirka 30 procent större sannolikhet att insjukna i ADHD än hos kontrollpersoner som inte haft atopiskt eksem «Schans JV, Çiçek R, de Vries TW ym. Association of...»79. En eventuell förklaring som presenterats är hur allmän överkänslighet, stress orsakad av eksem, sömnbrist och trötthet samt inflammationsmediatorer påverkar hjärnans utveckling.
- Ett aktiverat Th2-inflammationssvar är en eventuell etiologisk förklaring till neuropsykologiska associerade sjukdomar i samband med atopiskt eksem «Jackson-Cowan L, Cole EF, Arbiser JL ym. TH2 sensi...»80.
- I en amerikansk befolkningsstudie konstaterades också en ökad risk för ADHD-diagnos hos vuxna med atopiskt eksem «Fan R, Leasure AC, Damsky W ym. Association of ato...»81.
- Personer med atopiskt eksem har en högre risk för osteoporos och frakturer. Man känner inte till den exakta orsaken till detta, men det är möjligt att det har samband med en kronisk inflammation, en mer allmän D-vitaminbrist än hos den övriga befolkningen eller användningen av systemiska kortikosteroider «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63.
- Sambandet mellan atopiskt eksem och hjärt- och kärlsjukdomar samt tillhörande riskfaktorer är fortfarande oklart. Personer med svårt eksem har uppenbarligen mer hjärt- och kärlsjukdomar, men den absoluta risken är ändå liten «Silverberg JI. Comorbidities and the impact of ato...»82, «Ascott A, Mulick A, Yu AM ym. Atopic eczema and ma...»83. Hittills har det inte funnits några tecken på att en effektiv behandling av atopiskt eksem skulle minska risken «Davis DMR, Drucker AM, Alikhan A ym. American Acad...»63. Det går inte att ge en rekommendation om behov av noggrannare screening än normal åldersenlig uppföljning «Pandher K, Ghamrawi RI, Heron CE ym. Controversial...»84.
Livskvalitet och psykiska faktorer
- Svårt atopiskt eksem försämrar livskvaliteten avsevärt «Rehal B, Armstrong AW. Health outcome measures in ...»85. Se Atopiskt eksem: inverkan på olika livsområden «Atooppinen ekseema: vaikutus eri elämänalueisiin»10.
- Personer med atopiskt eksem har mer sömnstörningar och kronisk trötthet än den övriga befolkningen «Silverberg JI, Garg NK, Paller AS ym. Sleep distur...»86. I en svensk studie konstaterades att sannolikheten för allvarliga sömnstörningar hos personer med svårt atopiskt eksem var 7,9 gånger och för svår kronisk trötthet 10,2 gånger större jämfört med kontrollpersoner som inte hade atopiskt eksem «Theodosiou G, Montgomery S, Metsini A ym. Burden o...»87. Den förklarande faktorn torde vara klåda. Sömnbrist och trötthet kan också påverka koncentrationsförmågan.
- Eksemets svårighetsgrad, den upplevda stigman och nedstämdheten orsakad av eksem verkar vara de mest betydande faktorerna som försämrar livskvaliteten hos vuxna «Wittkowski A, Richards HL, Griffiths CE ym. The im...»88.
- Omfattande atopiskt eksem hos barn påverkar barnets och familjens livskvalitet åtminstone lika mycket som de flesta andra kroniska sjukdomar hos barn «Beattie PE, Lewis-Jones MS. A comparative study of...»89. Hos barn är klåda, skrapning och hudens ömhet de mest skadliga faktorerna som påverkar livskvaliteten «Gånemo A, Svensson A, Lindberg M ym. Quality of li...»90.
- Se också Aikakauskirja Duodecims artikel Atooppinen ihottuma vaikuttaa elämänlaatuun ja elämänhaluun «Koulu L. Atooppinen ihottuma vaikuttaa elämänlaatu...»91, «https://www.duodecimlehti.fi/lehti/2020/22/duo15895»2.
- Psykiska faktorer och stress är viktiga faktorer som förvärrar atopiskt eksem. I en finländsk uppföljningsstudie «Lammintausta K, Kalimo K, Raitala R ym. Prognosis ...»92 uppgav 45–67 procent av patienterna med svårt atopiskt eksem som vårdades inom den specialiserade sjukvården att stress är den största faktorn som förvärrar deras eksem. Man känner dåligt till stressmekanismerna som utlösare av atopiskt eksem. En del patienter med atopiskt eksem kan ha nytta av psykologiska vårdmetoder (beteendeterapeutiska tillvägagångssätt, psykoedukation och åtgärder som syftar till att minska stress) som stöd för medicinsk vård «Chida Y, Steptoe A, Hirakawa N ym. The effects of ...»93, «Ersser SJ, Cowdell F, Latter S ym. Psychological a...»94.
- En god anpassning till sjukdomen hos en patient med atopiskt eksem och hos föräldrarna till en barnpatient stöder behandlingsföljsamheten och garanterar ett så lyckat behandlingsresultat som möjligt. Genom patienthandledning försöker man förbättra den psykiska hanteringen av sjukdomen och den kan uppenbarligen minska svårighetsgraden av atopiskt eksem «Potilasohjauksella voidaan ilmeisesti vähentää atooppisen ekseeman vaikeusastetta.»B.
- Vårdtrötthet kan försämra behandlingsresultatet för atopiskt eksem och därför är det nödvändigt att identifiera det. Vården kan börja kännas frustrerande och belastande, varvid följsamheten i egenvården försämras. Det är bra om läkaren och sjukskötaren för vårdtrötthet på tal både i början av vården och under uppföljningsbesöken, särskilt om det uppstår problem i genomförandet av vården.
Allmänna principer för behandling av atopiskt eksem
- Målet med behandlingen är långvarig symtomkontroll: att minimera symtomen, minska antalet försämringsskov och lindra svårighetsgraden samt förbättra patientens livskvalitet och arbets- och funktionsförmåga.
- Behandlingen väljs individuellt och påverkas bland annat av eksemets omfattning och
svårighetsgrad, responsen på tidigare behandlingar och eventuella biverkningar, patientens
möjligheter att genomföra behandlingen, kontraindikationer för behandlingar samt patientens
övriga sjukdomar och medicineringar.
- För de flesta patienter räcker det med lokalbehandling.
- Om nivåstrukturering av behandlingsalternativen för atopiskt eksem se bilden Behandlingsalgoritm vid atopiskt eksem «Behandlingsalgoritm vid atopiskt eksem»1.
- Särdragen i vården av barn beskrivs i avsnittet Särdrag i behandlingen av atopiskt eksem hos barn (0–16-åringar) «A3»5.
Verktyg för bedömning av symtom, svårighetsgrad och vårdrespons vid atopiskt eksem
- Validerade mätare kan användas för en klinisk bedömning av eksemets svårighetsgrad. I synnerhet inom den specialiserade sjukvården rekommenderas användning av mätare som beskriver sjukdomens svårighetsgrad också i uppföljningen av vårdresponsen.
- God medicinsk praxis-arbetsgruppen rekommenderar i första hand EASI-mätaren för mätning
av eksemets svårighetsgrad i Finland.
- EASI (Eczema Area and Severity Index): en bedömning som görs av läkare för att fastställa svårighetsgraden av atopiskt eksem och som beaktar eksemets omfattning (procentandel) i huvudet, bålen och de övre och nedre extremiteterna enligt en separat bedömning samt rodnad, papler (knottror), svullnad, skrapspår och förgrovning av huden.
- EASI-75: EASI har minskat med minst 75 procent från utgångsläget.
- EASI-kalkylatorn se «hoi50077e.xlsx»3
- Vid bedömningen av sjukdomens svårighetsgrad är det också bra att beakta patientens
egen bedömning av sjukdomssymtomen. POEM lämpar sig väl för kliniskt arbete «Leshem YA, Chalmers JR, Apfelbacher C ym. Measurin...»95.
- POEM (Patient Oriented Eczema Measure): en enkät som mäter eksemsymtom utifrån patientens egen bedömning. Se «https://www.nottingham.ac.uk/research/groups/cebd/documents/methodological-resources/ao-av153560-poem-for-self-completion-finnish-finland-version-1-25aug2016.pdf.»3
- Den mest tillförlitliga mätaren för uppföljning av klåda och smärta är NRS-mätaren.
- NRS (numerical rating scale): patienten bedömer hudens maximala klåda eller smärta numeriskt (0–10) under de senaste 24 timmarna.
- Som mätare av livskvaliteten används i första hand DLQI-enkäten. Som mätare för livskvaliteten
hos barn i åldern 4–16 år används CDLQI-enkäten och IDQOL-enkäten för barn under 4
år.
- DLQI (Dermatology Life Quality Index): enkät om hudsjukdomar som används som livskvalitetsmätare för vuxna. Se «https://www.cardiff.ac.uk/medicine/resources/quality-of-life-questionnaires/dermatology-life-quality-index»4 (se punkten Different language versions, other languages).
- CDLQI (Children's Dermatology Life Quality Index): en enkät om hudsjukdomar som används som livskvalitetsmätare för 4–16-åringar.
- IDQOL (Infant's Dermatology Quality of Life Index): en enkät för föräldrar till barn under 4 år med atopiskt eksem som används som livskvalitetsmätare.
- I DLQI-, CDLQI- och IDQOL-enkäterna bedöms hudsjukdomens inverkan på livskvaliteten under den senaste veckan.
- För att bedöma den terapeutiska balansen för atopiskt eksem kan man använda ADCT-
eller RECAP-enkäter, varav ADCT är tillgänglig på finska och svenska «Simpson E, Eckert L, Gadkari A ym. Validation of t...»96.
- ADCT (Atopic Dermatitis Control Tool): i enkäten bedöms den terapeutiska balansen för atopiskt eksem under den senaste veckan. Se «https://www.adcontroltool.com/»5 (se punkten Information for patients och välj finska eller svenska i språkmenyn).
- RECAP (Recap of atopic eczema) (4/2023 ej översatt till finska eller svenska).
- Läs mer om Mätarna för bedömning av atopiskt eksem «Atooppisen ekseeman arvioinnissa käytettäviä mittareita»5.
Egenvård och patienthandledning
- Egenvård är hörnstenen i behandling av atopiskt eksem. Till egenvården hör
- alltid bassalvor och läkemedelssalvor enligt läkarens anvisningar
- undvikande av försämrande faktorer (se avsnittet Försämrande faktorer «A4»6).
- Att tvätta sig dagligen förvärrar inte atopiskt eksem «Päivittäinen pesu lienee hyväksi atoopikon ekseemaiselle iholle.»C.
- Tvätten tar bort smuts, svett, skorv och bakterier som irriterar huden.
- Vid behov används oparfymerat, surt eller neutralt tvättmedel eller tvål.
- Vid rengöring av atopisk hud används ofta bassalvor i stället för tvål. Det finns dock ingen forskningsevidens om nyttan med denna praxis «Tarr A, Iheanacho I. Should we use bath emollients...»97.
- Att använda en bassalva efter att man tvättat sig förhindrar uttorkning av huden och kan binda fukt i huden «Chiang C, Eichenfield LF. Quantitative assessment ...»98.
- Patienthandledningen är en del av en övergripande, multiprofessionell behandling av
en kronisk sjukdom. Målet med handledningen är att förbättra patienternas och familjernas
förmåga att klara sig samt behandlingsföljsamheten genom att öka förståelsen för den
kroniska sjukdomen och behandlingen av den.
- Med patienthandledning kan man uppenbarligen minska svårighetsgraden av atopiskt eksem «Potilasohjauksella voidaan ilmeisesti vähentää atooppisen ekseeman vaikeusastetta.»B, och med handledningen har det varit möjligt att effektivera bland annat en adekvat användning av bassalvor «Cork MJ, Britton J, Butler L ym. Comparison of par...»99.
- Behovet av patienthandledning och dess natur varierar individuellt och det går inte att ge detaljerade rekommendationer om effektiv patienthandledning.
- Det är särskilt viktigt att patienten får anvisningar om smörjning av huden.
- Se anvisningar för egenvård
- Handledd egenvård av atopiskt eksem hos vuxna «hoi50077c.pdf»1
- Handledd egenvård av atopiskt eksem hos barn «hoi50077d.pdf»2
- Anvisningar om atopiskt eksem för föräldrar «Ohje vanhemmille atooppisesta ekseemasta»1
- Videor: Atopiskt eksem hos vuxna «Atooppinen ekseema -suosituksen videot (aikuiset)»2 och «Yleistä atooppisesta ekseemasta (aikuiset) video»11 hos barn «Atooppinen ekseema -suosituksen videot (lapset)»3 och «Yleistä atooppisesta ekseemasta (lapset) video»12.
- Se anvisningar för egenvård
Lokalbehandling
- Den primära behandlingen av atopiskt eksem är lokalbehandling. Den omfattar
- regelbunden smörjning av huden med bassalva 1–2 gånger per dag
- behandling av eksemområden med läkemedelssalvor och bassalvor.
- Lokalbehandling behövs i allmänhet också i samband med UV-behandling och systemisk medicinering.
Bassalvor
- Bassalvor kan indelas i vanliga bassalvor och bassalvor som innehåller fuktbindande ämnen, dvs. humektanter (bl.a. karbamid, dvs. urea, glycerol och propylenglykol).
- Bassalvor används för att behandla torr hud. De kan binda fukt och mjukgöra huden. Målet är att få eksemet bättre under kontroll och förebygga återfall.
- Bassalvor är den huvudsakliga behandlingen av lindrigt atopiskt eksem och alltid också
en del av behandlingen av måttligt eller svårt atopiskt eksem. Vanligtvis räcker det
med 1–2 smörjningar per dag.
- Om huden är torr är det viktigt att en person som har atopiskt eksem använder bassalva regelbundet, särskilt vintertid, även om det inte förekommer några eksem.
- Bassalvan och läkemedelssalvan appliceras inte samtidigt på samma hudområde, utan det är bra att hålla en paus mellan dem så att den salva som applicerats först hinner absorberas.
- Bassalvor minskar uppenbarligen symtomen på atopiskt eksem, såsom klåda och antalet
försämringsskov «Perusvoiteet ilmeisesti vähentävät atooppisen ekseeman oireita.»B. De återfuktar huden och minimerar avdunstningen av vatten från huden. Fuktbindande
bassalva (innehåller karbamid eller glycerol) kan effektivare än enbart bassalva (eller
utan bassalva) minska eksemets svårighetsgrad och antalet försämringsskov «van Zuuren EJ, Fedorowicz Z, Christensen R ym. Emo...»100.
- Bassalva som innehåller karbamid kan orsaka sveda i huden, särskilt vid behandling av akut, sönderskrapat eksem.
- Det finns inga forskningsrön om användningen av karbamid vid behandling av atopiskt eksem hos små barn. I internationella vårdrekommendationer rekommenderar man att undvika karbamid hos spädbarn. Hos barn i lekåldern kan man använda lägre halter än vid behandling av vuxna «Wollenberg A, Kinberger M, Arents B ym. EuroGuiDer...»101.
- Valet av typ av salva beror på individuella faktorer.
- Det är bra om patienten själv väljer en lämplig bassalva «Williams HC. Clinical practice. Atopic dermatitis....»102, eftersom det förbättrar behandlingsföljsamheten.
- När behandlingen inleds kan det vara bra att börja med en medelfet bassalva som hos de flesta patienter lämpar sig bäst som grundbehandling. Om patienten redan en timme efter appliceringen av bassalvan känner att huden inte alls har smörjts in, bör man övergå till en fetare eller mer humektantrik salva. Om salvan däremot känns för fet kan det vara bra att övergå till en lättare.
- Om någon typ av salva orsakar sveda i huden kan man byta till en fetare salva.
- Valet av salva varierar också beroende på årstid: på vintern behövs fetare bassalvor och på sommaren räcker det med lättare salvor. En del patienter kan klara sig med mindre smörjning under sommaren.
- Lättare, mindre oljehaltiga salvor bör användas på håriga hudområden.
- Det finns inga bevis på takyfylaxi, dvs. att huden "tröttnar" på en bassalva, under en längre användning «Hoare C, Li Wan Po A, Williams H. Systematic revie...»103.
- Receptet ska innehålla en tillräckligt stor mängd bassalva. Om alla hudområden smörjs in använder en vuxen 1,0–1,5 kg bassalva per månad «Hannuksela-Svahn A, Hannuksela M. Ihotautien paika...»104.
- För att patienten ska få grundersättning för en bassalva som ersätts av FPA antecknas "kronisk hudsjukdom" på receptet.
- Mer information om bassalvornas egenskaper och användning vid atopiskt eksem finns i tilläggsmaterialet «Lisätietoa perusvoiteiden ominaisuuksista ja humektanttien vaikutuksista»13.
Lokala kortikosteroider
- Lokala kortikosteroider är de primära läkemedlen vid atopiskt eksem.
- Vanligtvis räcker milda eller medelstarka lokala kortikosteroider till för behandling av atopiskt eksem, men vid besvärligt eller förtjockat eksem kan även starka lokala kortikosteroider användas. Se tabell «Arbetsgruppens rekommendation, baserad på erfarenhet och klinisk användning, om effektivitetsklassen på kortikosteroidsalva som bör användas på olika hudområden hos vuxna (över 16 år). För personer över 75 år rekommenderas en försiktigare användning av kortikosteroider....»1.
- Kortikosteroidsalvor får användas vid hudsår orsakade av eksem och kan användas sommartid och under UV-behandling.
- Lokala kortikosteroider i Finland indelas i fyra grupper: svaga, medelstarka, starka
och mycket starka (mer information «Paikalliskortikosteroidien luokittelu vaikutuksen voimakkuuden mukaan»14).
- Övergången till ett starkare preparat ökar steroidens absorption i huden och i direkt proportion också biverkningarna.
- Hur lokala kortikosteroider tränger igenom huden varierar och är rikligast i tunn hud (ansikte, hals, genitalier).
- Svagare lokala kortikosteroider rekommenderas för tunn hud som är lättgenomtränglig och starkare för områden med tjock hud med sämre genomtränglighet (se tabell «Arbetsgruppens rekommendation, baserad på erfarenhet och klinisk användning, om effektivitetsklassen på kortikosteroidsalva som bör användas på olika hudområden hos vuxna (över 16 år). För personer över 75 år rekommenderas en försiktigare användning av kortikosteroider....»1).
- Lokala kortikosteroider bygger vanligen på en salva eller emulsionskräm, men på marknaden finns också lösningar för behandling av håriga hudområden såsom hårbotten. Salvbasen har en viss inverkan på behandlingseffekten. Fetare salvor kan vara effektivare «Nesbitt LT. Glucocorticoids. In: Bologna JL, Joriz...»105.
- Användning av kortikosteroidsalvor hos barn, se «A5»7.
- Kortikosteroidsalva används som periodisk behandling och dessutom vid behov som underhållsbehandling.
Det lönar sig att prioritera underhållsbehandling särskilt vid måttligt och svårt
samt vid atopiskt eksem som återkommer snabbt efter den dagliga behandlingsperioden.
Se anvisningen «Atooppisen ekseeman hoito lääkevoiteella»28.
- Vid periodisk behandling för vuxna används kortikosteroidsalva i allmänhet i 1–3 veckors
oavbrutna kurer «Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106. I ansiktet används vanligtvis kortare 1–2 veckors kurer.
- Vid behandling av atopiskt eksem hålls pauser mellan kurerna. Pauserna är minst lika långa som behandlingsperioden. I de svåraste fallen kan detta dock leda till att eksemet återkommer snabbt. Återfall av måttligt och svårt atopiskt eksem kan bromsas upp genom underhållsbehandling.
- Underhållsbehandling: När eksemet läkts används en medelstark eller stark kortikosteroidsalva
en gång per dag två gånger i veckan på de hudområden där eksemet vanligtvis framträder.
Underhållsbehandling kan vid behov användas i flera månader. Se anvisningen «Atooppisen ekseeman hoito lääkevoiteella»28.
- Underhållsbehandling efter en kur med lokal stark kortikosteroid (bål och extremiteter) två gånger i veckan verkar förhindra relapser av atopiskt eksem «Ylläpitohoito 2 kertaa viikossa vahvalla paikalliskortikosteroidilla näyttää ehkäisevän atooppisen ekseeman relapsia.»B utan betydande risk för hudförtunning «Danby SG, Chittock J, Brown K ym. The effect of ta...»107.
- I två omfattande (n = över 600) underhållsbehandlingsstudier som pågått i 4–5 månader konstaterades inga betydande biverkningar av stark kortikosteroidsalva «Hanifin J, Gupta AK, Rajagopalan R. Intermittent d...»108, «Berth-Jones J, Damstra RJ, Golsch S ym. Twice week...»109.
- Utifrån klinisk erfarenhet kan underhållsbehandling också genomföras med medelstark kortikosteroidsalva, men med mild kortikosteroidsalva är effekten i allmänhet otillräcklig «Wollenberg A, Kinberger M, Arents B ym. EuroGuiDer...»101.
- Vid periodisk behandling för vuxna används kortikosteroidsalva i allmänhet i 1–3 veckors
oavbrutna kurer «Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106. I ansiktet används vanligtvis kortare 1–2 veckors kurer.
- Medelstarka eller starka kortikosteroider används vanligtvis en gång per dag. Det finns ingen evidens på att flera smörjningar skulle öka behandlingens effekt «Williams HC. Established corticosteroid creams sho...»110, «Woods MT, Brown PA, Baig-Lewis SF ym. Effects of a...»111, «Bieber T, Vick K, Fölster-Holst R ym. Efficacy and...»112.
- Det finns ingen evidens på att lokala kortikosteroider skulle förlora sin effekt vid långvarig periodisk användning.
- Användningen av enbart kortikosteroidsalva minskar även hudens stafylokocker. Ju starkare kortikosteroid, desto effektivare kan man minska bakteriehalten «Stalder JF, Fleury M, Sourisse M ym. Local steroid...»113, «Nilsson EJ, Henning CG, Magnusson J. Topical corti...»114.
- Användningen av lokala kortikosteroider begränsas av de biverkningar de orsakar, av
vilka den viktigaste är en förtunning av huden när kollagenmängden i huden minskar
«Oikarinen A, Autio P, Kiistala U ym. A new method ...»115.
- En permanent förtunning av huden förutsätter ofta flera månaders oavbruten användning.
- Särskilt hudområden som är tunna från tidigare samt huden hos äldre personer är mottagliga för förtunning.
- Andra eventuella hudbiverkningar av behandlingen är strior, telangiektasier och blåmärken.
- Långvarig användning av medelstarka eller starka kortikosteroidsalvor i ansiktet som strider mot rekommendationerna kan orsaka rodnad, brännande och stickningar i huden som liknar rosacea när man gör uppehåll i medicineringen ("lokalt steroidberoende"). Fenomenet förekommer mest i ansiktet och genitalområdet hos kvinnor «Hajar T, Leshem YA, Hanifin JM ym. A systematic re...»116.
- Långvarig användning på ögonlocken kan orsaka gråstarr och glaukom «Haeck IM, Rouwen TJ, Timmer-de Mik L ym. Topical c...»117.
- Systembiverkningar, såsom hypokortisolism, är sällsynta men möjliga särskilt vid behandling av omfattande eksem hos barn «Axon E, Chalmers JR, Santer M ym. Safety of topica...»118.
| Hudområde | Salvans effektivitetsklass | |||
|---|---|---|---|---|
| * Vid behandling av periokulärt eksem är kalcineurinhämmare primära. Plustecknen beskriver styrkan i arbetsgruppens rekommendation. – = rekommenderas inte |
||||
| I | II | III | IV | |
| Ansikte, hals | +++ | + | - | - |
| Ögonlock | +* | - | - | - |
| Veck, genitalier | +++ | ++ | - | - |
| Bål, extremiteter | + | +++ | ++ | - |
| Handflator, fotsulor | - | ++ | +++ | + |
| Hårbotten, nacke | - | +++ | ++ | + |
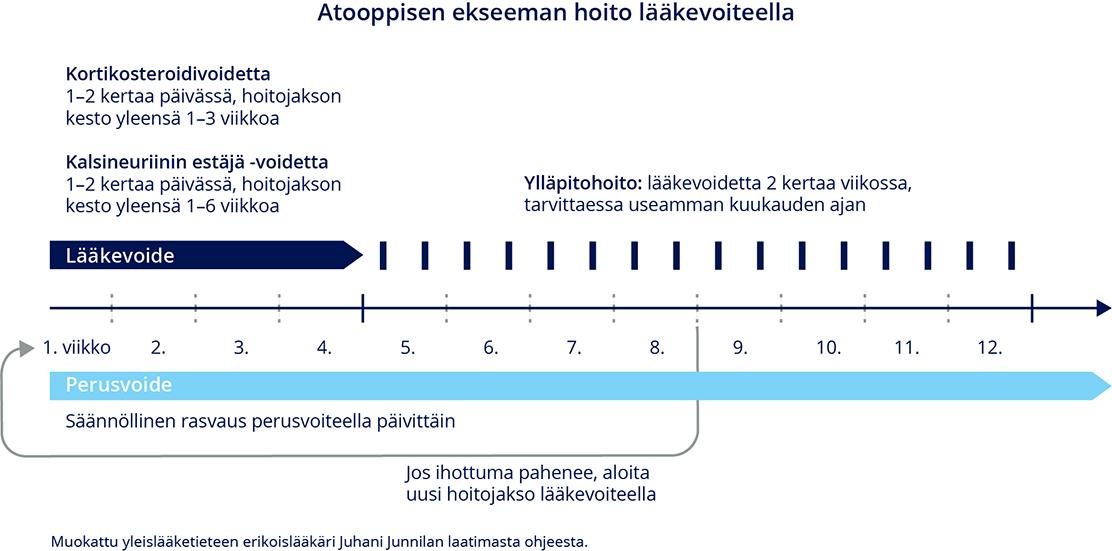
Atooppisen ekseeman hoito lääkevoiteella
Lokala kalcineurinhämmare (takrolimus och pimekrolimus)
- Kalcineurinhämmare är sekundära läkemedel mot atopiskt eksem. Om lokala kortikosteroider
inte ger tillräcklig långvarig respons används takrolimussalva eller pimekrolimusemulsionskräm.
- Ett undantag är områden med tunn hud (t.ex. ansiktet) där kalcineurinhämmare också kan användas som primära läkemedelssalvor «Kang S, Paller A, Soter N ym. Safe treatment of he...»119, «Doss N, Reitamo S, Dubertret L ym. Superiority of ...»120.
- Vid behandling av atopiskt eksem i ögonområdet är kalcineurinhämmare primära på grund
av biverkningar i anslutning till kortikosteroider «Kang S, Paller A, Soter N ym. Safe treatment of he...»119, «Murrell DF, Calvieri S, Ortonne JP ym. A randomize...»121.
- Kalcineurinhämmare påverkar inte hudens kollagensyntes och förtunnar därför inte huden ens vid långvarig behandling «Reitamo S, Rissanen J, Remitz A ym. Tacrolimus oin...»122, «Kyllönen H, Remitz A, Mandelin JM ym. Effects of 1...»123.
- Indikationen för takrolimus är måttligt eller svårt atopiskt eksem från och med två
års ålder.
- En 0,03-procentig takrolimussalva är avsedd för behandling av vuxna, unga och 2-åringar eller äldre barn.
- En 0,1-procentig takrolimussalva är avsedd för behandling av vuxna och unga (16-åringar eller äldre).
- Indikationen för pimekrolimus är lindrigt eller måttligt atopiskt eksem från 3 månaders ålder.
- Lokala kalcineurinhämmare hos barn, se punkt «A5»7.
- Takrolimussalva eller pimekrolimusemulsionskräm används i eksemområdena två gånger
per dag tills eksemet har läkt. När eksemet har läkt görs ett uppehåll i användningen.
När symtom framträder inleds genast en ny behandlingsperiod.
- Underhållsbehandlingen med takrolimussalva är effektiv för att förhindra försämringsskov hos både barn och vuxna. Eksemet behandlas två gånger per dag tills det har lugnat sig, varefter smörjningen fortsätter 2–3 gånger i veckan. Underhållsbehandlingen tolereras lika väl som behandlingen med salvbas «Ylläpitohoito takrolimuusivoiteella 2–3 kertaa viikossa alueille, joissa ihottumaa yleensä on esiintynyt, vähentää merkittävästi pahenemisvaiheita ja kortikosteroidivoiteiden käyttöä perusvoiteisiin verrattuna.»A. Se anvisningen «Atooppisen ekseeman hoito lääkevoiteella»28.
- Samtidig användning av kortikosteroidsalva och lokal kalcineurinhämmare på samma hudområden förbättrar uppenbarligen inte behandlingsresultatet jämfört med enbart kortikosteroidsalva. I en studie där pimekrolimusemulsionskräm kombinerades med en stark kortikosteroidsalva på samma behandlingsområde, förbättrades inte behandlingsresultaten jämfört med användning av enbart en stark kortikosteroidsalva hos barn med svårt atopiskt eksem «Meurer M, Eichenfield LF, Ho V ym. Addition of pim...»124.
- Att behandla känsliga hudområden, såsom ansiktet, med lokala kalcineurinhämmare och andra hudområden med kortikosteroidsalva kan vara ett praktiskt och kostnadseffektivt behandlingsalternativ «Wollenberg A, Kinberger M, Arents B ym. EuroGuiDer...»101.
- 0,03-procentig takrolimussalva är effektivare än en salvbas och behandling med mild kortikosteroidsalva (hydrokortisonacetat) «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125.
- 0,1-procentig takrolimussalva är effektivare än en salvbas och har samma effekt som en medelstark kortikosteroidsalva vid behandling av atopiskt eksem hos vuxna «Takrolimuusivoide (0,1-prosenttinen ja 0,03-prosenttinen) on tehokkaampi (EASI-pisteiden merkittävä väheneminen ja kutinan väheneminen) kuin voidepohja, ja 0,1-prosenttinen takrolimuusivoide on yhtä tehokas (mEASI pisteiden väheneminen) kuin hydrokortisoni-17-butyraattivoide atooppisen ekseeman hoidossa.»A. 0,1-procentig takrolimussalva verkar vara effektivare än en 1-procentig pimekrolimusemulsionskräm vid behandling av atopiskt eksem hos vuxna «0,1-prosenttinen takrolimuusivoide on ilmeisesti 1-prosenttista pimekrolimuusiemulsiovoidetta tehokkaampi (EASI-alenema 54 % vs. 35 %) aikuisten atooppisen ekseeman lyhytaikaisessa hoidossa.»B, «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125.
- Pimekrolimusemulsionskräm är effektivare än bassalva vid behandling av lindrigt och måttligt atopiskt eksem hos vuxna «Pimekrolimuusiemulsiovoide on voidepohjaa tehokkaampi aikuisten atooppisen ekseeman hoidossa.»A. Jämförande studier har inte publicerats mellan pimekrolimusemulsionskräm och svag lokal hydrokortisonbehandling. Pimekrolimus är ineffektivare vid behandling av atopiskt eksem än en medelstark eller stark lokal kortikosteroid (triamcinolonacetonid och betametasonvalerat) «Ashcroft DM, Chen LC, Garside R ym. Topical pimecr...»126.
- 0,1-procentig takrolimussalva orsakar i början av behandlingen hetta på huden hos cirka 50–60 procent av patienterna «Takrolimuusivoide aiheuttaa ihon kuumotusta hoidon alkuvaiheessa.»A. Hettan är mest besvärlig under de första dagarna av behandlingen men hos de flesta avtar den inom några dygn i och med regelbunden användning av salvan «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125, «Ashcroft DM, Chen LC, Garside R ym. Topical pimecr...»126. Ju svårare eksemet är när behandlingen inleds, desto kraftigare är oftast hettan på huden.
- Enligt studier som pågått i 3 veckor och 12 veckor verkar det inte finnas någon betydande skillnad i fråga om biverkningar mellan dem som behandlats med 0,03- och dem som behandlats med 0,1-procentig takrolimussalva «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125.
- Det verkar inte finnas någon signifikant skillnad i fråga om biverkningar efter 6 veckor mellan de som behandlats med 0,1-procentig takrolimussalva och de som behandlats med 1-procentig pimekrolimusemulsionskräm «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125.
- I början av behandlingen kan man ofta lindra hudens hetta genom att behandla eksemet med en lokal kortikosteroid i 1–2 veckor, varefter man genast inleder behandling med kalcineurinhämmare. Om hettan trots detta är kraftig och försvårar fortsatt behandling, kan acetylsalicylsyra eller eventuellt ibuprofen som tagits en timme före smörjningen vara till hjälp för att lindra hettan «Mandelin J, Remitz A, Reitamo S. Effect of oral ac...»127. Underhållsbehandlingen tolereras lika väl som behandling med salvbas och den kan uppenbarligen förhindra att hudens hetta återkommer «Ylläpitohoito takrolimuusivoiteella 2–3 kertaa viikossa alueille, joissa ihottumaa yleensä on esiintynyt, vähentää merkittävästi pahenemisvaiheita ja kortikosteroidivoiteiden käyttöä perusvoiteisiin verrattuna.»A.
- Takrolimus och pimekrolimus absorberas i blodomloppet endast i liten grad «Reitamo S, Wollenberg A, Schöpf E ym. Safety and e...»128, «Hanifin JM, Ling MR, Langley R ym. Tacrolimus oint...»129, «Ling M, Gottlieb A, Pariser D ym. A randomized stu...»130 och användningen av dem är i allmänhet inte förknippad med någon ökning av bakterie-, virus- eller svampinfektioner i huden «Cury Martins J, Martins C, Aoki V ym. Topical tacr...»125, «Ashcroft DM, Dimmock P, Garside R ym. Efficacy and...»131.
- Utifrån aktuell kunskap har man inte kunnat påvisa någon betydligt ökad cancerrisk i samband med användningen av lokala kalcineurinhämmare. Den längsta medianen för uppföljningstiden är 27 år «Legendre L, Barnetche T, Mazereeuw-Hautier J ym. R...»66. För mer information se «Syöpä- ja lymfoomariski kalsineuriinin estäjien paikallisen käytön yhteydessä»9.
- Ersättning av kalcineurinhämmare, se FPA:s webbplats «https://www.kela.fi/lakemedel317»6.
Förband och omslag
- Elastiska förband skyddar huden mot skrapning, vilket kan få eksemet att lugna sig snabbare. Förband lämpar sig för behandling av sönderskrapat eksem i extremiteterna. Under förbandet används lokal kortikosteroid eller bassalva. Vid behandling av mycket envist eksem kan ett förband som innehåller zinkoxidpasta, och som får sitta kvar i några dagar, användas som komplement till lokalbehandlingen.
- Den lokala kortikosteroidens absorption och effekt kan öka med ocklusionsbehandling. Ocklusionsbehandlingen lämpar sig särskilt för behandling av förtjockade eksem på små hudområden. Som ocklusionsförband används vanligen en hydrokolloidplatta som får sitta kvar i upp till en vecka. Hydrokolloidplattan fäster bäst om kortikosteroiden finns i en lösningsbas.
- Koksalt- eller 0,25-procentigt zinksulfatomslag lämpar sig för behandling av vätskande eksem i det första skedet. Omslagsbehandlingen avslutas när eksemet har börjat torka. Se patientanvisningarna om användning av fuktigt omslag vid behandling av atopiskt eksem på finska «Potilasohje kostean kääreen käytöstä atooppisen ekseeman hoidossa»15 och på svenska «Patientinformation om fuktigt bandage vid vård av atopiskt exem»16.
- Se videor om ocklusionsbehandling av atopiskt eksem (omslag) hos barn «Atooppisen ekseeman peittohoito (video)»17 och om ocklusionsbehandling av atopiskt eksem hos vuxna «Atooppisen ekseeman peittohoito (video)»18.
Lokala antimikrobiella medel
- Det finns inte evidens för nyttan av enbart lokalt verkande antimikrobiella medel vid behandling av atopiskt eksem «George SM, Karanovic S, Harrison DA ym. Interventi...»132.
- Kombinationspreparat som innehåller lokal kortikosteroid och antibiotika eller ett
antimikrobiellt medel kan vara effektivare än enbart lokal kortikosteroid för att
lindra eksemsymtom, men tilläggseffekten är mycket liten «George SM, Karanovic S, Harrison DA ym. Interventi...»132.
- Lokala antiseptiska ämnen (klorhexidin, kaliumpermanganat) i kombination med behandling med kortikosteroidsalva används för behandling av vätskande eller infekterat atopiskt eksem, men kontrollerade studier i ämnet har inte gjorts.
- Långvarig användning av lokala antibiotika rekommenderas att undvika för att hindra
utvecklingen av resistenta bakteriestammar.
- Enbart kortikosteroidsalva minskar antalet stafylokocker i huden. Ju starkare kortikosteroid, desto effektivare kan man minska bakteriehalten «Stalder JF, Fleury M, Sourisse M ym. Local steroid...»113, «Nilsson EJ, Henning CG, Magnusson J. Topical corti...»114.
- Även takrolimus har visat sig minska mängden stafylokocker vid atopiskt eksem «Remitz A, Kyllönen H, Granlund H ym. Tacrolimus oi...»133.
- Läs mer om bakterier vid atopiskt eksem «Lisätietoa bakteereista atooppisessa ekseemassa»19.
- Se också God medicinsk praxis-rekommendationen Hudinfektioner «Hudinfektioner»3.
- Svampinfektioner:
- Betydelsen av Malassezia-jästsvampen, som hör till hudens normala flora, vid atopiskt eksem är oklar och det finns inte tillräcklig evidens på effekten av antimykotiska systemiska eller lokala läkemedel «Mayser P, Kupfer J, Nemetz D ym. Treatment of head...»134, «Kaffenberger BH, Mathis J, Zirwas MJ. A retrospect...»135, «Svejgaard El, Larsen PØ, Deleuran M ym. Treatment ...»136.
- Läs mer om svampinfektioner i huden vid atopiskt eksem «Lisätietoa ihon sieni-infektioista atooppisessa ekseemassa»20.
UV-behandling
- UV-behandling kan användas vid måttligt och svårt atopiskt eksem hos vuxna om lokalbehandling inte ger tillräcklig respons. UV-behandling ges 2–3 gånger i veckan i perioder om 15–20 behandlingar. Den rekommenderade övre gränsen för årlig behandling är två perioder.
- Utrustningen klassificeras enligt UV-spektret «Eri valohoitolamppujen emittoiman UV-säteilyn aallonpituusspektrit»29. I Finland används huvudsakligen smalbandig UVB-behandling och i andra hand SUP-behandling
för behandling av atopiskt eksem.
- SUP-behandling (selektiv UV-behandling, våglängdsområdet motsvarar finländsk sommarsol) är en behandlingsform som håller på att försvinna.
- Inrättningar som ger UV-behandling ska följa myndigheternas anvisningar.
- UV-behandlingens effekt grundar sig på dämpning av den immunologiska inflammationsprocessen. UV-strålningen påverkar inflammationsceller, inflammationsmediatorer och antimikrobiella peptider «Krutmann J, Morita A. Mechanisms of ultraviolet (U...»137, «Tintle S, Shemer A, Suárez-Fariñas M ym. Reversal ...»138, «Gambichler T, Skrygan M, Tomi NS ym. Changes of an...»139.
- Den primära UV-behandlingen av vuxna patienter är smalbandig UVB (lysrör TL01, våglängdsområde 311 ± 2 nm) «Lübbe J. Secondary infections in patients with ato...»140, «Garritsen FM, Brouwer MW, Limpens J ym. Photo(chem...»141. Det finns få forskningsrön om UV-behandlingsdoser, behandlingens längd, responsens varaktighet och om eventuella långvariga biverkningar vid behandling av atopiskt eksem. Det finns inga studier om livskvaliteten i samband med UV-behandling. För att UV-behandlingen ska kunna placeras rätt i nivåstruktureringen av behandlingen, skulle det behövas ytterligare studier om smalbandig UVB-behandling med enhetliga mätare för långtidssäkerheten och responsen «Musters AH, Mashayekhi S, Harvey J ym. Phototherap...»142. Smalbandig UVB-behandling minskar uppenbarligen symtomen och fynden vid atopiskt eksem hos vuxna «Kapeakaistainen UVB-hoito ilmeisesti vähentää aikuisten atooppisen ekseeman oireita ja löydöksiä. Hoitovasteen pituudesta ei ole tietoa.»B.
- Det finns ganska lite information om remissionens längd: Tre månader efter avslutad behandling kan man uppenbarligen se en gynnsam respons hos cirka hälften av patienterna «Reynolds NJ, Franklin V, Gray JC ym. Narrow-band u...»143.
- Eventuella akuta biverkningar är rodnad i huden (UV-erytem) som uppkommer på grund av att dosen överskrider den minsta erytemdosen samt en aktivering av herpes simplex-infektion på huden.
- Det finns ingen information om behandlingen ökar risken för hudcancer eller inte.
- På basis av teoretisk modellering kunde 450 behandlingar med smalbandig UVB-behandling fastställas som övre gräns för antalet behandlingar «Ibbotson SH, Bilsland D, Cox NH ym. An update and ...»144, «Diffey BL. Factors affecting the choice of a ceili...»145. Det finns dock ingen konsensus i frågan.
- Finlands Dermatologförenings ljussektion har utarbetat riktgivande dosscheman för finländska hudtyper (mer information om behandling av hudsjukdomar med smalbandig UVB «hoi50062a.pdf»4).
- Se patientanvisningen för smalbandig UVB-behandling på finska «https://hoito-ohjeet.fi/OhjepankkiVSSHP/Kapeakaista-UVB%20valohoito.pdf»7 och på svenska «https://hoito-ohjeet.fi/OhjepankkiVSSHPRuotsi/UV311.pdf»8.
- Kontraindikationer för UV-behandling är
- infekterat (bakterie- och virusinfektioner) eller mycket irriterat eksem
- ett akut tillstånd i eksemet ska lugnas först
- ljuskänslighet (relativ kontraindikation)
- tidigare hudcancer (relativ kontraindikation)
- användning av vissa läkemedel (ljussensibiliserare, immunsuppressiva läkemedel, kalcineurinhämmare) (relativ kontraindikation)
- ciklosporinbehandling.
- infekterat (bakterie- och virusinfektioner) eller mycket irriterat eksem
- Användningen av UV-behandlingar begränsas av
- hur bindande behandlingen är (typisk behandlingsfrekvens 2–3 gånger per vecka sammanlagt 15–20 gånger)
- tillgång till vård, resor till vård
- vårdkostnader.
- UVA1-behandling (våglängdsområde 340–400 nm) används inte i Finland för behandling av atopiskt eksem.
- Det finns inga tillförlitliga forskningsrön om långtidssäkerheten av UV-behandling för barn. UV-behandling för barn (smalbandig UVB eller SUP) används endast noga övervägt under övervakning av en specialist.
- Klimatbehandling (solljusbehandling, helioterapi) kan lindra atopiskt eksem och förbättra patienternas livskvalitet. Det finns ingen tillförlitlig evidens på den gynnsamma effektens varaktighet «Ilmastohoito saattaa lievittää atooppista ihottumaa ja parantaa potilaiden elämänlaatua. Suotuisan vaikutuksen kestosta ei ole luotettavaa näyttöä.»C. Klimatbehandling bekostas inte med offentliga medel.
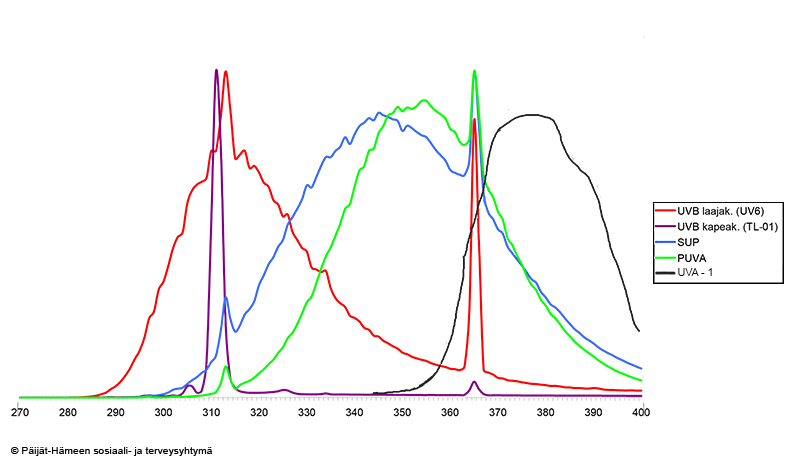
Eri valohoitolamppujen emittoiman UV-säteilyn aallonpituusspektrit
© Tapio Rantanen
Systemisk långvarig läkemedelsbehandling
- Målet med systemisk medicinering av atopiskt eksem är att få eksemet under kontroll långvarigt. Medicineringen inleds och följs upp av en specialist i hudsjukdomar eller barnsjukdomar. Läkemedel som används för långtidskontroll av eksem är traditionella immunsuppressiva läkemedel, biologiska läkemedel och JAK-hämmare. Inledandet av systemisk läkemedelsbehandling övervägs hos patienter med svårt atopiskt eksem som inte får tillräcklig respons med en väl genomförd lokalbehandling och eventuell UV-behandling.
- Av de traditionella immunsuppressiva läkemedlen är det endast ciklosporin som har atopiskt eksem som officiell indikation. Den officiella indikationen för abrocitinib, baricitinib, dupilumab, tralokinumab och upadacitinib är måttligt och svårt atopiskt eksem.
- Den systemiska läkemedelsbehandlingens respons och biverkningar ska följas upp regelbundet.
- Det rekommenderas att responsen bedöms första gången 12–16 veckor efter att behandlingen inletts och därefter regelbundet.
- Om responsen är bra konstateras i allmänhet en systematisk läkning både i patientens symtom och i eksemets objektiva svårighetsgrad.
- Systemiska läkemedel skiljer sig från varandra i fråga om effekt, biverkningar, kontraindikationer,
uppföljning som behandlingen kräver samt kostnader för individen och samhället. En
lämplig medicinering för patienten väljs individuellt.
- Även kriterierna för grundersättning av läkemedel påverkar ofta möjligheterna att genomföra läkemedelsbehandlingen i praktiken. Se de läkemedelsspecifika aktuella ersättningsvillkoren på FPA:s webbplats «https://www.kela.fi/samarbetspartner-lakemedelsersattningar-ersattningsrattigheter-for-lakemedel»9.
- Läkemedelskostnaderna för biologiska läkemedel och JAK-hämmare presenteras i tilläggsmaterialet «The number needed to treat (NNT) and cost per responder for systemic therapies for moderate-to-severe atopic dermatitis»21.
- Detta kapitel behandlar vuxna patienter. Systemisk läkemedelsbehandling av barn se punkten Särdrag i behandlingen av atopiskt eksem hos barn (0–16-åringar) «A3»5.
- I Reumahuset i Hälsobyn finns anvisningar för de flesta systemiska läkemedel som används
vid behandling av atopiskt eksem «https://www.terveyskyla.fi/sv/reumahuset/anvisningar-for-lakemedel-och-atgarder/anvisningar-for-antireumatiska-lakemedel»10. På webbplatsen finns anvisningar om bedömning av infektionskänslighet, vaccinationer
och uppföljningsprov «https://www.terveyskyla.fi/sv/reumahuset/anvisningar-for-lakemedel-och-atgarder/uppfoljningsprov-i-samband-med-antireumatiska-lakemedel»11. Se även det nationella vaccinationsprogrammet «https://thl.fi/sv/teman/infektionssjukdomar-och-vaccinationer/information-om-vaccinationer/det-nationella-vaccinationsprogrammet»12.
- Den föreskrivna uppföljningen med blodprov kan genomföras också inom primärvården.
- Innan systemiska läkemedel inleds uppdateras vid behov de vaccinationer som ingår
i det nationella vaccinationsprogrammet och immuniteten för vattkoppor och vid behov
mässling utreds.
- Säsongsinfluensavaccin rekommenderas för alla.
- Pneumokockvaccin rekommenderas för personer över 65 år och enligt läkarens övervägande även för andra.
- Bältrosvaccin kan övervägas särskilt för patienter över 50 år för vilka man planerar att inleda JAK-hämmare.
- Immunsuppressiv medicinering
- Munnen och tänderna ska hållas vid god hälsa under hela medicineringen.
- Uppehåll i medicineringen görs vid behov vid plötsliga infektioner och i samband med operationer.
- Regelbunden lokalbehandling av huden bör i allmänhet fortsätta parallellt med en systemisk läkemedelsbehandling.
Traditionella immunsuppressiva läkemedel
- Endast få dugliga kliniska prövningar har gjorts av immunsuppressiva läkemedel vid
behandling av atopiskt eksem.
- Bedömningen av vårdresponsen har varierat och patientantalet har varit litet.
- Mer forskningsevidens om läkemedlens effekt behövs.
- Ciklosporin
- Ciklosporin verkar lindra symtomen på behandlingsresistent atopiskt eksem vid kortvarig behandling «Siklosporiini saattaa vähentää aikuisten atooppisen ekseeman kliinisiä löydöksiä lyhytaikaisessa (6–8 viikkoa) hoidossa.»C.
- Man strävar efter att undvika långtidsbehandling (över 1–2 år) på grund av biverkningarna av ciklosporin.
- Ciklosporinbehandling ska inte kombineras med UV-behandling på grund av ökad risk för fotokarcinogenes «Sugie N, Fujii N, Danno K. Cyclosporin-A suppresse...»146.
- Doseringen av ciklosporin, kontraindikationer, biverkningar och uppföljningsprov presenteras i tabell 5 i God medicinsk praxis-rekommendationen Psoriasis och psoriasisartrit: Att beakta vid ciklosporinbehandling «Psoriasis och psoriasisartrit»4.
- Metotrexat
- Metotrexat kan vara effektivt vid behandling av atopiskt eksem även om forskningsrönen är få och det inte finns några placebokontrollerade studier «Metotreksaatti saattaa vähentää atooppisen ekseeman aktiivisuutta lyhytaikaisessa hoidossa yhtä paljon kuin atsatiopriini ja siklosporiini, mutta löydöksen kliinistä merkitystä on vaikea arvioida ilman lumevertailua.»C.
- Responsen uppnås långsamt, under flera veckor.
- Metotrexat lämpar sig för långtidsbehandling.
- Metotrexat är teratogent.
- Medicineringen kräver särskild noggrannhet på grund av den exceptionella doseringen.
- Metotrexat kan också doseras som subkutan injektion, varvid dess biotillgänglighet och tolererbarhet är bättre (mindre illamående).
- Doseringen av metotrexat, kontraindikationer, biverkningar och uppföljningsprov presenteras i tabell 4 i God medicinsk praxis-rekommendationen Psoriasis och psoriasisartrit: Att beakta vid metotrexatbehandling «Psoriasis och psoriasisartrit»4
- Azatioprin
- Azatioprin kan vara effektivt vid behandling av atopiskt eksem, men forskningsevidensen
är knapp «Atsatiopriini saattaa vähentää aikuisten atooppisen ekseeman aktiivisuutta lumelääkkeeseen verrattuna, mutta tehon kliinistä suuruutta on vaikea arvioida.»C
- I en liten RCT-studie var azatioprin och metotrexat lika effektiva vid behandling av atopiskt eksem «Schram ME, Roekevisch E, Leeflang MM ym. A randomi...»147.
- Azatioprin lämpar sig eventuellt för långtidsanvändning.
- Undersökning av polymorfier i tiopurinmetyltransferasen (TPMT) rekommenderas innan azatioprinbehandling inleds.
- De vanligaste biverkningarna i behandlingen är symtom i mag-tarmkanalen, förändringar i blodbilden och förhöjda levervärden.
- Mer information om behandling med azatioprin och uppföljningsprov finns i Reumahusets anvisningar i Hälsobyn «https://www.terveyskyla.fi/sv/reumahuset/anvisningar-for-lakemedel-och-atgarder/anvisningar-for-antireumatiska-lakemedel»10 och «https://www.terveyskyla.fi/sv/reumahuset/anvisningar-for-lakemedel-och-atgarder/uppfoljningsprov-i-samband-med-antireumatiska-lakemedel»11.
- Azatioprin kan vara effektivt vid behandling av atopiskt eksem, men forskningsevidensen
är knapp «Atsatiopriini saattaa vähentää aikuisten atooppisen ekseeman aktiivisuutta lumelääkkeeseen verrattuna, mutta tehon kliinistä suuruutta on vaikea arvioida.»C
- Mykofenolatmofetil
- Mykofenolatmofetil kan minska symtomen på atopiskt eksem, men tillförlitlig forskningsevidens saknas «Mykonefolaattimofetiili saattaa vähentää atooppisen ekseeman aktiivisuutta yhtä paljon kuin siklosporiini, mutta luotettava näyttö puuttuu ja kliinistä merkitystä on vaikea arvioida ilman lumevertailua.»D.
- I Finland finns det knapp erfarenhet av behandling av atopiskt eksem med mykofenolatmofetil.
- Mer information om behandling med mykofenolat och uppföljningsprov finns i Reumahusets anvisningar i Hälsobyn «https://www.terveyskyla.fi/sv/reumahuset/anvisningar-for-lakemedel-och-atgarder/anvisningar-for-antireumatiska-lakemedel»10 och «https://www.terveyskyla.fi/sv/reumahuset/anvisningar-for-lakemedel-och-atgarder/uppfoljningsprov-i-samband-med-antireumatiska-lakemedel»11.
Biologiska läkemedel
Dupilumab
- Dupilumab är en IL-4Rα-antikropp som förhindrar effekten av cytokin IL-4 och IL-13.
- Dupilumab minskar svårighetsgraden av atopiskt eksem.
- Vecka 16 uppnåddes EASI-75-respons utan samtidig användning av läkemedelssalvor med en dupilumabdos på 300 mg varannan vecka hos 48 procent av patienterna och med placebo hos 13 procent av patienterna «Dupilumab (initial dose of 600 mg followed by 300 mg every other week) alone or in combination with topical treatments compared to placebo increases the proportion of adults with moderate to severe atopic dermatitis reaching EASI-75 at week 16 when compared to placebo (48–66% vs. 13–25%).»A. Motsvarande siffror under samtidig användning av läkemedelssalva var 66 procent och 25 procent.
- Dupilumab minskar klådan i huden och förbättrar patienternas livskvalitet.
- I en placebokontrollerad studie verkade effekten av dupilumab bibehållas under ett års uppföljning «Blauvelt A, de Bruin-Weller M, Gooderham M ym. Lon...»148.
- Dupilumab verkar vara effektivt också hos barn och unga i åldern 6–17 år «In children (6-11 years) with severe atopic dermatitis dupilumab (100 mg every two weeks for children with weight of 15 to <30 kg and 200 mg every two weeks for children with weight of ≥30 kg) with topical corticosteroids appears to increase the proportion of patients reaching EASI-75 at week 16 when compared to placebo (67–70% vs. 27%).»B, «Simpson EL, Paller AS, Siegfried EC ym. Efficacy a...»149.
- Dupilumabs effekt har också påvisats vid svår astma typ 2 (se God medicinsk praxis-rekommendationen Astma «Astma»5), vid svår kronisk polypös rinosinuit samt vid prurigo nodularis «Husein-ElAhmed H, Steinhoff M. Dupilumab in prurig...»150.
- Dupilumabs effekt och säkerhet har undersökts i direkta jämförande studier där dupilumab
jämfördes med upadacitinib «Blauvelt A, Teixeira HD, Simpson EL ym. Efficacy a...»151 och abrocitinib «Reich K, Thyssen JP, Blauvelt A ym. Efficacy and s...»152, «Bieber T, Simpson EL, Silverberg JI ym. Abrocitini...»153.
- I en uppföljning på 16 veckor uppnådde en större del av patienterna EASI-75-respons
med upadacitinibdosen 30 mg/dygn än med en dupilumabdos på 300 mg varannan vecka (71
% vs. 61 %) «Blauvelt A, Teixeira HD, Simpson EL ym. Efficacy a...»151. Upadacitinib hade en snabbare effekt på klåda.
- Vecka 16 uppnådde 61 procent av patienterna EASI-90-respons med upadacitinib och 39 procent med dupilumab.
- Vecka 24 var andelen personer som uppnått EASI-75-respons 60 procent i dupilumabgruppen (95 % konfidensintervall 54–65) och 64 procent i upadacitinibgruppen (95 % konfidensintervall 59–69).
- När man jämförde abrocitinib med dosen 200 mg/dygn och dupilumab med dosen 300 mg
varannan vecka konstaterades att abrocitinib hade snabbare effekt mot klåda «Reich K, Thyssen JP, Blauvelt A ym. Efficacy and s...»152, «Bieber T, Simpson EL, Silverberg JI ym. Abrocitini...»153. Vecka 16 fanns det ingen statistiskt signifikant skillnad i EASI-75-responsen «Bieber T, Simpson EL, Silverberg JI ym. Abrocitini...»153.
- Vecka 16 uppnådde 54 procent EASI-90-respons med abrocitinib och 42 procent med dupilumab «Reich K, Thyssen JP, Blauvelt A ym. Efficacy and s...»152.
- Med dupilumab uppnås respons vanligtvis långsammare än med JAK-hämmare; responsen syns 1–2 månader efter att behandlingen inletts och förbättras ytterligare under flera månader.
- I en uppföljning på 16 veckor uppnådde en större del av patienterna EASI-75-respons
med upadacitinibdosen 30 mg/dygn än med en dupilumabdos på 300 mg varannan vecka (71
% vs. 61 %) «Blauvelt A, Teixeira HD, Simpson EL ym. Efficacy a...»151. Upadacitinib hade en snabbare effekt på klåda.
- I en uppföljning på ett år kan biverkningarna av dupilumab i huvudsak jämföras med placebo «Blauvelt A, de Bruin-Weller M, Gooderham M ym. Lon...»148, «Blauvelt A, Guttman-Yassky E, Paller AS ym. Long-T...»154. Den vanligaste biverkningen vid behandling med dupilumab är bindhinneinflammation i ögat, som i allmänhet är lindrig eller medelsvår «Siegels D, Heratizadeh A, Abraham S ym. Systemic t...»155. Vid behandlingen används vanligen fuktdroppar och -gel, mastcellsstabilisatorer i form av droppar samt antihistaminögondroppar. Om symtomen är svåra rekommenderas en ögonläkarkonsultation «Thyssen JP, Heegaard S, Ivert L ym. Management of ...»156.
- Dupilumab ökar inte den allmänna infektionskänsligheten och ingen laboratorieuppföljning behövs.
Tralokinumab
- Tralokinumab är en IL-13-antikropp. Det finns för närvarande inte att tillgå i Finland.
- Mer information «Tralokinumab in the treatment of adult atopic dermatitis»22.
JAK-hämmare
- JAK-hämmare är läkemedel i tablettform vars verkningsmekanism grundar sig på förhindrande av en intracellulär JAK-STAT-signaltransduktion, vilket leder till att effekten av flera cytokiner minskar. Mer information om JAK-hämmare «Janus-kinaasin estäjät (JAK-estäjät)»23.
- JAK-hämmarnas respons vid atopiskt eksem börjar snabbt, vanligtvis inom några veckor.
- JAK-hämmare verkar öka infektionsbenägenheten. Särskilt risken för herpes simplex-infektioner och bältros har varit förhöjd i studierna. Dessutom kan JAK-hämmare orsaka bland annat akneliknande eksem, illamående, förändringar i blodbilden och förhöjda fettvärden.
- JAK-hämmare har interaktioner som bör beaktas.
- Mer information om behandling med baricitinib och upadacitinib och uppföljningsblodprov
finns i Reumahusets anvisningar i Hälsobyn «https://www.terveyskyla.fi/sv/reumahuset/anvisningar-for-lakemedel-och-atgarder/anvisningar-for-antireumatiska-lakemedel»10 och «https://www.terveyskyla.fi/sv/reumahuset/anvisningar-for-lakemedel-och-atgarder/uppfoljningsprov-i-samband-med-antireumatiska-lakemedel»11.
- Med abrocitinib kan man följa liknande anvisningar för medicinering och blodprovsuppföljning som med baricitinib och upadacitinib.
- Hos patienter med ledgångsreumatism med vissa riskfaktorer har man observerat en ökad
risk för biverkningar vid behandling med JAK-hämmare jämfört med behandling med TNF-alfahämmare.
Se Fimea «https://fimea.fi/documents/147152901/159465460/AK+inhibitors+DHPC+Final-FI+2023-03-15.pdf/8481297f-801a-0bf7-9ca3-cb4a5cf096be/AK+inhibitors+DHPC+Final-FI+2023-03-15.pdf?t=1678882468734»13.
- Dessa biverkningar är betydande hjärt- och kärlhändelser, ventromboemboli, cancer, allvarliga infektioner och dödlighet.
- Enligt rekommendationen bör JAK-hämmare användas i följande patientgrupper endast om det inte finns andra lämpliga behandlingsalternativ: ≥ 65-åringar, numera rökare eller personer som rökt länge tidigare, patienter som har andra riskfaktorer för hjärt- eller kärlhändelser eller riskfaktorer i anslutning till cancer.
- Vid användning av JAK-hämmare ska försiktighet iakttas om patienten har andra än ovan nämnda riskfaktorer för ventromboemboli.
- Vid underhållsbehandling ska man överväga att använda den minsta effektiva dosen.
- Tills vidare finns det inga direkta jämförande studier om effekten och säkerheten hos olika JAK-hämmare vid behandling av atopiskt eksem.
Abrocitinib
- Abrocitinib minskar svårighetsgraden av atopiskt eksem.
- Vecka 12 uppnåddes EASI-75-respons utan samtidig användning av läkemedelssalvor med en dagsdos på 200 mg av 61–63 procent av patienterna och med placebo av 10–12 procent av patienterna «Abrocitinib in dose of 100 or 200 mg once daily alone or in combination with topical treatment increases the proportion of patients (age at least 12 years) with moderate-to-severe atopic dermatitis achieving EASI-75 response at week 12, when compared to placebo (100 mg: 40-58.7%, 200 mg: 61.»A. Motsvarande siffror under samtidig användning av läkemedelssalvor var 70 procent respektive 27 procent.
- Jämfört med placebo minskar abrocitinib uppenbarligen klådan och förbättrar patienternas livskvalitet.
- Direkt jämförelse mellan abrocitinib och dupilumab, se punkten Dupilumab «A6»8.
- I RCT-studier har illamående förekommit som en typisk biverkning av abrocitinib (i abrocitinibgruppen 15 % vs. placebogruppen 2 %) «Simpson EL, Silverberg JI, Nosbaum A ym. Integrate...»157.
Baricitinib
- Baricitinib verkar minska svårighetsgraden av atopiskt eksem.
- Vecka 16 uppnåddes EASI-75-respons utan samtidig användning av läkemedelssalvor med en dagsdos på 4 mg av 21–25 procent av patienterna och med placebo av 6–9 procent av patienterna «Baricitinib (2-4 mg/day) treatment alone or in combination with topical treatment appears to increase the proportion of adult patients with moderate-to-severe atopic dermatitis achieving EASI-75 response at week 16, when compared to placebo (2 mg: 18-43%, 4 mg: 21-48%, and placebo 6-23%).»B. Motsvarande siffror under samtidig användning av läkemedelssalva var 48 procent respektive 23 procent.
- Baricitinib kan minska klådan i huden och förbättra patienternas livskvalitet.
- I RCT-studier observerades biverkningar som är typiska för JAK-hämmare, se punkten JAK-hämmare «A11»9.
- Baricitinib är också indikerat för behandling av ledgångsreumatism och fläckvist håravfall.
Upadacitinib
- Upadacitinib minskar svårighetsgraden av atopiskt eksem.
- Vecka 16 uppnåddes EASI-75-respons utan samtidig användning av läkemedelssalvor med en dagsdos på 30 mg av 73–80 procent av patienterna och med placebo av 13–16 procent av patienterna «Oral upadacitinib at the dose of 15-30mg daily alone or in combination with topical treatment increases the proportion of adult patients with moderate-to-severe atopic dermatitis achieving EASI75 response at week 16, when compared to placebo (15 mg: 60.1-69.»A. Samtidig användning av läkemedelssalvor verkar inte öka antalet personer som fått behandlingsrespons.
- Upadacitinib minskar klådan i huden och förbättrar patienternas livskvalitet.
- I undergruppsanalyserna motsvarade resultaten för 12–17-åringar de vuxnas resultat «Guttman-Yassky E, Teixeira HD, Simpson EL ym. Once...»158.
- Direkt jämförelse mellan upadacitinib och dupilumab, se punkten Dupilumab «A6»8.
- I RCT-studier har som allmän biverkning av upadacitinib förekommit akneliknande eksem (med dosen 30 mg hos 15 % och med placebo hos 2 %) «Mendes-Bastos P, Ladizinski B, Guttman-Yassky E ym...»159.
- Upadacitinib har också indikation för ledgångsreumatism, psoriasisartrit, axial spondylartrit, ulcerös kolit och Crohns sjukdom.
| Läkemedel | Dupilumab | Abrocitinib | Baricitinib | Upadacitinib |
|---|---|---|---|---|
| EASI = Eczema Area and Severity Index, IL = interleukin, JAK = januskinas * I kliniska läkemedelsprövningar av atopiskt eksem är placebogruppernas respons relativt stor. I olika studier har 10–30 procent av patienterna uppnått EASI-75-respons i placebogruppen. I en del av studierna fick patienterna använda lokal läkemedelssalva. När patienten deltar i en klinisk läkemedelsprövning fäster man på ett övergripande sätt uppmärksamhet vid patientens tillstånd, vilket kan förbättra till exempel följsamheten för lokalbehandling (bassalva eller läkemedelssalva). ** Svar vecka 12. |
||||
| Typ | human monoklonal antikropp (IgG4) | JAK-hämmare | JAK-hämmare | JAK-hämmare |
| Effektmål | IL-4Rα | JAK 1 | JAK 1 JAK 2 |
JAK 1 |
| Dos | Startdos 600 mg, därefter 300 mg Med 2 veckors mellanrum s.c. |
Startdos 200 mg x 1, p.o. Fortsatt behandling enligt patientens individuella respons. För ≥ 65-åringar 100 mg x 1. |
Startdos 4 mg x 1, p.o. Fortsatt behandling enligt patientens individuella respons. 2 mg x 1 lämplig för ≥ 75-åringar. |
Startdos 15 mg eller 30 mg x 1, p.o. Fortsatt behandling enligt patientens individuella respons. För 12–17-åringar och ≥ 65-åringar 15 mg x 1. |
| Uppnådd EASI-75-respons* vecka 16 (% av patienterna), utan läkemedelssalva |
48 | 100 mg: 40–45** 200 mg: 61–63 ** |
2 mg: 18–19 4 mg: 21–25 |
15 mg: 60–70 30 mg: 73–80 |
| placebo: 13 |
placebo: 10–12** |
placebo: 6–9 |
placebo: 13–16 |
|
| Uppnådd EASI-75-respons* vecka 16 (% av patienterna), med läkemedelssalva |
66 | 100 mg: 59** 200 mg: 70** |
2 mg: 43 4 mg: 48 |
15 mg: 65 30 mg: 77 |
| placebo: 25 |
placebo: 27** |
placebo: 23 |
placebo: 26 |
|
| Uppnådd EASI-90-respons* vecka 16 (% av patienterna), utan läkemedelssalva |
30–36 | 100 mg: 19–24** 200 mg: 38–39** |
2 mg: 9–11 4 mg: 13–16 |
15 mg: 42–53 30 mg: 59–66 |
| placebo: 7–8 |
placebo: 4–5** |
placebo: 2,5–5 |
placebo: 5–8 |
|
Annan systemisk läkemedelsbehandling
Invärtes antibiotika
- Effektiv behandling av atopiskt eksem, dvs. korrigering av hudens skyddsbarriär och dämpning av inflammationen, minskar förekomsten av hudinfektioner «Wang V, Boguniewicz J, Boguniewicz M ym. The infec...»65.
- Invärtes antibiotika används inte vid behandling av icke infekterat atopiskt eksem
«Bath-Hextall FJ, Birnie AJ, Ravenscroft JC ym. Int...»160, «Sidbury R, Davis DM, Cohen DE ym. Guidelines of ca...»161. Se Avstå klokt-rekommendationen «Paikalliset antimikrobiset aineet ja sisäiset antibiootit atooppisen ekseeman hoidossa»24. Lokala antimikrobiella medel och invärtes antibiotika rekommenderas inte för behandling
av icke infekterat atopiskt eksem.
- Invärtes antibiotikabehandling av icke infekterat atopiskt eksem påverkar inte de kliniska symtomen, även om stafylokockhalten i huden minskar tillfälligt under antibiotikabehandlingen «Boguniewicz M, Sampson H, Leung SB ym. Effects of ...»162, «Ewing CI, Ashcroft C, Gibbs AC ym. Flucloxacillin ...»163.
- Stafylokockhalten återställs snabbt efter läkemedelsbehandlingen «Boguniewicz M, Sampson H, Leung SB ym. Effects of ...»162, «Ewing CI, Ashcroft C, Gibbs AC ym. Flucloxacillin ...»163, «Lübbe J. Secondary infections in patients with ato...»140.
- En stor del av patienterna med atopiskt eksem har Staphylococcus aureus-bakterier både på eksemområden och på hud som ser frisk ut, så beslut om eventuell antibiotikabehandling ska inte fattas enbart utifrån en bakterieodling av huden.
- Brister i skyddsbarriärens funktion i atopisk hud ökar dock risken för en sekundär infektion av huden.
- Antibiotikabehandling är motiverad endast om det utvecklas en sekundär infektion i eksemet. Den primära antibiotikabehandlingen av infekterat eksem är flukloxacillin eller första generationens cefalosporin. Se God medicinsk praxis-rekommendationen Hudinfektioner «Hudinfektioner»3.
- Sedvanliga lokalbehandlingen fortsätter vid sidan om antibiotikabehandlingen vid infekterat atopiskt eksem.
- Det är bra att lära patienterna att identifiera symtom och fynd på infekterat eksem (varigt sekret i eksemområdet, varblåsor, sårskorpor, atopiskt eksem som förvärras snabbt, feber och sjukdomskänsla).
- Se även kapitlet Lokala antimikrobiella medel «A7»10 i denna rekommendation.
Antihistaminer
- Använd inte antihistaminer utan särskilda skäl för behandling av klåda orsakad av
atopiskt eksem. Se Avstå klokt-rekommendationen «Antihistamiinit atooppisen ekseeman aiheuttaman kutinan hoidossa»25. Använd inte antihistaminer utan särskilda skäl för behandling av klåda orsakad av
atopiskt eksem. En effektiv behandling av eksemet lindrar bäst klådan vid atopiskt
eksem.
- Betydande transmittorer vid klåda på grund av atopiskt eksem är flera inflammationscytokiner «Atooppisen ekseeman patogeneesi pääpiirteissään»2. Histamin har liten betydelse.
- Icke-sederande antihistaminer har sannolikt ingen effekt på klådan vid atopiskt eksem «Antihistamiineilla paikallishoidon lisänä ei liene vaikutusta atooppisen ekseeman kutinaan.»C.
- Effekten av sederande antihistaminer på klådan grundar sig på deras sedativa effekt och inte på antihistamineffekten «Klein PA, Clark RA. An evidence-based review of th...»164.
Invärtes kortikosteroider
- På grund av systembiverkningar rekommenderas inte användning av invärtes kortikosteroider.
- Vid akut försämringsskov av svårt atopiskt eksem kan kortvariga invärtes kortikosteroidkurer
användas selektivt «Hoare C, Li Wan Po A, Williams H. Systematic revie...»103. Då ska man alltid se till att den samtidiga lokalbehandlingen är tillräckligt effektiv.
- Invärtes kortikosteroider har snabb men tillfällig effekt. Det finns dock inga placebokontrollerade kliniska prövningar om användningen av dem vid behandling av atopiskt eksem.
- Behovet av återkommande invärtes kortikosteroidkurer är ett tecken på en otillräcklig
terapeutisk balans för eksemet.
- En adekvat behandling med läkemedelssalva ska säkerställas och vid behov effektivera lokalbehandlingen.
- Vid behov ska patienten remitteras till en specialist för bedömning av inledning av systemisk långvarig läkemedelsbehandling.
- Mer information om användningen av invärtes kortikosteroider vid behandling av atopiskt eksem «Lisätietoa sisäisten kortikosteroidien käytöstä atooppisen ekseeman hoidossa»26.
Icke etablerade och alternativa behandlingar
- D-vitaminets roll i atopiskt eksem är föremål för forskning. Det behövs dock ytterligare
studier för att påvisa orsakssammanhanget mellan D-vitaminets effekter i patogenesen
av atopiskt eksem och en eventuell nytta av D-vitamintillskott vid behandling av atopiskt
eksem «Ng JC, Yew YW. Effect of Vitamin D Serum Levels an...»165. Atopiskt eksem i sig kan åtminstone tills vidare inte rekommenderas som indikation
för D-vitamintillskott «Vestita M, Filoni A, Congedo M ym. Vitamin D and a...»166, «Ong PY, Boguniewicz M. Investigational and unprove...»167.
- D-vitamin påverkar den naturliga och adaptiva immuniteten, bildandet av antimikrobiella peptider i huden samt differentieringen och tillväxten av hudceller.
- Kalcidiolhalten i blodet (25(OH)D) är betydligt lägre hos personer med atopiskt eksem än hos kontrollpersoner med frisk hud. Hos personer med svårt eksem är kalcidiolhalten lägre än hos personer med lindrigt eller måttligt eksem «Ng JC, Yew YW. Effect of Vitamin D Serum Levels an...»165.
- Patienter med en hudsjukdom använder ofta icke etablerade och alternativa behandlingar.
Den livslånga prevalensen i användningen har i olika studier varit 35–69 procent
«Ernst E, Pittler MH, Stevinson C. Complementary/al...»168, «Kim GW, Park JM, Chin HW ym. Comparative analysis ...»169.
- Av patienter med atopiskt eksem som remitterats till en universitetsklinik använde 50 procent av patienterna också alternativa behandlingar för sitt eksem «Simpson EL, Basco M, Hanifin J. A cross-sectional ...»170. I Irland hade 42,5 procent av barn med atopiskt eksem som remitterats till en klinik för hudsjukdomar genomgått alternativa behandlingar «Hughes R, Ward D, Tobin AM ym. The use of alternat...»171.
- De vanligaste alternativa behandlingarna är kinesiska örtpreparat, kosttillskott med essentiella fettsyror, homeopati och akupunktur.
- Missnöje med vanliga behandlingar och frustration med det atopiska eksemets kroniska natur leder till att patienterna prövar alternativa behandlingar.
- Det är bra att inkludera frågan om icke etablerade och alternativa behandlingar i anamnesen, eftersom patienter eller föräldrar till barnpatienter sällan spontant berättar om dessa behandlingar.
- I studier som utreder effekten av kinesiska örtpreparat är risken för missbedömningar stor, särskilt i fråga om blindning. I studier har man inte tydligt kunnat påvisa att kinesiska örtpreparat vid lokal eller systemisk användning skulle vara effektiva vid behandling av atopiskt eksem «Gu S, Yang AW, Xue CC ym. Chinese herbal medicine ...»172, «Tan HY, Zhang AL, Chen D ym. Chinese herbal medici...»173, «Gu S, Yang AW, Li CG ym. Topical application of Ch...»174. Kinesiska läkemedelsörter har beskrivits ha flera biverkningar och en del av dem är allvarliga (dilaterande kardiomyopati, levertoxicitet) «Hoare C, Li Wan Po A, Williams H. Systematic revie...»103, «Sheehan MP, Atherton DJ. One-year follow up of chi...»175.
- Betydande mängder potenta kortikosteroider har hittats i alternativa lokalbehandlingspreparat «Boneberger S, Rupec RA, Ruzicka T. Complementary t...»176.
- Essentiella fettsyror har inte konstaterats ha effekt på atopiskt eksem «Välttämättömillä rasvahapoilla ei ole tehoa atooppisen ekseeman hoidossa.»A, «Hoare C, Li Wan Po A, Williams H. Systematic revie...»103, «Bath-Hextall F, Williams H. Atopic eczema. Clin Ev...»177.
- Det finns ingen evidens på effekten av homeopati vid behandling av atopiskt eksem «Boneberger S, Rupec RA, Ruzicka T. Complementary t...»176, «Torley D, Futamura M, Williams HC ym. What's new i...»178.
- Utifrån metaanalyser kan akupunktur inte rekommenderas som behandling av atopiskt eksem «Jiao R, Yang Z, Wang Y ym. The effectiveness and s...»179.
- Mer information om icke etablerade behandlingar, se «Vakiintumattomat ja vaihtoehtoiset hoidot»27.
Atopiskt eksem i händerna
- En typisk plats för atopiskt eksem är händerna. Det är viktigt att ingripa i handeksemet
i ett tidigt skede innan eksemet blir kroniskt.
- En torr atopisk hud irriteras lätt av bland annat fukt och kontakt med tvålar, födoämnen, vatten, smuts och damm.
- Det är viktigt att skydda händerna mot fukt och irriterande faktorer om det har förekommit eksem i händerna (se anvisningar «https://www.terveyskyla.fi/sv/hudsjukdomshuset/hudsjukdomar/handeksem»14).
- Grunden för behandlingen av atopiskt handeksem är regelbunden smörjning med bassalva
vid behov flera gånger per dag och periodisk lokalbehandling med kortikosteroider
«Thyssen JP, Schuttelaar MLA, Alfonso JH ym. Guidel...»180.
- Vid behandling av handeksem behövs ofta starka kortikosteroidsalvor i grupp III och ibland mycket starka kortikosteroidsalvor i grupp IV. Kurerna är längre än på andra hudområden, vanligtvis 2–4 veckor. Kuren kan vid behov fortsättas fram till 6 veckor.
- När eksemet har läkt behövs ofta underhållsbehandling med stark kortikosteroidsalva två gånger i veckan för att förebygga återfall.
- Biverkningarna av kortikosteroidsalvor är desamma som i andra hudområden.
- Vid eksem i handflatorna har kalcineurinhämmare en sämre effekt på grund av hudens tjocklek.
- Bassalva rekommenderas istället för tvål för salvatvätt av händerna. Se Hudsjukdomshusets anvisning «https://www.terveyskyla.fi/ihotautitalo/Documents/Voidepesu_potilasohje.pdf»15.
- Handeksemet ska beaktas vid yrkesval (se avsnittet Yrkesval «A8»11).
Behandling under graviditet och amning
- Atopiskt eksem är den vanligaste hudsjukdomen under graviditeten «Koutroulis I, Papoutsis J, Kroumpouzos G. Atopic d...»181.
- Hos cirka 20 procent av dem som lider av atopiskt eksem lindras eksemet under graviditeten, men hos andra förblir eksemet oförändrat eller så försvåras det «Balakirski G, Novak N. Atopic dermatitis and pregn...»182. Försämring av atopiskt eksem under graviditeten kan förklaras av immunologiska faktorer, såsom förstärkning av Th2-responsen, samt av ökad fysisk och psykisk stress orsakad av graviditeten. Det är också vanligt att undvika aktiva behandlingar, vilket kan leda till underbehandling av den gravida mammans eksem «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183, «Weatherhead S, Robson SC, Reynolds NJ. Eczema in p...»184.
- Under graviditeten kan man utöver bassalvor fortsätta använda milda, medelstarka och
starka lokala kortikosteroider på normalt sätt «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183.
- Patienten hänvisas till den specialiserade sjukvården om medelstarka eller starka kortikosteroidsalvor inte är tillräckligt effektiva eller patienten använder dem över 200 g per månad.
- Det finns inget hinder för lokal användning av takrolimus eller pimekrolimus under graviditeten. Användningen ska begränsas endast till hudområden som kräver behandling och behandlingstiden ska vara den kortast möjliga som är tillräcklig. Vid lokal användning är absorptionen mycket liten, men kan öka om huden är sårig. Begränsad lokalbehandling förväntas inte medföra sådan exponering som påverkar fostrets utveckling «Malm H. Teratologinen palvelu. Henkilökohtainen ti...»185.
- Användning av kortikosteroidsalvor eller lokala kalcineurinhämmare är inget hinder för amning. Om behandlingen behövs i bröstområdet ska särskild försiktighet iakttas så att spädbarnet inte kommer i direkt kontakt med läkemedelssalvan. I praktiken ska salvan appliceras på bröstvårtan eller vårtgården genast efter amningen och man ska se till att bröstvårtan rengörs varsamt men noggrant före amningen «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183, «Weatherhead S, Robson SC, Reynolds NJ. Eczema in p...»184.
- Under graviditeten kan smalbandig UVB-behandling eller SUP-behandling användas «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183, «Weatherhead S, Robson SC, Reynolds NJ. Eczema in p...»184.
- Atopiskt eksem som kräver systemisk medicinering behandlas alltid inom den specialiserade
sjukvården.
- På grund av systembiverkningar rekommenderas inte användning av invärtes kortikosteroider vid atopiskt eksem, men i undantagsfall kan prednisolon användas för gravida. Då bör man använda högst 0,5 mg/kg/dygn som en så kort kur som möjligt (vanligen mindre än 2–3 veckor) «Vestergaard C, Wollenberg A, Barbarot S ym. Europe...»183, «Weatherhead S, Robson SC, Reynolds NJ. Eczema in p...»184.
- Ciklosporin kan med eftertanke och noggrann uppföljning användas vid svårt eksem under graviditet och amning.
- Fortsatt azatioprinbehandling kan övervägas under graviditeten «Mahadevan U, Long MD, Kane SV ym. Pregnancy and Ne...»186. Amning rekommenderas att undvikas i fyra timmar efter att läkemedlet tagits «Bar-Gil Shitrit A, Grisaru-Granovsky S, Ben Ya'aco...»187.
- Dupilumab rekommenderas inte under graviditet eller amning på grund av knappa forskningsrön.
- Användningen av metotrexat, mykofenolatmofetil och JAK-hämmare är kontraindicerat under graviditet eller amning. Kvinnor ska pausa metotrexat i 3 månader, mykofenolatmofetil i 6 veckor och JAK-hämmare 2–4 veckor före graviditeten «Russell MD, Dey M, Flint J ym. British Society for...»188.
- Män behöver inte pausa metotrexat, ciklosporin, azatioprin, biologiska läkemedel eller JAK-hämmare som används med doser för atopiskt eksem när familjetillökning planeras «https://www.terveyskyla.fi/sv/reumahuset/anvisningar-for-lakemedel-och-atgarder/antireumatisk-lakemedelsbehandling-under-graviditet-och-amning»16.
| Vård | Graviditet | Tilläggsinformation | Amning | Tilläggsinformation |
|---|---|---|---|---|
| Män behöver inte pausa systemläkemedel (som används med doser för atopiskt eksem) vid planering av familjeökning. | ||||
| Bassalvor | Tillåtet | Tillåtet | ||
| Kortikosteroidsalvor | Tillåtet | Tillåtet | ||
| Kalcineurinhämmare | Tillåtet | Tillåtet | ||
| Smalbandig UVB-behandling och SUP-behandling | Tillåtet | Tillåtet | ||
| Systemiska läkemedel: | ||||
| Systemiska kortikosteroider | Tillåtet | Minsta möjliga dos | Tillåtet | |
| Azatioprin | Tillåtet | Tillåtet med begränsningar | Amning tidigast 4 timmar efter intag av läkemedlet | |
| Ciklosporin | Tillåtet | Tillåtet | ||
| Metotrexat | Förbjudet | Teratogen, karenstid 3 mån. | Förbjudet | |
| Mykofenolatmofetil | Förbjudet | Teratogen, karenstid 6 veckor | Förbjudet | |
| Dupilumab | Rekommenderas inte | Ännu inte tillräckligt med forskningsdata | Rekommenderas inte | |
| JAK-hämmare | Förbjudet | Läkemedelsspecifik karenstid 2–4 veckor | Förbjudet | |
Särdrag i behandlingen av atopiskt eksem hos barn (0–16-åringar)
- Målet med behandlingen av atopiskt eksem hos barn är långvarig symtomkontroll: att minimera symtomen, minska antalet skov och lindra svårighetsgraden samt förbättra patientens livskvalitet och funktionsförmåga.
- En bra introduktion av föräldrarna i orsakerna till atopiskt eksem, genomgång av behandlingarnas effekt och biverkningar, styrning av vården och bedömning av prognosen är väsentliga för att behandlingen ska lyckas. Barnen ska tas med i handledningssamtalen enligt sin åldersnivå. En grundlig handledning av sjukskötaren har konstaterats förbättra behandlingsresultatet och öka användningen av salvor «Cork MJ, Britton J, Butler L ym. Comparison of par...»99, «García-Soto L, Martín-Masot R, Espadafor-López B y...»189.
- Som bilaga till rekommendationen finns ett kort tilläggsmaterial för föräldrar, anvisningar för egenvård och en video om smörjning av huden för läkare, skötare och föräldrar «Ohje vanhemmille atooppisesta ekseemasta»1, (Handledd egenvård av atopiskt eksem hos barn «hoi50077d.pdf»2, videor «Atooppinen ekseema -suosituksen videot (lapset)»3).
- Regelbunden smörjning med bassalva 1–2 gånger per dag och periodisk behandling med
lokal kortikosteroidsalva är den primära behandlingen av atopiskt eksem hos barn.
- Hos barn används vanligtvis milda eller medelstarka kortikosteroidsalvor. Starka kortikosteroidsalvor används endast i specialfall på ordination av en specialist.
- Forskningsresultaten betonar vikten av lokalbehandling av atopiskt eksem «Miyaji Y, Yang L, Yamamoto-Hanada K ym. Earlier ag...»190, «Kelleher MM, Dunn-Galvin A, Gray C ym. Skin barrie...»191. Studier visar att atopiskt eksem i spädbarnsåldern och nötprotein i hushållsdamm ökar risken för nötallergi i skolåldern «Brough HA, Simpson A, Makinson K ym. Peanut allerg...»192. En möjlig förklaring är att spädbarn blir överkänsliga för nötter via sårig hud.
- Underhållsbehandling som förebygger återfall av atopiskt eksem med kalcineurinhämmare, särskilt takrolimus, vid måttligt eller svårt atopiskt eksem hos barn, där man inte har fått tillräcklig respons med kortikosteroidsalvor, har visat sig vara en effektiv och säker behandlingsform som minskar försämringsskov «Ylläpitohoito takrolimuusivoiteella 2–3 kertaa viikossa alueille, joissa ihottumaa yleensä on esiintynyt, vähentää merkittävästi pahenemisvaiheita ja kortikosteroidivoiteiden käyttöä perusvoiteisiin verrattuna.»A.
Lokala kortikosteroider
- När eksem uppkommer används lokala kortikosteroider i kurer. Se tabell «Arbetsgruppens rekommendation, baserad på erfarenhet och klinisk användning, om effektivitetsklassen
på den kortikosteroidsalva som används hos barn i olika åldrar och på olika hudområden.
...»4.
- I en studie konstaterades användningen av mild och medelstark kortikosteroidsalva i kurer på 3–5 dygn för 1–3-åringar med måttligt eller svårt atopiskt eksem vara effektiv och säker «Salava A, Perälä M, Pelkonen A ym. Safety of tacro...»193, «Perälä M, Salava A, Malmberg P ym. Topical tacroli...»194.
- I den europeiska vårdrekommendationen ges möjlighet till underhållsbehandling med kortikosteroidsalvor i alla styrkor. Bevis på effekten av milda eller medelstarka kortikosteroidsalvor vid underhållsbehandling finns inte hos patienter i någon ålder «Wollenberg A, Kinberger M, Arents B ym. EuroGuiDer...»101.
- Forskningsevidens om underhållsbehandling med stark kortikosteroidsalva som används två gånger i veckan har erhållits i viss mån «Hanifin J, Gupta AK, Rajagopalan R. Intermittent d...»108, «Thomas KS, Armstrong S, Avery A ym. Randomised con...»195, «Ylläpitohoito 2 kertaa viikossa vahvalla paikalliskortikosteroidilla näyttää ehkäisevän atooppisen ekseeman relapsia.»B. Behandlingen lämpar sig endast för bålen och extremiteterna.
- Vid behandling av barn under 1 år används 1-procentig hydrokortisonkräm 1–2 gånger
per dygn i perioder på 3–7 dygn «Akdis CA, Akdis M, Bieber T ym. Diagnosis and trea...»58, varefter man gör ett uppehåll för att minimera biverkningarna.
- Behandlingen kan inledas med smörjning med hydrokortisonkräm två gånger per dag. Även om det ännu inte finns forskningsdata om doseringen av salva till små barn en gång per dag, räcker det enligt klinisk erfarenhet med smörjning en gång per dag i lindrigare eksem.
- Behandlingen kan effektiveras genom att lokalt använda förband, ocklusion eller fuktiga omslag «Devillers AC, Oranje AP. Efficacy and safety of 'w...»196, «Nicol NH, Boguniewicz M, Strand M ym. Wet wrap the...»197. Se också avsnittet Förband och omslag «A9»12.
- Vid behandling av 1–7-åringar kan man använda mild eller medelstark kortikosteroidsalva
en gång per dygn i perioder på 3–7 dygn (se tabell «Arbetsgruppens rekommendation, baserad på erfarenhet och klinisk användning, om effektivitetsklassen
på den kortikosteroidsalva som används hos barn i olika åldrar och på olika hudområden.
...»4). Hos skolelever kan behandlingsperioden vid behov vara 1–2 veckor «Ainley-Walker PF, Patel L, David TJ. Side to side ...»198. Behandlingspausen är minst lika lång som behandlingsperioden.
- Behandlingen kan effektiveras genom att lokalt använda förband, ocklusion eller fuktiga omslag «Devillers AC, Oranje AP. Efficacy and safety of 'w...»196, «Nicol NH, Boguniewicz M, Strand M ym. Wet wrap the...»197.
- En stark kortikosteroidsalva används endast enligt en specialistläkares anvisningar.
- Särskilt om man använder starka kortikosteroidsalvor för tunna hudområden under långa tider (över 2 veckor), ökar risken för lokala (hudens atrofi) och även systemiska biverkningar (suppression av hypotalamus-hypofys-binjurebarkaxeln) hos barn «Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106, «Davallow Ghajar L, Wood Heickman LK, Conaway M ym....»199. Hos barn med omfattande eksem har man även med milda kortikosteroidsalvor konstaterat kortvarig systemisk absorption av kortikosteroiden i inledningen av behandlingen «Davallow Ghajar L, Wood Heickman LK, Conaway M ym....»199, «Axon E, Chalmers JR, Santer M ym. Safety of topica...»118.
| Salvans effektivitetsklass | ||||
|---|---|---|---|---|
| * Vid behandling av periokulärt eksem är kalcineurinhämmare primära. Plustecknen beskriver styrkan i arbetsgruppens rekommendation. – = rekommenderas inte |
||||
| Patientens ålder (år) | I | II | III | IV |
| Under 1 | +++ | - | - | - |
| 1–6 | +++ | ++ | - | - |
| 7–16 | +++ | ++ | + | - |
| Hudområde | ||||
| Ansikte, hals* | +++ | - | - | - |
| Bål, extremiteter | +++ | ++ | - | - |
| Handflator, fotsulor | + | +++ | + | - |
| Armhålor, ljumskområdet | +++ | + | - | - |
| Hårbotten | ++ | + | - | - |
Lokala kalcineurinhämmare
- Om lokala kortikosteroidsalvor inte ger tillräcklig respons används takrolimussalva vid behandling av barn över 2 år eller pimekrolimusemulsionskräm vid behandling av barn över 3 månader tunt på eksemområdena två gånger per dag tills eksemet har läkt. Se videon om kalcineurinhämmare vid lokalbehandling av atopiskt eksem «Kalsineuriinin estäjät atooppisen ekseeman paikallishoidossa (video) (kesto 1:41)»28.
- Kalcineurinhämmare är effektiva och säkra vid behandling av atopiskt eksem hos barn.
- Indikationen för pimekrolimusemulsionskräm hos barn över 3 månader är lindrigt eller måttligt atopiskt eksem.
- Indikationen för 0,03-procentig takrolimus hos 2–15-åringar är måttligt eller svårt atopiskt eksem. En starkare (0,1-procentig) takrolimussalva används enligt specialistläkarens övervägande «Reitamo S, Rustin M, Harper J ym. A 4-year follow-...»200, «Wahn U, Bos JD, Goodfield M ym. Efficacy and safet...»201.
- Effekten av kalcineurinhämmare hos barn har påvisats.
- 1-procentig pimekrolimusemulsionskräm är effektivare än bassalva vid både kort och långvarig (12 mån) behandling av lindrigt eller måttligt atopiskt eksem hos barn. Den är effektiv och säker även för behandling av eksem i ansiktet och för spädbarn «1-prosenttinen pimekrolimuusiemulsiovoide on tehokkaampi kuin perusvoide lasten atooppisen ekseeman hoidossa. Se on tehokas ja turvallinen myös imeväisillä ja kasvojen alueen ihottuman hoidossa ja vähentää kortikosteroidivoiteen tarvetta.»A.
- En 1-procentig pimekrolimusemulsionskräm vid lindrigt och måttligt atopiskt eksem minskar användningen av kortikosteroider «Wahn U, Bos JD, Goodfield M ym. Efficacy and safet...»201.
- 0,03- och 0,1-procentig takrolimussalva är effektivare än hydrokortisonkräm vid behandling av måttligt eller svårt atopiskt eksem hos barn och lika effektiva som medelstark kortikosteroidsalva «0,03-prosenttinen ja 0,1-prosenttinen takrolimuusivoide ovat tehokkaampia kuin sekä perusvoide että hydrokortisonivoide lasten keskivaikean tai vaikean atooppisen ekseeman hoidossa. 0,03-prosenttinen takrolimuusivoide on yhtä tehokas kuin 0,005-prosenttinen flutikasonivoide lasten keskivaikean tai vaikean atooppisen ekseeman hoidossa.»A.
- Pimekrolimusemulsionskräm används i eksemområdena två gånger per dygn tills symtomen försvinner. Det kan ta flera veckor. När eksemet återkommer ska behandlingen inledas på nytt genast när de första symtomen framträder «Sigurgeirsson B, Ho V, Ferrándiz C ym. Effectivene...»202.
- Takrolimussalva används i eksemområdena 1–2 gånger per dag tills eksemet har läkt. Om eksemet återkommer inleds behandlingen på nytt.
- Om eksemet återkommer ofta kan man efter den dagliga behandlingen med takrolimussalva
fortsätta med underhållsbehandling tills eksemet har läkt helt eller nästan helt.
Vid underhållsbehandling används takrolimussalva två gånger i veckan en gång per dag
under högst 12 månader på områden där eksem vanligtvis förekommer. Därefter ska läkaren
bedöma patientens tillstånd och besluta om underhållsbehandlingen ska fortsätta. Om
eksemet förvärras under underhållsbehandlingen används salvan igen två gånger per
dag «Schmitt J, von Kobyletzki L, Svensson A ym. Effica...»203.
- Underhållsbehandling med takrolimussalva 2–3 gånger i veckan i områden där eksem i allmänhet har förekommit minskar betydligt försämringsskoven och användningen av kortikosteroidsalvor jämfört med bassalvor «Ylläpitohoito takrolimuusivoiteella 2–3 kertaa viikossa alueille, joissa ihottumaa yleensä on esiintynyt, vähentää merkittävästi pahenemisvaiheita ja kortikosteroidivoiteiden käyttöä perusvoiteisiin verrattuna.»A.
- Om effekten av pimekrolimusemulsionskrämen inte är tillräcklig, övergår man i försämringsskovet till att använda mild eller medelstark kortikosteroidsalva som en kort kur och när huden lugnat sig återgår man till enbart kalcineurinhämmaren «Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106.
- Takrolimussalva används vanligen som enda läkemedelssalva. Om effekten inte är tillräcklig
vid användning ensam kan man vid ett försämringsskov övergå till att använda medelstark
kortikosteroidsalva och när huden lugnat sig återgå till enbart kalcineurinhämmaren
«Eichenfield LF, Tom WL, Berger TG ym. Guidelines o...»106.
- En behandlingsperiod med kortikosteroidsalva som föregår lokalbehandlingen med takrolimus och som lindrar de kraftigaste symtomen kan öka behandlingsföljsamheten.
- Bassalvor kan störa absorptionen av kalcineurinhämmare, så bassalvan och läkemedelssalvan appliceras inte samtidigt på samma hudområde. Det är bra att ta en paus mellan användningen av salvor så att den salva som först applicerats hinner absorberas. Se anvisningen för egenvård Handledd egenvård av atopiskt eksem hos barn «hoi50077d.pdf»2.
- Takrolimussalva och pimekrolimusemulsionskräm kombineras inte med UV-behandlingar.
- En vanlig biverkning av kalcineurinhämmare är hetta i de behandlade hudområdena. Den är som kraftigast under de första behandlingsgångerna och minskar och försvinner oftast när behandlingen fortsätter. Det är viktigt att berätta detta för patienten eller patientens föräldrar innan behandlingen inleds.
- Kalcineurinhämmare orsakar inte hudatrofi «Reitamo S, Rissanen J, Remitz A ym. Tacrolimus oin...»122.
- Det finns inga tydliga bevis på att behandlingen med kalcineurinhämmare skulle öka antalet hudinflammationer orsakade av herpes simplex eller mollusker hos barn «Paul C, Cork M, Rossi AB ym. Safety and tolerabili...»204, «Kapp A, Papp K, Bingham A ym. Long-term management...»205, «Koo JY, Fleischer AB Jr, Abramovits W ym. Tacrolim...»206.
- Det har inte påvisats att barn har haft systemiska biverkningar eller betydande systemisk absorption i samband med användning av kalcineurinhämmare «Staab D, Pariser D, Gottlieb AB ym. Low systemic a...»207, «Alaiti S, Kang S, Fiedler VC ym. Tacrolimus (FK506...»208, «Remitz A, Harper J, Rustin M ym. Long-term safety ...»209, «Salava A, Perälä M, Pelkonen A ym. Safety of tacro...»193.
- Behandling med pimekrolimus och takrolimus har inte konstaterats påverka vaccinresponsen «Stiehm ER, Roberts RL, Kaplan MS ym. Pneumococcal ...»210, «Papp KA, Breuer K, Meurer M ym. Long-term treatmen...»211.
- Kalcineurinhämmare är begränsat grundersättningsgilla. Se «https://www.kela.fi/lakemedel317»6.
Systemiska långtidsläkemedel
- När barnets svåra atopiska eksem inte reagerar på adekvat genomförd lokalbehandling ska patienten remitteras till en specialist för bedömning. Inledandet av systemisk läkemedelsbehandling övervägs hos barn med svårt atopiskt eksem hos vilka man inte får tillräcklig respons med en väl genomförd lokalbehandling och eventuell UV-behandling. Möjliga läkemedel är traditionella immunsuppressiva läkemedel, biologiska läkemedel och JAK-hämmare (se punkten Systemisk långvarig läkemedelsbehandling (vuxna) «A10»13).
- Aktuella ersättningar för systemiska läkemedel, se FPA:s webbplats «https://www.kela.fi/samarbetspartner-lakemedelsersattningar-ersattningsrattigheter-for-lakemedel»9.
- Metotrexat och ciklosporin
- Det finns ingen tillförlitlig placebokontrollerad forskningsevidens på effekten av ciklosporin och metotrexat vid behandling av svårt atopiskt eksem hos barn.
- I ett litet material var metotrexat lika effektivt som ciklosporin vid behandling av svårt atopiskt eksem hos barn. Se också «Siklosporiini lasten atooppisen ekseeman hoidossa»29.
- Biverkningarna begränsar långtidsanvändningen av ciklosporin.
- Dupilumab
- Dupilumab verkar vara effektivt hos barn och unga i åldern 6–17 år som lider av måttligt
eller svårt atopiskt eksem. I en studie som pågick i 16 veckor var effekten och säkerheten
liknande som hos vuxna.
- Vecka 16 uppnådde 67–70 procent av patienterna i åldern 6–11 år EASI-75-respons i dupilumabgruppen (med viktmässig dosering) och 27 procent i placebogruppen, då båda grupperna också använde en lokal kortikosteroid «In children (6-11 years) with severe atopic dermatitis dupilumab (100 mg every two weeks for children with weight of 15 to <30 kg and 200 mg every two weeks for children with weight of ≥30 kg) with topical corticosteroids appears to increase the proportion of patients reaching EASI-75 at week 16 when compared to placebo (67–70% vs. 27%).»B. Motsvarande siffror för unga (12–17-åringar) utan samtidig användning av läkemedelssalva var 42 procent och 8 procent «Simpson EL, Paller AS, Siegfried EC ym. Efficacy a...»149.
- Dubilumab verkar vara effektivt vid behandling av måttligt och svårt atopiskt eksem
hos barn i åldern 0,5–5 år. I en studie som pågick i 16 veckor var effekten och säkerheten
liknande som hos äldre barn och vuxna «Paller AS, Simpson EL, Siegfried EC ym. Dupilumab ...»212.
- Vecka 16 uppnådde 53 procent av 0,5–5-åringarna i dupilumabgruppen och 11 procent i placebogruppen EASI-75-respons, då båda grupperna också använde en lokal kortikosteroid.
- Dupilumab verkar vara effektivt hos barn och unga i åldern 6–17 år som lider av måttligt
eller svårt atopiskt eksem. I en studie som pågick i 16 veckor var effekten och säkerheten
liknande som hos vuxna.
- Upadacitinib
- Upadacitinib verkar vara effektivt hos unga i åldern 12–17 år.
- I undergruppsanalyser motsvarade EASI-75-resultaten för 12–17-åringar (n = 228) de vuxnas resultat «Guttman-Yassky E, Teixeira HD, Simpson EL ym. Once...»158.
- Abrocitinib
- Abrocitinib har ingen officiell indikation för personer under 18 år (4/2023), men det har också undersökts vid behandling av atopiskt eksem hos barn och unga.
- Abrocitinib verkar vara effektivt hos barn och unga i åldern 12–17 år.
- I en studie som pågick i 12 veckor var effekten och säkerheten liknande som hos vuxna.
- Vecka 12 uppnådde 72 procent av patienterna EASI-75-respons i abrocitinib 200 mg-gruppen, 69 procent i abrocitinib 100 mg-gruppen och 42 procent i placebogruppen, då man samtidigt använde läkemedelssalvor «Eichenfield LF, Flohr C, Sidbury R ym. Efficacy an...»213.
Övriga behandlingar hos barn
- Probiotika verkar inte ha någon effekt vid behandling av atopiskt eksem «Boyle RJ, Bath-Hextall FJ, Leonardi-Bee J ym. Prob...»214, «Baquerizo Nole KL, Yim E, Keri JE. Probiotics and ...»215.
- Det finns inte tillräckligt med evidens för effekten av prebiotika vid behandling av eksem «van der Aa LB, Heymans HS, van Aalderen WM ym. Eff...»216.
- På grund av systembiverkningar rekommenderas inte användning av invärtes kortikosteroider.
- Effekten av UV-behandling av atopiskt eksem hos barn har inte utretts med kontrollerade och randomiserade studier, men responsen och biverkningarna motsvarar sannolikt resultaten hos vuxna.
- Det finns ingen tillförlitlig evidens på långtidssäkerheten av UV-behandling för barn.
- UV-behandling (SUP eller smalbandig UVB) kan användas vid måttligt och svårt atopiskt eksem hos barn i alla åldrar noga övervägt under övervakning av en specialist «Collins P, Ferguson J. Narrowband (TL-01) UVB air-...»217.
Ekonomisk information
- Se JAK-hämmarnas och biologiska läkemedels verkan (EASI-75-respons), jämförelse av läkemedelskostnader och behandlingsrespons vid behandling av atopiskt eksem «https://www.terveysportti.fi/apps/laake/laakekustannus/hoi50077»1 (kräver åtkommsrätt), mer information «The number needed to treat (NNT) and cost per responder for systemic therapies for moderate-to-severe atopic dermatitis»21 och video om hur man läser tabellen «Hoitovasteen kustannukset Käypä hoito -suosituksissa: näin luen taulukoita (video)»30.
Nivåstrukturerad vård
- Se bilden Behandlingsalgoritm vid atopiskt eksem «Behandlingsalgoritm vid atopiskt eksem»1.
- Praxis för nivåstrukturering av vården avtalas regionalt enligt hur kunskaper och färdigheter finns tillgängliga på olika nivåer.
- Inom primärvården ordnas utan konsultation av en specialist i hudsjukdomar och allergologi
eller barnsjukdomar
- diagnostik utifrån anamnesen och den kliniska bilden
- behandling av lindrigt och måttligt atopiskt eksem hos vuxna enligt rekommendationen och patienthandledning
- behandling av lindrigt atopiskt eksem hos barn enligt rekommendationen och patienthandledning
- kartläggning av faktorer som upprätthåller och förvärrar atopiskt eksem samt eventuella
associerade sjukdomar.
- Allergitester behövs i allmänhet inte.
- Patienthandledning: Se egenvårdsanvisningarna Handledd egenvård av atopiskt eksem
hos vuxna «hoi50077c.pdf»1, Handledd egenvård av atopiskt eksem hos barn «hoi50077d.pdf»2, «Ohje vanhemmille atooppisesta ekseemasta»1 och videor om smörjningshandledning, vuxna «Atooppinen ekseema -suosituksen videot (aikuiset)»2 och barn «Atooppinen ekseema -suosituksen videot (lapset)»3.
- Kalcineurinhämmare är begränsat grundersättningsgilla. B-utlåtandet kan förnyas inom primärvården. Se .
- Inom primärvården kan man inleda lokalbehandling med kalcineurinhämmare mot eksem i ansiktet om läkaren har erfarenhet av behandling av atopiskt eksem.
- Indikationer för konsultation av specialist
- minst måttligt atopiskt eksem hos barn
- misstanke om grundläggande födoämnesallergi hos barn (se God medicinsk praxis-rekommendationen Födoämnesallergi (barn) «Matallergi (barn)»2)
- svårt atopiskt eksem hos en vuxen: eksemet uppvisar omfattande eller svåra symtom trots adekvat behandling med läkemedelssalva
- även lindrigare eksem med problem i genomförandet av behandlingen eller dåligt terapisvar
- eksemet påverkar patientens arbets- eller funktionsförmåga
- differentialdiagnostiskt problem
- kriterierna för ersättning av lokal kalcineurinhämmare uppfylls och ett första B-utlåtande behövs
- övervägande av UV-behandlingar eller systemisk långvarig medicinering
- vid behov undersökning och behandling av associerade sjukdomar inom olika specialiteter
- Efter specialistkonsultationen
- den fortsatta vården sker vanligen inom primärvården
- upprepade konsultationer görs vid behov om sjukdomen inte är under kontroll.
- Patienter i alla åldrar med svår behandlingsresistens eller omfattande eksem följs upp inom den specialiserade sjukvården.
- Patienter som får systemisk långvarig läkemedelsbehandling följs upp av en specialist.
Begränsningar, förmåner och rehabilitering
Yrkesval
- Atopiskt eksem är den viktigaste riskfaktorn för arbetsrelaterat handeksem. Personer
som haft atopiskt eksem i barndomen har en ökad benägenhet att få handeksem i vuxen
ålder oberoende av arbete «Bryld LE, Hindsberger C, Kyvik KO ym. Risk factors...»218, «Johannisson A, Pontén A, Svensson Å. Prevalence, i...»219. Den atopiska hudens struktur, dvs. bristande funktion i skyddsbarriären, är förknippad
med en ökad risk för att få irritationseksem på händerna «Coenraads P-J, Diepgen TL. Risk for hand eczema i...»220.
- Faktorer som irriterar huden i arbetet ökar risken för att handeksem bryter ut.
- Faktorer som förvärrar handeksemet är våtarbete, hantering av livsmedel, riklig handtvätt, skyddshandskarnas baddande effekt, smutsiga och dammiga arbetsuppgifter, hantering av kemikalier som irriterar huden, såsom lösningsmedel, oljor och tvättmedel, samt en stor mekanisk irritation.
- Personer med atopiskt eksem löper dock ingen ökad risk att få allergiskt kontakteksem som framträder som handeksem. Allergiskt kontakteksem kan uppkomma vid exponering för allergiframkallande kemikalier i arbetet eller på fritiden.
- Faktorer som irriterar huden i arbetet ökar risken för att handeksem bryter ut.
- Det är bra att diskutera yrkesvalet med en karriärvägledare. Det är skäl att utreda riskerna i samband med arbete som irriterar huden för arbetstagaren «Työperäiset sairaudet. Työterveyslaitos 2008. www....»221, «http://www.ttl.fi»18.
- Anvisningar för yrkesval finns på Arbetshälsoinstitutets webbplats Töissä terveenä «https://www.ttl.fi/teemat/tyoterveys/toissa-terveena-ammatinvalinta-allergia-ihottuma-ja-astma»19 och «https://www.ttl.fi/teemat/tyoterveys/toissa-terveena-ammatinvalinta-allergia-ihottuma-ja-astma/riskialttiit-ammatit»20.
- Begränsningar i arbetet:
- Personer med lindrigt atopiskt eksem, hos vilka eksemet framträder närmast på vintern och som inte har eksem på händerna, har inga absoluta begränsningar. Men det vore bättre om de valde ett torrt och rent arbete.
- Personer med atopiskt eksem som har haft handeksem lämpar sig dåligt för alla typer av arbeten som belastar huden på händerna, såsom kontinuerligt vått och smutsigt eller mekaniskt irriterande arbete, arbeten som medför exponering för kemikalier samt arbeten som kräver frekvent handtvätt eller kontinuerlig användning av täta gummi- eller plasthandskar «Lindström I, Mäkelä M, Pelkonen A ym. Astma, atoop...»222.
Militärtjänst
- Lindrigt atopiskt eksem påverkar inte den allmänna tjänstedugligheten, men svårare atopiskt eksem som kräver daglig lokalbehandling är ofta ett hinder för tjänstgöring «Lindström I, Mäkelä M, Pelkonen A ym. Astma, atoop...»222.
- Klassificeringarna av tjänsteduglighet och de allmänna grunderna för dem presenteras i tilläggsmaterialet (TTO-anvisning «https://puolustusvoimat.fi/documents/1948673/2258811/PEVIESTOS-Terveystarkastusohje2012.pdf/d8fec7e9-1178-44bf-8b6e-cdd9fd585ec3»21).
Folkpensionsanstaltens förmåner
- Se uppdaterade uppgifter om ersättningsgilla läkemedel som används vid behandling av atopiskt eksem på FPA:s webbplats «https://www.kela.fi/samarbetspartner-lakemedelsersattningar-ersattningsrattigheter-for-lakemedel»9.
- Handikappbidrag för personer under 16 år betalas som ersättning för en minst 6 månader lång större belastning och bundenhet än normalt till följd av vård, omsorg och rehabilitering av ett barn som är sjukt eller som har en funktionsnedsättning. Bidraget beviljas i allmänhet för en viss tid, efter vilken man kan ansöka om förlängning av bidraget «http://www.kela.fi/kelan-etuusohjeet_ohjeet-etuuksittain»22.
- Handikappbidrag för vuxna kan beviljas en person som fyllt 16 år och vars funktionsförmåga på grund av sjukdom, lyte eller skada är nedsatt i minst ett år och som inte är pensionär. Om de grundläggande förutsättningarna uppfylls bestäms rätten till förmånen och förmånens storlek enligt de så kallade bestämningsgrunderna «http://www.kela.fi/kelan-etuusohjeet_ohjeet-etuuksittain»22.
- Vårdbidraget för pensionstagare är avsett för pensionärer som fyllt 16 år och som får pension som berättigar till vårdbidrag och som på grund av skada eller sjukdom behöver hjälp eller handledning «http://www.kela.fi/kelan-etuusohjeet_ohjeet-etuuksittain»22.
- FPA-ersättning betalas för receptbelagda läkemedel, kliniska näringspreparat och bassalvor som ordinerats för behandling av sjukdom och som ingår i de preparat som ersätts. Mer information om årssjälvrisken, dvs. läkemedelstaket, se «https://www.kela.fi/lakemedel-sjalvrisker»23 och om hälso- och sjukvårdens avgiftstak se «https://stm.fi/sv/avgiftstak-for-halso-och-sjukvarden»24.
- Om en person med atopiskt eksem inte har tillräckliga inkomster och tillgångar för läkemedel och annan vård, kan personen ansöka om utkomststöd från FPA. Om den sökande får ett avslagsbeslut från FPA kan också kompletterande och förebyggande utkomststöd för läkemedel komma i fråga i vissa sällsynta situationer. Stödet söks från välfärdsområdet.
- En person med atopiskt eksem bör också komma ihåg att ansöka om reseersättningar som betalas av FPA, i synnerhet om personen får UV-behandling och på medicinska grunder måste använda FPA:s avtalstaxi för sjukresor. För mer information se «https://www.kela.fi/resor»25
- FPA:s sjukdagpenning beviljas vid behov enligt allmän praxis.
- En person med atopiskt eksem kan få stöd från funktionshinderservicen till exempel för att skaffa en tvättmaskin eller kläder. Se «https://thl.fi/sv/publikationer/handbocker/handbok-om-funktionshinderservice»26.
Rehabilitering
- Företagshälsovårdens lagstadgade uppgift är att bedöma patientens återstående arbetsförmåga. Svårt atopiskt eksem orsakar ibland behov av yrkesinriktad eller medicinsk rehabilitering. Ansökan om rehabilitering görs enligt allmän praxis «https://www.kela.fi/rehabilitering»27.
- Ibland kan en person med atopiskt eksem ha en svår livssituation och flera långvariga problem. Behandlingen av sjukdomen förverkligas inte nödvändigtvis optimalt. Då kan social rehabilitering komma i fråga «https://stm.fi/sv/social-rehabilitering»28. Bedömningen av servicebehovet och beslut i ärendet fattas inom välfärdsområdets socialservice.
- En person med atopiskt eksem får kamratstöd och annat socialt, psykiskt och kunskapsmässigt stöd också från patientorganisationerna. Allergi-, hud- och astmaförbundet ordnar årligen kurser och tillhandahåller kostnadsfri sjukdoms- och socialrådgivning. Se «https://www.allergia.fi/palvelut/kurssit/»29 och «https://www.allergia.fi/palvelut/tukea-apua-tietoa/neuvontanumerot/»30.
- Information om patientorganisationernas medlemsföreningar, se «https://www.allergia.fi/jarjesto/yhdistykset/»31
Arbetsgrupp tillsatt av Finska Läkarföreningen Duodecim, Allmänmedicinska föreningen i Finland och Finlands Dermatologförening
För mer information om arbetsgruppsmedlemmar samt anmälan om intressekonflikter, se «Atooppinen ekseema»1 (på finska)
Översättare: Lingsoft Language Services Oy
Granskning av översättningen: Hanna Schalin
Litteratur
Atopiskt eksem. God medicinsk praxis-rekommendation. Arbetsgrupp tillsatt av Finska Läkarföreningen Duodecim, Allmänmedicinska föreningen i Finland och Finlands Dermatologförening. Helsingfors: Finska Läkarföreningen Duodecim, 2024 (hänvisning dd.mm.åååå). Tillgänglig på internet: www.kaypahoito.fi
Närmare anvisningar: «https://www.kaypahoito.fi/sv/god-medicinsk-praxis/nyttjanderattigheter/citering»32
Ansvarsbegränsning
God medicinsk praxis- och Avstå klokt-rekommendationerna är sammandrag gjorda av experter gällande diagnostik och behandling av bestämda sjukdomar. Rekommendationerna fungerar som stöd när läkare eller andra yrkesutbildade personer inom hälso- och sjukvården ska fatta behandlingsbeslut. De ersätter inte läkarens eller annan hälsovårdspersonals egen bedömning av vilken diagnostik, behandling och rehabilitering som är bäst för den enskilda patienten då behandlingsbeslut fattas.
Litteratur
- Tokura Y, Hayano S. Subtypes of atopic dermatitis: From phenotype to endotype. Allergol Int 2022;71:14-24 «PMID: 34344611»PubMed
- Johansson EK, Bergström A, Kull I ym. Prevalence and characteristics of atopic dermatitis among young adult females and males-report from the Swedish population-based study BAMSE. J Eur Acad Dermatol Venereol 2022;36:698-704 «PMID: 35032357»PubMed
- Williams H, Stewart A, von Mutius E ym. Is eczema really on the increase worldwide? J Allergy Clin Immunol 2008;121:947-54.e15 «PMID: 18155278»PubMed
- Roduit C, Frei R, Loss G ym. Development of atopic dermatitis according to age of onset and association with early-life exposures. J Allergy Clin Immunol 2012;130:130-6.e5 «PMID: 22521248»PubMed
- Vakharia PP, Silverberg JI. Adult-Onset Atopic Dermatitis: Characteristics and Management. Am J Clin Dermatol 2019;20:771-779 «PMID: 31140066»PubMed
- Vartiainen E, Petäys T, Haahtela T ym. Allergic diseases, skin prick test responses, and IgE levels in North Karelia, Finland, and the Republic of Karelia, Russia. J Allergy Clin Immunol 2002;109:643-8 «PMID: 11941314»PubMed
- von Hertzen L, Mäkelä MJ, Petäys T ym. Growing disparities in atopy between the Finns and the Russians: a comparison of 2 generations. J Allergy Clin Immunol 2006;117:151-7 «PMID: 16387599»PubMed
- Mortz CG, Andersen KE, Dellgren C ym. Atopic dermatitis from adolescence to adulthood in the TOACS cohort: prevalence, persistence and comorbidities. Allergy 2015;70:836-45 «PMID: 25832131»PubMed
- Silverberg JI, Hanifin JM. Adult eczema prevalence and associations with asthma and other health and demographic factors: a US population-based study. J Allergy Clin Immunol 2013;132:1132-8 «PMID: 24094544»PubMed
- Barbarot S, Auziere S, Gadkari A ym. Epidemiology of atopic dermatitis in adults: Results from an international survey. Allergy 2018;73:1284-1293 «PMID: 29319189»PubMed
- Sinikumpu SP, Huilaja L, Jokelainen J ym. High prevalence of skin diseases and need for treatment in a middle-aged population. A Northern Finland Birth Cohort 1966 study. PLoS One 2014;9:e99533 «PMID: 24911008»PubMed
- Lee HH, Patel KR, Singam V ym. A systematic review and meta-analysis of the prevalence and phenotype of adult-onset atopic dermatitis. J Am Acad Dermatol 2019;80:1526-1532.e7 «PMID: 29864464»PubMed
- Langan SM, Irvine AD, Weidinger S. Atopic dermatitis. Lancet 2020;396:345-360 «PMID: 32738956»PubMed
- Reijula J, Latvala J, Mäkelä M ym. Long-term trends of asthma, allergic rhinitis and atopic eczema in young Finnish men: a retrospective analysis, 1926-2017. Eur Respir J 2020;56: «PMID: 32764114»PubMed
- Dharmage SC, Lowe AJ, Matheson MC ym. Atopic dermatitis and the atopic march revisited. Allergy 2014;69:17-27 «PMID: 24117677»PubMed
- Haider S, Fontanella S, Ullah A ym. Evolution of Eczema, Wheeze, and Rhinitis from Infancy to Early Adulthood: Four Birth Cohort Studies. Am J Respir Crit Care Med 2022;206:950-960 «PMID: 35679320»PubMed
- IIlli S, von Mutius E, Lau S ym. The natural course of atopic dermatitis from birth to age 7 years and the association with asthma. J Allergy Clin Immunol 2004;113:925-31 «PMID: 15131576»PubMed
- Williams HC, Strachan DP. The natural history of childhood eczema: observations from the British 1958 birth cohort study. Br J Dermatol 1998;139:834-9 «PMID: 9892950»PubMed
- Bieber T. Atopic dermatitis. N Engl J Med 2008;358:1483-94 PMID: 18385500
- Apfelbacher CJ, Diepgen TL, Schmitt J. Determinants of eczema: population-based cross-sectional study in Germany. Allergy 2011;66:206-13 «PMID: 20804468»PubMed.
- Sliz E, Huilaja L, Pasanen A ym. Uniting biobank resources reveals novel genetic pathways modulating susceptibility for atopic dermatitis. J Allergy Clin Immunol 2022;149:1105-1112.e9 «PMID: 34454985»PubMed
- Palmer CN, Irvine AD, Terron-Kwiatkowski A ym. Common loss-of-function variants of the epidermal barrier protein filaggrin are a major predisposing factor for atopic dermatitis. Nat Genet 2006;38:441-6 «PMID: 16550169»PubMed
- Luukkonen TM, Kiiski V, Ahola M ym. The Value of FLG Null Mutations in Predicting Treatment Response in Atopic Dermatitis: An Observational Study in Finnish Patients. Acta Derm Venereol 2017;97:456-463 «PMID: 27840886»PubMed
- van Smeden J, Bouwstra JA. Stratum Corneum Lipids: Their Role for the Skin Barrier Function in Healthy Subjects and Atopic Dermatitis Patients. Curr Probl Dermatol 2016;49:8-26 «PMID: 26844894»PubMed
- Joo KM, Hwang JH, Bae S ym. Relationship of ceramide-, and free fatty acid-cholesterol ratios in the stratum corneum with skin barrier function of normal, atopic dermatitis lesional and non-lesional skins. J Dermatol Sci 2015;77:71-4 «PMID: 25455137»PubMed
- Geoghegan JA, Irvine AD, Foster TJ: Staphylococcus aureus and Atopic Dermatitis: A Complex and Evolving Relationship. Trends in Microbiology 2018;26:484-497
- Legat FJ. Itch in Atopic Dermatitis - What Is New? Front Med (Lausanne) 2021;8:644760 «PMID: 34026782»PubMed
- Ständer S, Simpson EL, Guttman-Yassky E ym. Clinical Relevance of Skin Pain in Atopic Dermatitis. J Drugs Dermatol 2020;19:921-926 «PMID: 33026764»PubMed
- Greer FR, Sicherer SH, Burks AW ym. The Effects of Early Nutritional Interventions on the Development of Atopic Disease in Infants and Children: The Role of Maternal Dietary Restriction, Breastfeeding, Hydrolyzed Formulas, and Timing of Introduction of Allergenic Complementary Foods. Pediatrics 2019;143: «PMID: 30886111»PubMed
- Boyle RJ, Ierodiakonou D, Khan T ym. Hydrolysed formula and risk of allergic or autoimmune disease: systematic review and meta-analysis. BMJ 2016;352:i974 «PMID: 26956579»PubMed
- Osborn DA, Sinn JK, Jones LJ. Infant formulas containing hydrolysed protein for prevention of allergic disease. Cochrane Database Syst Rev 2018;10:CD003664 «PMID: 30338526»PubMed
- Foisy M, Boyle RJ, Chalmers JR ym. Overview of Reviews The prevention of eczema in infants and children: an overview of Cochrane and non-Cochrane reviews. Evid Based Child Health 2011;6:1322-1339 «PMID: 22822349»PubMed
- Netting MJ, Middleton PF, Makrides M. Does maternal diet during pregnancy and lactation affect outcomes in offspring? A systematic review of food-based approaches. Nutrition 2014;30:1225-41 «PMID: 25280403»PubMed
- Zutavern A, Brockow I, Schaaf B ym. Timing of solid food introduction in relation to eczema, asthma, allergic rhinitis, and food and inhalant sensitization at the age of 6 years: results from the prospective birth cohort study LISA. Pediatrics 2008;121:e44-52 «PMID: 18166543»PubMed
- Williams HC, Chalmers J. Prevention of Atopic Dermatitis. Acta Derm Venereol 2020;100:adv00166 «PMID: 32419030»PubMed
- Obbagy JE, English LK, Wong YP ym. Complementary feeding and food allergy, atopic dermatitis/eczema, asthma, and allergic rhinitis: a systematic review. Am J Clin Nutr 2019;109:890S-934S «PMID: 30982864»PubMed
- Pfefferle PI, Prescott SL, Kopp M. Microbial influence on tolerance and opportunities for intervention with prebiotics/probiotics and bacterial lysates. J Allergy Clin Immunol 2013;131:1453-63; quiz 1464 «PMID: 23643095»PubMed
- Kuitunen M. Probiotics and prebiotics in preventing food allergy and eczema. Curr Opin Allergy Clin Immunol 2013;13:280-6 «PMID: 23594506»PubMed
- Li L, Han Z, Niu X ym. Probiotic Supplementation for Prevention of Atopic Dermatitis in Infants and Children: A Systematic Review and Meta-analysis. Am J Clin Dermatol 2019;20:367-377 «PMID: 30465329»PubMed
- Osborn DA, Sinn JK. Prebiotics in infants for prevention of allergy. Cochrane Database Syst Rev 2013;:CD006474 «PMID: 23543544»PubMed
- Sestito S, D'Auria E, Baldassarre ME ym. The Role of Prebiotics and Probiotics in Prevention of Allergic Diseases in Infants. Front Pediatr 2020;8:583946 «PMID: 33415087»PubMed
- Kelleher MM, Cro S, Cornelius V ym. Skin care interventions in infants for preventing eczema and food allergy. Cochrane Database Syst Rev 2021;2:CD013534 «PMID: 33545739»PubMed
- Liang J, Hu F, Tang H ym. Systematic review and network meta-analysis of different types of emollient for the prevention of atopic dermatitis in infants. J Eur Acad Dermatol Venereol 2023;37:501-510 «PMID: 36415973»PubMed
- Simpson EL, Chalmers JR, Hanifin JM ym. Emollient enhancement of the skin barrier from birth offers effective atopic dermatitis prevention. J Allergy Clin Immunol 2014;134:818-23 «PMID: 25282563»PubMed
- Horimukai K, Morita K, Narita M ym. Application of moisturizer to neonates prevents development of atopic dermatitis. J Allergy Clin Immunol 2014;134:824-830.e6 «PMID: 25282564»PubMed
- Skjerven HO, Rehbinder EM, Vettukattil R ym. Skin emollient and early complementary feeding to prevent infant atopic dermatitis (PreventADALL): a factorial, multicentre, cluster-randomised trial. Lancet 2020;395:951-961 «PMID: 32087121»PubMed
- Chalmers JR, Haines RH, Bradshaw LE ym. Daily emollient during infancy for prevention of eczema: the BEEP randomised controlled trial. Lancet 2020;395:962-972 «PMID: 32087126»PubMed
- Brenninkmeijer EE, Schram ME, Leeflang MM ym. Diagnostic criteria for atopic dermatitis: a systematic review. Br J Dermatol 2008;158:754-65 «PMID: 18241277»PubMed
- Champion RH ym. (toim.) Textbook of Dermatology, 6. painos, 1998
- Williams HC, Burney PG, Pembroke AC ym. The U.K. Working Party's Diagnostic Criteria for Atopic Dermatitis. III. Independent hospital validation. Br J Dermatol 1994;131:406-16 «PMID: 7918017»PubMed
- Li JX, Dong RJ, Zeng YP. Characteristics, mechanism, and management of pain in atopic dermatitis: A literature review. Clin Transl Allergy 2021;11:e12079 «PMID: 34962720»PubMed
- Thomas KS, Apfelbacher CA, Chalmers JR ym. Recommended core outcome instruments for health-related quality of life, long-term control and itch intensity in atopic eczema trials: results of the HOME VII consensus meeting. Br J Dermatol 2021;185:139-146 «PMID: 33393074»PubMed
- Czarnowicki T, He H, Krueger JG ym. Atopic dermatitis endotypes and implications for targeted therapeutics. J Allergy Clin Immunol 2019;143:1-11 «PMID: 30612663»PubMed
- Tokura Y, Hayano S. Subtypes of atopic dermatitis: From phenotype to endotype. Allergol Int 2022;71:14-24 «PMID: 34344611»PubMed
- Paternoster L, Savenije OEM, Heron J ym. Identification of atopic dermatitis subgroups in children from 2 longitudinal birth cohorts. J Allergy Clin Immunol 2018;141:964-971 «PMID: 29129583»PubMed
- Roduit C, Frei R, Depner M ym. Phenotypes of Atopic Dermatitis Depending on the Timing of Onset and Progression in Childhood. JAMA Pediatr 2017;171:655-662 «PMID: 28531273»PubMed
- Renert-Yuval Y, Thyssen JP, Bissonnette R ym. Biomarkers in atopic dermatitis-a review on behalf of the International Eczema Council. J Allergy Clin Immunol 2021;147:1174-1190.e1 «PMID: 33516871»PubMed
- Akdis CA, Akdis M, Bieber T ym. Diagnosis and treatment of atopic dermatitis in children and adults: European Academy of Allergology and Clinical Immunology/American Academy of Allergy, Asthma and Immunology/PRACTALL Consensus Report. J Allergy Clin Immunol 2006;118:152-69 «PMID: 16815151»PubMed
- Zhao CY, Hao EY, Oh DD ym. A comparison study of clinician-rated atopic dermatitis outcome measures for intermediate- to dark-skinned patients. Br J Dermatol 2017;176:985-992 «PMID: 28012183»PubMed
- Werfel T, Heratizadeh A, Niebuhr M ym. Exacerbation of atopic dermatitis on grass pollen exposure in an environmental challenge chamber. J Allergy Clin Immunol 2015;136:96-103.e9 «PMID: 26044854»PubMed
- Nankervis H, Pynn EV, Boyle RJ ym. House dust mite reduction and avoidance measures for treating eczema. Cochrane Database Syst Rev 2015;1:CD008426 «PMID: 25598014»PubMed
- Ring J, Alomar A, Bieber T ym. Guidelines for treatment of atopic eczema (atopic dermatitis) part I. J Eur Acad Dermatol Venereol 2012;26:1045-60 «PMID: 22805051»PubMed
- Davis DMR, Drucker AM, Alikhan A ym. American Academy of Dermatology Guidelines: Awareness of comorbidities associated with atopic dermatitis in adults. J Am Acad Dermatol 2022;86:1335-1336.e18 «PMID: 35085682»PubMed
- Hamann CR, Hamann D, Egeberg A ym. Association between atopic dermatitis and contact sensitization: A systematic review and meta-analysis. J Am Acad Dermatol 2017;77:70-78 «PMID: 28392290»PubMed
- Wang V, Boguniewicz J, Boguniewicz M ym. The infectious complications of atopic dermatitis. Ann Allergy Asthma Immunol 2021;126:3-12 «PMID: 32771354»PubMed
- Legendre L, Barnetche T, Mazereeuw-Hautier J ym. Risk of lymphoma in patients with atopic dermatitis and the role of topical treatment: A systematic review and meta-analysis. J Am Acad Dermatol 2015;72:992-1002 «PMID: 25840730»PubMed
- Hsu JI, Pflugfelder SC, Kim SJ. Ocular complications of atopic dermatitis. Cutis 2019;104:189-193 «PMID: 31675394»PubMed
- Andersen YM, Egeberg A, Gislason GH ym. Autoimmune diseases in adults with atopic dermatitis. J Am Acad Dermatol 2017;76:274-280.e1 «PMID: 27742171»PubMed
- Narla S, Silverberg JI. Association between atopic dermatitis and autoimmune disorders in US adults and children: A cross-sectional study. J Am Acad Dermatol 2019;80:382-389 «PMID: 30287311»PubMed
- Ivert LU, Wahlgren CF, Lindelöf B ym. Association between atopic dermatitis and autoimmune diseases: a population-based case-control study. Br J Dermatol 2021;185:335-342 «PMID: 33091150»PubMed
- Kauppi S, Jokelainen J, Timonen M ym. Atopic Dermatitis Is Associated with Dermatitis Herpetiformis and Celiac Disease in Children. J Invest Dermatol 2021;141:191-193.e2 «PMID: 32540248»PubMed
- Rønnstad ATM, Halling-Overgaard AS, Hamann CR ym. Association of atopic dermatitis with depression, anxiety, and suicidal ideation in children and adults: A systematic review and meta-analysis. J Am Acad Dermatol 2018;79:448-456.e30 «PMID: 30119868»PubMed
- Silverberg JI, Gelfand JM, Margolis DJ ym. Symptoms and diagnosis of anxiety and depression in atopic dermatitis in U.S. adults. Br J Dermatol 2019;181:554-565 «PMID: 30838645»PubMed
- Kern C, Wan J, LeWinn KZ ym. Association of Atopic Dermatitis and Mental Health Outcomes Across Childhood: A Longitudinal Cohort Study. JAMA Dermatol 2021;157:1200-1208 «PMID: 34468686»PubMed
- Patel KR, Immaneni S, Singam V ym. Association between atopic dermatitis, depression, and suicidal ideation: A systematic review and meta-analysis. J Am Acad Dermatol 2019;80:402-410 «PMID: 30365995»PubMed
- Kauppi S, Jokelainen J, Timonen M ym. Adult Patients with Atopic Eczema have a High Burden of Psychiatric Disease: A Finnish Nationwide Registry Study. Acta Derm Venereol 2019;99:647-651 «PMID: 30848288»PubMed
- de Bruin-Weller M, Thaçi D, Smith CH ym. Dupilumab with concomitant topical corticosteroid treatment in adults with atopic dermatitis with an inadequate response or intolerance to ciclosporin A or when this treatment is medically inadvisable: a placebo-controlled, randomized phase III clinical trial (LIBERTY AD CAFÉ). Br J Dermatol 2018;178:1083-1101 «PMID: 29193016»PubMed
- Simpson EL, Wollenberg A, Bissonnette R ym. Patient-Reported Symptoms and Disease Impacts in Adults With Moderate-to-Severe Atopic Dermatitis: Results From a Phase 2b Study With Abrocitinib. Dermatitis 2021;32:S53-S61 «PMID: 33795561»PubMed
- Schans JV, Çiçek R, de Vries TW ym. Association of atopic diseases and attention-deficit/hyperactivity disorder: A systematic review and meta-analyses. Neurosci Biobehav Rev 2017;74:139-148 «PMID: 28111269»PubMed
- Jackson-Cowan L, Cole EF, Arbiser JL ym. TH2 sensitization in the skin-gut-brain axis: How early-life Th2-mediated inflammation may negatively perpetuate developmental and psychologic abnormalities. Pediatr Dermatol 2021;38:1032-1039 «PMID: 34338364»PubMed
- Fan R, Leasure AC, Damsky W ym. Association of atopic dermatitis with attention-deficit hyperactivity disorder among US adults in the "All of Us" research program: A case-control study. J Am Acad Dermatol 2022;87:691-692 «PMID: 35283246»PubMed.
- Silverberg JI. Comorbidities and the impact of atopic dermatitis. Ann Allergy Asthma Immunol 2019;123:144-151 «PMID: 31034875»PubMed
- Ascott A, Mulick A, Yu AM ym. Atopic eczema and major cardiovascular outcomes: A systematic review and meta-analysis of population-based studies. J Allergy Clin Immunol 2019;143:1821-1829 «PMID: 30576754»PubMed
- Pandher K, Ghamrawi RI, Heron CE ym. Controversial cardiovascular and hematologic comorbidities in atopic dermatitis. Arch Dermatol Res 2022;314:317-324 «PMID: 33973062»PubMed
- Rehal B, Armstrong AW. Health outcome measures in atopic dermatitis: a systematic review of trends in disease severity and quality-of-life instruments 1985-2010. PLoS One 2011;6:e17520 «PMID: 21533286»PubMed
- Silverberg JI, Garg NK, Paller AS ym. Sleep disturbances in adults with eczema are associated with impaired overall health: a US population-based study. J Invest Dermatol 2015;135:56-66 «PMID: 25078665»PubMed
- Theodosiou G, Montgomery S, Metsini A ym. Burden of Atopic Dermatitis in Swedish Adults: A Population-based Study. Acta Derm Venereol 2019;99:964-970 «PMID: 31289842»PubMed
- Wittkowski A, Richards HL, Griffiths CE ym. The impact of psychological and clinical factors on quality of life in individuals with atopic dermatitis. J Psychosom Res 2004;57:195-200 «PMID: 15465076»PubMed
- Beattie PE, Lewis-Jones MS. A comparative study of impairment of quality of life in children with skin disease and children with other chronic childhood diseases. Br J Dermatol 2006;155:145-51 «PMID: 16792766»PubMed
- Gånemo A, Svensson A, Lindberg M ym. Quality of life in Swedish children with eczema. Acta Derm Venereol 2007;87:345-9 «PMID: 17598039»PubMed
- Koulu L. Atooppinen ihottuma vaikuttaa elämänlaatuun ja elämänhaluun. Duodecim 2020;136:2479-83
- Lammintausta K, Kalimo K, Raitala R ym. Prognosis of atopic dermatitis. A prospective study in early adulthood. Int J Dermatol 1991;30:563-8 «PMID: 1938054»PubMed
- Chida Y, Steptoe A, Hirakawa N ym. The effects of psychological intervention on atopic dermatitis. A systematic review and meta-analysis. Int Arch Allergy Immunol 2007;144:1-9 «PMID: 17449959»PubMed
- Ersser SJ, Cowdell F, Latter S ym. Psychological and educational interventions for atopic eczema in children. Cochrane Database Syst Rev 2014;2014:CD004054 «PMID: 24399641»PubMed
- Leshem YA, Chalmers JR, Apfelbacher C ym. Measuring atopic eczema symptoms in clinical practice: The first consensus statement from the Harmonising Outcome Measures for Eczema in clinical practice initiative. J Am Acad Dermatol 2020;82:1181-1186 «PMID: 31926221»PubMed
- Simpson E, Eckert L, Gadkari A ym. Validation of the Atopic Dermatitis Control Tool (ADCT©) using a longitudinal survey of biologic-treated patients with atopic dermatitis. BMC Dermatol 2019;19:15 «PMID: 31690295»PubMed
- Tarr A, Iheanacho I. Should we use bath emollients for atopic eczema? BMJ 2009;339:b4273 «PMID: 19914950»PubMed
- Chiang C, Eichenfield LF. Quantitative assessment of combination bathing and moisturizing regimens on skin hydration in atopic dermatitis. Pediatr Dermatol 2009;26:273-8 «PMID: 19706087»PubMed
- Cork MJ, Britton J, Butler L ym. Comparison of parent knowledge, therapy utilization and severity of atopic eczema before and after explanation and demonstration of topical therapies by a specialist dermatology nurse. Br J Dermatol 2003;149:582-9 «PMID: 14510993»PubMed
- van Zuuren EJ, Fedorowicz Z, Christensen R ym. Emollients and moisturisers for eczema. Cochrane Database Syst Rev 2017;2:CD012119 «PMID: 28166390»PubMed
- Wollenberg A, Kinberger M, Arents B ym. EuroGuiDerm Guideline on Atopic Eczema Version 2.1, December 2022. https://www.guidelines.edf.one/guidelines/atopic-ezcema. «https://www.guidelines.edf.one/guidelines/atopic-ezcema»33 Viitattu 30.3.2023.
- Williams HC. Clinical practice. Atopic dermatitis. N Engl J Med 2005;352:2314-24 «PMID: 15930422»PubMed
- Hoare C, Li Wan Po A, Williams H. Systematic review of treatments for atopic eczema. Health Technol Assess 2000;4:1-191 «PMID: 11134919»PubMed
- Hannuksela-Svahn A, Hannuksela M. Ihotautien paikallishoito ja ultraviolettivalohoito. Kirjassa Ihotaudit. Hannuksela, Peltonen, Reunala, Suhonen toim. Kustannus Oy Duodecim 2011
- Nesbitt LT. Glucocorticoids. In: Bologna JL, Jorizzo JL. Dermatology, 2nd edition. Mosby Elsevier 2008; 1923-34.
- Eichenfield LF, Tom WL, Berger TG ym. Guidelines of care for the management of atopic dermatitis: section 2. Management and treatment of atopic dermatitis with topical therapies. J Am Acad Dermatol 2014;71:116-32 «PMID: 24813302»PubMed
- Danby SG, Chittock J, Brown K ym. The effect of tacrolimus compared with betamethasone valerate on the skin barrier in volunteers with quiescent atopic dermatitis. Br J Dermatol 2014;170:914-21 «PMID: 24328907»PubMed
- Hanifin J, Gupta AK, Rajagopalan R. Intermittent dosing of fluticasone propionate cream for reducing the risk of relapse in atopic dermatitis patients. Br J Dermatol 2002;147:528-37 «PMID: 12207596»PubMed
- Berth-Jones J, Damstra RJ, Golsch S ym. Twice weekly fluticasone propionate added to emollient maintenance treatment to reduce risk of relapse in atopic dermatitis: randomised, double blind, parallel group study. BMJ 2003;326:1367 «PMID: 12816824»PubMed
- Williams HC. Established corticosteroid creams should be applied only once daily in patients with atopic eczema. BMJ 2007;334:1272 «PMID: 17569936»PubMed
- Woods MT, Brown PA, Baig-Lewis SF ym. Effects of a novel formulation of fluocinonide 0.1% cream on skin barrier function in atopic dermatitis. J Drugs Dermatol 2011;10:171-6 «PMID: 21283922»PubMed
- Bieber T, Vick K, Fölster-Holst R ym. Efficacy and safety of methylprednisolone aceponate ointment 0.1% compared to tacrolimus 0.03% in children and adolescents with an acute flare of severe atopic dermatitis. Allergy 2007;62:184-9 «PMID: 17298428»PubMed
- Stalder JF, Fleury M, Sourisse M ym. Local steroid therapy and bacterial skin flora in atopic dermatitis. Br J Dermatol 1994;131:536-40 «PMID: 7947206»PubMed
- Nilsson EJ, Henning CG, Magnusson J. Topical corticosteroids and Staphylococcus aureus in atopic dermatitis. J Am Acad Dermatol 1992;27:29-34 «PMID: 1619073»PubMed
- Oikarinen A, Autio P, Kiistala U ym. A new method to measure type I and III collagen synthesis in human skin in vivo: demonstration of decreased collagen synthesis after topical glucocorticoid treatment. J Invest Dermatol 1992;98:220-5 «PMID: 1732386»PubMed
- Hajar T, Leshem YA, Hanifin JM ym. A systematic review of topical corticosteroid withdrawal ("steroid addiction") in patients with atopic dermatitis and other dermatoses. J Am Acad Dermatol 2015;72:541-549.e2 «PMID: 25592622»PubMed
- Haeck IM, Rouwen TJ, Timmer-de Mik L ym. Topical corticosteroids in atopic dermatitis and the risk of glaucoma and cataracts. J Am Acad Dermatol 2011;64:275-81 «PMID: 21122943»PubMed
- Axon E, Chalmers JR, Santer M ym. Safety of topical corticosteroids in atopic eczema: an umbrella review. BMJ Open 2021;11:e046476 «PMID: 34233978»PubMed
- Kang S, Paller A, Soter N ym. Safe treatment of head/neck AD with tacrolimus ointment. J Dermatolog Treat 2003;14:86-94 «PMID: 12775315»PubMed
- Doss N, Reitamo S, Dubertret L ym. Superiority of tacrolimus 0.1% ointment compared with fluticasone 0.005% in adults with moderate to severe atopic dermatitis of the face: results from a randomized, double-blind trial. Br J Dermatol 2009;161:427-34 «PMID: 19416227»PubMed
- Murrell DF, Calvieri S, Ortonne JP ym. A randomized controlled trial of pimecrolimus cream 1% in adolescents and adults with head and neck atopic dermatitis and intolerant of, or dependent on, topical corticosteroids. Br J Dermatol 2007;157:954-9 «PMID: 17935515»PubMed
- Reitamo S, Rissanen J, Remitz A ym. Tacrolimus ointment does not affect collagen synthesis: results of a single-center randomized trial. J Invest Dermatol 1998;111:396-8 «PMID: 9740230»PubMed
- Kyllönen H, Remitz A, Mandelin JM ym. Effects of 1-year intermittent treatment with topical tacrolimus monotherapy on skin collagen synthesis in patients with atopic dermatitis. Br J Dermatol 2004;150:1174-81 «PMID: 15214906»PubMed
- Meurer M, Eichenfield LF, Ho V ym. Addition of pimecrolimus cream 1% to a topical corticosteroid treatment regimen in paediatric patients with severe atopic dermatitis: a randomized, double-blind trial. J Dermatolog Treat 2010;21:157-66 «PMID: 20394491»PubMed
- Cury Martins J, Martins C, Aoki V ym. Topical tacrolimus for atopic dermatitis. Cochrane Database Syst Rev 2015;2015:CD009864 «PMID: 26132597»PubMed
- Ashcroft DM, Chen LC, Garside R ym. Topical pimecrolimus for eczema. Cochrane Database Syst Rev 2007;2007:CD005500 «PMID: 17943859»PubMed
- Mandelin J, Remitz A, Reitamo S. Effect of oral acetylsalicylic acid on burning caused by tacrolimus ointment in patients with atopic dermatitis. Arch Dermatol 2010;146:1178-80 «PMID: 20956662»PubMed
- Reitamo S, Wollenberg A, Schöpf E ym. Safety and efficacy of 1 year of tacrolimus ointment monotherapy in adults with atopic dermatitis. The European Tacrolimus Ointment Study Group. Arch Dermatol 2000;136:999-1006 «PMID: 10926735»PubMed
- Hanifin JM, Ling MR, Langley R ym. Tacrolimus ointment for the treatment of atopic dermatitis in adult patients: part I, efficacy. J Am Acad Dermatol 2001;44:S28-38 «PMID: 11145793»PubMed
- Ling M, Gottlieb A, Pariser D ym. A randomized study of the safety, absorption and efficacy of pimecrolimus cream 1% applied twice or four times daily in patients with atopic dermatitis. J Dermatolog Treat 2005;16:142-8 «PMID: 16096179»PubMed
- Ashcroft DM, Dimmock P, Garside R ym. Efficacy and tolerability of topical pimecrolimus and tacrolimus in the treatment of atopic dermatitis: meta-analysis of randomised controlled trials. BMJ 2005;330:516 «PMID: 15731121»PubMed
- George SM, Karanovic S, Harrison DA ym. Interventions to reduce Staphylococcus aureus in the management of eczema. Cochrane Database Syst Rev 2019;2019: «PMID: 31684694»PubMed
- Remitz A, Kyllönen H, Granlund H ym. Tacrolimus ointment reduces staphylococcal colonization of atopic dermatitis lesions. J Allergy Clin Immunol 2001;107:196-7 «PMID: 11150013»PubMed
- Mayser P, Kupfer J, Nemetz D ym. Treatment of head and neck dermatitis with ciclopiroxolamine cream--results of a double-blind, placebo-controlled study. Skin Pharmacol Physiol 2006;19:153-8 «PMID: 16612143»PubMed
- Kaffenberger BH, Mathis J, Zirwas MJ. A retrospective descriptive study of oral azole antifungal agents in patients with patch test-negative head and neck predominant atopic dermatitis. J Am Acad Dermatol 2014;71:480-3 «PMID: 24925733»PubMed
- Svejgaard El, Larsen PØ, Deleuran M ym. Treatment of head and neck dermatitis comparing itraconazole 200 mg and 400 mg daily for 1 week with placebo. J Eur Acad Dermatol Venereol 2004;18:445-9 «PMID: 15196159»PubMed
- Krutmann J, Morita A. Mechanisms of ultraviolet (UV) B and UVA phototherapy. J Investig Dermatol Symp Proc 1999;4:70-2 «PMID: 10537012»PubMed
- Tintle S, Shemer A, Suárez-Fariñas M ym. Reversal of atopic dermatitis with narrow-band UVB phototherapy and biomarkers for therapeutic response. J Allergy Clin Immunol 2011;128:583-93.e1-4 «PMID: 21762976»PubMed
- Gambichler T, Skrygan M, Tomi NS ym. Changes of antimicrobial peptide mRNA expression in atopic eczema following phototherapy. Br J Dermatol 2006;155:1275-8 «PMID: 17107401»PubMed
- Lübbe J. Secondary infections in patients with atopic dermatitis. Am J Clin Dermatol 2003;4:641-54 «PMID: 12926982»PubMed
- Garritsen FM, Brouwer MW, Limpens J ym. Photo(chemo)therapy in the management of atopic dermatitis: an updated systematic review with implications for practice and research. Br J Dermatol 2014;170:501-13 «PMID: 24116934»PubMed
- Musters AH, Mashayekhi S, Harvey J ym. Phototherapy for atopic eczema. Cochrane Database Syst Rev 2021;10:CD013870 «PMID: 34709669»PubMed
- Reynolds NJ, Franklin V, Gray JC ym. Narrow-band ultraviolet B and broad-band ultraviolet A phototherapy in adult atopic eczema: a randomised controlled trial. Lancet 2001;357:2012-6 «PMID: 11438134»PubMed
- Ibbotson SH, Bilsland D, Cox NH ym. An update and guidance on narrowband ultraviolet B phototherapy: a British Photodermatology Group Workshop Report. Br J Dermatol 2004;151:283-97 «PMID: 15327535»PubMed
- Diffey BL. Factors affecting the choice of a ceiling on the number of exposures with TL01 ultraviolet B phototherapy. Br J Dermatol 2003;149:428-30 «PMID: 12932263»PubMed
- Sugie N, Fujii N, Danno K. Cyclosporin-A suppresses p53-dependent repair DNA synthesis and apoptosis following ultraviolet-B irradiation. Photodermatol Photoimmunol Photomed 2002;18:163-8 «PMID: 12390669»PubMed
- Schram ME, Roekevisch E, Leeflang MM ym. A randomized trial of methotrexate versus azathioprine for severe atopic eczema. J Allergy Clin Immunol 2011;128:353-9 «PMID: 21514637»PubMed
- Blauvelt A, de Bruin-Weller M, Gooderham M ym. Long-term management of moderate-to-severe atopic dermatitis with dupilumab and concomitant topical corticosteroids (LIBERTY AD CHRONOS): a 1-year, randomised, double-blinded, placebo-controlled, phase 3 trial. Lancet 2017;389:2287-2303 «PMID: 28478972»PubMed
- Simpson EL, Paller AS, Siegfried EC ym. Efficacy and Safety of Dupilumab in Adolescents With Uncontrolled Moderate to Severe Atopic Dermatitis: A Phase 3 Randomized Clinical Trial. JAMA Dermatol 2020;156:44-56 «PMID: 31693077»PubMed
- Husein-ElAhmed H, Steinhoff M. Dupilumab in prurigo nodularis: a systematic review of current evidence and analysis of predictive factors to response. J Dermatolog Treat 2022;33:1547-1553 «PMID: 33200955»PubMed
- Blauvelt A, Teixeira HD, Simpson EL ym. Efficacy and Safety of Upadacitinib vs Dupilumab in Adults With Moderate-to-Severe Atopic Dermatitis: A Randomized Clinical Trial. JAMA Dermatol 2021;157:1047-1055 «PMID: 34347860»PubMed
- Reich K, Thyssen JP, Blauvelt A ym. Efficacy and safety of abrocitinib versus dupilumab in adults with moderate-to-severe atopic dermatitis: a randomised, double-blind, multicentre phase 3 trial. Lancet 2022;400:273-282 «PMID: 35871814»PubMed
- Bieber T, Simpson EL, Silverberg JI ym. Abrocitinib versus Placebo or Dupilumab for Atopic Dermatitis. N Engl J Med 2021;384:1101-1112 «PMID: 33761207»PubMed
- Blauvelt A, Guttman-Yassky E, Paller AS ym. Long-Term Efficacy and Safety of Dupilumab in Adolescents with Moderate-to-Severe Atopic Dermatitis: Results Through Week 52 from a Phase III Open-Label Extension Trial (LIBERTY AD PED-OLE). Am J Clin Dermatol 2022;23:365-383 «PMID: 35567671»PubMed
- Siegels D, Heratizadeh A, Abraham S ym. Systemic treatments in the management of atopic dermatitis: A systematic review and meta-analysis. Allergy 2021;76:1053-1076 «PMID: 33074565»PubMed
- Thyssen JP, Heegaard S, Ivert L ym. Management of Ocular Manifestations of Atopic Dermatitis: A Consensus Meeting Using a Modified Delphi Process. Acta Derm Venereol 2020;100:adv00264 «PMID: 32926175»PubMed
- Simpson EL, Silverberg JI, Nosbaum A ym. Integrated Safety Analysis of Abrocitinib for the Treatment of Moderate-to-Severe Atopic Dermatitis From the Phase II and Phase III Clinical Trial Program. Am J Clin Dermatol 2021;22:693-707 «PMID: 34406619»PubMed
- Guttman-Yassky E, Teixeira HD, Simpson EL ym. Once-daily upadacitinib versus placebo in adolescents and adults with moderate-to-severe atopic dermatitis (Measure Up 1 and Measure Up 2): results from two replicate double-blind, randomised controlled phase 3 trials. Lancet 2021;397:2151-2168 «PMID: 34023008»PubMed
- Mendes-Bastos P, Ladizinski B, Guttman-Yassky E ym. Characterization of acne associated with upadacitinib treatment in patients with moderate-to-severe atopic dermatitis: A post hoc integrated analysis of 3 phase 3 randomized, double-blind, placebo-controlled trials. J Am Acad Dermatol 2022;87:784-791 «PMID: 35714786»PubMed
- Bath-Hextall FJ, Birnie AJ, Ravenscroft JC ym. Interventions to reduce Staphylococcus aureus in the management of atopic eczema: an updated Cochrane review. Br J Dermatol 2010;163:12-26 «PMID: 20222931»PubMed
- Sidbury R, Davis DM, Cohen DE ym. Guidelines of care for the management of atopic dermatitis: section 3. Management and treatment with phototherapy and systemic agents. J Am Acad Dermatol 2014;71:327-49 «PMID: 24813298»PubMed
- Boguniewicz M, Sampson H, Leung SB ym. Effects of cefuroxime axetil on Staphylococcus aureus colonization and superantigen production in atopic dermatitis. J Allergy Clin Immunol 2001;108:651-2 «PMID: 11590398»PubMed
- Ewing CI, Ashcroft C, Gibbs AC ym. Flucloxacillin in the treatment of atopic dermatitis. Br J Dermatol 1998;138:1022-9 «PMID: 9747366»PubMed
- Klein PA, Clark RA. An evidence-based review of the efficacy of antihistamines in relieving pruritus in atopic dermatitis. Arch Dermatol 1999;135:1522-5 «PMID: 10606058»PubMed
- Ng JC, Yew YW. Effect of Vitamin D Serum Levels and Supplementation on Atopic Dermatitis: A Systematic Review and Meta-analysis. Am J Clin Dermatol 2022;23:267-275 «PMID: 35246808»PubMed
- Vestita M, Filoni A, Congedo M ym. Vitamin D and atopic dermatitis in childhood. J Immunol Res 2015;2015:257879 «PMID: 25973433»PubMed
- Ong PY, Boguniewicz M. Investigational and unproven therapies in atopic dermatitis. Immunol Allergy Clin North Am 2010;30:425-39 «PMID: 20670823»PubMed
- Ernst E, Pittler MH, Stevinson C. Complementary/alternative medicine in dermatology: evidence-assessed efficacy of two diseases and two treatments. Am J Clin Dermatol 2002;3:341-8 «PMID: 12069640»PubMed
- Kim GW, Park JM, Chin HW ym. Comparative analysis of the use of complementary and alternative medicine by Korean patients with androgenetic alopecia, atopic dermatitis and psoriasis. J Eur Acad Dermatol Venereol 2013;27:827-35 «PMID: 22620682»PubMed
- Simpson EL, Basco M, Hanifin J. A cross-sectional survey of complementary and alternative medicine use in patients with atopic dermatitis. Am J Contact Dermat 2003;14:144-7 «PMID: 14744405»PubMed
- Hughes R, Ward D, Tobin AM ym. The use of alternative medicine in pediatric patients with atopic dermatitis. Pediatr Dermatol 2007;24:118-20 «PMID: 17461804»PubMed
- Gu S, Yang AW, Xue CC ym. Chinese herbal medicine for atopic eczema. Cochrane Database Syst Rev 2013;:CD008642 «PMID: 24018636»PubMed
- Tan HY, Zhang AL, Chen D ym. Chinese herbal medicine for atopic dermatitis: a systematic review. J Am Acad Dermatol 2013;69:295-304 «PMID: 23759835»PubMed
- Gu S, Yang AW, Li CG ym. Topical application of Chinese herbal medicine for atopic eczema: a systematic review with a meta-analysis. Dermatology 2014;228:294-302 «PMID: 24821063»PubMed
- Sheehan MP, Atherton DJ. One-year follow up of children treated with Chinese medicinal herbs for atopic eczema. Br J Dermatol 1994;130:488-93 «PMID: 8186115»PubMed
- Boneberger S, Rupec RA, Ruzicka T. Complementary therapy for atopic dermatitis and other allergic skin diseases: facts and controversies. Clin Dermatol 2010;28:57-61 «PMID: 20082952»PubMed
- Bath-Hextall F, Williams H. Atopic eczema. Clin Evid 2006;15:1-20
- Torley D, Futamura M, Williams HC ym. What's new in atopic eczema? An analysis of systematic reviews published in 2010-11. Clin Exp Dermatol 2013;38:449-56 «PMID: 23750610»PubMed
- Jiao R, Yang Z, Wang Y ym. The effectiveness and safety of acupuncture for patients with atopic eczema: a systematic review and meta-analysis. Acupunct Med 2020;38:3-14 «PMID: 31495184»PubMed
- Thyssen JP, Schuttelaar MLA, Alfonso JH ym. Guidelines for diagnosis, prevention, and treatment of hand eczema. Contact Dermatitis 2022;86:357-378 «PMID: 34971008»PubMed
- Koutroulis I, Papoutsis J, Kroumpouzos G. Atopic dermatitis in pregnancy: current status and challenges. Obstet Gynecol Surv 2011;66:654-63 «PMID: 22112526»PubMed
- Balakirski G, Novak N. Atopic dermatitis and pregnancy. J Allergy Clin Immunol 2022;149:1185-1194 «PMID: 35090948»PubMed
- Vestergaard C, Wollenberg A, Barbarot S ym. European task force on atopic dermatitis position paper: treatment of parental atopic dermatitis during preconception, pregnancy and lactation period. J Eur Acad Dermatol Venereol 2019;33:1644-1659 «PMID: 31231864»PubMed
- Weatherhead S, Robson SC, Reynolds NJ. Eczema in pregnancy. BMJ 2007;335:152-4 «PMID: 17641349»PubMed
- Malm H. Teratologinen palvelu. Henkilökohtainen tiedonanto. 9.2.2023
- Mahadevan U, Long MD, Kane SV ym. Pregnancy and Neonatal Outcomes After Fetal Exposure to Biologics and Thiopurines Among Women With Inflammatory Bowel Disease. Gastroenterology 2021;160:1131-1139 «PMID: 33227283»PubMed
- Bar-Gil Shitrit A, Grisaru-Granovsky S, Ben Ya'acov A ym. Management of Inflammatory Bowel Disease During Pregnancy. Dig Dis Sci 2016;61:2194-2204 «PMID: 27068171»PubMed
- Russell MD, Dey M, Flint J ym. British Society for Rheumatology guideline on prescribing drugs in pregnancy and breastfeeding: immunomodulatory anti-rheumatic drugs and corticosteroids. Rheumatology (Oxford) 2023;62:e48-e88 «PMID: 36318966»PubMed
- García-Soto L, Martín-Masot R, Espadafor-López B ym. Evaluation of atopy schools for parents. Allergol Immunopathol (Madr) 2021;49:1-5 «PMID: 33641287»PubMed
- Miyaji Y, Yang L, Yamamoto-Hanada K ym. Earlier aggressive treatment to shorten the duration of eczema in infants resulted in fewer food allergies at 2 years of age. J Allergy Clin Immunol Pract 2020;8:1721-1724.e6 «PMID: 31821918»PubMed
- Kelleher MM, Dunn-Galvin A, Gray C ym. Skin barrier impairment at birth predicts food allergy at 2 years of age. J Allergy Clin Immunol 2016;137:1111-1116.e8 «PMID: 26924469»PubMed
- Brough HA, Simpson A, Makinson K ym. Peanut allergy: effect of environmental peanut exposure in children with filaggrin loss-of-function mutations. J Allergy Clin Immunol 2014;134:867-875.e1 «PMID: 25282568»PubMed
- Salava A, Perälä M, Pelkonen A ym. Safety of tacrolimus 0.03% and 0.1% ointments in young children with atopic dermatitis: a 36-month follow-up study. Clin Exp Dermatol 2022;47:889-902 «PMID: 34798685»PubMed
- Perälä M, Salava A, Malmberg P ym. Topical tacrolimus and corticosteroids in childhood moderate-to-severe atopic dermatitis with impact on airways: A long-term randomized open-label study. Clin Exp Dermatol 2023;: «PMID: 36916653»PubMed
- Thomas KS, Armstrong S, Avery A ym. Randomised controlled trial of short bursts of a potent topical corticosteroid versus prolonged use of a mild preparation for children with mild or moderate atopic eczema. BMJ 2002;324:768 «PMID: 11923161»PubMed
- Devillers AC, Oranje AP. Efficacy and safety of 'wet-wrap' dressings as an intervention treatment in children with severe and/or refractory atopic dermatitis: a critical review of the literature. Br J Dermatol 2006;154:579-85 «PMID: 16536797»PubMed
- Nicol NH, Boguniewicz M, Strand M ym. Wet wrap therapy in children with moderate to severe atopic dermatitis in a multidisciplinary treatment program. J Allergy Clin Immunol Pract 2014;2:400-6 «PMID: 25017527»PubMed
- Ainley-Walker PF, Patel L, David TJ. Side to side comparison of topical treatment in atopic dermatitis. Arch Dis Child 1998;79:149-52 «PMID: 9797597»PubMed
- Davallow Ghajar L, Wood Heickman LK, Conaway M ym. Low Risk of Adrenal Insufficiency After Use of Low- to Moderate-Potency Topical Corticosteroids for Children With Atopic Dermatitis. Clin Pediatr (Phila) 2019;58:406-412 «PMID: 30694073»PubMed
- Reitamo S, Rustin M, Harper J ym. A 4-year follow-up study of atopic dermatitis therapy with 0.1% tacrolimus ointment in children and adult patients. Br J Dermatol 2008;159:942-51 «PMID: 18637898»PubMed
- Wahn U, Bos JD, Goodfield M ym. Efficacy and safety of pimecrolimus cream in the long-term management of atopic dermatitis in children. Pediatrics 2002;110:e2 «PMID: 12093983»PubMed
- Sigurgeirsson B, Ho V, Ferrándiz C ym. Effectiveness and safety of a prevention-of-flare-progression strategy with pimecrolimus cream 1% in the management of paediatric atopic dermatitis. J Eur Acad Dermatol Venereol 2008;22:1290-301 «PMID: 18624866»PubMed
- Schmitt J, von Kobyletzki L, Svensson A ym. Efficacy and tolerability of proactive treatment with topical corticosteroids and calcineurin inhibitors for atopic eczema: systematic review and meta-analysis of randomized controlled trials. Br J Dermatol 2011;164:415-28 «PMID: 20819086»PubMed
- Paul C, Cork M, Rossi AB ym. Safety and tolerability of 1% pimecrolimus cream among infants: experience with 1133 patients treated for up to 2 years. Pediatrics 2006;117:e118-28 «PMID: 16361223»PubMed
- Kapp A, Papp K, Bingham A ym. Long-term management of atopic dermatitis in infants with topical pimecrolimus, a nonsteroid anti-inflammatory drug. J Allergy Clin Immunol 2002;110:277-84 «PMID: 12170269»PubMed
- Koo JY, Fleischer AB Jr, Abramovits W ym. Tacrolimus ointment is safe and effective in the treatment of atopic dermatitis: results in 8000 patients. J Am Acad Dermatol 2005;53:S195-205 «PMID: 16021175»PubMed
- Staab D, Pariser D, Gottlieb AB ym. Low systemic absorption and good tolerability of pimecrolimus, administered as 1% cream (Elidel) in infants with atopic dermatitis--a multicenter, 3-week, open-label study. Pediatr Dermatol 2005;22:465-71 «PMID: 16191004»PubMed
- Alaiti S, Kang S, Fiedler VC ym. Tacrolimus (FK506) ointment for atopic dermatitis: a phase I study in adults and children. J Am Acad Dermatol 1998;38:69-76 «PMID: 9448208»PubMed
- Remitz A, Harper J, Rustin M ym. Long-term safety and efficacy of tacrolimus ointment for the treatment of atopic dermatitis in children. Acta Derm Venereol 2007;87:54-61 «PMID: 17225017»PubMed
- Stiehm ER, Roberts RL, Kaplan MS ym. Pneumococcal seroconversion after vaccination for children with atopic dermatitis treated with tacrolimus ointment. J Am Acad Dermatol 2005;53:S206-13 «PMID: 16021176»PubMed
- Papp KA, Breuer K, Meurer M ym. Long-term treatment of atopic dermatitis with pimecrolimus cream 1% in infants does not interfere with the development of protective antibodies after vaccination. J Am Acad Dermatol 2005;52:247-53 «PMID: 15692469»PubMed
- Paller AS, Simpson EL, Siegfried EC ym. Dupilumab in children aged 6 months to younger than 6 years with uncontrolled atopic dermatitis: a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2022;400:908-919 «PMID: 36116481»PubMed
- Eichenfield LF, Flohr C, Sidbury R ym. Efficacy and Safety of Abrocitinib in Combination With Topical Therapy in Adolescents With Moderate-to-Severe Atopic Dermatitis: The JADE TEEN Randomized Clinical Trial. JAMA Dermatol 2021;157:1165-1173 «PMID: 34406366»PubMed
- Boyle RJ, Bath-Hextall FJ, Leonardi-Bee J ym. Probiotics for the treatment of eczema: a systematic review. Clin Exp Allergy 2009;39:1117-27 «PMID: 19573037»PubMed
- Baquerizo Nole KL, Yim E, Keri JE. Probiotics and prebiotics in dermatology. J Am Acad Dermatol 2014;71:814-21 «PMID: 24906613»PubMed
- van der Aa LB, Heymans HS, van Aalderen WM ym. Effect of a new synbiotic mixture on atopic dermatitis in infants: a randomized-controlled trial. Clin Exp Allergy 2010;40:795-804 «PMID: 20184604»PubMed
- Collins P, Ferguson J. Narrowband (TL-01) UVB air-conditioned phototherapy for atopic eczema in children. Br J Dermatol 1995;133:653-5 «PMID: 7577604»PubMed
- Bryld LE, Hindsberger C, Kyvik KO ym. Risk factors influencing the development of hand eczema in a population-based twin sample. Br J Dermatol 2003;149:1214-20 «PMID: 14674899»PubMed
- Johannisson A, Pontén A, Svensson Å. Prevalence, incidence and predictive factors for hand eczema in young adults - a follow-up study. BMC Dermatol 2013;13:14 «PMID: 24164871»PubMed
- Coenraads P-J, Diepgen TL. Risk for hand eczema in employees with past or present atopic dermatitis. Int Arch Occup Environ Health 1998;71:7-13
- Työperäiset sairaudet. Työterveyslaitos 2008. www.ttl.fi «http://www.ttl.fi»18
- Lindström I, Mäkelä M, Pelkonen A ym. Astma, atooppinen ihottuma ja allergiat on huomioitava ammatinvalinnassa ja varusmiespalveluksessa. Suom Lääkäril 2023;78:e33929

