Förmaksflimmer
Hur kan man hänvisa till God medicinsk praxis-rekommendationen? «K1»1
Den här svenskspråkiga God medicinsk praxis-rekommendationen har översatts från den finska God medicinsk praxis-rekommendationen (Käypä hoito -suositus Eteisvärinä «Eteisvärinä»1). Om det finns skillnader i texterna gäller den uppdaterade finskspråkiga versionen.
Huvudsakligen finns evidenssammandragen och bakgrundsmaterialen samt internetlänkarna på finska.
Centrala rekommendationer
- Förmaksflimmer är den vanligaste långvariga rytmrubbningen. Den orsakar över en tredjedel av sjukhusvårdperioder med anknytning till rytmrubbningar och belastar även öppenvården i hög grad.
- Vid sidan av ålder är de mest betydande faktorerna som ökar risken för förmaksflimmer förhöjt blodtryck, hjärtsjukdomar, diabetes och övervikt.
- Obehandlat förmaksflimmer ökar dödligheten, ökar risken för stroke och andra tromboemboliska komplikationer, försämrar livskvaliteten och kan orsaka hjärtsvikt (s.k. takykardiomyopati).
- Behandlingen av förmaksflimmer väljs individuellt så att man beaktar de symtom som
rytmrubbningen orsakar samt patientens underliggande sjukdomar och önskemål. De viktigaste
behandlingsformerna är
- antikoagulationsbehandling som hindrar tromboemboliska komplikationer
- behandling av underliggande sjukdomar och andra faktorer som ökar risken för rytmrubbningar
- optimering av kammarfrekvens (frekvenskontroll)
- återställning av sinusrytm med elkonvertering eller farmakologisk kardioversion och förhindrande av att rytmrubbningen upprepas (rytmkontroll).
- Med tanke på patientens prognos är det viktigaste en korrekt genomförd antikoagulationsbehandling.
- Invasiv behandling är motiverad om responsen på medicineringen är bristfällig eller läkemedlen orsakar biverkningar.
Rekommendationens syfte
- Syftet med rekommendationen är att utifrån färska forskningsdata ge en praktisk anvisning om behandling av förmaksflimmer, förtydliga grunderna för val av individuell vårdlinje och precisera arbetsfördelningen mellan primärvården och den specialiserade sjukvården.
Målgrupper
- Den primära målgruppen är läkare inom primärvården och den specialiserade sjukvården som deltar i behandlingen av förmaksflimmer, men rekommendationen lämpar sig också för andra yrkesutbildade personer inom hälso- och sjukvården.
Avgränsning av ämnet
- Rekommendationen gäller behandling av förmaksflimmer hos vuxna men lämpar sig inte som sådan för specialsituationer, såsom förmaksflimmer i samband med hjärtinfarkt eller vid invasiva åtgärder (bl.a. hjärtoperation, ballongdilatation av kranskärlen).
- Förmaksfladder och andra supraventrikulära rytmrubbningar som är nära förknippade med förmaksflimmer behandlas endast till den del de har ett väsentligt samband med behandlingen av förmaksflimmer.
Definition och klassificering
- Förmaksflimmer är en supraventrikulär rytmrubbning som karakteriseras av snabb, oreglerad elektrisk och mekanisk funktion i förmaken.
- Förmaksflimmer kan beroende på återfallsbenägenhet och varaktighet delas in i tre huvudtyper «Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHR...»1, «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, (bild «Klassificering av förmaksflimmer enligt återfall och varaktighet»1):
- Anfallsvisuppträdande (paroxysmalt) förmaksflimmer (ICD-10-kod I48.0): sinusrytmen återställs spontant av sig själv eller aktivt genom kardioversion (elkonvertering eller farmakologiskt) inom 7 dygn.
- Ihållande (persistent) förmaksflimmer (I48.1): sinusrytmen återställs inte inom 7 dygn eller återställs genom elektrisk eller farmakologisk kardioversion efter att rytmrubbningen varat i mer än 7 dygn. I specialsituationer där man väljer rytmkontroll som behandlingslinje, även om förmaksflimmer har varit den dominerande rytmen i över ett år, kan man använda benämningen långvarigt persisterande (long-standing persistent) förmaksflimmer till skillnad från kroniskt förmaksflimmer.
- Kroniskt (permanent) förmaksflimmer (I48.2): rytmrubbningen godkänns eftersom en kardioversion inte lyckas eller anses obefogad.
- Latent förmaksflimmer (silent, subclinical) innebär att patienten har symtom som tyder på förmaksflimmer, men det har ännu inte kunnat diagnostiseras med EKG, eller en symtomfri patient har kortvariga förmaksrelaterade rytmrubbningar till exempel i pacemakerns minne.
- Den engelska termen "lone atrial fibrillation" används för förmaksflimmer som förekommer hos i övrigt friska patienter «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Kopecky SL, Gersh BJ, McGoon MD ym. The natural hi...»3. Det förekommer främst hos personer under 60 år.
- Om patienten får associerade sjukdomar med åldern är det inte längre fråga om s.k. "lone atrial fibrillation".
- Akut förmaksflimmer innebär ett symptomatiskt förmaksflimmeranfall som börjat nyligen. Det är viktigt att fastställa längden på ett akut förmaksflimmeranfall (under 12 timmar, 12–24 timmar eller 24–48 timmar) för att bedöma om en tidig kardioversion är möjlig.
- Förmaksflimmerbördan (atrial fibrillation burden) avser den andel av tiden under vilken patienten befann sig i förmaksflimmer under hjärtmonitoreringen.

Paroxysmalt förmaksflimmer har en benägenhet att med tiden bli svårare att behandla och tenderar bli ihållande och sedan kroniskt.
Epidemiologi
Prevalens
- Förmaksflimmer är den vanligaste långvariga rytmrubbningen. Prevalensen bland vuxna
är i genomsnitt 2–4 % och den förväntas öka 2,3-faldigt före 2060 «Chugh SS, Havmoeller R, Narayanan K ym. Worldwide ...»4.
- o I Finland är prevalensen av förmaksflimmer i genomsnitt 4,1 % och ca 230 000 patienter uppskattas ha förmaksflimmer i nuläget «Lehto M, Haukka J, Aro A, ym. Comprehensive nation...»5.
- Prevalensen varierar stort beroende på patientens ålder och underliggande sjukdomar «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Förmaksflimmer är sällsynt hos personer under 60 år (0,4 %), men det blir snabbt vanligare med åldern och över 20 % av personer över 75 år har förmaksflimmer «Lehto M, Haukka J, Aro A, ym. Comprehensive nation...»5.
- Patienternas medelålder är 75 år och cirka 70 % av patienterna är över 65 år «Feinberg WM, Blackshear JL, Laupacis A ym. Prevale...»6.
- Förmaksflimmer förekommer särskilt hos personer med hjärtsvikt.
- Hos cirka 4 % av dem som lider av lindrig hjärtsvikt och av dem som lider av svår hjärtsvikt med vilosymtom (NYHA IV) har till och med hälften förmaksflimmer «Savelieva I, John Camm A. Atrial fibrillation and ...»7.
Incidens
- Förmaksflimmer förekommer årligen hos 0,1 % av alla personer under 40 år men hos nästan
2 % av alla över 80 år «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Var tredje person över 55 år upplever förmaksflimmer under sitt liv «Lloyd-Jones DM, Wang TJ, Leip EP ym. Lifetime risk...»8, «Magnussen C, Niiranen TJ, Ojeda FM ym. Sex Differe...»9.
- Incidensen av förmaksflimmer ökar i takt med att befolkningen åldras och associerade sjukdomar blir vanligare «Miyasaka Y, Barnes ME, Gersh BJ ym. Secular trends...»10.
- Män löper nästan dubbelt så stor risk att insjukna i förmaksflimmer jämfört med kvinnor i samma ålder «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
Uppkomstmekanismer
- Förmaksflimmer uppkommer när tätt återkommande extraslag leder till (s.k. fokalt förmaksflimmer)
uppkomsten av flera oreglerade återinträden i förmaksvävnaden, «Rensma PL, Allessie MA, Lammers WJ ym. Length of e...»12, «Allessie MA, Boyden PA, Camm AJ ym. Pathophysiolog...»13, «Nattel S. New ideas about atrial fibrillation 50 y...»14, «Tieleman RG. The pathophysiology of maintenance of...»15.
- Extraslagen härstammar oftast från området kring lungvenerna «Haïssaguerre M, Jaïs P, Shah DC ym. Spontaneous in...»16, «Chen SA, Chen YJ, Yeh HI ym. Pathophysiology of th...»17, «Nattel S. Basic electrophysiology of the pulmonary...»18.
- Många strukturella förändringar, såsom förmaksmyopati, ökning i förmaksstorleken och
ansamling av bindväv samt funktionella faktorer (t.ex. tonus i det autonoma nervsystemet)
påverkar uppkomsten av förmaksflimmer och dess fortbestånd (bild «Förmaksflimmers uppkomstmekanismer»2).
- Vagalt förmaksflimmer börjar vanligen när slagfrekvensen blir långsammare på natten och i vila efter ansträngning eller måltider.
- Sympatikotont förmaksflimmer uppkommer i allmänhet när slagfrekvensen blir snabbare på grund av fysisk eller psykisk belastning.
- Förmaksflimmer föder sig själv så att det formar förmakens elektriska «Wijffels MC, Kirchhof CJ, Dorland R ym. Atrial fib...»19, «Allessie M, Ausma J, Schotten U. Electrical, contr...»20 och mekaniska funktion «Sparks PB, Mond HG, Vohra JK ym. Mechanical remode...»21, «Schotten U, Duytschaever M, Ausma J ym. Electrical...»22 samt strukturer «Nattel S, Li D, Yue L. Basic mechanisms of atrial ...»23, «Burstein B, Nattel S. Atrial fibrosis: mechanisms ...»24 så att rytmrubbningen blir långvarig och återställandet av sinusrytm försvåras (remodellering) (bild «Eteisvärinän luonnollinen kulku»3).
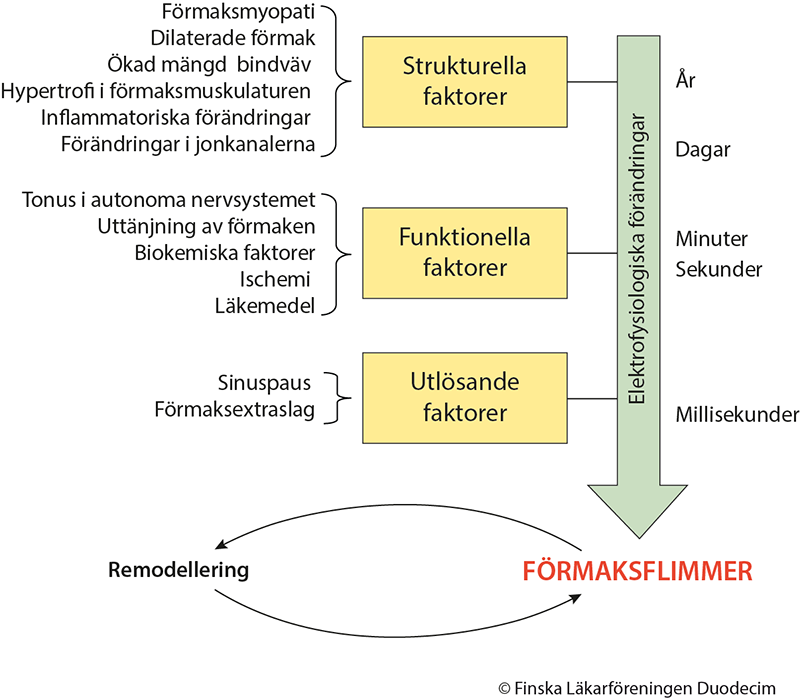
Uppkomsten och upprätthållandet av förmaksflimmer påverkas av många strukturella och funktionella faktorer. Förmaksflimmer föder sig själv genom att orsaka förändringar i förmakens elektriska och mekaniska funktion samt i strukturer som ökar risken för rytmrubbningar och upprätthåller störningen (remodeling).

Eteisvärinän luonnollinen kulku. Eteisvärinä ruokkii itse itseään, minkä takia kohtauksittaisella eteisvärinällä on taipumus muuttua vaikeammin hoidettavaksi jatkuvaksi ja edelleen pysyväksi eteisvärinäksi. Useimmissa tapauksissa potilaalla on ollut useita “piileviä” eteisvärinäepisodeja ennen kuin rytmihäiriö “saadaan kiinni”.
© Suomalainen Lääkäriseura Duodecim
Predisponerande faktorer
- Den största enskilda faktorn som ökar risken för förmaksflimmer är ålder.
- Hos personer över 50 år fördubblas risken för att insjukna i förmaksflimmer för varje tionde levnadsår «Benjamin EJ, Levy D, Vaziri SM ym. Independent ris...»11.
- Över 70 % av patienterna med förmaksflimmer har en strukturell hjärtsjukdom eller någon annan systemisk sjukdom som ökar risken för rytmrubbningar (tabell «Faktorer som ökar risken för förmaksflimmer...»1).
- De viktigaste hjärt- och cirkulationsrelaterade faktorerna som ökar risken för förmaksflimmer
är «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2
- högt blodtryck
- hjärtsvikt
- hjärtklaffel
- kranskärlssjukdom.
- Dessutom kan många supraventrikulära takykardier, såsom förmaksfladder, atrioventrikulär nodal återkopplingstakykardi och takykardi i samband med en medfödd accessorisk retledningsbana, utlösa förmaksflimmer om de blir långvariga.
- Extrakardiella predisponerande orsaker är särskilt diabetes, fetma och sömnapné, men även störningar i sköldkörtelns funktion, njursvikt och kroniska lungsjukdomar ökar risken «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Schoonderwoerd BA, Smit MD, Pen L ym. New risk fac...»25.
- Långvarig, regelbundet återkommande exceptionellt belastande uthållighetsträning (>
1 500 timmars kumulativ träningsbelastning) ökar risken för att senare utveckla förmaksflimmer «Elosua R, Arquer A, Mont L ym. Sport practice and ...»26, «Mont L, Sambola A, Brugada J ym. Long-lasting spor...»27, «Abdulla J, Nielsen JR. Is the risk of atrial fibri...»28, «Wilhelm M, Roten L, Tanner H ym. Atrial remodeling...»29, «Andersen K, Farahmand B, Ahlbom A ym. Risk of arrh...»30, «Karjalainen J, Kujala UM, Kaprio J ym. Lone atrial...»31, «Turagam MK, Flaker GC, Velagapudi P ym. Atrial Fib...»32, «Calvo N, Ramos P, Montserrat S ym. Emerging risk f...»33.
- De positiva effekterna av motion är dock så stora med tanke på hjärt- och cirkulationssjukdomar att det i allmänhet inte är förnuftigt att sluta motionera för att försöka förhindra förmaksflimmer «Aizer A, Gaziano JM, Cook NR ym. Relation of vigor...»34.
- Motion hos fysiskt svaga och överviktiga personer förhindrar uppkomsten av förmaksflimmer «Manolis AS, Manolis AA. Exercise and Arrhythmias: ...»35.
- Akuta, tillfälliga faktorer som utlöser förmaksflimmer är bland annat överkonsumtion
av alkohol ("baksmällsflimmer"), akut hjärtinfarkt, perikardit, myokardit och lungemboli.
- Behandling av den bakomliggande faktorn återställer ofta sinusrytmen i dessa tillstånd.
- Många faktorer som ökar risken för förmaksflimmer, såsom kranskärlssjukdom och blodtryckssjukdom
är ärftliga.
- Även benägenheten för s.k. "lone atrial fibrillation" kan vara familjär och enstaka jonkanalmutationer som ökar risken för förmaksflimmer har hittats «Brugada R, Tapscott T, Czernuszewicz GZ ym. Identi...»36, «Troughton RW, Asher CR, Klein AL. The role of echo...»37, «Andalib A, Brugada R, Nattel S. Atrial fibrillatio...»38.
- Genetiska undersökningar är enligt nuvarande uppfattning inte befogade.
| Hjärtrelaterade orsaker | Övriga orsaker |
|---|---|
| Högt blodtryck | Diabetes |
| Hjärtsvikt | Fetma |
| Klaffel | Sömnapné |
| Kranskärlssjukdom | Funktionsstörningar i sköldkörteln |
| Akut eller tidigare hjärtinfarkt | Njursvikt |
| Perikardit | Inflammatoriska sjukdomar |
| Myokardit | Dyslipidemi |
| Medfödda hjärtfel | Elektrolytstörningar |
| Hypertrofisk kardiomyopati | Akut eller kronisk lungsjukdom
|
| Dilaterad kardiomyopati | Feokromocytom |
| Sjuk sinusknuta | Riklig alkoholkonsumtion ("baksmällsflimmer") |
| Andra supraventrikulära rytmrubbningar | Användning av tobaks- och nikotinpreparat |
| Tillstånd efter hjärtoperation | Användning av droger (t.ex. kokain) |
Konsekvenser
Dödlighet
- Som rytmrubbning är förmaksflimmer sällan livshotande.
- I omfattande epidemiologiska studier har dödligheten hos patienter med förmaksflimmer jämfört med personer med sinusrytm konstaterats vara ungefär dubbelt så stor «Krahn AD, Manfreda J, Tate RB ym. The natural hist...»39, «Benjamin EJ, Wolf PA, D'Agostino RB ym. Impact of ...»40, «Stevenson WG, Stevenson LW, Middlekauff HR ym. Imp...»41.
- Dödligheten hos patienter med förmaksflimmer är så nära förknippad med hjärtsjukdomens svårighetsgrad och medicineringen av förmaksflimmer att det är osäkert om förmaksflimmer är en självständig riskfaktor eller ett tecken på en svår kardiovaskulär sjukdom eller beror på den använda arytmimedicineringen «Eteisvärinään liittyy lisääntynyt kuolleisuus, mutta on epäselvää johtuuko se rytmihäiriöstä sinänsä, taustalla olevasta sydänsairaudesta tai muusta sairaudesta vai käytetystä lääkityksestä.»C.
Tromboemboliska komplikationer
- Förmaksflimmer är den mest centrala faktorn som ökar risken för hjärtrelaterad embolisation.
- I genomsnitt 20–30 % av patienter med ischemisk stroke har förmaksflimmer och ca 10 % av kryptogena strokefall förklaras av förmaksflimmer.
- En del ischemiska hjärnembolier kan framkomma enbart som demens eller nedsatt kognitiv funktion «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Knecht S, Oelschläger C, Duning T ym. Atrial fibri...»42.
- Risken för emboli är särskilt stor 1–2 veckor efter en kardioversion.
- Förekomsten av hjärninfarkt hos patienter med förmaksflimmer i förhållande till personer
med sinusrytm är enligt riskfaktorerna ca dubbelt så stor «Aivohalvaus ilmaantuu keskimäärin 5 %:lle eteisvärinäpotilaista vuodessa, mutta vaaratekijöistä riippuen ilmaantuvuus vaihtelee 1–12 %.»A.
- Vid förmaksflimmer i samband med reumatiskt klaffel är risken för stroke upp till 17 gånger större «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Tack vare god behandling av riskfaktorer och intensifierad antikoagulationsbehandling minskade incidensen av stroke under det senaste decenniet till under hälften «Teppo K, Airaksinen KEJ, Jaakkola J, ym. Trends in...»43.
- De viktigaste faktorerna som ökar risken för hjärninfarkt vid förmaksflimmer är
- tidigare stroke eller TIA
- ålder ≥ 75 år
- måttlig eller svår mitralstenos eller mekanisk klaffprotes
- hypertrofisk kardiomyopati.
- Andra riskfaktorer som beaktas i CHA 2DS 2VA-poängsättningen är
- hjärtsvikt
- högt blodtryck
- diabetes
- 65–74 års ålder
- artärsjukdom (bl.a. betydande kranskärlssjukdom, plack i aortabågen eller halspulsådern eller perifer artärsjukdom).
- Andra kliniskt betydande riskfaktorer är
- njursvikt
- dyslipidemi
- rökning.
- Enligt den rådande uppfattningen är det kvinnliga könet inte en självständig trombosriskfaktor och könet påverkar inte behovet av antikoagulationsbehandling «Teppo K, Lip GYH, Airaksinen KEJ, ym. Comparing CH...»44, «Penttilä T, Lehto M, Niiranen J, ym. Differences i...»45.
- I praktiken bedöms risken för tromboemboliska komplikationer med hjälp av CHA2DS2VA-poängsättning (tabell «Bedömning av risken för tromboemboliska komplikationer med hjälp av modifierad CHA2DS2VASc-poängsättning....»2) «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Lip GY, Nieuwlaat R, Pisters R ym. Refining clinic...»46, «Van Staa TP, Setakis E, Di Tanna GL ym. A comparis...»47, ().
- Vid paroxysmalt förmaksflimmer är risken för trombos aningen mindre än vid ihållande eller kroniskt förmaksflimmer «Steinberg BA, Hellkamp AS, Lokhnygina Y ym. Higher...»48, «Vanassche T, Lauw MN, Eikelboom JW ym. Risk of isc...»49, men riskfaktorerna och vårdrekommendationen är alltid desamma.
- Vid hypertrofisk kardiomyopati, betydande mitralstenos och hjärtamyloidos är en permanent antikoagulationsbehandling motiverad för att förhindra tromboser i samband med förmaksflimmer oberoendeav CHA2DS2VASc-poäng «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
| Riskfaktor | Poäng | |
|---|---|---|
| Chronic heart failure | Hjärtsvikt | 1 |
| Hypertension | Högt blodtryck | 1 |
| A2ge ≥ 75 years | Ålder ≥ 75 år | 2 |
| Diabetes | Diabetes | 1 |
| S2troke or TIA | Tidigare stroke eller TIA | 2 |
| Vascular disease | Artärsjukdom 1 | 1 |
| Age 65–74 years | Ålder 65–74 år | 1 |
| Riskfaktorer märkta med rött kan inte påverkas, men risken för andra faktorer kan
minskas genom god behandling av dem. Hjärtsvikt som orsakat dekompensation ökar benägenheten
för tromboser oberoende av ejektionsfraktionen i vänster kammare. Maximipoängen är8 eftersom åldern ger en eller två poäng. Rekommendationen om val av antitrombotisk behandling som baserar sig på poängsättning har beskrivits i bild «Val av antitrombotisk behandling vid förmaksflimmer»4. 1 Betydande kranskärlssjukdom (symtom orsakade av kranskärlssjukdom och/eller betydande stenos som konstaterats vid radiologisk undersökning), plack i aortabågen, halsartärstenos eller svår perifer artärsjukdom. |
||

Indikationerna för en antikoagulationsbehandling (AK) bedöms i förhållande till patientens individuella risk för stroke genom att använda CHA2DS2VASc -riskpoängsättningen. Hos patienter med hög risk (CHA2DS2VASc ≥ 2) är AK-behandling (direkta orala antikoagulantia eller warfarin) indicerad nästan utan undantag. Hos patienter med medelhög risk (CHA2DS2VASc = 1) bedöms behovet av AK-behandling individuellt. Man kan avstå från behandlingen om blödningsrisken är hög, patienten inte vill använda AK-behandling, riskfaktorn (t.ex. blodtrycket) har behandlats väl och patienten inte har andra mindre riskfaktorer (bl.a. rökning, dyslipidemi, njursvikt). Patienter med låg risk (CHA2DS2VASc = 0) får ingen antikoagulationsbehandling, eftersom nyttan är mindre än nackdelarna. ASA och ADP-receptorblockerare lämpar sig inte för att förhindra tromboser med anknytning till förmaksflimmer på grund av sin svaga effekt och sina biverkningar. NNT (number needed to treat) är antalet patienter varav en patient undviker stroke jämfört med personer som fått placebo under ett års behandling (se tilläggsmaterialet «Antitromboottisen hoidon valinta eteisvärinässä»). Under ingrepp och operationer som orsakar blödningsrisk kan AK-behandlingen vid behov pausas med undantag av patienter med den högsta risken.
Hemodynamiska effekter
- Hjärtats minutvolym minskar på grund av förmaksflimmer med cirka 15–30 % «Alboni P, Scarfò S, Fucà G ym. Hemodynamics of idi...»50, «Clark DM, Plumb VJ, Epstein AE ym. Hemodynamic eff...»51, eftersom
- förmakssammandragningar saknas och förmaken och kamrarna fungerar i olika takt
- kammarresponsen är för snabb och oregelbunden med tanke på situationen.
- Den minskade minutvolymen har liten betydelse om sammandragningskapaciteten i vänster kammare är normal, men vid hjärtsvikt kan förmaksflimmer leda till plötsliga hemodynamiska problem «Lau CP, Leung WH, Wong CK ym. Haemodynamics of ind...»52.
- Förmaksflimmer kan orsaka hjärtsvikt (s.k. takykardiomyopati) om kammarresponsen kontinuerligt är för snabb «Shinbane JS, Wood MA, Jensen DN ym. Tachycardia-in...»53.
Livskvalitet
- Oavsett typ av förmaksflimmer (paroxysmalt, ihållande eller kroniskt) är patienternas
livskvalitet sämre under en rytmrubbning än under sinusrytm «Dorian P, Jung W, Newman D ym. The impairment of h...»54, «Lüderitz B. Dirk Durrer (1918-1984). J Interv Card...»55, «van den Berg MP, Hassink RJ, Tuinenburg AE ym. Qua...»56.
- I icke-kontrollerade studier observerades inga skillnader i livskvaliteten mellan de randomiserade patienterna för rytm- och frekvenskontroll, men i båda vårdlinjerna var livskvaliteten bättre hos patienter i sinusrytm «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Livskvaliteten hos patienter med förmaksflimmer är till många delar sämre än hos patienter
som kommer för ballongvidgning av kranskärlen och de som har haft hjärtinfarkt och
i genomsnitt på samma nivå som hos patienter med hjärtsvikt «van den Berg MP, Hassink RJ, Tuinenburg AE ym. Qua...»56.
- Livskvaliteten verkar försämras mer hos kvinnor än hos män «Paquette M, Roy D, Talajic M ym. Role of gender an...»57.
Diagnostik
- Förmaksflimmerdiagnosen ska alltid säkerställas med EKG (EKG med 12 avledningar eller vilken som helst tillräckligt lång EKG-registrering av god kvalitet som kontrollerats av läkare).
Symtom och kliniska fynd
- De symtom som förmaksflimmer orsakar och de kliniska fynden varierar beroende på hjärt- och andra associerade sjukdomar, rytmrubbningens varaktighet, kammarfrekvensen samt patientens kondition och vakenhetstillstånd.
- Förmaksflimmer kan vara helt symtomfritt, vilket försvårar diagnostiken.
- De vanligaste symtomen på förmaksflimmer är
- hjärtklappning (palpitation)
- trötthet och nedsatt prestationsförmåga
- yrsel
- bröstsmärta
- andnöd
- polyuri.
- Vid bedömning av symtomens svårighetsgrad rekommenderas EHRA-klassifikationen som utvecklats av European Heart Rhythm Association (se tabell «EHRA-klassificering av symtom orsakade av förmaksflimmer...»3), «Kirchhof P, Bax J, Blomstrom-Lundquist C ym. Early...»59.
- Synkope är sällsynt och väcker misstanke om allvarlig associerad sjukdom, såsom funktionsstörning i sinus- eller AV-knutan, aortastenos eller Wolff-Parkinson-Whites (WPW) syndrom.
- Det vanligaste kliniska fyndet är oregelbunden kammarfrekvens, som lätt kan konstateras genom auskultation av hjärtat
eller genom att känna på artärslagfrekvensen.
- På grund av "pulsunderskott" är slagfrekvensen i handleden ofta långsammare än auskulterat med stetoskop eller mätt med EKG.
| EHRA-klass | Kriterier |
|---|---|
| 1 | Inga symtom |
| 2 | Lindriga symtom som inte påverkar det dagliga livet |
| 3 | Svåra symtom som försvårar det dagliga livet |
| 4 | Outhärdliga symtom som lett till nödvändiga ändringar i det dagliga livet |
EKG-fynd
- På grund av förmakens täta (450–600/min) och icke- organiserade elektriska funktion urskiljs inte en normal P-våg och EKG-baslinjen är ojämn (bild «EKG med 12 avledningar som registrerats under förmaksflimmer»5)
- Kammarfrekvensen är oregelbunden när de elektriska impulserna går från förmak till kammare med varierande hastighet.
- QRS-komplexet är i allmänhet smalt, men det kan vara brett vid funktionellt (aberration) och permanent grenblock eller WPW-syndrom.
- Mycket snabbt (över 200/min) förmaksflimmer med breda QRS-komplex är sällsynt och tyder på WPW-syndrom (bild «Snabbt förmaksflimmer i samband med WPW-syndrom som konstaterats hos en ung kvinna»6).
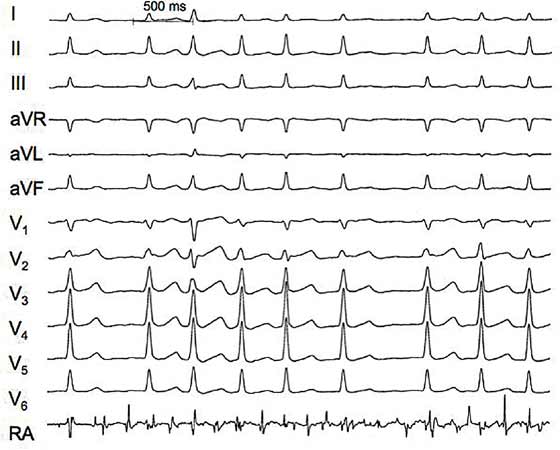
Observera oregelbundna slagintervall, varierande baslinje och avsaknad av P-vågor. Kammarresponsen vid förmaksflimmer är tydligt tätare hos denna patient (cirka 120–150/min). Det nedersta är EKG som registrerats från höger förmak och som visar en mycket snabb och ojämn förmaksrytm

Observera det breda QRS-komplexet på grund av deltavågen och den mycket snabba kammarfrekvensen (över 350/min). Sinusrytmen återställdes med kardioversion och patienten genomgick en lyckad kateterablation där två retledningsbanor kapades.
EKG-upptagningar från rytmkontrollanordningar och implanterbar EKG-monitor
- Rytmkontrollapparater (pacemaker för långsam slagfrekvens eller hjärtsvikt, implanterbar
defibrillator) och implanterbar EKG-monitor följer kontinuerligt med hjärtrytmen och
avslöjar därmed latent förmaksflimmer lättare än ett vanligt EKG med 12 avledningar,
Holter-registrering eller ett EKG som tagits då symptom uppkommit.
- Vid enkanalsregistrering eller registrering som sparats av pacemakern förutsätter diagnosen förmaksflimmer en rytmrubbning på minst 30 sekunder (jämför registreringen med upptagning under sinusrytm) «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Det är dock ännu oklart hur långt förmaksflimmer som sparats i apparatens minne som
är av betydelse vid kontinuerlig uppföljning med tanke på behovet av antikoagulationsbehandling.
- Enligt de senaste studierna kan rutinmässig antikoagulationsbehandling till och med vara skadlig för patienter som har korta (> 6 minuter men < 24 timmar) förmaksrelaterade rytmrubbningar (s.k. AHRE, atrial high rate episode) i pacemakerns minne «Kirchhof P, Toennis T, Goette A, ym. Anticoagulati...»60, «Healey JS, Lopes RD, Granger CB, ym. Apixaban for ...»61.
- I praktiken bör man även beakta eventuella andra trombosriskfaktorer utöver arytmibelastningen då man övervägerantikoagulationsbehandling. Antikoagulationsbehandling ska inte inledas utan en registrering där förmaksflimmer observerats.
- Det är värt att utnyttja de diagnostiska egenskaperna hos rytmkontrollapparater för att hitta symtomfritt förmaksflimmer hos patienter med stor trombosrisk. Vidbehov kan man söka efter förmaksflimmer efter en kryptogen hjärninfarkt genom att implantera en EKG-monitor «Toni D, Lorenzano S, Strano S ym. Detection of Sil...»62, se God medicinsk praxis-rekommendationen Hjärninfarkt och TIA «Hjärninfarkt och TIA»2, «Aivoinfarkti ja TIA. Käypä hoito -suositus. Suomal...»63
Smarttelefonapplikationer och andra apparater avsedda för självständig rytmuppföljning
- Det finns flera olika apparater och smarttelefonapplikationer som kan användas för
att registrera EKG eller följa slagfrekvensen och pulsvågen till exempel i handleden
eller fingertoppen utan invasiva åtgärder «Fung E, Järvelin MR, Doshi RN ym. Electrocardiogra...»64.
- Apparaterna är enkla att använda och gör det enkelt att följa hjärtats slagfrekvens under flera veckor eller till och med längre.
- Patienter med särskilt stor risk för förmaksflimmer (t.ex. ålder över 75 år, högt blodtryck, sömnapné) kan använda dem för självständig rytmobservation. Ämnet undersöks aktivt och mer information fås ständigt.
- I en del av apparaterna baseras identifieringen av förmaksflimmer enbart på analys
av hjärtfrekvensvariabiliteten och de sparar inte den egentliga EKG-mätningen.
- Trots utvecklingen av identifieringsalgoritmer kräver diagnosen förmaksflimmer alltid en EKG-registrering som kontrollerats av läkare.
Pulstagning
- Att ta pulsen från handleden eller halsen är ett grundläggande verktyg för screening av förmaksflimmer.
- Det lönar sig att i samband med mottagningsbesök lära alla äldre eller patienter som i övrigt har stor risk för förmaksflimmer att ta pulsen.
- Vid pulstagning fäster man uppmärksamhet förutom vid pulsfrekvensen även vid slagfrekvensens
regelbundenhet.
- Om slagfrekvensen även vid upprepad mätning är exceptionellt snabb eller oregelbunden är EKG befogat.
Differentialdiagnostik
- De viktigaste alternativen för differentialdiagnostik av förmaksflimmer är andra förmaksrelaterade
rytmrubbningar, såsom förmaksfladder (EKG-databas «Tyypillinen eteislepatus»1 (kräver åtkomsträtt)) och supraventrikulär takykardi (EKG-databas «Eteis-kammiosolmukkeen kiertoaktivaatiotakykardia»2 (kräver åtkomsträtt)).
- En jämn hjärtrusning som börjar och slutar plötsligt tyder på supraventrikulär takykardi.
- En jämn hjärtklappning som börjar och slutar så småningom passar bättre in på sinustakykardi än förmaksflimmer.
- Förmaksflimmer i samband med aberrant eller permanent grenblock och tidig aktivering av kammare kan likna kammartakykardi (EKG-databas «Sydäninfarktin arven aiheuttama takykardia»3 (kräver åtkomsträtt)).
Undersökningar
- Rekommendation om undersökningar av förmaksflimmerpatienter presenteras i tabell «Rekommenderade undersökningar för förmaksflimmerpatienter...»4.
- Basundersökningar ska göras för alla patienter när etiologin för förmaksflimmer utreds och långvarig behandling planeras, men omfattande laboratorie- och bilddiagnostiska undersökningar behövs i allmänhet inte vid behandling av akuta anfall.
| Basundersökningar | |
|---|---|
| 1. Anamnes och klinisk undersökning | |
|
|
| 2. EKG | |
|
|
| 3. Laboratorieundersökningar | |
|
|
| 4. Ultraljudsundersökning av hjärtat | |
|
|
| Ytterligare undersökningar | |
| 1. Andra bilddiagnostiska undersökningar | |
|
|
| 2. Långtidsregistrering av EKG eller symtom-EKG | |
|
|
| 3. Kliniskt belastningsprov | |
|
|
| 4. Ultraljudsundersökning av hjärtat via matstrupen | |
|
|
| 5. Elektrofysiologisk undersökning | |
|
|
Anamnes och klinisk undersökning
- Anamnes
- faktorer som ökar risken för tromboser (CHA2DS2VASc-poäng) och blödningar (HASBLED-poäng)
- symtom under rytmrubbningen (EHRA-klassificering)
- högt blodtryck och andra sjukdomar och faktorer som ökar risken för förmaksflimmer
- grov bedömning av den kognitiva funktionsförmågan (vid behov minnestest)
- rytmrubbningens varaktighet och anfallsfrekvens (typ av förmaksflimmer)
- sätt på vilket rytmrubbningen började och slutade (plötsligt eller så småningom)
- utlösande faktorer
- läkemedel och andra behandlingar
- rytmrubbningar och hjärtsjukdomar hos nära släktingar.
- Klinisk undersökning:
- noggrann kardiovaskulär undersökning: undersökning av artärslagfrekvensen, auskultation av hjärta och lungor, blodtrycksmätning och kontroll av tidigare mätresultat
- förmaksflimmerns inverkan på hemodynamiken (blodtrycket) och syretillförseln till hjärtmuskeln (ST-T-förändringar)
- tecken på faktorer som ökar risken för förmaksflimmer och tromboemboliska komplikationer samt andra hjärtsjukdomar.
EKG
- I EKG som registrerats under rytmrubbningen uppmärksammas förutom avsaknaden av P-våg även kammarfrekvens och fynd som tyder på hjärtsjukdomar.
- Under normal sinusrytm kan registrerad EKG avslöja många faktorer som är väsentliga för behandlingen av förmaksflimmer:
- P-vågens form och varaktighet: en lång P-våg med två toppar är ett tecken på långsammare överledning i förmaken eller mellan dessa eller att förmaken belastas, vilket ökar risken för förmaksflimmer
- QRS-komplexets form och varaktighet: hypertrofi i vänster kammare, infarktärr, grenblock, deltavåg
- PQ-tid: förkortad vid WPW-syndrom, förlängd vid störningar i atrioventrikulära överledningen.
- QT-tid: långt QT-syndrom och andra repolarisationsstörningar.
- EKG kan även användas för att följa upp läkemedelseffekten genom att analysera förändringar
orsakade av medicinering i
- pulsfrekvensen
- PQ-tiden
- QRS-komplexets form och varaktighet
- QT-tidens längd.
Laboratorieundersökningar
- När förebyggande behandling planeras efter det första anfallet eller när förmaksflimret
överraskande upprepas under behandlingen görs följande grundläggande undersökningar:
- liten blodbild
- plasmaelektrolyter
- plasmaglukos
- serumlipider
- funktionstest av sköldkörteln
- urinscreening (proteinuri, glukosuri)
- undersökningar i samband med inledande och uppföljning av antikoagulationsbehandling och profylax.
Ultraljudsundersökning av hjärtat
- För att konstatera eventuella strukturella hjärtsjukdomar rekommenderas att ultraljudsundersökning
av hjärtat görs en gång fhos alla patienter som konstateras ha förmaksflimmer.
- Hos äldre patienter som inte har några tecken på hjärtsjukdomar kan man dock avstå från detta om man väljer frekvenskontroll som vårdlinje och förmaksflimrets kammarfrekvens är "ekonomisk".
- En ultraljudsundersökning av hjärtat är särskilt viktig
- vid planering av inledande av egentlig arytmimedicinering (läkemedel i grupp I eller III) eller
- när det i övriga undersökningar konstateras symtom eller fynd som tyder på strukturell hjärtsjukdom.
- Vid ultraljudsundersökning av hjärtat fästs särskild uppmärksamhet vid faktorer som
påverkar valet av vårdlinje, profylaktisk behandling (arytmimedicinering, invasiv
behandling) och antikoagulationsbehandling «Troughton RW, Asher CR, Klein AL. The role of echo...»37, «McNamara RL, Tamariz LJ, Segal JB ym. Management o...»65:
- vänstra kammarens storlek och funktion
- vänstra förmakets storlek
- andra strukturella avvikelser i hjärtat, såsom infarktärr, klaffel och vägghypertrofi
- intrakardiella tromber.
- Ultraljudsundersökning av hjärtat via esofagus (TEE) utesluter på ett tillförlitligt
sätt intrakardiella tromber «Manning WJ, Weintraub RM, Waksmonski CA ym. Accura...»66, «Saarela E, Koskela V, Strandberg M ym. Ruokatorven...»67.
- En TEE-undersökning är nödvändig när omedelbar kardioversion planeras hos en icke antikoagulerad patient med förmaksflimmer som varat över 24-48 timmar eller är när durationen är oklar «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
Hjärt- och lungröntgen
- Röntgenbild av hjärtat och lungorna tas om man misstänker att orsaken till förmaksflimmer är en kronisk lungsjukdom eller någon annan sjukdom eller faktor som kan konstateras i en röntgenbild.
Övriga undersökningar
- Långtidsregistrering av EKG, symtom-EKG eller smarttelefon- eller andra applikationer som registrerar EKG kan användas inte bara för diagnostik utan även för utvärdering av vårdresponsen.
- Ettkliniskt belastningsprov är användbart vid diagnostik av förmaksflimmer som uppkommer under ansträngning, vid bedömning av frekvenskontroll vid kroniskt förmaksflimmer och uteslutning av ischemi när man planerar att inleda arytmiläkemedel i IC-gruppen.
- Bilddiagnostiska undersökningarav kranskärl och hjärta (kontrastundersökning, datortomografi, magnetundersökning, isotopundersökning) kan vara befogade om förmaksflimret är förknippat med bröstsmärta, andnöd eller andra hjärtsymtom. Bilddiagnostik kan också användas för att utreda anatomi i vänster förmak före kateterablation (datortomografi, magnetundersökning) och för att utesluta tromb i vänster förmak (datortomografi).
- Pulstagningpå egen hand hjälper vid identifiering av symtomfritt förmaksflimmer. Både pulstagning och ovan nämnda smarttelefon- och andra applikationer kan vara till nytta vid screening av patienter med hög risk och uppföljning av vården «Camm AJ, Lip GY, De Caterina R ym. 2012 focused up...»68.
Val av vårdlinje: frekvens- eller rytmkontroll
- Förmaksflimmer är ett mångfacetterat tillstånd som ofta kräver multiprofessionell kompetens och gott samarbete mellan olika specialiteter (bl.a. kardiologi, internmedicin, neurologi, kirurgi och hematologi) samt primärvården.
- Vid valet av individuell behandling av förmaksflimmer (tabell «Helhetsvård av förmaksflimmer...»5) beaktas
- andra (hjärt)sjukdomar
- riskfaktorer för tromboemboliska komplikationer
- patientens symtom (EHRA-klassificering)
- rytmrubbningens varaktighet
- förväntade fördelar och nackdelar med vården
- patientens önskemål.
- Vid det första symtomatiska förmaksflimmeranfallet lönar det sig nästan utan undantag
att försöka återställa sinusrytmen.
- Sinusrytmen återhämtar sig av sig själv inom 1–2 dygn utan åtgärder i 50–70 % av förmaksflimmeranfallen «Danias PG, Caulfield TA, Weigner MJ ym. Likelihood...»69, «Dell'Orfano JT, Patel H, Wolbrette DL ym. Acute tr...»70, «Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoit...»71.
- Hos äldre patienter utan symtom eller med lindriga symtom (EHRA 1–2) är prognosen
och livskvaliteten minst lika bra under frekvenskontroll som vid rytmkontroll «Sykkeenhallinta on eteisvärinässä parempi vaihtoehto kuin rytminhallinta aivohalvauksien ja kokonaiskuolleisuuden suhteen, mutta hoidot ovat samanarvoisia kuolleisuuden ja potilaiden elämänlaadun suhteen.»A.
- I dessa fall kan man avstå från kardioversion och koncentrera sig på behandling av förhöjt blodtryck, hjärtsvikt, diabetes och andra eventuella riskfaktorer samt antikoagulationsbehandling och frekvenskontroll «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Hohnloser SH, Kuck KH, Lilienthal J. Rhythm or rat...»72, «Wyse DG, Waldo AL, DiMarco JP ym. A comparison of ...»73, «Van Gelder IC, Hagens VE, Bosker HA ym. A comparis...»74, «Carlsson J, Miketic S, Windeler J ym. Randomized t...»75, «Opolski G, Torbicki A, Kosior DA ym. Rate control ...»76, «Roy D, Talajic M, Nattel S ym. Rhythm control vers...»77. Se även Avstå klokt-rekommendationen «Eteisvärinän rytminsiirto lieväoireisilla iäkkäillä potilailla»1: Undvik kardioversion av förmaksflimmer hos äldre patienter med lindriga symtom.
- För personer i arbetsför ålder lönar det sig i allmänhet att göra kardioversion en gång, även om patienten är symtomfri.
- Andra faktorer som talar för frekvenskontroll är
- kontrollerbarhet av symtom med läkemedel som minskar kammarresponsen
- snabbt återfall av förmaksflimmer (mindre än 1–2 månader efter kardioversion) trots profylaktisk behandling
- stort vänster förmak: det är osannolikt att kardioversionen lyckas och sinusrytmen bevaras om diametern av vänster förmak är över 5 cm «McNamara RL, Tamariz LJ, Segal JB ym. Management o...»65
- förmaksflimret varar utan avbrott i mer än 6–12 månader
- låg fysisk aktivitet.
- Rytmkontroll är det primära alternativet oberoende av patientens underliggande sjukdomar om
- svåra symtom (EHRA 3–4) eller hemodynamiska problem konstateras trots medicinering som minskar kammarfrekvensen
- responsen på profylaktisk behandling av rytmrubbningar är bra
- vänster förmak är normalstort
- rytmrubbningen har varat i mindre än 6 månader
- patienten är fysiskt aktiv.
- I följande stycken presenteras arytmiläkemedel enligt Vaughan-Williams indelning (bild «Rytmihäiriölääkkeiden jako Vaughan-Williamsin mukaan»7).

Rytmihäiriölääkkeiden jako Vaughan–Williamsin mukaan. Osalla lääkkeistä on useamman kuin yhden ryhmän mukaisia vaikutuksia. Digoksiini ja vernakalantti eivät sovi suoraan mihinkään näistä ryhmistä. Suluissa olevat lääkkeet ovat saatavana Suomessa ainoastaan erityisluvalla.
© Suomalainen Lääkäriseura Duodecim
Helhetsvård av förmaksflimmer
- Delområdena för helhetsvården av förmaksflimmer presenteras i tabellen «Helhetsvård av förmaksflimmer...»5.
- Det viktigaste med tanke på prognosen är en god behandling av underliggande sjukdomar och förebyggande av tromboemboliska komplikationer.
| 1. God behandling av underliggande sjukdomar och eliminering av predisponerande och utlösande faktorer för rytmrubbningar | |
| 2. Förebyggande av tromboemboliska komplikationer | |
|
|
| 3. Frekvenskontroll eller optimering av kammarfrekvensen | |
|
|
| 4. Rytmkontroll | |
A. Kardioversion, dvs. återställande av sinusrytm
|
|
B. Upprätthållande av sinusrytm
|
|
Behandling av underliggande sjukdomar
- En sammanfattning av de vanligaste bakgrundsfaktorerna för förmaksflimmer och behandlingen
av dem presenteras i tabellen «Behandlingsmål och behandlingsformer för de vanligaste bakomliggande faktorerna till
förmaksflimmer....»6.
- Evidensbaserad diagnostik och behandling av dessa tillstånd behandlas närmare i God medicinsk praxis-rekommendationerna Högt blodtryck «Högt blodtryck»3, «Kohonnut verenpaine. Käypä hoito -suositus. Suomal...»78, Hjärtsvikt «Sydämen vajaatoiminta»4, «Sydämen vajaatoiminta. Käypä hoito -suositus. Suom...»79, Typ 2-diabetes «Typ 2-diabetes»5, «Tyypin 2 diabetes. Käypä hoito -suositus. Suomalai...»80, Fetma (barn, unga och vuxna) «Fetma (barn, unga och vuxna)»6, «Lihavuus (lapset, nuoret ja aikuiset). Käypä hoito...»81, Sömnapné «Sömnapné (obstruktiv sömnapné hos vuxna)»7, «Uniapnea (obstruktiivinen uniapnea aikuisilla). Kä...»82 och Tobaks- och nikotinberoende – profylax och behandling «Tobaks- och nikotinberoende – profylax och behandling»8, «Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito...»83
| Bakomliggande faktor | Målsättning för behandlingen | Behandlingsmetoder |
|---|---|---|
| * betablockerare, hämmare av angiotensinkonvertasenzymet (ACE), angiotensinreceptorblockerare (ATR), mineralokortikoidreceptorblockerare (MRA), kombination av ATR-blockerare och neprilycinhämmare, hämmare av natrium- och glukostransportprotein 2 (SGLT2). | ||
| Högt blodtryck | < 130 mmHg / 80 mmHg | ACE-hämmare/ATR-blockerare i allmänhet det primära alternativet |
| Hjärtsvikt | Undvikande av vätskeansamling Hantering av symtom |
Läkemedelbehandling* och övrig behandling enligt vårdrekommendationerna Optimal användning av diuretika |
| Typ 2-diabetes | HbA1c < 48-53 mmol/mol Fastesocker < 6-7 mmo/l | Diabetesmedicinering enligt vårdrekommendationerna (särskilt SGLT2-hämmare eller GLP-1-receptoragonister) |
| Fetma (obesitet) | BMI < 27 kg/m2 eller minst 10% viktminskning | Kostanvisningar Läkemedelsbehandling Fetmaoperation |
| Obstruktiv sömnapné | Minimering av apnéperioder | CPAP-behandling |
| Låg fysisk aktivitetsnivå | Individuell handledning för regelbunden motion | Motionsrecept |
| Överkonsumtion av alkohol | Överkonsumtion av alkohol | Handledning och kamratstöd |
| Rökning | Fullständig rökfrihet | Handledning och kamratstöd Läkemedelsbehandling av abstinenssymtom |
| Övriga bakomliggande faktorer | Tidig identifiering | Behandling enligt rekommendationerna |
Högt blodtryck och hjärtsvikt
- Effektiv behandling av högt blodtryck och hjärtsvikt minskar förekomsten av förmaksflimmer
och förhindrar återfall av förmaksflimmer.
- I en metaanalys av sju randomiserade studier minskade ACE-hämmare och ATR-blockerare förekomsten av förmaksflimmer hos patienter med hjärtsvikt och högt blodtryck med 43 %. «Madrid AH, Peng J, Zamora J ym. The role of angiot...»171.
- Målet med behandlingen av blodtrycket är systoliskt blodtryck < 130 mmHg och diastoliskt
blodtryck < 80 mmHg.
- Primära läkemedel är ACE-hämmare och ATR-blockerare som minskar förekomsten av förmaksflimmer vid högt blodtryck och hjärtsvikt «ACE:n estäjät ja angiotensiinireseptorin (AT) salpaajat saattavat vähentää eteisvärinän ilmaantumista vajaatoiminta- ja verenpainepotilailla.»C.
- Vid hjärtsvikt är det viktigt att optimera läkemedels- och apparatbehandlingen som förbättrar prognosen för hjärtsvikt och förhindra ansamlingen av överflödig vätska (svullnad, lungkongestion) med diuretika. Kateterablation av förmaksflimmer kan genomföras i vissa fall på utvalda patienter (se närmare nedan).
Diabetes
- Cirka 25 % av patienter med förmaksflimmer har typ 2-diabetes «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Dålig terapeutisk balans (stort HbA1c-värde) ökar förekomsten av förmaksflimmer.På motsvarande sätt förebygger god sockerbalans uppkomsten av förmaksflimmer, minskar desssymtom och förbättrar vårdresultaten av rytmkontroll.
- Diabetesläkemedlens inverkan på förmaksflimmer varierar.
- Den bästa evidensen vid förmaksflimmer är från SGLT2-hämmare och GLP-1-receptoragonister «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
Behandling av fetma
- Det finns ett tydligt samband mellan övervikt och förmaksflimmer och viktminskning
har en gynnsam inverkan på förekomsten och behandlingen av förmaksflimmer «Schnabel RB, Yin X, Gona P ym. 50 year trends in a...»174.
- Hos överviktiga minskar förekomsten av förmaksflimmer i direkt proportion till viktminskningen, men dess inverkan på patienternas prognos är kontroversiell ("obesity paradox") «Miller JD, Aronis KN, Chrispin J ym. Obesity, Exer...»175, «Nalliah CJ, Sanders P, Kottkamp H ym. The role of ...»176, «Cambeiro G, Cristina M, Mañero R ym. Review Of Obe...»177, «Goudis CA, Korantzopoulos P, Ntalas IV ym. Obesity...»178.
- Målet är BMI < 27 kg/m2 eller en viktminskning på minst 10 %.
Sömnapné
- Sömnapné ökar incidensen av förmaksflimmer och försämrar effekten av profylaktisk
behandling.
- CPAP-övertrycksbehandling kan förbättra effekten av förmaksflimrets behandling hos vissa patienter, men resultaten är motstridiga.
Dyslipidemi
- Dyslipidemi och dyslipidemimedicinering påverkar inte nämnvärt förekomsten och återfallsrisken
för förmaksflimmer «Yao Y, Liu F, Wang Y, ym. Lipid levels and risk of...»179.
- Å andra sidan har statiner en gynnsam effekt på kranskärlssjukdom och de kan minska förekomsten av förmaksflimmer efter en hjärtoperation, men forskningsresultaten är motstridiga «Savelieva I, Camm J. Statins and polyunsaturated f...»172.
Kost
- För patienter med förmaksflimmer rekommenderas hjärtvänlig kost «https://sydan.fi/sydantietoa/ruoka-ravitsemus/»1.
- Fiskoljepreparat hindrar enligt nuvarande uppfattning inte återfall av förmaksflimmer «Savelieva I, Camm J. Statins and polyunsaturated f...»172, «Kowey PR, Reiffel JA, Ellenbogen KA ym. Efficacy a...»173.
- Fiskoljor kan öka risken för blödningar om de används tillsammans med antikoagulationsbehandling.
Behandling av akut anfall
- Elkonvertering bör utföras omedelbart oberoende av rytmrubbningens varaktighet eller antikoagulationsbehandling om patientens hemodynamik kollapsar på grund av förmaksflimmer.
- Hos hemodynamiskt stabila patienter återvänder sinusrytmen spontant inom ett dygn
i nästan 70 % av fallen. En kardioversion av patienter med lindriga symtom är därmed
inte nödvändig omedelbart och i början kan man i stället koncentrera sig på god pulskontroll.
- För personer med låg eller medelhög risk för trombos (CHA2DS2VA ≤ 1) ska man dock inte vänta över 48 timmar på att sinusrytmen återställs, så att
man inte är tvungen att skjuta upp kardioversionen tills en effektiv antikoagulationsbehandling
har använts i minst 3 veckor.
- Man ska inte vänta över 24 timmar på att sinusrytmen återvänder spontant hos patienter utan antikoagulationsbehandling som löper hög risk för trombos (CHA2DS2VA ≥ 2), så att man inte behöver skjuta upp kardioversionen.
- Hos personer som använder permanent antikoagulationsbehandling vars medicinering är terapeutisk nivå kan en omedelbar kardioversion göras oberoende av rytmrubbningens längd.
- För personer med låg eller medelhög risk för trombos (CHA2DS2VA ≤ 1) ska man dock inte vänta över 48 timmar på att sinusrytmen återställs, så att
man inte är tvungen att skjuta upp kardioversionen tills en effektiv antikoagulationsbehandling
har använts i minst 3 veckor.
- Om orsaken till förmaksflimmer är en akut hjärtinfarkt, plötslig försämring av hjärtsvikt, hjärtmuskelinflammation, hypertyreos, elektrolytstörning eller någon annan faktor som kan behandlas, ska behandlingen först riktas mot den underliggande orsaken och sinusrytmen återställas först därefter «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoit...»71.
- Behovet av antikoagulationsbehandling ska bedömas även om sinusrytmen återställs spontant «Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä»8, «Antitromboottinen hoito eteisvärinässä»9.
- Behovet av antikoagulationsbehandling «Antikoagulationsbehandling (AK) vid akut förmaksflimmer (under 48 timmar)»10, «Val av antitrombotisk behandling vid förmaksflimmer»4 ska bedömas i samtliga fall.
- Permanent antikoagulationsbehandling av högriskpatienter (CHA2DS2VA ≥ 2) är motiverad även i dessa fall.
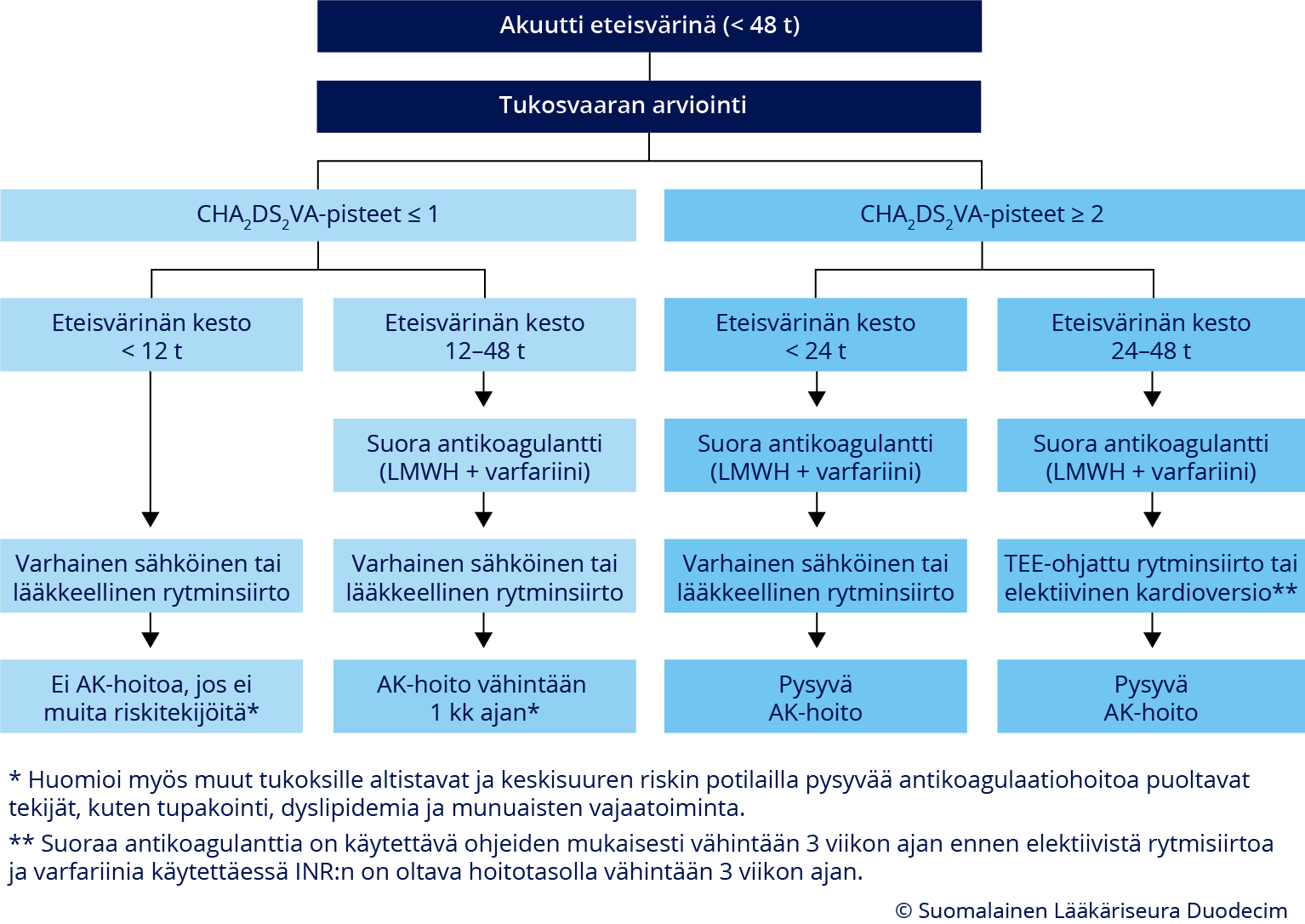
Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä. Akuutissa eteisvärinässä varhaisen rytminsiirron mahdollisuus arvioidaan tukosvaaratekijöiden ja rytmihäiriön keston perusteella. Pienen ja keskisuuren riskin potilailla eteisvärinän kardioversioon liittyvä tulosvaara on niin pieni, että antikoagulaatiohoitoa ei tarvita ennen eikä jälkeen rytminsiirron, jos rytmihäiriön kesto on alle 12 tuntia. Jos rytmihäiriön kesto on 12–48 tuntia myös heille annetaan ensimmäinen annos suoraa antikoagulantti (tai pieni molekyylistä hepariinia ja varfariina) jo ennen rytminsiirtoa, kuten suuren riskin potilaille ja rytminsiirron jälkeen AK-hoitoa jatketaan riskitekijöiden mukaan vähintään 1 kuukauden ajan tai pysyvästi (ks. tarkemmin teksti).
© Suomalainen Lääkäriseura Duodecim
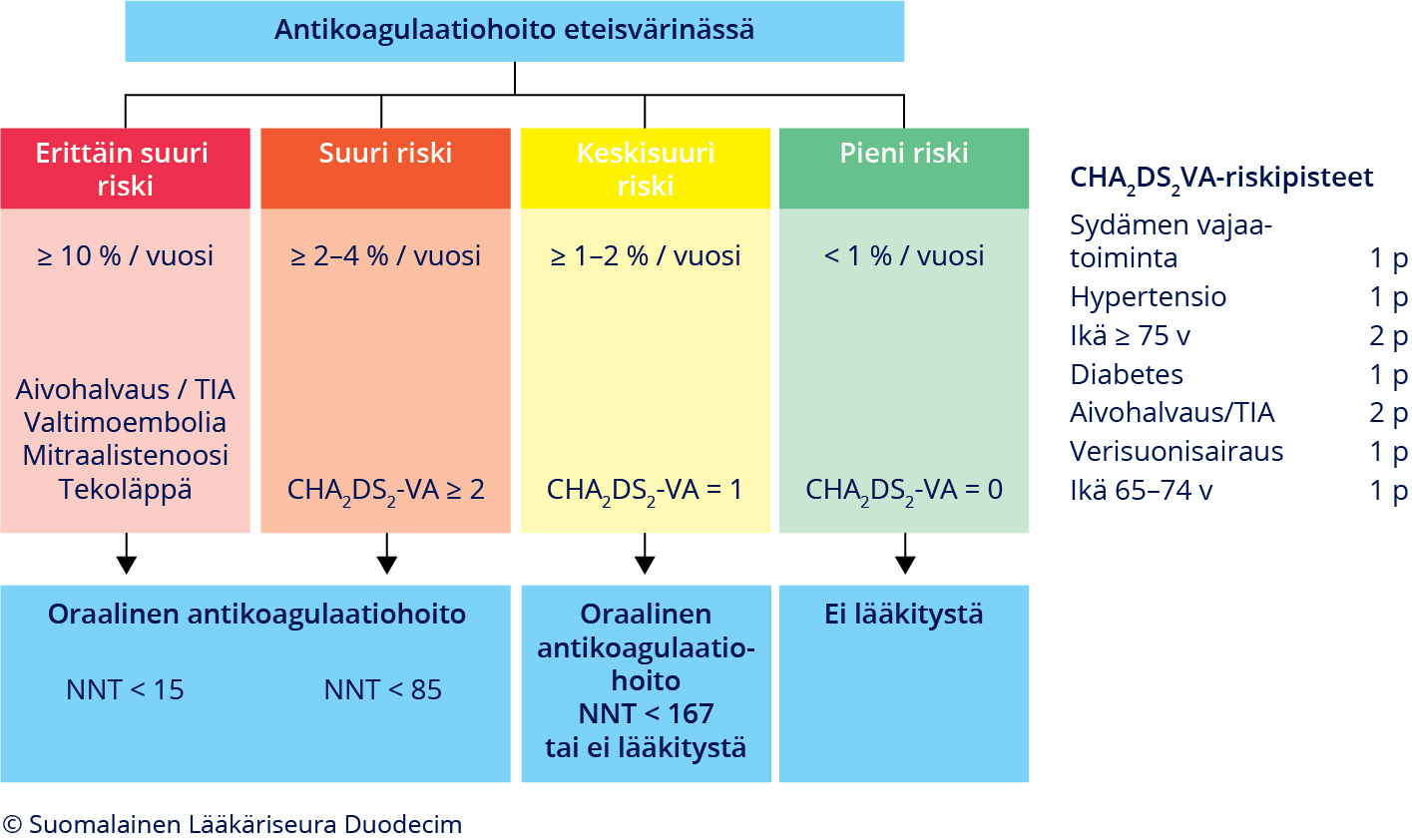
Antitromboottinen hoito eteisvärinässä. Pysyvän antikoaglaatiohoidon (AK) aiheellisuus arvioidaan suhteutettuna potilaan yksilölliseen aivohalvauksen vaaraan CHA2DS2VA-riskipisteytystä käyttämällä. Suuren riskin potilailla (CHA2DS2VA ≥ 2) AK-hoito (yleensä suora antikoaglantti) on aiheellinen lähes poikkeuksetta. Keskisuuren riskin potilailla (CHA2DS2VA = 1) AK-hoidon tarve arvioidaan yksilöllisesti. Siitä voidaan luopua, jos vuotovaara on suuri, potilas ei halua käyttää AK-hoitoa, vaaratekijä (esim. verenpaine) on hoidettu hyvin eikä potilaalla ole muita pienempiä vaaratekijöitä (mm. tupakointi, dyslipidemia, munuaisten vajaatoiminta). Pienen riskin potilaille (CHA2DS2VA = 0) antikoagulaatiohoitoa ei anneta, koska sen hyöty on heillä haittoja vähäisempi. ASA ja ADP-reseptorin salpaajat eivät sovellu heikon tehonsa ja haittavaikutustensa takia eteisvärinään liittyvien tukosten estoon. NNT (number needed to treat) on niiden potilaiden lukumäärä, joista yksi välttää aivohalvauksen lumelääkettä saaneisiin verrattuna yhden vuoden hoidon aikana (ks. lisätietoaineisto «Antitromboottisen hoidon valinta eteisvärinässä»). Vuotovaaran aiheuttavien toimenpiteiden ja leikkausten ajaksi AK-hoito voidaan tarvittaessa tauottaa suurimman riskin potilaita lukuun ottamatta.
© Suomalainen Lääkäriseura Duodecim

Antikoagulationsbehandling (AK) vid akut förmaksflimmer (< 48 timmar). Hos patienter med låg och medelhög risk kan kardioversion av akut förmaksflimmer göras utan föregående AK-behandling om rytmrubbningen varat mindre än 12 timmar. I övriga fall inleds antingen direkta orala antikoagulantia eller lågmolekylär heparinbehandling (LMWH) och warfarin redan före kardioversionen. Efter kardioversionen fortsätter AK-behandlingen enligt riskfaktorer i minst 1 månad eller permanent (se närmare i texten).
Bromsning av kammarresponsen vid akut förmaksflimmer
- I början av ett hemodynamiskt stabilt anfall av förmaksflimmer fokuserar man på att
lindra patientens symtom genom att minska kammarfrekvensen med läkemedel som bromsar
den atrioventrikulära överledningen (tabell «Intravenösa läkemedel som visat sig vara effektiva för att sänka kammarresponsen vid
akut förmaksflimmer...»7). Målet är en frekvens lägre än 110/min «Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoit...»71.
- Intravenösa läkemedel ger snabb effekt.
- Betablockerare sänker effektivt kammarfrekvensen vid akut förmaksflimmer genom blockering av det
adrenerga systemet «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Segal JB, McNamara RL, Miller MR ym. The evidence ...»84, «Snow V, Weiss KB, LeFevre M ym. Management of newl...»85, «Grönefeld GC, Hohnloser SH. Beta-blocker therapy i...»86.
- De är ett tryggt alternativ vid kranskärlssjukdom och rätt doserade även vid hjärtsvikt.
- Kalciumantagonister (verapamil och diltiazem) sänker kammarresponsen vid akut förmaksflimmer genom att
direkt påverka AV-knutan «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Segal JB, McNamara RL, Miller MR ym. The evidence ...»84, «Snow V, Weiss KB, LeFevre M ym. Management of newl...»85.
- De tolereras väl av patienter som inte har konstaterats ha hjärtsjukdomar.
- De ska dock användas med försiktighet vid hjärtsvikt eftersom de kan orsaka svår hypotension genom att försvaga pumpkraften i vänster kammare.
- Digoxin sänker kammarresponsen vid akut förmaksflimmer, men effekten börjar långsammare och
är sämre än med betablockerare och kalciumantagonister «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Segal JB, McNamara RL, Miller MR ym. The evidence ...»84.
- Vid akut hjärtsvikt (t.ex. lungödem) är digoxin säkrare för hemodynamiken än betablockerare eller kalciumantagonister.
- Kalciumantagonister, digoxin och betablockerare ökar den konkurrerande ledningen i retledningsbanan och rekommenderas därför inte för behandling av förmaksflimmer hos patienter med konstaterad preexcitation av kammarna (deltavåg).
- Amiodaron sänker kammarresponsen vid akut förmaksflimmer genom blockering av både det adrenerga
systemet och långsamma kalciumkanaler «Singh BN. Antiarrhythmic actions of amiodarone: a ...»87, «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88
- Amiodaron är inte det primära läkemedlet för en sänkning av kammarresponsen vid akut förmaksflimmer, även om extrakardiella biverkningar och proarytmi är sällsynta vid kortvarig användning.
- Tack vare sin knappa negativa inotropiska effekt är amiodaron ofta ett bra alternativ för behandling av postoperativa, kritiskt sjuka eller annars hemodynamiskt instabila patienters förmaksrelaterade rytmrubbningar «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Clemo HF, Wood MA, Gilligan DM ym. Intravenous ami...»89.
- Amiodaron bromsar även överledningen i accessoriska retledningsbanor varför det med eftertanke även kan användas vid WPW-syndrom.
- Dronedaron vid sänkning av kammarresponsen vid akut förmaksflimmer har inte undersökts.
- På grund av sina allvarliga biverkningar är det kontraindicerat vid kroniskt förmaksflimmer, även om det effektivt sänker kammarresponsen «Page RL, Hamad B, Kirkpatrick P. Dronedarone. Nat ...»90, «Hoy SM, Keam SJ. Dronedarone. Drugs 2009;69:1647-6...»91.
- Sotalol sänker kammarresponsen, men ska inte användas för detta ändamål på grund av risken för torsade de pointes.
- Ibutilid och vernakalant påverkar inte kammarfrekvensen «Murray KT. Ibutilide. Circulation 1998;97:493-7 ...»92, «Cheng JW. Vernakalant in the management of atrial ...»93.
- Läkemedel i grupp I medför med undantag av WPW-syndromet ingen nytta för reglering av kammarrespons «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Vid förmaksflimmer kan de paradoxalt nog höja kammarresponsen genom att sänka förmaksfrekvensen.
- Vid WPW-syndrom sänker de kammarresponsen genom att förhindra överledning i den accessoriska retledningsbanan.
- Samtidig användning av betablockerare och kalciumantagonister rekommenderas inte för att minska kammarresponsen vid akut förmaksflimmer. Däremot kan digoxin användas med både betablockerare och kalciumantagonist.
| Läkemedel | Rekommenderad dos |
|---|---|
| Betablockerare | |
| Esmolol | Startdos 10–50 mg som snabb injektion, fortsatt infusion 1–4 mg/min enligt pulsfrekvens och blodtryck |
| Metoprolol | 5 mg som långsam injektion; kan upprepas 2–3 gånger var femte minut |
| Kalciumantagonister | |
| Verapamil | 2,5–5 mg som långsam injektion; upprepas vid behov upp till en totaldos av 10 mg |
| Övriga läkemedel | |
| Digoxin | 0,25–0,5 mg som långsam injektion; kan upprepas 2–3 gånger med 1–2 timmars mellanrum (total dos högst 1 mg/dygn) |
| Amiodaron | Startdos 150–300 mg som infusion på 10–60 minuter, fortsatt infusion 1 200–1 800 mg/dygn |
| I icke-brådskande situationer kan även preparat som administreras oralt användas för frekvenskontroll. | |
Kardioversion
- Elkonvertering bör göras genast om patientens hemodynamik kollapsar på grund av förmaksflimmer.
- I övriga fall bedöms behovet av kardioversion individuellt enligt anvisningarna ovan (se punkten Val av vårdlinje «A1»2).
- Vid akut förmaksflimmer (< 24-48 timmar) beror behovet av antikoagulationsbehandling
på övriga trombosriskfaktorer och rytmrubbningens längd «Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä»8.
- Om antalet trombosriskfaktorer eller rytmrubbningens längd är oklar, är det säkrast att inleda antikoagulationsbehandling.
- För patienter med hög risk (CHA2DS2VA ≥ 2) påbörjas antingen en peroral direkt antikoagulant eller lågmolekylärt heparin och warfarin före kardioversionen och antikoagulationsbehandlingen fortsätter permanent.
- Vid användning av warfarin fortsätter det enligt vikten doserade lågmolekylära heparinet tills INR är på terapeutisk nivå «Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä»8.
- Risken för trombos hos patienter med låg och medelhög risk (CHA2DS2VA ≤ 1) är så liten att kardioversionen kan göras utan antikoagulationsbehandling om rytmrubbningen varat under 12 timmar. Om rytmrubbningen varat i 12–48 timmar inleds antikoagulationsbehandling före kardioversionen, såsom för patienter med hög risk, och den fortsätter beroende på riskfaktorerna i minst en månad eller permanent.
- Vid långvarigt förmaksflimmer (över 48 timmar) eller förmaksflimmer med oklar längd
förutsätter kardioversion något av följande: «Nagarakanti R, Ezekowitz MD, Oldgren J ym. Dabigat...»94, «Piccini JP, Stevens SR, Lokhnygina Y ym. Outcomes ...»95, «Flaker G, Lopes RD, Al-Khatib SM ym. Efficacy and ...»96, «Cappato R, Ezekowitz MD, Klein AL ym. Rivaroxaban ...»97, «Caldeira D, Costa J, Ferreira JJ ym. Non-vitamin K...»98:
- Direkta orala antikoagulantia (apixaban, dabigatran, edoxaban, rivaroxaban) har använts regelbundet i minst 3 veckor.
- Antikoagulationsbehandling med warfarin har varit på terapeutisk nivå (INR > 2) i minst 3 veckor före kardioversionen.
- Inga intrakardiella tromber observeras vid ultraljudsundersökning av hjärtat via esofagus eller vid datortomografi av hjärtat.
Elkonvertering
- Elkonvertering kan användas både vid behandling av akut förmaksflimmer och elektivt.
- Vid förmaksflimmer som varat i under 48 timmar är kardioversion effektivt i över 90 % av fallen..
- Vid långvarigt förmaksflimmer försämras effekten av kardioversionen och därför ska onödiga fördröjningar undvikas vid elektiv kardioversion.
- Vid elkonvertering återställs sinusrytmen genom en till QRS-komplexet synkroniserad
bifasisk likströmschock under lätt anestesi (bild «Elkonvertering»11). Se artikeln Sähköisen rytminsiirron suoritus i Lääkärin käsikirja «Sähköisen rytminsiirron suoritus»4 (kräver åtkomsträtt).
- Fördelarna med elkonvertering jämfört med läkemedel är att den har en god effekt och är trygg «Sähköinen rytminsiirto on lääkkein tehtyä rytminsiirtoa tehokkaampi ja turvallinen.»A.
- Vid elkonvertering rekommenderas man direkt använda maximal energi istället för att börja med mindre effekt och sedan gradvis öka «Schmidt AS, Lauridsen KG, Torp P ym. Maximum-fixed...»99.
- Om sinusrytmen inte återställs med maximal energi kan man
- överväga att ge ibutilid (1 mg som 10 minuters infusion), förutsatt att det inte finns kontraindikationer för det och sedan upprepa kardioversionsförsöket under samma anestesi «Oral H, Souza JJ, Michaud GF ym. Facilitating tran...»100
- påbörja arytmimedicinering oralt och upprepa kardioversionsförsöket senare när läkemedlets effekt har stabiliserats (antikoagulationen ska vara på terapeutisk nivå) «Marcus GM, Sung RJ. Antiarrhythmic agents in facil...»101, «Van Noord T, Van Gelder IC, Crijns HJ. How to enha...»102.
- Elkonvertering är kontraindicerad om
- orsaken till förmaksflimret kan behandlas (t.ex. elektrolytstörning, digitalisförgiftning eller svår hypertyreos ska korrigeras före kardioversionen)
- patienten har en svår funktionsstörning i sinus- eller atrioventrikulärknutan och inte har pacemaker
- rytmen varierar spontant mellan sinusrytm och förmaksflimmer (arytmiläkemedel kan användas).

Elektriciteten styrs bäst genom hjärtat om en av defibrilleringselektroderna placeras på patientens rygg (apex-posterior eller anterior-posterior). Om det inte finns en elektrod som kan placeras på patientens rygg tillgänglig, rekommenderas det att man sätter den ena elektroden vid hjärtspetsen och den andra uppe, en aning till höger om bröstbenet (apex-anterior). Hos kvinnor får elektroder inte placeras ovanpå bröstet. Tillräckligt med pasta ska läggas under elektroderna och handelektroderna ska tryckas tillräckligt kraftigt mot huden. Vid kardioversion används en bifasisk defibrilliering och redan vid första defibrilleringen används apparatens maximala effekt. Ett nytt kardioversionsförsök kan göras genast när blodtrycket och förmaksflimmerrytmen har stabiliserats, dvs. i praktiken cirka en minut efter föregående försök. Vid kardioversion av pacemakerpatient placeras elektroderna så att axeln mellan dem är tvärs över pacemakern och hjärtspetsaxeln. För patienter med implanterbar defibrillator (ICD) är det säkrast att göra en kardioversion av förmaksflimmer genom att programmera ICD:n till att ge en synkroniserad intrakardiell defibrillering i lätt anestesi. Om detta inte fungerar, görs kardioversionen på samma sätt som hos pacemakerpatienter.
Bildkälla: Heikkilä J et al. (red.) Kardiologia. Kustannus Oy Duodecim 2008, s. 544.
Farmakologisk kardioversion
- Farmakologisk kardioversion har god effekt vid akut förmaksflimmer, men ska inte användas
vid elektiv kardioversion eftersom läkemedlen snabbt förlorar sin effekt när förmaksflimret
blir långvarigt «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Vid farmakologisk kardioversion behövs varken anestesi eller föregående fasta, vilket gör det lättare att genomföra den än en elkonvertering.
- Nackdelarna är en sämre effekt än elkonvertering «Sähköinen rytminsiirto on lääkkein tehtyä rytminsiirtoa tehokkaampi ja turvallinen.»A, risken för proarytmi och andra läkemedelsbiverkningar.
- Anvisningar för genomförande av en farmakologisk kardioversion presenteras i tabell «Genomförande av farmakologisk kardioversion...»8.
- De läkemedel som idag används för kardioversion av förmaksflimmer presenteras i tabell «Läkemedel som används vid kardioversion av akut förmaksflimmer....»9.
- Flekainid «Flekainidi palauttaa sinusrytmin akuutissa eteisvärinässä tehokkaammin kuin lumelääke.»A är effektivare än placebo vid kardioversion av förmaksflimmer.
- Oralt administrerat flekainid lämpar sig också för användning inom primärvården om hjärtat tidigare har konstaterats vara friskt.
- Kammarrelaterade proarytmier är sällsynta, men för att undvika paradoxal ökning av kammarresponsen rekommenderas att patienten ges betablockerare eller något annat läkemedel som bromsar den atrioventrikulära överledningen före flekainiddosen «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Flekainid kan också efter övervägande användas vid ett förmaksflimmeranfall i samband med WPW-syndrom, eftersom det bromsar överledningen i den accessoriska retledningsbanan «Crozier I. Flecainide in the Wolff-Parkinson-White...»103.
- Flekainid ska inte användas vid kardioversion av förmaksflimmer «Raatikainen MJP, Sigurd B. Atrial fibrillation - t...»104 om
- rytmrubbningen har ett samband med akut hjärtinfarkt eller försämrad hjärtsvikt
- patienten har konstaterats ha hjärtinfarkt eller hjärtsvikt
- patienten har konstaterats ha en funktionsstörning i sinusknutan, ett andra eller tredje gradens AV-block eller grenblock (eller QRS-komplexet har breddats i övrigt) och det inte är möjligt att pacemakerstimulera hjärtat
- patienten har förmaksfladder (ökar risken för 1:1-atrioventrikulär överledning).
- De vanligaste biverkningarna av flekainid är «Capucci A, Villani GQ, Aschieri D ym. Safety of or...»105, «Aliot E, De Roy L, Capucci A ym. Safety of a contr...»106, «Kishore AG, Camm AJ. Guidelines for the use of pro...»107
- lindriga neurologiska symtom såsom yrsel och synstörningar
- övergående blodtrycksfall
- paradoxal ökning av kammarresponsen
- bradykardi som följer efter återställd sinusrytm.
- Intravenöst vernakalant är effektivare än placebo vid kardioversion av akut (< 48 timmar) förmaksflimmer «Suonensisäisesti annettu vernakalantti on lumelääkettä tehokkaampi kääntämään eteisvärinän sinusrytmiin.»A. Effekten försämras tydligt vid förmaksflimmer som varat över 72 timmar.
- Vernakalant blockerar ultrasnabba kalium- och natriumkanaler i hjärtmuskelcellerna, vilket gör att det i huvudsak påverkar förmaken och att QT-tiden inte förlängs avsevärt «Naccarelli GV, Wolbrette DL, Samii S ym. Vernakala...»108.
- Fördelen är en snabb effekt: sinusrytmen återställs i genomsnitt 11 minuter efter att infusionen inletts «Roy D, Pratt CM, Torp-Pedersen C ym. Vernakalant h...»109, «Kowey PR, Dorian P, Mitchell LB ym. Vernakalant hy...»110.
- De vanligaste biverkningarna är övergående smakkänningar, domningssymtom, illamående och nysningar «Naccarelli GV, Wolbrette DL, Samii S ym. Vernakala...»108
- Allvarliga biverkningar är sällsynta, men hypotoni är möjlig.
- Vernakalant är kontraindicerat vid svår hjärtsvikt, aortastenos och vid ett färskt kranskärlssjukdomsanfall.
- Amiodaron är effektivare än placebo vid kardioversion av förmaksflimmer, men dess effekt är
långsammare än hos andra läkemedel som används för detta ändamål «Amiodaroni palauttaa sinusrytmin akuutissa eteisvärinässä tehokkaammin kuin lumelääke.»B.
- Amiodaron kan också selektivt användas för behandling av förmaksrelaterade rytmrubbningar hos postoperativa, kritiskt sjuka eller annars hemodynamiskt instabila patienter «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Clemo HF, Wood MA, Gilligan DM ym. Intravenous ami...»89.
- Karakteristiska extrakardiella biverkningar vid långvarig amiodaronbehandling är sällsynta vid akut behandling.
- Ibutilid är effektivare än placebo vid kardioversion av akut förmaksflimmer «Ibutilidi on lumelääkettä tehokkaampi eteisvärinän rytminsiirrossa.»A.
- Fördelen med ibutilid är dess goda effekt på förmaksfladder «Raatikainen MJ, Lindgren K. Uusien ryhmän III lääk...»111.
- På grund av risken för torsade de pointes är det skäl att begränsa användningen av ibutilid till specialister som är insatta i behandlingen av rytmrubbningar.
- Ibutilid är kontraindicerat om patienten har diagnostiserats med sjuk sinusknuta, andra eller tredje gradens atrioventrikulärt block, polymorf kammartakykardi, hypokalemi eller om den korrigerade QT-tiden (QTc) är över 0,44 s eller kammarfrekvensen under 50/min «Murray KT. Ibutilide. Circulation 1998;97:493-7 ...»92, «Raatikainen MJ, Lindgren K. Uusien ryhmän III lääk...»111.
- Det finns inga bevis på betablockerares effekt vid kardioversion av akut förmaksflimmer, men de lindrar symtomen genom att sänka kammarresponsen.
- Kalciumantagonister «Kalsiuminestäjät eivät ilmeisesti palauta sinusrytmiä akuutissa eteisvärinässä.»B, digoxin och sotalol «Suonensisäisesti tai suun kautta annettu sotaloli ei ole merkitsevästi parempi kuin lumelääke akuutin eteisvärinän rytminsiirrossa (alle 7 vuorokautta).»B är ineffektiva vid kardioversion av förmaksflimmer, men de kan lindra symtomen genom
att sänka kammarresponsen.
- Kalciumantagonister och digoxin kan förlänga durationen av förmaksflimmeranfallet och provocera återfall «McNamara RL, Tamariz LJ, Segal JB ym. Management o...»65, «Snow V, Weiss KB, LeFevre M ym. Management of newl...»85, «Raatikainen MJ. Is verapamil a double-edged sword ...»112.
- Behandling där patienten självständigt tar flekainid genast när rytmrubbningen har
börjat ("pill in the pocket") kräver specialistbedömning «Alboni P, Botto GL, Baldi N ym. Outpatient treatme...»113.
- En förutsättning är att man på sjukhus tidigare genomfört en kardioversion med samma preparat.
| 1. Se till att det finns tillräckliga övervakningsmöjligheter (EKG-övervakning, blodtrycksmätning, mätning av syremättnad) och beredskap att behandla eventuell proarytmi (defibrillator). |
| 2. Koppla upp patienten till EKG-monitorn. |
| 3. Öppna en intravenös infart och påbörja vid behov vätsketillförsel med till exempel fysiologisk koksaltlösning. |
| 4. Sänk kammarresponsen med betablockerare (eller kalciumantagonist eller digoxin). |
| 5. Välj det läkemedel som ska användas för kardioversionen individuellt så att du beaktar för- och nackdelarna med olika läkemedel. |
|
| 6. Efter att sinusrytm återställts fortsätter EKG-övervakningen enligt läkemedlet i minst 3–4 timmar, varefter patienter i gott skick kan skrivas ut. |
| 7. Om sinusrytm inte återställs efter administreringen av läkemedlet ska patienten hänvisas till elkonvertering. Nytt försök med farmakologisk kardioversion med hjälp av ett annat preparat bör undvikas. |
| Läkemedel | Rekommenderad dos | Evidensgrad |
|---|---|---|
| Har konstaterats vara effektiva | ||
| Flekainid | Intravenöst 1–2 mg/kg som 10–30 minuters infusion (högst 150 mg) Oral engångsdos 300 mg |
«Flekainidi palauttaa sinusrytmin akuutissa eteisvärinässä tehokkaammin kuin lumelääke.»A |
| Vernakalant | Intravenöst 3 mg/kg som 10 minuters infusion (högst 339 mg), vid behov efter 15 minuter 2 mg/kg som 10 minuters infusion (högst 226 mg) | «Suonensisäisesti annettu vernakalantti on lumelääkettä tehokkaampi kääntämään eteisvärinän sinusrytmiin.»A |
| Amiodaron | Startdos 150–300 mg intravenöst, fortsatt infusion 1 200–1 800 mg/dygn1) | «Amiodaroni palauttaa sinusrytmin akuutissa eteisvärinässä tehokkaammin kuin lumelääke.»B |
| Ibutilid | Intravenöst 1 mg/10 min (kan upprepas en gång efter 10 minuter) | «Ibutilidi on lumelääkettä tehokkaampi eteisvärinän rytminsiirrossa.»A |
| Otillräcklig information om effekten | ||
| Betablockerare | ||
| Dronedaron | ||
| Har konstaterats ineffektiva | ||
| Digoxin | Ineffektivt både oralt och intravenöst | |
| Kalciumantagonist | Ineffektiv både oralt och intravenöst | «Kalsiuminestäjät eivät ilmeisesti palauta sinusrytmiä akuutissa eteisvärinässä.»B |
| Sotalol | Ineffektivt både oralt och intravenöst | «Suonensisäisesti tai suun kautta annettu sotaloli ei ole merkitsevästi parempi kuin lumelääke akuutin eteisvärinän rytminsiirrossa (alle 7 vuorokautta).»B |
| 1) I särskilda fall kan även större doser användas. | ||
Antikoagulationsbehandling i samband med kardioversion av förmaksflimmer
- Även kardioversion av akut förmaksflimmer kan vara förknippad med betydande trombosrisk.
- Trombosrisken beror på hur länge förmaksflimmeranfallet varat och de trombosriskfaktorer som bedöms med hjälp av CHA2DS2VA-poängsättningen «Airaksinen KE, Grönberg T, Nuotio I ym. Thromboemb...»114.
- Risken för tromboemboliska komplikationer är särskilt stor under de första dagarna efter kardioversionen. Mediantiden för uppkomsten av trombos är 2 dygn efter kardioversionen «Airaksinen KE, Grönberg T, Nuotio I ym. Thromboemb...»114.
- För att undvika tromboser efter en tidig kardioversion ges alla högriskpatienter den
första dosen direkt antikoagulant (eller lågmolekylärt heparin och warfarin) redan
före kardioversionen och antikoagulationsbehandlingen fortsätter permanent.
- Effekten av direkta orala antikoagulanter börjar snabbt och lågmolekylärt heparin behövs inte. «Nagarakanti R, Ezekowitz MD, Oldgren J ym. Dabigat...»94, «Piccini JP, Stevens SR, Lokhnygina Y ym. Outcomes ...»95, «Flaker G, Lopes RD, Al-Khatib SM ym. Efficacy and ...»96, «Cappato R, Ezekowitz MD, Klein AL ym. Rivaroxaban ...»97, «Caldeira D, Costa J, Ferreira JJ ym. Non-vitamin K...»98, «Steffel J, Verhamme P, Potpara TS ym. The 2018 Eur...»116.
- Vid användning av warfarin fortsätter det lågmolekylära heparinet med en behandlingsdos enligt vikten tills INR är på terapeutisk nivå «European Heart Rhythm Association., European Assoc...»115. Behandlingsdoserna för lågmolekylära hepariner presenteras i tilläggsmaterialet «Pienimolekyylisten hepariinien annostelu eteisvärinän rytmisiirron yhteydessä»2.
- För patienter med låg risk kan kardioversion göras utan antikoagulationsbehandling om rytmrubbningen varat i mindre än 12 timmar. Om rytmrubbningen varat i 12–48 timmar ska anvisningarna på bilden «Antikoagulaatiohoito (AK) akuutissa (alle 48 tuntia kestäneessä) eteisvärinässä»8 följas.
- Vid förmaksflimmer som pågått i mer än 48 timmar eller under okänd tid orsakar en kardioversion som genomförts utan antikoagulationsbehandling en embolirisk
på 5–7 % «Bjerkelund CJ, Orning OM. The efficacy of anticoag...»117, «Arnold AZ, Mick MJ, Mazurek RP ym. Role of prophyl...»118 och en kardioversion bör inte utföras, om
- direkta orala antikoagulantia (apixaban, dabigatran, edoxaban, rivaroxaban) inte har använts regelbundet i minst 3 veckor eller
- warfarinbehandlingen inte har varit på terapeutisk nivå (INR > 2,0) i minst 3 veckor eller
- intrakardiella tromber inte har uteslutits genom ultraljudsundersökning av hjärtat via esofagus eller via datortomografi av hjärtat (se närmare nedan).
- Efter elektiv kardioversion fortsätter antikoagulationsbehandlingen (se närmare punkten Antikoagulationsbehandling «A2»3) enligt följande:
- Hos patienter med hög risk fortsätter antikoagulationsbehandlingen bestående (CHA2DS2VA ≥ 2), även om sinusrytm uppnås «European Heart Rhythm Association., European Assoc...»115, «Thibault B, Talajic M, Dubuc M ym. Thromboembolic ...»119.
- Antikoagulationsbehandlingen av patienter med låg och medelhög risk (CHA2DS2VA = 1) fortsätter i minst 1 månad eller permanent. Faktorer som ökar risken för trombos och stöder permanent antikoagulationsbehandling är bland annat rökning, dyslipidemi och njursvikt.
- Det är mycket viktigt att säkerställa att INR hålls över 2,0 även efter kardioversionen hos personer som använder warfarin.
- Vid kardioversion av förmaksfladder följs samma anvisningar som vid förmaksflimmer «Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoit...»71, «European Heart Rhythm Association., European Assoc...»115, «Biblo LA, Yuan Z, Quan KJ ym. Risk of stroke in pa...»120.
Ultraljudsundersökning av hjärtat via esofagus vid kardioversion av förmaksflimmer
- Kardioversion kan även utföras utan föregåendes antikoagulationsbehandling vid förmaksflimmer
som varat i mer än 48 timmar, om ingen intrakardiell tromb upptäcks vid ultraljudsundersökning
av hjärtat via esofagus (TEE) «Eteisvärinän rytminsiirto voidaan tehdä ilman edeltävää antikoagulaatiohoitoa, jos ruokatorven kautta tehtävässä sydämen kaikututkimuksessa (TEE) ei havaita sydämen sisäistä verihyytymää.»A, (bild «Kardioversion av förmaksflimmer på basis av ultraljudsundersökning via esofagus»12).
- Kardioversion som görs efter TEE-undersökning kan övervägas om det är nödvändigt att snabbt återställa sinusrytmen på grund av svåra symtom (EHRA 3–4).
- För personer med lindriga symtom (EHRA 1) och "ekonomiskt" förmaksflimmer är TEE-undersökning och tidig kardioversion i allmänhet inte nödvändiga.
- En intrakardiell tromb «Sydämensisäinen trombi»13 är en absolut kontraindikation, medan "rökfenomen" (savuilmiö «Sydämen kaikututkimuksessa havaittava savuilmiö»14och långsamt flöde i vänster förmaksöra «Sydämen kaikututkimuksessa havaittava eteiskorvakkeen hidastunut tyhjenemisnopeus»15 är relativa kontraindikationer för tidig kardioversion «Troughton RW, Asher CR, Klein AL. The role of echo...»37, «Saarela E, Koskela V, Strandberg M ym. Ruokatorven...»67
- En TEE-styrd kardioversion påskyndar sinusrytmens återhämtning, vilket
- förhindrar en remodellering av förmaken så att de gynnar rytmrubbningar
- förbättrar möjligheterna för en lyckad kardioversion «Saarela E, Koskela V, Strandberg M ym. Ruokatorven...»67, «Corrado G, Santarone M, Beretta S ym. Early cardio...»121, «Klein AL, Grimm RA, Murray RD ym. Use of transesop...»122 «Weigner MJ, Thomas LR, Patel U ym. Early cardiover...»123, «Roijer A, Eskilsson J, Olsson B. Transoesophageal ...»124, men effekten på bevarandet av sinusrytmen är osäker «Bartel T, Erbel R, Acute Trial Investigators.. Tra...»125, «Klein AL, Murray RD, Grimm RA. Role of transesopha...»126
- minskar kostnaderna för vården «Seto TB, Taira DA, Tsevat J ym. Cost-effectiveness...»127, «Klein AL, Murray RD, Becker ER ym. Economic analys...»128.

Kardioversion av förmaksflimmer kan göras utan föregående antikoagulationsbehandling om ingen intrakardiell tromb upptäcks vid transesofageal ultraljudsundersökning (TEE). Före en tidig kardioversion inleds antikoagulationsbehandling med antingen direkta orala antikoagulantia eller lågmolekylärt heparin (LMWH) och warfarin. I det senare fallet fortsätter man när sinusrytmen återställs tills INR är på terapeutisk nivå. Vid användning av direkta orala antikoagulantia behövs inte LMWH. Antikoagulationsbehandlingen fortsätter enligt andra riskfaktorer i minst en månad eller permanent. TEE-undersökning förutsätter lång erfarenhet av den som utför undersökningen, vilket begränsar användningen.

Sydämensisäinen trombi. Ruokatorven kautta tehdyssä sydämen kaikututkimuksessa havaittu trombi on ehdoton vasta-aihe varhaiselle rytminsiirrolle. Rintakehän päältä tehtävän sydämen tavallisen kaikututkimuksen erottelukyky ei riitä varhaisen rytminsiirron ohjaukseen.

Sydämen kaikututkimuksessa havaittava savuilmiö. Ruokatorven kautta tehdyssä sydämen kaikututkimuksessa havaittava “savuilmiö” on merkki lisääntyneestä trombivaarasta, mutta ei ehdoton vasta-aihe varhaiselle rytminsiirrolle.

Sydämen kaikututkimuksessa havaittava eteiskorvakkeen hidastunut tyhjenemisnopeus. Ruokatorven kautta tehdyssä sydämen kaikututkimuksessa havaittava eteiskorvakkeen hidastunut tyhjenemisnopeus on merkki lisääntyneestä trombivaarasta, mutta ei ehdoton vasta-aihe varhaiselle rytminsiirrolle.
Profylaktisk behandling (rytmkontroll)
- Ihållande förmaksflimmer återkommer efter kardioversion utan behandling hos upp till
80–90 % av patienterna under det följande året «Lévy S, Breithardt G, Campbell RW ym. Atrial fibri...»129.
- Risken för återfall vid paroxysmalt förmaksflimmer är större än vid ihållande förmaksflimmer.
- Profylaktisk behandling ska övervägas om patienten tolererar förmaksflimmret dåligt.
- Profylaktisk medicinering är i allmänhet långvarig, men i vissa fall kan även kortvarig medicinering användas (t.ex. flekainid 4 veckor efter kardioversion).
- Kortvarig medicinering minskar tidiga relapser men är inte lika effektiv som långvarig medicinering «Kirchhof P, Andresen D, Bosch R ym. Short-term ver...»131.
- Tidig profylaktisk behandling förbättrar behandlingens effekt «Kirchhof P, Camm AJ, Goette A ym. Early Rhythm-Con...»130.
- Profylaktisk behandling planeras individuellt genom att även ta i beaktande underliggande bidragande sjukdomar samt möjligheterna till invasiv behandling (tabell «Helhetsvård av förmaksflimmer...»5).
Profylaktisk medicinering
- Valet av profylaktisk medicinering påverkas i synnerhet av patientens övriga hjärtsjukdomar (bild «Val av profylaktisk medicinering vid förmaksflimmer»16) och medicineringen för dessa «Raatikainen MJ. Rytmihäiriölääkkeiden kliininen kä...»132.
- Behandling med betablockerare kan i allmänhet inledas inom primärvården efter de grundläggande undersökningar som nämns i tabell «Rekommenderade undersökningar för förmaksflimmerpatienter...»4.
- Användningen av egentliga arytmiläkemedel (amiodaron, dronedaron, flekainid och sotalol)
ska inledas av en kardiolog eller en specialist i internmedicin, men läkare inom primärvården
kan oftast ansvara för patienternas uppföljning.
- Användningen av flekainid, dronedaron och amiodaron kan i allmänhet inledas polikliniskt efter tillräckliga hjärtundersökningar (tabell «Rekommenderade undersökningar för förmaksflimmerpatienter...»4).
- Det rekommenderas att användningen av sotalol inleds i telemetriövervakning på sjukhus.
- Arytmiläkemedelsdoserna vid profylax av förmaksflimmer och faktorer som påverkar doseringen
presenteras i tabell «Dosering av de vanligaste arytmiläkemedlen vid profylaktisk behandling av förmaksflimmer.
Vid profylaktisk behandling lönar det sig att alltid välja långverkande preparat som
tas en gång per dygn när ett sådant finns tillgängligt....»10.
- Innan dosen ändras eller medicineringen avslutas på grund av utebliven effekt ska man säkerställa att läkemedlets effekt har hunnit stabiliseras «Raatikainen MJ. Rytmihäiriölääkkeiden kliininen kä...»132.
- Objektiv evidens på läkemedlets effekt fås till exempel genom långtidsregistrering av EKG eller genom ett kliniskt belastningsprov.
- Koncentrationen av läkemedelssubstansen korrelerar dåligt med den kliniska responsen, men koncentrationsbestämningar kan användas till exempel vid misstanke om förgiftning eller läkemedelsinteraktioner.
- Arytmimedicinering förhindrar endast sällan förmaksflimmer helt och hållet.
- Ett realistiskt mål är att lindra subjektiva symtom och minska antalet anfall.
- De mest problematiska biverkningarna i hjärtat är proarytmi (tabell «Proarytmiska effekter av arytmiläkemedel som används i behandlingen av förmaksflimmer samt behandling och förebyggande av dessa...»11) och försämring av hjärtsvikt till följd av negativ inotropisk effekt.
- De vanligaste extrakardiella biverkningarna av arytmimedicinering presenteras i tabell «Extrakardiella biverkningar av arytmiläkemedel vid behandling av förmaksflimmer. Alla arytmiläkemedel kan dessutom orsaka allergiska reaktioner som uppträder som olika hudsymtom eller andra symtom. Läkemedel inom parentes är tillgängliga endast med specialtillstånd i Finland....»12.
| Läkemedel | Rekommenderad underhållsdos/dygn | Evidensgrad | Dosändring vid hjärtsvikt | ||
|---|---|---|---|---|---|
| Njurar | Lever | Hjärta | |||
| Har konstaterats effektiva | |||||
| Flekainid | 100–200 mg x 1 | «Flekainidi estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A | Minska | Kontraindicerat | |
| Betablockerare1) | «Beetasalpaajat näyttävät vähentävän eteisvärinän uusiutumista rytminsiirron jälkeen verrattuna lumelääkkeeseen.»B | ||||
| atenolol | 50–100 mg x 1 | Minska | |||
| bisoprolol | 5–10 mg x 1 | ||||
| karvedilol | 25–50 mg x 1 | ||||
| metoprolol | 95–190 mg x 1 | Minska | |||
| Amiodaron | 100–200 mg x 1 | «Amiodaroni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A | Minska | ||
| Dronedaron2) | 400 mg x 2 | «Dronedaroni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A | Kontraindicerat | ||
| Sotalol | 80–160 mg x 2 | «Sotaloli estää kohtauksittaisen ja jatkuvan (persistoivan) eteisvärinän uusiutumisen rytminsiirron jälkeen tehokkaammin kuin lumelääke.»A | Minska | Var försiktig med användning | |
| Har visat sig vara ineffektiva eller har undersökts otillräckligt | |||||
| Diltiazem | «Kalsiuminestäjät yksinään eivät estä eteisvärinän uusiutumista.»C | Minska | Undvik användning | ||
| Verapamil | «Kalsiuminestäjät yksinään eivät estä eteisvärinän uusiutumista.»C | Minska | Undvik användning | ||
| Digoxin | Minska | ||||
| 1) Betablockerare ska användas försiktigt vid hjärtsvikt och dosen ska ökas långsamt
enligt tillverkarens anvisningar. 2) Dronedaron är kontraindicerat vid svår njur- och leversvikt, men vid lindriga funktionsstörningar behöver dosen inte ändras. |
|||||
| Proarytmi | Typiska patogener | Kliniska drag | Vård och förebyggande |
|---|---|---|---|
| Förmaksrelaterad takykardi | |||
| Förmaksfladder med kammarrespons 1:1 | Läkemedel i grupp IA och IC | Snabb och jämn kammarrespons (150–220/min), ofta brett QRS-komplex | Fördröjning av atrioventrikulära överledningen (betablockerare, kalciumantagonist
eller digoxin) Kateterablation av förmaksfladder |
| Snabbare kammarrespons vid förmaksflimmer | Läkemedel i grupp IA och IC | Kammarresponsen blir snabbare och ibland blir förmaksflimret till förmaksfladder | Fördröjning i atrioventrikulära överledningen |
| Kammarrelaterad takykardi | |||
| Monomorf kammartakykardi | Läkemedel i grupp IC | Utlösande faktor är vanligen ischemi eller hjärtsvikt. Takykardi kan vara nästan kontinuerlig (dominerande) och relativt långsam |
Undvik användning om patienten har ett strukturellt hjärtfel. Kateterablation |
| Torsade de pointes | Läkemedel i grupp IA och III | Polymorf kammartakykardi, där polariteten i QRS-komplexet varierar spolformat, "kort-lång-kort" -startsekvens, ökning i QT-tiden och QT-dispersionen | Korrigering av elektrolytstörningar, magnesium, isoprenalin, antitakykardipacing och i skydd av den betablockerare eller kalciumantagonist |
| Övriga | |||
| Sinusbradykardi | Betablockerare, sotalol, kalciumantagonister, digoxin, amiodaron och dronedaron | Särskilt när sinusrytmen återställs | Avslutande av medicinering, vid behov pacing |
| Atrioventrikulärt block | Betablockerare, sotalol, kalciumantagonister, digoxin, amiodaron och dronedaron, flekainid | Långsam och jämn kammarrespons vid förmaksflimmer | Avslutande av medicinering, vid behov pacing |
| Läkemedel | Allmänna biverkningar | Sällsynta biverkningar |
|---|---|---|
| Flekainid | yrsel, synstörningar | illamående, kräkningar |
| (Propafenon) | förstoppning, illamående, domningar i munnen och muntorrhet, besk smak, hypotension | eksem, leukopeni, leverskada, anorexi, extrapyramidala symtom, synrubbningar, sömnstörningar |
| Betablockerare | nedsatt fysisk prestationsförmåga, trötthet, kyla i extremiteterna, försämrad klaudikation, sömnstörningar | bronkusspasm, hypoglykemi, depression, muskelkramper, impotens |
| Amiodaron | störningar i sköldkörtelfunktionen, förhöjda levervärden, känslighet för ljus, yrsel, sömnstörningar, illamående, kräkningar, hornhinnegrumling | alveolit, lungfibros, leverskada, perifer neuropati, yrsel, sömnstörningar, illamående, kräkningar |
| Dronedaron | störningar i matsmältningsorganen (diarré, kräkningar, illamående, buksmärtor, dyspepsi), eksem, trötthet, svaghet | ljuskänslighet, smakstörningar |
| Ibutilid | illamående | |
| Sotalol | samma som hos betablockerare | illamående, kräkningar, diarré |
| Vernakalant | smakstörningar, taktila hallucinationer, yrsel, bradykardi, hypotension, illamående, kräkningar, muntorrhet, nysningar, smärta vid infusionsstället | sveda, luktstörningar, sömnighet, irritation i ögonen, överledningsstörningar, andnöd, diarré, smärta i extremiteterna |
| Diltiazem | vristsvullnad, hudrodnad, huvudvärk, illamående, förstoppning, yrsel | eksem, leverskada |
| Verapamil | förstoppning, vristsvullnad, huvudvärk, yrsel, hypotension | hudrodnad, huvudvärk, illamående, kräkningar, yrsel |
| Digoxin | aptitlöshet, illamående, kräkningar, diarré | gynekomasti, trombocytopeni, eosinofili, synrubbningar, trötthet, huvudvärk |

Valet av profylaktiskt läkemedel påverkas väsentligt av patientens övriga (hjärt)sjukdomar. Inom öppenvården är det primära läkemedelsalternativet i allmänhet betablockerare. Primära egentliga arytmiläkemedel vid s.k. lone atrial fibrillation är läkemedel i grupp IC (flekainid). Kinidin och disopyramid lämpar sig särskilt för behandling av vagalt förmaksflimmer. Strukturell hjärtsjukdom är en kontraindikation för arytmiläkemedel i grupp I. Användningen av Sotalol begränsas av risken för torsde de pointes. Amiodaron och dronedaron orsakar många extrakardiella biverkningar, vilket begränsar användningen av dem. ACE-hämmare och angiotensin II-receptorns (AR-) blockerare verkar förhindra att förmaksflimmer uppkommer vid hjärtsvikt och blodtryckssjukdom. Läkemedel inom parentes är numera tillgängliga endast med specialtillstånd i Finland.
Läkemedel i grupp II (betablockerare)
- Betablockerare förhindrar förmaksflimmer effektivare än placebo «Beetasalpaajat näyttävät vähentävän eteisvärinän uusiutumista rytminsiirron jälkeen verrattuna lumelääkkeeseen.»B.
- De är särskilt effektiva hos patienter med förhöjt blodtryck «Van Noord T, Tieleman RG, Bosker HA ym. Beta-block...»133och hjärtsvikt «Meng F, Yoshikawa T, Baba A ym. Beta-blockers are ...»134.
- De är också trygga efter en hjärtinfarkt «Kühlkamp V, Bosch R, Mewis C ym. Use of beta-block...»135.
- De stärker effekten av andra arytmiläkemedel och minskar den proarytmi som de orsakar «Grönefeld GC, Hohnloser SH. Beta-blocker therapy i...»86.
- De kan göra symtomatiskt förmaksflimmer symtomfritt genom att sänka kammarresponsen «Page RL, Reiffel JA, Tavel ME. Asymptomatic atrial...»136, «Page RL. beta-blockers for atrial fibrillation: mu...»137.
- Avvikande från de egentliga arytmiläkemedlen kan behandlingen inledas inom primärvården.
Arytmiläkemedel i grupp IC
- Flekainid förhindrar återfall av förmaksflimmer effektivare än placebo «Flekainidi estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A eller läkemedel i grupp IA «Lévy S, Breithardt G, Campbell RW ym. Atrial fibri...»129, «Naccarelli GV, Dorian P, Hohnloser SH ym. Prospect...»138, «Lee SH, Chen SA, Chiang CE ym. Comparisons of oral...»139, «Grey E, Silverman DI. Efficacy of type 1C antiarrh...»140.
- Flekainid är säkert vid behandling av essentiellt förmaksflimmer men kontraindicerat
vid hjärtinfarkt, symtomatisk kranskärlssjukdom, hjärtsvikt och andra svåra strukturella
hjärtsjukdomar.
- Hos patienter som haft en hjärtinfarkt ökar flekainid dödligheten cirka 2,5 gånger jämfört med placebo «Echt DS, Liebson PR, Mitchell LB ym. Mortality and...»141.
- Hos personer med friskt hjärta påverkar flekainid inte dödligheten och allvarliga biverkningar är sällsynta «Hughes MM, Trohman RG, Simmons TW ym. Flecainide t...»142, «Chimienti M, Cullen MT Jr, Casadei G. Safety of lo...»143, «Anderson JL, Platt ML, Guarnieri T ym. Flecainide ...»144, «Wehling M. Meta-analysis of flecainide safety in p...»145.
- För personer med blodtryckssjukdom kan flekainid användas om kammarväggarna inte är hypertrofiska (över 14 mm) «Joglar JA, Chung MK, Armbruster AL, ym. 2023 ACC/A...»146.
- Flekainid kan också efter övervägande användas vid behandling av förmaksflimmer i samband med WPW-syndrom «Crozier I. Flecainide in the Wolff-Parkinson-White...»103.
- Innan medicinering i grupp IC inleds
- ska hjärtats strukturer och funktion undersökas med ultraljud
- kliniskt belastningsprov (eller bilddiagnostisk undersökning av kranskärlen) kan göras om inte hjärtmuskelischemi kan uteslutas tillräckligt säkert (bild «Inledning av arytmimedicinering i grupp IC och uppföljning av patienten»17).
- För att minska de proarytmiska effekterna (tabell «Proarytmiska effekter av arytmiläkemedel som används i behandlingen av förmaksflimmer samt behandling och förebyggande av dessa...»11) rekommenderas att flekainid kombineras med en betablockerare eller något annat läkemedel som fördröjer den atrioventrikulära överledningen «Raatikainen MJP, Sigurd B. Atrial fibrillation - t...»104.
- Propafenon «Propafenoni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A är idag tillgängligt endast med specialtillstånd.

Innan medicineringen i grupp IC inleds ska man säkerställa att hjärtat är strukturellt friskt med en ultraljudsundersökning. Ett kliniskt belastningsprov görs alltid om kranskärlssjukdom inte annars kan uteslutas med säkerhet. I specialfall kan man efter att medicineringen stabiliserats använda ett belastningstest för att hitta patienter som är känsliga för proarytmi och de med långsam metaboli. VES = kammarextraslag.
Läkemedel i grupp III (kaliumkanalblockerare)
- Amiodaron förhindrar återfall av förmaksflimmer betydligt bättre än placebo «Amiodaroni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A.
- I randomiserade dubbelblindstudier har amiodaron visat sig vara effektivare än dronedaron «Le Heuzey JY, De Ferrari GM, Radzik D ym. A short-...»147, sotalol, propafenon «Roy D, Talajic M, Dorian P ym. Amiodarone to preve...»148 och kinidin «Vitolo E, Tronci M, Larovere MT ym. Amiodarone ver...»149.
- Enligt metaanalysen verkar amiodaron också vara effektivare än flekainid vid profylaktisk behandling av förmaksflimmer «Zarembski DG, Nolan PE Jr, Slack MK ym. Treatment ...»150.
- Användning av amiodaron kräver många försiktighetsåtgärder och noggrann uppföljning «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Raatikainen MJ. Rytmihäiriölääkkeiden kliininen kä...»132, «Singh BN. Amiodarone: the expanding antiarrhythmic...»151, «Siddoway LA. Amiodarone: guidelines for use and mo...»152.
- Långtidsanvändningen försvåras av många extrakardiella biverkningar och samverkningar med andra läkemedel (t.ex. warfarin och direkta orala antikoagulantia), varför amiodaron inte kan betraktas som ett förstahandsläkemedel vid behandlingen av förmaksflimmer «European Heart Rhythm Association., European Assoc...»115, «Connolly SJ. Evidence-based analysis of amiodarone...»153.
- Å andra sidan orsakar den sällan proarytmi «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Hohnloser SH, Klingenheben T, Singh BN. Amiodarone...»154 och det kan även användas hos personer som haft en hjärtinfarkt och hos personer med hjärtsvikt «Julian DG, Camm AJ, Frangin G ym. Randomised trial...»155, «Cairns JA, Connolly SJ, Roberts R ym. Randomised t...»156, «Doval HC, Nul DR, Grancelli HO ym. Randomised tria...»157, «Deedwania PC, Singh BN, Ellenbogen K ym. Spontaneo...»158.
- Vid profylaktisk behandling av förmaksflimmer ska man sträva efter att använda en så liten dos som möjligt (100–200 mg/dygn) efter laddningsdosen (t.ex. 600 mg/dygn i 2 veckor) för att undvika allvarliga biverkningar.
- Dronedaron (400 mg x 2/dygn) förhindrar återfall av förmaksflimmer effektivare än placebo «Dronedaroni estää eteisvärinän uusiutumista tehokkaammin kuin lumelääke.»A.
- Dronedaron har en effekt i alla kategorier enligt Vaughan-Williams, precis som amiodaron.
- Dronedaron har sämre effekt än amiodaron «Le Heuzey JY, De Ferrari GM, Radzik D ym. A short-...»147, «Piccini JP, Hasselblad V, Peterson ED ym. Comparat...»159 och eventuellt även andra arytmiläkemedel «Lafuente-Lafuente C, Mouly S, Longas-Tejero MA ym....»160, «Freemantle N, Lafuente-Lafuente C, Mitchell S ym. ...»161.
- Utöver den förebyggande effekten för återfall av rytmrubbningen minskar dronedaron
uppenbarligen behovet av sjukhusvård och dödligheten hos utvalda patienter med förmaksflimmer «Dronedaroni saattaa parantaa valikoitujen eteisvärinäpotilaiden ennustetta ja vähentää sairaalahoidon tarvetta.»B.
- Prognoseffekten är tydligast hos personer med kranskärlssjukdom.
- Dronedaron är kontraindicerat
- vid hjärtsvikt (ökar dödligheten) «Køber L, Torp-Pedersen C, McMurray JJ ym. Increase...»162
- vid kroniskt förmaksflimmer (ökar dödligheten) «Connolly SJ, Camm AJ, Halperin JL ym. Dronedarone ...»163
- hos patienter med konstaterad toxicitet i levern eller lungorna under amiodaronbehandling
- under dabigatranbehandling.
- Dronedaronmedicinering förutsätter omsorgsfullt val av patient och regelbunden uppföljning
(se bild «Dronedaronin käyttö eteisvärinän estohoidossa»18).
- Innan medicineringen inleds ska andra behandlingsalternativ övervägas.
- Medicineringen ska inledas av en specialist och följas upp enligt specialistens anvisningar.
- Under behandlingen ska hjärtrytmen (EKG med 6 månaders mellanrum) och pumpförmågan samt leverfunktionen följas upp regelbundet.
- Medicineringen ska avslutas om förmaksflimret blir kroniskt eller om det förekommer andra kontraindikationer.
- Sotalol förhindrar återfall av förmaksflimmer efter kardioversionen effektivare än placebo «Sotaloli estää kohtauksittaisen ja jatkuvan (persistoivan) eteisvärinän uusiutumisen rytminsiirron jälkeen tehokkaammin kuin lumelääke.»A.
- Effekten enligt grupp III framkommer endast vid stora doser (över 160 mg/dygn). I mindre doser fungerar läkemedlet som en vanlig betablockerare.
- I jämförande undersökningar har sotalol varit lika effektivt i förebyggandet av förmaksflimmer som kinidin «Juul-Möller S, Edvardsson N, Rehnqvist-Ahlberg N. ...»164, propafenon «Bellandi F, Simonetti I, Leoncini M ym. Long-term ...»165 och bisoprolol «Plewan A, Lehmann G, Ndrepepa G ym. Maintenance of...»166 men sämre än amiodaron «Roy D, Talajic M, Dorian P ym. Amiodarone to preve...»148.
- På grund av risken för torsade de pointes «Brendorp B, Pedersen O, Torp-Pedersen C ym. A bene...»167borde användningen av sotalol begränsas till specialister som är insatta i behandlingen av rytmrubbningar.

Dronedaronin käyttö eteisvärinän estohoidossa. Dronedaronin turvallinen käyttö eteisvärinän estohoidossa edellyttää huolellista potilasvalintaa ja säännöllistä seurantaa. Ennen hoidon aloittamista on sydämen kaikututkimuksen avulla varmistettava, ettei potilaalla ole sydämen vajaatoimintaa. Lisäksi tehdään maksan ja munuaisten toimintakokeet. Jos seerumin alaniiniaminotransferaasin (S-ALAT) pitoisuus on yli kolminkertainen normaalialueen ylärajaan verrattuna, dronedaronia ei pidä aloittaa. Jos ALAT-arvo suurenee seurannan aikana ≥ 3 × normaalin ylärajan, seurantakoe on tehtävä 2–3 vuorokauden kuluessa. Jos arvo on edelleen suurentunut, lääkitys on lopetettava. Dronedaroni ei juuri vaikuta munuaisten toimintaan, mutta seerumin kreatiniinipitoisuus saattaa suurentua, koska lääke kilpailee munuaisissa kreatiniinin erittymisen kanssa. Kreatiniinipitoisuus mitataan ennen hoidon aloittamista ja viikon kuluttua sen jälkeen. Jos arvo on suurentunut, mittaus toistetaan 2 viikon kohdalla. Kliininen arvio on tehtävä enintään 6 kuukauden välein ja samalla on otettava myös EKG. Maksa-arvoja (ALAT) seurataan aluksi tiheään määrittämällä ALAT hoidon aloituksen jälkeen 1 viikon sekä 1, 2, 3, 4, 5, 6, 9 ja 12 kk:n kuluttua. Sen jälkeen kokeet voidaan ottaa harvemmin. Jos seurannan aikana todetaan sydämen vajaatoimintaan tai keuhkojen toimintahäiriöön viittaavia oireita tai löydöksiä, sydämen kaikututkimus tai keuhkojen toimintakokeet on tehtävä viivyttelemättä ja tarvittaessa lääkitys on lopetettava. Dronedaroni on vasta-aiheinen pysyvässä eteisvärinässä, ja sen käyttö on lopetettava, jos eteisvärinä kroonistuu hoidon aikana. Käytännössä myös INR-arvojen sekä digoksiinin pitoisuuden seurantaa on tehostettava dronedaronin aloituksen jälkeen.
© Suomalainen Lääkäriseura Duodecim
Arytmiläkemedel i grupp IA
- Kinidin «Kinidiini vähentää eteisvärinän ilmaantumista merkittävästi enemmän kuin lumelääke tai lääkkeetön hoito ja yhtä tehokkaasti kuin IC-luokan lääkkeet ja sotaloli, mutta huonommin kuin amiodaroni.»A och disopyramid «Disopyramidi estää paremmin toistuvia eteisvärinäkohtauksia kuin lumelääke ja yhtä hyvin kuin IC-luokan lääkkeet, mutta sen teho on huonompi kuin amiodaronin.»A som är tillgängliga endast med specialtillstånd används numera sällan vid profylaktisk
behandling av förmaksflimmer «Coplen SE, Antman EM, Berlin JA ym. Efficacy and s...»168.
- De har bäst effekt på vagalt förmaksflimmer.
- Typiska biverkningar är diarré orsakad av kinidin och muntorrhet, urinretention och förstoppning i samband med den kraftiga antikolinergiska effekten av disopyramid.
- Arytmiläkemedel i grupp IB (mexiletin och lidokain) används inte vid profylaktisk behandling av förmaksflimmer.
Läkemedel i grupp IV (kalciumantagonister)
- Verapamil och diltiazem hindrar inte återfall av förmaksflimmer «Kalsiuminestäjät yksinään eivät estä eteisvärinän uusiutumista.»C men de kan intensifiera effekten av andra arytmiläkemedel och minska risken för proarytmi «Patten M, Maas R, Bauer P ym. Suppression of parox...»169, «Fetsch T, Bauer P, Engberding R ym. Prevention of ...»170.
Digoxin
- Digoxin hindrar inte återfall av förmaksflimmer utan kan till och med öka och förlänga vagala förmaksflimmeranfall «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- Vid återfall av förmaksflimmer kan digoxin dock förhindra snabb kammarrespons, vilket talar för användning av läkemedlet hos sådana patienter som lider av hjärtsvikt och som har en dålig tolerans för andra läkemedel som gör slagfrekvensen långsammare «European Heart Rhythm Association., European Assoc...»115.
Pacemakerbehandling vid förmaksflimmer
- Pacemakerbehandling har inte kunnat påvisas förebygga återfall av förmaksflimmer «Tahdistinhoidon ei ole voitu osoittaa toimivan itsenäisesti eteisvärinän ehkäisyssä.»B.
- När insättningen av pacemaker är motiverad av andra orsaker kan man genom att välja
pacemakertyp påverka förekomsten av förmaksflimmer.
- Vid funktionsstörningar i sinusknutan lönar det sig att gynna förmakspacing och undvika kammarpacing «Jos potilaalla on todettu perinteinen tahdistinhoidon indikaatio, eteistahdistus näyttää vähentävän eteisvärinän ilmaantuvuutta verrattaessa kammiotahdistukseen.»B, «Andersen HR, Nielsen JC, Thomsen PE ym. Long-term ...»180, «Kerr CR, Connolly SJ, Abdollah H ym. Canadian Tria...»181, «Nielsen JC, Kristensen L, Andersen HR ym. A random...»182.
- Behandling av hjärtsvikt med pacemaker och retledningspacing kan förbättra funktionen i vänster kammare och minska mitralinsufficiens, vilket kan ha en gynnsam effekt på förmaksflimmer. «Vajaatoimintatahdistinhoito saattaa palauttaa sinusrytmin joillakin eteisvärinästä kärsivillä potilailla.»D.
- Pacemakerbehandling av patienter som har benägenhet för sinusbradykardi underlättar genomförandet av arytmimedicinering och kan därmed förhindra förmaksflimmer.
- Intrakardiella förmaksdefibrillatorer används inte längre «Burns JL, Sears SF, Sotile R ym. Do patients accep...»184, «Boodhoo LE, Mitchell AR, Sulke N. The clinical and...»185.
Kateterablation vid förmaksflimmer
- Målet med kateterablation är att minska patientens symtom och förbättra livskvaliteten.
- Allmänt taget förbättrar kateterablation inte prognosen för patienter med förmaksflimmer «Packer DL, Mark DB, Robb RA ym. Effect of Catheter...»186.
- Vid svår systolisk hjärtsvikt kan den dock förbättra prognosen för utvalda patienter «Packer DL, Mark DB, Robb RA ym. Effect of Catheter...»186, «Sohns C, Fox H, Marrouche NF, ym. Catheter Ablatio...»187, se God medicinsk praxis-rekommendationen Hjärtsvikt «Sydämen vajaatoiminta»4, «Sydämen vajaatoiminta. Käypä hoito -suositus. Suom...»79.
- Vid kateterablationsbehandling av förmaksflimmer isoleras de rytmrubbningshärdar som finns i lungvenernas rotområde från annan förmaksvävnad (isolation av lungvenerna) antingen parvis genom att göra en enhetlig ablationslinje med radiofrekvensenergi «Eteisvärinän katetriablaatiohoito»19 eller en i taget med en s.k. kryoballong eller pulsfältsablation «Eteisvärinän ablaatiohoito kryopallolla»20, «Eteisvärinän pulssikenttäablaatio (pulsed field ablation, PFA)»21.
- Huvudindikationen för kateterablation är paroxysmalt eller ihållande förmaksflimmer
med kraftiga symtom som inte reagerar på läkemedelsbehandling.
- Som förstahandsbehandling kan ablation övervägas för en person som har s.k lone atrial fibrillation, om personen så önskar «Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHR...»1, «Cosedis Nielsen J, Johannessen A, Raatikainen P ym...»188.
- Ablationsbehandling lämpar sig bäst för patienter
- som har paroxysmalt förmaksflimmer
- som inte konstaterats ha en betydande hjärtsjukdom
- vars vänster förmak inte är märkbart utvidgad (diameter under 5 cm)
- som konstateras ha rikligt med förmaksextraslag som infaller på T-vågen ("P-on-T"-fenomen) (bild «Extraslag som träffar T-vågen (P-on-T) och som är karakteristiska för fokalt förmaksflimmer»22).
- Kateterablation av förmaksflimmer förhindrar återfall av paroxysmalt och ihållande
förmaksflimmer effektivare än läkemedelsbehandling «Katetriablaatiohoito estää eteisvärinän uusiutumista tehokkaammin kuin lääkehoito.»A och förbättrar märkbart patienternas livskvalitet «Hakalahti A, Biancari F, Nielsen JC ym. Radiofrequ...»189, «Mark DB, Anstrom KJ, Sheng S ym. Effect of Cathete...»190, «Blomström-Lundqvist C, Gizurarson S, Schwieler J y...»191. Numera finns det evidens från uppföljningar på 5 år «Nielsen JC, Johannessen A, Raatikainen P ym. Long-...»192, «Raatikainen MJ, Hakalahti A, Uusimaa P ym. Radiofr...»193.
- Kateterablationsbehandlingen ger effekt hos 60–85 % av patienter med s.k. lone atrial fibrillation och hos vilka läkemedelsbehandling har visat sig vara otillräcklig «Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHR...»1, «European Heart Rhythm Association., European Assoc...»115, «Cappato R, Calkins H, Chen SA ym. Updated worldwid...»194, «Piccini JP, Lopes RD, Kong MH ym. Pulmonary vein i...»195, «Gjesdal K, Vist GE, Bugge E ym. Curative ablation ...»196, «Calkins H, Reynolds MR, Spector P ym. Treatment of...»197, «Blomström-Lundqvist C, Gizurarson S, Schwieler J y...»191.
- Det finns inga nämnvärda skillnader i effekten av radiofrekvensablation, kryoterapi och pulsfältsablation vid paroksysmalt förmaksflimmer «Schmidt M, Dorwarth U, Andresen D ym. Cryoballoon ...»198, «Reddy VY, Gerstenfeld EP, Natale A, ym. Pulsed Fie...»199.
- Vid strukturellt hjärtfel, långvarigt förmaksflimmer och hos tydligt överviktiga personer är resultaten av kateterablation sämre. För överviktiga rekommenderas viktminskning före ingreppet «Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHR...»1, «European Heart Rhythm Association., European Assoc...»115.
- Kostnaderna för ablationsbehandling är i början högre, men uppenbarligen redan om 3–5 år är de totala kostnaderna lägre än för läkemedelsbehandling «Weerasooriya R, Jaïs P, Le Heuzey JY ym. Cost anal...»200, «Andrikopoulos G, Tzeis S, Maniadakis N ym. Cost-ef...»201. Fördelen är störst bland unga patienter «Aronsson M, Walfridsson H, Janzon M ym. The cost-e...»202.
- Ablationsbehandling av förmaksflimmer är ett komplicerat elektrofysiologiskt ingrepp
med risk för sällsynta men allvarliga komplikationer «European Heart Rhythm Association., European Assoc...»115, «Cappato R, Calkins H, Chen SA ym. Updated worldwid...»194, «Spragg DD, Dalal D, Cheema A ym. Complications of ...»203.
- Komplikationerna är färre, men de är allvarligare än problemen i samband med läkemedelsbehandling «Calkins H, Reynolds MR, Spector P ym. Treatment of...»197.
- Allvarliga komplikationer är bland annat tamponad (1–2 %), lungvensstenos (under 1 %), tromboemboliska komplikationer (under 1 %), förlamning av diafragmanerven (1-2 %) och esofagusperforation (under 0,1 %).
- Biverkningarna av ablationsbehandling framträder i allmänhet snabbt efter ingreppet, men biverkningarna av läkemedelsbehandling kan komma fram först efter flera år.
- Antikoagulation vid ablationsbehandling av förmaksflimmer:
- Kateterablation är inget alternativ till antikoagulationsbehandling, utan vid antikoagulation följs samma principer som i andra patientgrupper.
- För att undvika tromboemboliska komplikationer i samband med ingreppet rekommenderas att även patienter med låg risk påbörjar direkta orala antikoagulantia senast 3 veckor före ingreppet (vid användning av warfarin ska INR vara på terapeutisk nivå i minst 3 veckor).
- Efter ingreppet fortsätter antikoagulationsbehandlingen för patienter med låg risk i 2–3 månader och för personer som löper stor risk för trombos (CHA2DS2VASc ≥ 2) rekommenderas permanent antikoagulationsbehandling.
- Närmare anvisningar om genomförandet av antikoagulationsbehandlingen ges av de sjukhus som utför ingreppen.
- Om utlösaren av förmaksflimmer är någon annan rytmrubbning (t.ex. atrioventrikulär-nodal
återkopplingstakykardi, atrioventrikulär återkopplingstakykardi, förmakstakykardi
eller förmaksfladder), kan kateterablationsbehandling av dessa även förhindra förmaksflimmer «European Heart Rhythm Association., European Assoc...»115, «Blomström-Lundqvist C, Scheinman MM, Aliot EM ym. ...»204.
- Kateterablation av förmaksfladder minskar förekomsten av förmaksflimmer men avlägsnar det inte helt «Nabar A, Rodriguez LM, Timmermans C ym. Effect of ...»205, «Ahvenvaara T, Uusimaa P, Huikuri HV, Raatikainen M...»206.
- Snabbt förmaksflimmer i samband med WPW-syndrom är livshotande. För sådana personer är det absolut nödvändigt att göra en kateterablation av retledningsbanan «European Heart Rhythm Association., European Assoc...»115, «Blomström-Lundqvist C, Scheinman MM, Aliot EM ym. ...»204.

Eteisvärinän katetriablaatiohoito. Kuvassa A nähdään elektroanatomista kartoituslaitteistoa (CartoTM) käyttämällä tehty kolmiulotteinen malli vasemmasta eteisestä ja keuhkolaskimoista takaapäin katsottuna. Keuhkolaskimot on merkitty välillisillä putkilla ja katetriablaatiokohteet punaisilla pallukoilla. Kuvassa B nähdään, kuinka sähköinen aktiviteetti häviää oikean puoleisesta yläkeuhkolaskimoista ablaation vaikutuksesta. Tämä on merkki siitä, että keuhkolaskimo on eristetty eikä sen sisällä sijaitseva rytmihäiriöpesäke pysty enää käynnistämään eteisvärinää. Myös muut laskimot tarkastettiin toimenpiteen aikana eikä niissä yhdessäkään havaittu sähköistä aktiviteettia, joka olisi pystynyt käynnistämään eteisvärinän.
kuva A © Pekka Raatikainen
kuva B © Suomalainen Lääkäriseura Duodecim

Eteisvärinän ablaatiohoito kryopallolla. Tässä menetelmässä kaikki keuhkolaskimot käsitellään erikseen ja tulos varmistetaan pallokatetrin lävitse keuhkolaskimon sisälle viedyllä sirkulaarisella diagnostisella katetrilla samaan tapaan kuin radiotaajuusenergialla tehdyssä ablaatiossa. Kuvassa näkyy kryopallo täytettynä vasemmassa yläkeuhkolaskimossa. Pallo tukkii suonen hyvin, sillä sen läpi ruiskutettu varjoaine ei vapaudu lainkaan eteisen puolella. Hyvä “okkluusio” on onnistuneen kryoablaation edellytys.
© Pekka Raatikainen
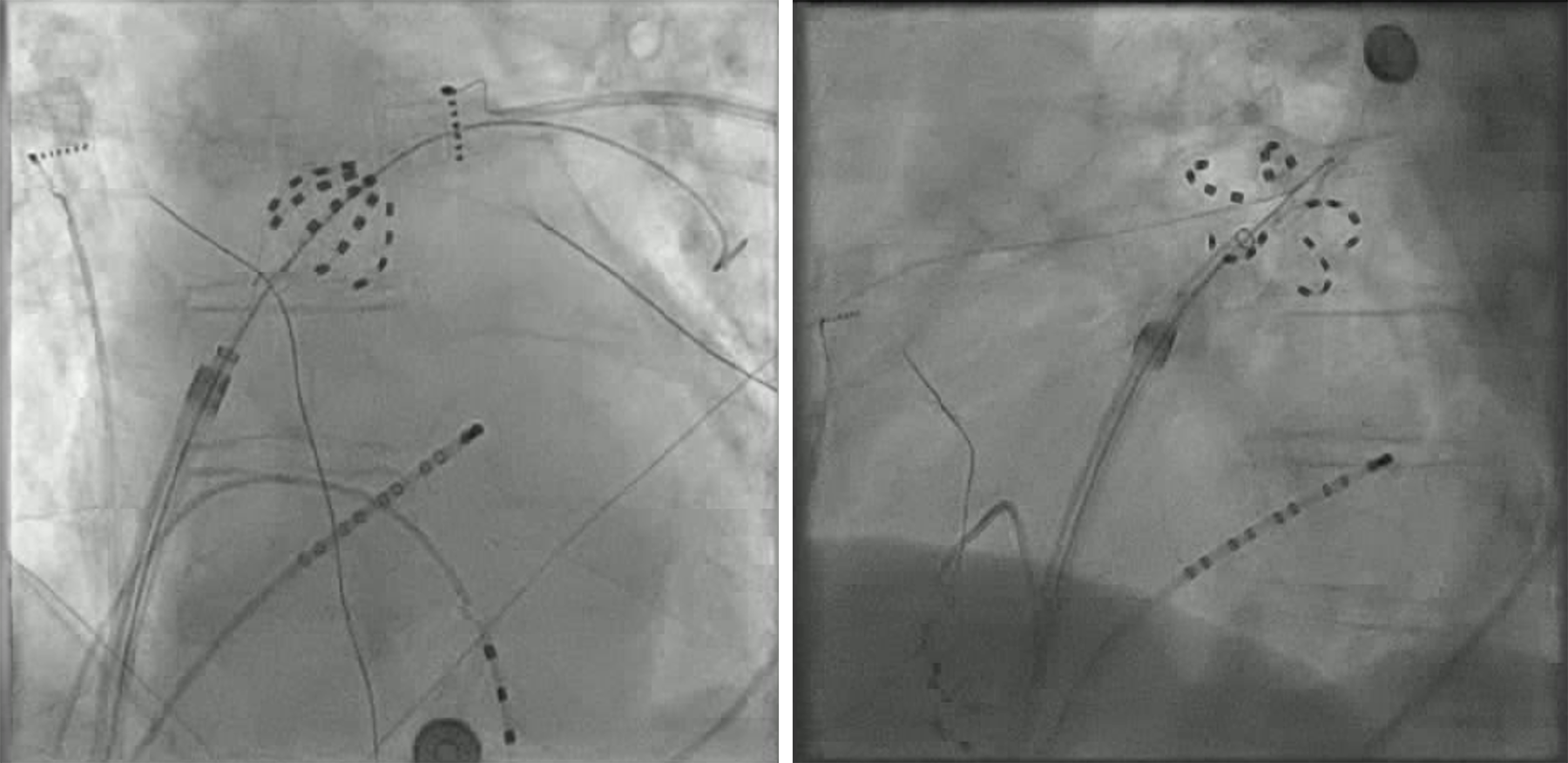
Eteisvärinän pulssikenttäablaatio (pulsed field ablation, PFA)
Kuvassa nähdään PFA-katetri vasemmassa yläkeuhkolaskimossa ensin ns. korimuodossa (AP-suunta) hieman laskimon sisäpuolelle ulottuen ja toisessa kuvassa sama katetri hieman laskimon suuaukon ulkopuolella ns. kukkamuodossa (LAO 60 -suunta). Tällä katetrilla keuhkolaskimot eristetään yksitellen tekemällä jokaiseen laskimoon vähintään kahdeksan lyhytkestoista (4 s) hoitoa. Menetelmän etuna on nopeuden lisäksi myös turvallisuus, sillä PFA-energia kohdistuu enimmäkseen sydänlihakseen ja vaara muiden rakenteiden, kuten palleahermon tai ruokatorven, vaurioitumisesta on pienempi kuin radiotaajuusenergialla tai jäädyttämällä tehtävässä ablaatiossa.
© Pekka Raatikainen

Extraslag som träffar T-vågen (P-on-T) och som är karakteristiska för fokalt förmaksflimmer. Dessa härstammar i allmänhet från lungvenerna och utlöser ofta paroxysmalt förmaksflimmer.
Kirurgisk behandling av förmaksflimmer
- Ett tilläggsingrepp i samband med hjärtkirurgi som syftar till att avlägsna förmaksflimmer
förhindrar effektivt återfall av förmaksflimmer «Sydänkirurgian yhteydessä tehtävä erillinen eteisvärinän poistoon suuntautuva lisätoimenpide estää eteisvärinän uusiutumista.»A.
- Under de senaste åren har man vid kirurgisk behandling av förmaksflimmer i stället för labyrintoperation (bild «Traditionell Cox labyrintoperation (MAZE-operation)»23), «Prasad SM, Maniar HS, Camillo CJ ym. The Cox maze ...»207 använt nästan enbart radiofrekvens- eller kryotekniker som har gjort åtgärden snabbare och säkrare «Cox JL. Cardiac surgery for arrhythmias. J Cardiov...»208, (bild «Kirurgisk epikardiell ablationsbehandling av förmaksflimmer»24).
- Kirurgisk behandling kan övervägas om en patient med förmaksflimmer genomgår en hjärtoperation
av någon annan orsak och efter att andra behandlingsformer visat sig vara resultatlösa
eller kontraindicerade hos utvalda patienter.
- Ett strukturellt hjärtfel är inget hinder för kirurgisk behandling av förmaksflimmer – tvärtom kan uppkomsten av förmaksflimmer påskynda operationsbeslutet vid mitralklaffdefekt.
- Allvarliga komplikationer är sällsynta, men i enstaka fall har kirurgisk ablation beskrivits orsaka perforationer i matstrupen «McLellan CS, Abdollah H, Brennan FJ ym. Atrial fib...»209 och kranskärlsförträngningar.
- Erfarenheterna av mini-invasiva åtgärder och åtgärder som utförs med hjälp av endoskopi samt s.k. hybridåtgärder är lovande. Dessa kan övervägas som den enda åtgärden om kateterablationsbehandlingen inte har gett resultat och symtomen fortfarande är svåra eller det finns skäl att avstå från transseptal kateterbehandling till exempel på grund av tidigare förslutning av en förmaksseptumdefekt «Boersma LV, Castella M, van Boven W ym. Atrial fib...»210, «Castellá M, Pereda D, Mestres CA ym. Thoracoscopic...»212.

I den traditionella Cox labyrintoperationen (MAZE-operation) skar kirurgen förmaket i mindre delar och sydde det ihop igen. Med denna metod har sinusrytmen återställts hos upp till 90 % av patienterna. Metoden är dock arbetsam och tidskrävande och den har till stor del slopats till förmån för kirurgisk ablationsbehandling.

Metoden är lättare att genomföra än vanlig MAZE-operation eftersom lesioner görs med radiofrekvensenergi, kryoterapi eller mikrovågsprob. Ingreppet kan också göras som en titthålsoperation som torde passa bättre för behandling av enbart förmaksflimmer.
Sänkning av kammarrespons vid kroniskt förmaksflimmer (frekvenskontroll)
- Om beslut fattas om kroniskt förmaksflimmer och frekvenskontroll är det bra att för
att förbättra följsamheten informera patienten om att
- prognosen är lika bra för patienter med lindriga symtom (EHRA 1–2) under frekvenskontrollen som under en farmakologisk rytmkontroll «Sykkeenhallinta on eteisvärinässä parempi vaihtoehto kuin rytminhallinta aivohalvauksien ja kokonaiskuolleisuuden suhteen, mutta hoidot ovat samanarvoisia kuolleisuuden ja potilaiden elämänlaadun suhteen.»A
- kroppen vänjer sig i allmänhet vid kroniskt förmaksflimmer genom optimering av pulsfrekvensen ("ekonomiskt flimmer") «Levy T, Walker S, Mason M ym. Importance of rate c...»213, «Van Gelder IC, Van Veldhuisen DJ, Crijns HJ ym. RA...»214.
- Vid kroniskt förmaksflimmer justeras kammarfrekvensen individuellt (bild «Frekvenskontroll vid kroniskt förmaksflimmer»25).
- Målet är att patienten är symtomfri och att kammarresponsen är under 110/min i vila.
- Patienter med symtom har nytta av strängare frekvenskontroll, där den målinriktade kammarresponsen är 60–80/min i vila och 90–115/min vid lätt ansträngning, såsom gång.
- Vid systolisk hjärtsvikt bör man att se till att kammarresponsen inte sänks för mycket.
- Genomförandet av frekvenskontrollen måste vid behov säkerställas genom långtidsregistrering
av EKG, ett kliniskt belastningstest eller båda.
- Ständigt för snabb kammarrespons (genomsnittlig pulsfrekvens över 110/min) kan leda till hjärtsvikt (s.k. takykardiomyopati) «Shinbane JS, Wood MA, Jensen DN ym. Tachycardia-in...»53.

Den medicinering som används för att sänka kammarresponsen väljs och dosen justeras individuellt så att patienten är symtomfri. Minimimålet för symtomfria patienter är att kammarresponsen är under 110/min i vila. Strängare pulsgränser används hos patienter med symtom. Målet är då att vilopulsen ska vara 60–80/min och vid lätt ansträngning, såsom gång, 90–115/min. Om ett läkemedel inte räcker till kan kombinationer användas och om det inte hjälper ska patienten hänvisas till konsultation hos rytmkardiolog för bedömning av invasiv behandling (pacemaker och kateterablation av AV-knutan).
Läkemedelsbehandling
- Den medicinering som används för att sänka kammarresponsen (tabell «De vanligaste läkemedlen för optimering av kammarfrekvens vid kroniskt förmaksflimmer...»13) väljs individuellt och dosen justeras enligt målen ovan.
- Betablockerare är effektiva och trygga vid frekvenskontroll av förmaksflimmer «Beetasalpaajat ovat turvallisia ja tehokkaita pysyvän eteisvärinän kammiovasteen hidastamisessa.»A, «Olshansky B, Rosenfeld LE, Warner AL ym. The Atria...»215.
- I behandlingen lönar det sig att prioritera användningen av preparat (bisoprolol, karvedilol och metoprolol) vars effekt och trygghet vid andra hjärtsjukdomar har dokumenterats väl «Grönefeld GC, Hohnloser SH. Beta-blocker therapy i...»86.
- Betablockerare (pindolol och acebutolol) med egenstimulerande sympatomimetisk effekt (ISA) sänker viloslagfrekvensen mindre än andra betablockerare. Patienter med långsam kammarrespons i vila men för snabb under ansträngning tål ofta dessa bättre än andra betablockerare «Grönefeld GC, Hohnloser SH. Beta-blocker therapy i...»86, «Leclercq JF, Rosengarten MD, Kural S ym. Effects o...»216.
- Kalciumantagonister (verapamil och diltiazem) minskar effektivt kammarresponsen vid kroniskt förmaksflimmer «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- De lämpar sig särskilt för patienter som rör sig mycket och som inte har konstaterats ha hjärtsjukdomar.
- Digoxin sänker kammarresponsen i vila effektivare än placebo, men dess effekt försämras vid
fysisk eller psykisk ansträngning «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Sethi NJ, Nielsen EE, Safi S ym. Digoxin for atria...»211.
- Det lämpar sig främst för patienter med låg rörlighet och personer med hjärtsvikt.
- Hur digoxin påverkar prognosen för patienter med förmaksflimmer är kontroversiellt «Al-Khateeb M, Qureshi WT, Odeh R ym. The impact of...»217, «Wang ZQ, Zhang R, Chen MT ym. Digoxin Is Associate...»218, «Chao TF, Liu CJ, Tuan TC ym. Rate-control treatmen...»220, «Gheorghiade M, Fonarow GC, van Veldhuisen DJ ym. L...»221.
- Amiodaron sänker kammarresponsen vid förmaksflimmer, men långvarig användning ska undvikas
på grund av extrakardiella biverkningar «Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiri...»88, «Raatikainen MJ. Rytmihäiriölääkkeiden kliininen kä...»132.
- I allmänhet ska användningen av amiodaron avslutas om patienten hålls i kroniskt förmaksflimmer, om det inte finns någon annan indikation till användningen såsom kammartakykardi.
- Amiodaron kan dock användas som brygga i avvaktan på ablation av AV-knutan.
- Om betablockeraren eller kalciumantagonisten inte i sig räcker till för att optimera
kammarresponsen, kan man använda kombinationsmedicinering eller implantera en pacemaker
och sedan utföra en ablation av AV-knutan (bild «Frekvenskontroll vid kroniskt förmaksflimmer»25), «Eteis-kammiojohtumisen katkaisu ja pysyvä tahdistinhoito vähentänee vaikeaoireisen eteisvärinäpotilaan oireisuutta mutta ei kuolleisuutta.»B.
- De mest användbara kombinationerna är betablockerare och digoxin samt kalciumantagonist och digoxin.
- I de mest problematiska fallen kan man också använda en kombination av betablockerare och kalciumantagonist (och digoxin) eller amiodaron.
- Dronedaron är kontraindicerat vid kroniskt förmaksflimmer, även om det effektivt sänker kammarresponsen «Davy JM, Herold M, Hoglund C ym. Dronedarone for t...»222, «Singh BN, Connolly SJ, Crijns HJ ym. Dronedarone f...»223.
- Det ökar dödligheten, risken för stroke och hjärthändelser samt behovet av sjukhusvård för patienter med kroniskt förmaksflimmer och andra riskfaktorer «Connolly SJ, Camm AJ, Halperin JL ym. Dronedarone ...»163.
| Läkemedel | Rekommenderad underhållsdos/dygn | Evidensgrad |
|---|---|---|
| Betablockerare | «Beetasalpaajat ovat turvallisia ja tehokkaita pysyvän eteisvärinän kammiovasteen hidastamisessa.»A | |
| Atenolol | 50–100 mg x 1 | |
| Bisoprolol | 5–10 mg x 1 (högst 20 mg) | |
| Karvedilol | 25–50 mg x 1 | |
| Metoprolol | 95–190 mg x 1 | |
| Kalciumantagonist | «Kalsiuminestäjät eivät ilmeisesti palauta sinusrytmiä akuutissa eteisvärinässä.»B | |
| Diltiazem | 180–360 mg (kan vid behov delas upp i två doser) | |
| Verapamil | 120–480 mg (kan vid behov delas upp i två doser) | |
| Övriga | ||
| Amiodaron | 100–200 mg x 1 | |
| Digoxin | 0,0625–0,375 mg x 1 |
Kateterablation av atrioventrikulär knutan
- Ablation av AV-knutan förbättrar livskvaliteten och minskar behovet av sjukhusvård men påverkar inte dödligheten «Eteis-kammiojohtumisen katkaisu ja pysyvä tahdistinhoito vähentänee vaikeaoireisen eteisvärinäpotilaan oireisuutta mutta ei kuolleisuutta.»B.
- Vid ingreppet implanteras först en permanent pacemaker och vanligen 2–3 veckor därefter
framkallas ett fullständigt atrioventrikulärt block med kateterablation «Aliot E ym. Catheter ablation or modulation of the...»224.
- Hos en del patienter kan dosen av pulsdämpande läkemedel höjas efter implantering av pacemaker så att ingen kapning av AV-knutan behövs.
- En ablation av AV-knutan avlägsnar inte förmaksflimmer eller behovet av antikoagulationsbehandling.
- Efter ablation ska hjärtat pacemakerstimuleras i 1–3 månader snabbare än vanligt (cirka 70–90/min) för att undvika proarytmi «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Nowinski K, Gadler F, Jensen-Urstad M ym. Transien...»225.
- Ingreppet är befogat om
- viloslagfrekvensen trots maximal medicinering är över 110/min och rytmkontroll inte är möjlig även om patienten har lindriga symtom
- patienten får svåra symtom vid snabb puls (palpitation, svimning e.d.)
- pulsdämpande medicinering orsakar svåra biverkningar
- patienten har konstaterats ha takykardiomyopati
- kammarresponsen är så snabb att den biventrikulära hjärtsviktspacingen är mindre än 90 % av tiden.
- Vid kroniskt förmaksflimmer används kammarpacing (VVIR).
- Vid paroxysmalt och ihållande förmaksflimmer är det i allmänhet skäl att undvika ablation av AV-knutan, men om man beslutar sig för detta används fysiologisk pacing.
- Biventrikulär hjärtsviktspacing eller retledningspacing är i allmänhet ett bättre alternativ än en vanlig pacing av höger kammare, särskilt om funktionen i vänster kammare är nedsatt «Jos vasemman kammion toiminta on alentunut, olisi suositeltavaa asentaa sydämen vajaatoimintatahdistin (biventrikulaarinen tahdistin) eteis-kammiosolmukkeen katkaisun yhteydessä.»B, «Vijayaraman P, Chung MK, Dandamudi G ym. His Bundl...»219.
Antikoagulationsbehandling
- Vid sidan av god behandling av underliggande sjukdomar är en korrekt genomförd antikoagulationsbehandling
det viktigaste med tanke på förmaksflimmerpatientens prognos.
- Risken för hjärtrelaterad embolisering och stroke samt vårdrekommendationen är den samma vid symtomfritt och symtomatiskt förmaksflimmer «European Heart Rhythm Association., European Assoc...»115.
- Vid paroxysmalt förmaksflimmer är vårdrekommendationen densamma som vid ihållande och kroniskt förmaksflimmer, även om risken för stroke uppenbarligen är något mindre «Steinberg BA, Hellkamp AS, Lokhnygina Y ym. Higher...»48, «Vanassche T, Lauw MN, Eikelboom JW ym. Risk of isc...»49.
- Vid förmaksfladder är vårdrekommendationen densamma som vid förmaksflimmer, även om risken för trombos uppenbarligen är aningen mindre än vid förmaksflimmer «European Heart Rhythm Association., European Assoc...»115, «Wood KA, Eisenberg SJ, Kalman JM ym. Risk of throm...»226.
- Behovet av antikoagulationsbehandling bedöms med hjälp av den CHA2DS2VA-poängsättningen (tabell «Bedömning av risken för tromboemboliska komplikationer med hjälp av modifierad CHA2DS2VASc-poängsättning....»2) alltid när patienten konstateras ha förmaksflimmer «Val av antitrombotisk behandling vid förmaksflimmer»4).
- För patienter med hög risk (CHA2DS2VA ≥ 2) är antikoagulationsbehandling i allmänhet befogad även om blödningsrisken är förhöjd.
- Hos patienter med medelhög risk (CHA2DS2VA = 1) fattas beslutet om antikoagulationsbehandling individuellt så att man beaktar
- resultaten av behandlingen av riskfaktorer (t.ex. betydelsen av förhöjt blodtryck är liten om den är i god terapeutisk balans)
- mindre riskfaktorer för tromboser (t.ex. rökning, dyslipidemi och njursvikt ökar trombosrisken)
- blödningsrisken (antikoagulationsbehandling bör avstås från om blödningsrisken är förhöjd).
- Patienter med låg risk (CHA2DS2VA = 0) får ingen antikoagulationsbehandling, eftersom nyttan för dem är mindre än nackdelarna.
- Riskpoängen verkar förutsäga risk för stroke även hos personer med sinusrytm, men det finns ingen evidens på effekten av antikoagulationsbehandling «Ilmeisesti riski-indeksit CHADS2 ja CHA2DS2-VASc ennustavat aivohalvauksen vaaraa myös sinusrytmissä.»B.
- Under antikoagulationsbehandlingen ökar blödningsrisken bland annat av
- > 65 års ålder
- tidigare konstaterad allvarlig blödning
- högt blodtryck (systoliskt blodtryck > 160 mmHg)
- svår njursvikt
- svår leversvikt
- cancer och andra sjukdomar och tillstånd som ökar benägenheten för blödning (t.ex. anemi, trombocytopeni, störning i trombocytfunktionen, diabetes)
- övriga antikoagulationsmedel (t.ex. ASA, antiinflammatoriska läkemedel) och fiskoljepreparat
- riklig alkoholkonsumtion
- genetiska faktorer
- demens
- yrke eller hobby som utsätter för olycksfall
- dålig patientföljsamhet (oförklarlig variation i INR-värden eller oregelbunden användning av direkta orala antikoagulanter)
- I kliniskt arbete kan blödningsrisken bedömas med hjälp av HAS-BLED-poängsättningen (tabell «Bedömning av blödningsrisken med hjälp av HAS-BLED-poängsättning....»14), «Verenvuodon vaaraa varfariinihoidon aikana lisäävät erityisesti korkea ikä, verenhyytymiseen vaikuttavat lääkkeet, INR > 4 ja lukuisat potilaan lisäsairaudet ja kliiniset ominaisuudet.»A, «Vakavien vuotokomplikaatioiden ennustaminen HAS-BLED-indeksin avulla»3.
- Hos personer med hög trombosrisk är antikoagulationsbehandling nästan alltid befogad, även vid förhöjd blödningsrisk.
- Behovet av antikoagulationsbehandling bör bedömas särskilt noggrant om HAS-BLED >
CHA2DS2VA.
- Beakta även eventuell anemi och/eller trombocytopeni.
- Vid användning av direkta orala antikoagulantia uppkommer intrakraniella blödningar mer sällan än vid warfarinbehandling, där de särskilt hänför sig till tidigare stroke, hög ålder, användning av ASA samt tillhörighet till annan än kaukasisk befolkning «Kallonsisäisiä vuotoja ilmeisesti ilmaantuu NOAC-hoitojen aikana harvemmin kuin varfariinihoidossa, jossa ne liittyvät aikaisempaan aivohalvaukseen, muuhun kuin valkoihoiseen väestöön kuulumiseen ja ASAn käyttöön sekä korkeaan ikään.»B.
- Man strävar efter att korrigera alla faktorer som kan behandlas och som ökar benägenheten
för blödningar.
- Vid behandling av högt blodtryck är målet < 130/< 80 mmHg.
- Betydelsen av fallolyckor ska bedömas individuellt. I allmänhet är de inget hinder för antikoagulationsbehandling «Cairns JA. Stroke prevention in atrial fibrillatio...»227.
| Varje punkt är värd ett poäng. Riskfaktorer märkta med rött kan inte påverkas, men i de flesta fall kan risken för andra faktorer minskas genom god vård. Blödningsrisken är förhöjd om poängsumman är minst 3. Beakta även eventuell anemi och trombocytopeni. | ||
|---|---|---|
| Riskfaktor | Poäng | |
| Hypertension | Hypertension Systoliskt blodtryck över 160 mmHg |
1 |
| Abnormal liver or kidney function | Svår lever- eller njursvikt | 1 för båda |
| Stroke | Tidigare stroke | 1 |
| Bleeding | Blödningsbenägenhet 1) | 1 |
| Labile INR | Variationer i INR-värden | 1 |
| Elderly | Ålder över 65 år | 1 |
| Drugs or alcohol | Medicinering eller riklig alkoholkonsumtion som ökar blödningsrisken | 1 för båda |
| 1) cancer, anemi, trombocytopeni, trombocyt dysfunktion, tidigare blödning | ||
Åtgärder innan antikoagulationsbehandling inleds
- Innan användning av direkta orala antikoagulantia eller warfarin inleds ska man
- säkerställa att patienten inte har kontraindikationer för antikoagulationsbehandling eller ett specifikt läkemedel
- undersöka om blödningsrisken är förhöjd och korrigera alla de faktorer som kan påverkas.
- Om risken för allvarlig blödning trots detta är större än risken för trombos orsakad av förmaksflimmer ska antikoagulationsbehandling inte inledas, men en förslutning av vänster förmakstöra kan komma i fråga
- utreda om läkemedel som ökar trombos- eller blödningsrisken används (interaktioner)
- kontrollera blodtrycket samt njurarnas och leverns funktion
- säkerställa vårdföljsamheten.
- Rekommenderade laboratorieundersökningar är liten blodbild (Hb, trombocyter), Krea (eGFR), ALAT och P-TT (INR).
Direkta orala antikoagulantia
- Av direkta orala antikoagulantia används numera direkta trombinhämmaren dabigatran
och faktor Xa-hämmare apixaban, edoxaban och rivaroxaban (tabell «Direkta orala antikoagulantias egenskaper samt doseringsanvisningar...»15).
- En sammanställning av för- och nackdelarna med direkta orala antikoagulantia jämfört med warfarin presenteras i tabell «Fördelar och nackdelar med direkta orala antikoagulantia jämfört med warfarin...»16.
- Idag finns det en specifik antidot mot alla direkta orala antikoagulantia
- idarusizumab upphäver effekten av dabigatran «Pollack CV Jr, Reilly PA, Eikelboom J ym. Idaruciz...»228, «Connolly SJ, Crowther M, Eikelboom JW ym. Full Stu...»229 ja
- andexanet alfa upphäver effekten av faktor Xa-hämmare (rivaroxaban, apixaban och edoxaban) «Connolly SJ, Crowther M, Eikelboom JW ym. Full Stu...»229, «Siegal DM, Curnutte JT, Connolly SJ ym. Andexanet ...»230
- protrombinkomplexkoncentrat (PCC) upphäver effekten av faktor Xa-hämmare men inte dabigatran
- Direkta antikoagulanter är kontraindicerade vid måttlig eller svår mitralstenos och
hos patienter med mekanisk klaffprotes.
- Om patienten har en biologisk klaffprotes som inte kräver warfarinbehandling kan direkta orala antikoagulantia användas på samma sätt som hos andra patienter med förmaksflimmer «Raatikainen MJP. Oraalinen antikoagulaatiohoito sy...»231.
- Vid stabil kranskärlssjukdom hos en patient med förmaksflimmer räcker enbart direkta
orala antikoagulantia för att förhindra incidenter i anslutning till både förmaksflimmer
och artärsjukdom.
- Samtidig användning av ASA eller ADP (P2Y12)-receptorhämmare tillsammans med direkta orala antikoagulantia ökar blödningsrisken men förbättrar inte den antitrombotiska effekten vid stabil kranskärlssjukdom.
- Efter ballongvidgning av kranskärl är däremot tillfällig samtidig användning av direkta orala antikoagulantia och antitrombotika befogad.
- Vid användning av direkta orala antikoagulantia är rutinmässig uppföljning av prover
som mäter koaguleringen inte nödvändig, men blodbilden och njurfunktionen (eGFR) måste
följas upp regelbundet «Steffel J, Verhamme P, Potpara TS ym. The 2018 Eur...»116.
- Faktorer som ska beaktas vid klinisk användning av direkta orala antikoagulantia behandlas i detalj i EHRA:s anvisning «Steffel J, Verhamme P, Potpara TS ym. The 2018 Eur...»116, vars sammanfattning också har publicerats på finska (www «https://www.fincardio.fi/site/assets/files/1381/keymessages_ehra_noac_finland_bd.pdf»2), och i ESC:s vårdrekommendation «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2.
- I särskilda situationer (t.ex. blödning eller trombos under behandlingen, hjärtingrepp) lönar det sig med låg tröskel att konsultera en koagulationsexpert eller kardiolog.
| Dabigatran | Apixaban | Edoxaban | Rivaroxaban | |
|---|---|---|---|---|
| Verkningsmekanism | Direkt trombin (faktor II) hämmare | Direkt faktor Xa-hämmare | Direkt faktor Xa-hämmare | Direkt faktor Xa-hämmare |
| Biologisk nyttoandel | 3–7 % | 50 % | 62 % | 66 %* |
| Matens inverkan på absorptionen | Ingen inverkan | Ingen inverkan | 6–22 % mer med mat | 39 % mer med mat |
| Toppkoncentration (timmar) | 2 | 1–4 | 1–2 | 2–4 |
| Eliminering | 80 % via njurarna och 20 % annan väg |
27 % via njurarna och 73 % annan väg |
50 % via njurarna och 50 % annan väg |
35 % via njurarna och 65 % annan väg |
| Halveringstid (timmar) | 12–17 | 9–14 | 10–14 | 5–13 |
| Normal dos vid förmaksflimmer | 150 mg x 2 Patientens ålder och vikt ska beaktas i doseringen |
5 mg x 2 Patientens ålder och vikt ska beaktas i doseringen |
60 mg x 1 Patientens vikt ska beaktas i doseringen |
20 mg x 1 Ska tas med mat |
| Dosering vid njursvikt | ||||
| eGFR > 50 ml/min | 150 mg x 2 | 5 mg x 2 | 60 mg x 1 | 20 mg x 1 |
| eGFR 30–49 ml/min | 110 mg x 2 | 5 mg x 2 | 30 mg x 1 | 15 mg x 1 |
| eGFR 15–29 ml/min | Kontraindicerat | (2,5 mg x 2)** | (30 mg x 1)** | (15 mg x 1)** |
| eGFR < 15 ml/min | Kontraindicerat | Kontraindicerat | Kontraindicerat | Kontraindicerat |
| Interaktioner | ||||
| P-glykoprotein | Ja | Ja | Ja | Ja |
| CYP3A4 | Nej | Ja (måttlig) | Ja (liten) | Ja (måttlig) |
| Upphävande av inverkan | Idarucizumab | Andexanet alfa PCC |
Andexanet alfa PCC |
Andexanet alfa PCC |
| Särdrag | Dyspepsi hos 5–10 % Syrahämmande läkemedel försämrar absorptionen 12–30 %*** Förvaras i folieförpackning |
Effekten kan försämras om eGFR > 95 ml/min *** | ||
| * Nästan 100 % med mat ** Vid användning ska särskild försiktighet iakttas och andra alternativ övervägas *** Liten klinisk betydelse PCC = protrombinkomplexkoncentrat |
||||
| Fördelar |
| Färre intrakraniella blödningar |
| Standarddosering och mer förutsägbar doseffekt |
| Variation i intag av K-vitamin (kosten) ändrar inte effekten |
| Färre läkemedelsinteraktioner |
| Inget behov av att monitorera rutinmässig läkemedelseffekt (enklare och bekvämare att genomföra) |
| Betydande nackdelar |
| Kontraindicerade vid mitralstenos och hos patienter med mekanisk klaffprotes |
| Kontraindicerade vid svår njursvikt (reducerad dos i lindrigare fall) |
| Övrigt att beakta |
| Sämre tillgång till monitoreringsmetoder (uppföljning av läkemedelseffekt och behandlingsföljsamhet är mer krävande när det finns behov av det) |
| Patientens ålder och vikt påverkar doseringen av vissa preparat |
| Andra biverkningar än blödningar är vanligare (t.ex. dyspepsi) |
| Pris |
Dabigatran
- Dabigatran är en direkt trombinhämmare som tas två gånger per dygn och som förhindrar stroke
minst lika bra som warfarin «Suora trombiinin estäjä dabigatraani ilmeisesti estää aivohalvauksia yhtä hyvin kuin varfariini ja aiheuttaa vähemmän kallonsisäisiä verenvuotoja.»B.
- Dygnsdosen 150 mg x 2 förhindrar stroke betydligt bättre (NNT 182) och orsakar färre intrakraniella blödningar än warfarin «Connolly SJ, Ezekowitz MD, Yusuf S ym. Dabigatran ...»232.
- Dosen 110 mg x 2 förhindrar stroke lika effektivt som warfarin (NNT 718) och orsakar färre blödningar «Connolly SJ, Ezekowitz MD, Yusuf S ym. Dabigatran ...»232.
- Den rekommenderade dygnsdosen för apixaban för att förhindra trombos som orsakats av förmaksflimmer är 150 mg x 2.
- Dosminskning (110 mg x 2) rekommenderas i följande fall:
- Patienten är över 80 år.
- Patienten använder verapamil.
- Kreatininclearance (eGFR) är 30–50 ml/min.
- De viktigaste kontraindikationerna för dabigatran är
- överkänslighet
- mekanisk klaffprotes
- mitralstenos
- eGFR < 30 ml/min
- ALAT > 2 x övre gränsen för normalt
- samtidig användning av starka P-glykoproteinhämmare (systemisk användning av ketokonazol, ciklosporin, itrakonazol eller takrolimus) och dronedaron.
- I nödsituationer (t.ex. svår blödning, brådskande operation) kan effekten av dabigatran hävas med en specifik antidot (idarucizumab) «Pollack CV Jr, Reilly PA, Eikelboom J ym. Idaruciz...»228.
- PCC upphäver knappt effekten av dabigatran.
Apixaban
- Apixaban är en faktor Xa-hämmare som tas två gånger per dygn och som förhindrar stroke mer effektivt och orsakar färre intrakraniella blödningar än warfarin «Suora tekijä Xa:n estäjä apiksabaani ilmeisesti estää aivohalvauksia paremmin kuin varfariini ja aiheuttaa vähemmän kallonsisäisiä ja vakavia verenvuotoja.»B, «Granger CB, Alexander JH, McMurray JJ ym. Apixaban...»233.
- Den rekommenderade dygnsdosen för apixaban för att förhindra trombos som orsakats av förmaksflimmer är 5 mg x 2.
- Dosminskning (2,5 mg x 2) rekommenderas om minst två av följande egenskaper uppfylls:
- Patienten är ≥ 80 år.
- Patienten väger ≤ 60 kg.
- Kreatininkoncentrationen i serum är ≥ 130 mikromol/l.
- De viktigaste kontraindikationerna för apixaban är
- överkänslighet
- mekanisk klaffprotes
- mitralstenos
- svår leversjukdom
- samtidig användning av starka CYP3A4- och P-glykoproteinhämmare (t.ex. azolgruppens svampläkemedel).
- I nödsituationer kan apixabanets effekt hävas med en specifik antidot (andexanet alfa). Även PCC upphäver effekten av apixaban.
Edoxaban
- Edoxaban är en faktor X-hämmare som tas en gång per dag och som förhindrar stroke minst lika bra som warfarin «Suora tekijä Xa -estäjä edoksabaani ilmeisesti estää aivohalvauksia vähintään yhtä hyvin ja aiheuttaa vähemmän kallonsisäisiä verenvuotoja kuin varfariini.»B, «Giugliano RP, Ruff CT, Braunwald E ym. Edoxaban ve...»234.
- Den rekommenderade dosen för att förhindra trombos som orsakats av förmaksflimmer
är 60 mg x 1.
- Läkemedlets effekt försämras om njurfunktionen är exceptionellt bra «Bohula EA, Giugliano RP, Ruff CT ym. Impact of Ren...»235.
- Dosen ska minskas (30 mg x 1) om
- eGFR är 15–49 ml/min (GFR-räknare «GFR-laskuri»1) eller
- vikten är under 60 kg.
- De viktigaste kontraindikationerna för edoxaban är
- överkänslighet
- mekanisk klaffprotes
- mitralstenos
- eGFR < 15 ml/min
- samtidig användning av starka CYP3A4 och P-glykoproteinhämmare (t.ex. azolgruppens svampläkemedel).
- I nödsituationer kan edoxabanets effekt hävas med en specifik antidot (andexanet alfa). Även PCC upphäver effekten av edoxaban.
Rivaroxaban
- Rivaroxaban är en faktor Xa-hämmare som tas en gång per dygn och som förhindrar stroke lika effektivt och orsakar färre intrakraniella blödningar än warfarin «Suora hyytymistekijä Xa:n estäjä rivaroksabaani ilmeisesti estää aivohalvauksia paremmin kuin varfariini. Hoito aiheuttaa vakavia verenvuotoja saman verran ja kallonsisäisiä verenvuotoja vähemmän kuin varfariini.»B, «Patel MR, Mahaffey KW, Garg J ym. Rivaroxaban vers...»236.
- Den rekommenderade dygnsdosen av rivaroxaban vid profylaktisk behandling av tromboser orsakade av förmaksflimmer är 20 mg x 1 oberoende av patientens ålder och vikt.
- Dosminskning (15 mg x 1) rekommenderas om eGFR = 30–49 ml/min.
- De viktigaste kontraindikationerna för rivaroxaban är
- överkänslighet
- mekanisk klaffprotes
- mitralstenos
- eGFR < 15 ml/min
- svår leversjukdom
- samtidig användning av starka CYP3A4- och P-glykoproteinhämmare.
- I nödsituationer kan rivaroxabanets effekt hävas med en specifik antidot (andexanet alfa). Även PCC upphäver effekten av rivaroxaban.
Warfarin
- Warfarin förhindrar stroke betydligt bättre än placebo «Oraalinen antikoagulaatiohoito estää hyvin aivohalvauksien ilmaantumista eteisvärinäpotilailla primaaripreventiossa (vaaran väheneminen 59 %) ja sekundaaripreventiossa (68 %, yhdistettynä 62 %) (95 % luottamusvälit 48–72 %) lumeeseen verrattuna.»A och ASA «Varfariini estää aivohalvauksia merkittävästi paremmin kuin ASA.»A.
- För att förhindra ett fall av stroke ska 15–238 patienter behandlas med warfarin under ett års tid (bild «Val av antitrombotisk behandling vid förmaksflimmer»4) beroende på hur stor risken är. Se tilläggsmaterial «Antikoagulaatiohoidon hyöty suhteessa aivoinfarktin riskin suuruuteen»4.
- Warfarindosen är individuell och fastställs utifrån INR-mätningar
- För förebyggande av stroke och blödningskomplikationer är INR 2–3 den idealiska terapeutiska nivån «Varfariinihoito estää tehokkaasti aivohalvauksia, kun hoitotasapaino on hyvä.»A, (bild «INR-värdets inverkan»26).
- Vid långvarig behanling fastställs INR vanligen en gång i månaden och mätningarna görs oftare om värdena varierar eller patientens övriga medicinering eller tillstånd ändras.
- Mer information om genomförandet av warfarinbehandling finns i tilläggsmaterialet «Varfariinin annosteluohje»5 och på internet «https://www.julkari.fi/bitstream/handle/10024/120375/antikoagluaatiohoidon%20k%c3%a4sikirja.pdf?sequence=1&isAllowed=y»3 samt tilläggsinformation om genomförande av antikoagulationsbehandling i specialfall i ESC:s vårdrekommendation «European Heart Rhythm Association., European Assoc...»115.
- TTR-värdet ("time in therapeutic range") beskriver den tid (%) då medicineringen varit
på terapeutisk nivå (INR=2–3). TTR-räknaren finns på adressen «http://www.terveyskirjasto.fi/xmedia/pgr/200.054.html»4.
- Warfarinbehandlingens effekt och säkerhet bäst när TTR är över 70 % «Lehto M, Luojus A, Halminen O, ym. Time-in-therape...»237.
- Exceptionellt höga eller låga individuella INR-värden ökar risken för trombos- och blödningskomplikationer oberoende av TTR «Varfariinihoito estää tehokkaasti aivohalvauksia, kun hoitotasapaino on hyvä.»A, «European Heart Rhythm Association., European Assoc...»115, «Nilsson GH, Björholt I, Krakau I. Anticoagulant tr...»238.
- Vid kranskärlssjukdom hos en patient med förmaksflimmer räcker det i allmänhet med
enbart warfarinbehandling för att förhindra händelser med anknytning till både förmaksflimmer
och artärsjukdom «European Heart Rhythm Association., European Assoc...»115.
- Samtidig användning av ASA eller ADP (P2Y12)-receptorhämmare tillsammans med warfarin ökar blödningsrisken men förbättrar inte den antitrombotiska effekten vid stabil kranskärlssjukdom.
- Undantag är patienter med mekanisk mitralklaffprotes (permanent samtidig användning) eller genomgången ballongvidgning av kranskärl (tillfällig samtidig användning).
- I nödsituationer kan warfarinets effekt hävas med PCC eller K-vitamin.

INR-värdets inverkan på risken för stroke och intrakraniella blödningar under warfarinbehandlingen. INR = 2–3 är idealisk för behandlingseffekten och blödningskomplikationer.
Acetylsalicylsyra (ASA)
- ASA ska inte användas för att förhindra tromboemboliska komplikationer i samband med
förmaksflimmer, eftersom
- dess antitrombotiska effekt i anknytning till förmaksflimmer hos patienter med hög och medelhög risk är betydligt sämre än med warfarin «Varfariini estää aivohalvauksia merkittävästi paremmin kuin ASA.»A och direkta orala antikoagulantia «Connolly SJ, Eikelboom J, Joyner C ym. Apixaban in...»239
- nyttan av ASA hos patienter med låg risk är mindre än dess nackdelar «ASA estää aivohalvauksia eteisvärinäpotilailla noin 20 % lumelääkkeeseen verrattuna. Teho antikoagulaatiohoitoon verrattuna on kuitenkin matala.»A.
- Det rekommenderas att användningen av ASA avslutas när direkta orala antikoagulantia
eller warfarin inleds.
- Samtidig användning ökar risken för blödningar men förbättrar inte den antitrombotiska effekten.
- Undantag är patienter med genomgången ballongvidgning av kranskärl (tillfällig samtidig användning).
ADP (P2Y12)-receptorhämmare
- ADP (P2Y12)-receptorhämmare (klopidogrel, prasugrel, ticagrelol, ticlodipine) har inte undersökts för att förhindra stroke i samband med förmaksflimmer, alltså ska de inte användas för att förhindra stroke i samband med förmaksflimmer.
- Kombinationen av klopidogrel och ASA förhindrar stroke bättre än enbart ASA, men den ökar blödningskomplikationerna «Klopidogreeli-ASA -yhdistelmähoidon aivohalvauksia estävä teho on parempi kuin pelkän ASA-hoidon, mutta kliinistä hyötyä ei ole yhdistelmän aiheuttamien verenvuotojen vuoksi.»B och dess effekt är betydligt sämre än warfarinets «Klopidogreeli-ASA -yhdistelmähoidon aivohalvauksia estävä teho on parempi kuin pelkän ASA-hoidon, mutta kliinistä hyötyä ei ole yhdistelmän aiheuttamien verenvuotojen vuoksi.»B.
- Tillfällig samtidig användning med direkta orala antikoagulantia eller warfarin kan vara befogad i samband med ballongvidgning av kranskärlen.
Val av orala antikoagulantia
- Valet mellan direkta orala antikoagulantia och warfarin görs individuellt så att man beaktar läkemedlens fördelar och nackdelar (tabell «Fördelar och nackdelar med direkta orala antikoagulantia jämfört med warfarin...»16), patientens önskemål och de faktorer som nämns nedan.
- På grund av bättre följsamhet och trygghet är direkta orala antikoagulanter det primära valet för de flesta nya patienter med förmaksflimmer «Zalesak M, Siu K, Francis K ym. Higher persistence...»240, «Gorst-Rasmussen A, Skjøth F, Larsen TB ym. Dabigat...»241.
-
- Direkta antikoagulanter är minst lika effektiva och säkrare än warfarin i synnerhet med tanke på intrakraniella blödningar i förebyggandet av stroke vid förmaksflimmer «Suorat antikoagulatit ovat tehokkaampia ja turvallisempia kuin varfariini eteisvärinään liittyvien aivohalvauksien estossa.»A
- Fördelen med direkta antikoagulanter vid kortvarig behandling (bl.a. i samband med kardioversion eller ablationsbehandling) är att effekten börjar snabbt och den terapeutiska nivån uppnås betydligt snabbare än med warfarin.
- Vid långvarig behandling kan en väl genomförd warfarinbehandling fortsättas «Joosten LPT, van Doorn S, van de Ven PM, ym. Safet...»242, eftersom ett rutinmässigt byte till direkta antikoagulanter till och med kan vara
skadligt särskilt för äldre och sköra patienter.
- För äldre och multisjuka kan regelbundna hälso- och sjukvårdskontakter i anslutning till INR-uppföljningen vara till nytta.
- Ett snabbt byte till direkta antikoagulanter är motiverat om
- warfarin inte kan fortsättas på grund av allergi eller andra biverkningar
- INR-uppföljningen inte lyckas.
- Om TTR är < 70 % utreds orsaken till den dåliga balansen och man bedömer om situationen kan korrigeras genom effektivering av warfarinbehandlingen eller genom byte till direkta orala antikoagulantia.
- Direkta orala antikoagulantia har inte jämförts sinsemellan och man kan inte i detta skede ta ställning till valet mellan dem.
Förslutning av vänster förmaksöra
- En perkutan kateterburen förslutning av vänster förmaksöra förhindrar tromboemboliska
hjärnhändelser lika effektivt som warfarinbehandling «Vasemman eteiskorvakkeen sulku perkutaanisella sydämen sisältä katetriteitse asennettavalla sulkulaitteella estää tromboembolisia aivotapahtumia todennäköisesti yhtä tehokkaasti kuin varfariinihoito korkean tromboembolian ja korkean vuotoriskin potilailla.»B.
- Trots komplikationsrisken kan åtgärden övervägas för patienter med stor trombosrisk, hos vilka oral antikoagulationsbehandling är kontraindicerad.
- Dessutom kan ingreppet övervägas om en högriskpatient drabbas av en allvarlig blödningskomplikation under pågående adekvat antikoagulationsbehandling.
- Fullständig förslutning av vänster förmaksöra i samband med en hjärtoperation torde
minska förmaksflimmerpatientens tromboemboliska komplikationer lika effektivt som
warfarinbehandling «Muun sydänkirurgian yhteydessä tehtävä vasemman eteiskorvakkeen täydellinen sulku vähentänee eteisvärinäpotilaan tromboembolisia komplikaatioita yhtä tehokkaasti kuin varfariinihoito.»B.
- En ofullständig kirurgisk förslutning av förmaksörat kan vara skadligare än att låta bli att försluta «Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ES...»2, «Aryana A, Singh SK, Singh SM ym. Association betwe...»243.
- Ingreppet kan övervägas i samband med en annan hjärtoperation om benägenheten för förmaksflimmer är uppenbar och patienten även har andra riskfaktorer för störningar i hjärnans blodcirkulation.
- Antikoagulationsbehandling behövs fortfarande efter förslutning eller borttagning av förmaksörat i samband med en hjärtoperation . Ingreppet i kombination med antikoagulationsbehandling minskar uppenbarligen tromboemboliska komplikationer bättre än enbart antikoagulationsbehandling. «Whitlock RP, Belley-Cote EP, Paparella D, ym. Left...»244
Uppföljning
- Förmaksflimmer är en kronisk sjukdom som kräver regelbunden uppföljning.
- Det första uppföljningsbesöket är i allmänhet befogat cirka ett halvt år efter att förmaksflimmer konstaterats och därefter ordnas uppföljningsbesök beroende på patientens underliggande sjukdomar och helhetssituation samt förekomsten av rytmrubbningar.
- För majoriteten av patienterna kan uppföljningen genomföras inom primärvården.
- Under uppföljningsbesöket utreds
- kontrolleras och effektiveras vården av underliggande sjukdomar vid behov, eller så ordnas nödvändiga tilläggsundersökningar
- om riskfaktorerna för störningar i hjärnans blodcirkulation och blödningar förändrats (CHA2DS2VASc- och HAS-BLED-poängsättning)
- om patienten har haft symtom som tyder på störningar i hjärnans blodcirkulation
- om antikoagulationsbehandlingen har genomförts enligt rekommendationerna (vid warfarinbehandling är TTR-målet över 70 %)
- om patientens symtom på rytmrubbningar har lindrats på grund av behandlingen (EHRA-klass)
- om kontraindikationer har uppkommit för den använda arytmimedicineringen (breddökning av QRS-komplexet, förlängd QT-tid, hypertrofi i vänster kammare, ischemi, insufficiens)
- om typen av förmaksflimmer har ändrats från paroxysmalt till ihållande eller kroniskt förmaksflimmer
- om kammarresponsen vid kroniskt förmaksflimmer är "ekonomisk".
- Utöver anamnes och klinisk undersökning kontrolleras rutinmässigt EKG med 12 avledningar, där man bland annat fäster uppmärksamhet vid de faktorer som presenteras i tabell «Rekommenderade undersökningar för förmaksflimmerpatienter...»4.
- Behovet av andra undersökningar bedöms individuellt. Möjliga undersökningar är bland
annat:
- laboratorieundersökningar (t.ex. liten blodbild, trombocyter, elektrolyter, kreatinin, glukos, lipider, trygghetsprov för antikoagulationsbehandling och arytmimedicinering)
- ultraljudsundersökning av hjärtat
- thorax-röntgen
- långtidsregistrering av EKG
- belastnings-EKG
- invasiva undersökningar
- noggrannare neurologiska utredningar.
- Förmaksflimmer orsakar i allmänhet inte långvarig arbetsoförmåga och hindrar inte
bilkörning.
- En kortvarig sjukskrivning kan dock vara befogad på grund av ett arytmianfall, en kardioversion eller till exempel kateterablationsbehandling.
- För att fortsätta som yrkesbilist krävs antikoagulationsbehandling som genomförs enligt rekommendationerna.
Nivåstrukturerad vård
- Behandlingen av förmaksflimmer är komplicerad och kräver multiprofessionell kompetens och gott samarbete mellan olika specialiIteter (bl.a. kardiologi, internmedicin, neurologi och koagulationsexperter) och primärvården.
- Den specialiserade sjukvården är skyldig att säkerställa att de regionala vårdkedjorna fungerar och ordna utbildning och tillräckliga konsultationsmöjligheter för vårdpersonalen i sitt område.
- Primärvårdens läkare ska när det gäller en arytmipatient ha goda grundläggande kunskaper
om
- antikoagulationsbehandlingens indikationer och genomförande
- faktorer som påverkar valet av vårdlinje (frekvens- eller rytmkontroll)
- optimering av kammarfrekvensen
- indikationer och uppföljning av profylaktisk medicinering
- indikationer för invasiv vård
- Det finns rikligt med material och guider för patienthandledning bland annat på Hjärtförbundets «https://sydan.fi/»5och Hälsobyns webbplatser «https://www.terveyskyla.fi/»6, och patientorganisationerna erbjuder också kamratstöd.
- Behandling av underliggande sjukdomar och predisponerande faktorer
- God behandling av underliggande sjukdomar utgör hörnstenen i behandlingen av förmaksflimmer oberoende av vilken vårdlinje som valts (tabell «Behandlingsmål och behandlingsformer för de vanligaste bakomliggande faktorerna till förmaksflimmer....»6).
- Primärvårdens läkare har huvudansvaret för diagnostik och behandling av de vanligaste associerade sjukdomarna som ökar risken för förmaksflimmer och tromboemboliska komplikationer, såsom hypertension och diabetes.
- Inom den specialiserade sjukvården är det skäl att behandla patienter som reagerar dåligt på sedvanlig medicinering och patienter vars associerade sjukdom kräver invasiva undersökningar eller behandling.
- Behandling av akut förmaksflimmer
- Vårdlinjen (frekvens- eller rytmkontroll) kan i allmänhet avgöras inom primärvården. I problemfall är det skäl att konsultera kardiolog.
- Elkonvertering kräver anestesi och därför lämpar den sig endast sällan inom primärvården.
- En farmakologisk kardioversion kan också göras på en välutrustad hälsovårdscentral.
- Profylaktisk behandling av förmaksflimmer (rytmkontroll)
- Behandling med betablockerare kan inledas inom primärvården.
- Den egentliga arytmimedicineringen (läkemedel i grupp I och III) inleds av en kardiolog eller en internmedicinsk läkare som är insatt i behandlingen av hjärtsjukdomar.
- En hälsocentralläkare eller företagsläkare kan ansvara för den fortsatta uppföljningen av patienten enligt specialistens anvisningar.
- Planering och genomförandet av invasiv åtgärder hör till rytmkardiolog.
- Optimering av kammarfrekvens (frekvenskontroll)
- Primärvårdens läkare har huvudansvaret för optimeringen och uppföljningen av kammarfrekvensen vid kroniskt förmaksflimmer.
- Inom den specialiserade sjukvården är det skäl att behandla patienter som reagerar dåligt på sedvanlig medicinering och patienter vars associerade sjukdom kräver specialiserad sjukvård.
- Antikoagulationsbehandling
- Primärvårdens läkare har huvudansvaret för genomförandet av antikoagulationsbehandlingen.
- Ovan nämnda rekommendationer är riktgivande och kan anpassas lokalt så att den regionala vårdkedjan fungerar så effektivt som möjligt.
Arbetsgrupp tillsatt av Finska Läkarföreningen Duodecim och Kardiologiska Föreningen i Finland
För mer information om arbetsgruppsmedlemmar samt anmälan om intressekonflikter, se «Eteisvärinä»1 (på finska)
Översättare: Lingsoft Language Services Oy
Granskning av översättningen: Jon Holmström
Litteratur
Förmaksflimmer. God medicinsk praxis-rekommendation. Arbetsgrupp tillsatt av Finska Läkarföreningen Duodecim och Kardiologiska Föreningen i Finland. Helsingfors: Finska Läkarföreningen Duodecim, 2021 (hänvisning dd.mm.åååå). Tillgänglig på internet: www.kaypahoito.fi
Närmare anvisningar: «https://www.kaypahoito.fi/sv/god-medicinsk-praxis/nyttjanderattigheter/citering»7
Ansvarsbegränsning
God medicinsk praxis- och Avstå klokt-rekommendationerna är sammandrag gjorda av experter gällande diagnostik och behandling av bestämda sjukdomar. Rekommendationerna fungerar som stöd när läkare eller andra yrkesutbildade personer inom hälso- och sjukvården ska fatta behandlingsbeslut. De ersätter inte läkarens eller annan hälsovårdspersonals egen bedömning av vilken diagnostik, behandling och rehabilitering som är bäst för den enskilda patienten då behandlingsbeslut fattas.
Litteratur
- Calkins H, Hindricks G, Cappato R ym. 2017?HRS/EHRA/ECAS/APHRS/SOLAECE expert consensus statement on catheter and surgical ablation of atrial fibrillation: Executive summary. Europace 2018;20:157-208 «PMID: 29016841»PubMed
- Van Gelder IC, Rienstra M, Bunting KV, ym. 2024 ESC Guidelines for the management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2024;45(36):3314-3414 «PMID: 39210723»PubMed
- Kopecky SL, Gersh BJ, McGoon MD ym. The natural history of lone atrial fibrillation. A population-based study over three decades. N Engl J Med 1987;317:669-74 «PMID: 3627174»PubMed
- Chugh SS, Havmoeller R, Narayanan K ym. Worldwide epidemiology of atrial fibrillation: a Global Burden of Disease 2010 Study. Circulation 2014;129:837-47 «PMID: 24345399»PubMed
- Lehto M, Haukka J, Aro A, ym. Comprehensive nationwide incidence and prevalence trends of atrial fibrillation in Finland. Open Heart 2022;9(2): «PMID: 36414332»PubMed
- Feinberg WM, Blackshear JL, Laupacis A ym. Prevalence, age distribution, and gender of patients with atrial fibrillation. Analysis and implications. Arch Intern Med 1995;155:469-73 «PMID: 7864703»PubMed
- Savelieva I, John Camm A. Atrial fibrillation and heart failure: natural history and pharmacological treatment. Europace 2004;5 Suppl 1:S5-19 «PMID: 15450275»PubMed
- Lloyd-Jones DM, Wang TJ, Leip EP ym. Lifetime risk for development of atrial fibrillation: the Framingham Heart Study. Circulation 2004;110:1042-6 «PMID: 15313941»PubMed
- Magnussen C, Niiranen TJ, Ojeda FM ym. Sex Differences and Similarities in Atrial Fibrillation Epidemiology, Risk Factors, and Mortality in Community Cohorts: Results From the BiomarCaRE Consortium (Biomarker for Cardiovascular Risk Assessment in Europe). Circulation 2017;136:1588-1597 «PMID: 29038167»PubMed.
- Miyasaka Y, Barnes ME, Gersh BJ ym. Secular trends in incidence of atrial fibrillation in Olmsted County, Minnesota, 1980 to 2000, and implications on the projections for future prevalence. Circulation 2006;114:119-25 «PMID: 16818816»PubMed
- Benjamin EJ, Levy D, Vaziri SM ym. Independent risk factors for atrial fibrillation in a population-based cohort. The Framingham Heart Study. JAMA 1994;271:840-4 «PMID: 8114238»PubMed
- Rensma PL, Allessie MA, Lammers WJ ym. Length of excitation wave and susceptibility to reentrant atrial arrhythmias in normal conscious dogs. Circ Res 1988;62:395-410 «PMID: 3338122»PubMed
- Allessie MA, Boyden PA, Camm AJ ym. Pathophysiology and prevention of atrial fibrillation. Circulation 2001;103:769-77 «PMID: 11156892»PubMed
- Nattel S. New ideas about atrial fibrillation 50 years on. Nature 2002;415:219-26 «PMID: 11805846»PubMed
- Tieleman RG. The pathophysiology of maintenance of atrial fibrillation. Pacing Clin Electrophysiol 2003;26:1569-71 «PMID: 12914604»PubMed
- Haïssaguerre M, Jaïs P, Shah DC ym. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. N Engl J Med 1998;339:659-66 «PMID: 9725923»PubMed
- Chen SA, Chen YJ, Yeh HI ym. Pathophysiology of the pulmonary vein as an atrial fibrillation initiator. Pacing Clin Electrophysiol 2003;26:1576-82 «PMID: 12914606»PubMed
- Nattel S. Basic electrophysiology of the pulmonary veins and their role in atrial fibrillation: precipitators, perpetuators, and perplexers. J Cardiovasc Electrophysiol 2003;14:1372-5 «PMID: 14678116»PubMed
- Wijffels MC, Kirchhof CJ, Dorland R ym. Atrial fibrillation begets atrial fibrillation. A study in awake chronically instrumented goats. Circulation 1995;92:1954-68 «PMID: 7671380»PubMed
- Allessie M, Ausma J, Schotten U. Electrical, contractile and structural remodeling during atrial fibrillation. Cardiovasc Res 2002;54:230-46 «PMID: 12062329»PubMed
- Sparks PB, Mond HG, Vohra JK ym. Mechanical remodeling of the left atrium after loss of atrioventricular synchrony. A long-term study in humans. Circulation 1999;100:1714-21 «PMID: 10525491»PubMed
- Schotten U, Duytschaever M, Ausma J ym. Electrical and contractile remodeling during the first days of atrial fibrillation go hand in hand. Circulation 2003;107:1433-9 «PMID: 12642366»PubMed
- Nattel S, Li D, Yue L. Basic mechanisms of atrial fibrillation--very new insights into very old ideas. Annu Rev Physiol 2000;62:51-77 «PMID: 10845084»PubMed
- Burstein B, Nattel S. Atrial fibrosis: mechanisms and clinical relevance in atrial fibrillation. J Am Coll Cardiol 2008;51:802-9 «PMID: 18294563»PubMed
- Schoonderwoerd BA, Smit MD, Pen L ym. New risk factors for atrial fibrillation: causes of 'not-so-lone atrial fibrillation'. Europace 2008;10:668-73 «PMID: 18480076»PubMed
- Elosua R, Arquer A, Mont L ym. Sport practice and the risk of lone atrial fibrillation: a case-control study. Int J Cardiol 2006;108:332-7 «PMID: 15963583»PubMed
- Mont L, Sambola A, Brugada J ym. Long-lasting sport practice and lone atrial fibrillation. Eur Heart J 2002;23:477-82 «PMID: 11863350»PubMed
- Abdulla J, Nielsen JR. Is the risk of atrial fibrillation higher in athletes than in the general population? A systematic review and meta-analysis. Europace 2009;11:1156-9 «PMID: 19633305»PubMed
- Wilhelm M, Roten L, Tanner H ym. Atrial remodeling, autonomic tone, and lifetime training hours in nonelite athletes. Am J Cardiol 2011;108:580-5 «PMID: 21658663»PubMed
- Andersen K, Farahmand B, Ahlbom A ym. Risk of arrhythmias in 52 755 long-distance cross-country skiers: a cohort study. Eur Heart J 2013;34:3624-31 «PMID: 23756332»PubMed
- Karjalainen J, Kujala UM, Kaprio J ym. Lone atrial fibrillation in vigorously exercising middle aged men: case-control study. BMJ 1998;316:1784-5 «PMID: 9624065»PubMed
- Turagam MK, Flaker GC, Velagapudi P ym. Atrial Fibrillation In Athletes: Pathophysiology, Clinical Presentation, Evaluation and Management. J Atr Fibrillation 2015;8:1309 «PMID: 27957228»PubMed
- Calvo N, Ramos P, Montserrat S ym. Emerging risk factors and the dose-response relationship between physical activity and lone atrial fibrillation: a prospective case-control study. Europace 2016;18:57-63 «PMID: 26333377»PubMed
- Aizer A, Gaziano JM, Cook NR ym. Relation of vigorous exercise to risk of atrial fibrillation. Am J Cardiol 2009;103:1572-7 «PMID: 19463518»PubMed
- Manolis AS, Manolis AA. Exercise and Arrhythmias: A Double-Edged Sword. Pacing Clin Electrophysiol 2016;39:748-62 «PMID: 27120033»PubMed
- Brugada R, Tapscott T, Czernuszewicz GZ ym. Identification of a genetic locus for familial atrial fibrillation. N Engl J Med 1997;336:905-11 «PMID: 9070470»PubMed
- Troughton RW, Asher CR, Klein AL. The role of echocardiography in atrial fibrillation and cardioversion. Heart 2003;89:1447-54 «PMID: 14617563»PubMed
- Andalib A, Brugada R, Nattel S. Atrial fibrillation: evidence for genetically determined disease. Curr Opin Cardiol 2008;23:176-83 «PMID: 18382204»PubMed
- Krahn AD, Manfreda J, Tate RB ym. The natural history of atrial fibrillation: incidence, risk factors, and prognosis in the Manitoba Follow-Up Study. Am J Med 1995;98:476-84 «PMID: 7733127»PubMed
- Benjamin EJ, Wolf PA, D'Agostino RB ym. Impact of atrial fibrillation on the risk of death: the Framingham Heart Study. Circulation 1998;98:946-52 «PMID: 9737513»PubMed
- Stevenson WG, Stevenson LW, Middlekauff HR ym. Improving survival for patients with atrial fibrillation and advanced heart failure. J Am Coll Cardiol 1996;28:1458-63 «PMID: 8917258»PubMed
- Knecht S, Oelschläger C, Duning T ym. Atrial fibrillation in stroke-free patients is associated with memory impairment and hippocampal atrophy. Eur Heart J 2008;29:2125-32 «PMID: 18667399»PubMed
- Teppo K, Airaksinen KEJ, Jaakkola J, ym. Trends in treatment and outcomes of atrial fibrillation during 2007-17 in Finland. Eur Heart J Qual Care Clin Outcomes 2023;9(7):673-679 «PMID: 36542420»PubMed
- Teppo K, Lip GYH, Airaksinen KEJ, ym. Comparing CHA(2)DS(2)-VA and CHA(2)DS(2)-VASc scores for stroke risk stratification in patients with atrial fibrillation: a temporal trends analysis from the retrospective Finnish AntiCoagulation in Atrial Fibrillation (FinACAF) cohort. Lancet Reg Health Eur 2024;43():100967 «PMID: 39171253»PubMed
- Penttilä T, Lehto M, Niiranen J, ym. Differences in the risk of stroke, bleeding events, and mortality between female and male patients with atrial fibrillation during warfarin therapy. Eur Heart J Cardiovasc Pharmacother 2019;5(1):29-36 «PMID: 30052822»PubMed
- Lip GY, Nieuwlaat R, Pisters R ym. Refining clinical risk stratification for predicting stroke and thromboembolism in atrial fibrillation using a novel risk factor-based approach: the euro heart survey on atrial fibrillation. Chest 2010;137:263-72 «PMID: 19762550»PubMed
- Van Staa TP, Setakis E, Di Tanna GL ym. A comparison of risk stratification schemes for stroke in 79,884 atrial fibrillation patients in general practice. J Thromb Haemost 2011;9:39-48 «PMID: 21029359»PubMed
- Steinberg BA, Hellkamp AS, Lokhnygina Y ym. Higher risk of death and stroke in patients with persistent vs. paroxysmal atrial fibrillation: results from the ROCKET-AF Trial. Eur Heart J 2015;36:288-96 «PMID: 25209598»PubMed
- Vanassche T, Lauw MN, Eikelboom JW ym. Risk of ischaemic stroke according to pattern of atrial fibrillation: analysis of 6563 aspirin-treated patients in ACTIVE-A and AVERROES. Eur Heart J 2015;36:281-7a «PMID: 25187524»PubMed
- Alboni P, Scarfò S, Fucà G ym. Hemodynamics of idiopathic paroxysmal atrial fibrillation. Pacing Clin Electrophysiol 1995;18:980-5 «PMID: 7659571»PubMed
- Clark DM, Plumb VJ, Epstein AE ym. Hemodynamic effects of an irregular sequence of ventricular cycle lengths during atrial fibrillation. J Am Coll Cardiol 1997;30:1039-45 «PMID: 9316536»PubMed
- Lau CP, Leung WH, Wong CK ym. Haemodynamics of induced atrial fibrillation: a comparative assessment with sinus rhythm, atrial and ventricular pacing. Eur Heart J 1990;11:219-24 «PMID: 2318225»PubMed
- Shinbane JS, Wood MA, Jensen DN ym. Tachycardia-induced cardiomyopathy: a review of animal models and clinical studies. J Am Coll Cardiol 1997;29:709-15 «PMID: 9091514»PubMed
- Dorian P, Jung W, Newman D ym. The impairment of health-related quality of life in patients with intermittent atrial fibrillation: implications for the assessment of investigational therapy. J Am Coll Cardiol 2000;36:1303-9 «PMID: 11028487»PubMed
- Lüderitz B. Dirk Durrer (1918-1984). J Interv Card Electrophysiol 2000;4:547 «PMID: 11203445»PubMed
- van den Berg MP, Hassink RJ, Tuinenburg AE ym. Quality of life in patients with paroxysmal atrial fibrillation and its predictors: importance of the autonomic nervous system. Eur Heart J 2001;22:247-53 «PMID: 11161936»PubMed
- Paquette M, Roy D, Talajic M ym. Role of gender and personality on quality-of-life impairment in intermittent atrial fibrillation. Am J Cardiol 2000;86:764-8 «PMID: 11018197»PubMed
- Hekkala AM. Suomalaisten eteisvärinäpotilaiden kokemuksia sairautensa hoidosta. Suom Lääkäril 2021;76(10):650-2
- Kirchhof P, Bax J, Blomstrom-Lundquist C ym. Early and comprehensive management of atrial fibrillation: proceedings from the 2nd AFNET/EHRA consensus conference on atrial fibrillation entitled 'research perspectives in atrial fibrillation'. Europace 2009;11:860-85 «PMID: 19531542»PubMed
- Kirchhof P, Toennis T, Goette A, ym. Anticoagulation with Edoxaban in Patients with Atrial High-Rate Episodes. N Engl J Med 2023;389(13):1167-1179 «PMID: 37622677»PubMed
- Healey JS, Lopes RD, Granger CB, ym. Apixaban for Stroke Prevention in Subclinical Atrial Fibrillation. N Engl J Med 2024;390(2):107-117 «PMID: 37952132»PubMed
- Toni D, Lorenzano S, Strano S ym. Detection of Silent Atrial Fibrillation aFter Ischemic StrOke (SAFFO) guided by implantable loop recorder: multicentre Italian trial based on stroke unit network with paired cardio-arrhythmology units (Italian Neurocardiology Unit Network). Int J Stroke 2016;11:361-7 «PMID: 26873942»PubMed
- Aivoinfarkti ja TIA. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Neurologinen yhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2024 (viitattu 15.1.2025). Saatavilla internetissä: www.kaypahoito.fi
- Fung E, Järvelin MR, Doshi RN ym. Electrocardiographic patch devices and contemporary wireless cardiac monitoring. Front Physiol 2015;6:149 «PMID: 26074823»PubMed
- McNamara RL, Tamariz LJ, Segal JB ym. Management of atrial fibrillation: review of the evidence for the role of pharmacologic therapy, electrical cardioversion, and echocardiography. Ann Intern Med 2003;139:1018-33 «PMID: 14678922»PubMed
- Manning WJ, Weintraub RM, Waksmonski CA ym. Accuracy of transesophageal echocardiography for identifying left atrial thrombi. A prospective, intraoperative study. Ann Intern Med 1995;123:817-22 «PMID: 7486462»PubMed
- Saarela E, Koskela V, Strandberg M ym. Ruokatorven kautta tehtävä sydämen kaikukuvaus eteisvärinän rytminsiirrossa. Duodecim 2004;120:1575-81 «http://www.duodecimlehti.fi/web/guest/etusivu/artikkeli?tunnus=duo94376»8
- Camm AJ, Lip GY, De Caterina R ym. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: an update of the 2010 ESC Guidelines for the management of atrial fibrillation--developed with the special contribution of the European Heart Rhythm Association. Europace 2012;14:1385-413 «PMID: 22923145»PubMed
- Danias PG, Caulfield TA, Weigner MJ ym. Likelihood of spontaneous conversion of atrial fibrillation to sinus rhythm. J Am Coll Cardiol 1998;31:588-92 «PMID: 9502640»PubMed
- Dell'Orfano JT, Patel H, Wolbrette DL ym. Acute treatment of atrial fibrillation: spontaneous conversion rates and cost of care. Am J Cardiol 1999;83:788-90, A10 «PMID: 10080441»PubMed
- Raatikainen MJ. Akuutin eteisvärinäkohtauksen hoito. Suom Lääkäril 2002;57:5029-36
- Hohnloser SH, Kuck KH, Lilienthal J. Rhythm or rate control in atrial fibrillation--Pharmacological Intervention in Atrial Fibrillation (PIAF): a randomised trial. Lancet 2000;356:1789-94 «PMID: 11117910»PubMed
- Wyse DG, Waldo AL, DiMarco JP ym. A comparison of rate control and rhythm control in patients with atrial fibrillation. N Engl J Med 2002;347:1825-33 «PMID: 12466506»PubMed
- Van Gelder IC, Hagens VE, Bosker HA ym. A comparison of rate control and rhythm control in patients with recurrent persistent atrial fibrillation. N Engl J Med 2002;347:1834-40 «PMID: 12466507»PubMed
- Carlsson J, Miketic S, Windeler J ym. Randomized trial of rate-control versus rhythm-control in persistent atrial fibrillation: the Strategies of Treatment of Atrial Fibrillation (STAF) study. J Am Coll Cardiol 2003;41:1690-6 «PMID: 12767648»PubMed
- Opolski G, Torbicki A, Kosior DA ym. Rate control vs rhythm control in patients with nonvalvular persistent atrial fibrillation: the results of the Polish How to Treat Chronic Atrial Fibrillation (HOT CAFE) Study. Chest 2004;126:476-86 «PMID: 15302734»PubMed
- Roy D, Talajic M, Nattel S ym. Rhythm control versus rate control for atrial fibrillation and heart failure. N Engl J Med 2008;358:2667-77 «PMID: 18565859»PubMed
- Kohonnut verenpaine. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Verenpaineyhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2020 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Sydämen vajaatoiminta. Käypä hoito -suositus. Suomalaisen Lääkäriseura Duodecimin ja Suomen Kardiologisen Seuran asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2023 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Tyypin 2 diabetes. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Sisätautilääkärien yhdistyksen ja Diabetesliiton Lääkärineuvoston asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2024 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Lihavuus (lapset, nuoret ja aikuiset). Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Lihavuustutkijat ry:n ja Suomen Lastenlääkäriyhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2024 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Uniapnea (obstruktiivinen uniapnea aikuisilla). Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Keuhkolääkäriyhdistyksen ja Suomen Unitutkimusseura ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2022 (viitattu 5.11.2024). Saatavilla internetissä: www.kaypahoito.fi
- Tupakka- ja nikotiiniriippuvuuden ehkäisy ja hoito. Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Yleislääketieteen yhdistyksen asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2024 (viitattu 15.1.2025). Saatavilla internetissä: www.kaypahoito.fi
- Segal JB, McNamara RL, Miller MR ym. The evidence regarding the drugs used for ventricular rate control. J Fam Pract 2000;49:47-59 «PMID: 10678340»PubMed
- Snow V, Weiss KB, LeFevre M ym. Management of newly detected atrial fibrillation: a clinical practice guideline from the American Academy of Family Physicians and the American College of Physicians. Ann Intern Med 2003;139:1009-17 «PMID: 14678921»PubMed
- Grönefeld GC, Hohnloser SH. Beta-blocker therapy in atrial fibrillation. Pacing Clin Electrophysiol 2003;26:1607-12 «PMID: 12914610»PubMed
- Singh BN. Antiarrhythmic actions of amiodarone: a profile of a paradoxical agent. Am J Cardiol 1996;78:41-53 «PMID: 8780328»PubMed
- Raatikainen MJ, Huikuri HV. Amioidaroni rytmihäiriöiden hoidossa. Duodecim 1998;114:1923-36 «http://www.duodecimlehti.fi/web/guest/etusivu/artikkeli?tunnus=duo80400»9
- Clemo HF, Wood MA, Gilligan DM ym. Intravenous amiodarone for acute heart rate control in the critically ill patient with atrial tachyarrhythmias. Am J Cardiol 1998;81:594-8 «PMID: 9514456»PubMed
- Page RL, Hamad B, Kirkpatrick P. Dronedarone. Nat Rev Drug Discov 2009;8:769-70 «PMID: 19794441»PubMed
- Hoy SM, Keam SJ. Dronedarone. Drugs 2009;69:1647-63 «PMID: 19678715»PubMed
- Murray KT. Ibutilide. Circulation 1998;97:493-7 «PMID: 9490245»PubMed
- Cheng JW. Vernakalant in the management of atrial fibrillation. Ann Pharmacother 2008;42:533-42 «PMID: 18334607»PubMed
- Nagarakanti R, Ezekowitz MD, Oldgren J ym. Dabigatran versus warfarin in patients with atrial fibrillation: an analysis of patients undergoing cardioversion. Circulation 2011;123:131-6 «PMID: 21200007»PubMed
- Piccini JP, Stevens SR, Lokhnygina Y ym. Outcomes after cardioversion and atrial fibrillation ablation in patients treated with rivaroxaban and warfarin in the ROCKET AF trial. J Am Coll Cardiol 2013;61:1998-2006 «PMID: 23500298»PubMed
- Flaker G, Lopes RD, Al-Khatib SM ym. Efficacy and safety of apixaban in patients after cardioversion for atrial fibrillation: insights from the ARISTOTLE Trial (Apixaban for Reduction in Stroke and Other Thromboembolic Events in Atrial Fibrillation). J Am Coll Cardiol 2014;63:1082-7 «PMID: 24211508»PubMed
- Cappato R, Ezekowitz MD, Klein AL ym. Rivaroxaban vs. vitamin K antagonists for cardioversion in atrial fibrillation. Eur Heart J 2014;35:3346-55 «PMID: 25182247»PubMed
- Caldeira D, Costa J, Ferreira JJ ym. Non-vitamin K antagonist oral anticoagulants in the cardioversion of patients with atrial fibrillation: systematic review and meta-analysis. Clin Res Cardiol 2015;104:582-90 «PMID: 25643952»PubMed
- Schmidt AS, Lauridsen KG, Torp P ym. Maximum-fixed energy shocks for cardioverting atrial fibrillation. Eur Heart J 2020;41:626-631 «PMID: 31504412»PubMed
- Oral H, Souza JJ, Michaud GF ym. Facilitating transthoracic cardioversion of atrial fibrillation with ibutilide pretreatment. N Engl J Med 1999;340:1849-54 «PMID: 10369847»PubMed
- Marcus GM, Sung RJ. Antiarrhythmic agents in facilitating electrical cardioversion of atrial fibrillation and promoting maintenance of sinus rhythm. Cardiology 2001;95:1-8 «PMID: 11385184»PubMed
- Van Noord T, Van Gelder IC, Crijns HJ. How to enhance acute outcome of electrical cardioversion by drug therapy: importance of immediate reinitiation of atrial fibrillation. J Cardiovasc Electrophysiol 2002;13:822-5 «PMID: 12212706»PubMed
- Crozier I. Flecainide in the Wolff-Parkinson-White syndrome. Am J Cardiol 1992;70:26A-32A «PMID: 1509995»PubMed
- Raatikainen MJP, Sigurd B. Atrial fibrillation - the role of flecainide. Oy Sevenprint Ltd, Rovaniemi 2008
- Capucci A, Villani GQ, Aschieri D ym. Safety of oral propafenone in the conversion of recent onset atrial fibrillation to sinus rhythm: a prospective parallel placebo-controlled multicentre study. Int J Cardiol 1999;68:187-96 «PMID: 10189007»PubMed
- Aliot E, De Roy L, Capucci A ym. Safety of a controlled-release flecainide acetate formulation in the prevention of paroxysmal atrial fibrillation in outpatients. Ann Cardiol Angeiol (Paris) 2003;52:34-40 «PMID: 12710293»PubMed
- Kishore AG, Camm AJ. Guidelines for the use of propafenone in treating supraventricular arrhythmias. Drugs 1995;50:250-62 «PMID: 8521758»PubMed
- Naccarelli GV, Wolbrette DL, Samii S ym. Vernakalant--a promising therapy for conversion of recent-onset atrial fibrillation. Expert Opin Investig Drugs 2008;17:805-10 «PMID: 18447605»PubMed
- Roy D, Pratt CM, Torp-Pedersen C ym. Vernakalant hydrochloride for rapid conversion of atrial fibrillation: a phase 3, randomized, placebo-controlled trial. Circulation 2008;117:1518-25 «PMID: 18332267»PubMed
- Kowey PR, Dorian P, Mitchell LB ym. Vernakalant hydrochloride for the rapid conversion of atrial fibrillation after cardiac surgery: a randomized, double-blind, placebo-controlled trial. Circ Arrhythm Electrophysiol 2009;2:652-9 «PMID: 19948506»PubMed
- Raatikainen MJ, Lindgren K. Uusien ryhmän III lääkkeiden asema rytmihäiriöiden hoidossa. Suom Lääkäril 2001;56:5101-6
- Raatikainen MJ. Is verapamil a double-edged sword in rate control of paroxysmal atrial fibrillation? Heart Rhythm 2010;7:584-5 «PMID: 20189494»PubMed
- Alboni P, Botto GL, Baldi N ym. Outpatient treatment of recent-onset atrial fibrillation with the "pill-in-the-pocket" approach. N Engl J Med 2004;351:2384-91 «PMID: 15575054»PubMed
- Airaksinen KE, Grönberg T, Nuotio I ym. Thromboembolic complications after cardioversion of acute atrial fibrillation: the FinCV (Finnish CardioVersion) study. J Am Coll Cardiol 2013;62:1187-92 «PMID: 23850908»PubMed
- European Heart Rhythm Association., European Association for Cardio-Thoracic Surgery., Camm AJ ym. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010;31:2369-429 «PMID: 20802247»PubMed
- Steffel J, Verhamme P, Potpara TS ym. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J 2018;39:1330-1393 «PMID: 29562325»PubMed
- Bjerkelund CJ, Orning OM. The efficacy of anticoagulant therapy in preventing embolism related to D.C. electrical conversion of atrial fibrillation. Am J Cardiol 1969;23:208-16 «PMID: 4180019»PubMed
- Arnold AZ, Mick MJ, Mazurek RP ym. Role of prophylactic anticoagulation for direct current cardioversion in patients with atrial fibrillation or atrial flutter. J Am Coll Cardiol 1992;19:851-5 «PMID: 1545081»PubMed
- Thibault B, Talajic M, Dubuc M ym. Thromboembolic events occur despite sinus rhythm maintenance in patients treated for atrial fibrillation: The Canadian Trial of Atrial Fibrillation experience. Can J Cardiol 2004;20:195-9 «PMID: 15010743»PubMed
- Biblo LA, Yuan Z, Quan KJ ym. Risk of stroke in patients with atrial flutter. Am J Cardiol 2001;87:346-9, A9 «PMID: 11165976»PubMed
- Corrado G, Santarone M, Beretta S ym. Early cardioversion of atrial fibrillation and atrial flutter guided by transoesophageal echocardiography: a single centre 8.5-year experience. Europace 2000;2:119-26 «PMID: 11225938»PubMed
- Klein AL, Grimm RA, Murray RD ym. Use of transesophageal echocardiography to guide cardioversion in patients with atrial fibrillation. N Engl J Med 2001;344:1411-20 «PMID: 11346805»PubMed
- Weigner MJ, Thomas LR, Patel U ym. Early cardioversion of atrial fibrillation facilitated by transesophageal echocardiography: short-term safety and impact on maintenance of sinus rhythm at 1 year. Am J Med 2001;110:694-702 «PMID: 11403753»PubMed
- Roijer A, Eskilsson J, Olsson B. Transoesophageal echocardiography-guided cardioversion of atrial fibrillation or flutter. Selection of a low-risk group for immediate cardioversion. Eur Heart J 2000;21:837-47 «PMID: 10781356»PubMed
- Bartel T, Erbel R, Acute Trial Investigators.. Transoesophageal echocardiography for immediate and safe cardioversion in patients with atrial fibrillation. Eur Heart J 2001;22:2041-4 «PMID: 11686658»PubMed
- Klein AL, Murray RD, Grimm RA. Role of transesophageal echocardiography-guided cardioversion of patients with atrial fibrillation. J Am Coll Cardiol 2001;37:691-704 «PMID: 11693739»PubMed
- Seto TB, Taira DA, Tsevat J ym. Cost-effectiveness of transesophageal echocardiographic-guided cardioversion: a decision analytic model for patients admitted to the hospital with atrial fibrillation. J Am Coll Cardiol 1997;29:122-30 «PMID: 8996304»PubMed
- Klein AL, Murray RD, Becker ER ym. Economic analysis of a transesophageal echocardiography-guided approach to cardioversion of patients with atrial fibrillation: the ACUTE economic data at eight weeks. J Am Coll Cardiol 2004;43:1217-24 «PMID: 15063433»PubMed
- Lévy S, Breithardt G, Campbell RW ym. Atrial fibrillation: current knowledge and recommendations for management. Working Group on Arrhythmias of the European Society of Cardiology. Eur Heart J 1998;19:1294-320 «PMID: 9792255»PubMed
- Kirchhof P, Camm AJ, Goette A ym. Early Rhythm-Control Therapy in Patients with Atrial Fibrillation. N Engl J Med 2020;383:1305-1316 «PMID: 32865375»PubMed
- Kirchhof P, Andresen D, Bosch R ym. Short-term versus long-term antiarrhythmic drug treatment after cardioversion of atrial fibrillation (Flec-SL): a prospective, randomised, open-label, blinded endpoint assessment trial. Lancet 2012;380:238-46 «PMID: 22713626»PubMed
- Raatikainen MJ. Rytmihäiriölääkkeiden kliininen käyttö. Kirjassa: Heikkilä J ym. (toim). Kardiologia. Kustannus Oy Duodecim, 2008; 2:s. 692-711
- Van Noord T, Tieleman RG, Bosker HA ym. Beta-blockers prevent subacute recurrences of persistent atrial fibrillation only in patients with hypertension. Europace 2004;6:343-50 «PMID: 15172659»PubMed
- Meng F, Yoshikawa T, Baba A ym. Beta-blockers are effective in congestive heart failure patients with atrial fibrillation. J Card Fail 2003;9:398-403 «PMID: 14583902»PubMed
- Kühlkamp V, Bosch R, Mewis C ym. Use of beta-blockers in atrial fibrillation. Am J Cardiovasc Drugs 2002;2:37-42 «PMID: 14727997»PubMed
- Page RL, Reiffel JA, Tavel ME. Asymptomatic atrial fibrillation: problems of management. Chest 2001;119:628-31 «PMID: 11171747»PubMed
- Page RL. beta-blockers for atrial fibrillation: must we consider asymptomatic arrhythmias? J Am Coll Cardiol 2000;36:147-50 «PMID: 10898426»PubMed
- Naccarelli GV, Dorian P, Hohnloser SH ym. Prospective comparison of flecainide versus quinidine for the treatment of paroxysmal atrial fibrillation/flutter. The Flecainide Multicenter Atrial Fibrillation Study Group. Am J Cardiol 1996;77:53A-59A «PMID: 8607392»PubMed
- Lee SH, Chen SA, Chiang CE ym. Comparisons of oral propafenone and quinidine as an initial treatment option in patients with symptomatic paroxysmal atrial fibrillation: a double-blind, randomized trial. J Intern Med 1996;239:253-60 «PMID: 8772625»PubMed
- Grey E, Silverman DI. Efficacy of type 1C antiarrhythmic agents for treatment of resistant atrial fibrillation. Pacing Clin Electrophysiol 1993;16:2235-40 «PMID: 7508600»PubMed
- Echt DS, Liebson PR, Mitchell LB ym. Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial. N Engl J Med 1991;324:781-8 «PMID: 1900101»PubMed
- Hughes MM, Trohman RG, Simmons TW ym. Flecainide therapy in patients treated for supraventricular tachycardia with near normal left ventricular function. Am Heart J 1992;123:408-12 «PMID: 1736577»PubMed
- Chimienti M, Cullen MT Jr, Casadei G. Safety of long-term flecainide and propafenone in the management of patients with symptomatic paroxysmal atrial fibrillation: report from the Flecainide and Propafenone Italian Study Investigators. Am J Cardiol 1996;77:60A-75A «PMID: 8607393»PubMed
- Anderson JL, Platt ML, Guarnieri T ym. Flecainide acetate for paroxysmal supraventricular tachyarrhythmias. The Flecainide Supraventricular Tachycardia Study Group. Am J Cardiol 1994;74:578-84 «PMID: 8074041»PubMed
- Wehling M. Meta-analysis of flecainide safety in patients with supraventricular arrhythmias. Arzneimittelforschung 2002;52:507-14 «PMID: 12189773»PubMed
- Joglar JA, Chung MK, Armbruster AL, ym. 2023 ACC/AHA/ACCP/HRS Guideline for the Diagnosis and Management of Atrial Fibrillation: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation 2024;149(1):e1-e156 «PMID: 38033089»PubMed
- Le Heuzey JY, De Ferrari GM, Radzik D ym. A short-term, randomized, double-blind, parallel-group study to evaluate the efficacy and safety of dronedarone versus amiodarone in patients with persistent atrial fibrillation: the DIONYSOS study. J Cardiovasc Electrophysiol 2010;21:597-605 «PMID: 20384650»PubMed
- Roy D, Talajic M, Dorian P ym. Amiodarone to prevent recurrence of atrial fibrillation. Canadian Trial of Atrial Fibrillation Investigators. N Engl J Med 2000;342:913-20 «PMID: 10738049»PubMed
- Vitolo E, Tronci M, Larovere MT ym. Amiodarone versus quinidine in the prophylaxis of atrial fibrillation. Acta Cardiol 1981;36:431-44 «PMID: 7039195»PubMed
- Zarembski DG, Nolan PE Jr, Slack MK ym. Treatment of resistant atrial fibrillation. A meta-analysis comparing amiodarone and flecainide. Arch Intern Med 1995;155:1885-91 «PMID: 7677555»PubMed
- Singh BN. Amiodarone: the expanding antiarrhythmic role and how to follow a patient on chronic therapy. Clin Cardiol 1997;20:608-18 «PMID: 9220176»PubMed
- Siddoway LA. Amiodarone: guidelines for use and monitoring. Am Fam Physician 2003;68:2189-96 «PMID: 14677664»PubMed
- Connolly SJ. Evidence-based analysis of amiodarone efficacy and safety. Circulation 1999;100:2025-34 «PMID: 10556230»PubMed
- Hohnloser SH, Klingenheben T, Singh BN. Amiodarone-associated proarrhythmic effects. A review with special reference to torsade de pointes tachycardia. Ann Intern Med 1994;121:529-35 «PMID: 8067651»PubMed
- Julian DG, Camm AJ, Frangin G ym. Randomised trial of effect of amiodarone on mortality in patients with left-ventricular dysfunction after recent myocardial infarction: EMIAT. European Myocardial Infarct Amiodarone Trial Investigators. Lancet 1997;349:667-74 «PMID: 9078197»PubMed
- Cairns JA, Connolly SJ, Roberts R ym. Randomised trial of outcome after myocardial infarction in patients with frequent or repetitive ventricular premature depolarisations: CAMIAT. Canadian Amiodarone Myocardial Infarction Arrhythmia Trial Investigators. Lancet 1997;349:675-82 «PMID: 9078198»PubMed
- Doval HC, Nul DR, Grancelli HO ym. Randomised trial of low-dose amiodarone in severe congestive heart failure. Grupo de Estudio de la Sobrevida en la Insuficiencia Cardiaca en Argentina (GESICA) Lancet 1994;344:493-8 «PMID: 7914611»PubMed
- Deedwania PC, Singh BN, Ellenbogen K ym. Spontaneous conversion and maintenance of sinus rhythm by amiodarone in patients with heart failure and atrial fibrillation: observations from the veterans affairs congestive heart failure survival trial of antiarrhythmic therapy (CHF-STAT). The Department of Veterans Affairs CHF-STAT Investigators. Circulation 1998;98:2574-9 «PMID: 9843465»PubMed
- Piccini JP, Hasselblad V, Peterson ED ym. Comparative efficacy of dronedarone and amiodarone for the maintenance of sinus rhythm in patients with atrial fibrillation. J Am Coll Cardiol 2009;54:1089-95 «PMID: 19744618»PubMed
- Lafuente-Lafuente C, Mouly S, Longas-Tejero MA ym. Antiarrhythmics for maintaining sinus rhythm after cardioversion of atrial fibrillation. Cochrane Database Syst Rev 2007;4:CD005049 «PMID: 17943835»PubMed
- Freemantle N, Lafuente-Lafuente C, Mitchell S ym. Mixed treatment comparison of dronedarone, amiodarone, sotalol, flecainide, and propafenone, for the management of atrial fibrillation. Europace 2011;13:329-45 «PMID: 21227948»PubMed
- Køber L, Torp-Pedersen C, McMurray JJ ym. Increased mortality after dronedarone therapy for severe heart failure. N Engl J Med 2008;358:2678-87 «PMID: 18565860»PubMed
- Connolly SJ, Camm AJ, Halperin JL ym. Dronedarone in high-risk permanent atrial fibrillation. N Engl J Med 2011;365:2268-76 «PMID: 22082198»PubMed
- Juul-Möller S, Edvardsson N, Rehnqvist-Ahlberg N. Sotalol versus quinidine for the maintenance of sinus rhythm after direct current conversion of atrial fibrillation. Circulation 1990;82:1932-9 «PMID: 2242519»PubMed
- Bellandi F, Simonetti I, Leoncini M ym. Long-term efficacy and safety of propafenone and sotalol for the maintenance of sinus rhythm after conversion of recurrent symptomatic atrial fibrillation. Am J Cardiol 2001;88:640-5 «PMID: 11564387»PubMed
- Plewan A, Lehmann G, Ndrepepa G ym. Maintenance of sinus rhythm after electrical cardioversion of persistent atrial fibrillation; sotalol vs bisoprolol. Eur Heart J 2001;22:1504-10 «PMID: 11482924»PubMed
- Brendorp B, Pedersen O, Torp-Pedersen C ym. A benefit-risk assessment of class III antiarrhythmic agents. Drug Saf 2002;25:847-65 «PMID: 12241126»PubMed
- Coplen SE, Antman EM, Berlin JA ym. Efficacy and safety of quinidine therapy for maintenance of sinus rhythm after cardioversion. A meta-analysis of randomized control trials. Circulation 1990;82:1106-16 «PMID: 2144796»PubMed
- Patten M, Maas R, Bauer P ym. Suppression of paroxysmal atrial tachyarrhythmias--results of the SOPAT trial. Eur Heart J 2004;25:1395-404 «PMID: 15321697»PubMed
- Fetsch T, Bauer P, Engberding R ym. Prevention of atrial fibrillation after cardioversion: results of the PAFAC trial. Eur Heart J 2004;25:1385-94 «PMID: 15302102»PubMed
- Madrid AH, Peng J, Zamora J ym. The role of angiotensin receptor blockers and/or angiotensin converting enzyme inhibitors in the prevention of atrial fibrillation in patients with cardiovascular diseases: meta-analysis of randomized controlled clinical trials. Pacing Clin Electrophysiol 2004;27:1405-10 «PMID: 15511250»PubMed
- Savelieva I, Camm J. Statins and polyunsaturated fatty acids for treatment of atrial fibrillation. Nat Clin Pract Cardiovasc Med 2008;5:30-41 «PMID: 18094671»PubMed
- Kowey PR, Reiffel JA, Ellenbogen KA ym. Efficacy and safety of prescription omega-3 fatty acids for the prevention of recurrent symptomatic atrial fibrillation: a randomized controlled trial. JAMA 2010;304:2363-72 «PMID: 21078810»PubMed
- Schnabel RB, Yin X, Gona P ym. 50 year trends in atrial fibrillation prevalence, incidence, risk factors, and mortality in the Framingham Heart Study: a cohort study. Lancet 2015;386:154-62 «PMID: 25960110»PubMed
- Miller JD, Aronis KN, Chrispin J ym. Obesity, Exercise, Obstructive Sleep Apnea, and Modifiable Atherosclerotic Cardiovascular Disease Risk Factors in Atrial Fibrillation. J Am Coll Cardiol 2015;66:2899-906 «PMID: 26718677»PubMed
- Nalliah CJ, Sanders P, Kottkamp H ym. The role of obesity in atrial fibrillation. Eur Heart J 2016;37:1565-72 «PMID: 26371114»PubMed
- Cambeiro G, Cristina M, Mañero R ym. Review Of Obesity And Atrial Fibrillation: Exploring The Paradox. J Atr Fibrillation 2015;8:1259 «PMID: 27957191»PubMed
- Goudis CA, Korantzopoulos P, Ntalas IV ym. Obesity and atrial fibrillation: A comprehensive review of the pathophysiological mechanisms and links. J Cardiol 2015;66:361-9 «PMID: 25959929»PubMed
- Yao Y, Liu F, Wang Y, ym. Lipid levels and risk of new-onset atrial fibrillation: A systematic review and dose-response meta-analysis. Clin Cardiol 2020;43(9):935-943 «PMID: 32720403»PubMed
- Andersen HR, Nielsen JC, Thomsen PE ym. Long-term follow-up of patients from a randomised trial of atrial versus ventricular pacing for sick-sinus syndrome. Lancet 1997;350:1210-6 «PMID: 9652562»PubMed
- Kerr CR, Connolly SJ, Abdollah H ym. Canadian Trial of Physiological Pacing: Effects of physiological pacing during long-term follow-up. Circulation 2004;109:357-62 «PMID: 14707022»PubMed
- Nielsen JC, Kristensen L, Andersen HR ym. A randomized comparison of atrial and dual-chamber pacing in 177 consecutive patients with sick sinus syndrome: echocardiographic and clinical outcome. J Am Coll Cardiol 2003;42:614-23 «PMID: 12932590»PubMed
- Wijesuriya N, Mehta V, De Vere F, ym. The role of conduction system pacing in patients with atrial fibrillation. Front Cardiovasc Med 2023;10():1187754 «PMID: 37304966»PubMed
- Burns JL, Sears SF, Sotile R ym. Do patients accept implantable atrial defibrillation therapy? Results from the Patient Atrial Shock Survey of Acceptance and Tolerance (PASSAT) Study. J Cardiovasc Electrophysiol 2004;15:286-91 «PMID: 15030417»PubMed
- Boodhoo LE, Mitchell AR, Sulke N. The clinical and electrophysiological implications of asymptomatic atrial fibrillation. Minerva Cardioangiol 2004;52:547-52 «PMID: 15729215»PubMed
- Packer DL, Mark DB, Robb RA ym. Effect of Catheter Ablation vs Antiarrhythmic Drug Therapy on Mortality, Stroke, Bleeding, and Cardiac Arrest Among Patients With Atrial Fibrillation: The CABANA Randomized Clinical Trial. JAMA 2019;321:1261-1274 «PMID: 30874766»PubMed
- Sohns C, Fox H, Marrouche NF, ym. Catheter Ablation in End-Stage Heart Failure with Atrial Fibrillation. N Engl J Med 2023;389(15):1380-1389 «PMID: 37634135»PubMed
- Cosedis Nielsen J, Johannessen A, Raatikainen P ym. Radiofrequency ablation as initial therapy in paroxysmal atrial fibrillation. N Engl J Med 2012;367:1587-95 «PMID: 23094720»PubMed
- Hakalahti A, Biancari F, Nielsen JC ym. Radiofrequency ablation vs. antiarrhythmic drug therapy as first line treatment of symptomatic atrial fibrillation: systematic review and meta-analysis. Europace 2015;17:370-8 «PMID: 25643988»PubMed
- Mark DB, Anstrom KJ, Sheng S ym. Effect of Catheter Ablation vs Medical Therapy on Quality of Life Among Patients With Atrial Fibrillation: The CABANA Randomized Clinical Trial. JAMA 2019;321:1275-1285 «PMID: 30874716»PubMed
- Blomström-Lundqvist C, Gizurarson S, Schwieler J ym. Effect of Catheter Ablation vs Antiarrhythmic Medication on Quality of Life in Patients With Atrial Fibrillation: The CAPTAF Randomized Clinical Trial. JAMA 2019;321:1059-1068 «PMID: 30874754»PubMed
- Nielsen JC, Johannessen A, Raatikainen P ym. Long-term efficacy of catheter ablation as first-line therapy for paroxysmal atrial fibrillation: 5-year outcome in a randomised clinical trial. Heart 2017;103:368-376 «PMID: 27566295»PubMed
- Raatikainen MJ, Hakalahti A, Uusimaa P ym. Radiofrequency catheter ablation maintains its efficacy better than antiarrhythmic medication in patients with paroxysmal atrial fibrillation: On-treatment analysis of the randomized controlled MANTRA-PAF trial. Int J Cardiol 2015;198:108-14 «PMID: 26163901»PubMed
- Cappato R, Calkins H, Chen SA ym. Updated worldwide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation. Circ Arrhythm Electrophysiol 2010;3:32-8 «PMID: 19995881»PubMed
- Piccini JP, Lopes RD, Kong MH ym. Pulmonary vein isolation for the maintenance of sinus rhythm in patients with atrial fibrillation: a meta-analysis of randomized, controlled trials. Circ Arrhythm Electrophysiol 2009;2:626-33 «PMID: 20009077»PubMed
- Gjesdal K, Vist GE, Bugge E ym. Curative ablation for atrial fibrillation: a systematic review. Scand Cardiovasc J 2008;42:3-8 «PMID: 18273730»PubMed
- Calkins H, Reynolds MR, Spector P ym. Treatment of atrial fibrillation with antiarrhythmic drugs or radiofrequency ablation: two systematic literature reviews and meta-analyses. Circ Arrhythm Electrophysiol 2009;2:349-61 «PMID: 19808490»PubMed
- Schmidt M, Dorwarth U, Andresen D ym. Cryoballoon versus RF ablation in paroxysmal atrial fibrillation: results from the German Ablation Registry. J Cardiovasc Electrophysiol 2014;25:1-7 «PMID: 24134539»PubMed
- Reddy VY, Gerstenfeld EP, Natale A, ym. Pulsed Field or Conventional Thermal Ablation for Paroxysmal Atrial Fibrillation. N Engl J Med 2023;389(18):1660-1671 «PMID: 37634148»PubMed
- Weerasooriya R, Jaïs P, Le Heuzey JY ym. Cost analysis of catheter ablation for paroxysmal atrial fibrillation. Pacing Clin Electrophysiol 2003;26:292-4 «PMID: 12687831»PubMed
- Andrikopoulos G, Tzeis S, Maniadakis N ym. Cost-effectiveness of atrial fibrillation catheter ablation. Europace 2009;11:147-51 «PMID: 19098290»PubMed
- Aronsson M, Walfridsson H, Janzon M ym. The cost-effectiveness of radiofrequency catheter ablation as first-line treatment for paroxysmal atrial fibrillation: results from a MANTRA-PAF substudy. Europace 2015;17:48-55 «PMID: 25341739»PubMed
- Spragg DD, Dalal D, Cheema A ym. Complications of catheter ablation for atrial fibrillation: incidence and predictors. J Cardiovasc Electrophysiol 2008;19:627-31 «PMID: 18462327»PubMed
- Blomström-Lundqvist C, Scheinman MM, Aliot EM ym. ACC/AHA/ESC guidelines for the management of patients with supraventricular arrhythmias--executive summary. a report of the American college of cardiology/American heart association task force on practice guidelines and the European society of cardiology committee for practice guidelines (writing committee to develop guidelines for the management of patients with supraventricular arrhythmias) developed in collaboration with NASPE-Heart Rhythm Society. J Am Coll Cardiol 2003;42:1493-531 «PMID: 14563598»PubMed
- Nabar A, Rodriguez LM, Timmermans C ym. Effect of right atrial isthmus ablation on the occurrence of atrial fibrillation: observations in four patient groups having type I atrial flutter with or without associated atrial fibrillation. Circulation 1999;99:1441-5 «PMID: 10086967»PubMed
- Ahvenvaara T, Uusimaa P, Huikuri HV, Raatikainen MJP. Eteislepatuksen katetriablaatiohoito. Suom Lääkäril 2004;59:2355-61
- Prasad SM, Maniar HS, Camillo CJ ym. The Cox maze III procedure for atrial fibrillation: long-term efficacy in patients undergoing lone versus concomitant procedures. J Thorac Cardiovasc Surg 2003;126:1822-8 «PMID: 14688693»PubMed
- Cox JL. Cardiac surgery for arrhythmias. J Cardiovasc Electrophysiol 2004;15:250-62 PMID: 15028063
- McLellan CS, Abdollah H, Brennan FJ ym. Atrial fibrillation in the pacemaker clinic. Can J Cardiol 2003;19:492-4 «PMID: 12717483»PubMed
- Boersma LV, Castella M, van Boven W ym. Atrial fibrillation catheter ablation versus surgical ablation treatment (FAST): a 2-center randomized clinical trial. Circulation 2012;125:23-30 «PMID: 22082673»PubMed
- Sethi NJ, Nielsen EE, Safi S ym. Digoxin for atrial fibrillation and atrial flutter: A systematic review with meta-analysis and trial sequential analysis of randomised clinical trials. PLoS One 2018;13:e0193924 «PMID: 29518134»PubMed
- Castellá M, Pereda D, Mestres CA ym. Thoracoscopic pulmonary vein isolation in patients with atrial fibrillation and failed percutaneous ablation. J Thorac Cardiovasc Surg 2010;140:633-8 «PMID: 20117799»PubMed
- Levy T, Walker S, Mason M ym. Importance of rate control or rate regulation for improving exercise capacity and quality of life in patients with permanent atrial fibrillation and normal left ventricular function: a randomised controlled study. Heart 2001;85:171-8 «PMID: 11156667»PubMed
- Van Gelder IC, Van Veldhuisen DJ, Crijns HJ ym. RAte Control Efficacy in permanent atrial fibrillation: a comparison between lenient versus strict rate control in patients with and without heart failure. Background, aims, and design of RACE II. Am Heart J 2006;152:420-6 «PMID: 16923407»PubMed
- Olshansky B, Rosenfeld LE, Warner AL ym. The Atrial Fibrillation Follow-up Investigation of Rhythm Management (AFFIRM) study: approaches to control rate in atrial fibrillation. J Am Coll Cardiol 2004;43:1201-8 «PMID: 15063430»PubMed
- Leclercq JF, Rosengarten MD, Kural S ym. Effects of intrinsic sympathetic activity of beta-blockers on SA and AV nodes in man. Eur J Cardiol 1981;12:367-75 «PMID: 6113145»PubMed
- Al-Khateeb M, Qureshi WT, Odeh R ym. The impact of digoxin on mortality in patients with chronic systolic heart failure: A propensity-matched cohort study. Int J Cardiol 2017;228:214-218 «PMID: 27865188»PubMed
- Wang ZQ, Zhang R, Chen MT ym. Digoxin Is Associated With Increased All-cause Mortality in Patients With Atrial Fibrillation Regardless of Concomitant Heart Failure: A Meta-analysis. J Cardiovasc Pharmacol 2015;66:270-5 «PMID: 26348825»PubMed
- Vijayaraman P, Chung MK, Dandamudi G ym. His Bundle Pacing. J Am Coll Cardiol 2018;72:927-947 «PMID: 30115232»PubMed
- Chao TF, Liu CJ, Tuan TC ym. Rate-control treatment and mortality in atrial fibrillation. Circulation 2015;132:1604-12 «PMID: 26384160»PubMed
- Gheorghiade M, Fonarow GC, van Veldhuisen DJ ym. Lack of evidence of increased mortality among patients with atrial fibrillation taking digoxin: findings from post hoc propensity-matched analysis of the AFFIRM trial. Eur Heart J 2013;34:1489-97 «PMID: 23592708»PubMed
- Davy JM, Herold M, Hoglund C ym. Dronedarone for the control of ventricular rate in permanent atrial fibrillation: the Efficacy and safety of dRonedArone for the cOntrol of ventricular rate during atrial fibrillation (ERATO) study. Am Heart J 2008;156:527.e1-9 «PMID: 18760136»PubMed
- Singh BN, Connolly SJ, Crijns HJ ym. Dronedarone for maintenance of sinus rhythm in atrial fibrillation or flutter. N Engl J Med 2007;357:987-99 «PMID: 17804843»PubMed
- Aliot E ym. Catheter ablation or modulation of the atrioventricular node. Kirjassa: Zipes DP, Haissaguerre M (toim.). Armonk: Futura Publishing Company, Inc., 2002; s. 205-23
- Nowinski K, Gadler F, Jensen-Urstad M ym. Transient proarrhythmic state following atrioventricular junctional radiofrequency ablation. Pacing Clin Electrophysiol 2002;25:291-9 «PMID: 11990658»PubMed
- Wood KA, Eisenberg SJ, Kalman JM ym. Risk of thromboembolism in chronic atrial flutter. Am J Cardiol 1997;79:1043-7 «PMID: 9114761»PubMed
- Cairns JA. Stroke prevention in atrial fibrillation trial. Circulation 1991;84:933-5 «PMID: 1860238»PubMed
- Pollack CV Jr, Reilly PA, Eikelboom J ym. Idarucizumab for Dabigatran Reversal. N Engl J Med 2015;373:511-20 «PMID: 26095746»PubMed
- Connolly SJ, Crowther M, Eikelboom JW ym. Full Study Report of Andexanet Alfa for Bleeding Associated with Factor Xa Inhibitors. N Engl J Med 2019;380:1326-1335 «PMID: 30730782»PubMed
- Siegal DM, Curnutte JT, Connolly SJ ym. Andexanet Alfa for the Reversal of Factor Xa Inhibitor Activity. N Engl J Med 2015;373:2413-24 «PMID: 26559317»PubMed
- Raatikainen MJP. Oraalinen antikoagulaatiohoito sydänsairauksissa. Suom Lääkäril 2019:74:443-8
- Connolly SJ, Ezekowitz MD, Yusuf S ym. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009;361:1139-51 «PMID: 19717844»PubMed
- Granger CB, Alexander JH, McMurray JJ ym. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2011;365:981-92 «PMID: 21870978»PubMed
- Giugliano RP, Ruff CT, Braunwald E ym. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2013;369:2093-104 «PMID: 24251359»PubMed
- Bohula EA, Giugliano RP, Ruff CT ym. Impact of Renal Function on Outcomes With Edoxaban in the ENGAGE AF-TIMI 48 Trial. Circulation 2016;134:24-36 «PMID: 27358434»PubMed
- Patel MR, Mahaffey KW, Garg J ym. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med 2011;365:883-91 «PMID: 21830957»PubMed
- Lehto M, Luojus A, Halminen O, ym. Time-in-therapeutic-range defined warfarin and direct oral anticoagulants in atrial fibrillation: a Nationwide Cohort Study. Ann Med 2024;56(1):2364825 «PMID: 38873855»PubMed
- Nilsson GH, Björholt I, Krakau I. Anticoagulant treatment of patients with chronic atrial fibrillation in primary health care in Sweden--a retrospective study of incidence and quality in a registered population. Fam Pract 2004;21:612-6 «PMID: 15465879»PubMed
- Connolly SJ, Eikelboom J, Joyner C ym. Apixaban in patients with atrial fibrillation. N Engl J Med 2011;364:806-17 «PMID: 21309657»PubMed
- Zalesak M, Siu K, Francis K ym. Higher persistence in newly diagnosed nonvalvular atrial fibrillation patients treated with dabigatran versus warfarin. Circ Cardiovasc Qual Outcomes 2013;6:567-74 «PMID: 23922182»PubMed
- Gorst-Rasmussen A, Skjøth F, Larsen TB ym. Dabigatran adherence in atrial fibrillation patients during the first year after diagnosis: a nationwide cohort study. J Thromb Haemost 2015;13:495-504 «PMID: 25594442»PubMed
- Joosten LPT, van Doorn S, van de Ven PM, ym. Safety of Switching From a Vitamin K Antagonist to a Non-Vitamin K Antagonist Oral Anticoagulant in Frail Older Patients With Atrial Fibrillation: Results of the FRAIL-AF Randomized Controlled Trial. Circulation 2024;149(4):279-289 «PMID: 37634130»PubMed
- Aryana A, Singh SK, Singh SM ym. Association between incomplete surgical ligation of left atrial appendage and stroke and systemic embolization. Heart Rhythm 2015;12:1431-7 «PMID: 25998141»PubMed
- Whitlock RP, Belley-Cote EP, Paparella D, ym. Left Atrial Appendage Occlusion during Cardiac Surgery to Prevent Stroke. N Engl J Med 2021;384(22):2081-2091 «PMID: 33999547»PubMed

