Epilepsiat ja kuumekouristukset (lapset ja nuoret)
Miten viitata Käypä hoito -suositukseen? «K1»1
Keskeinen sisältö
- Lapsuusiässä alkavat epilepsiat ovat etiologialtaan, oireiltaan ja ennusteeltaan monimuotoinen neurologinen sairausryhmä, jossa hyvän hoidon edellytyksenä on mahdollisimman tarkka diagnoosi.
- Epilepsiadiagnoosi perustuu kohtausanamneesiin, jota täydennetään EEG- ja kuvantamistutkimuksilla. Joissain tapauksissa geenitutkimukset auttavat hoidon suunnittelussa.
- Epilepsian esiintyvyys alle 16-vuotiailla suomalaisilla on noin 3/1000.
- Epilepsiaoireyhtymän tunnistaminen auttaa hoidon valinnassa ja lisätutkimusten tarpeen ja epilepsian ennusteen arvioinnissa.
- Lääkehoidon valinta riippuu epilepsiaoireyhtymästä. Jos taas oireyhtymä ei ole tunnistettavissa, valinta tehdään epilepsiatyypin mukaan siten, että otetaan huomioon haittavaikutusriskit.
- Hoidon tavoitteena on kohtauksettomuus ilman merkittäviä haittavaikutuksia.
- Lapsuusiän vaikeahoitoisissa epilepsioissa tulee arvioida epilepsiakirurgian ja dieettihoidon mahdollisuudet.
- Hoidossa on huomioitava kohtausten lisäksi muut lapsen kasvuun, kehitykseen ja toimintakykyyn vaikuttavat seikat.
- Vaikea epilepsia haittaa usein lapsen kehitystä, joten tehokas ja varhainen diagnostiikka ja hoitomahdollisuuksien arvioiminen ovat tärkeitä.
- Kuumekouristuksia esiintyy 7 vuoden ikään mennessä 2–5 %:lla lapsista.
- Kuumekouristuksen estoon ei suositella jatkuvaa epilepsialääkitystä.
Tiivistelmä ja potilasversio
- Suosituksen tiivistelmä «Epilepsiat ja kuumekouristukset (lapset)»1 ja lyhyt abstrakti englanniksi «Epilepsy and febrile seizures (children)»2
- Suosituksen yleiskielinen potilasversio suomeksi «Epilepsiat ja kuumekouristukset lapsilla ja nuorilla»3 ja ruotsiksi «Epilepsi och feberkramper hos barn»4
Tavoitteet
- Suosituksen tavoitteena on yhtenäistää hoitokäytäntöjä ja edistää lasten ja nuorten epilepsioiden ja kuumekouristusten tutkimusnäyttöön perustuvien suositusten mukaista diagnostiikkaa ja hoitoa.
Kohderyhmät
- Suositus on tarkoitettu kaikille lasten epilepsioita ja kuumekouristuksia hoitaville terveydenhuollon ammattilaisille.
Aiheen rajaus
- Suositus käsittelee kuumekouristuksia ja alle 16-vuotiaiden lasten ja nuorten epilepsioita.
- Yli 16-vuotiaiden epilepsian diagnostiikkaa ja hoitoa käsitellään Käypä hoito -suosituksessa
Epilepsiat (aikuiset) «Epilepsiat (aikuiset)»5 .
- Paikallisalkuisten epilepsioiden hoidossa käytettävien lääkkeiden tehon arvioinnissa on jouduttu suurelta osin turvautumaan pääasiassa aikuisilla tehtyihin tutkimuksiin niin sanotun ekstrapolaation avulla «Paikallisalkuisen epilepsian hoitoon tarkoitettujen antiepileptisten lääkkeiden aikuisilla osoitetun tehon ekstrapolaatio lapsipotilaisiin»1. Näytönaste on näissä tapauksissa ilmaistu lisämaininnalla ’aikuisilla’.
- Suosituksen ulkopuolelle on jätetty
- alle kuukauden ikäisten kohtausoireet, koska niiden etiologia, ennuste ja hoito ovat oleellisesti erilaiset kuin muissa ikäryhmissä
- eteneviin aivosairauksiin (esim. neuronaalisiin seroidilipofuskinooseihin eli NCL-tauteihin) liittyvät epilepsiat, koska niissä muut neurologiset oireet ovat hallitsevampia «Gaily E. Kuinka hoidan kehitysvammaisen epilepsiaa...»1.
- kohtausoireiden akuutin vaiheen diagnostiikka ja hoito, jota käsitellään Käypä hoito -suosituksessa Epileptinen kohtaus (pitkittynyt) «Pitkittynyt epileptinen kohtaus ja status epilepticus»6, «Epileptinen kohtaus (pitkittynyt; status epileptic...»2.
Määritelmät ja kliiniset oireet
Epilepsiakohtauksen määritelmä ja oireet
- Epileptinen kohtaus on ohimenevä aivotoiminnan häiriö, jonka syynä on laajuudeltaan vaihtelevalla anatomisella aivoalueella tapahtuva poikkeava, liiallinen tai synkroninen hermosolujen sähköinen toiminta «Engel J Jr, International League Against Epilepsy ...»3, «Fisher RS, van Emde Boas W, Blume W ym. Epileptic ...»4, «Berg AT, Berkovic SF, Brodie MJ ym. Revised termin...»5.
- Kohtausten kesto vaihtelee yleensä muutamista sekunneista muutamiin minuutteihin, mutta pitkittynyt kohtaus voi kestää tunteja tai jopa vuorokausia. Ks. Käypä hoito -suositus Epileptinen kohtaus (pitkittynyt) «Pitkittynyt epileptinen kohtaus ja status epilepticus»6, «Epileptinen kohtaus (pitkittynyt; status epileptic...»2.
- Epileptisen kohtauksen kliinisiä oireita voivat olla muun muassa «International League Against Epilepsy, http://www....»6
- tajunnan osittainen tai täydellinen hämärtyminen (tajunta voi myös pysyä normaalina)
- tahdosta riippumattomat motoriset oireet, kuten rytminen nykiminen, jäykistyminen, yksittäiset lihasnykäykset tai lihasvelttous
- automatismit, esimerkiksi nieleskely, hypistely ja stereotyyppinen liikehdintä
- itsestään syntyvät aistielämykset (näkö-, kuulo-, tunto-, maku- ja hajuaistimukset)
- affektiiviset ilmiöt (esim. pelko)
- paikalliset inhibitoriset oireet, kuten kyvyttömyys puhua tai ylläpitää raajan asentoa.
- Epilepsian ensimmäinen havaittu oire alle kouluikäisellä lapsella voi olla myös kehityksen hidastuminen tai puheen taantuminen.
Epilepsian määritelmä
- Epilepsia on aivojen sairaus, jossa potilaalla on pitkäkestoinen taipumus saada epileptisiä kohtauksia ja johon saattaa liittyä myös muita neurologisia, kognitiivisia, psyykkisiä tai sosiaalisia toimintakyvyn ongelmia «Fisher RS, van Emde Boas W, Blume W ym. Epileptic ...»4.
Epilepsiaoireyhtymän määritelmä
- Epilepsiaoireyhtymällä tarkoitetaan oirekokonaisuutta, jossa tietyt kohtaustyypit, EEG-löydökset ja kuvantamislöydökset esiintyvät yhdessä. Sillä on usein myös tyypillinen epilepsian alkamisikä ja ennuste, kohtauksia laukaisevat tekijät ja kohtauksien esiintymisen vuorokausivaihtelu. Epilepsiaoireyhtymään liittyy usein tyypillisiä lisäsairauksia ja oireita, kuten oppimisvaikeuksia ja psyykkisiä oireita. Epilepsiaoireyhtymän tunnistaminen vaikuttaa etiologisiin tutkimuksiin, hoidon valintaan ja ennusteen arviointiin «Scheffer IE, Berkovic S, Capovilla G ym. ILAE clas...»7.
Vaikea epilepsia
- Vaikea epilepsia on tila, jossa asianmukaisesta lääkehoidosta huolimatta esiintyy merkittäviä arkielämää haittaavia epilepsiaan liittyviä oireita, kuten toistuvia kohtauksia, kognitiivisia tai käyttäytymisen ongelmia, kehityksen hidastumista tai hoidon haittavaikutuksia. "Asianmukaisesta lääkehoidosta huolimatta" tarkoittaa, ettei kahdella kohtaustyypin tai epilepsiaoireyhtymän mukaan oikein valitulla ja riittävällä annoksella käytetyllä lääkityksellä (ainoana lääkkeenä tai yhdistelmälääkityksenä) ole saavutettu kohtauksettomuutta «STM nimeämä vaikean epilepsian diagnostiikan ja ho...»8.
Epilepsiadiagnoosi
- Epilepsiadiagnoosi edellyttää, että a) potilaalla on ollut vähintään kaksi ilman merkittäviä altistavia tekijöitä esiintynyttä epileptistä kohtausta, joiden välillä on ollut yli 24 tuntia, b) potilaalla on ollut yksi ilman altistavia tekijöitä ilmennyt epileptinen kohtaus ja hänen aivoissaan havaitaan jokin pitkäaikainen kohtauksille altistava tekijä, jonka vuoksi kohtausten uusimisriski on yli 60 % seuraavan 10 vuoden aikana (eli sama kuin kahden kohtauksen jälkeen), tai c) potilaalle tehdään jonkin epilepsiaoireyhtymän diagnoosi «Fisher RS, Acevedo C, Arzimanoglou A ym. ILAE offi...»9.
Luokittelu ja syyt
Kuva 1. Epilepsioiden luokittelu ILAE:n mukaan (mukailtu lähteestä «Scheffer IE, Berkovic S, Capovilla G ym. ILAE clas...»7, «Epilepsioiden luokittelu ILAE:n mukaan»1)
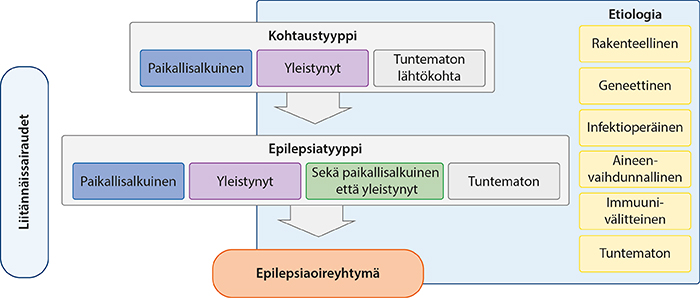
- Epilepsiat ovat etiologialtaan, alkamisiältään, oireiltaan ja ennusteeltaan monimuotoisia neurologisia sairauksia.
- Epilepsioiden luokittelu on portaittainen prosessi, jossa ensin määritetään kohtaustyyppi,
sen jälkeen epilepsiatyyppi ja sitten mahdollinen epilepsiaoireyhtymä. EEG:tä käytetään
tukena luokittelussa. Lisäksi määritetään aina myös epilepsian taustasyy ja liitännäissairaudet
«Scheffer IE, Berkovic S, Capovilla G ym. ILAE clas...»7.
- Luokittelu voi olla etenkin alkuvaiheessa vaikeaa, jos potilaalla esimerkiksi on pelkästään tajuttomuus-kouristuskohtauksia ja EEG-löydös ja aivojen kuvantamislöydös ovat normaaleja.
- Epilepsiat luokitellaan paikallisalkuisiin epilepsioihin, yleistyneisiin epilepsioihin,
epilepsioihin, joissa on sekä paikallisalkuisia että yleistyneitä piirteitä, ja epilepsioihin,
joiden tyyppiä ei pystytä määrittämään
- Paikallisalkuiset kohtaukset alkavat paikallisesti vain yhteen aivopuoliskoon rajoittuvassa hermoverkostossa. Purkaus voi kuitenkin myöhemmin levitä molempiin aivopuoliskoihin ja kohtaus voi edetä tajuttomuus-kouristus-kohtaukseksi (paikallisalkuinen tajuttomuus-kouristuskohtaus).
- Yleistyneissä kohtauksissa purkaukset alkavat ja leviävät heti molempiin aivopuoliskoihin ja kliiniset piirteet ja EEG-löydös ilmentävät molempien aivopuoliskojen tai niiden osien yhtäaikaista aktivoitumista kohtauksen alusta lähtien.
- Lähtökohdaltaan tuntemattomina pidetään kohtauksia, joista ei ole riittävästi tietoa niiden luokittelemiseksi paikallisalkuiseksi tai yleistyneeksi. Kohtausten luokitusta tulisi tällöin pyrkiä säännöllisin välein arvioimaan uudelleen.
- Epilepsian syiksi luetaan «Scheffer IE, Berkovic S, Capovilla G ym. ILAE clas...»7
- rakenteelliset syyt (sekä synnynnäiset, kuten aivojen kuorikerroksen kehityshäiriö, että hankinnaiset syyt, kuten perinataalinen aivovaurio)
- geneettiset syyt
- Geneettisellä epilepsialla tarkoitetaan sitä, että joko tunnetulla tai oletetulla geenivariantilla tai -varianteilla on merkittävä vaikutus epilepsian synnyssä ja epilepsiakohtaukset ovat sairauden keskeinen ilmentymä «Scheffer IE, Berkovic S, Capovilla G ym. ILAE clas...»7. Tällaisia ovat yhden tai usean tunnetun geenivirheen aiheuttamat epilepsiat, epilepsiat, joissa väestötutkimusten perusteella tiedetään olevan geneettinen tausta, vaikka yksittäisiä vaikuttavia geenejä ei toistaiseksi tunnetakaan (esim. lapsuusiän itsestään rajoittuvat epilepsiat, kuten lapsuusiän poissaoloepilepsia ja niin sanottu rolandinen epilepsia, sekä nuoruusiän myoklooninen epilepsia), ja sukuanamneesin perusteella autosomaalisesti dominantisti periytyvät epilepsiat.
- infektioperäiset syyt
- Epilepsia johtuu suoraan infektion aiheuttamasta aivovauriosta ja kohtaukset ovat sairauden ydinoire. Epilepsia voi ilmetä vasta infektion akuutin vaiheen jälkeen
- aineenvaihdunnalliset syyt
- Epilepsia johtuu suoraan tunnetusta tai oletetusta aineenvaihduntasairaudesta, ja epilepsiakohtaukset ovat häiriön ydinoire.
- immuunivälitteiset syyt
- Epilepsia johtuu suoraan tunnetusta tai oletetusta immunologisesta sairaudesta ja epilepsiakohtaukset ovat häiriön ydinoire.
- tuntemattomat syyt.
- Epilepsian taustalla voi olla toistaiseksi tuntematon syy. Etiologialtaan tuntemattoman vaikean epilepsian syytä tulee arvioida säännöllisesti uudelleen.
- Epilepsian syy voi myös kuulua yhtä aikaa useampaan kategoriaan (esim. aivojen infektion, immunovälitteisen syyn tai geneettisen syyn aiheuttama rakenteellinen poikkeavuus).
- Aiemmin käytettiin jakoa idiopaattisiin (itsestään syntyviin), symptomaattisiin (aivojen rakenteen tai aineenvaihdunnan muutoksiin liittyviin) ja kryptogeenisiin (tuntemattomista syistä johtuviin) epilepsioihin.
- Epilepsiaoireyhtymällä tarkoitetaan oirekokonaisuutta, jossa tietyt kohtaustyypit, EEG-löydökset ja kuvantamislöydökset esiintyvät yhdessä. Sillä on usein myös tyypillinen epilepsian alkamisikä ja ennuste, tyypilliset kohtauksia laukaisevat tekijät ja tyypillinen vuorokausivaihtelu. Epilepsiaoireyhtymään liittyy usein tyypillisiä lisäsairauksia ja oireita, kuten oppimisvaikeuksia ja psyykkisiä oireita. Epilepsiaoireyhtymän tunnistaminen vaikuttaa etiologisiin tutkimuksiin, hoidon valintaan ja ennusteen arviointiin «Scheffer IE, Berkovic S, Capovilla G ym. ILAE clas...»7.
- Oireyhtymätasoinen diagnoosi ei ole aina mahdollinen.
- Väestöpohjaisissa tutkimuksissa vain noin kolmasosa kaikista lapsuusiällä tehdyistä epilepsiadiagnooseista oli oireyhtymätasoisia «Aaberg KM, Surén P, Søraas CL ym. Seizures, syndro...»10, «Sokka A, Olsen P, Kirjavainen J ym. Etiology, synd...»11. Imeväisillä epilepsiaoireyhtymät ovat yleisempiä «Gaily E, Lommi M, Lapatto R ym. Incidence and outc...»12.
- Epilepsiatyypin määrittäminen on hoidon suunnittelun kannalta tärkeää niilläkin potilailla, joilla ei päästä oireyhtymädiagnoosiin.
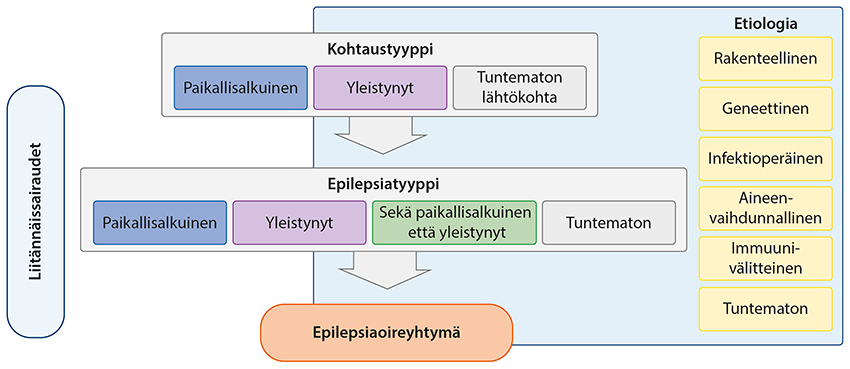
Epilepsioiden luokittelu ILAE:n mukaan. Mukaeltu lähteestä: Scheffer IE, Berkovic S, Capovilla G, ym. ILAE classification of the epilepsies: Position paper of the ILAE Commission for Classification and Terminology. Epilepsia 2017;58:512-21
Epidemiologia
Epilepsia
- Kansainvälisissä tutkimuksissa on todettu, että epilepsian ilmaantuvuus lapsilla on 0,41–1,87/1000 ja suurin ilmaantuvuus on alle 1-vuotiaiden ikäryhmässä «Camfield P, Camfield C. Incidence, prevalence and ...»13.
- Suomalaisessa tutkimuksessa epilepsian ilmaantuvuudeksi alle 16-vuotiailla on todettu 0,63/1000/v «Saarinen MM, Sillanpää M, Schmidt D ym. Long-term ...»14.
- Ensimmäisen ikävuoden aikana ilmaantuvuudeksi Suomessa on todettu 1,24/1000 «Gaily E, Lommi M, Lapatto R ym. Incidence and outc...»12.
- Epilepsian esiintyvyys alle 16-vuotiailla on kehittyneissä maissa 0,32–0,55 % «Camfield P, Camfield C. Incidence, prevalence and ...»13.
- Aktiivisen epilepsian (ainakin yksi epileptinen kohtaus viimeisten 5 vuoden aikana) esiintyvyydeksi alle 16-vuotiailla on kahdessa suomalaisessa tutkimuksessa todettu 2,3 ja 3,9/1000 «Eriksson KJ, Koivikko MJ. Prevalence, classificati...»15, «Sillanpää M, Jalava M, Kaleva O ym. Long-term prog...»16.
- Pitkäaikaisseurannassa (40 vuotta) lapsena idiopaattiseen epilepsiaan sairastuneista 92 % on tullut kohtauksettomiksi ja 86 % on voinut lopettaa lääkityksen. Kryptogeenisen epilepsian ryhmässä vastaavat luvut ovat olleet 68 % ja 57 % ja symptomaattisessa 45 % ja 19 % «Sillanpää M, Jalava M, Kaleva O ym. Long-term prog...»16.
- Lapsena epilepsiaan sairastuneiden kuolleisuus on suurempi kuin muun lapsiväestön,
paitsi lapsuusiän itsestään rajoittuvissa epilepsioissa «Callenbach PM, Westendorp RG, Geerts AT ym. Mortal...»17, «Camfield CS, Camfield PR, Veugelers PJ. Death in c...»18, «Berg AT, Shinnar S, Testa FM ym. Mortality in chil...»19.
- Epilepsiaa sairastavien lapsipotilaiden odottamattoman äkkikuoleman (SUDEP, Sudden Unexpected Death in Epilepsy) vuotuiseksi ilmaantuvuudeksi on arvioitu 1/4 500 epilepsiaa sairastavaa lasta, joka on pienempi kuin epilepsiaa sairastavassa aikuisväestössä «Harden C, Tomson T, Gloss D ym. Practice guideline...»20. Hoitoresistenttien toonis-kloonisten kohtausten esiintyminen ja lääkityksen käyttämättä jättäminen suurentavat riskiä «Saxena A, Jones L, Shankar R ym. Sudden unexpected...»21, «Verducci C, Hussain F, Donner E ym. SUDEP in the N...»22.
- Itsestään rajoittuvissa lapsuusiän epilepsioissa suurentunutta SUDEP-riskiä ei kuitenkaan ole todettu suomalaisessa väestössä «Sillanpää M, Shinnar S. SUDEP and other causes of ...»23.
Hoidon porrastus
- Lapsi, jolla epäillään epilepsiaa (ks. kohta Määritelmät ja kliiniset oireet «A1»2), tulee lähettää erikoissairaanhoitoon tilanteen mukaan päivystys- tai kiireellisenä potilaana, tai harkinnan mukaan tulee muutoin konsultoida erikoissairaanhoitoa.
- Epilepsiadiagnoosin tekee ja hoidosta vastaa lastenneurologi tai riittävän asiantunteva
lastenlääkäri tai kehitysvammalääkäri.
- Osa seurantakäynneistä voidaan toteuttaa perusterveydenhuollossa tai kehitysvammahuollossa yhteistyössä hoidosta vastaavan erikoislääkärin kanssa.
- Kun potilaan todetaan sairastuneen vaikeaan epilepsiaan, diagnoosin tarkistamiseksi ja hoidon mahdollisuuksien arvioimiseksi on ilman tarpeetonta viivettä konsultoitava vaikeaan epilepsiaan perehtynyttä lastenneurologia ja harkittava potilaan lähettämistä erikoissairaanhoidon yksikköön, jossa on vaikeaan epilepsiaan perehtynyt lastenneurologi, mahdollisuus tasokkaaseen kuvantamiseen, video-EEG-rekisteröintiin ja geenidiagnostiikkaan sekä moniammatillinen työryhmä.
- Epilepsian invasiivinen diagnostiikka (kallonsisäiset video-EEG-rekisteröinnit), päätökset epilepsialeikkauksista ja epilepsiakirurgia on Suomessa keskitetty kahteen keskukseen (HUS ja KYS).
- Haasteellisissa harvinaisissa ja vaikeissa epilepsioissa järjestetään kansallisen moniammatillisen työryhmän kokouksia. Jos näissä ei löydetä ratkaisua, on mahdollista konsultoida Euroopan harvinaisten ja vaikeiden epilepsioiden osaamisverkostoa (European Reference Network EpiCARE) sen jäsenkeskusten kautta.
- Hoitovastuu siirretään aikuisneurologille paikallisen työnjaon mukaisesti, yleensä
noin 16 vuoden iässä.
- Siirtymistä edeltää lastenneurologian yksikössä siirtymävaihe, joka alkaa jo useita vuosia ennen varsinaista siirtymistä, ja jonka aikana valmistellaan pääasiallisen omahoitovastuun siirtymistä mahdollisuuksien mukaan huoltajilta nuorelle itselleen.
- Aikuisneurologin tulisi aloittaa 16 vuotta täyttäneiden vastadiagnosoitujen potilaiden hoito, jotta jatkuvuus varmistuisi.
Epilepsioiden diagnostiikka
- Tarkka diagnoosi eli kohtaustyyppien, etiologian ja mahdollisen epilepsiaoireyhtymän tunnistaminen on hyvän hoidon perusta.
- Diagnoosi perustuu anamneesiin ja lääkärin tutkimukseen, jota täydennetään EEG-rekisteröinnillä
ja tarvittaessa video-EEG- «Eriksson K, Peltola J, Kälviäinen R. Kohtausten ho...»24, kuvantamis- ja laboratoriotutkimuksilla.
- Anamneesissa on tärkeää selvittää tarkasti kohtausoireiden tyyppi ja kohtauksen kulku.
- EEG:n tulee sisältää valvetta, unta ja heräämisvaihe sekä tilanteen mukaan vilkkuvalo-
ja hyperventilaatioprovokaatiot.
- Normaali EEG ei sulje pois epilepsiaa, eikä poikkeava EEG-löydös yleensä yksin todista, että lapsella olisi epilepsia. Poikkeuksena ovat hypsarytmia tai multifokaaliset piikit yhdistyneenä sarjana tulevaan paroksysmaaliseen nopeaan toimintaan imeväisikäisellä «Eeg-Olofsson O, Petersén I, Selldén U. The develop...»25 tai tilanne, jossa EEG:n aikana esiintyy epileptinen kohtaus.
- Alle vuoden ikäisillä uni-EEG-rekisteröinnin tulisi sisältää vähintään 15 minuuttia valveillaoloa heräämisen jälkeen.
- Video-EEG-tutkimus on tarpeen epäselvissä tilanteissa erotusdiagnostiikan ja epilepsialuokituksen
varmistamiseksi.
- Diagnostisia ongelmia aiheuttavat useimmiten imeväisten ja kehitys- ja liikuntavammaisten ei-epileptiset kohtausoireet sekä toiminnalliset kohtaukset.
- Vaikeassa epilepsiassa video-EEG:tä tarvitaan epilepsiadiagnoosin tarkentamiseksi, kohtaustyypin ja oireyhtymän määrittämiseksi ja leikkaushoidon mahdollisuuksien arvioimiseksi.
- Aivojen rakenteellisten muutosten tunnistamiseksi pään kuvantaminen on tarpeen.
- Pään kuvantamisessa käytetään aivojen magneettikuvausta «Berg AT, Testa FM, Levy SR ym. Neuroimaging in chi...»26, «Shevell MI, Rosenblatt B, Watters GV ym. "Pseudo-B...»27, «Gelisse P, Corda D, Raybaud C ym. Abnormal neuroim...»28, «Gaillard WD, Chiron C, Cross JH ym. Guidelines for...»29.
- Uusintakuvausta harkitaan, jos epilepsia osoittautuu vaikeaksi tai ensimmäinen kuvaus on tehty alle 2-vuotiaana, jos lapsen kehitys taantuu tai hänelle ilmaantuu uusia oireita. Vaikeaa epilepsiaa sairastavalle lapselle uusi kuvaus kannattaa tehdä 3T-MRI-laitteella ja protokollalla, joka on erityisesti suunniteltu epilepsiaan liittyvien poikkeavuuksien toteamiseen «Ladino LD, Balaguera P, Rascovsky S ym. Clinical B...»30.
- Aivojen kuvantamista ei tarvita tyypillisissä geneettisissä epilepsioissa, esimerkiksi
lapsuusiän poissaoloepilepsiassa «Gaillard WD, Chiron C, Cross JH ym. Guidelines for...»29.
- Diagnoosin on tällöin oltava varma, koska osalla potilaista, joilla on geneettiseksi tulkittu epilepsia, on todettu rakenteellisia aivomuutoksia «Shevell MI, Rosenblatt B, Watters GV ym. "Pseudo-B...»27, «Gelisse P, Corda D, Raybaud C ym. Abnormal neuroim...»28.
- Tunnettujen epilepsiaa aiheuttavien tai sitä modifioivien geenien määrä lisääntyy,
ja geneettisten tutkimusten kliiniset käyttömahdollisuudet tarkentuvat nopeasti.
- Joidenkin epilepsian taustalla olevien geenimutaatioiden tunnistaminen voi vaikuttaa potilaan lääkehoitoon, muuhun hoitoon (esim. ruokavaliohoito), seurantaan ja perinnöllisyysneuvontaan.
- Nykyisin tarjolla olevia geneettisiä tutkimuksia ovat kromosomitutkimus, molekyylikaryotyypitys, yksittäisten geenien tutkiminen, geenipaneelitutkimus ja eksomisekvensointi. Tulevaisuudessa koko genomin sekvensointi korvannee edellä mainittuja tutkimuksia myös kliinisessä työssä.
- Tutkimusstrategia valitaan potilaskohtaisesti, tarvittaessa epilepsiaan perehtyneen
kliinikon ja geneetikon yhteistyönä.
- Molekyylikaryotyypitys on ensisijainen tutkimus potilailta, joilla on epilepsian lisäksi kehityshäiriöitä, älyllinen kehitysvamma tai dysmorfioita.
- Rengaskromosomi ei välttämättä tule esiin molekyylikaryotyypityksessä.
- Laaja epilepsioiden geenipaneelitutkimus tai eksomisekvenointi kannattaa ottaa kaikilta
etiologialtaan tuntemattomilta enkefalopatiaa tai vaikeaa epilepsiaa sairastavilta
lapsilta.
- Geneettinen tutkimus osoittaa mahdollisen taustatekijän noin neljänneksellä niistä lapsista, joilla taustatekijältään tuntematon epilepsia on alkanut alle 3 vuoden iässä «Berg AT, Coryell J, Saneto RP ym. Early-Life Epile...»31.
- Toistojaksomuutokset eivät välttämättä tule näkyviin geenipaneeleissa tai eksomeissa.
- Yksittäisten geenien tutkiminen tulee kyseeseen potilailla, joilla kliinisten syiden
pohjalta epäillään tai löydösten perusteella tiedetään olevan spesifinen sairaus:
- EPM1-geeni Unverricht–Lundborgin taudissa
- muut suomalaisen tautiperimän sairaudet.
- Yksittäisten geenien tarkempi analysointi voi tulla kyseeseen myös potilailla, joilla
kliinisten syiden pohjalta epäillään tai löydösten perusteella tiedetään olevan spesifinen
sairaus, mutta paneelitutkimuksessa tai eksomisekvenoinnissa ei ole löytynyt mutaatiota:
- TSC1- ja TSC2-geenit tuberoosiskleroosipotilaalla
- glukoosin kuljettajaproteiini tyyppi 1:n häiriö (SLC2A1-geeni, sisältää geenin sekvensoinnin ja deleetio- tai duplikaatioanalyysin)
Hoidon tavoitteet, toteutus ja seuranta
- Hoidon tavoitteet ovat kohtauksettomuus, epilepsian aiheuttamien kognitiivisten ongelmien estäminen ilman merkittäviä haittavaikutuksia ja mahdollisimman hyvä elämänlaatu.
- Ensimmäisen paikallisalkuisen tai yleistyneen toonis-kloonisen kohtauksen uusiutumisriski lapsilla riippuu etiologiasta ja on ensimmäisen puolen vuoden seuranta-aikana 22–55 % ja kahteen vuoteen mennessä 37–69 % «Shinnar S, Berg AT, Moshe SL ym. The risk of seizu...»32, «Arthur TM, deGrauw TJ, Johnson CS ym. Seizure recu...»33.
- Epilepsian lääkehoito aloitetaan useimmiten toisen kohtauksen jälkeen.
- Ensimmäisen kohtauksen pitkittyminen tai status epilepticus ensimmäisenä kohtauksena eivät yksinään riitä epilepsiadiagnoosiin eivätkä välttämättä edellytä epilepsialääkityksen aloittamista «Fisher RS, Acevedo C, Arzimanoglou A ym. ILAE offi...»9, «Hirtz D, Berg A, Bettis D ym. Practice parameter: ...»34.
- Ensimmäisen kohtauksen jälkeen säännöllistä lääkitystä voidaan kohtauksen kestosta riippumatta harkita, jos uusiutumisriskin arvioidaan olevan yli 60 %. Tällaisia suuren uusiutumisriskin tilanteita ovat esimerkiksi kliinisten oireiden ja EEG-löydöksen perusteella todettu epilepsiaoireyhtymä, jossa kohtaustaipumuksen arvioidaan olevan pitkäaikainen, tai lapsella todettu rakenteellinen aivojen poikkeavuus ja siihen sopiva epileptiforminen EEG-muutos «Fisher RS, Acevedo C, Arzimanoglou A ym. ILAE offi...»9, «Arthur TM, deGrauw TJ, Johnson CS ym. Seizure recu...»33, «Sansevere AJ, Avalone J, Strauss LD ym. Diagnostic...»35.
- Lääkityksen aloittaminen heti ensimmäisen tai vasta toisen kohtauksen jälkeen ei näytä vaikuttavan todennäköisyyteen saavuttaa 2 vuoden kohtauksettomuus «Lääkityksen aloittaminen lapsen 1. tai 2.»B.
- Lääkkeen valinta riippuu epilepsiatyypistä ja lääkkeen haittavaikutusprofiilista. Annos lasketaan potilaan painon mukaan, mutta aikuisille suositeltua aloitusannosta ei tule ylittää.
- Lääkehoidon aloittamisen perusteista on tärkeää keskustella aina potilaan ja hänen
huoltajansa kanssa.
- Epilepsiadiagnoosin jälkeen perheelle järjestetään hoidonohjaus, jossa käydään läpi
lääkehoidon toteuttaminen, hoidon mahdolliset haittavaikutukset, hoitovasteen seuranta,
epilepsian vaikutukset jokapäiväiseen elämään ja koulunkäyntiin sekä mahdolliset rajoitukset
ammatinvalintaan ja ajokykyyn. Lisäksi tarkistetaan sosiaaliturva.
- Nuoren (yli 12-vuotiaan) kanssa tulee keskustella myös kahden kesken, koska se tukee hänen vastuullisuutensa ja itsenäistymisensä kehitystä ja mahdollistaa luottamuksellisen keskustelun.
- Jo yksittäinen epileptinen kohtaus johtaa EU-direktiivin 2009/113/ETY mukaan moottoriajoneuvon kuljettamista koskeviin rajoituksiin «Ajoterveyden arviointiohjeet lääkäreille. Liikente...»36, «Epilepsiat (aikuiset). Käypä hoito -suositus. Suom...»37. Ks. lisätietoja Käypä hoito -suosituksesta Epilepsiat (aikuiset) «Ajoterveyden arviointiohjeet lääkäreille. Liikente...»36, «Epilepsiat (aikuiset). Käypä hoito -suositus. Suom...»37.
- Ennen lääkehoidon aloittamista määritetään kaikilta perusverenkuva ja ALAT. Potilailta, joille aloitetaan okskarbatsepiini, määritetään lisäksi seerumin natriumpitoisuus. EKG tutkitaan harkinnan mukaan.
- Seurantaverinäytteet on suositeltavaa ottaa noin 4–6 viikkoa hoidon aloituksen jälkeen ja sen jälkeen tarvittaessa haittavaikutuksia epäiltäessä, lääkemuutosten yhteydessä ja monilääkehoidossa.
- Lääkepitoisuuksien määrittäminen saattaa olla tarpeen, jos
- lääkitys ei tehoa
- epäillään lääkeaineiden yhteisvaikutuksia tai potilaan hoitomyöntyvyyttä
- käytetään fenytoiinia (nonlineaarinen kinetiikka)
- käytetään valproaattia, jolloin tavoitteena on toteuttaa hoito mahdollisimman pienellä valproaattiannoksella ja -tasolla (yksilöllinen metabolia).
- Epilepsiadiagnoosin jälkeen perheelle järjestetään hoidonohjaus, jossa käydään läpi
lääkehoidon toteuttaminen, hoidon mahdolliset haittavaikutukset, hoitovasteen seuranta,
epilepsian vaikutukset jokapäiväiseen elämään ja koulunkäyntiin sekä mahdolliset rajoitukset
ammatinvalintaan ja ajokykyyn. Lisäksi tarkistetaan sosiaaliturva.
- Laboratoriotutkimusten rutiininomainen seuranta ei ole tarpeen «Verenkuvaa sekä maksa- ja munuaisfunktioita ei tarvinne seurata lapsilla, jotka ovat kohtauksettomia eikä kliinisiä haittavaikutusoireita esiinny.»C.
- Laboratoriotutkimuksia tärkeämpää on havaita seurannassa kliiniset oireet ja arvioida lapsen kehitystä ja kasvua. Tavanomaiset neuvola- ja kouluterveydenhuollon palvelut, rokotukset mukaan luettuina, on syytä toteuttaa.
- Lääkehoitoa on yleensä syytä jatkaa vähintään niin kauan, että potilas on ollut 2
vuotta kohtaukseton «Vähintään 2 vuoden kohtauksettomuus lääkehoidon aikana lisää lapsilla kohtauksettomuuden todennäköisyyttä lääkehoidon lopettamisen jälkeen.»B.
- Tietyissä epilepsioissa, kuten nuoruusiän myoklonusepilepsiassa, kohtaukset kuitenkin uusiutuvat valtaosalla potilaista, jos lääkitys lopetetaan. Hoitoa on siten syytä jatkaa pitkäaikaisesti «Healy L, Moran M, Singhal S ym. Relapse after trea...»38, «Höfler J, Unterberger I, Dobesberger J ym. Seizure...»39.
- Lapsuusiän itsestään rajoittuvissa epilepsioissa hoidon kestoksi saattaa riittää yksi kohtaukseton vuosi «Braathen G, Andersson T, Gylje H ym. Comparison be...»40.
- Epilepsiakohtausten uusiutumisriski lääkehoidon lopetuksen jälkeen lapsilla vaihtelee
useiden eri tekijöiden mukaan. Uusiutumisriskin suuruuteen vaikuttavat epilepsian
etiologia (esim. epilepsiaoireyhtymä, geneettinen etiologia tai aivojen rakenteellinen
poikkeavuus), EEG-poikkeavuus, epilepsian alkamisikä, lapsen kehitystaso, kohtausten
määrä ennen lääkitystä ja kohtauksettomuuden saavuttamiseen kulunut aika «Lamberink HJ, Otte WM, Geerts AT ym. Individualise...»41, «Berg AT, Rychlik K, Levy SR ym. Complete remission...»42, «Sillanpää M, Saarinen M, Schmidt D. Clinical condi...»43.
- 5 vuoden kohtauksettomuus saavutetaan noin kahdessa kolmasosassa lapsuusiässä alkaneista epilepsioista «Sillanpää M, Schmidt D. Long-term outcome of medic...»44.
- 5 vuoden kohtauksettomuuden jälkeen epilepsia uusiutuu noin 10 %:lla lapsena sairastuneista potilaista, ja heistä noin viidesosalla osoittautuu vaikeahoitoiseksi «Camfield PR, Camfield CS. Intractable seizures aft...»45.
- Epilepsialääkitys lopetetaan asteittain.
- Epilepsian uusiutumisriski ei lapsilla riippune lääkityksen lopettamisvaiheen kestosta, jos se on vähintään 6 viikkoa «Epilepsian uusiutumisriskiin lapsilla ei liene vaikutusta sillä, puretaanko lääkitys 6 viikon vai 9 kuukauden aikana.»C.
- Epilepsia on pitkäaikaissairaus, jossa potilaan ja hänen perheensä hoitoon sitoutuminen vaatii diagnoosin teon ja seurantakäyntien yhteydessä potilaan ja hänen huoltajiensa hoidon tarkoituksen ja tavoitteiden kertausta ja syventämistä. Se toteutetaan sairaanhoitajien (epilepsiahoitajat) sekä tarvittavien erityistyöntekijöiden ja hoidosta vastaavan lääkärin moniammatillisena yhteistyönä. Onnistunut hoito voi potilaan sairauden mukaan vaatia tiivistä yhteistyötä myös potilaan muiden lähiomaisten sekä päivähoidon tai koulun kanssa. Perhe ja potilas saattavat tarvita myös psykologista tukea.
Siirtymävaihe
- Siirtymävaihe on pitkäkestoinen vaihe, joka alkaa jo useita vuosia ennen varsinaista siirtymistä lastenneurologin hoidosta aikuisneurologin hoitoon ja jonka aikana valmistellaan pääasiallisen omahoitovastuun siirtymistä mahdollisuuksien mukaan huoltajilta nuorelle itselleen. Osa siirtymävaihetta on, että nuori alkaa tavata lääkäriä ilman huoltajiaan.
- Nuori siirtyy lastenneurologin hoidosta neurologin hoitoon yleensä noin 16 vuoden iässä. Tarkkaan siirtymisajankohtaan vaikuttavat nuoren elämäntilanne ja epilepsian hoitovaihe.
- Kaikki hoitoa tarvitsevat lapsuusiässä epilepsiaan sairastuneet potilaat siirtyvät neurologin tai kehitysvammalääkärin hoitoon.
- Viimeisen lastenneurologin käynnin yhteydessä varmistetaan riittävän tiedon välittyminen jatkohoidosta vastaavalle hoitoyhteenvedolla, jossa käydään läpi ainakin potilaan kohtaustyypit, epilepsiatyyppi ja -oireyhtymä, etiologia ja liitännäissairaudet. Myös potilaalla tehokkaiksi todetut lääke- ja muut hoidot (esim. ketogeeninen ruokavalio ja vagusstimulaattorihoito) ja merkittävät hoitojen haittavaikutukset on syytä kirjata. Epilepsiarekisterin käyttö helpottaa tiedonsiirtoa.
- Fimean ohje on, että teratogeenisten riskien vuoksi valproaattihoidon saa aloittaa tytöille vain, jos muut hoidot ovat tehottomia tai potilas ei siedä niitä.
- Valproaattia käyttävien tyttöjen osalta tulee ennen puberteettia arvioida, onko valproaattilääkitys välttämätön tai voiko annosta pienentää «Tomson T, Marson A, Boon P ym. Valproate in the tr...»46 (ks. tarkemmin Käypä hoito -suositus Epilepsia (aikuiset) «Epilepsiat (aikuiset)»5, «Epilepsiat (aikuiset). Käypä hoito -suositus. Suom...»37, Valproaatin käyttöä epilepsian hoidossa hedelmällisessä iässä olevilla naispuolisilla potilailla koskevat ohjeet).
- Raskaus on suljettava pois ennen valproaattihoidon aloittamista. Naisille, jotka voivat tulla raskaaksi, ei saa aloittaa valproaattihoitoa ilman terveyspalvelujen tuottajan vahvistamaa negatiivista raskaustestitulosta (raskaustesti plasmasta), jotta suljetaan pois tahaton käyttö raskauden aikana. Jos valproaattia määrätään tytölle tai naiselle, joka voi tulla raskaaksi, hoito on arvioitava säännöllisesti vähintään kerran vuodessa. Samalla varmistetaan, että potilas ja hänen perheensä ovat ymmärtäneet sekä perussairauteen että valproaatin käyttöön liittyvät riskit mahdollisen raskauden kannalta.
- Potilaalle annetaan potilasopas ja sairauskertomukseen kirjataan tieto neuvonnan ja oppaan antamisesta. Lisäksi varmistetaan, että potilas noudattaa Fimean ohjeistamaa raskaudenehkäisyohjelmaa «https://www.fimea.fi/-/uusia-ohjeita-valproaatin-kayttoon-raskaudenaikaisen-altistuksen-valttamiseksi»1.
- Ensiapulääkityksen tarve harkitaan tarkasti. Ainoastaan jos potilaalla on epilepsiaoireyhtymän, etiologian tai anamneesin perusteella taipumus uhkaaviin status epilepticus -kohtauksiin, hän voi edelleen aikuisena hyötyä posken limakalvolle tai peräsuoleen annostellusta ensiapulääkkeestä. Lääkkeen antaa aina siihen opastuksen saanut henkilö, eikä potilas itse kuljeta lääkettä mukanaan, ellei opastuksen saanutta henkilöä ei ole paikalla «Gaily E, Lommi M, Lapatto R ym. Incidence and outc...»12.
- Ennen siirtymistä neurologin hoitoon tulee varmistaa, että nuorella on riittävästi tietoa omasta epilepsiastaan ja lääkityksestään, epilepsian mahdollisista vaikutuksista hänen elämäänsä (elämäntavat, ajokyky, ammatinvalinta, varusmiespalvelus) ja siitä, minkälaisissa tilanteissa epilepsia tulee erityisesti huomioida (esim. raskauden ehkäisy, suunnittelu ja epilepsialääkkeiden vaikutus näihin).
Imeväis- ja leikki-iässä alkavat epilepsiat
Infantiilispasmioireyhtymä (Westin oireyhtymä)
- Tyypillinen kohtaus on infantiilispasmisarja, jonka aikana lapsi jäykistyy toistuvasti
0,5–1 sekunnin ajaksi koukistus- tai ojennusasentoon.
- Spasmit voivat tunnistetun etiologian ryhmässä olla vähäoireisia tai epäsymmetrisiä «Gaily E, Liukkonen E, Paetau R ym. Infantile spasm...»47.
- Lisäoireena on usein kehityksen pysähtyminen tai taantuminen, joka voidaan huomata jo ennen kohtausoireita.
- Tyypillinen alkamisikä on 6 kuukautta (vaihteluväli 2–12 kuukautta).
- EEG-löydöksiä ovat hypsarytmia, modifioitu hypsarytmia tai multifokaaliset piikit «Gaily E, Liukkonen E, Paetau R ym. Infantile spasm...»47.
- Etiologia on tunnistettu (aiemmin: symptomaattinen) noin kahdella kolmasosalla ja tuntematon (aiemmin: idiopaattinen tai kryptogeeninen) noin yhdellä kolmasosalla «Gaily E, Lommi M, Lapatto R ym. Incidence and outc...»12.
- Suomalaisessa väestöpohjaisessa tutkimuksessa infantiilispasmien syynä oli hankinnainen aivovaurio 26 %:lla (näistä yleisimmät perinataalinen aivoinfarkti, hypoksisiskeeminen aivovaurio ja keskushermostoinfektio), aivojen kehityshäiriö 15 %:lla, tuberoosiskleroosi 9 %:lla, geneettinen 6 %:lla ja muu syy (esim. neurodegeneratiivinen sairaus) 8 %:lla potilaista. Syy jäi tuntemattomaksi 36 %:lla potilaista «Gaily E, Lommi M, Lapatto R ym. Incidence and outc...»12.
- Nykyhoidolla spasmit loppuvat lähes kaikilta tuntemattoman etiologian ryhmässä ja noin puolelta tunnistetun etiologian ryhmässä «Gaily E, Lommi M, Lapatto R ym. Incidence and outc...»12.
- Normaali tai lähes normaali kehitys jatkuu niillä tuntemattoman etiologian ryhmän lapsilla, joilla spasmit saadaan loppumaan kokonaan, ja myös osalla hoitoon hyvin reagoineista tunnistetun etiologian ryhmän lapsista «Gaily E, Lommi M, Lapatto R ym. Incidence and outc...»12, «Gaily E, Liukkonen E, Paetau R ym. Infantile spasm...»47, «Granström ML, Gaily E, Liukkonen E. Treatment of i...»48.
- Lapset, joiden spasmit jatkuvat vielä yhden vuoden iässä, osoittautuvat yleensä seurannassa kehitysvammaisiksi «Gaily E, Liukkonen E, Paetau R ym. Infantile spasm...»47, «Granström ML, Gaily E, Liukkonen E. Treatment of i...»48.
- Lyhyt hoitoviive saattaa parantaa kehitysennustetta «O'Callaghan FJ, Lux AL, Darke K ym. The effect of ...»49.
Hoito
- Hoito aloitetaan joko ACTH:lla (synteettinen pitkävaikutteinen tetrakosaktidi) tai
vigabatriinilla «ACTH/steroidi ja vigabatriini ilmeisesti ovat tehokkaita ensihoitoja infantiilispasmioireyhtymässä.»B.
- Vigabatriinia suositellaan ensisijaiseksi, jos etiologia on tuberoosiskleroosi «Vigabatriini saattaa olla tehokkaampi kuin hydrokortisoni lopettamaan tuberoosiskleroosista johtuvat spasmit kuukauden kuluessa hoidon alusta.»C.
- ACTH saattaa olla vigabatriinia tehokkaampi muusta syystä kuin tuberoosiskleroosista johtuvissa infantiilispasmeissa «Hormonaalinen hoito (ACTH ja prednisoloni) saattaa olla vigabatriinia tehokkaampi lopettamaan muusta syystä kuin tuberoosiskleroosista johtuvat infantiilispasmit 14 vuorokauden kuluessa hoidon alusta.»C.
- Hoidon aloitukseen ACTH:lla saattaa liittyä parempi kehitysennuste 14 kuukauden ja 4 vuoden iässä kuin hoidon aloitukseen vigabatriinilla niillä lapsilla, joilla infantiilispasmien etiologia on tuntematon «Infantiilispasmien hormonaaliseen ensihoitoon (ACTH ja prednisoloni) saattaa liittyä parempi kehitysennuste, mutta ei kohtausennuste, 14 kuukauden ja 4 vuoden iässä kuin vigabatriinilla aloitettuun hoitoon niillä lapsilla, joilla infantiilispasmien etiologia on tuntematon.»C.
- Hoidon aloitukseen yhtä aikaa sekä ACTH:lla että vigabatriinilla saattaa liittyä nopeampi spasmien loppuminen kuin vain yhdellä lääkkeellä aloitettuun hoitoon «Hoidon aloitukseen yhtä aikaa sekä ACTH:lla ja vigabatriinilla saattaa liittyä nopeampi spasmien loppuminen kuin vain yhdellä lääkkeellä aloitettuun hoitoon, mutta näyttöä pitkäaikaishyödystä ei ole.»C, «O'Callaghan FJ, Edwards SW, Alber FD ym. Safety an...»50.
- Näyttöä siitä, että ACTH:n ja vigabatriinin yhdistelmä ensimmäisenä hoitona parantaisi kehitysennustetta, ei ole «O'Callaghan FJK, Edwards SW, Alber FD ym. Vigabatr...»51.
- Prednisolonihoitoa voidaan käyttää, jos ACTH:ta ei ole käytettävissä «Lux AL, Edwards SW, Hancock E ym. The United Kingd...»52. Prednisoloni 4 mg/kg/vrk:n annoksena voi olla tehokkaampi kuin 2 mg/kg/vrk:n annoksena, kun hoitotulos arvioidaan kliinisesti 14 vuorokauden jälkeen hoidon aloittamisesta «Chellamuthu P, Sharma S, Jain P ym. High dose (4 m...»53.
- Sekä ACTH että vigabatriini soveltuvat toissijaiseksi lääkkeeksi niille lapsille, joiden kohtausoireet eivät lopu ensin aloitetulla hoidolla 2–3 viikossa.
- Hoitovaste tulee varmistaa EEG tai video-EEG-tutkimuksella, koska lääkehoito voi lieventää spasmit vaikeasti havaittaviksi «Granström ML, Gaily E, Liukkonen E. Treatment of i...»48.
- ACTH-hoitoon «Infantiilispasmien ACTH-hoitoon näyttäisi liittyvän lisääntynyt kuolemanvaara ja muita vakavia haittavaikutuksia kuten verenpaineen nousu, vaikea infektio, elektrolyyttihäiriö sekä lisämunuaisakselin toimintahäiriö.»C ja vigabatriinihoitoon «Vigabatriinihoitoon ilmeisesti liittyy konsentrisen näkökenttäpuutoksen lähes puolella aikuispotilaista ja myös osalla lapsipotilaista.»B, «Vanhatalo S, Nousiainen I, Eriksson K ym. Visual f...»54 liittyvien vakavien haittavaikutusten vaaran vuoksi on pyrittävä käyttämään pienintä tehokasta annosta ja mahdollisimman lyhyttä hoitoaikaa.
- Työryhmä suosittelee pitkävaikutteisen ACTH:n aloitusannokseksi 0,5 mg lihakseen joka toinen päivä ja hoidon kestoksi 2 viikkoa, jonka jälkeen hoito muutetaan predniso(lo)niksi ja lopetetaan asteittain 2 viikon aikana «Lux AL, Edwards SW, Hancock E ym. The United Kingd...»52, «Leivonen, Peltola, Gaily. Tunnistatko infantiilisp...»55.
- Jos ACTH:ta ei ole saatavilla, työryhmä suosittelee vaihtoehdoksi prednisolonia 10 mg x 4/vrk 2 viikon ajan ja asteittaista lopetusta kuten ACTH-hoidon jälkeen «Lux AL, Edwards SW, Hancock E ym. The United Kingd...»52, «Chellamuthu P, Sharma S, Jain P ym. High dose (4 m...»53, «Wanigasinghe J, Arambepola C, Sri Ranganathan S ym...»56.
- Jos spasmit jatkuvat ensimmäisen hoitoviikon jälkeen, työryhmä suosittelee aloitetun hoidon mukaan joko ACTH-annoksen suurentamista 0,75 mg:aan tai prednisoloniannoksen suurentamista 20 mg:aan x 3/vrk toisen hoitoviikon ajaksi «Leivonen, Peltola, Gaily. Tunnistatko infantiilisp...»55.
- Työryhmä suosittelee vigabatriinin aloitusannokseksi 50 mg/kg/vrk. Ylläpitoannokseksi titrataan 3 vuorokauden kuluessa hoidon aloituksesta 100 mg/kg/vrk, joka tarvittaessa suurennetaan annokseen 150 mg/kg/vrk. Vigabatriinin teho on tutkimuksissa osoitettu annoksella 100–150 mg/kg/vrk «Vigabatriini annoksella 100–150 mg/kg/vrk saattaa olla pientä (alle 40 mg/kg/vrk) vigabatriiniannosta tehokkaampi lopettamaan infantiilispasmit 2 viikon kuluessa hoidon alusta.»C. Hoidon kestoksi suosittelemme 3–6 kuukautta, mutta optimaalisesta hoidon kestosta ei ole tutkimusnäyttöä.
- Vigabatriinihoidon kesto on raportoitu vain yhdessä kontrolloidussa tutkimuksessa «Lux AL, Edwards SW, Hancock E ym. The United Kingd...»57, jossa sitä jatkettiin hoitoon reagoineilla lapsilla 14 kuukauden ikään asti.
- Hoitoon reagoineille tunnistetun etiologian (rakenteellis-aineenvaihdunnallisen) ryhmän lapsille voidaan harkita epilepsialääkityksen jatkamista esimerkiksi valproaatilla «Valproaatti saattaa lopettaa spasmit tai vähentää niitä ACTH:lle resistenteillä infantiilispasmioireyhtymää sairastavilla lapsilla, mutta luotettava näyttö puuttuu.»D ACTH:n ja vigabatriinin käytön lopettamisen jälkeen, ellei valproaatille ole vasta-aihetta.
- Jos ensisijaiset hoidot (ACTH ja vigabatriini) eivät lopeta spasmeja, toissijaisia hoitomahdollisuuksia ovat valproaatti «Valproaatti saattaa lopettaa spasmit tai vähentää niitä ACTH:lle resistenteillä infantiilispasmioireyhtymää sairastavilla lapsilla, mutta luotettava näyttö puuttuu.»D, topiramaatti «Topiramaatti saattaa lopettaa spasmit muille hoidoille resistentissä infantiilispasmioireyhtymässä, mutta luotettava näyttö puuttuu.»D, lamotrigiini «Lamotrigiini saattaa lopettaa spasmit muille hoidoille resistentissä infantiilispasmioireyhtymässä, mutta luotettava näyttö puuttuu.»D, nitratsepaami «Nitratsepaami saattaa vähentää infantiilispasmeja, mutta luotettava näyttö puuttuu.»D ja ketogeeninen dieetti «Prezioso G, Carlone G, Zaccara G ym. Efficacy of k...»58. Luotettava näyttö näiden tehosta kuitenkin puuttuu.
- Myös pyridoksiini (B6-vitamiini) saattaa lopettaa infantiilispasmit joillakuilla potilailla «Pyridoksiini (B6-vitamiini) saattaa lopettaa infantiilispasmit joillakin potilailla, mutta luotettava näyttö puuttuu.»D.
- Seuranta ACTH-hoidon aikana ja jälkeen:
- ACTH-hoitoon näyttää liittyvän suurentunut kuolemanvaara ja muita vakavia haittavaikutuksia, kuten verenpaineen nousu, vaikea infektio, elektrolyyttihäiriö ja lisämunuaisakselin toimintahäiriö «Infantiilispasmien ACTH-hoitoon näyttäisi liittyvän lisääntynyt kuolemanvaara ja muita vakavia haittavaikutuksia kuten verenpaineen nousu, vaikea infektio, elektrolyyttihäiriö sekä lisämunuaisakselin toimintahäiriö.»C, «Granström ML, Gaily E, Liukkonen E. Treatment of i...»48, «Riikonen R, Donner M. ACTH therapy in infantile sp...»59, «Hrachovy RA, Frost JD Jr, Glaze DG. High-dose, lon...»60, «Perheentupa J, Riikonen R, Dunkel L ym. Adrenocort...»61.
- Verenpaineen ja elektrolyyttitasapainon seuranta ja infektioiden huolellinen hoito ACTH-hoidon aikana ovat tärkeitä.
- Hydrokortisonikorvaushoito on tarpeen ACTH-hoidon loputtua «Perheentupa J, Riikonen R, Dunkel L ym. Adrenocort...»61, kunnes lisämunuaisten toiminta on normaalistunut «Leivonen, Peltola, Gaily. Tunnistatko infantiilisp...»55, «Heiskala H, Riikonen R, Santavuori P ym. West synd...»62.
- Seuranta vigabatriinihoidon aikana ja jälkeen:
- Vigabatriinihoito ilmeisesti aiheuttaa konsentrisen näkökenttäpuutoksen lähes puolelle
aikuispotilaista «Vigabatriinihoitoon ilmeisesti liittyy konsentrisen näkökenttäpuutoksen lähes puolella aikuispotilaista ja myös osalla lapsipotilaista.»B.
- Vigabatriinin käyttöön liittyviä näkökenttäpuutoksia esiintyy myös lapsipotilailla «Vanhatalo S, Nousiainen I, Eriksson K ym. Visual f...»54, «Riikonen R, Rener-Primec Z, Carmant L ym. Does vig...»63.
- Imeväisiässä vigabatriinin aiheuttama näkökenttäpuutoksen riski saattaa olla pienempi kuin aikuisilla «Gaily E, Jonsson H, Lappi M. Visual fields at scho...»64, «Schwarz MD, Li M, Tsao J ym. A lack of clinically ...»65, «Vigabatriinihoitoon ilmeisesti liittyy konsentrisen näkökenttäpuutoksen lähes puolella aikuispotilaista ja myös osalla lapsipotilaista.»B, mutta luotettava näyttö asiasta puuttuu.
- Kaikkien vigabatriinia saavien lasten näkökenttiä tulee hoidon aikana seurata niillä menetelmillä, joiden käyttö on lapsen iän ja kehitystason pohjalta mahdollista, ja hoidon päättymisen jälkeen sellaisessa iässä (yleensä 7–10 vuoden iässä), jolloin lapsen yhteistyökyky on riittävä luotettavan tuloksen saamiseksi.
- Imeväisiällä annettuun vigabatriinihoitoon saattaa liittyä magneettikuvauksessa esiin
tulevia ohimeneviä signaalimuutoksia «Imeväisiällä annettuun vigabatriinihoitoon saattaa liittyä magneettikuvauksessa esiin tulevia, hoidon lopetuksen jälkeen ohimeneviä signaalimuutoksia.»C.
- Useimmat lapset ovat oireettomia, joten rutiininomainen kuvaus hoidon aikana ei ole aiheellista.
- Pienelle osalle lapsista tulee liikehäiriötyyppisiä oireita (yleensä dystonia). Oireisilla tulee harkita MRI-kuvausta ja vigabatriinihoidon lopettamista.
- Vigabatriinihoito ilmeisesti aiheuttaa konsentrisen näkökenttäpuutoksen lähes puolelle
aikuispotilaista «Vigabatriinihoitoon ilmeisesti liittyy konsentrisen näkökenttäpuutoksen lähes puolella aikuispotilaista ja myös osalla lapsipotilaista.»B.
Imeväisiän itsestään rajoittuva paikallisalkuinen epilepsia (benign familial or nonfamilial infantile seizures)
- Potilaalla on paikallisalkuisia kohtauksia, jotka esiintyvät usein ryöppyinä «International League Against Epilepsy, http://www....»6.
- Ilmaantuvuus ensimmäisen ikävuoden aikana on 0,2:1 000 «Gaily E, Lommi M, Lapatto R ym. Incidence and outc...»12.
- Tyypillinen alkamisikä on 4–7 kuukautta.
- EEG on kohtausten välillä yleensä normaali.
- Etiologia on geneettinen: noin kolmasosalla potilaista ensimmäisen asteen sukulaisella on ollut samanlaisia kohtauksia ensimmäisen ikävuotensa aikana «Gaily E, Lommi M, Lapatto R ym. Incidence and outc...»12. Esimerkiksi PRRT2-geenin virheitä on yhdistetty tähän epilepsiaan «Schubert J, Paravidino R, Becker F ym. PRRT2 mutat...»66.
- Hoito on samanlaista kuin muissa paikallisalkuisissa epilepsioissa (ks. kohta Paikallisalkuiset epilepsiat «A2»3). Hyvä hoitovaste tukee diagnoosia.
- Kohtaustaipumus häviää viimeistään 2 vuoden ikään mennessä.
- Kehitys etenee normaalisti.
Dravet'n oireyhtymä (aiempi termi imeväisiän vaikea myoklooninen epilepsia, severe myoclonic epilepsy of infancy, SMEI)
- Dravet'n oireyhtymä on harvinainen neurologinen sairaus, jonka ensimmäinen oire on epilepsia «Gaily E, Roivainen R. Dravet´n oireyhtymä - vaikea...»67. Sitä tulee epäillä, jos pitkittyneet (yli 15 minuuttia) kohtaukset kuumeen yhteydessä toistuvat ensimmäisen ikävuoden aikana.
- Kohtaukset alkavat ensimmäisen ikävuoden aikana kuumeiden ja infektioiden yhteydessä.
- Kohtaustyypit «International League Against Epilepsy, http://www....»6:
- Ensimmäisen ikävuoden aikana esiintyy pitkittyneitä, toispuolisia ja puolta vaihtavia toonis-kloonisia kohtauksia.
- Myöhemmin useimmilla potilailla esiintyy paikallisalkuisia ja toonisia kohtauksia
- Monilla potilailla on myös myokloonisia kohtauksia ja epätyypillisiä poissaolokohtauksia.
- Pitkittyneet kohtaukset ja status epilepticukset ovat tavallisia kuumeen yhteydessä ennen asianmukaisen lääkehoidon aloittamista.
- EEG ja magneettikuvauslöydös ovat normaaleja ensimmäisten ikävuosien aikana.
- Etiologia on 80 %:lla potilaista natriumkanavageeni SCN1A:n virhe.
- Kohtaukset ovat vaikeahoitoisia.
- Kognitiivinen kehitys hidastuu kaikilla potilailla. Monelle potilaalle tulee jo lapsuusiällä vaihtelevanasteinen motorinen häiriö.
Hoito
- Työryhmä suosittelee, että hoito aloitetaan yleensä valproaatilla «Chiron C, Dulac O. The pharmacologic treatment of ...»68.
- Jos pitkittyneet kohtaukset jatkuvat, valproaattiin liitetään asteittain klobatsaami ja stiripentoli. Niiden yhdistelmä vähentää tehokkaasti kohtauksia «Stripentolin, valproaatiin ja klobatsaamin yhdistelmä ilmeisesti vähentää lasten ja nuorten kohtauksia Dravet’n oireyhtymässä.»B.
- Topiramaatti voi vähentää kohtauksia «Topiramaatti saattaa vähentää lasten ja nuorten kohtauksia Dravet’n oireyhtymän hoidossa, mutta luotettava näyttö puuttuu.»D.
- Ketogeenisesta ruokavaliohoidosta voi olla hyötyä Dravet'n oireyhtymässä «Dressler A, Trimmel-Schwahofer P, Reithofer E ym. ...»69.
- Bromidi voi vähentää kohtauksia Dravet'n oireyhtymässä, mutta luotettava näyttö asiasta puuttuu «Lotte J, Haberlandt E, Neubauer B ym. Bromide in p...»70.
- Kannabidioli yhdistettynä muihin epilepsialääkkeisiin saattaa vähentää kohtauksia Dravet'n oireyhtymässä «Kannabidioli lisälääkkeenä muiden epilepsialääkkeiden kanssa saattaa vähentää lasten ja nuorten kohtauksia Dravet’n oireyhtymässä.»C.
- Fenfluramiini saattaa vähentää kohtauksia Dravet'n oireyhtymässä, mutta luotettava näyttö asiasta puuttuu «Ceulemans B, Boel M, Leyssens K ym. Successful use...»71, «Schoonjans A, Paelinck BP, Marchau F ym. Low-dose ...»72.
- Fenfluramiinin haittavaikutukset pitkäaikaisessa käytössä voivat olla vähäisiä, mutta luotettava näyttö asiasta puuttuu «Ceulemans B, Schoonjans AS, Marchau F ym. Five-yea...»73.
- Levetirasetaamin tehosta ei ole näyttöä «Chhun S, Troude P, Villeneuve N ym. A prospective ...»74.
- Lamotrigiini «Lamotrigiini saattaa lisätä lasten ja nuorten kohtauksia Dravet’n oireyhtymässä, mutta luotettava näyttö puuttuu.»D ja karbamatsepiini «Karbamatsepiini saattaa lisätä lasten ja nuorten kohtauksia Dravet’n oireyhtymässä, mutta luotettava näyttö puuttuu.»D taas saattavat lisätä kohtauksia.
Myokloonis-atoninen epilepsia
- Myokloonis-atonista epilepsiaa on aiemmin nimitetty myoklonis-astaattiseksi epilepsiaksi tai Doosen oireyhtymäksi.
- Kohtaustyyppejä «International League Against Epilepsy, http://www....»6 ovat
- toonis-klooniset kohtaukset
- myoklooniset kohtaukset
- atoniset kohtaukset
- epätyypilliset poissaolokohtaukset.
- Tavallisin alkamisikä on 2–5 vuotta. Joillakuilla lapsilla on kuumekohtauksia ennen epilepsian toteamista.
- EEG:ssä havaitaan 2–4 Hz:n piikki-hidasaaltopurkauksia ja normaali taustatoiminta. Joillakuilla potilailla vilkkuvalo provosoi purkauksia.
- Etiologia on yleensä tuntematon ja ennuste vaihteleva.
- Osalla potilaista kohtaukset ovat lääkeresistenttejä. Heillä geneettiset tutkimukset ovat aiheellisia.
- Glukoosin kuljettajaproteiini tyyppi 1:n puutosta aiheuttava SLC2A1-geenin mutaatio on yhdessä tutkimuksessa todettu 5 %:lla myokloonis-atonista epilepsiaa sairastavista lapsista «Mullen SA, Marini C, Suls A ym. Glucose transporte...»75. Näillä potilailla ketogeeninen dieetti on tehokas ja ensisijainen epilepsian hoito.
- Merkittäviä kehityksen ongelmia on pitkäaikaisseurannassa 10–20 %:lla «Kilaru S, Bergqvist AGC. Current treatment of myoc...»76, «Oguni H, Tanaka T, Hayashi K ym. Treatment and lon...»77.
Hoito
- Valproaatista «Valproaatti vähentänee lasten kohtauksia myoklonis-atoonisessa epilepsiassa (MAE), mutta luotettava näyttö puuttuu.»D, etosuksimidista «Etosuksimidi vähentänee lasten kohtauksia myokloonisastaattisessa epilepsiassa (MAE), mutta luotettava näyttö puuttuu.»D, klonatsepaamista «Klonatsepaami vähentänee lasten kohtauksia myoklonis-atonisessa epilepsiassa (MAE), mutta luotettava näyttö puuttuu.»D, nitratsepaamista «Nitratsepaami vähentänee lasten kohtauksia myoklonis-atonisessa epilepsiassa (MAE), mutta luotettava näyttö puuttuu.»D, topiramaatista «Topiramaatti vähentänee lasten kohtauksia myoklonis-atoonisessa epilepsiassa (MAE), mutta luotettava näyttö puuttuu.»D, ACTH:sta «ACTH vähentänee lasten kohtauksia myoklonis-atonisessa epilepsiassa (MAE), mutta luotettava näyttö puuttuu.»D, lamotrigiinista «Lamotrigiini saattaa vähentää tai lopettaa kohtaukset lasten myoklonis-atonisessa epilepsiassa (MAE), mutta luotettava näyttö puuttuu.»D ja ketogeenisesta ruokavaliosta «Ketogeeninen dieetti saattaa olla tehokas lasten hoitoresistentin myoklonis-atonisen epilepsian (MAE) hoidossa, mutta luotettava näyttö puuttuu.»Dsaattaa olla hyötyä, mutta luotettavia tutkimuksia aiheesta ei ole. Myös harvinaislääke rufinamidi saattaa olla käyttökelpoinen «von Stülpnagel C, Coppola G, Striano P ym. First l...»78.
- Karbamatsepiini saattaa lisätä kohtauksia «Karbamatsepiinista saattaa olla haittaa lasten myoklonis-atonisen epilepsian (MAE) hoidossa, mutta luotettava näyttö puuttuu.»D.
- Työryhmä suosittelee hoidon aloittamista valproaatilla, johon yhdistetään yleisimmän kohtaustyypin perusteella lamotrigiini tai etosuksimidi. Bentsodiatsepiinilääkitys voi olla tarpeen, jos kohtauksia on paljon. Vaikeahoitoisilla potilailla kannattaa jo 2–3 lääkkeen jälkeen harkita etenemistä ketogeeniseen ruokavaliohoitoon.
Lennox–Gastaut'n oireyhtymä (LGS)
- Lennox–Gastaut'n oireyhtymän diagnoosi perustuu kliiniseen kuvaan, kohtaustyyppeihin ja EEG-löydökseen.
- Tyypillisiä kohtausoireita «International League Against Epilepsy, http://www....»6 ovat tooniset kohtaukset (kaikilla), epätyypilliset poissaolokohtaukset, atoniset kohtaukset (tonuksenmenetyskohtaukset). Lisäksi potilailla on usein epileptisiä spasmeja, myoklonioita ja paikallisalkuisia kohtauksia.
- Tooniset ja atoniset kohtaukset voivat johtaa yllättäviin kaatumisiin, minkä vuoksi niihin liittyy merkittävä tapaturmariski.
- Oireyhtymälle tyypilliset oireet alkavat 1–8 vuoden iässä. Etiologia on monitekijäinen, useimmiten rakenteellinen. Osalla on aiemmin ollut hoitoresistentti infantiilispasmioireyhtymä tai muu vaikea imeväisiän epilepsia.
- EEG:ssä havaitaan hitaita (alle 3 Hz) piikki-hidasaaltopurkauksia, hidastunut taustatoiminta ja unenaikaisia monipiikkipurkauksia.
- Oireyhtymään liittyy vaihtelevan asteinen kehitysvammaisuus ja käyttäytymisen ongelmia.
Hoito
- Kontrolloituja lääketutkimuksia on taudin monimuotoisen taudinkuvan ja harvinaisuuden vuoksi vain vähän.
- Valproaatista on kokemusperäisesti ja avoimien tutkimusten perusteella «Jeavons PM, Clark JE, Maheshwari MC. Treatment of ...»79 hyötyä «Valproaatti monoterapiana saattaa joillain Lennox-Gastaut'n oireyhtymää sairastavilla potilailla lopettaa kohtaukset, mutta luotettava näyttö puuttuu.»D.
- Lamotrigiinista «Lamotrigiini saattaa vähentää lasten Lennox–Gastaut´n oireyhtymän atoonisia ja toonisia kaatumiskohtauksia (drop-kohtaus) ja kaikkia kohtauksia 4 kuukauden seurannassa.»C, «Eriksson AS, Nergårdh A, Hoppu K. The efficacy of ...»80, topiramaatista «Topiramaatti saattaa vähentää Lennox–Gastaut´n oireyhtymän (LGS) atoonisten ja toonisten kaatumiskohtausten (drop-kohtaus) ja tooniskloonisten kohtausten yhteismäärää 2 kuukauden seurannassa.»C ja felbamaatista saattaa olla lisälääkkeinä hyötyä ainakin motoristen kohtausten
(atoniset, tooniset tai lysähtämiset ja toonis-klooniset) osalta.
- Lamotrigiinin on epäilty voivan aiheuttaa hyvin tiheästi toistuvia myoklonisia kohtauksia LGS-potilaalle «Guerrini R, Belmonte A, Parmeggiani L ym. Myocloni...»81.
- Felbamaatin käyttöä rajoittaa aplastisen anemian riski «Pennell PB, Ogaily MS, Macdonald RL. Aplastic anem...»82.
- Rufinamidi saattaa vähentää epätyypillisiä poissaolokohtauksia ja lysähtämiskohtauksia Lennox–Gastaut'n oireyhtymässä, mutta luotettavaa tutkimusnäyttöä asiasta ei ole «Rufinamidi saattaa vähentää epätyypillisiä poissaolo- ja drop-kohtauksia Lennox–Gastaut´n epilepsiassa.»C, «Hancock EC, Cross JH. Treatment of Lennox-Gastaut ...»83.
- Vigabatriinista voi olla hyötyä epileptisten spasmien ja toonisten kohtausten hoidossa
«Vigabatriini valproaatin lisälääkkeenä saattaa vähentää lasten ja nuorten kohtauksia Lennox-Gastaut'n oireyhtymässä, mutta luotettava näyttö puuttuu.»D, mutta se saattaa myös pahentaa myokloonisia kohtauksia «Lortie A, Chiron C, Mumford J ym. The potential fo...»84, «Coppola G, Terraciano AM, Pascotto A. Vigabatrin a...»85.
- Vigabatriinin käyttöä rajoittaa näkökenttäpuutosten riski «Vigabatriinihoitoon ilmeisesti liittyy konsentrisen näkökenttäpuutoksen lähes puolella aikuispotilaista ja myös osalla lapsipotilaista.»B, «Vanhatalo S, Nousiainen I, Eriksson K ym. Visual f...»54.
- Nitratsepaamista «Nitratsepaami lisälääkkeenä saattaa lyhytaikaisesti vähentää lasten Lennox–Gastaut'n oireyhtymän kohtauksia, mutta luotettava näyttö puuttuu.»D, klobatsaamista «Klobatsaami lisälääkkeenä saattaa vähentää Lennox-Gastaut´n oireyhtymän kohtauksia.»C ja klonatsepaamista «Klonatsepaami lisälääkkeenä saattaa vähentää lasten Lennox-Gastau'n oireyhtymän kohtauksia, mutta luotettava näyttö puuttuu.»D voi olla hyötyä, mutta niiden vaarana on toonisten kohtausten paheneminen atyyppistä poissaolokohtausstatusta hoidettaessa «DiMario FJ Jr, Clancy RR. Paradoxical precipitatio...»86, «Livingston JH, Brown JK. Non-convulsive status epi...»87, «Tassinari CA, Dravet C, Roger J ym. Tonic status e...»88.
- Ketogeenisesta ruokavaliosta saattaa olla hyötyä «Ketogeeninen dieetti saattaa vähentää kohtauksia lasten epilepsian hoidossa.»C.
- Kannabidioli lisälääkkeenä vähentänee äkillisiin kaatumisiin johtavia kohtauksia «Kannabidioli lienee tehokas lisälääke äkilliseen kaatumiseen johtavien kohtausten hoitoon Lennox–Gastaut´n oireyhtymän (LGS) hoidossa.»B.
- Prednisonista, prednisolonista ja ACTH:sta voi olla hyötyä LGS:n hoidossa «ACTH, prednisoni ja prednisoloni saattavat vähentää lasten ja nuorten kohtauksia Lennox-Gastaut´n oireyhtymässä, mutta luotettava näyttö puuttuu.»D.
- Työryhmä suosittelee, että ensisijaisena lääkkeenä käytetään valproaattia ja lisälääkkeinä
lamotrigiinia tai rufinamidia. Usein tarvitaan myös bentsodiatsepiinia. Tarvittaessa
voidaan kokeilla vallitsevan kohtaustyypin perusteella ketogeenista dieettiä, kannabidiolia,
topiramaattia, etosuksimidia, levetirasetaamia tai felbamaattia. Työryhmä suosittelee
yleensä käytettäväksi kerrallaan korkeintaan kolmea lääkettä. Täydellisen kohtauksettomuuden
saavuttaminen on harvinaista.
- Samansuuntaiseen suositukseen ovat päätyneet yhdysvaltalaiset ja eurooppalaiset asiantuntijat «Wheless JW, Clarke DF, Carpenter D. Treatment of p...»89, «Wheless JW, Clarke DF, Arzimanoglou A ym. Treatmen...»90.
- Lennox–Gastaut-potilaan osalta tulee arvioida myös stimulaattorihoidon ja leikkaushoidon mahdollisuudet.
Epileptinen enkefalopatia, johon liittyy jatkuva unenaikainen purkaustoiminta EEG:ssä
- Epilepsiaoireyhtymästä tai EEG-löydöksestä käytetään myös nimityksiä CSWS (continuous spike and wave during slow wave sleep) ja ESES (electric status epilepticus in sleep).
- Kyseessä on epilepsiaoireyhtymä, jonka diagnoosi perustuu kliiniseen kuvaan ja EEG-löydöksiin. Kliiniseen kuvaan liittyy kognitiivisen kehityksen hidastuminen tai taantuminen, neurologisia oireita, käytöshäiriöitä ja useimmilla potilailla epilepsiakohtauksia. Epilepsiakohtaukset ovat epätyypillisiä poissaolokohtauksia, negatiivisia myoklonioita ja paikallisalkuisia kohtauksia (jotka voivat edetä toonis-kloonisiksi kohtauksiksi) «International League Against Epilepsy, http://www....»6. EEG:ssä havaitaan lähes jatkuvaa piikki-hidasaaltotoimintaa hidasaaltounen aikana.
- Yleisesti hyväksyttyjä yksityiskohtaisia diagnostisia kriteereitä ei ole.
- Taustasyitä ovat rakenteelliset syyt (mm. polymikrogyria ja perinataalinen talamusvaurio) ja geneettiset syyt (mm. GRIN2A-geenimutaatio «Lemke JR, Lal D, Reinthaler EM ym. Mutations in GR...»91). Myös lapsuusiän epilepsiaoireyhtymät voivat harvoin kehittyä CSWS-oireyhtymän suuntaan.
- Oireyhtymää edeltää yleensä muun tyyppinen epilepsia, joka alkaa 2 kuukauden–8 vuoden iässä. Oireyhtymä ilmaantuu 1–2 vuotta epilepsian alkamisen jälkeen.
Hoito
- Oireyhtymän harvinaisuuden ja sen määrittelyn vaikeuden vuoksi hoitotutkimukset ovat pieniä ja hyvin heterogeenisiä
- Hoidon tehoa tulisi mitata ennen kaikkea kehitystä seuraamalla, ja sen tulisi näkyä kognitiivisen/motorisen kehityksen taantumisen pysähtymisenä tai kehityksen vauhdittumisena tai käytöshäiriöiden lievittymisenä.
- EEG-ilmiön lieventyminen mahdollisesti korreloi kehityksen kohentumiseen, mutta yhteys ei ole suoraviivainen eikä hoidon suunnittelu perustu pelkkään EEG-löydökseen
- Kortikoidisteroidihoito ja bentsodiatsepiinit saattavat tehota CSWS-oireyhtymään paremmin kuin tavanmukaiset epilepsialääkkeet «Steroidihoito, kirurginen hoito ja saattavat olla tehokkaita CSWS-epilepsian hoidossa.»C.
- Tavanmukaisista epilepsialääkkeistä ja hoidoista valproaatista, etosuksimidista «Inutsuka M, Kobayashi K, Oka M ym. Treatment of ep...»92, sultiaamista «Fejerman N, Caraballo R, Cersósimo R ym. Sulthiame...»93, topiramaatista «Vrielynck P, Marique P, Ghariani S ym. Topiramate ...»94, asetatsolamidista «Fine AL, Wirrell EC, Wong-Kisiel LC ym. Acetazolam...»95, levetirasetaamista «Levetirasetaami saattaa vähentää EEG-purkauksia ja kliinisiä oireita CSWS- tai ESES-oireyhtymää sairastavilla lapsilla ja nuorilla, mutta luotettava näyttö puuttuu.»D, lakosamidista «Grosso S, Parisi P, Giordano L ym. Lacosamide effi...»96, amantadiinista «Wilson RB, Eliyan Y, Sankar R ym. Amantadine: A ne...»97 ja ketogeenisestä ruokavaliosta «Nikanorova M, Miranda MJ, Atkins M ym. Ketogenic d...»98 on raportoitu hyötyä pienissä potilasaineistoissa ja vaihtelevilla lääkeyhdistelmillä. Näitä hoitoja voidaan käyttää myös CSWS-oireyhtymään liittyvien epilepsiakohtausten hoidossa.
- Karbamatsepiini ja okskarbatsepiini voivat provosoida epilepsian evoloitumisen CSWS-oireyhtymäksi «Pavlidis E, Rubboli G, Nikanorova M ym. Encephalop...»99.
- Leikkaushoito voi tulla kyseeseen kuratiivisena (hemisfärotomia potilailla, joilla CSWS -oireyhtymän taustalla on laaja keskimmäisen aivovaltimon perinataalinen infarkti tai toispuoleinen aivokuoren kehityshäiriö) tai palliatiivisena (aivokurkiaisen halkaisuleikkaus). Erityisesti edellisissä ryhmissä leikkaushoidon mahdollisuus tulisi arvioida viiveettä CSWS-oireyhtymän osoittauduttua vaikeahoitoiseksi
- Työryhmä suosittelee, että potilaalla, jolla epäillään CSWS-oireyhtymää, mahdollinen
natriumsalpaajalääkitys vaihdetaan valproaatiksi tai levetirasetaamiksi.
- Jos potilaalla todetaan CSWS-oireyhtymä (EEG-ilmiö ja kognitiivinen tai käytöksen muutos), aloitetaan klobatsaami.
- Klobatsaamiin voidaan kombinoida tai sen tilalle vaihtaa valproaatti, levetirasetaami tai topiramaatti.
- Kohtaustyypin mukaan voidaan käyttää lisänä edellä mainittuja lääkkeitä epilepsiakohtausten hoitoon.
- Jos potilaan kehitys taantuu tai on pysähtynyt, harkitaan jo varhaisessa vaiheessa kortikosteroidihoitoa.
Landau–Kleffnerin oireyhtymä
- Landau–Kleffnerin oireyhtymä on hankinnainen afasia, tyypillisimmin verbaalinen auditiivinen agnosia «International League Against Epilepsy, http://www....»6.
- Taudin etiologia on useimmiten tuntematon. Alle 10 %:lla todetaan GRIN2A-geenin mutaatio «Yang X, Qian P, Xu X ym. GRIN2A mutations in epile...»100, «Myers KA, Scheffer IE. GRIN2A-Related Speech Disor...»101.
- Epileptisiä kohtauksia esiintyy 70–80 %:lla potilaista.
- Tauti alkaa 3–8 vuoden iässä.
- EEG:ssä on poikkeava löydös, usein jatkuva unen aikainen purkaustoiminta.
Hoito
- Hoitoperiaate on sama kuin CSWS-oireyhtymässä.
- Spesifisesti Landau–Kleffnerin oireyhtymän hoitoa koskevat tutkimukset ovat olleet hyvin pieniä ja heterogeenisiä, eikä vahvaa näyttöä tehoavista hoidoista ole.
- Pieniä potilasaineistoja on ACTH:n ja kortikosteroidien «ACTH:n ja kortikosteroidien hyödystä lasten Landau-Kleffnerin oireyhtymän hoidossa ei ole luotettavaa tutkimusnäyttöä.»D, epilepsialääkkeiden «Epilepsialääkkeiden hyödystä Landau-Kleffnerin oireyhtymän hoidossa ei ole luotettavaa näyttöä.»D ja suonensisäisen immunoglobuliinin «IV-immunoglobuliin hyödystä lasten Landau-Kleffnerin oireyhtymän hoidossa ei ole luotettavaa tutkimusnäyttöä.»D käytöstä.
Paikallisalkuiset epilepsiat
Lapsuusiän epilepsia, jossa esiintyy keskitemporaalisia piikkejä (ns. rolandinen epilepsia, childhood epilepsy with centrotemporal spikes)
- Potilaalla on toispuolisia kasvojen, suun alueen, kielen ja kurkunpään puutumis- ja nykinäkohtauksia. Osalla potilaista on myös öisiä tajuttomuus-kouristuskohtauksia.
- Osuus paikallisalkuisista lapsuusiässä alkavista epilepsioista on noin 8 % «Fisher RS, Acevedo C, Arzimanoglou A ym. ILAE offi...»9, «Sokka A, Olsen P, Kirjavainen J ym. Etiology, synd...»11, «Kramer U, Nevo Y, Neufeld MY ym. Epidemiology of e...»102.
- Kohtausten esiintyminen rajoittuu useimmilla 3–16 vuoden ikään.
- EEG:ssä havaitaan normaali taustarytmi ja keskitemporaalisia tai keskialueen piikkejä joko yksittäisinä tai ryppäinä 1,5–3 Hz:n taajuudella. Piikit lisääntyvät unessa.
- Aivojen rakennekuvauksissa potilailla ei havaita poikkeavuuksia, eikä heillä ole muita merkittäviä neurologisia oireita.
- Osalla rolandista epilepsiaa sairastavista on kognitiivisia erityisvaikeuksia «Goldberg-Stern H, Gonen OM, Sadeh M ym. Neuropsych...»103, «Neri ML, Guimarães CA, Oliveira EP ym. Neuropsycho...»104, «Wickens S, Bowden SC, D'Souza W. Cognitive functio...»105.
- Alkamisiän, EEG:n ja kuvantamislöydösten osalta tyypillisissä tapauksissa ennuste on kohtausten kannalta erittäin hyvä: vain noin 1 %:lla esiintyy kohtausoireita 16. ikävuoden jälkeen «Camfield CS, Camfield PR. Rolandic epilepsy has li...»106.
Panayiotopouloksen oireyhtymä
- Kohtaukset alkavat usein autonomisina (esim. ihon kalpeus, punoitus tai syanoosi,
pupillien koon vaihtelu, ruumiin lämmönsäätelyn häiriöt, sydämen rytmin ja hengityksen
epäsäännöllisyys) ja niihin liittyy pahoinvointia ja usein oksentamista, mutta tajunta
voi säilyä normaalina «Eriksson KJ, Koivikko MJ. Prevalence, classificati...»15.
- Vajaa puolet kohtauksista pitkittyy autonomiseksi status epilepticukseksi.
- Kohtauksen edetessä tajunta usein häiriintyy ja katse tai pää voi devioida, ja noin
puolet kohtauksista päättyy joko hemikonvulsiivisena tai tajuttomuus-kouristuskohtauksena.
- Motoristen oireiden sijasta saattaa esiintyä pelkkä tajuttomuus ja velttous ("iktaalinen synkopee").
- Kaksi kolmasosaa kohtauksista alkaa yöllä.
- Yleisin alkamisikä on noin 5 vuotta.
- EEG:ssä havaitaan normaali taustatoiminta. Oksipitaalisia piikkejä voi esiintyä, mutta EEG:ssä saatetaan havaita multifokaalisia piikkejä, joita uni aktivoi. Unessa piikkitoiminta voi olla hyvin runsasta tai jopa jatkuvaa. Löydös voi harvoin olla myös normaali. Silmien sulkeminen voi aktivoida etenkin oksipitaalisia piikkejä.
- Ennuste on erittäin hyvä: useimmat potilaat saavat vain 1–3 kohtausta elämänsä aikana ja saavuttavat remission 1–2 vuoden kuluessa ensimmäisestä kohtauksesta «Eriksson KJ, Koivikko MJ. Prevalence, classificati...»15.
Lapsuusiän takaraivolohkoepilepsia
- Gastaut'n oireyhtymä, childhood occipital epilepsy «Eriksson KJ, Koivikko MJ. Prevalence, classificati...»15:
- Visuaaliset hallusinaatiot ja näköhäiriöt (hetkellinen sokeus tai näkökenttäpuutos)
ovat yleisimpiä kohtausoireita.
- Tajunta säilyy useimmissa kohtauksissa, mutta se voi häiriintyä, jos kohtaus pitkittyy tai yleistyy.
- Ei-visuaalisina oireina esiintyy katseen deviaatiota, okulokloonisia kohtauksia ja silmien räpyttelyä.
- Yleistymistä tajuttomuus-kouristuskohtaukseksi, hemikonvulsiivisiksi tai tajunnanhämärtymiskohtauksiksi esiintyy 13–43 %:lla potilaista.
- Kohtauksia esiintyy useita päivässä. Niiden kesto on lyhyt mutta vaihtelu suurta (1 sekunnista 3 minuuttiin).
- Yleisin alkamisikä noin 8 vuotta.
- EEG:ssä havaitaan normaali taustatoiminta ja oksipitaalisia piikkejä, etenkin kun silmät suljetaan tai peitetään. Joskus piikit esiintyvät vain unessa.
- Ennuste on epävarma, mutta kohtauksettomaksi tulemisen todennäköisyydeksi on arvioitu noin 60 %.
Muut geneettiset paikallisalkuiset epilepsiat
- Paikallisalkuisten epilepsioiden taustalla on tunnistettu useita geenivirheitä (mm. autosomaalisesti dominantisti periytyvä yöllinen otsalohkoepilepsia) «Boillot M, Baulac S. Genetic models of focal epile...»107.
- Geneettisiä tutkimuksia tulisi harkita erityisesti silloin, kun kuvantamistutkimukset ovat jääneet negatiivisiksi ja epilepsia on vaikea.
Rakenteelliset ja tuntemattomasta syystä johtuvat paikallisalkuiset epilepsiat
- Yli puolet lapsuus- ja nuoruusiässä alkavista paikallisalkuisista epilepsioista on rakenteellisia ja tuntemattomasta syystä johtuvia paikallisalkuisia epilepsioita.
- Kohtausoireiden tyyppi määräytyy sen perusteella, miltä aivoalueelta ne ovat peräisin.
- Rakenteellisissa ja tuntemattomasta syystä johtuvissa epilepsioissa diagnoosi perustuu kliinisiin piirteisiin, jotka sopivat kohtausten paikallisalkuisuuteen sekä EEG:hen ja kuvantamislöydöksiin.
- Kohtaukset voivat alkaa missä iässä tahansa, myös ensimmäisen ikävuoden aikana.
Paikallisalkuisten epilepsioiden hoito
- Lääkkeen valintaan vaikuttavat epilepsiaoireyhtymä, ikä, sukupuoli ja lääkkeen siedettävyys.
- Itsestään rajoittuvissa geneettisissä, paikallisalkuisissa epilepsiaoireyhtymissä
lääkehoitoa ei aina tarvita, etenkään jos kohtauksia esiintyy harvoin eivätkä ne yleisty
tajuttomuus-kouristuskohtauksiksi «Loiseau P, Duché B, Cordova S ym. Prognosis of ben...»108.
- Tyypillisessä rolandisessa epilepsiassa lääkehoidon (jos sitä tarvitaan) kestoksi saattaa riittää yksi kohtaukseton vuosi «Braathen G, Andersson T, Gylje H ym. Comparison be...»40, «Tan HJ, Singh J, Gupta R ym. Comparison of antiepi...»109.
- Paikallisalkuisten epilepsioiden lääkehoidon tehon arvioinnissa voidaan yli kaksivuotiailla lapsilla hyödyntää ekstrapolaatioperiaatteen «Paikallisalkuisen epilepsian hoitoon tarkoitettujen antiepileptisten lääkkeiden aikuisilla osoitetun tehon ekstrapolaatio lapsipotilaisiin»1 mukaisesti myös aikuisilla tehtyjä tutkimuksia. Kliinisessä käytössä on kuitenkin huomioitava kunkin lääkkeen viralliset käyttöaiheet eri ikäryhmissä.
- Paikallisalkuisten epilepsioiden hoidossa ensisijainen lääke on okskarbatsepiini «Okskarbatsepiini saattaa olla tehokas lasten ja nuorten paikallisalkuisten epileptisten kohtausten ensisijaislääkkeenä.»B (aikuisilla «Okskarbatsepiini on tehokas paikallisalkuisten ja toonis-kloonisten kohtausten ensisijaislääke.»A) tai karbamatsepiini «Karbamatsepiini ja fenytoiini lienevät yhtä tehokkaita lasten ja nuorten paikallisalkuisen epilepsian ensisijaislääkkeinä.»C (aikuisilla «Karbamatsepiini on tehokas paikallisalkuisten ja toonis-kloonisten kohtausten ensisijaislääke.»A) tai levetirasetaami «Levetirasetaami saattaa olla yhtä tehokas kuin karbamatsepiini tai okskarbatsepiini lasten ja nuorten paikallisalkuisen epilepsian ensisijaislääkkeinä, mutta luotettava näyttö puuttuu.»D (aikuisilla «Levetirasetaami on kliiniseltä käytettävyydeltään karbamatsepiinia vastaava paikallisalkuisen epilepsian ja toonis-kloonisten kohtausten ensisijaislääke.»A).
- Vaihtoehtoisia monoterapialääkkeitä ovat lamotrigiini «Lamotrigiini saattaa olla yhtä tehokas kuin karbamatsepiini paikallisalkuisen epilepsian ensisijaislääkkeenä.»C, (aikuisilla «Lamotrigiini on ilmeisesti teholtaan ja haittavaikutuksiltaan kliinisesti karbamatsepiinia vastaava paikallisalkuisen epilepsian ja toonis-kloonisten kohtausten ensisijaislääke.»B),klobatsaami «Klobatsaami saattaa olla yhtä tehokas kuin fenytoiini tai karbamatsepiini lasten ja nuorten paikallisalkuisissa ja yleistyneissä toonis-kloonisissa kohtauksissa.»C, topiramaatti «Topiramaatti saattaa olla yhtä tehokas kuin karbamatsepiini ja valproaatti lasten ja nuorten paikallisalkuisten kohtausten ensisijaislääkkeenä.»B, (aikuisilla «Topiramaatti on tehokas paikallisalkuisten ja toonis-kloonisten kohtausten ensisijaislääke.»A), sekä eslikarbatsepiini (lapsilla ei tutkimuksia, aikuisilla «Eslikarbatsepiiniasetaatti lienee teholtaan karbamatsepiinin veroinen paikallisalkuisen epilepsian ensisijaislääkkeenä.»B), gabapentiini (aikuisilla «Gabapentiini on ilmeisesti kliiniseltä käytettävyydeltään karbamatsepiinia vastaava paikallisalkuisten kohtausten ensisijaislääke.»B), lakosamidi (aikuisilla «Lakosamidi on ilmeisesti kliiniseltä käytettävyydeltään karbamatsepiinia vastaava paikallisalkuisen epilepsian ja toonis-kloonisten kohtausten ensisijaislääke.»B) ja tsonisamidi (aikuisilla «Tsonisamidi on ilmeisesti kliiniseltä käytettävyydeltään karbamatsepiinia vastaava paikallisalkuisen epilepsian ja toonis-kloonisten kohtausten ensisijaislääke.»B) . Myös valproaattia «Karbamatsepiini- ja valproaattimonoterapiat lienevät yhtä tehokkaita lasten ja nuorten paikallisalkuisten ja toonis-kloonisten kohtausten ensisijaislääkkeinä.»C (aikuisilla «Valproaatti on tehokas paikallisalkuisten ja toonis-kloonisten kohtausten ensisijaislääke.»A) voi käyttää ottaen huomioon sen käyttörajoitukset.
- Paikallisalkuisten epilepsioiden lisälääkkeinä voidaan käyttää gabapentiinia «Gabapentiini saattaa olla tehokas lasten paikallisen epilepsian lisälääke mutta luotettava näyttö puuttuu.»D (aikuisilla «Gabapentiini on tehokas paikallisalkuisen epilepsian lisälääke.»A), lamotrigiinia «Lamotrigiini on ilmeisesti tehokas lasten ja nuorten paikallisalkuisen epilepsian lisälääke.»B (aikuisilla «Lamotrigiini on tehokas paikallisalkuisen epilepsian lisälääke.»A), , lakosamidia «Lakosamidi lisälääkkeenä saattaa vähentää osalla paikallisalkuista epilepsiaa sairastavilla lapsilla ja nuorilla epileptisiä kohtauksia ja on kohtalaisen hyvin siedetty.»B (aikuisilla «Lakosamidi vähentää lisälääkkeenä lumelääkkeeseen verrattuna paikallisalkuisia epilepsiakohtauksia.»A), levetirasetaamia «Levetirasetaami lisälääkkeenä vähentää kohtauksia lasten paikallisalkuisessa epilepsiassa. Levetirasetaami lisälääkkeenä vähentää kohtauksia lasten paikallisalkuisessa epilepsiassa.»A, okskarbatsepiinia «Okskarbatsepiini saattaa vähentää kohtauksia paikallisalkuisen epilepsian lisälääkkeenä alle kouluikäisillä lapsilla.»Ctai topiramaattia «Topiramaatti saattaa olla tehokas lasten ja nuorten paikallisalkuisen epilepsian lisälääke.»B (aikuisilla «Topiramaatti on tehokas paikallisalkuisen epilepsian lisälääke.»A) sekä perampaneelia (lapsilla ei tutkimuksia, aikuisilla «Pitkävaikutteinen risperidoni ilmeisesti on tehokas kaksisuuntaisen mielialahäiriön (tyypin 1) ylläpitohoidossa estämään mielialan kohoamisia.»B), tsonisamidia (aikuisilla «Tsonisamidi on tehokas paikallisalkuisen epilepsian lisälääke.»A), brivarasetaamia (aikuisilla «Brivarasetaami on tehokas paikallisalkuisen epilepsian lisälääke nuorilla ja aikuisilla ainakin lyhytaikaisessa käytössä.»A), eslikarbatsepiinia (aikuisilla «Brivarasetaami on tehokas paikallisalkuisen epilepsian lisälääke nuorilla ja aikuisilla ainakin lyhytaikaisessa käytössä.»A) tai klobatsaamia «Patsalos PN, Spencer EP, Berry DJ. Therapeutic Dru...»110.
- Erityistilanteissa (esim. muiden lääkkeiden tehon puute) voidaan käyttää fenytoiinia
«Karbamatsepiini ja fenytoiini lienevät yhtä tehokkaita lasten ja nuorten paikallisalkuisen epilepsian ensisijaislääkkeinä.»C, fenobarbitaalia «de Silva M, MacArdle B, McGowan M ym. Randomised c...»111 tai vigabatriinia «Zamponi N, Cardinali C. Open comparative long-term...»112.
- Vigabatriinia käytettäessä on otettava huomioon näkökenttäpuutoksen riski «Vigabatriinihoitoon ilmeisesti liittyy konsentrisen näkökenttäpuutoksen lähes puolella aikuispotilaista ja myös osalla lapsipotilaista.»B, «Vanhatalo S, Nousiainen I, Eriksson K ym. Visual f...»54.
- Fenytoiinin käyttöä rajoittavat muun muassa sen yhteisvaikutukset, haittavaikutukset, pitoisuuden seurantatarve ja kapea terapeuttinen hoitoalue.
- Fenobarbitaalin pitkäaikaista käyttöä tulisi välttää lapsilla, sillä sen on osoitettu aiheuttavan lievän mutta palautumattoman kognitiivisen tason laskun «Farwell JR, Lee YJ, Hirtz DG ym. Phenobarbital for...»113.
- Lääkkeen valinta edellyttää aina yksilöllisten tekijöiden huomioimista ja hoidon tehon ja mahdollisten haittavaikutusten suhteen arviointia.
- Kehityksen ja mahdollisten neurologisten oireiden huomioiminen on tärkeää myös itsestään rajoittuviksi diagnosoiduissa lapsuusiän epilepsioissa.
Lapsuus- ja nuoruusiän yleistyneet epilepsiat
- Yleistyneet epilepsiat muodostavat lapsuus- ja nuoruusiässä oireyhtymäjatkumon, johon
kuuluvat lapsuusiän poissaoloepilepsia ja muut yleistyneet, vaihtelevasti ilmenevät
epilepsiat:
- nuoruusiän poissaoloepilepsia, nuoruusiän myokloonusepilepsia ja epilepsia, jossa esiintyy ainoastaan yleistyneitä tajuttomuus-kouristuskohtauksia.
Lapsuusiän poissaoloepilepsia
- Lapsuusiän poissaoloepilepsia «Eriksson KJ, Koivikko MJ. Prevalence, classificati...»15:
- Potilaalla on lyhyitä (4–20 sekuntia) ja tiheästi (kymmeniä päivässä) esiintyviä poissaolokohtauksia, joihin kuuluu yhtäkkinen lyhyt tajunnanhäiriö.
- Hieman yli 10 %:lla esiintyy myöhemmin yleistyneitä toonis-kloonisia kohtauksia «Shinnar S, Cnaan A, Hu F ym. Long-term outcomes of...»114.
- Sairaus alkaa 2. ja 12. ikävuoden välillä, useimmiten 5–7 vuoden iässä.
- Neurologinen kehitys on normaalia, mutta kolmasosalla esiintyy tarkkaavuushäiriötä «Masur D, Shinnar S, Cnaan A ym. Pretreatment cogni...»115.
- Kohtausten aikana EEG:ssä havaitaan lapsuusiän poissaoloepilepsiassa säännöllisiä 3 Hz:n piikkihidasaaltopurkauksia.
- Poissaoloepilepsia on epätodennäköinen, ellei 5 minuutin hyperventilaatiolla saada esiin tyypillistä EEG-poikkeavuutta.
Hoito
- Etosuksimidi ja valproaatti lienevät yhtä tehokkaita lapsuusiän poissaolokohtausten
hoidossa «Etosuksimidilla ja valproaatilla on ilmeisesti yhtä hyvä ja lamotrigiinia parempi teho poissaolokohtauksiin lapsuusiän poissaoloepilepsiassa.»B.
- Aloituslääkkeeksi suositellaan lapsuusiän poissaoloepilepsiaan ensisijaisesti etosuksimidia, koska valproaatilla saattaa olla enemmän haittavaikutuksia «Glauser TA, Cnaan A, Shinnar S ym. Ethosuximide, v...»116, «Glauser TA, Cnaan A, Shinnar S ym. Ethosuximide, v...»117.
- Jos lapsella on ollut tajuttomuus-kouristuskohtauksia, aloitetaan valproaatilla.
- Ellei ensin aloitettu lääke tehoa, se voidaan vaihtaa toiseen «Cnaan A, Shinnar S, Arya R ym. Second monotherapy ...»118.
- Jos kohtaukset jatkuvat, voidaan käyttää yhdistelmälääkitystä.
- Tässä epilepsiaoireyhtymässä valproaattia voidaan käyttää sekä tytöillä että pojilla, koska kohtaustaipumus suurimmalla osalla potilaista häviää ennen murrosikää «Morse E, Giblin K, Chung MH ym. Historical trend t...»119.
- Lisälääkkeenä voidaan käyttää lapsuusiän poissaoloepilepsiassa lamotrigiinia «Besag FM, Wallace SJ, Dulac O ym. Lamotrigine for ...»120, tai klonatsepaamia «Naito H, Wachi M, Nishida M. Clinical effects and ...»121, tai amantadiinia «Sreedharan M, Devadathan K, Pathan HK ym. Amantadi...»122, «Perry MS, Bailey LJ, Kotecha AC ym. Amantadine for...»123.
- Levetirasetaamin tehosta lapsuusiän poissaoloepilepsiassa ei ole näyttöä «Fattore C, Boniver C, Capovilla G ym. A multicente...»124. Sama koskee topiramaattia «Näyttö topiramaatin tehosta lasten ja nuorten poissaoloepilepsiassa puuttuu.»D, «Biton V, Montouris GD, Ritter F ym. A randomized, ...»125, «Piña-Garza JE, Schwarzman L, Wiegand F ym. A pilot...»126.
- Karbamatsepiini, fenytoiini, okskarbatsepiini, vigabatriini, gabapentiini ja pregabaliini voivat lisätä kohtauksia «Glauser T, Ben-Menachem E, Bourgeois B ym. ILAE tr...»127.
Nuoruusiän poissaoloepilepsia, nuoruusiän myokloonusepilepsia ja yleistyneet heräämisen yhteydessä ilmenevät tajuttomuus-kouristuskohtaukset
- Nämä epilepsiat alkavat yleensä noin 10–15 vuoden iässä.
- Kohtaustaipumus on pitkäaikainen, eikä lääkitystä pidä yrittää purkaa lapsuus- ja nuoruusiällä «Healy L, Moran M, Singhal S ym. Relapse after trea...»38, «Höfler J, Unterberger I, Dobesberger J ym. Seizure...»39.
- Nuoruusiän poissaoloepilepsian «Epilepsiat (aikuiset)»5 ja nuoruusiän myokloonusepilepsia «Epilepsiat (aikuiset)»5 osalta viitataan Käypä hoito -suositukseen Epilepsia (aikuiset) «Epilepsiat (aikuiset)»5, «Epilepsiat (aikuiset). Käypä hoito -suositus. Suom...»37.
Hoito yleistyneissä epilepsioissa, joissa oireyhtymädiagnoosi on jäänyt epäselväksi
- Valproaattia voi käyttää ensisijaislääkkeenä muilla kuin fertiili-ikäisillä ja fertiili-ikää lähestyvillä tytöillä «Nevitt SJ, Sudell M, Weston J ym. Antiepileptic dr...»128.
- Vaihtoehtoisia ensisijaislääkkeitä ovat levetirasetaami ja lamotrigiini «Nevitt SJ, Sudell M, Weston J ym. Antiepileptic dr...»128.
- Topiramaatti saattaa olla yhtä tehokas kuin valproaatti yleistyneen epilepsian ainoana lääkkeenä «Lasten ja nuorten yleistyneissä epilepsioissa valproaatti lienee tehokkaampi kuin lamotrigiini sekä yhtä tehokas, mutta paremmin siedetty, kuin topiramaatti.»C, mutta sillä voi olla enemmän sivuvaikutuksia kuin valproaatilla «Marson AG, Al-Kharusi AM, Alwaidh M ym. The SANAD ...»129 sekä enemmän teratogeenisia vaikutuksia kuin levetirasetaamilla ja lamotrigiinilla «Vossler DG. Comparative Risk of Major Congenital M...»130.
- Tsonisamidi saattaa olla tehokas ainoana lääkkeenä «Kothare SV, Kaleyias J, Mostofi N ym. Efficacy and...»131, mutta sillä on virallinen käyttöaihe vain paikallisalkuiseen epilepsiaan.
- Lisälääkkeinä voidaan käyttää, haittavaikutusprofiilien mukaan yhtä tai useampia seuraavista
(aakkosjärjestyksessä):
- lamotrigiini «Lamotrigiini lisälääkkeenä vähentänee lasten ja nuorten yleistyneitä toonis-kloonisia kohtauksia.»C
- levetirasetaami «Levetirasetaami lisälääkkeenä vähentää toonis-kloonisten ja myoklonisten kohtausten esiintymistä lasten ja nuorten yleistyneessä epilepsiassa.»A ja
- perampaneeli «French JA, Krauss GL, Wechsler RT ym. Perampanel f...»132
- topiramaatti «Topiramaatti lisälääkkeenä ilmeisesti vähentää lasten ja nuorten yleistyneitä toonis-kloonisia kohtauksia.»B
- tsonisamidi «Marinas A, Villanueva V, Giráldez BG ym. Efficacy ...»133 tai
- valproaatti «Coulter DL, Wu H, Allen RJ. Valproic acid therapy ...»134, «Tomson T, Battino D, Bonizzoni E ym. Dose-dependen...»135.
Unverricht–Lundborgin tauti (EPM1)
- Unverricht–Lundborgin tauti on yleisin progressiivinen myokloonusepilepsia, jonka ennuste vaihtelee ja joka kuuluu suomalaiseen tautiperintöön.
- Tauti aiheutuu kystatiini B (CSTB) -geenin mutaatiosta. Suurimmalla osalla suomalaisista EPM1-potilaista (99 %) tauti aiheutuu geenin säätelyalueen 12 emästä käsittävän (dodekameeri) toistojakson monistumamutaatiosta, joka ei tule esiin tavanomaisissa geenipaneelitutkimuksissa.
- Kliinisinä oireina on ulkoisten ärsykkeiden laukaisemia myoklonioita, toonis-kloonisia kohtauksia ja ataksiaa. Lisäksi voi olla muita neurologisia oireita ja löydöksiä «Unverricht-Lundborgin tauti (progressiivinen myoklonusepilepsia tyyppi 1, EPM1)»1 (vaatii käyttöoikeuden)
- Diagnoosi perustuu kliiniseen kuvaan ja DNA-tutkimukseen.
- Sairaus alkaa 6–15 vuoden iässä. EEG:ssä todetaan yleistyneet 3–5 Hz:n piikki-monipiikki-hidasaaltopurkaukset ja selkeä vilkkuvaloherkkyys. Taustatoiminta muuttuu usein normaalia hitaammaksi taudin jatkuessa.
- Hoitoa käsitellään Käypä hoito -suosituksessa Epilepsia (aikuiset) «Epilepsiat (aikuiset)»5, «Epilepsiat (aikuiset). Käypä hoito -suositus. Suom...»37.
Epilepsian kirurginen hoito
- Kirurgisen hoidon mahdollisuudet tulisi selvittää lapsen kehitystasosta riippumatta,
jos epilepsia on osoittautunut vaikeaksi. Ks. kohta Määritelmät ja kliiniset oireet
«A1»2, «Granström ML, Gaily E, Herrgård E. Kannattaako las...»136, «Cross JH. Epilepsy surgery in childhood. Epilepsia...»137, «Immonen A, Kälviäinen R, Gaily E, Blomstedt G. Kuk...»138, «Gaily E. Epilepsian kirurginen hoito voi muuttaa l...»139.
- Sama koskee imeväisikäisiä ja infantiilispasmioireyhtymää, Lennox–Gastaut'n ja CSWS-oireyhtymää «Kwon HE, Eom S, Kang HC ym. Surgical treatment of ...»140, «Peltola ME, Liukkonen E, Granström ML ym. The effe...»141, «Jeong A, Strahle J, Vellimana AK ym. Hemispherotom...»142, «Lee YJ, Kang HC, Lee JS ym. Resective pediatric ep...»143.
- Sama koskee lisäksi niitä lapsia, joiden magneettikuvauslöydös on tulkittu normaaliksi «Ansari SF, Maher CO, Tubbs RS ym. Surgery for extr...»144 tai joilla ei ole paikantavaa EEG-löydöstä «Wyllie E, Lachhwani DK, Gupta A ym. Successful sur...»145, «Yasuhara A, Yoshida H, Hatanaka T ym. Epilepsy wit...»146, ellei ole tiedossa sellaista etiologiaa, joka sulkee leikkaushoidon pois.
- Sama koskee tuberoosiskleroosipotilaita, joilla on useita kortikaalisia kyhmyjä .
- Geneettinen etiologia ei ole ehdoton este leikkaushoidolle, mutta se saattaa huonontaa leikkauksen jälkeistä kohtauksettomuuden ennustetta «Stevelink R, Sanders MW, Tuinman MP ym. Epilepsy s...»148.
- Vaikeahoitoisuuden toteamiseen voi imeväisiässä riittää muutama kuukausi «Cross JH. Epilepsy surgery in childhood. Epilepsia...»137.
- Leikkaushoito on ilmeisesti lääkehoitoa tehokkaampi kohtauksettomuuden saavuttamisessa leikkaushoitoon sopivilla vaikeaa epilepsiaa sairastavilla lapsipotilailla yhden vuoden seurannassa «Epilepsian kirurginen hoito ilmeisesti on tehokkaampi kuin lääkehoito lapsipotilailla, joilla on leikkaushoitoon soveltuva vaikea epilepsia.»B.
- Ohimolohkoepilepsian leikkaushoito:
- Lääkehoidosta huolimatta oireilevan ohimolohkoepilepsian leikkaushoito ilmeisesti lopettaa kohtaukset yli puolella aikuispotilaista ja on tehokkaampaa kuin lääkehoito «Lääkehoidosta huolimatta oireilevan ohimolohkoepilepsian leikkaushoito aikuisilla ilmeisesti lopettaa kohtaukset yli puolella potilaista, ja on tehokkaampaa kuin lääkehoito.»B.
- Ohimolohkoepilepsian leikkaushoito lapsuusiässä saattaa lopettaa kohtaukset noin 2/3:lla
potilaista «Ohimolohkoepilepsian leikkaushoito lapsuus- ja nuoruusiässä saattaa lopettaa kohtaukset noin 2/3:lla potilaista.»C.
- Pitkäaikaistulokset (vähintään 5 vuoden seuranta) ovat samansuuntaisia kuin tulokset vuoden seurannan jälkeen «Téllez-Zenteno JF, Dhar R, Wiebe S. Long-term seiz...»149.
- Kognitiivinen kokonaissuoriutuminen ja muisti säilyvät leikkauksen jälkeen joko entisellään tai paranevat yli 70 %:lla potilaista «Flint AE, Waterman M, Bowmer G ym. Neuropsychologi...»150.
- Ohimolohkon ulkopuolisen epilepsian leikkaushoito:
- Ohimolohkon ulkopuolisen paikallisalkuisen epilepsian leikkaushoito lapsuusiässä saattaa
lopettaa kohtaukset yli puolella potilaista, kun seuranta-aika on vähintään 12 kuukautta,
mutta luotettava tieto asiasta puuttuu «Ohimolohkon ulkopuolisen paikallisalkuisen epilepsian leikkaushoito lapsuus- ja nuoruusiässä saattaa lopettaa kohtaukset yli puolella potilaista mutta luotettava näyttö puuttuu.»D.
- Takaraivolohkon ja päälaenlohkon epilepsian leikkaushoito lapsuusiässä lopettaa kohtaukset vähintään vuoden seurannassa 40–80 %:lla potilaista «Ansari SF, Maher CO, Tubbs RS ym. Surgery for extr...»144, «Ramantani G, Stathi A, Brandt A ym. Posterior cort...»151, «Sierra-Marcos A, Fournier-Del Castillo MC, Álvarez...»152, «Liava A, Mai R, Tassi L ym. Paediatric epilepsy su...»153, «Englot DJ, Breshears JD, Sun PP ym. Seizure outcom...»154.
- Otsalohkoepilepsian leikkaushoito lapsuusiässä lopettaa kohtaukset vähintään vuoden seurannassa 40–60 %:lla potilaista «Ansari SF, Maher CO, Tubbs RS ym. Surgery for extr...»144, «Ramantani G, Kadish NE, Mayer H ym. Frontal Lobe E...»155.
- Pitkäaikaisseurannassa kohtauksettomien osuus pienenee mutta tulokset vaihtelevat suuresti tutkimusten välillä. Vähintään 5 vuoden seurannassa kohtauksettomia on 27–70 % leikatuista «Téllez-Zenteno JF, Dhar R, Wiebe S. Long-term seiz...»149, «Englot DJ, Han SJ, Rolston JD ym. Epilepsy surgery...»156.
- Ohimolohkon ulkopuolisen paikallisalkuisen epilepsian leikkaushoito lapsuusiässä saattaa
lopettaa kohtaukset yli puolella potilaista, kun seuranta-aika on vähintään 12 kuukautta,
mutta luotettava tieto asiasta puuttuu «Ohimolohkon ulkopuolisen paikallisalkuisen epilepsian leikkaushoito lapsuus- ja nuoruusiässä saattaa lopettaa kohtaukset yli puolella potilaista mutta luotettava näyttö puuttuu.»D.
- Aivopuoliskon poistoa (hemisfärektomia) tai hermoyhteyksien katkaisuleikkausta (hemisfärotomia)
voidaan harkita potilaille, joilla on useita aivolohkoja käsittävä toispuolinen epilepsiaa
aiheuttava alue ja toispuolihalvaus jo ennen leikkausta «Granström ML, Gaily E, Herrgård E. Kannattaako las...»136, «Cross JH. Epilepsy surgery in childhood. Epilepsia...»137, «Pulsifer MB, Brandt J, Salorio CF ym. The cognitiv...»157, «Gaily E, Hellén H, Metsähonkala L ym. Aivopuolisko...»158.
- Yli 70 % potilaista on kohtauksettomia vähintään vuoden leikkauksen jälkeen «Gaily E, Hellén H, Metsähonkala L ym. Aivopuolisko...»158, «Griessenauer CJ, Salam S, Hendrix P ym. Hemisphere...»159, «Hu WH, Zhang C, Zhang K ym. Hemispheric surgery fo...»160.
- Yli puolet potilaista (61 %) on kohtauksettomia vähintään 5 vuotta leikkauksen jälkeen «Téllez-Zenteno JF, Dhar R, Wiebe S. Long-term seiz...»149, «Moosa AN, Jehi L, Marashly A ym. Long-term functio...»161, «Althausen A, Gleissner U, Hoppe C ym. Long-term ou...»162.
- Niillä potilailla, joilla vaikeaa epilepsiaa aiheuttavaa aivoaluetta ei ole mahdollista poistaa eikä eristää, kohtauksia voidaan yrittää lievittää aivokurkiaisen halkaisulla «Gaily E, Esko L, Blomstedt G ym. Aivokurkiaisen ha...»163. Aivokurkiaisen halkaisu vähentää merkittävästi kaatumiseen johtavia kohtauksia yli 50 %:lla potilaista «Téllez-Zenteno JF, Dhar R, Wiebe S. Long-term seiz...»149, «Graham D, Tisdall MM, Gill D. Corpus callosotomy o...»164.
- Niillä lapsilla, joilla leikkausmahdollisuuden selvittelyn tuloksena on soveltumattomuus
leikkaushoitoon, voidaan yrittää vähentää tai lievittää kohtauksia vagushermostimulaatiolla
(VNS).
- Vagusstimulaattorihoito saattaa vähentää kohtauksia lisähoitona lasten vaikeassa epilepsiassa «Vagusstimulaattorihoito lisähoitona saattaa vähentää kohtauksia lasten ja nuorten vaikeassa epilepsiassa.»C. Syväaivostimulaatiosta (deep brain stimulation, DBS) ei ole lapsilla tutkimustietoa.
- Potilailla, joille on asennettu vagusstimulaattori, tulisi ennen siirtoa aikuisneurologian puolelle kirjata potilaskertomukseen, onko vagusstimulaattorilla ollut vastetta ja tulisiko stimulaattorin paristo vaihtaa siinä vaiheessa, kun sen virta on loppumassa.
- Oikein valituilla potilailla eivät neurologiset tai kognitiiviset ongelmat lisäänny merkittävästi leikkaushoidon jälkeen «Pulsifer MB, Brandt J, Salorio CF ym. The cognitiv...»157, «Gaily E, Esko L, Blomstedt G ym. Aivokurkiaisen ha...»163, «Korkman M, Granström ML, Kantola-Sorsa E ym. Two-y...»165, «Téllez-Zenteno JF, Dhar R, Hernandez-Ronquillo L y...»166.
- Leikkaushoito voi estää epilepsian aiheuttamaa kognitiivista heikentymistä ja vähentää epilepsian aiheuttamia käytöshäiriöitä lapsilla «Sibilia V, Barba C, Metitieri T ym. Cognitive outc...»167, «Otsuki T, Kim HD, Luan G ym. Surgical versus medic...»168, «Law N, Kerr E, Smith ML. Evaluation of behavioral ...»169, «Elliott IM, Lach L, Kadis DS ym. Psychosocial outc...»170, «Puka K, Smith ML. Long-term outcomes of behavior p...»171.
- Epilepsialääkkeiden vähentäminen kirurgisen hoidon jälkeen saattaa parantaa lasten kognitiivista ennustetta «Boshuisen K, van Schooneveld MM, Uiterwaal CS ym. ...»172, «Viggedal G, Olsson I, Carlsson G ym. Intelligence ...»173.
- Lapsuusiässä tehty epilepsiakirurgia voi parantaa sosiaalista hyvinvointia nuoressa aikuisiässä ja elämänlaatua niillä potilailla, joiden kohtaukset ovat pysyneet poissa leikkauksen jälkeen verrattuna edelleen kohtauksia saaviin lapsuusiällä leikattuihin ja leikkaamattomiin potilaisiin «Gaily E. Epilepsian kirurginen hoito voi muuttaa l...»139.
Epilepsian ruokavaliohoito
- Ruokavaliohoitoja ovat klassinen ketogeeninen ruokavaliohoito, modifioitu ketogeeninen ruokavaliohoito ja vähähiilihydraattinen ruokavaliohoito (low glycemic index) «Kossoff EH, McGrogan JR, Bluml RM ym. A modified A...»174.
- Ketogeenisissa ruokavalioissa hiilihydraattien ja proteiinien saantia on rajoitettu.
Energia saadaan pääasiassa rasvoista, jolloin aivot käyttävät energianlähteenä glukoosin
sijasta pääasiassa ketoaineita «Wheless JW. The ketogenic diet: Fa(c)t or fiction....»175.
- Ruokavaliohoidon vaikutusmekanismia ei tunneta tarkkaan «Schwartzkroin PA. Mechanisms underlying the anti-e...»176, «Martin-McGill KJ, Jackson CF, Bresnahan R ym. Keto...»177.
- Ruokavalio toteutetaan epilepsiaan perehtyneen lääkärin ja ravitsemusterapeutin ohjauksessa.
- Ketogeenisista ruokavalioista saattaa olla hyötyä erityyppisten epilepsioiden hoidossa
«Ketogeeninen dieetti saattaa vähentää kohtauksia lasten epilepsian hoidossa.»C, «Martin-McGill KJ, Jackson CF, Bresnahan R ym. Keto...»177.
- Ketogeenista ruokavaliota voidaan käyttää vaikean epilepsian hoidossa, jos epilepsialääkkeillä ei saada riittävää vastetta, kirurgisen hoidon mahdollisuudet on arvioitu eikä vasta-aiheita ruokavaliohoidolle ole. Tietyissä oireyhtymissä ruokavaliohoitoa kannattaa harkita heti (glukoosin kuljettajaproteiini tyyppi 1:n puutos eli Glut1DS-oireyhtymä) tai varhaisessa vaiheessa (esim. myokloonis-atoninen epilepsia ja Dravet'n oireyhtymä).
- Ruokavaliohoidon tehoa arvioidaan noin 3 kuukauden jaksoissa. Jos se osoittautuu hyödylliseksi ja turvalliseksi, hoitoa voidaan jatkaa vuosia. Käytännön ohje ruokavalion toteutuksesta on suosituksen lisämateriaalissa «Ketogeenisen ruokavalion toteutus lapsen epilepsian hoidossa»2.
Kuumekouristukset (kuumekohtaukset)
- Kuumekouristukset (kuumekohtaukset) ovat kuumeen yhteydessä yleensä ½–6 vuoden iässä esiintyviä kohtauksia, joiden oireina ovat tajuttomuus ja lihasten jäykistyminen, nykiminen tai velttous «Capovilla G, Mastrangelo M, Romeo A ym. Recommenda...»178, «Steering Committee on Quality Improvement and Mana...»179.
- Kuumekouristuksia saa 7 vuoden ikään mennessä 2–5 % lapsista «Capovilla G, Mastrangelo M, Romeo A ym. Recommenda...»178, «Sillanpää M, Camfield P, Camfield C ym. Incidence ...»180. Perheenjäsenillä esiintyneisiin kuumekouristuksiin liittyy suurentunut kuumekouristuksen riski «Graves RC, Oehler K, Tingle LE. Febrile seizures: ...»181. Geneettinen tausta on kuitenkin tuntematon «Seinfeld SA, Pellock JM, Kjeldsen MJ ym. Epilepsy ...»182.
- Yksinkertaisella kuumekouristuksella tarkoitetaan neurologisesti terveellä lapsella
kuumeen yhteydessä ilman paikallisalkuisen kohtauksen piirteitä esiintyvää aivoperäistä kohtausta, jonka kesto on alle
15 minuuttia ja joka ei toistu 24 tunnin sisällä. Kuumekouristus on monimuotoinen,
jos se kestää 15 minuuttia tai kauemmin, siihen sisältyy paikallisen kohtauksen piirteitä
tai se uusiutuu 24 tunnin kuluessa.
- Yksinkertaisia kuumekouristuksia saaneilla lapsilla epilepsian ilmaantuvuus ei ole normaaliväestöä suurempi «Nelson KB, Ellenberg JH. Prognosis in children wit...»183, «Verity CM, Golding J. Risk of epilepsy after febri...»184.
- Monimuotoisen kuumekouristuksen saaneella lapsuusiän epilepsiariski on 4–6 % «Nelson KB, Ellenberg JH. Prognosis in children wit...»183, «Verity CM, Golding J. Risk of epilepsy after febri...»184.
- Väestöpohjaisissa tutkimuksissa on todettu, että kuumekouristuksia saaneet lapset
menestyvät ikätovereidensa kaltaisesti «Nelson KB, Ellenberg JH. Prognosis in children wit...»183, «Verity CM, Greenwood R, Golding J. Long-term intel...»185.
- Lapset, joilla on esiintynyt monimuotoisia kuumekouristuksia, eivät ole psykologisissa testeissä mitatun älyllisen kehityksensä, käyttäytymisensä tai koulumenestyksensä osalta keskimäärin eronneet 10-vuotiaina ikätovereistaan «Verity CM, Greenwood R, Golding J. Long-term intel...»185.
- Havaintotutkimuksista on saatu viitteitä, että raudan puute liittyy kuumekouristusten lisääntyneeseen esiintyvyyteen «Kwak BO, Kim K, Kim SN ym. Relationship between ir...»186 ja että seerumin sinkin ja seleenin pitoisuus on kuumekouristuksen saaneilla lapsilla pienempi kuin lapsilla, joilla ei esiinny kuumekouristuksia «Saghazadeh A, Mahmoudi M, Meysamie A ym. Possible ...»187. Syy-yhteys ilmiöiden ja kuumekouristusten välillä on epäselvä ja tulosten soveltaminen suomalaisiin lapsiin epävarmaa.
- Kuumekouristuksen diagnostiikassa ei tarvita rutiininomaista EEG tutkimusta. Kunnollista tutkimusnäyttöä EEG-tutkimuksen vaikuttavuudesta ei ole «Shah PB, James S, Elayaraja S. EEG for children wi...»188.
- Kuumekouristukset eivät ole este normaalin rokotusohjelman toteuttamiselle, vaikka MMR-rokotteeseen saattaa liittyä suurentunut kuumekouristuksen riski lähiviikkojen aikana «Demicheli V, Rivetti A, Debalini MG ym. Vaccines f...»189. Rokotusten hyödyt ylittävät haitat.
- Kuumekouristusten ensiapuhoito toteutetaan samoilla periaatteilla kuin epileptisen kohtauksen. Ks. Käypä hoito -suositus Epileptinen kohtaus (pitkittynyt) «Pitkittynyt epileptinen kohtaus ja status epilepticus»6, «Epileptinen kohtaus (pitkittynyt; status epileptic...»2.
- Akuuttitilanteessa suljetaan pois vakavat infektiot ja potilas lähetetään tarvittaessa
sairaalatutkimuksiin.
- Jos alle 1-vuotiaalla on pitkittynyt kuumekouristus, bakteerimeningiitin riski on merkittävä ja lapsi on syytä välittömästi lähettää sairaalatutkimuksiin «Chin RF, Neville BG, Scott RC. Meningitis is a com...»190, «Leung AK, Hon KL, Leung TN. Febrile seizures: an o...»191.
- 6–18 kuukauden ikäisellä lapsella, jolla on ollut lyhyt kuumekouristus ja jonka kliinisen tutkimuksen tulos on kuumetta lukuun ottamatta normaali, bakteerimeningiitin riski näyttää kuitenkin olevan hyvin pieni «Hom J, Medwid K. The low rate of bacterial meningi...»192.
- Jos isommalla lapsella ei ole kliinistä epäilyä bakteerin aiheuttamasta meningiitistä, sen todennäköisyys on hyvin pieni «Guedj R, Chappuy H, Titomanlio L ym. Do All Childr...»193.
- Jatkohoito toteutetaan neuvomalla vanhemmille ensiavun antaminen. Harkinnan mukaan
neuvotaan joko midatsolaamin bukkaalinen tai diatsepaamin rektaalinen käyttö (ks.
Käypä hoito -suositus Epileptinen kohtaus (pitkittynyt) «Pitkittynyt epileptinen kohtaus ja status epilepticus»6, «Epileptinen kohtaus (pitkittynyt; status epileptic...»2). Tämä koskee erityisesti potilaita, joiden kuumekohtaus on ollut pitkittynyt tai
joilla pitkähköön kuumekouristukseen liittyy esimerkiksi matkasta johtuva viive ensiapua
antavaan yksikköön. Midatsolaamia tai diatsepaamia ohjataan tällöin käyttämään tilanteissa,
joissa kuumekouristus pitkittyy yli 5 minuutin pituiseksi. Ensiapulääkettä ei määrätä
rutiininomaisesti kotiin kaikille kuumekouristuspotilaille.
- Pitkittyneen kouristuskohtauksen lääkehoidon vaihtoehdot ovat
- bukkaalinen midatsolaami 0,20–0,25 mg/kg tai iän mukaisesti annosteltuna (ks. Duodecim lääketietokanta «https://www.terveysportti.fi/apps/laake/»2 (vaatii käyttöoikeuden))
- rektaalinen diatsepaami 0,5(–0,75) mg/kg.
- Bukkaalinen midatsolaami on tehokas pitkittyneiden epileptisten kohtausten ensihoidossa «Bukkaalinen midatsolaami on teholtaan ja turvallisuudeltaan suonensisäisen diatsepaamin veroinen ja rektaalista diatsepaamia tehokkaampi lasten ja nuorten pitkittyneiden epileptisten kohtausten ensihoidossa.»A. Ks. lisätietoja Käypä hoito -suosituksesta Epileptinen kohtaus (pitkittynyt) «Pitkittynyt epileptinen kohtaus ja status epilepticus»6, «Epileptinen kohtaus (pitkittynyt; status epileptic...»2.
- Kuume hoidetaan kuten muillakin lapsilla.
- Parasetamolista, ibuprofeenista tai diklofenaakista «Kuumeen aikana annettava parasetamoli, ibuprofeeni tai diklofenaakki eivät estä lasten kuumekouristuksia.»A ei kuitenkaan ole apua kuumekouristusten estossa. Ks. Vältä viisaasti -suositus «Kuumetta alentava lääkitys kuumekouristuksen estossa»3.
- Pitkittyneen kouristuskohtauksen lääkehoidon vaihtoehdot ovat
- Kuumekouristusten estolääkitystä ei tule käyttää.
- Jaksottainen diatsepaamilääkitys pienentää kuumekouristuksen toistumisen riskiä vuoden aikana noin 30 % «Offringa M, Newton R, Cozijnsen MA ym. Prophylacti...»194. Jotta yhden lapsen kohdalla voitaisiin välttää kuumekouristuksen uusiminen, noin 13 lasta tulisi hoitaa jaksottaisella diatsepaamilla.
- Jatkuva fenobarbitaali lääkitys pienentää kuumekouristuksen toistumisen riskiä vuoden aikana noin 40 %, mutta intermittoiva lääkitys ei pienennä riskiä «Offringa M, Newton R, Cozijnsen MA ym. Prophylacti...»194. Haittavaikutustensa vuoksi «Jatkuva fenobarbitaalilääkitys näyttäisi heikentävän lasten älyllistä kehittymistä.»C jatkuvaa fenobarbitaali lääkitystä ei tule käyttää kuumekouristuksen estoon.
- Jatkuva valproaattilääkitys ei estä kuumekouristuksen toistumista «Offringa M, Newton R, Cozijnsen MA ym. Prophylacti...»194.
- Kuumekouristusten estoon käytetyllä jaksoittaisella diatsepaamilääkityksellä «Knudsen FU, Paerregaard A, Andersen R ym. Long ter...»195 tai jatkuvalla profylaktisella epilepsialääkityksellä «Farwell JR, Lee YJ, Hirtz DG ym. Phenobarbital for...»196 ei ole osoitettu voitavan estää epilepsian kehittymistä.
- Jatkotutkimuksia ei tarvita, jos 1/2–6 vuoden ikäisellä lapsella esiintyy ainoastaan kuumeen aikana tajuttomuus-kouristuskohtauksia, joista lapsi toipuu normaalisti.
Suomalaisen Lääkäriseuran Duodecimin ja Suomen Lastenneurologinen Yhdistys ry:n asettama työryhmä
Epilepsiat ja kuumekouristukset (lapset) -suosituksen historiatiedot «Epilepsiat ja kuumekouristukset (lapset ja nuoret), Käypä hoito -suosituksen historiatiedot»4
Puheenjohtaja:
Liisa Metsähonkala, LT, dos., lastenneurologian erikoislääkäri
Jäsenet:
Eija Gaily, lastenneurologian dosentti, osastonylilääkäri; HUS Lasten ja nuorten sairaala
Olga Gilbert, LL, terveyskeskuslääkäri; Vantaan kaupunki
Jarkko Kirjavainen, LT, lastenneurologian erikoislääkäri; KYS
Jorma Komulainen, LT, dos., lastentautien ja lastenendokrinologian erikoislääkäri, Käypä hoito -päätoimittaja; Suomalainen Lääkäriseura Duodecim
Tuire Lähdesmäki, LT, lastentautien ja lastenneurologian erikoislääkäri; TYKS
Päivi Vieira, LT, lastenneurologian erikoislääkäri; OYS lasten ja nuorten klinikka
Sidonnaisuudet
Sidonnaisuusilmoitukset on kerätty 27.2.2020 julkaistun suosituksen laatimisen yhteydessä.
Eija Gaily: Sivutoimet: Konsultoiva lastenneurologi, Etelä-Pohjanmaan sairaanhoitopiiri. Luento-, koulutus- ja asiantuntijapalkkiot: Biocodex, UCB Pharma, Eisai. Tutkimusrahoitus: Sage Therapeutics.
Olga Gilbert: Ei sidonnaisuuksia.
Jarkko Kirjavainen: Korvaukset koulutus- ja kongressikuluista: Biogen - SMA:n ja nusinerseeni lääkehoidon kongresseja ja asiantuntija tapaamisia. Luento-, koulutus- ja asiantuntijapalkkiot: UCB, EISAI advisory board. Luottamustoimet: SLNY:n puheenjohtaja. Muut sidonnaisuudet: UCB kliininen lääketutkimus.
Jorma Komulainen: Sivutoimet: Konsultoiva lastenendokrinologi, Eksote. Luento-, koulutus- ja asiantuntijapalkkiot: Kustannus Oy Duodecim. Luottamustoimet: Guidelines International Network Nordic: Steering group jäsen 2/2019 saakka; Väestöliitto: Hallituksen jäsen; ITLA: Hallituksen varajäsen. Ohjaushankkeet: STM: Palveluvalikoimaneuvosto (pysyvä asiantuntija), palvelutuotannon kehittämisryhmä (pysyvä asiantuntija), hoitoon pääsyn ja yhtenäisten hoidon kriteereiden työryhmä (jäsen); Kela: Sosiaalilääketieteellinen neuvottelukunta (jäsen vuoden 2018 loppuun saakka); THL: TOIMIA-ohjausryhmä (jäsen syksyyn 2019 saakka). Muut sidonnaisuudet: Kustannus Oy Duodecim: EBMeDS toimituksen jäsen.
Tuire Lähdesmäki: Sivutoimet: Lastenneurologian kliininen opettaja, Turun yliopisto. Korvaukset koulutus- ja kongressikuluista: Biogen, Duodecim/Tampereen lääkäripäivä. Luento-, koulutus- ja asiantuntijapalkkiot: Sarepta Pharmaceuticals (advisory board), Biogen, PTC-Therapeutics. Luottamustoimet: Suomen lastenneurologinen yhdistys (SLNY) hallitus, varapj; Suomen lääkäriliitto, Lastenneurologit alajaos, pj. Ohjaushankkeet: THL Palveluvalikoimaneuvosto: asiantuntijana lihastautien alalla. Muut sidonnaisuudet: Turun Lastenlääkäripalvelut Oy, lastenneurologi (konsultointi, yksityislääkäritoiminta); UCB Pharma, kliininen lääketutkimus .
Liisa Metsähonkala: Sivutoimet: Epilepsialiitto hallituksen pj. Tutkimusrahoitus: UCB, alkamassa. Korvaukset koulutus- ja kongressikuluista: Omamedical. Luento-, koulutus- ja asiantuntijapalkkiot: UCB,Novartis, Eisai, Omamedical. Luottamustoimet: Epilepsialiitto, hallituksen pj.
Päivi Vieira: Korvaukset koulutus- ja kongressikuluista: Biogen, Eisai, Novartis, Sanofi Genzyme. Luento-, koulutus- ja asiantuntijapalkkiot: PTC Therapeutics, UCB Pharma. Muut sidonnaisuudet: Orion.
Kirjallisuusviite
Epilepsiat ja kuumekouristukset (lapset). Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Lastenneurologinen Yhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2020 (viitattu pp.kk.vvvv). Saatavilla internetissä: www.kaypahoito.fi
Tarkemmat viittausohjeet: «http://www.kaypahoito.fi/web/kh/viittaaminen»3
Vastuun rajaus
Käypä hoito -suositukset ja Vältä viisaasti -suositukset ovat asiantuntijoiden laatimia yhteenvetoja yksittäisten sairauksien diagnostiikan ja hoidon vaikuttavuudesta. Suositukset toimivat lääkärin tai muun terveydenhuollon ammattilaisen päätöksenteon tukena hoitopäätöksiä tehtäessä. Ne eivät korvaa lääkärin tai muun terveydenhuollon ammattilaisen omaa arviota yksittäisen potilaan parhaasta mahdollisesta diagnostiikasta, hoidosta ja kuntoutuksesta hoitopäätöksiä tehtäessä.
Tiedonhakukäytäntö
Systemaattinen kirjallisuushaku on hoitosuosituksen perusta. Lue lisää artikkelista khk00007
Kirjallisuutta
- Gaily E. Kuinka hoidan kehitysvammaisen epilepsiaa? Duodecim 2006;122:1917-21 «http://www.duodecimlehti.fi/web/guest/etusivu/artikkeli?tunnus=duo9507»4
- Epileptinen kohtaus (pitkittynyt; status epilepticus). Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin, Suomen Lastenneurologinen Yhdistys ry:n ja Suomen Neurologinen Yhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2016 (viitattu 31.1.2020). Saatavilla internetissä: www.kaypahoito.fi
- Engel J Jr, International League Against Epilepsy (ILAE). A proposed diagnostic scheme for people with epileptic seizures and with epilepsy: report of the ILAE Task Force on Classification and Terminology. Epilepsia 2001;42:796-803 «PMID: 11422340»PubMed
- Fisher RS, van Emde Boas W, Blume W ym. Epileptic seizures and epilepsy: definitions proposed by the International League Against Epilepsy (ILAE) and the International Bureau for Epilepsy (IBE). Epilepsia 2005;46:470-2 «PMID: 15816939»PubMed
- Berg AT, Berkovic SF, Brodie MJ ym. Revised terminology and concepts for organization of seizures and epilepsies: report of the ILAE Commission on Classification and Terminology, 2005-2009. Epilepsia 2010;51:676-85 «PMID: 20196795»PubMed
- International League Against Epilepsy, http://www.ilae.org/ «http://www.ilae.org/»5
- Scheffer IE, Berkovic S, Capovilla G ym. ILAE classification of the epilepsies: Position paper of the ILAE Commission for Classification and Terminology. Epilepsia 2017;58:512-521 «PMID: 28276062»PubMed
- STM nimeämä vaikean epilepsian diagnostiikan ja hoidon yhteensovittamistyöryhmä, 2018
- Fisher RS, Acevedo C, Arzimanoglou A ym. ILAE official report: a practical clinical definition of epilepsy. Epilepsia 2014;55:475-82 «PMID: 24730690»PubMed
- Aaberg KM, Surén P, Søraas CL ym. Seizures, syndromes, and etiologies in childhood epilepsy: The International League Against Epilepsy 1981, 1989, and 2017 classifications used in a population-based cohort. Epilepsia 2017;58:1880-1891 «PMID: 28949013»PubMed
- Sokka A, Olsen P, Kirjavainen J ym. Etiology, syndrome diagnosis, and cognition in childhood-onset epilepsy: A population-based study. Epilepsia Open 2017;2:76-83 «PMID: 29750215»PubMed
- Gaily E, Lommi M, Lapatto R ym. Incidence and outcome of epilepsy syndromes with onset in the first year of life: A retrospective population-based study. Epilepsia 2016;57:1594-1601 «PMID: 27574005»PubMed
- Camfield P, Camfield C. Incidence, prevalence and aetiology of seizures and epilepsy in children. Epileptic Disord 2015;17:117-23 «PMID: 25895502»PubMed
- Saarinen MM, Sillanpää M, Schmidt D ym. Long-term changes in the incidence of childhood epilepsy. A population study from Finland. Epilepsy Behav 2016;58:81-5 «PMID: 27064826»PubMed
- Eriksson KJ, Koivikko MJ. Prevalence, classification, and severity of epilepsy and epileptic syndromes in children. Epilepsia 1997;38:1275-82 «PMID: 9578522»PubMed
- Sillanpää M, Jalava M, Kaleva O ym. Long-term prognosis of seizures with onset in childhood. N Engl J Med 1998;338:1715-22 «PMID: 9624191»PubMed
- Callenbach PM, Westendorp RG, Geerts AT ym. Mortality risk in children with epilepsy: the Dutch study of epilepsy in childhood. Pediatrics 2001;107:1259-63 «PMID: 11389240»PubMed
- Camfield CS, Camfield PR, Veugelers PJ. Death in children with epilepsy: a population-based study. Lancet 2002;359:1891-5 «PMID: 12057550»PubMed
- Berg AT, Shinnar S, Testa FM ym. Mortality in childhood-onset epilepsy. Arch Pediatr Adolesc Med 2004;158:1147-52 «PMID: 15583099»PubMed
- Harden C, Tomson T, Gloss D ym. Practice guideline summary: Sudden unexpected death in epilepsy incidence rates and risk factors: Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology and the American Epilepsy Society. Neurology 2017;88:1674-1680 «PMID: 28438841»PubMed
- Saxena A, Jones L, Shankar R ym. Sudden unexpected death in epilepsy in children: a focused review of incidence and risk factors. J Neurol Neurosurg Psychiatry 2018;89:1064-1070 «PMID: 29632029»PubMed
- Verducci C, Hussain F, Donner E ym. SUDEP in the North American SUDEP Registry: The full spectrum of epilepsies. Neurology 2019;93:e227-e236 «PMID: 31217259»PubMed
- Sillanpää M, Shinnar S. SUDEP and other causes of mortality in childhood-onset epilepsy. Epilepsy Behav 2013;28:249-55 «PMID: 23746924»PubMed
- Eriksson K, Peltola J, Kälviäinen R. Kohtausten hoidosta epilepsian hoitoon - tunnista epilepsiaoireyhtymä. Duodecim 2005;121:505-12 «http://www.duodecimlehti.fi/duo94845»6
- Eeg-Olofsson O, Petersén I, Selldén U. The development of the electroencephalogram in normal children from the age of 1 through 15 years. Paroxysmal activity. Neuropadiatrie 1971;2:375-404 «PMID: 5171489»PubMed
- Berg AT, Testa FM, Levy SR ym. Neuroimaging in children with newly diagnosed epilepsy: A community-based study. Pediatrics 2000;106:527-32 «PMID: 10969098»PubMed
- Shevell MI, Rosenblatt B, Watters GV ym. "Pseudo-BECRS": intracranial focal lesions suggestive of a primary partial epilepsy syndrome. Pediatr Neurol 1996;14:31-5 «PMID: 8652012»PubMed
- Gelisse P, Corda D, Raybaud C ym. Abnormal neuroimaging in patients with benign epilepsy with centrotemporal spikes. Epilepsia 2003;44:372-8 «PMID: 12614393»PubMed
- Gaillard WD, Chiron C, Cross JH ym. Guidelines for imaging infants and children with recent-onset epilepsy. Epilepsia 2009;50:2147-53 «PMID: 19389145»PubMed
- Ladino LD, Balaguera P, Rascovsky S ym. Clinical Benefit of 3 Tesla Magnetic Resonance Imaging Rescanning in Patients With Focal Epilepsy and Negative 1.5 Tesla Magnetic Resonance Imaging. Rev Invest Clin 2016;68:112-8 «PMID: 27408997»PubMed
- Berg AT, Coryell J, Saneto RP ym. Early-Life Epilepsies and the Emerging Role of Genetic Testing. JAMA Pediatr 2017;171:863-871 «PMID: 28759667»PubMed
- Shinnar S, Berg AT, Moshe SL ym. The risk of seizure recurrence after a first unprovoked afebrile seizure in childhood: an extended follow-up. Pediatrics 1996;98:216-25 «PMID: 8692621»PubMed
- Arthur TM, deGrauw TJ, Johnson CS ym. Seizure recurrence risk following a first seizure in neurologically normal children. Epilepsia 2008;49:1950-4 «PMID: 19154398»PubMed
- Hirtz D, Berg A, Bettis D ym. Practice parameter: treatment of the child with a first unprovoked seizure: Report of the Quality Standards Subcommittee of the American Academy of Neurology and the Practice Committee of the Child Neurology Society. Neurology 2003;60:166-75 «PMID: 12552027»PubMed
- Sansevere AJ, Avalone J, Strauss LD ym. Diagnostic and Therapeutic Management of a First Unprovoked Seizure in Children and Adolescents With a Focus on the Revised Diagnostic Criteria for Epilepsy. J Child Neurol 2017;32:774-788 «PMID: 28503985»PubMed
- Ajoterveyden arviointiohjeet lääkäreille. Liikenteen turvallisuusvirasto 1.7.2018. https://asiointi.trafi.fi/omatrafi-formservlet-web/lomake/ohje1 «https://asiointi.trafi.fi/omatrafi-formservlet-web/lomake/ohje1»7
- Epilepsiat (aikuiset). Käypä hoito -suositus. Suomalaisen Lääkäriseuran Duodecimin ja Suomen Neurologinen Yhdistys ry:n asettama työryhmä. Helsinki: Suomalainen Lääkäriseura Duodecim, 2014 (viitattu 31.1.2020). Saatavilla internetissä: www.kaypahoito.fi
- Healy L, Moran M, Singhal S ym. Relapse after treatment withdrawal of antiepileptic drugs for Juvenile Absence Epilepsy and Juvenile Myoclonic Epilepsy. Seizure 2018;59:116-122 «PMID: 29807291»PubMed
- Höfler J, Unterberger I, Dobesberger J ym. Seizure outcome in 175 patients with juvenile myoclonic epilepsy--a long-term observational study. Epilepsy Res 2014;108:1817-24 «PMID: 25443450»PubMed
- Braathen G, Andersson T, Gylje H ym. Comparison between one and three years of treatment in uncomplicated childhood epilepsy: a prospective study. I. Outcome in different seizure types. Epilepsia 1996;37:822-32 «PMID: 8814094»PubMed
- Lamberink HJ, Otte WM, Geerts AT ym. Individualised prediction model of seizure recurrence and long-term outcomes after withdrawal of antiepileptic drugs in seizure-free patients: a systematic review and individual participant data meta-analysis. Lancet Neurol 2017;16:523-531 «PMID: 28483337»PubMed
- Berg AT, Rychlik K, Levy SR ym. Complete remission of childhood-onset epilepsy: stability and prediction over two decades. Brain 2014;137:3213-22 «PMID: 25338950»PubMed
- Sillanpää M, Saarinen M, Schmidt D. Clinical conditions of long-term cure in childhood-onset epilepsy: a 45-year follow-up study. Epilepsy Behav 2014;37:49-53 «PMID: 24975821»PubMed
- Sillanpää M, Schmidt D. Long-term outcome of medically treated epilepsy. Seizure 2017;44:211-216 «PMID: 27646715»PubMed
- Camfield PR, Camfield CS. Intractable seizures after a lengthy remission in childhood-onset epilepsy. Epilepsia 2017;58:2048-2052 «PMID: 28983902»PubMed
- Tomson T, Marson A, Boon P ym. Valproate in the treatment of epilepsy in girls and women of childbearing potential. Epilepsia 2015;56:1006-19 «PMID: 25851171»PubMed
- Gaily E, Liukkonen E, Paetau R ym. Infantile spasms: diagnosis and assessment of treatment response by video-EEG. Dev Med Child Neurol 2001;43:658-67 «PMID: 11665822»PubMed
- Granström ML, Gaily E, Liukkonen E. Treatment of infantile spasms: results of a population-based study with vigabatrin as the first drug for spasms. Epilepsia 1999;40:950-7 «PMID: 10403219»PubMed
- O'Callaghan FJ, Lux AL, Darke K ym. The effect of lead time to treatment and of age of onset on developmental outcome at 4 years in infantile spasms: evidence from the United Kingdom Infantile Spasms Study. Epilepsia 2011;52:1359-64 «PMID: 21668442»PubMed
- O'Callaghan FJ, Edwards SW, Alber FD ym. Safety and effectiveness of hormonal treatment versus hormonal treatment with vigabatrin for infantile spasms (ICISS): a randomised, multicentre, open-label trial. Lancet Neurol 2017;16:33-42 «PMID: 27838190»PubMed
- O'Callaghan FJK, Edwards SW, Alber FD ym. Vigabatrin with hormonal treatment versus hormonal treatment alone (ICISS) for infantile spasms: 18-month outcomes of an open-label, randomised controlled trial. Lancet Child Adolesc Health 2018;2:715-725 «PMID: 30236380»PubMed
- Lux AL, Edwards SW, Hancock E ym. The United Kingdom Infantile Spasms Study comparing vigabatrin with prednisolone or tetracosactide at 14 days: a multicentre, randomised controlled trial. Lancet 2004;364:1773-8 «PMID: 15541450»PubMed
- Chellamuthu P, Sharma S, Jain P ym. High dose (4 mg/kg/day) versus usual dose (2 mg/kg/day) oral prednisolone for treatment of infantile spasms: an open-label, randomized controlled trial. Epilepsy Res 2014;108:1378-84 «PMID: 25048310»PubMed
- Vanhatalo S, Nousiainen I, Eriksson K ym. Visual field constriction in 91 Finnish children treated with vigabatrin. Epilepsia 2002;43:748-56 «PMID: 12102679»PubMed
- Leivonen, Peltola, Gaily. Tunnistatko infantiilispasmit? Nopea hoidon aloitus voi parantaa ennustetta. Suom Lääkäril 2016;19:1377-8
- Wanigasinghe J, Arambepola C, Sri Ranganathan S ym. Randomized, Single-Blind, Parallel Clinical Trial on Efficacy of Oral Prednisolone Versus Intramuscular Corticotropin on Immediate and Continued Spasm Control in West Syndrome. Pediatr Neurol 2015;53:193-9 «PMID: 26216500»PubMed
- Lux AL, Edwards SW, Hancock E ym. The United Kingdom Infantile Spasms Study (UKISS) comparing hormone treatment with vigabatrin on developmental and epilepsy outcomes to age 14 months: a multicentre randomised trial. Lancet Neurol 2005;4:712-7 «PMID: 16239177»PubMed
- Prezioso G, Carlone G, Zaccara G ym. Efficacy of ketogenic diet for infantile spasms: A systematic review. Acta Neurol Scand 2018;137:4-11 «PMID: 28875525»PubMed
- Riikonen R, Donner M. ACTH therapy in infantile spasms: side effects. Arch Dis Child 1980;55:664-72 «PMID: 6254450»PubMed
- Hrachovy RA, Frost JD Jr, Glaze DG. High-dose, long-duration versus low-dose, short-duration corticotropin therapy for infantile spasms. J Pediatr 1994;124:803-6 «PMID: 8176573»PubMed
- Perheentupa J, Riikonen R, Dunkel L ym. Adrenocortical hyporesponsiveness after treatment with ACTH of infantile spasms. Arch Dis Child 1986;61:750-3 «PMID: 3017239»PubMed
- Heiskala H, Riikonen R, Santavuori P ym. West syndrome: individualized ACTH therapy. Brain Dev 1996;18:456-60 «PMID: 8980843»PubMed
- Riikonen R, Rener-Primec Z, Carmant L ym. Does vigabatrin treatment for infantile spasms cause visual field defects? An international multicentre study. Dev Med Child Neurol 2015;57:60-7 «PMID: 25145415»PubMed
- Gaily E, Jonsson H, Lappi M. Visual fields at school-age in children treated with vigabatrin in infancy. Epilepsia 2009;50:206-16 «PMID: 19215279»PubMed
- Schwarz MD, Li M, Tsao J ym. A lack of clinically apparent vision loss among patients treated with vigabatrin with infantile spasms: The UCLA experience. Epilepsy Behav 2016;57:29-33 «PMID: 26921595»PubMed
- Schubert J, Paravidino R, Becker F ym. PRRT2 mutations are the major cause of benign familial infantile seizures. Hum Mutat 2012;33:1439-43 «PMID: 22623405»PubMed
- Gaily E, Roivainen R. Dravet´n oireyhtymä - vaikea neurologinen harvinaissairaus. Suom Lääkäril 2018;73:1488-93
- Chiron C, Dulac O. The pharmacologic treatment of Dravet syndrome. Epilepsia 2011;52 Suppl 2:72-5 «PMID: 21463285»PubMed
- Dressler A, Trimmel-Schwahofer P, Reithofer E ym. Efficacy and tolerability of the ketogenic diet in Dravet syndrome - Comparison with various standard antiepileptic drug regimen. Epilepsy Res 2015;109:81-9 «PMID: 25524846»PubMed
- Lotte J, Haberlandt E, Neubauer B ym. Bromide in patients with SCN1A-mutations manifesting as Dravet syndrome. Neuropediatrics 2012;43:17-21 «PMID: 22430156»PubMed
- Ceulemans B, Boel M, Leyssens K ym. Successful use of fenfluramine as an add-on treatment for Dravet syndrome. Epilepsia 2012;53:1131-9 «PMID: 22554283»PubMed
- Schoonjans A, Paelinck BP, Marchau F ym. Low-dose fenfluramine significantly reduces seizure frequency in Dravet syndrome: a prospective study of a new cohort of patients. Eur J Neurol 2017;24:309-314 «PMID: 27790834»PubMed
- Ceulemans B, Schoonjans AS, Marchau F ym. Five-year extended follow-up status of 10 patients with Dravet syndrome treated with fenfluramine. Epilepsia 2016;57:e129-34 «PMID: 27197941»PubMed
- Chhun S, Troude P, Villeneuve N ym. A prospective open-labeled trial with levetiracetam in pediatric epilepsy syndromes: continuous spikes and waves during sleep is definitely a target. Seizure 2011;20:320-5 «PMID: 21256770»PubMed
- Mullen SA, Marini C, Suls A ym. Glucose transporter 1 deficiency as a treatable cause of myoclonic astatic epilepsy. Arch Neurol 2011;68:1152-5 «PMID: 21555602»PubMed
- Kilaru S, Bergqvist AGC. Current treatment of myoclonic astatic epilepsy: clinical experience at the Children's Hospital of Philadelphia. Epilepsia 2007;48:1703-1707 «PMID: 17651420»PubMed
- Oguni H, Tanaka T, Hayashi K ym. Treatment and long-term prognosis of myoclonic-astatic epilepsy of early childhood. Neuropediatrics 2002;33:122-32 «PMID: 12200741»PubMed
- von Stülpnagel C, Coppola G, Striano P ym. First long-term experience with the orphan drug rufinamide in children with myoclonic-astatic epilepsy (Doose syndrome). Eur J Paediatr Neurol 2012;16:459-63 «PMID: 22266062»PubMed
- Jeavons PM, Clark JE, Maheshwari MC. Treatment of generalized epilepsies of childhood and adolescence with sodium valproate ("epilim"). Dev Med Child Neurol 1977;19:9-25 «PMID: 403104»PubMed
- Eriksson AS, Nergårdh A, Hoppu K. The efficacy of lamotrigine in children and adolescents with refractory generalized epilepsy: a randomized, double-blind, crossover study. Epilepsia 1998;39:495-501 «PMID: 9596201»PubMed
- Guerrini R, Belmonte A, Parmeggiani L ym. Myoclonic status epilepticus following high-dosage lamotrigine therapy. Brain Dev 1999;21:420-4 «PMID: 10487478»PubMed
- Pennell PB, Ogaily MS, Macdonald RL. Aplastic anemia in a patient receiving felbamate for complex partial seizures. Neurology 1995;45:456-60 «PMID: 7898696»PubMed
- Hancock EC, Cross JH. Treatment of Lennox-Gastaut syndrome. Cochrane Database Syst Rev 2013;:CD003277 «PMID: 23450537»PubMed
- Lortie A, Chiron C, Mumford J ym. The potential for increasing seizure frequency, relapse, and appearance of new seizure types with vigabatrin. Neurology 1993;43:S24-7 «PMID: 8232984»PubMed
- Coppola G, Terraciano AM, Pascotto A. Vigabatrin as add-on therapy in children and adolescents with refractory epilepsy: an open trial. Brain Dev 1997;19:459-63 «PMID: 9408591»PubMed
- DiMario FJ Jr, Clancy RR. Paradoxical precipitation of tonic seizures by lorazepam in a child with atypical absence seizures. Pediatr Neurol 1988;4:249-51 «PMID: 3149484»PubMed
- Livingston JH, Brown JK. Non-convulsive status epilepticus resistant to benzodiazepines. Arch Dis Child 1987;62:41-4 «PMID: 3545098»PubMed
- Tassinari CA, Dravet C, Roger J ym. Tonic status epilepticus precipitated by intravenous benzodiazepine in five patients with Lennox-Gastaut syndrome. Epilepsia 1972;13:421-35 «PMID: 4626571»PubMed
- Wheless JW, Clarke DF, Carpenter D. Treatment of pediatric epilepsy: expert opinion, 2005. J Child Neurol 2005;20 Suppl 1:S1-56; quiz S59-60 «PMID: 16615562»PubMed
- Wheless JW, Clarke DF, Arzimanoglou A ym. Treatment of pediatric epilepsy: European expert opinion, 2007. Epileptic Disord 2007;9:353-412 «PMID: 18077226»PubMed
- Lemke JR, Lal D, Reinthaler EM ym. Mutations in GRIN2A cause idiopathic focal epilepsy with rolandic spikes. Nat Genet 2013;45:1067-72 «PMID: 23933819»PubMed
- Inutsuka M, Kobayashi K, Oka M ym. Treatment of epilepsy with electrical status epilepticus during slow sleep and its related disorders. Brain Dev 2006;28:281-6 «PMID: 16376508»PubMed
- Fejerman N, Caraballo R, Cersósimo R ym. Sulthiame add-on therapy in children with focal epilepsies associated with encephalopathy related to electrical status epilepticus during slow sleep (ESES). Epilepsia 2012;53:1156-61 «PMID: 22509732»PubMed
- Vrielynck P, Marique P, Ghariani S ym. Topiramate in childhood epileptic encephalopathy with continuous spike-waves during sleep: A retrospective study of 21 cases. Eur J Paediatr Neurol 2017;21:305-311 «PMID: 27641809»PubMed
- Fine AL, Wirrell EC, Wong-Kisiel LC ym. Acetazolamide for electrical status epilepticus in slow-wave sleep. Epilepsia 2015;56:e134-8 «PMID: 26230617»PubMed
- Grosso S, Parisi P, Giordano L ym. Lacosamide efficacy in epileptic syndromes with continuous spike and waves during slow sleep (CSWS). Epilepsy Res 2014;108:1604-8 «PMID: 25262499»PubMed
- Wilson RB, Eliyan Y, Sankar R ym. Amantadine: A new treatment for refractory electrical status epilepticus in sleep. Epilepsy Behav 2018;84:74-78 «PMID: 29754107»PubMed
- Nikanorova M, Miranda MJ, Atkins M ym. Ketogenic diet in the treatment of refractory continuous spikes and waves during slow sleep. Epilepsia 2009;50:1127-31 «PMID: 19220407»PubMed
- Pavlidis E, Rubboli G, Nikanorova M ym. Encephalopathy with status epilepticus during sleep (ESES) induced by oxcarbazepine in idiopathic focal epilepsy in childhood. Funct Neurol 2015;30:139-41 «PMID: 26415787»PubMed
- Yang X, Qian P, Xu X ym. GRIN2A mutations in epilepsy-aphasia spectrum disorders. Brain Dev 2018;40:205-210 «PMID: 29056244»PubMed
- Myers KA, Scheffer IE. GRIN2A-Related Speech Disorders and Epilepsy. 2016 Sep
- Kramer U, Nevo Y, Neufeld MY ym. Epidemiology of epilepsy in childhood: a cohort of 440 consecutive patients. Pediatr Neurol 1998;18:46-50 «PMID: 9492091»PubMed
- Goldberg-Stern H, Gonen OM, Sadeh M ym. Neuropsychological aspects of benign childhood epilepsy with centrotemporal spikes. Seizure 2010;19:12-6 «PMID: 19963405»PubMed
- Neri ML, Guimarães CA, Oliveira EP ym. Neuropsychological assessment of children with rolandic epilepsy: executive functions. Epilepsy Behav 2012;24:403-7 «PMID: 22683244»PubMed
- Wickens S, Bowden SC, D'Souza W. Cognitive functioning in children with self-limited epilepsy with centrotemporal spikes: A systematic review and meta-analysis. Epilepsia 2017;58:1673-1685 «PMID: 28801973»PubMed
- Camfield CS, Camfield PR. Rolandic epilepsy has little effect on adult life 30 years later: a population-based study. Neurology 2014;82:1162-6 «PMID: 24562059»PubMed
- Boillot M, Baulac S. Genetic models of focal epilepsies. J Neurosci Methods 2016;260:132-43 «PMID: 26072248»PubMed
- Loiseau P, Duché B, Cordova S ym. Prognosis of benign childhood epilepsy with centrotemporal spikes: a follow-up study of 168 patients. Epilepsia 1988;29:229-35 «PMID: 3371279»PubMed
- Tan HJ, Singh J, Gupta R ym. Comparison of antiepileptic drugs, no treatment, or placebo for children with benign epilepsy with centro temporal spikes. Cochrane Database Syst Rev 2014;:CD006779 «PMID: 25190506»PubMed
- Patsalos PN, Spencer EP, Berry DJ. Therapeutic Drug Monitoring of Antiepileptic Drugs in Epilepsy: A 2018 Update. Ther Drug Monit 2018;40:526-548 «PMID: 29957667»PubMed
- de Silva M, MacArdle B, McGowan M ym. Randomised comparative monotherapy trial of phenobarbitone, phenytoin, carbamazepine, or sodium valproate for newly diagnosed childhood epilepsy. Lancet 1996;347:709-13 «PMID: 8601999»PubMed
- Zamponi N, Cardinali C. Open comparative long-term study of vigabatrin vs carbamazepine in newly diagnosed partial seizures in children. Arch Neurol 1999;56:605-7 «PMID: 10328256»PubMed
- Farwell JR, Lee YJ, Hirtz DG ym. Phenobarbital for febrile seizures--effects on intelligence and on seizure recurrence. N Engl J Med 1990;322:364-9 «PMID: 2242106»PubMed
- Shinnar S, Cnaan A, Hu F ym. Long-term outcomes of generalized tonic-clonic seizures in a childhood absence epilepsy trial. Neurology 2015;85:1108-14 «PMID: 26311751»PubMed
- Masur D, Shinnar S, Cnaan A ym. Pretreatment cognitive deficits and treatment effects on attention in childhood absence epilepsy. Neurology 2013;81:1572-80 «PMID: 24089388»PubMed
- Glauser TA, Cnaan A, Shinnar S ym. Ethosuximide, valproic acid, and lamotrigine in childhood absence epilepsy. N Engl J Med 2010;362:790-9 «PMID: 20200383»PubMed
- Glauser TA, Cnaan A, Shinnar S ym. Ethosuximide, valproic acid, and lamotrigine in childhood absence epilepsy: initial monotherapy outcomes at 12 months. Epilepsia 2013;54:141-55 «PMID: 23167925»PubMed
- Cnaan A, Shinnar S, Arya R ym. Second monotherapy in childhood absence epilepsy. Neurology 2017;88:182-190 «PMID: 27986874»PubMed
- Morse E, Giblin K, Chung MH ym. Historical trend toward improved long-term outcome in childhood absence epilepsy. Epilepsy Res 2019;152:7-10 «PMID: 30856420»PubMed
- Besag FM, Wallace SJ, Dulac O ym. Lamotrigine for the treatment of epilepsy in childhood. J Pediatr 1995;127:991-7 «PMID: 8523205»PubMed
- Naito H, Wachi M, Nishida M. Clinical effects and plasma concentrations of long-term clonazepam monotherapy in previously untreated epileptics. Acta Neurol Scand 1987;76:58-63 «PMID: 3630646»PubMed
- Sreedharan M, Devadathan K, Pathan HK ym. Amantadine for the Treatment of Refractory Absence Seizures in Children. J Pediatr Neurosci 2018;13:131-136 «PMID: 30090124»PubMed
- Perry MS, Bailey LJ, Kotecha AC ym. Amantadine for the treatment of refractory absence seizures in children. Pediatr Neurol 2012;46:243-5 «PMID: 22490771»PubMed
- Fattore C, Boniver C, Capovilla G ym. A multicenter, randomized, placebo-controlled trial of levetiracetam in children and adolescents with newly diagnosed absence epilepsy. Epilepsia 2011;52:802-9 «PMID: 21320119»PubMed
- Biton V, Montouris GD, Ritter F ym. A randomized, placebo-controlled study of topiramate in primary generalized tonic-clonic seizures. Topiramate YTC Study Group. Neurology 1999;52:1330-7 «PMID: 10227614»PubMed
- Piña-Garza JE, Schwarzman L, Wiegand F ym. A pilot study of topiramate in childhood absence epilepsy. Acta Neurol Scand 2011;123:54-9 «PMID: 20219018»PubMed
- Glauser T, Ben-Menachem E, Bourgeois B ym. ILAE treatment guidelines: evidence-based analysis of antiepileptic drug efficacy and effectiveness as initial monotherapy for epileptic seizures and syndromes. Epilepsia 2006;47:1094-120 «PMID: 16886973»PubMed
- Nevitt SJ, Sudell M, Weston J ym. Antiepileptic drug monotherapy for epilepsy: a network meta-analysis of individual participant data. Cochrane Database Syst Rev 2017;6:CD011412 «PMID: 28661008»PubMed
- Marson AG, Al-Kharusi AM, Alwaidh M ym. The SANAD study of effectiveness of valproate, lamotrigine, or topiramate for generalised and unclassifiable epilepsy: an unblinded randomised controlled trial. Lancet 2007;369:1016-26 «PMID: 17382828»PubMed
- Vossler DG. Comparative Risk of Major Congenital Malformations With 8 Different Antiepileptic Drugs: A Prospective Cohort Study of the EURAP Registry. Epilepsy Curr 2019;19:83-85 «PMID: 30955418»PubMed
- Kothare SV, Kaleyias J, Mostofi N ym. Efficacy and safety of zonisamide monotherapy in a cohort of children with epilepsy. Pediatr Neurol 2006;34:351-4 «PMID: 16647993»PubMed
- French JA, Krauss GL, Wechsler RT ym. Perampanel for tonic-clonic seizures in idiopathic generalized epilepsy A randomized trial. Neurology 2015;85:950-7 «PMID: 26296511»PubMed
- Marinas A, Villanueva V, Giráldez BG ym. Efficacy and tolerability of zonisamide in idiopathic generalized epilepsy. Epileptic Disord 2009;11:61-6 «PMID: 19264587»PubMed
- Coulter DL, Wu H, Allen RJ. Valproic acid therapy in childhood epilepsy. JAMA 1980;244:785-8 «PMID: 6771426»PubMed
- Tomson T, Battino D, Bonizzoni E ym. Dose-dependent teratogenicity of valproate in mono- and polytherapy: an observational study. Neurology 2015;85:866-72 «PMID: 26085607»PubMed
- Granström ML, Gaily E, Herrgård E. Kannattaako lasten epilepsiakirurgia? Duodecim 2000;116:2011-3 «http://www.duodecimlehti.fi/web/guest/etusivu/artikkeli?tunnus=duo91764»8
- Cross JH. Epilepsy surgery in childhood. Epilepsia 2002;43 Suppl 3:65-70 «PMID: 12060008»PubMed
- Immonen A, Kälviäinen R, Gaily E, Blomstedt G. Kuka hyötyy epilepsiakirurgiasta? Duodecim 2008;124(20):2383-91 «http://www.duodecimlehti.fi/web/guest/etusivu/artikkeli?tunnus=duo97584»9
- Gaily E. Epilepsian kirurginen hoito voi muuttaa lapsen tulevaisuuden (pääkirjoitus). Suomen Lääkärilehti 2011;66:892
- Kwon HE, Eom S, Kang HC ym. Surgical treatment of pediatric focal cortical dysplasia: Clinical spectrum and surgical outcome. Neurology 2016;87:945-51 «PMID: 27466475»PubMed
- Peltola ME, Liukkonen E, Granström ML ym. The effect of surgery in encephalopathy with electrical status epilepticus during sleep. Epilepsia 2011;52:602-9 «PMID: 21087244»PubMed
- Jeong A, Strahle J, Vellimana AK ym. Hemispherotomy in children with electrical status epilepticus of sleep. J Neurosurg Pediatr 2017;19:56-62 «PMID: 27791702»PubMed
- Lee YJ, Kang HC, Lee JS ym. Resective pediatric epilepsy surgery in Lennox-Gastaut syndrome. Pediatrics 2010;125:e58-66 «PMID: 20008422»PubMed
- Ansari SF, Maher CO, Tubbs RS ym. Surgery for extratemporal nonlesional epilepsy in children: a meta-analysis. Childs Nerv Syst 2010;26:945-51 «PMID: 20013124»PubMed
- Wyllie E, Lachhwani DK, Gupta A ym. Successful surgery for epilepsy due to early brain lesions despite generalized EEG findings. Neurology 2007;69:389-97 «PMID: 17646632»PubMed
- Yasuhara A, Yoshida H, Hatanaka T ym. Epilepsy with continuous spike-waves during slow sleep and its treatment. Epilepsia 1991;32:59-62 «PMID: 1985831»PubMed
- Jansen FE, van Huffelen AC, Algra A ym. Epilepsy surgery in tuberous sclerosis: a systematic review. Epilepsia 2007;48:1477-84 «PMID: 17484753»PubMed
- Stevelink R, Sanders MW, Tuinman MP ym. Epilepsy surgery for patients with genetic refractory epilepsy: a systematic review. Epileptic Disord 2018;20:99-115 «PMID: 29620010»PubMed
- Téllez-Zenteno JF, Dhar R, Wiebe S. Long-term seizure outcomes following epilepsy surgery: a systematic review and meta-analysis. Brain 2005;128:1188-98 «PMID: 15758038»PubMed
- Flint AE, Waterman M, Bowmer G ym. Neuropsychological outcomes following paediatric temporal lobe surgery for epilepsies: Evidence from a systematic review. Seizure 2017;52:89-116 «PMID: 29032016»PubMed
- Ramantani G, Stathi A, Brandt A ym. Posterior cortex epilepsy surgery in childhood and adolescence: Predictors of long-term seizure outcome. Epilepsia 2017;58:412-419 «PMID: 28098941»PubMed
- Sierra-Marcos A, Fournier-Del Castillo MC, Álvarez-Linera J ym. Functional surgery in pediatric drug-resistant posterior cortex epilepsy: Electro-clinical findings, cognitive and seizure outcome. Seizure 2017;52:46-52 «PMID: 28963933»PubMed
- Liava A, Mai R, Tassi L ym. Paediatric epilepsy surgery in the posterior cortex: a study of 62 cases. Epileptic Disord 2014;16:141-64 «PMID: 24853765»PubMed
- Englot DJ, Breshears JD, Sun PP ym. Seizure outcomes after resective surgery for extra-temporal lobe epilepsy in pediatric patients. J Neurosurg Pediatr 2013;12:126-33 «PMID: 23768201»PubMed
- Ramantani G, Kadish NE, Mayer H ym. Frontal Lobe Epilepsy Surgery in Childhood and Adolescence: Predictors of Long-Term Seizure Freedom, Overall Cognitive and Adaptive Functioning. Neurosurgery 2018;83:93-103 «PMID: 29106684»PubMed
- Englot DJ, Han SJ, Rolston JD ym. Epilepsy surgery failure in children: a quantitative and qualitative analysis. J Neurosurg Pediatr 2014;14:386-95 «PMID: 25127098»PubMed
- Pulsifer MB, Brandt J, Salorio CF ym. The cognitive outcome of hemispherectomy in 71 children. Epilepsia 2004;45:243-54 «PMID: 15009226»PubMed
- Gaily E, Hellén H, Metsähonkala L ym. Aivopuoliskon hermoyhteyksien katkaisu lasten ja nuorten vaikean epilepsian hoidossa. Suom Lääkäril 2014;69:871-8
- Griessenauer CJ, Salam S, Hendrix P ym. Hemispherectomy for treatment of refractory epilepsy in the pediatric age group: a systematic review. J Neurosurg Pediatr 2015;15:34-44 «PMID: 25380174»PubMed
- Hu WH, Zhang C, Zhang K ym. Hemispheric surgery for refractory epilepsy: a systematic review and meta-analysis with emphasis on seizure predictors and outcomes. J Neurosurg 2016;124:952-61 «PMID: 26495944»PubMed
- Moosa AN, Jehi L, Marashly A ym. Long-term functional outcomes and their predictors after hemispherectomy in 115 children. Epilepsia 2013;54:1771-9 «PMID: 23980759»PubMed
- Althausen A, Gleissner U, Hoppe C ym. Long-term outcome of hemispheric surgery at different ages in 61 epilepsy patients. J Neurol Neurosurg Psychiatry 2013;84:529-36 «PMID: 23268362»PubMed
- Gaily E, Esko L, Blomstedt G ym. Aivokurkiaisen halkaisu lapsuus- ja nuoruusiän vaikean epilepsian hoidossa. Duodecim 1999;115:1995-2003
- Graham D, Tisdall MM, Gill D. Corpus callosotomy outcomes in pediatric patients: A systematic review. Epilepsia 2016;57:1053-68 «PMID: 27237542»PubMed
- Korkman M, Granström ML, Kantola-Sorsa E ym. Two-year follow-up of intelligence after pediatric epilepsy surgery. Pediatr Neurol 2005;33:173-8 «PMID: 16139731»PubMed
- Téllez-Zenteno JF, Dhar R, Hernandez-Ronquillo L ym. Long-term outcomes in epilepsy surgery: antiepileptic drugs, mortality, cognitive and psychosocial aspects. Brain 2007;130:334-45 «PMID: 17124190»PubMed
- Sibilia V, Barba C, Metitieri T ym. Cognitive outcome after epilepsy surgery in children: A controlled longitudinal study. Epilepsy Behav 2017;73:23-30 «PMID: 28605630»PubMed
- Otsuki T, Kim HD, Luan G ym. Surgical versus medical treatment for children with epileptic encephalopathy in infancy and early childhood: Results of an international multicenter cohort study in Far-East Asia (the FACE study). Brain Dev 2016;38:449-60 «PMID: 26686601»PubMed
- Law N, Kerr E, Smith ML. Evaluation of behavioral outcomes in children 1 year after epilepsy surgery. Epilepsia 2015;56:1605-14 «PMID: 26289039»PubMed
- Elliott IM, Lach L, Kadis DS ym. Psychosocial outcomes in children two years after epilepsy surgery: has anything changed? Epilepsia 2008;49:634-41 «PMID: 18177356»PubMed
- Puka K, Smith ML. Long-term outcomes of behavior problems after epilepsy surgery in childhood. J Neurol 2016;263:991-1000 «PMID: 27007483»PubMed
- Boshuisen K, van Schooneveld MM, Uiterwaal CS ym. Intelligence quotient improves after antiepileptic drug withdrawal following pediatric epilepsy surgery. Ann Neurol 2015;78:104-14 «PMID: 25899932»PubMed
- Viggedal G, Olsson I, Carlsson G ym. Intelligence two years after epilepsy surgery in children. Epilepsy Behav 2013;29:565-70 «PMID: 24201119»PubMed
- Kossoff EH, McGrogan JR, Bluml RM ym. A modified Atkins diet is effective for the treatment of intractable pediatric epilepsy. Epilepsia 2006;47:421-4 «PMID: 16499770»PubMed
- Wheless JW. The ketogenic diet: Fa(c)t or fiction. J Child Neurol 1995;10:419-23 «PMID: 8576550»PubMed
- Schwartzkroin PA. Mechanisms underlying the anti-epileptic efficacy of the ketogenic diet. Epilepsy Res 1999;37:171-80 «PMID: 10584967»PubMed
- Martin-McGill KJ, Jackson CF, Bresnahan R ym. Ketogenic diets for drug-resistant epilepsy. Cochrane Database Syst Rev 2018;11:CD001903 «PMID: 30403286»PubMed
- Capovilla G, Mastrangelo M, Romeo A ym. Recommendations for the management of "febrile seizures": Ad Hoc Task Force of LICE Guidelines Commission. Epilepsia 2009;50 Suppl 1:2-6 «PMID: 19125841»PubMed
- Steering Committee on Quality Improvement and Management, Subcommittee on Febrile Seizures American Academy of Pediatrics.. Febrile seizures: clinical practice guideline for the long-term management of the child with simple febrile seizures. Pediatrics 2008;121:1281-6 «PMID: 18519501»PubMed
- Sillanpää M, Camfield P, Camfield C ym. Incidence of febrile seizures in Finland: prospective population-based study. Pediatr Neurol 2008;38:391-4 «PMID: 18486819»PubMed
- Graves RC, Oehler K, Tingle LE. Febrile seizures: risks, evaluation, and prognosis. Am Fam Physician 2012;85:149-53 «PMID: 22335215»PubMed
- Seinfeld SA, Pellock JM, Kjeldsen MJ ym. Epilepsy After Febrile Seizures: Twins Suggest Genetic Influence. Pediatr Neurol 2016;55:14-6 «PMID: 26638777»PubMed
- Nelson KB, Ellenberg JH. Prognosis in children with febrile seizures. Pediatrics 1978;61:720-7 «PMID: 662510»PubMed
- Verity CM, Golding J. Risk of epilepsy after febrile convulsions: a national cohort study. BMJ 1991;303:1373-6 «PMID: 1760604»PubMed
- Verity CM, Greenwood R, Golding J. Long-term intellectual and behavioral outcomes of children with febrile convulsions. N Engl J Med 1998;338:1723-8 «PMID: 9624192»PubMed
- Kwak BO, Kim K, Kim SN ym. Relationship between iron deficiency anemia and febrile seizures in children: A systematic review and meta-analysis. Seizure 2017;52:27-34 «PMID: 28957722»PubMed
- Saghazadeh A, Mahmoudi M, Meysamie A ym. Possible role of trace elements in epilepsy and febrile seizures: a meta-analysis. Nutr Rev 2015;73:760-79 «PMID: 26433016»PubMed
- Shah PB, James S, Elayaraja S. EEG for children with complex febrile seizures. Cochrane Database Syst Rev 2017;10:CD009196 «PMID: 28986982»PubMed
- Demicheli V, Rivetti A, Debalini MG ym. Vaccines for measles, mumps and rubella in children. Cochrane Database Syst Rev 2012;:CD004407 «PMID: 22336803»PubMed
- Chin RF, Neville BG, Scott RC. Meningitis is a common cause of convulsive status epilepticus with fever. Arch Dis Child 2005;90:66-9 «PMID: 15613516»PubMed
- Leung AK, Hon KL, Leung TN. Febrile seizures: an overview. Drugs Context 2018;7:212536 «PMID: 30038660»PubMed
- Hom J, Medwid K. The low rate of bacterial meningitis in children, ages 6 to 18 months, with simple febrile seizures. Acad Emerg Med 2011;18:1114-20 «PMID: 22092892»PubMed
- Guedj R, Chappuy H, Titomanlio L ym. Do All Children Who Present With a Complex Febrile Seizure Need a Lumbar Puncture? Ann Emerg Med 2017;70:52-62.e6 «PMID: 28259480»PubMed
- Offringa M, Newton R, Cozijnsen MA ym. Prophylactic drug management for febrile seizures in children. Cochrane Database Syst Rev 2017;2:CD003031 «PMID: 28225210»PubMed
- Knudsen FU, Paerregaard A, Andersen R ym. Long term outcome of prophylaxis for febrile convulsions. Arch Dis Child 1996;74:13-8 «PMID: 8660037»PubMed
- Farwell JR, Lee YJ, Hirtz DG ym. Phenobarbital for febrile seizures--effects on intelligence and on seizure recurrence. N Engl J Med 1990;322:364-9 «PMID: 2242106»PubMed

